Углеродсодержащий фотокатализатор на основе диоксида титана, способ его получения и применение (варианты)
Иллюстрации
Показать всеИзобретение может быть использовано в химической, строительной и других отраслях промышленности. Предложен углеродсодержащий фотокатализатор на основе диоксида титана, обладающий более эффективным поглощением света в области λ≥400 нм по сравнению с чистым диоксидом титана и характеризующийся при температуре 5 К спектром электронного парамагнитного резонанса (ЭПР), имеющим только один интенсивный сигнал в интервале значений g от 1,97 до 2,05, а также рентгеновским фотоэлектронным спектром, в котором интенсивная полоса поглощения при энергии связи при 285,6 эВ относится к полосе O1s при 530 эВ. Для получения такого фотокатализатора соединение титана с удельной площадью поверхности, по меньшей мере, 50 м2/г по методу BET тщательно смешивают с углеродсодержащим веществом и смесь подвергают термической обработке при температуре, не превышающей 400°С. Содержание углерода в фотокатализаторе составляет от 0,05 до 4 мас.%. Изобретение позволяет повысить эффективность производства фотокатализатора, активного при дневном свете, улучшить его оптические свойства. 6 н. и 25 з.п. ф-лы, 11 ил.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к углеродсодержащему фотокатализатору на основе диоксида титана, который является фотоактивным в видимой области спектра, в дальнейшем называемому vlp-TiO2.
Кроме того, изобретение относится к способу получения углеродсодержащих диоксидов титана (vlp-TiO2), которые действуют в качестве фотокатализатора при облучении видимым светом.
Уровень техники
Фотокаталитические материалы представляют собой полупроводники, в которых под действием света возникает пара электрон-дырка, при этом на поверхности материала образуются свободные радикалы с высокой реакционной активностью. Диоксид титана является именно таким полупроводником. Известно, что диоксид титана можно использовать для удаления природных или промышленных загрязнителей в воздухе и воде при УФ-облучении, при этом кислород воздуха восстанавливается, а примесь окисляется с образованием безвредного конечного продукта (минерализуется). Кроме того, поверхность диоксида титана благодаря поглощению УФ-света становится сверхгидрофильной. На этом основано защитное действие тонкой пленки диоксида титана на зеркалах или оконных стеклах.
Существенным недостатком диоксида титана является то, что при катализе может использоваться лишь УФ-область спектра, т.е. только 3-4% излучения, а рассеянный дневной свет либо не вызывает, либо вызывает очень слабое каталитическое действие.
В связи с этим с давних пор предпринимались попытки модифицировать диоксид титана таким образом, чтобы для индуцирования указанного явления можно было использовать основную часть спектра фотохимически активного солнечного света, а именно видимую область спектра от приблизительно 400 нм до приблизительно 700 нм.
Одним из способов получения TiO2, фотокаталитически активного при дневном свете, является его легирование ионами металлов, таких как V, Pt, Cr, Fe и т.п. Другим вариантом является образование кислородных вакансий в кристаллической решетке ТiO2 за счет восстановления Ti4+. Оба способа требуют применения сложных технологий, таких как ионное внедрение или плазменная обработка. В многочисленных патентах описан модифицированный азотом диоксид титана, который фотокаталитически активен в видимой области спектра (например, ЕР 1178011 А1, ЕР 1254863 А1).
Кроме того, известно, что фотокаталитическая активность диоксида титана при облучении видимым светом возрастает при модификации углеродом. Например, в JP 11333304 А описан диоксид титана, поверхность которого по меньшей мере частично покрыта графитом, аморфным углеродом, алмазоподобным углеродом или углеводородами. В ЕР 0997191 А1 сообщается о диоксиде титана, на поверхность которого за счет осаждения из газовой фазы нанесен карбид титана. Фотокаталитические материалы, в которых диоксид титана содержит наряду с другими компонентами азот, серу, углерод или другие элементы в качестве аниона, описаны, например, в ЕР 1205244 А1 и ЕР 1205245 А1. Анионы должны располагаться на месте атомов кислорода, или находиться в узлах кристаллической решетки, или на границах зерен поликристаллических частиц диоксида титана. Однако не описана характеристика материалов, или не описаны их каталитические или физические свойства.
Кроме того, известен способ получения диоксида титана гидролизом алкоголята титана соляной кислотой с последующим нагреванием при 350°С, содержащего от 1,0 до 1,7 мас.% углерода (C.Lettmann и др., Applied Catalysis В, 32, 215 (2001)). В этом случае углерод образуется из лигандов соединения титана.
В других работах указано, что гидролиз тетрахлорида титана гидроксидом тетрабутиламмония и последующим прокаливанием при 400°С приводит к образованию препарата диоксида титана, который содержит 0,42 мас.% углерода (S.Sakthivel и H.Kisch, Angew. Chem. Int. Ed., 42, 4908 (2003)). В этом случае углерод образуется из осадителя и, вероятно, распределяется относительно равномерно по всему объему (объемное легирование).
Недостаток известных фотокаталитических материалов заключается в том, что способ их получения непригоден для промышленного производства. Способы неприменимы в производственном масштабе по техническим причинам или являются экономически невыгодными. Кроме того, большинство полученных продуктов обладают недостаточной фотокаталитической активностью при разложении вредных веществ в видимом свете в области ≥400 нм и вызывают только незначительное индуцированное светом повышение гидрофильных свойств.
Кроме того, до настоящего времени материалы оптимизировали исключительно по их фотокаталитическим свойствам. Окраска и яркость, т.е. оптические свойства до сих пор не принимались во внимание. Чрезвычайно яркий vlp-TiO2 с незначительной собственной окраской и более высокой каталитической активностью обладает преимуществом по сравнению с другими материалами, для которых нехарактерна такая незначительная окраска или которые содержат только незначительное количество соответственно окрашенного vlp-TiO2, как, например, при применении в качестве материалов для специальных красок, лаков и покрытий.
Раскрытие изобретения
Целью изобретения является разработка высокоактивного при дневном освещении фотокатализатора на основе диоксида титана, модифицированного углеродом, и разработка экономически приемлемого способа его получения.
Цель изобретения достигается получением углеродсодержащего диоксида титана, обладающего по сравнению с чистым диоксидом титана более эффективным поглощением света в области λ≥400 нм (vlp-TiO2), причем такой материал характеризуется спектром электронного парамагнитного резонанса (ЭПР), измеренным при температуре 5 К, в котором в области значений g от 1,97 до 2,05 наблюдается только один интенсивный сигнал. Кроме того, цель изобретения достигается разработкой способа получения, согласно которому соединение титана, которое характеризуется удельной площадью поверхности по меньшей мере от 50 м2/г по данным метода BET (Brunauer-Emmett-Teller), тщательно смешивают с углеродсодержащим соединением и смесь нагревают при температуре до 400°С. Другие преимущества способа по изобретению приводятся ниже в формуле изобретения.
Свойства материала
vlp-TiO2 по настоящему изобретению обладает более высокой фотокаталитической активностью по сравнению с другими материалами, описанными в уровне техники. Для определения фотокаталитической активности (далее обозначенной как фотоактивность) используют разложение 4-хлорфенола в присутствии определенного количества vlp-TiO2 при облучении в течение 120 мин светом с длиной волны ≥455 нм. Способ измерения подробно описан ниже. По данным указанного анализа фотоактивность vlp-TiO2 по изобретению составляет по меньшей мере 20%, предпочтительно по меньшей мере 40%, прежде всего по меньшей мере 50%.
Содержание углерода находится в интервале от 0,05 до 4 мас.% в расчете на TiO2, предпочтительно от 0,05 до 2,0 мас.%, более предпочтительно от 0,03 до 1,5 мас.%. Более высокая фотоактивность наблюдается при содержании углерода от 0,4 до 0,8 мас.%.
Частицы диоксида титана содержат углерод только в поверхностном слое и поэтому в дальнейшем обозначаются как "углерод-модифицированные", в отличие от легированного по объему диоксида титана, полученного по методу Sakthivel и Kisch (2003). Предполагают, что углерод или соединения углерода в составе vlp-TiO2 по изобретению ковалентно связаны с кислородом на поверхности TiO2 и отщепляются в присутствии щелочи.
В дополнительном или другом варианте фотокатализатор может также содержать кислород и/или серу.
В отличие от немодифицированного TiO2 материал по изобретению vlp-TiO2 поглощает видимый свет при длине волны ≥400 нм. При этом относительное поглощение (пропорциональное функции Кубелка-Мунка F(R)) при 500 нм составляет приблизительно 50%, а при 600 нм приблизительно 20% от значения при 400 нм.
Спектр ЭПР vlp-TiO2 по изобретению, измеренный при температуре 5К, характеризуется интенсивным сигналом при значении g от 2,002 до 2,004, прежде всего 2,003. В интервале значений g от 1,97 до 2,05 не наблюдается никаких сигналов. Интенсивность сигналов при g приблизительно 2,003 возрастает при облучении светом с длиной волны ≥380 нм (галогеновая лампа мощностью 100 Вт, не содержащая УФ-составляющей, интерференционный фильтр KG5) по сравнению с измерением в темноте.
Рентгеновский-фотоэлектронный спектр (РФЭ) vlр-ТiO2 по изобретению характеризуется интенсивной полосой поглощения при энергии связи 285,6 эВ, относящейся к полосе O1s при 530 эВ.
Характерно, что vlp-TiO2 в отличие от фотокатализатора, полученного методом по Sakthivel и Kisch (2003), не содержит полосу карбоната в спектре РФЭ и в ИК спектре.
При облучении видимым светом для vlp-TiO2 краевой угол в воде составляет приблизительно 8°, в то время как для немодифицированного ТiO2 краевой угол составляет приблизительно 21°.
Новый фотокатализатор обеспечивает разложение вредных веществ не только при искусственном видимом свете, но и при рассеянном дневном свете во внутренних помещениях. Его можно использовать для разложения примесей и токсичных веществ в жидкостях или газах, прежде всего в воде и воздухе.
Фотокатализатор можно наносить в виде тонкого слоя на различные носители, такие как стекло (обычное и зеркальное), дерево, волокна, керамика, бетон, строительные материалы, SiO2, металл, бумага и полимерные материалы. В связи с этим, а также благодаря простому способу получения открываются возможности применения такого материала во многих отраслях, таких, например, как строительство, производство керамики и автомобильная промышленность (для создания самоочищающихся поверхностей) или системы для защиты окружающей среды (кондиционеры, системы очистки воздуха и стерилизации воздуха, очистки воды, прежде всего питьевой воды, например, для антибактериальной и антивирусной очистки). Фотокатализатор можно использовать в составе отделочных материалов (покрытий) внутренних и внешних поверхностей, таких, например, как краски, лакокрасочные материалы, лаки и глазури, предназначенных для нанесения на кирпичную стену, оштукатуренную поверхность, шпаклевку, обои или на деревянную, металлическую, стеклянную или керамическую поверхность или строительные конструкции, такие, например, как системы парового отопления и внешние элементы фасада здания, а также дорожное покрытие и полимерные материалы, пленки, волокна и бумага. Фотокатализатор можно использовать в строительной промышленности в качестве компонента покрытия элементов стандартных строительных блоков. Кроме того, фотокатализатор можно использовать при производстве сборных железобетонных конструкций, бетонной брусчатки, кровельной черепицы, керамики, плиток, обоев, тканей, панелей и элементов обшивки для покрытия и отделки внешних и внутренних поверхностей.
Благодаря индуцированному светом повышению гидрофильности поверхности, покрытой TiO2, указанные материалы можно использовать и в других отраслях промышленности, таких, например, как производство свободных от налета (конденсата) зеркал и оконных стекол для сантехники или в транспортной и строительной промышленности.
Кроме того, фотокатализатор можно использовать в фотоэлектрических элементах и для разложения воды.
Краткое описание чертежей
Свойства vlp-TiO2 по изобретению иллюстрируются ниже на фиг.1-9.
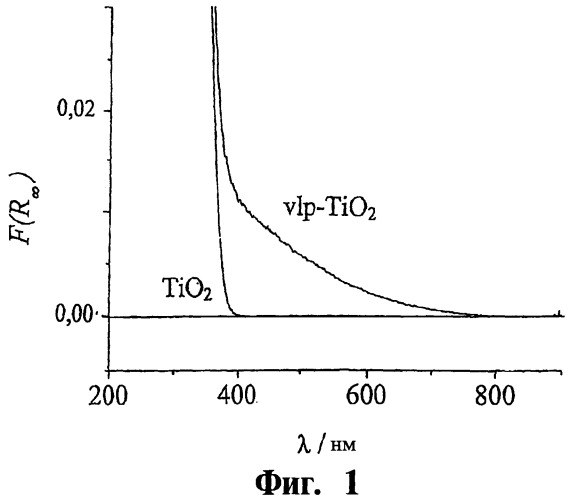
На фиг.1 приводится график зависимости от длины волны функции Кубелка-Мунка F(R∞), пропорциональной относительному поглощению, для немодифицированного TiO2 и для TiO2, модифицированного углеродом (vlp-TiO2).
На фиг.2 приведены спектры ЭПР для vlp-TiO2 по изобретению (спектр А) и TiO2, полученного по методу Sakthivel и Kisch (спектр В), измеренные в темноте и при температуре 5К.
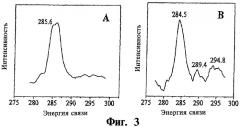
На фиг.3 приведены спектры РФЭ для vlp-TiO2 по изобретению (спектр А) и известного TiO2, полученного методом Sakthivel и Kisch из тетрахлорида титана осаждением гидроксидом тетрабутиламмония (спектр В).
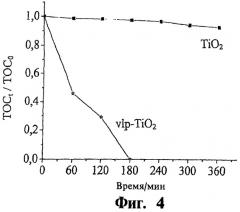
На фиг.4 показано фотокаталитическое действие vlp-TiO2 по сравнению с немодифицированным ТiO2 на примере реакции разложения 4-хлорфенола (2,5×10-4 М раствор в воде) при искусственном освещении в видимой области спектра (λ≥455 нм).
На фиг.5 иллюстрируется фотокаталитическое действие vlp-TiO2 при сравнении с немодифицированным TiO2 в реакции разложения 4-хлорфенола (2,5×10-4 М раствор в воде) при освещении рассеянным дневным светом в помещении.
На фиг.6 представлено фотокаталитическое действие vlp-TiO2 по сравнению с немодифицированным ТiO2 на примере реакции разложения бензола (5 об.%), ацетальдегида (2 об.%) и монооксида углерода (5 об.%) при освещении рассеянным дневным светом в помещении.
На фиг.7 представлена рентгенограмма порошка vlp-TiO2, на которой указаны только рефлексы (отраженные сигналы) анатаза.
На фиг.8 представлено изображение кристаллической решетки кристаллического vlp-TiO2 в поле электронного микроскопа высокого разрешения (НТЕМ).
На фиг.9 представлен профиль включения углерода в vlp-TiO2 в виде соотношения C/Ti.
Осуществление изобретения
На фиг.1 представлен график, из которого видно, что vlp-TiO2 в отличие от немодифицированного диоксида титана поглощает в видимой области спектра. Величина F(R∞) составляет при 500 нм приблизительно 50%, а при 600 нм приблизительно 20% от значений функции, полученных при 400 нм.
В спектре А, представленном на фиг.2, наблюдается только один интенсивный сигнал при значении g 2,003. В спектре В наряду с основным сигналом при g приблизительно 2,003 наблюдаются три дополнительных сигнала в интервале g от 1,97 до 2,05.
Спектр vlp-TiO2, представленный на фиг.3, характеризуется интенсивным C1s-сигналом при энергии связи 285,6 эВ, относящимся к полосе поглощения O1s при 530 эВ, что указывает на присутствие элементарного углерода. В отличие от этого в спектре В присутствует C1s-сигнал элементарного углерода при энергии связи 284,5 эВ, а также дополнительные полосы при 289,4 эВ и 294,8 эВ, которые указывают на присутствие карбоната. В соответствующих ИК-спектрах также наблюдаются типичные полосы 1738, 1096 и 798 см-1, характерные для карбоната.
Результаты фотокаталитического действия vlp-TiO2 по сравнению с немодифицированным TiO2 представлены на фиг.4 в виде графика снижения общего содержания органического углерода (ТОСt) в растворе относительно исходного значения (ТОС0). При использовании vlp-TiO2 полное разложение достигается через 3 ч.
На фиг.5 результаты фотокаталитического действия vlp-TiO2 представлены в форме снижения общего содержания органического углерода (ТОСt) в растворе относительно исходного значения (ТОС0). Даже при освещении рассеянным дневным светом с низкой интенсивностью (7-10 Вт/м2 в области 400-1200 нм) vlp-TiO2 обеспечивает 80% разрушения указанного соединения через 6 ч. Даже при очень низкой интенсивности рассеянного дневного света (от 1,6 до <1 Вт/м2) vlp-TiO2 в отличие от стандартного фотокатализатора TiOg (Degussa P25, Kemira UV-Titan, Sachtieben Hombikat, Tayca MT-100SA) еще обладает заметной фотоактивностью. Измерение скорости разложения 2,5×10-4 М раствора 4-хлорфенола в воде проводили, как описано выше.
а) Интенсивность света: 1.6 Вт/м2, продолжительность 12 ч
| Катализатор | Уд. площадь, метод BET | Скорость разложения |
| vlp-TiO2 | 170 м2/г | 16% |
| Р25 | 50 м2/г | 4% |
| УФ-титан | 20 м2/г | 5% |
| Hombikat | 240 м2/г | 9% |
| MT-100SA | 50 м2/г | 5% |
б) Интенсивность света: <1 Вт/м2 , продолжительность 24 ч
| Катализатор | Уд. площадь, метод BET | Скорость разложения |
| vlp-TiO2 | 170 м2/г | 18% |
| Hombikat | 240 м2/г | 3% |
Реакцию разложения бензола (5 об.%), ацетальдегида (2 об.%) и монооксида углерода (5 об.%) под действием vlp-TiO2 проводили в круглодонной колбе объемом 1 л, содержащей 12 мг диоксида титана на круглом бумажном фильтре (диаметром 15 см). Результаты представлены на фиг.6 в виде графика снижения общего содержания органического углерода (TOCt) в атмосфере относительно исходного значения (ТОС0). На графике показано разложение бензола, ацетальдегида или монооксида углерода соответственно фотокатализатором vlp-TiO2 по изобретению, а также разложение ацетальдегида немодифицированным диоксидом титана.
На основании рентгенограммы, приведенной на фиг.7, по методу Шеррера были рассчитаны размеры кристаллов vlp-TiO2, которые составляют 10 нм.
Профиль содержания углерода в vlp-TiO2, показанный на фиг.9, получали методом ионной бомбардировки (Ar+) и методом ЭСХА (электронная спектроскопия для химического анализа). Время бомбардировки 5×103 с соответствует глубине включения 5 нм.
Способ получения
Согласно способу по изобретению в качестве исходного материала используют соединение титана в форме аморфного, частично кристаллического или кристаллического оксида титана, или водосодержащего оксида титана, и/или гидратированного диоксида титана и/или оксигидрата титана, которое в настоящем описании обозначается как исходное соединение титана.
Исходное соединение титана можно получить, например, в виде диоксида титана сульфатным способом или хлоридным способом. Гидратированный диоксид титана, или оксигидрат титана, или метатитановую кислоту осаждают, например, гидролизом сульфата титана или хлорида титана.
Исходное соединение титана представляет собой мелкозернистое твердое вещество или суспензию с содержанием соответствующих частиц твердого вещества по меньшей мере 15 мас.%, причем удельная площадь поверхности твердых частиц составляет по меньшей мере 50 м2/г по методу BET, предпочтительно от приблизительно 150 до
350 м2/г по методу BET, прежде всего от приблизительно 150 до 250 м2/г по методу BET.
Для промышленного применения способа по изобретению по экономическим причинам предпочтителен способ получения исходного соединения титана из гидратированного диоксида титана сульфатным методом. В настоящее время наиболее рентабельным способом получения гидратированного диоксида титана является нейтрализация и промывание от примеси серной кислоты до содержания сульфата в твердом продукте после высушивания <1 мас.% в расчете на SO3.
Углеродсодержащий компонент характеризуется температурой разложения не более 400°С, предпочтительно <350°С, более предпочтительно <300°С. Пригодными материалами являются такие углеродсодержащие материалы, как, например, дерево, сажа или активированный уголь и прежде всего органические углеродсодержащие соединения, такие как углеводороды, содержащие по меньшей мере одну функциональную группу. Такие функциональные группы включают ОН, СНО, СООН, NHx, SHx, COOR, где R означает алкил или арил. Например, можно использовать янтарную кислоту, глицерин или этиленгликоль. Можно использовать также сахара или другие углеводы, а также гидроксиды органических производных аммония, прежде всего тетраалкиламмония. Пригодны также смеси указанных соединений. Предпочтительным является использование водорастворимых многоатомных спиртов с относительным содержанием углерод/кислород от приблизительно 0,7 до приблизительно 1,5, предпочтительно приблизительно 1, прежде всего пентаэритрита. Углеродсодержащие соединения можно использовать в виде твердого вещества или в виде раствора или суспензии.
Органические углеродсодержащие соединения должны обладать возможно более высоким сродством к поверхности исходного соединения титана, чтобы обеспечить равномерное контактирование с указанной поверхностью.
Исходное соединение титана тщательно смешивают с органическим углеродсодержащим соединением, чтобы обеспечить распределение углеродсодержашего соединения по поверхности исходного соединения титана. При этом органическое углеродсодержащее соединение удерживается на поверхности исходного соединения титана за счет физической или химической сорбции. Обработку поверхности исходного соединения титана проводят растворением углеродсодержащего соединения в суспензии исходного соединения титана или перемешиванием суспензии углеродсодержащего соединения с суспензией исходного соединения титана, а также интенсивно перемешивают углеродсодержащее соединение с предварительно высушенным порошкообразным исходным соединением титана. В случае использования гидратированного диоксида титана углеродсодержащее соединение можно также добавлять в гидролизуемый раствор на стадии получения гидратированного диоксида титана. В полученной смеси исходного соединения титана и углеродсодержащего соединения содержание углеродсодержащего соединения относительно исходного соединения титана (в расчете на твердое вещество) составляет от 1 до 40 мас.%.
Если смесь представляет собой суспензию, то для последующей обработки ее высушивают и получают порошкообразный твердый продукт. Для этого используют известные методы высушивания в распылительной сушилке или в сушилке с псевдоожиженным слоем.
Полученную и необязательно предварительно высушенную смесь нагревают при температуре не более 400°С. Термическую обработку проводят в присутствии окислителя, предпочтительно в присутствии воздуха или смеси воздуха с кислородом. При этом происходит разложение органического углеродсодержащего соединения на поверхности исходного соединения титана и высвобождение H2O, CO2 и СО. Хотя термическую обработку можно также проводить в периодическом режиме при использовании, например, обычной лабораторной печи, по экономическим причинам предпочтительным является непрерывный режим, при котором можно поддерживать необходимую температуру. В качестве непрерывного способа можно использовать все известные способы, в которых реализуется соответствующий температурный режим и необходимая продолжительность обработки. Прежде всего пригодными аппаратами для обжига являются прямо или косвенно обогреваемые трубчатые вращающиеся печи. Можно также использовать в непрерывном режиме проточные реакторы, сушилки с псевдоожиженным слоем и реактор с лопастной мешалкой. Три вышеупомянутых аппарата для обжига можно также использовать и в периодическом режиме.
Термическую обработку предпочтительно проводят до образования продукта (vlp-TiO2) с содержанием углерода от 0,05 до 4,0 мас.%, предпочтительно от 0,05 до 2,0 мас.%, более предпочтительно от 0,3 до 1,5 мас.%, наиболее предпочтительно от 0,4 до 0,8 мас.%. В процессе термической обработки происходит изменение окраски с белой на коричневую и, наконец, на бежевую. Конечный продукт характеризуется окраской от бежевой до светлой желто-коричневой. Он отличается тем, что углерод включен в аморфные и поликристаллические участки поверхностного слоя, а также содержится на поверхности. Продукт проявляет фотоактивность в видимом свете.
После термической обработки продукт измельчают известными способами, например, в стержневой мельнице, в струйной мельнице или в противоточной струйной мельнице. При термической обработке порошкообразной предварительно высушенной смеси образуется главным образом продукт, не содержащий агломератов и не требующий измельчения. Достигаемая зернистость зависит от размера частиц исходного соединения титана. Зернистость или удельная площадь поверхности продукта ненамного меньше или соответствует размерам частиц эдукта. Требуемый размер частиц фотокатализатора зависит от области применения фотокатализатора. Обычно размер частиц соответствует частицам пигментных красителей на основе TiO2, однако размер частиц можно изменять в сторону уменьшения или увеличения. Удельная площадь по данным метода BET составляет от 100 до 200 м2/г, предпочтительно от 130 до 200 м2/г, более предпочтительно от 130 до 170 м2/г.
Примеры
Изобретение иллюстрируется следующими примерами, не ограничивающими объем притязаний.
Пример 1
Оксигидрат титана в виде водной пасты (35 мас.% твердого вещества), полученный сульфатным способом, разбавляли дистиллированной водой при комнатной температуре до образования перемешиваемой суспензии. При этом содержание твердого вещества составляло от 20 до 25%. Затем в суспензию добавляли раствор NaOH (36 мас.%) до рН 6,0-7,0. Затем суспензию фильтровали и промывали дистиллированной водой до содержания SO3 в высушенном остатке 1 мас.%. Полученный нейтрализованный и промытый оксигидрат титана еще раз разбавляли дистиллированной водой до перемешиваемой суспензии (содержание твердого вещества 25%) и добавляли 12 мас.% янтарной кислоты в расчете на твердое вещество. Янтарную кислоту добавляли в виде твердого вещества и суспензию перемешивали до полного растворения янтарной кислоты. Для повышения растворимости янтарной кислоты суспензию нагревали до приблизительно 60°С. Полученную суспензию упаривали на роторном испарителе (при ИК-облучении) до образования пастообразной массы. Пастообразную массу высушивали в сушильном шкафу при 150°С до содержания твердого вещества >98%.
300 г высушенной смеси оксигидрат титана с янтарной кислотой измельчали в тонкодисперсный порошок (например, с использованием ступки и сита) и полученный порошок в кварцевой кювете с крышкой нагревали при 290°С в сушильном шкафу. Через 1-2 ч кювету извлекали и порошок перемешивали еще раз. Через 13-15 ч нагревания в сушильном шкафу окраска порошка изменялась от исходной желтоватой на серовато-черную, а затем на желтовато-коричневую. Термическую обработку завершали после образования vlp-TiO2, при этом содержание углерода снижалось от начального 5-5,5 мас.% до приблизительно 0,65-0,80 мас.%. В заключение фотокатализатор измельчали и определяли содержание углерода, оптические свойства, удельную площадь поверхности по методу BET и фотоактивность.
Пример 2
Конечный продукт получали аналогично тому, как описано в примере 1, за исключением того, что в суспензию оксигидрата титана в качестве твердого вещества добавляли 12 мас.% пентаэритрита.
Пример 3
Конечный продукт получали аналогично тому, как описано в примере 2, за исключением того, что в суспензию оксигидрата титана в качестве твердого вещества добавляли 5 мас.% пентаэритрита.
Пример 4
Суспензию оксигидрата титана пентаэритрита получали добавлением 5 мас.% пентаэритрита аналогично тому, как описано в примере 1. В отличие от примера 1 термическую обработку полученной суспензии проводили в непрерывном режиме во вращающейся трубчатой печи по следующей методике.
Вращающуюся трубчатую печь использовали в противоточном режиме и обогревали непосредственно газовой горелкой. Открытое пламя газовой горелки защищали жаровой трубой и тем самым препятствовали прямому контактированию с продуктом (vlp-TiO2). Нагреваемая длина печи составляла 7 м, а диаметр 0,3 м. Суспензию распыляли во входном отверстии печи. Скорость подачи суспензии составляла 40 кг/ч. Цепное устройство на входном отверстии печи обеспечивало высокую турбулентность, при этом происходило быстрое высушивание и заключительное измельчение высушенного материала. Продолжительность производственного цикла в непрерывно эксплуатируемой печи составляла 1 ч. Температура печи в выходном отверстии печи составляла 260°С, которую регулировали скоростью подачи газа в горелку. Продукт vlp-TiO2 в выходном отверстии печи представлял собой тонокодисперсный порошок желто-коричневого цвета. Наконец, vlp-TiO2 измельчали в смесителе (фирма Braun, MX 2050) и определяли содержание углерода, оптические свойства, удельную площадь поверхности методом BET и фотоактивность.
Пример 5
Продукт получали аналогично тому, как описано в примере 4, за исключением того, что температуру в выходном отверстии печи устанавливали на уровне 280°С, регулируя скорость подачи газа в горелку.
Пример 6
Суспензию оксигидрата титана/пентаэритрита получали при добавлении 5 мас.% пентаэритрита аналогично тому, как описано в примере 1. В отличие от примера 1 суспензию предварительно высушивали в электрической печи до порошкообразного твердого вещества с остаточной влажностью 22%. Термическую обработку предварительно высушенного порошкообразного материала проводили в непрерывном режиме во вращающейся трубчатой печи с косвенным нагревом по следующей методике.
Вращающуюся трубчатую печь использовали в прямоточном режиме и обогревали электрическим нагревателем в трех зонах. Общая нагреваемая длина печи составляла 2700 мм, а диаметр 390 мм. Порошкообразное твердое вещество подавали дозирующим шнеком во входное отверстие печи. Цепное устройство, расположенное по всей длине печи, обеспечивало равномерное распределение порошка и снижение шлакования на стенке печи. Скорость подачи твердого вещества составляла 25 кг/ч. Продолжительность производственного цикла через непрерывно эксплуатируемую печь составляла 0,5 ч. Температуру печи в трех зонах нагрева регулировали электрическим нагревателем. Температуру в трех зонах регулировали в каждой зоне отдельно. В выходном отверстии печи vlp-TiO2 представлял собой тонкодисперсный порошок бежевого цвета. Наконец, vlp-TiO2 измельчали в смесителе (фирма Braun, MX 2050) и определяли содержание углерода, оптические свойства, поверхность по BET и фотоактивность.
Пример для сравнения
Пигмент на основе TiO2 (анатаз) с удельной площадью поверхности по методу BET 10 м2/г (коммерческий продукт фирмы Kronos 1000) смешивали с 12% пентаэритрита аналогично тому, как описано в примере 2, и подвергали термической обработке.
| Пример | Орг.соединение | Термическая обработка | Анализ vlp-TiO2 | Фотоактив-ность | |||||
| °С | Время (ч) | Содержание С | Анализ PLV | Метод BET | Разлож. 4-ХФ, 120 мин (%) | ||||
| (%) | L* | b* | а* | м2/г | |||||
| 1 | Янтарная кислота | 290 | 13 | 0.79 | 85.4 | 9.85 | 1.63 | 164 | 48 |
| 2 | Пентаэритрит | 290 | 28 | 0.75 | 86.9 | 10,08 | 1.53 | 158 | 50 |
| 3 | Пентаэритрит | 290 | 10 | 0.76 | 83.7 | 10.03 | 1.59 | 140 | 63 |
| 4 | Пентаэритрит | 260* | 1** | 0.92 | 85.1 | 11.7 | 1.2 | 152 | 58 |
| 5 | Пентаэритрит | 280* | 1** | 0.50 | 85.8 | 9.4 | 2.2 | 160 | 68 |
| 6 | Пентаэритрит | 300*** | 0.5** | 0.78 | 83,0 | 11.0 | 2.6 | 167 | 86 |
| Сравн. пример | Пентаэритрит | 290 | 42 | 0.82 | 74.7 | 9.12 | 2.50 | 11.6 | <5 |
| * Максимальная температура, измеренная в выходном отверстии печи.** Время продолжительности цикла (прохождения материала через печь).*** Температура в трех зонах нагрева, измеренная в области размещения нагревательных элементов. |
В таблице представлены результаты анализа и определения фотоактивности vlp-TiO2 по изобретению.
vlp-TiO2, полученный из гидратированного диоксида титана (примеры 1-6), обладает достаточно высокими оптическими параметрами (анализ PLV) и чрезвычайно высокой фотокаталитической активностью в видимой части спектра. Применение анатаз-пигмента вместо гидрата титана в качестве исходного соединения титана приводит к образованию продукта, не обладающего указанной фотоактивностью (см. сравнительный пример).
Пример 7
5 г диоксида титана (коммерчески и продукт Tronox титангидрат-0, фирма Kerr-McGee Pigments GmbH) суспендировали при комнатной температуре в 20 мл дистиллированной воды, добавляли 5 мл этиленгликоля (коммерческий препарат, фирма Fluka AG) и обрабатывали в течение 30 мин в ультразвуковой бане (Sonorex Super RK 106, фирма Bandelin Eletronic, Берлин, 35 кГц, эффективная вч-мощность 120 Вт). После перемешивания на магнитной мешалке в течение ночи растворитель предпочтительно удаляли в вакууме, остаток высушивали при температуре от 100 до 200°С, предпочтительно при 200°С, по меньшей мере в течение 12 ч, нагревали в закрытом сосуде при 300°С в течение 1 ч, а затем выдерживали при указанной температуре в течение еще 3 ч. При этом цвет порошка изменялся от белого на темно-коричневый и, наконец, на бежевый. При более продолжительном нагревании образуется бесцветный неактивный порошок. По данным элементного анализа продукта получены следующие результаты: 2,58 мас.% углерода, 0,02 мас.% азота и 0,40 мас.% водорода.
Немодифицированный ТiO2 характеризуется следующим составом: 0,07 мас.% углерода, 0,0 мас.% азота и 0,0 мас.% водорода.
Пример 8
Для удаления поверхностного слоя углеродсодержащего соединения, 5 г vlp-TiO2 перемешивали в течение ночи в 100 мл 2 М гидроксида натрия (рН 12). Суспензию центрифугировали, экстракт желто-коричневого цвета удаляли, слабоокрашенный беловатый остаток высушивали при 100°С. Полученный порошок по данным анализа разложения 4-хлорфенола в видимом свете не проявлял никакой активности. Если порошок снова смешивали с экстрактом и нагревали, предпочтительно при приблизительно 200°С, он обладал активностью необработанного щелочью vlp-TiO2.
Пример 9
Для нанесения покрытия на синтетическую пленку порошок, полученный, как указано в примере 6, суспендировали в ультразвуковой бане в жидкости, такой как метанол или этанол, и полученную суспензию наносили пульверизатором на пленку по возможности тонким слоем. После высушивания при температуре 343К нанесение слоя повторяли для достижения необходимой толщины слоя.
Вместо синтетической пленки можно использовать другую подложку, такую как бумага (см. эксперимент, фиг.6) или алюминий (см. метод испытаний з: "метод погружения".
Методы измерения
а) Определение оптических свойств (анализ PLV)
Метод использовали для определения оптических свойств, таких как яркость L*, оттенок а* и оттенок b* для vlp-TiO2. Из анализируемых образцов vlp-TiO2 в определенных условиях на гидравлическом прессе (фирма Matra, Франкфурт) получали порошковые прессовки. Затем с использованием колориметра с тремя входным сигналами (Hunterlab) определяли коэффициент яркости прессовок.
Для получения порошковых прессовок образцы vlp-TiO2 измельчали. Для этого 100 г полученного vlp-TiO2 помещали в обычный смеситель (фирма Braun, модель MX 2050) и измельчали (12 циклов по 5 с). После каждого цикла смеситель открывали и порошок перемешивали. На нижнюю пластину с крестообразным углублением помещали с обеих сторон лист белой бумаги и с помощью пресса впечатывали в углубление металлическое кольцо (высотой 4 см, диаметром 2,4 см). В металлическое кольцо при легком встряхивании и постукивании вносили приблизительно 25 г измельченного vlp-TiO2. Порошок спрессовывали при давлении 2-3 кН. Процесс прессования повторяли дважды до достижения требуемого рабочего давления 15 кН. Металлическое кольцо отделяли от нижней пластины при легком вращении и вытягивании. Лист бумаги между пластиной и кольцом удаляли. В кольце оставалась прессовка, яркость которой измеряли на колориметре (Hunterlab). Параметры L*, а* и b* считывали непосредственно с колориметра.
б) Определение фотоактивности (разложение вредных веществ)
При искусственном освещении:
15 г vlp-TiO2 диспергировали в 15 мл 2,5×10-4 М раствора 4-хлорфенола в течение 10 мин на ультразвуковой бане, а затем освещали в охлаждаемой водой круглой кювете на оптической скамье. При определении фотоактивности освещение проводили с использованием лампы с фокусирующим устройством (Amko, mod. A1020, фокусное расстояние 30 см) Osram XBO 150 Вт (ксеноновая лампа с коротким цоколем). Спектр этой лампы представлен на фиг.10. Реакции проводили в охлаждаемой водой круглой кювете объемом 15 мл с внутренним диаметром 30 мм и длиной оптического пути 20 мм. Суспензию перемешивали механической мешалкой или магнитной мешалкой. Круглая кювета представлена на фиг 11. Кювету фиксировали в фокусе лампы. Свет фокусировали таким образом, чтобы освещался только рабочий объем кюветы. Все узлы установки прочно закрепляли на оптической скамье. Для исключения УФ-облучения использовали фильтр (фирма Schott) с областью пропускания λ1455 нм. Для снижения возможного перегрева реакционную смесь освещали через ИК-фильтр, установленный на световом пути. Сама кювета представляла собой цилиндр (диаметром 6 см, высотой 10 см), заполненный водой. Снижение концен