Способ получения окислителя на основе ферратов щелочных металлов и установка для его осуществления
Иллюстрации
Показать всеИзобретение может быть использовано для получения регентов для обеззараживания и очистки хозяйственно-бытовых и промышленных сточных вод. Для получения окислителя на основе ферратов щелочных металлов проводят окисление железосодержащего вещества в расплаве соединений щелочных металлов в две стадии. На первой стадии ведут окисление исходного железосодержащего вещества в расплаве сульфатов щелочных металлов и/или промышленных отходов, содержащих сульфаты щелочных металлов, при пропускании через расплав электрического тока до получения полупродукта, содержащего оксиды железа и ферриты щелочных металлов. На второй стадии осуществляют последующее окисление оксидов железа и ферритов щелочных металлов, содержащихся в полупродукте, в расплаве гидроксидов щелочных металлов, в присутствии газообразного кислорода до получения продукта, содержащего ферраты (IV) и (VI) щелочных металлов. Предложена установка для получения указанного окислителя. Изобретение позволяет снизить энергетические затраты и продолжительность процесса получения окислителя, расширить ассортимент отходов, используемых в качестве сырья. 2 н. и 33 з.п. ф-лы, 17 ил.
Реферат
Изобретение относится к области производства реагентов окислителей, которые могут быть использованы для обеззараживания хозяйственно-бытовых сточных вод после биологической очистки, разложения цианидов, сульфидов и органических примесей в технологиях очистки промышленных сточных вод, обезвреживания радиоактивных сточных вод, путем перевода радионуклидов в малорастворимые соли, разложения фосфорорганических соединений и очистки хозяйственно-бытовых и производственных сточных вод от фосфат-ионов, очистки и водоподготовки питьевой воды природных источников от токсичных соединений мышьяка, марганца и ряда других тяжелых и цветных металлов.
Окислитель на основе ферратов (IV) и (VI) щелочных металлов обладает сильными окислительными свойствами, которые обусловлены входящими в его состав ферратами (IV) и (VI) калия и натрия. Степени окисления выше «+3» являются для железа не характерными, и соединения железа (IV) и (VI) являются, как правило, неустойчивыми и сравнительно легко разлагаются при нагревании и при взаимодействии с молекулами воды или с восстановителями. Все это предъявляет достаточно высокие требования к условиям получения, хранения и применения реагентов, содержащих ферраты (IV) и (VI) калия и натрия.
Известен способ получения феррата (IV) натрия путем прокаливания феррита натрия Na2Fe2O4 при 400-600°C с трехкратным избытком соды Na2CO3 в инертной атмосфере в течение четырех часов с последующим прокаливанием в течение одного часа в токе кислорода (патент США №2835553, опубл. 1958 г.). Недостатками данного способа являются:
- большая длительность процесса (5 часов), обусловленная низкой скоростью процессов, связанной с температурным интервалом 400-600°С;
- использование дефицитного феррита натрия, который не выпускается в промышленных масштабах;
- создание инертной атмосферы, требующей герметизации установки.
Известен также способ получения ферратов (IV) щелочных металлов, при котором нагревают реакционную смесь, состоящую из частиц элементарного железа и пероксида натрия (Na2O2) в молярном отношении 1:1,8-1:1,25 при температурах выше 500°С в течение времени, достаточного для протекания экзотермической реакции между реагентами. Реакцию ведут в отсутствие свободного кислорода, в атмосфере инертного газа (патент США №4385045, опубл. 24.05.83). Недостатками способа являются:
- использование пероксида натрия, который имеет сравнительно высокую стоимость;
- создание атмосферы инертного газа, требующей герметизации установки.
Известен способ непрерывного синтеза феррата (аналог), включающий смешивание водного раствора, содержащего соль железа и окисляющий агент в смешивающей камере, доставку части водного раствора в реакционную камеру, в которой вырабатывается феррат, а также устройство для непрерывного синтеза феррата и доставки его к месту использования, содержащее два резервуара, соединенную с ними смешивающую камеру и реакционную камеру, соединенную с возможностью управления со смешивающей камерой и приспособленной для приема и удержания ферратной смеси, пока концентрация феррата не достигнет заданного уровня (патент RU №2276657, опубл. 20.05.2006). Недостатками способа являются:
- использование солей железа, большая часть которых выпускается химической промышленностью в крупных масштабах реактивной квалификации и имеет высокую стоимость, а химическое или электрохимическое окисление природного железа в водных растворах не обеспечивает высокие производительности процессов и требует применения крупномасштабных устройств для размещения больших объемов воды;
- использование окисляющих реагентов для солей железа в водном растворе приводит к загрязнению образующихся веществ продуктами восстановления окислителей и к повышенному риску вторичного загрязнения очищаемых водных растворов;
- использование устройства для непрерывного синтеза феррата, содержащего два резервуара, смешивающую и реакционную камеры, в котором железосодержащие реагенты используются в виде солей, приводит к удорожанию образующихся ферратов.
Наиболее близким аналогом, принятым за прототип, является способ получения феррата (IV) натрия путем взаимодействия натрийсодержащего соединения, взятого в виде сульфата натрия, с железосодержащим веществом, в качестве которого может использоваться лом черных металлов, в окислительной атмосфере при 850-1100°С при пропускании через расплав переменного тока с помощью съемного пакета стальных электродов. Состав расплава изменяется от сульфата до феррата (IV) натрия в образующемся едком натре. Процесс ведут до достижения массовой доли сульфата натрия в продукте не более 1%, непрерывно поддерживая расплав в жидком состоянии корректировкой напряжения на электродах, что требует значительных затрат энергии для обеспечения достаточной температуры и продолжительности протекающих реакций (патент RU №2149833, опубл. 27.05.2000).
Недостатками способа являются:
- высокий расход электроэнергии, требующийся для электрохимического разложения натрийсодержащих соединений до достижения остаточной массовой доли сульфата натрия 1%;
- высокое энергопотребление, обусловленное необходимостью плавки исходной порции сульфата натрия, которая заливается в реактор, поскольку температура плавления Na2SO4 составляет 884°С;
- необходимость поддержания высоких температур расплава, поскольку с накоплением в его составе оксида натрия, имеющего температуру плавления 1275°С, для поддержания расплавленного состояния температура в реакторе должна быть повышена до 1100°С;
- малоэффективное влияние пероксида натрия, являющегося промежуточным продуктом реакций, на образование феррата (IV) натрия в интервале температур 850-1100°С в объеме расплава, поскольку Na2O2 разлагается выше 400°С.
Известно устройство, для получения окислителя на основе феррата (IV) натрия, содержащее корпус для размещения реакционной массы, съемный пакет стальных электродов, барботер, принятое за прототип в отношении устройства (патент RU №2149833, опубл. 27.05.2000).
Недостатками устройства являются:
- необходимость использования съемного пакета электродов, требующего дополнительных затрат на его изготовление;
- необходимость поддержания температуры расплава в интервале 850-1100°С на всем протяжении процесса приводит к увеличению энергозатрат;
- необходимость использования барботера для непрерывной подачи воздуха в объем расплава и перемешивания расплавленной массы на всем протяжении процесса приводит к увеличению энергозатрат.
Задачей, на решение которой направлено данное техническое решение, является снижение энергетических затрат на получение продукта путем снижения температуры процессов и повышения скорости растворения железосодержащего вещества в расплаве соединений щелочных металлов, расширение ассортимента отходов, которые могут быть использованы в качестве дешевого сырья.
Для решения поставленной задачи в способе получения окислителя на основе ферратов щелочных металлов, включающем окисление железосодержащего вещества в расплаве соединений щелочных металлов согласно изобретению, процесс окисления ведут в две стадии, при этом на первой стадии ведут окисление исходного железосодержащего вещества в расплаве сульфатов щелочных металлов и/или промышленных отходов, содержащих сульфаты щелочных металлов при пропускании через расплав электрического тока до получения полупродукта, содержащего оксиды железа и ферриты щелочных металлов, а на второй стадии осуществляют последующее окисление оксидов железа и ферритов щелочных металлов, содержащихся в полупродукте, в расплаве гидроксидов щелочных металлов, в присутствии газообразного кислорода до получения продукта, содержащего ферраты (IV) и (VI) щелочных металлов.
В качестве исходного железосодержащего вещества используют металлическое железо, и/или его сплавы, и/или отходы металлообработки изделий из черных металлов, например скрап, и/или отходы черной металлургии.
В качестве сульфатов щелочных металлов на первой стадии способа используют сульфаты натрия и/или калия, и/или промышленные отходы, содержащие сульфаты натрия и/или калия.
В качестве гидроксидов щелочных металлов на второй стадии способа используют гидроксиды натрия и/или калия, и/или промышленные отходы, содержащие гидроксиды натрия и/или калия.
Первую стадию способа ведут при температуре 850-1100°С до достижения массовой доли соединений железа (III) в полу продукте 4-39%, в пересчете на железо.
Вторую стадию ведут при температуре 640-880°С, до достижения массовой доли соединений железа (IV) и (VI) в продукте, содержащем ферраты щелочных металлов 2,7-21,8%, в пересчете на железо (VI).
На первой стадии осуществляют электрохимическое или комбинированное химико-электрохимическое окисление железосодержащего вещества.
Электрохимическое окисление железосодержащего вещества в расплаве сульфата натрия и/или калия осуществляют переменным током или выпрямленным или переменным током с поляризацией электродов.
Газообразный кислород на второй стадии способа подают непрерывно в составе газовоздушной смеси, содержащей по объему 21-100% кислорода.
Газовоздушную смесь, содержащую газообразный кислород, барботируют через расплав гидроксида натрия или калия для одновременного окисления соединений железа, содержащихся в полупродукте, и перемешивания расплава. Возможен вариант подачи газовоздушной смеси, содержащей кислород, на поверхность расплава.
Для решения поставленной задачи установка, включающая устройство для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов, содержащее корпус для размещения реакционной массы и электроды, согласно изобретению, снабжена устройством для окисления железосодержащего вещества - полупродукта, содержащего оксиды железа (III) и ферриты щелочных металлов, в расплаве гидроксидов щелочных металлов до получения готового продукта, содержащего ферраты (IV) и (VI) щелочных металлов, включающим реакционную камеру с устройством внешнего нагрева, блок управления режимами нагрева и устройство для подачи кислорода в реакционную камеру, а устройство для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов содержит, по меньшей мере, один, железосодержащий съемный электрод и снабжено блоком управления режимами работы электродов.
Корпус устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов может быть выполнен из огнеупорного материала, обладающего свойствами диэлектрика, при этом указанное устройство содержит, по меньшей мере, два электрода, погруженные в расплав, и снабжено средством для подачи и размещения железосодержащего вещества в объеме расплава, образующегося при пропускании через него электрического тока.
Корпус устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов может быть выполнен металлическим, например, из стали, и является при этом одним из электродов, причем, по крайней мере, один, железосодержащий съемный электрод расположен над корпусом, для создания ограниченной зоны расплава при пропускании через расплав электрического тока, размеры которой достаточны для формирования в расплаве реакционной массы полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов.
Корпус устройства для окисления исходного железосодержащего вещества может быть выполнен в виде металлической монолитной плиты произвольной формы с замкнутой прямоугольной, или трапециевидной, или овальной выемкой для размещения реакционной массы.
Возможно выполнение корпуса устройства для окисления исходного железосодержащего вещества в виде бруска, имеющего вытянутую по длине бруска выемку прямоугольной, или трапециевидной, или овальной формы для размещения реакционной массы.
По меньшей мере, один электрод установлен в корпусе устройства для окисления исходного железосодержащего вещества с возможностью взаимного перемещения относительно корпуса и/или других электродов в горизонтальной и вертикальной плоскостях для изменения положения и размеров зоны расплава и/или изменения электросопротивления расплава.
Устройство для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов снабжено дозирующим устройством для подачи железосодержащего вещества и/или сульфатов щелочных металлов, установленным перед, по меньшей мере, одним из электродов.
Электроды могут быть расположены вертикально, при этом дозирующее устройство для подачи железосодержащего вещества и/или сульфатов щелочных металлов установлено с возможностью размещения железосодержащего вещества на дне корпуса.
По меньшей мере, один электрод может быть расположен горизонтально, при этом дозирующее устройство для подачи железосодержащего вещества и/или сульфатов щелочных металлов установлено с возможностью размещения железосодержащего вещества в объеме расплава на поверхности этого электрода.
Блок управления режимами работы электродов включает трансформатор и блок-преобразователь для управления фазовыми характеристиками электрического тока.
Устройство для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов содержит вспомогательный электрод для начального перевода кристаллических соединений щелочных металлов в расплавленную форму при подключении этого электрода к блоку управления режимами работы электродов.
В качестве реакционной массы в устройстве для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов используют смесь исходного железосодержащего вещества и кристаллических соединений щелочных металлов.
В качестве исходного железосодержащего вещества используют металлическое железо, и/или его сплавы, и/или отходы металлообработки изделий из черных металлов, например, скрап, и/или отходы черной металлургии, а в качестве соединений щелочных металлов используют кристаллические сульфаты натрия и/или калия и/или промышленные отходы, содержащие кристаллические сульфаты натрия и/или калия.
В качестве железосодержащего вещества - полупродукта используют полупродукт, содержащий оксид железа (III) и ферриты щелочных металлов, полученный предварительно в устройстве для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов, а в качестве соединений щелочных металлов используют гидроксиды натрия, и/или калия, и/или промышленные отходы, содержащие гидроксиды натрия и/или калия.
Реакционная камера устройства для окисления железосодержащего вещества - полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов, в расплаве гидроксида натрия или калия может быть выполнена в форме цилиндра или параллелепипеда и установлена вертикально или под углом к вертикальной оси, при этом длина реакционной камеры превышает ее поперечные размеры.
Возможен вариант, когда реакционная камера устройства для окисления железосодержащего вещества - полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов, в расплаве гидроксида натрия и/или калия установлена горизонтально и имеет плоское дно произвольной формы, по которому реакционная масса равномерно распределяется тонким слоем.
Реакционная камера устройства для окисления железосодержащего вещества - полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов, в расплаве гидроксида натрия и/или калия может быть установлена под углом к горизонту для обеспечения, за счет сил гравитации, продвижения реакционной массы вдоль реакционной камеры и одновременного перемешивания реагентов и взаимодействия их с кислородом, содержащимся в газовоздушной смеси, которая подается на поверхность расплава.
Устройство для окисления железосодержащего вещества - полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов, снабжено устройством загрузки полупродукта, и гидроксидов натрия и/или калия и устройством выгрузки хотя бы части готового продукта, содержащего ферраты (IV) и (VI) щелочных металлов.
Установка снабжена устройством, обеспечивающим хранение полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов и его транспортировку в реакционную камеру устройства для окисления полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов в расплаве гидроксидов натрия и/или калия.
Получение ферратов щелочных металлов в две стадии предусматривает на первой стадии окисление металлического железа расплавом сульфатов щелочных металлов до, преимущественно, соединений железа (III) и на второй стадии дальнейшее их окисление кислородом в расплаве гидроксидов щелочных металлов. При осуществлении первой стадии процесса, которая требует применения достаточно высоких температур, снижаются требования к однородности состава получающихся веществ и, как следствие, уменьшаются продолжительность процесса и затраты энергии на проведение реакций, а в качестве исходных веществ могут быть использованы технологические отходы различных производств.
Использование расплава гидроксидов щелочных металлов, имеющих по сравнению с сульфатами щелочных металлов более низкие температуры плавления, позволяет снизить границы температурного интервала, в котором происходит образование ферратов щелочных металлов и, тем самым, уменьшить общее энергопотребление.
Стадия получения полупродукта, содержащего оксид железа (III) и ферриты натрия и/или калия, резко снижает продолжительность процесса окисления железа в расплавах сульфатов натрия и/или калия, т.к. не требует их подачи в расплавленном виде, исключая их предварительное расплавление, не требует снижения массовой доли соединений серы до 1% и не требует непрерывной подачи кислорода в расплав. В результате резко сокращаются затраты энергии и снижаются требования к качеству исходных веществ.
Замена расплавов сульфатов натрия и/или калия на расплавы гидроксидов натрия и/или калия на второй стадии окисления железосодержащего вещества при непрерывной подаче кислорода позволяет снизить температуру получения целевого (готового) продукта и повысить его окислительную способность за счет образования смеси ферратов (IV) и (VI) натрия и/или калия.
Для сокращения энергозатрат окисление железосодержащего вещества в расплаве сульфатов натрия и/или калия осуществляется в реакционной камере при отсутствии устройства для барботирования газовоздушной смеси. Окисление, в соответствии с реакциями (2), осуществляют до образования оксидов железа и ферритов натрия и/или калия, а контроль полноты протекания реакций окисления железосодержащего вещества проводят по содержанию окисленных форм железа, что резко сокращает продолжительность процесса окисления железа и/или железного лома по сравнению с прототипом, в котором процесс ведут до достижения остаточного содержания сульфатов щелочных металлов 1%.
В отличие от прототипа корпус реакционной камеры может быть выполнен как из диэлектрического материала, так и быть металлическим, например, сделанным из стали, нагрев реакционной массы может осуществляться за счет электрического тока, пропускаемого через расплав, или внешним нагревателем любого типа, например, с помощью теплоэлектронагревателей или газовых горелок, а вместо пакета электродов использован хотя бы один съемный электрод, который изготавливается из теплоэлектронагревателей или газовых горелок, а вместо пакета электродов использован хотя бы один съемный электрод, который изготавливается из металлического лома, что позволяет использовать металлические отходы различных размеров, формы и происхождения.
Блок управления режимами работы электродов позволяет плавно изменять фазовые и амплитудные характеристики переменного тока, глубину погружения хотя бы одного из электродов в расплав соли, а также взаимное положение хотя бы одного из электродов относительно другого или других электродов и/или относительно корпуса.
Блок управления режимами работы электронагревателей позволяет плавно изменять фазовые и амплитудные характеристики переменного тока, поддерживая заданные температурные режимы процесса получения готового продукта.
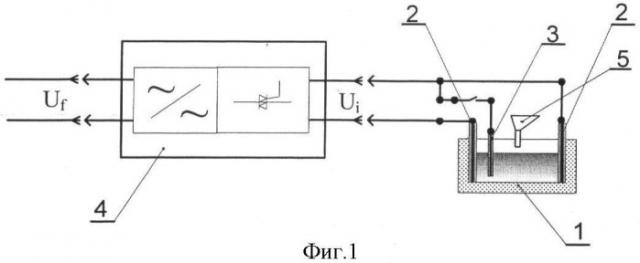
На фиг.1 представлена схема устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов до получения полупродукта (корпус для размещения реакционной массы выполнен из огнеупорного материала, электроды вертикально расположены в расплаве сульфата щелочного металла).
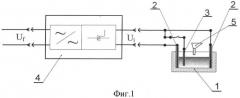
На фиг.2 представлена схема устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов до получения полупродукта (корпус для размещения реакционной массы выполнен из огнеупорного материала, один или несколько электродов вертикально расположены в расплаве сульфата щелочного металла, один из электродов горизонтально расположен в расплаве).
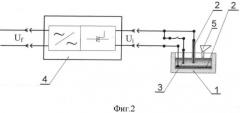
На фиг.3 представлена схема устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов до получения полупродукта (корпус для размещения реакционной массы выполнен металлическим в виде монолитной плиты (круга) с замкнутой прямоугольной выемкой, электроды вертикально расположены в расплаве сульфата щелочного металла).
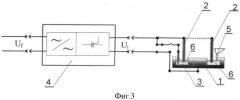
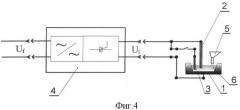
На фиг.4 представлена схема устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов до получения полупродукта (корпус для размещения реакционной массы выполнен металлическим в виде бруска с вытянутой по длине трапециевидной выемкой, электроды вертикально расположены в расплаве сульфата щелочного металла).
На фиг.5 представлена схема устройства для окисления полупродукта в расплаве гидроксидов щелочных металлов, содержащего вертикально расположенную реакционную камеру.
На фиг.6 представлена схема устройства для окисления полупродукта в расплаве гидроксидов щелочных металлов, содержащего горизонтально расположенную реакционную камеру.
На фиг.7 представлена схема устройства для окисления полупродукта в расплаве гидроксидов щелочных металлов, содержащего реакционную камеру, расположенную под углом к горизонту.
На фиг.8 представлена схема изогнутой реакционной камеры в устройстве для окисления полупродукта в расплаве гидроксидов щелочных металлов.
На фиг.9 представлена схема наклонной реакционной камеры в устройстве для окисления полупродукта в расплаве гидроксидов щелочных металлов.
На фиг.10 представлена схема наклонной вращающейся реакционной камеры в устройстве для окисления полупродукта в расплаве гидроксидов щелочных металлов.
На фиг.11 представлена форма электрического напряжения сети Uf, которое используется для преобразования в питающее напряжение.
На фиг.12 представлена форма питающего напряжения Ui на выходе блока управления для пакетно-импульсного режима преобразования.
На фиг.13 представлена форма питающего напряжения Ui на выходе блока управления для импульсно-фазового режима преобразования.
На фиг.14 представлена форма питающего напряжения Ui на выходе блока управления для выпрямляющего режима преобразования.
На фиг.15 представлена форма питающего напряжения Ui на выходе блока управления для поляризующего режима преобразования.
На фиг.16 представлен общий вид устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов до получения полупродукта, разрез которого показан на фиг.3 (корпус для размещения реакционной массы выполнен металлическим в виде монолитной плиты (круга) с замкнутой прямоугольной выемкой, электроды вертикально расположены в расплаве сульфата щелочного металла).
На фиг.17 представлен общий вид устройства для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов до получения полупродукта, разрез которого показан на фиг.4 (корпус для размещения реакционной массы выполнен металлическим в виде плоского бруска линейной формы с вытянутой по длине трапециевидной выемкой, электроды вертикально расположены в расплаве сульфата щелочного металла).
Способ получения окислителя на основе ферратов щелочных металлов осуществляют в две стадии. На первой стадии ведут окисление исходного железосодержащего вещества в расплаве сульфатов щелочных металлов при пропускании через расплав электрического тока до получения железосодержащего вещества - полупродукта, содержащего оксиды железа (III) и ферриты щелочных металлов. На второй стадии осуществляют последующее окисление оксидов железа и ферритов щелочных металлов, содержащихся в полупродукте, в расплаве гидроксидов щелочных металлов, в присутствии кислорода до получения продукта, содержащего ферраты (IV) и (VI) щелочных металлов.
При выборе сырья преимущество отдавалось нетоксичным и недорогим материалам, производимым в достаточных количествах химической промышленностью или образующихся в виде отходов в металлургических и металлообрабатывающих технологиях. На первой стадии процесса окисления в качестве исходного железосодержащего вещества используют металлическое сырье в виде металлического железа, и/или его сплавы и/или отходы металлообработки изделий из черных металлов, например, скрап, и/или отходы черной металлургии.
В качестве исходных веществ - сульфатов щелочных металлов - на первой стадии способа используют сульфаты натрия и/или калия, и/или промышленные отходы, содержащие сульфаты натрия и/или калия.
В качестве гидроксидов щелочных металлов на второй стадии способа используют гидроксиды натрия и/или калия и/или промышленные отходы, содержащие гидроксиды натрия и/или калия.
Суммарный процесс превращения сульфата натрия и стальных электродов в феррат (IV) натрия представлен следующей схемой:
Окисление железосодержащего вещества осуществляют в фазе расплава. Температурный интервал первой стадии процесса определяется температурами плавления сульфатов натрия, калия, а также продуктов их разложения и составляет 850-1100°С. Ниже 850°С наблюдается загустевание реакционной массы, а выше 1100°С происходит образование магнетита, который в дальнейшем практически не поддается переводу в ферраты (IV) и (VI) щелочных металлов.
Основные реакции, связанные с окислением железосодержащего вещества в расплаве сульфатов натрия и/или калия приводят к образованию смеси, содержащей преимущественно оксид железа (III), ферриты натрия и/или калия и оксиды натрия и/или калия:
Продукт окисления железа в расплаве сульфата натрия и/или калия после охлаждения представляет собой поликристаллический многокомпонентный сплав, состав которого зависит от исходного отношения (Na,K)2SO4:Fe, температуры и продолжительности взаимодействия железа с расплавами сульфатов щелочных металлов.
Первую стадию ведут до достижения массовой доли соединений железа (III) в полупродукте 4-39%, в пересчете на железо. Содержание железа в полупродукте контролируется химическими методами анализа.
В основе процессов, протекающих на первой стадии, лежат химические реакции взаимодействия металлического железа в расплаве (Na,K)2SO4 в соответствии с уравнением (2). В простейшем случае для проведения этих реакций требуется расплав, для получения которого используется косвенный нагрев от независимого источника тепла, например муфельная или шахтная или тоннельная печи. В заявляемом способе осуществляется электрохимическое окисление железного анода в указанных расплавах, причем электрический ток используется одновременно для поддержания необходимой температуры расплава.
В заявляемом способе реализованы два варианта первой стадии, различающиеся условиями окисления железосодержащего вещества в расплаве сульфатов натрия или калия - электрохимическое растворение железного анода, который изготавливается из железосодержащего вещества, например, лома черных металлов и комбинация химического и электрохимического окисления железа.
Электрический ток обеспечивает прямой нагрев реакционной массы, поддерживая необходимую температуру расплава, и служит для интенсификации процессов окисления металлического железа.
Для электрохимического растворения железа используют выпрямленный или переменный ток любой конфигурации. В случае использования выпрямленного тока окислению подвергается электрод из железосодержащего вещества, соединенный с положительным полюсом внешнего источника тока, а при использовании знакопеременного тока окисляется электрод (анод), на который подается положительный импульс или положительная полуволна.
В результате окисления железного анода в расплаве последовательно образуются соединения железа (II) и железа (III).
Одновременно с окислением железосодержащего вещества на аноде происходит разложение сульфат-ионов. Образующиеся в результате этих процессов оксид серы (VI) и кислород ускоряют растворение металлического железа в расплаве сульфатов натрия и калия.
Электрод, который поляризован отрицательно (катод) является инертным, и материал, из которого он изготовлен, электрохимическому окислению не подвергается и расходуется только в результате окисления кислородом воздуха. Основные реакции, которые протекают в катодном пространстве, связаны с восстановлением сульфат-ионов в соответствии со схемой (3)
В объеме расплава из образующихся катионов и анионов формируются оксиды и сульфиды железа (II) и железа (III), оксиды щелочных металлов, сульфаты и сульфиты железа (III), сульфит и сульфиды щелочных металлов. Между катионами железа (II) и сульфат-ионами протекают реакции, приводящие к образованию феррит-ионов:
которые после охлаждения образуют ферриты щелочных металлов.
Поскольку реакции осуществляются в атмосферном воздухе, образующиеся феррит-ионы в присутствии кислорода частично окисляются до феррат(IV)-анионов:
соответствующих образованию ферратов (IV) щелочных металлов.
В условиях проведения первой стадии процесса реакция (5) протекает с небольшим выходом ферратов щелочных металлов, и в дальнейшем они рассматриваются как примеси, существенно не влияющие на качество образующегося полупродукта, хотя и облегчающие проведение второй стадии получения реагента-окислителя.
Комбинация химического и электрохимического окисления железа является предпочтительным вариантом первой стадии осуществления способа. Электрический ток одновременно используется для окисления железного анода, который может быть выполнен из железосодержащего вещества, например железного лома, и для поддержания необходимой температуры расплава, в котором растворяется железосодержащее вещество в виде технологических отходов, например отходов металлообработки железа и его сплавов, в частности стружки или сыпучих полидисперсных металлических масс.
Для электрохимического растворения железа используется выпрямленный или переменный ток любой конфигурации. Протекающий через расплав электрический ток увеличивает скорость химического окисления железа сульфатом натрия или калия. Для уменьшения поляризационных процессов, связанных с накоплением вблизи поверхности растворяемого железосодержащего вещества продуктов электролиза, которые замедляют окисление металлического железа, предпочтительно использовать знакопеременную форму тока или комбинацию переменного тока с частичной поляризацией одного из электродов выпрямленным напряжением.
Особенности комбинированного химического и электрохимического взаимодействия железосодержащего вещества с расплавом сульфатов щелочных металлов связаны с направленным перемещением ионов в расплаве электролита, что приводит к росту скорости окисления металлического железа. Также в результате катодного восстановления катионов щелочных металлов в объеме расплава образуются металлические натрий и калий, окисляющиеся при контакте с кислородом воздуха до пероксида Na2O2 и надпероксида КО2, которые обладают сильными окислительными свойствами и ускоряют окисление железосодержащего вещества.
По окончании первой стадии окисления железосодержащего вещества в расплаве сульфата натрия и/или калия образуется полупродукт, содержащий преимущественно оксид железа (III) и ферриты натрия и/или калия. Полупродукт применяется в качестве железосодержащего вещества на второй стадии процесса для получения ферратов (IV) и (VI) натрия и/или калия, как в виде расплавленной массы непосредственно после окончания первой стадии процесса, так и в виде кристаллической массы по истечении любого интервала времени после охлаждения. Охлажденный полупродукт представляет собой поликристаллический многокомпонентный сплав от темно-бурой до темно-коричневой окраски. Основу полупродукта составляет поликристаллическая смесь оксида железа (III) и ферритов натрия и калия, содержащая в виде примесей сульфиды, сульфаты и сульфиты железа, оксиды, сульфаты, сульфиты и сульфиды натрия и калия. Полупродукт содержит также ферраты (IV) натрия и калия, которые облегчают протекание второй стадии получения реагента-окислителя на основе ферратов (IV) и (VI) щелочных металлов.
Срок хранения полупродукта не ограничен, что позволяет накапливать его в необходимых количествах, транспортировать на любые расстояния и использовать по мере необходимости. Перед применением кристаллический полупродукт рекомендуется измельчать.
На второй стадии процесса получения ферратов (IV) и (VI) щелочных металлов в качестве железосодержащего вещества используют полупродукт, содержащий соединения железа (III) в виде оксида железа (III) и ферритов натрия и/или калия, а в качестве соединений щелочных металлов используют гидроксиды натрия и/или калия, и/или промышленные отходы, содержащие гидроксиды натрия и/или калия. Вторая стадия осуществляется в расплаве при непрерывной подаче кислорода в объем или на поверхность расплава в составе газовоздушной смеси, содержащей по объему 21-100% газообразного кислорода.
Протекающие на второй стадии реакции превращения железосодержащего вещества в расплаве при непрерывной подаче кислорода приводят к образованию смеси, содержащей ферраты (IV) и (VI) натрия и калия
Поскольку гидроксиды натрия и калия имеют значительно меньшие температуры плавления, по сравнению с сульфатами натрия и калия, окисление железосодержащего вещества на второй стадии процесса осуществляют при более низких температурах расплава, что резко снижает расход энергии на осуществление всего процесса. Температурный интервал второй стадии процесса составляет 640-880°С. Ниже 640°С скорости реакций становятся настолько малыми, что процесс образования ферратов (IV) и (VI) практически прекращается, а выше 880°С происходит термическое разложение образующихся ферратов (IV) и (VI) щелочных металлов.
Вторую стадию ведут до достижения массовой доли соединений железа (IV) и (VI) в продукте 2,7-21,8%, в пересчете на железо (VI). Содержание окисленных форм железа в продукте контролируется химическими и спектрофотометрическими методами анализа.
Заявляемая установка для получения окислителя на основе ферратов щелочных металлов обеспечивает получение окислителя на основе ферратов (IV) и (VI) щелочных металлов в две стадии и включает устройство для окисления исходного железосодержащего вещества в расплаве сульфатов щелочных металлов до получения полупродукта, содержащего оксиды железа (III) и ферриты щелочных металлов, и устройство для окисления полупродукта, содержащего оксид железа (III) и ферриты щелочных металлов, в расплаве гидроксидов щелочных металлов.
Устройство для окисления исходного железосодержащего вещества в расплаве сульфатов щ