Замещенные арилпиразолы в качестве агентов для уничтожения паразитов
Иллюстрации
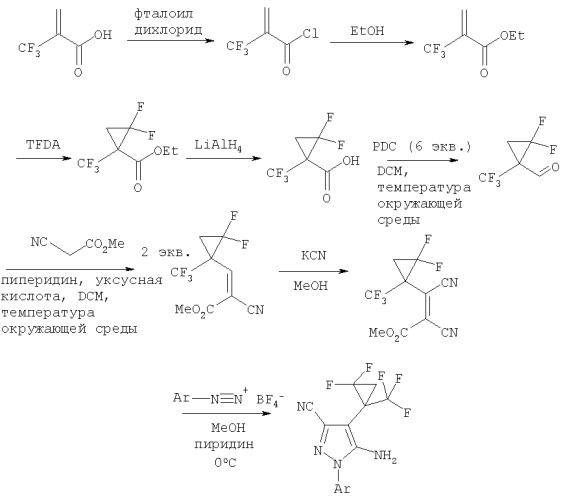
Показать всеИзобретение относится к комбинированному продукту, содержащему соединение формулы (I):
где R1 и R2 представляют собой СF3; R3 и R4 представляют собой фторо; R5 и R6 представляют собой водород; R7 представляет собой Сl; Х представляет собой CR8, где R8 представляет собой Сl; и R9 представляет собой NH2; или его ветеринарно приемлемую соль, и б) дорамектин. Изобретение также относится к противопаразитарной ветеринарной композиции на основе указанного комбинированного продукта. Технический результат - получение комбинированного продукта, который может быть использован в ветеринарии для лечения паразитарной инфекции у млекопитающих. 4 н.п. ф-лы, 1 ил., 1 табл.
Реферат
Настоящее изобретение относится к производным пиразола, имеющим противопаразитарные свойства. Представляющие интерес соединения являются фторированными циклопропиларилпиразолами и, более конкретно, настоящее изобретение относится к 1-арил-4-циклопропилпиразолам, в которых присутствует по меньшей мере один атом фтора, присоединенный к циклопропильному кольцу.
В публикации международной заявки на патент WO 9824767, публикациях заявок на европейский патент ЕР933363 и ЕР957094 описаны 4-циклопропиларилпиразолы, обладающие противопаразитарными свойствами для борьбы с членистоногими.
Соединения из уровня техники не всегда демонстрируют хорошую активность или длительное время действия против паразитов. Аналогично, некоторые противопаразитарные агенты полезны только в отношении узкого ряда паразитов. Цель настоящего изобретения заключается в том, чтобы преодолеть различные недостатки или улучшить свойства соединений из уровня техники. Таким образом, цель настоящего изобретения заключается в том, чтобы предложить арилпиразол, который имеет улучшенную активность против паразитов по сравнению с соединениями из уровня техники. Соединения по настоящему изобретению обладают особенно хорошей способностью контролировать широкий ряд членистоногих, как видно из результатов тестов, демонстрирующих их активность и эффективность. В частности, соединения по изобретению гораздо более активны в отношении блох, чем аналогичные соединения из уровня техники.
Еще одной целью является предложение соединений с длительным временем действия. Наиболее предпочтительно, соединения сдерживают инвазию членистоногими паразитами в течение периода времени по меньшей мере двадцать восемь суток. Пролонгированное действие обычно относится к пролонгированному периоду полувыведения соединения in vivo в хозяине-млекопитающем.
Также нужно, чтобы соединения по настоящему изобретению имели улучшенный фармакокинетический профиль, улучшенную безопасность, улучшенную устойчивость и улучшенную растворимость.
Таким образом, согласно настоящему изобретению предложено соединение формулы (I):
где
R1 представляет собой CF3, OCF2H, ОСF3, -SCF3, -SOCF3, -SО2СF3 или SF5;
R2 представляет собой Н, фторо или С1-4алкил, возможно замещенный 1-5 атомами галогена, независимо выбранными из хлоро и фторо;
R3, R4, R5 и R6 независимо представляют собой Н, С1-4алкил, возможно замещенный 1-5 галогеновыми группами, независимо выбранными из хлоро и фторо либо хлоро или фторо;
R7 представляет собой Cl или фторо;
Х представляет собой CR8 или N, где R8 представляет собой Cl или фторо; и
R9 представляет собой NRaRb;
Ra выбран из водорода, C1-6алкила, С2-6алкенила, С3-8циклоалкила, группы С(O)ОС1-6алкил и С1-6алканоила, где каждая из вышеуказанных групп может включать, где это химически возможно, один или более чем один возможный заместитель, независимо выбранный из галогено, het, фенила, гидрокси, групп -С(O)ОН, -С(O)ОС1-6алкила, C1-6алкила, C1-6галогеналкила, С3-8циклоалкила, С1-6алкокси, С1-6галогеналкокси, амино, С1-6алкиламино и ди-С1-6алкиламино;
Rb выбран из водорода, С1-6алкила, С2-6алкенила, С1-6алканоила и группы С(O)ОС1-6алкила, где каждая из вышеуказанных групп может включать, где это химически возможно, один или более чем один возможный заместитель, независимо выбранный из галогено, фенила, гидрокси, групп -СООН, -С(O)ОС1-6алкил, С1-6алкила, С1-6галогеналкила, С3-8циклоалкила, С1-6алкокси, С1-6галогеналкокси, амино, С1-6алкиламино и ди-С1-6алкиламино;
или Ra и Rb вместе с атомом N, к которому они присоединены, могут образовывать 3-7-членное гетероциклическое кольцо, содержащее один или более чем один дополнительный атом N, О или S, и где указанное гетероциклическое кольцо может нести один или более чем один возможный заместитель, выбранный из оксо, галогено, het, фенила, гидрокси, групп -СООН, -С(O)ОС1-6алкил, С1-6алкила, С1-6галогеналкила, С3-8циклоалкила, С1-6алкокси, С1-6галогеналкокси, амино, С1-6алкиламино и ди-С1-6алкиламино; и
het представляет собой 4-7-членную гетероциклическую группу, которая является ароматической или неароматической и которая содержит один или более чем один гетероатом, выбранный из азота, кислорода, серы и их смесей, и где указанное гетероциклическое кольцо возможно замещено, где это позволяет валентность, одним или более заместителями, выбранными из галогено, циано, нитро, С1-6алкила, С1-6галогеналкила, С1-6алкокси, групп ОС(O)С1-6алкил, С(O)С1-6алкил, С(O)ОС1-6алкил и NRcRd, где Rc и Rd независимо выбраны из водорода, С1-6алкила и С2-6алкенила, причем каждая из вышеуказанных групп может включать, где это химически возможно, один или более чем один возможный заместитель, независимо выбранный из галогено, фенила, гидрокси, группы -СООН, С(O)ОС1-6алкил, С1-6алкила, С1-6галогеналкила, С3-8циклоалкила, С1-6алкокси, С1-6галогеналкокси, амино, С1-6алкиламино и ди-С1-6алкиламино; или его фармацевтически приемлемую соль или пролекарство;
при условии, что по меньшей мере один из R2, R3, R4, R5 или R6 представляет собой фторо.
В соединениях формулы (I) С1-6галогеналкил или С1-6галогеналкокси означает С1-6алкил или С1-6алкокси, замещенный 1-5 группами хлоро или фторо, выбранными независимо. Также "галогено" означает группу, выбранную из фторо, бромо, хлоро, бромо или йодо.
Подходящим образом R1 представляет собой СF3 или SF5, предпочтительно СF3.
Подходящим образом R2 представляет собой СF3 или CHF2, предпочтительно СF3. В альтернативном подходящем воплощении R2 представляет собой фторо.
Подходящим образом R3, R4, R5 и R6 независимо представляют собой Н или фторо.
Предпочтительно R2 представляет собой СF3, и R3, R4, R5 и R6 независимо представляют собой 2, 3 или 4 группы фторо, более предпочтительно 2 группы фторо, наиболее предпочтительно на R3, и R4, и R5 и R6 представляют собой Н.
Также предпочтительно R2 представляет собой CHF2, и R3, R4, R5 и R6 независимо представляют собой 2, 3 или 4 группы фторо, более предпочтительно 2 группы фторо, наиболее предпочтительно на R3, и R4, и R5 и R6 представляют собой Н.
Также предпочтительно R2 представляет собой фторо, и R3, R4, R5 и R6 независимо представляют собой 2, 3 или 4 группы фторо, более предпочтительно оба R3 и R4 представляют собой фторо, и R5 и R6 представляют собой Н, или все из R3, R4, R5 и R6 представляют собой фторо.
Предпочтительно Х представляет собой CR8. Более предпочтительно R8 представляет собой хлоро.
Другими предпочтительными соединениями являются те, в которых R7 и R8 одинаковые. Более предпочтительно оба R7 и R8 представляют собой Cl.
Подходящим образом R3 представляет собой С(O)ОС1-6алкил, например этил, пропил или изопропил, с возможным замещением, выбранным из групп фторо в количестве от одной до пяти, например с образованием 2,2,2-трифторэтила, ди-С1-6алкиламино, например диметиламино, и net, например, пирролидинил, пиридил и имидазолил. Более подходящим образом R3 представляет собой этоксикарбонил, диметиламиноэтоксикарбонил, 2,2,2-трифторэтоксикарбонил, изопропоксикарбонил, 4-пиридилметоксикарбонил, 3-пиридилметоксикарбонил, 2-пиридилметоксикарбонил, 1Н-имидазол-5-илметоксикарбонил или 2-пирролидин-1-илэтоксикарбонил.
Также подходящим образом Ra представляет собой С1-6алкил, например метил, с возможным замещением, выбранным из групп фторо в количестве от одной до пяти, например с образованием трифторметила, С3-8циклоалкил, например циклогексил, фенил и net, например пиридил, например 4-пиридил, пиперидинил, морфолинил, пирролидинил или пиперазинил. Более подходящим образом Ra представляет собой метил или 4-пиридилметил.
Также подходящим образом Ra и Rb вместе с атомом N, к которому они присоединены, образуют пирролидинил, пиперидинил, пиперазинил, морфолинил или 2-оксо-оксазолидинил, например группу 2-оксо-1,3-оксазолидин-3-ил, более подходящим образом группу 2-оксо-1,3-оксазолидин-3-ил.
Подходящим образом Rb представляет собой водород.
Предпочтительно или альтернативно R9 выбран из NH2, С1-6алкоксикарбониламино, с возможным замещением по группе алкокси одной-пятью группами фторо, ди-С1-6алкиламино и het, и С1-6 алкиламино, с возможным замещением по алкильной группе одной-пятью группами фторо, С3-8циклоалкилом, фенилом и het. Наиболее предпочтительно R9 представляет собой NН2.
Предпочтительные индивидуальные соединения по изобретению выбраны из:
5-амино-1-[2,6-дихлор-4-пентафтортиофенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(1,2,2-трифторциклопропил)-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(пентафторциклопропил)-1Н-пиразол-3-карбонитрила;
5-амино-4-(2,2-дихлор-1-фторциклопропил)-1-[2,6-дихлор-4-(трифторметил)фенил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-пентафтортиофенил]-4-(пентафторциклопропил)-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-пентафтортиофенил]-4-(1,2,2-трифторциклопропил)-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[1-(дифторметил)-2,2-дифторциклопропил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(2,2-дифторциклопропил)-1Н-пиразол-3-карбонитрила;
5-амино-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1-[2,6-дифтор-4-(трифторметил)фенил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-пентафтортиофенил]-4-[1-(дифторметил)-2,2-дифторциклопропил]-1Н-пиразол-3-карбонитрила;
5-aминo-4-{1-[xлop(фтop)метил]-2,2-дифтopциклoпpoпил}-1-[2,6-диxлop-4-(трифторметил)фенил]-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[1-(дифторметил)-2,2,3,3-тетрафторциклопропил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2,3,3-тетрафтор-1-(трифторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-5-(метиламино)-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметокси)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметокси)фенил]-4-[1-(дифторметил)-2,2,3,3-тетрафторциклопропил]-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметокси)фенил]-4-[1-(дифторметил)-2,2-дифторциклопропил]-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(фторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-(2,2-дифтор-1-метилциклопропил)-1Н-пиразол-3-карбонитрила;
5-амино-1-{2,6-дихлор-4-[(трифторметил)тио]фенил}-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-3-карбонитрила;
этил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-5-илкарбамата;
1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-5-(2-оксо-1,3-оксазолидин-3-ил)-1Н-пиразол-3-карбонитрила;
5-амино-1-[3-хлор-5-(трифторметил)пиридин-2-ил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
2-(диметиламино)этил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-5-илкарбамата;
2,2,2-трифторэтил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-5-илкарбамата;
5-амино-1-{2,6-дихлор-4-[(трифторметил)сульфонил]фенил}-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-3-карбонитрила;
1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-5-[(пиридин-4-илметил)амино]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-(дифторметокси)фенил]-4-[2,2-дифтор-1 -(трифторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-пентафтортиофенил]-4-[1-(дифторметил)-2,2,3,3-тетрафторциклопропил]-1Н-пиразол-3-карбонитрила;
изопропил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1Н-пиразол-5-илкарбамата;
пиридин-4-илметил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-5-илкарбамата;
пиридин-3-илметил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1Н-пиразол-5-ил]-карбамата;
пиридин-2-илметил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1Н-пиразол-5-илкарбамата;
1Н-имидазол-5-илметил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-5-илкарбамата;
2-пирролидин-1-илэтил-3-циано-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-5-илкарбамата; и
5-амино-4-{1-[хлор(дифтор)метил]-2,2-дифторциклопропил}-1-[2,6-дихлор-4-(трифторметил)фенил]-1Н-пиразол-3-карбонитрила; или их фармацевтически приемлемой соли или пролекарства.
Более предпочтительные индивидуальные соединения по настоящему изобретению выбраны из:
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1H-пиразол-3-карбонитрила;
(-)-5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
5-aминo-1-[2,6-диxлop-4-(тpифтopмeтил)фeнил]-4-[1-(дифтopмeтил)-2,2-дифторциклопропил]-1H-пиразол-3-карбонитрила;
5-амино-1-[2,6-дихлор-4-пентафтортиофенил]-4-[1-(дифторметил)-2,2-дифторциклопропил]-1Н-пиразол-3-карбонитрила;
5-aминo-4-{1-[хлор(фтор)метил]-2,2-дифтopциклoпpoпил}-1-[2,6-диxлop-4-(трифторметил)фенил]-1Н-пиразол-3-карбонитрила;
5-aминo-1-[2,6-диxлop-4-(тpифтopмeтил)фeнил]-4-[1-(дифтopмeтил)-2,2,3,3-тетрафторциклопропил]-1Н-пиразол-3-карбонитрила; и
5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2,3,3-тетрафтор-1-(трифторметил)циклопропил]-1Н-пиразол-3-карбонитрила;
или их фармацевтически приемлемой соли или пролекарства.
В объем изобретения входят так называемые "пролекарства" соединений формулы (I). Так, некоторые производные соединений формулы (I), которые сами могут обладать незначительной фармакологической активностью или не обладать ею, могут, при введении на или в организм, превращаться в соединения формулы (I), обладающие нужной активностью, например посредством гидролитического расщепления. Такие производные упоминаются как "пролекарства". Понятно, что некоторые соединения формулы (I) сами могут действовать как пролекарства других соединений формулы (I). Дополнительную информацию по применению пролекарств можно найти в 'Pro-drugs as Novel Delivery Systems, Vol.14, ACS Symposium Series (T Higuchi и W Stella) и 'Bioreversible Carriers in Drug Design', Pergamon Press, 1987 (ed. E В Roche, American Pharmaceutical Association).
Пролекарства в соответствии с настоящим изобретением могут, например, быть получены путем замещения 5-амино-заместителя на пиразольном кольце в соединениях формулы (I) определенными группировками, известными специалисту в данной области техники как "пролекарственные группировки", как описано, например, в "Design of Prodrugs" Н Bundgaard (Elsevier, 1985); "Design и application of prodrugs," Textbook of Drug Design и Discovery, (3rd Edition), 2002, 410-458, (Taylor и Francis Ltd., London); и ссылках, приведенных в них.
Подходящие пролекарства могут иметь N-содержащую группу в положении 5 пиразольного кольца формулы (I) и присоединяться к кольцу через N. 5-N-группа может быть одно- или двузамещенной. Примеры заместителей включают: алкиламины, ариламины, амиды, мочевины, карбаматы, циклические карбаматы, имины, енамины, имиды, циклические имиды, сульфенамиды и сульфонамиды. Углеводородная часть этих групп содержит С1-6алкил, фенил, гетероарил, такой как пиридил, С2-6алкенил и С3-8циклоалкил; где каждая из вышеперечисленных групп, где это химически возможно, может включать один или более чем два возможных заместителя, независимо выбранных из: галогено; гидрокси; С1-6алкила и С1-6алкокси.
Дополнительные примеры замещающих групп в соответствии с вышеприведенными примерами и примерами других типов пролекарств можно найти в вышеуказанных ссылках.
Пролекарство согласно изобретению может быть легко идентифицировано посредством введения его подопытному животному и отбора пробы жидкости тела на соединение формулы (I).
В дополнительном аспекте в настоящем изобретении предложены способы получения соединения формулы (I) или его приемлемой фармацевтически, ветеринарно или в сельском хозяйстве соли, или его приемлемого фармацевтически, ветеринарно или в сельском хозяйстве сольвата (включая гидрат) любой категории, как проиллюстрировано ниже.
Специалисту в данной области техники понятно, что для чувствительных функциональных групп может требоваться защита и снятие защиты в ходе синтеза соединений по изобретению. Этого можно достичь обычными способами, например, как описано в "Protective Groups in Organic Synthesis" TW Greene и PGM Wuts, John Wiley & Sons Inc (1999), и ссылках, приведенных там.
Таким образом, следующие способы иллюстрируют общие процессы синтеза, которые могут быть адаптированы с целью получения соединений по изобретению.
1. Соединение формулы (I) можно получить циклопропанированием алкена формулы (II):
где R1, R2, R3, R4, R7 и Х являются такими, как определено ранее для формулы (I), и R9′ представляет собой R9 или N-защищенный R9, с последующим снятием защиты, когда это необходимо. Подходящая защита включает имидоформамидную защиту, например с использованием N,N-диметилимидоформамида, которая может быть снята в стандартных условиях. Соединения формулы (II) могут взаимодействовать с карбеноидной частицей, :C5R6, в которой R5 и R6 являются такими, как определено ранее для формулы (I), которая может быть образована in situ. Например, когда R5=R6=F, реакционноспособная частица, такая как триметилсилилдифтор(фторсульфонил)ацетат (TFDA), может взаимодействовать с соединением формулы (II), где R9′ представляет собой N-защищенный R9, с возможным неполярным растворителем при повышенной температуре в присутствии фторида натрия с получением продукта формулы (I) после снятия защиты. Другие конкретные способы включают обработку хлороформа основанием, предпочтительно в условиях катализа фазового перехода, термолиз подходящего металлорганического предшественника, такого как арилтрифторметильное, трихлорметильное или фенил(трифторметил)ртутное производное, или обработку диазоалканом в присутствии катализатора - переходного металла и обработку диазоалканом в отсутствии катализатора - переходного металла с последующим термолизом промежуточного пиразолина, или получение из илида серы.
Соединение формулы (II), где R9′ представляет собой N-защищенную группу, может быть получено из соединения формулы (IV):
где X' представляет собой бромо или йод, и R1, R7 и Х являются такими, как определено ранее для формулы (11а), например посредством реакции кросс-сочетания (IV), катализируемой переходным металлом, с подходящим реагентом винилирования в подходящем, возможно дегазированном растворителе. Подходящим образом переходный металл представляет собой палладий, а реагент для винилирования представляет собой оловоорганическое производное, бороновоорганическую кислоту или цинкорганическое производное. Альтернативно, (IV) можно нагревать с обратным холодильником с алкенилбороновыми кислотами, замещенными подходящим образом, в присутствии тетракис(трифенилфосфин)палладия(0) и гидрокарбоната натрия в подходящем растворителе. Альтернативно, (IV) может быть обработано цинкорганическим соединением, например активированным цинком (таким как цинк Райка (Rieke)), в атмосфере инертного газа с подходящим бромалкеном, таким как бромтрифторэтилен или бромдифторэтилен, в апротонном растворителе в присутствии палладиевого(0) продукта, такого как тетракис(трифенилфосфин)палладий(0) при повышенной температуре. Альтернативно, (IV) может быть обработано активированным цинком (цинк Райка) в апротонном растворителе с получением органического цинката, который затем может быть подвергнут кросс-сочетанию с галогеналкеном в присутствии палладиевого(II) продукта, такого как дихлорбис(трифенилфосфин)палладий(II), и восстановителя, такого как диизобутилалюминийгидрид, при нагревании с обратным холодильником в апротонном растворителе.
Соединения формулы (IV) могут быть полезны для получения промежуточных соединений формулы (V).
Таким образом, соединение формулы (IV) может быть обработано реагентом Гриньяра, таким как изопропилмагния хлорид, в атмосфере инертного газа с использованием апротонного растворителя при пониженной температуре, затем обработано хлорангидридом или ангидридом хлоралкановой кислоты, при нагревании до комнатной температуры получают нужный кетонный продукт, представленную формулой (V).
Соединения формулы (V) можно использовать для получения соединений формулы (II), где R3 и R4 представляют собой Н, и R9 является N-защищенным. Таким образом, соединение формулы (V) может быть метиленировано при обработке реагентом Виттига в атмосфере инертного газа при пониженной температуре в растворителе, таком как тетрагидрофуран.
Соединения формулы (II), где R9 является N-защищенным, могут также быть получены из соединений формулы (V), путем обработки галогеналкеном, таким как дибромдифторметан, в присутствии трифенилфосфина и цинка Райка в апротонном растворителе.
Альтернативно, соединения формулы (II), где R9 является N-защищенным, могут быть получены из соединений формулы (IV) через соответствующий третичный спирт с последующими стандартными операциями хлорирования-дегидрохлорирования.
Соединение формулы (IV) может быть получено из соединения формулы (VI), где R1, R7 и Х такие, как ранее определено для формулы (I):
за две стандартные стадии бромирования/иодирования и защиты, любая из которых может быть осуществлена первой. Соединения формулы (VI) могут быть легко защищены, например в виде имидоформамида, и затем могут быть превращены непосредственно в соединения формулы (V) путем взаимодействия с реакционноспособным ангидридом кислоты в аполярном растворителе.
2. Соединение формулы (I) также можно получить путем получения требуемого карбеноидного продукта из пиразолсодержащего предшественника и обработки его соответствующим алкеном. Например, алкилметаллическую соль, предпочтительно литиевую соль, соединения формулы (VII):
где Аr представляет собой фенил или нафтил, любой из которых возможно замещен С1-С4алкилом, С1-С4алкокси или галогено, и R1, R2, R7, R9 и Х являются такими, как определено ранее, можно термически разложить в присутствии катализатора - переходного металла, такого как ацетат родия(II), и алкена формулы (VIII):
где R3, R4, R5 и R6 являются такими, как определено ранее для формулы (I), возможно в подходящем растворителе, таком как дихлорметан, и возможно под давлением, с получением соединения формулы (I).
3. Соединения формулы (I) можно получить посредством реакции Яппа-Клингеманна. Эта реакция описана в Org. React, 1959, 10, 143-178. Она обычно необходима для осуществления дальнейших стадий синтеза для образования 3,4,5-тризамещенных пиразолов с более разнообразными 4-заместителями. Кроме того, группы, которые можно ввести таким способом, ограничены группами, производными от первоначально введенного 4-заместителя. Однако авторы изобретения обнаружили способ, которым можно получить 3,4,5-тризамещенные 1-арилпиразолы непосредственно в ходе реакции, которая включает сочетание частиц арилдиазония с соответствующим образом замещенным предшественником, несущим нужный заместитель. Нужный заместитель вводят одновременно в положение С-4 в способе, который не включает в себя какую-либо перегруппировку. Кроме того, в реакции получается непосредственно тризамещенный пиразол. Отпадает необходимость в длинной процедуре синтеза и необходимости нескольких обработок промежуточных продуктов, и приводит к хорошему выходу. Значительным преимуществом этого способа является то, что С-4 заместитель может быть встроен в исходное тетразамещенное этановое производное, которое является одним из исходных веществ и которое взаимодействует с частицами арилдиазония с образованием пиразола. Контроль положения заместителя на полученном в результате пиразольном кольце, таким образом, в данной реакции является абсолютным. Более того, удобно и прямо может быть введен очень широкий ряд 4-заместителей.
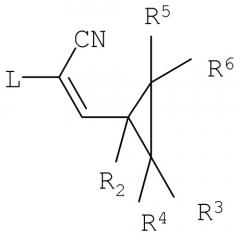
Таким образом, соединение формулы (I), в котором R9 представляет собой NH2, можно получить путем взаимодействия соединения формулы (IX)
с соединением формулы (X)
возможно в присутствии кислоты, где:
R1-R8 являются такими, как определено выше в отношении соединений формулы (I);
L представляет собой активирующую группу; и
Z представляет собой совместимый противоион
с последующим удалением группы L.
Противоион Z- может представлять собой любой подходящий противоион, обычно обнаруживаемый в диазореакциях. Предпочтительно, Z- представляет собой галоген, HSO4 - или тетрафторборат, и наиболее предпочтительно тетрафторборат.
Группа L представляет собой электроноакцепторную группу, которая стабилизирует анионное промежуточное соединение в данном способе. Таким образом, предпочтительно L представляет собой группу, которая способна стабилизировать отрицательный заряд на соседнем атоме углерода. Группа L также должна быть удаляемой. L может быть удалена в щелочных условиях, например посредством щелочного гидролиза, или может быть удалена посредством восстановления и/или отщепления. Группа L является важной, так как служит для управления взаимодействием частиц диазония с соединением формулы (IX), но затем удаляется на последующих стадиях реакции. Предпочтительно L представляет собой сложноэфирную группу или группу COR10. Более предпочтительно L представляет собой группу, выбранную из: -S(O)pR11, где р равно 1 или 2, (R11O)2PO, COOR11 и
-COR10, где R10 выбран из: С1-8алкила, ди-С1-8алкиламино, С1-8алкилтио, С3-8циклоалкила, (CH2)nPh и (СН2)nгетероарила, где n=0, 1 или 2, причем каждая из этих групп может быть возможно замещена по любому атому углерода одной или более группами, независимо выбранными из: галогена, гидрокси, циано, нитро, С1-4алкокси, С1-4галогеналкокси, С1-4алканоила, С1-4галогеналканоила, С1-4алкилсульфинила, С1-4галогеналкилсульфинила, С1-4алкилсульфонила, С1-4галогеналкилсульфонила, С3-8циклоалкила и С3-8галогеноциклоалкила; и R10 может быть водородом; и где R11 выбран из: С1-8алкила, C3-8циклоалкила, (CH2)nPh и (СН2)nгетероарила, где n=0, 1 или 2, причем каждая из этих групп может быть возможно замещена по любому атому углерода одной или более группами, независимо выбранными из: галогена, гидрокси, циано, нитро, С1-4алкокси, С1-4галогеналкокси, С1-4алканоила, С1-4галогеналканоила, С1-4алкилсульфинила, С1-4галогеналкилсульфинила, С1-4алкилсульфонила, С1-4галогеналкилсульфонила,
С3-8циклоалкила и С3-8галогеноциклоалкила; и R11 может быть водородом. Предпочтительно L представляет собой группу, выбранную из COR10 и COOR11. Наиболее предпочтительно L представляет собой -СООМе или -COOEt.
В определенных случаях природа уходящей группы L подразумевает, что полученное в результате промежуточное соединение находится в неправильном окислительном состоянии. Таким образом, где это необходимо, могут быть добавлены одна или несколько стадий, чтобы гарантировать, что перед циклизацией с получением арилпиразола достигнуто правильное окислительное состояние.
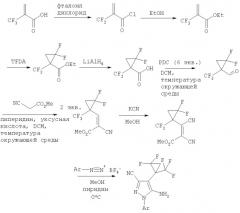
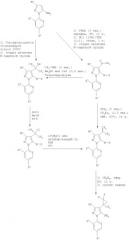
Вышеупомянутый способ сочетания может быть использован для получения любого из соединений формулы (I). Например, Схемы 1 и 2 ниже иллюстрируют общие способы, которые используются при получении 5-амино-1-[2,6-дихлор-4-(трифторметил)фенил]-4-[2,2-дифтор-1-(трифторметил)-циклопропил]-1Н-пиразол-3-карбонитрила.
Схема 1
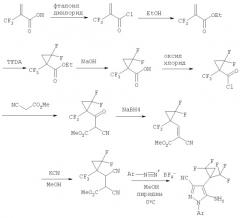
Схема 2
Идеально для реакции сочетания с получением соединения формулы (I), растворитель должен быть полярным растворителем, который не взаимодействует ни с солью или катионом диазония, ни с соединением формулы (IX). Реакция может быть возможно проведена в мягких кислых условиях.
Диазониевая соль формулы (X) может быть получена обычными способами и может быть получена in situ с целью дальнейшего взаимодействия или может быть выделена и использована на следующей стадии реакции.
Конкретные примеры соединений формулы (IX) и (XI) показаны на Схеме 1 и 2. Альтернативные соединения формулы (IX) могут быть аналогичным образом получены из соединений формулы (XI), где R2, R3, R4, R5, R6 и L являются такими, как определено выше, например посредством обработки соединения формулы (XI) источником цианид-ионов.
Соединения формулы (XI) могут быть получены восстановлением и затем дегидратированием соединения формулы (XII).
Соединения формулы (XII) можно получить, например, конденсацией алкилцианоалканоата, например метилцианоацетата, с хлориангидридом в апротонном растворителе, таком как дихлорметан, в присутствии кислоты Льюиса, такой как хлорид магния, и мягкого основания, такого как триэтиламин, при пониженной температуре.
Альтернативно, как показано на Схеме 1, соединения формулы (XI) могут быть получены конденсацией Кневенагеля подходящего альдегида с алкилалканоатом, таким как метилцианоацетат.
Эффективные условия для получения циклопропилзамещенных соединений с использованием триметилсилил-2,2-дифтор-2-(фторсульфонил)ацетата (TFDA), источника дифторкарбена, описаны в Dolbier et al., J. Fluor Chem., 2004, 125, 459.
Соединения формулы (XIII) также могут быть использованы в реакции Яппа-Клингеманна при взаимодействии с соединениями формулы (X) с целью синтеза соединений формулы (VI) по аналогии с вышеописанными условиями.
Соединения формулы (XIII), где L=СO2С1-С6алкил, синтезируют, медленно добавляя гликолонитрила, возможно при повышенной температуре, к С1-С6алкилцианоацетату, в апротонном растворителе, таком как диметилформамид, с последующим добавлением основания, такого как карбонат калия.
Промежуточные соединения формул (VIII), (XI) и (XII) также могут быть получены либо аналогично Схемам 1 и 2, либо с использованием обычных синтетических способов в соответствии со стандартными руководствами органической химии или предшествующей литературой, из легкодоступных исходных веществ с использованием соответствующих реагентов и условий реакции.
4. В другом аспекте изобретения предложены способы получения соединений формулы (I) из альтернативных соединений формулы (I). Например, соединения, в которых R9=NRaRb, где Ra и Rb являются такими, как определено в формуле (I), могут быть получены путем стандартных взаимодействий из соединения формулы (I), где R9 представляет собой NH2.
Соединения формулы (VI) могут быть получены из соединений формулы (XIV)
где CO2R11 представляет собой подходящую сложноэфирную группу, путем превращения сложного эфира в амид (XV) с последующим восстановлением оксихлоридом фосфора при повышенной температуре.
Соединения формулы (XIV) могут быть получены взаимодействием подходящего сложного эфира 3-циано-2-оксопропионовой кислоты, например этилового эфира, с подходящим образом замещенным гидразином соединения (XVII) в спиртовом растворителе при повышенной температуре с последующим добавлением основания, такого как карбонат натрия, и дальнейшим нагреванием.
Соединения формулы (XVII) легко получить, используя стандартные условия, например, путем замещения соответствующего фторпроизводного гидразиновым реагентом, таким как гидразина моногидрат, при дефлегмации в спиртовом растворителе, таком как этанол.
Соединение формулы (I), где R2 представляет собой CF3, R3 и R4 представляют собой фторо, R5 и R6 представляют собой водород и R9 представляет собой NH2, можно легко получить согласно следующей Схеме 3.
Схема 3
N-защитная группа представляет собой подходящую кислотолабильную защитную группу, например группу диметиламидоформамидо, которая может быть включена в соответствии со способами, описанным здесь, и удалена в кислых условиях, таких как соляная кислота в метаноле и диоксане при повышенной температуре. Описанные здесь превращения хорошо известны специалистам в данной области техники и частично описаны здесь более подробно.
Специалистам в данной области техники будет понятно, что существуют вариации и альтернативы описанным здесь способам, которые позволяют получить соединения формулы (I).
Специалистам в данной области техники также будет понятно, что в рамках некоторых описанных способов порядок используемых стадий синтеза может меняться и будет зависеть, среди прочего, от таких факторов, как природа других функциональных групп, присутствующих в конкретном субстрате, доступность ключевых промежуточных соединений и применяемая стратегия защитных групп (если имеются). Несомненно, такие факторы будут также влиять на выбор используемого реагента на указанных стадиях синтеза.
Специалисту понятно, что соединения по изобретению могут быть получены способами, отличными от описанных здесь, путем адаптации способов, описанных здесь, и/или с помощью адаптации способов, известных из уровня техники, например уровня техники, описанного здесь, или с использованием стандартных руководств, таких как "Comprehensive Organic Transformations - A Guide to Functional Group Transformations", RC Larock, Wiley-VCH (1999 или более поздние издания).
Понятно, что способы синтетической трансформации, упомянутые здесь, являются только примерами и могут быть осуществлены в различных других последовательностях с тем, чтобы эффективно получать нужные соединения. Опытный химик будет использовать свое мнение и опыт в отношении наиболее эффективной последовательности реакций для синтеза данного целевого соединения.
Настоящее изобретение также относится к промежуточным соединениям формулы (IA) ниже:
где R1-R7, X и Ra и Rb являются такими, как определено в отношении соединений формулы (I) и где предпочтительные значения, относящиеся к R1-R7 и X, равным образом относятся к формуле (IA). Со ссылкой на формулу (IA), подходящим образом Ra=Rb=метил.
Понятно, что соединения формулы (I) могут содержать один или более асимметрических атомов углерода, таким образом, соединения по изобретению могут существовать в виде двух или более стереоизомеров.
В объем настоящего изобретения входят все стереоизомеры, такие как энантиомеры и диастереомеры, все геометрические изо