Лекарственное средство на основе модифицированного интерферона альфа с пролонгированным терапевтическим действием
Иллюстрации
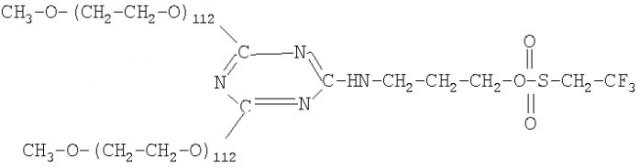
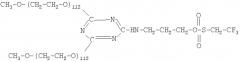
Показать всеИзобретение относится к области фармацевтической промышленности, в частности к лекарственному средству с активностью интерферона альфа. Лекарственное средство с активностью интерферона альфа представляет собой конъюгат с молекулой разветвленного полиэтиленгликоля общей формулы:
где: INF - полипептид интерферона альфа;
R - радикалы 2-аминоэтанола -HN-CH2-CH2-O-, 3-аминопропанола -HN-CH2-CH2-CH2-O-, гомосерина -HN-CH(COOH)-CH2-CH2-O-; n и n1 - одинаковые или различные =50-170, в котором с аминогруппами полипептида интерферона альфа ковалентно связаны остатки разветвленного полиэтиленгликоля с молекулярной массой 5000-15000 Да. Вышеописанное средство является эффективным противовирусным и антипролиферативным препаратом. 1 з.п. ф-лы, 3 табл.
Реферат
Изобретение относится к области медицины и химико-фармацевтической промышленности и касается новых средств с активностью интерферона альфа.
Интерферон альфа широко известен как иммуномодулятор, противовирусное и противоопухолевое средство. Интерферон альфа ингибирует репликацию внутриклеточных паразитов, например вирусов и хламидий. Обладает антипролиферативным действием, тормозит деления клеток, в особенности опухолевых. Оказывает угнетающее влияние на синтез некоторых онкогенов, позволяет остановить неопластическую трансформацию клеток и ингибировать опухолевый рост. Интерферон стимулирует процесс презентации антигена иммунокомпетентным клеткам, обладает способностью стимулировать фагоцитарную активность макрофагов, а также цитотоксическую активность Т-клеток и "натуральных киллеров", участвующих в противовирусном иммунитете. Благодаря иммуномодулирующей активности происходит активизация иммунитета и последующая нормализация иммунного статуса организма.
Препарат может применяться при инфекционных заболеваниях, таких как гепатит В, B+D, С, папилломатоз, кондиломы, энцефалит и менингоэнцефалит, конъюнктивит, кератоконъюнктивит, цитомегаловирусная инфекция, герпес, хламидиоз, уреаплазмоз и др. Онкологических заболеваниях: при волосатоклеточном лейкозе, хроническом миелолейкозе, неходжкинской лимфоме, меланоме, множественной миеломе, саркоме Капоши на фоне СПИД, прогрессирующем раке почки.
Однако биологическая активность интерферона, так же как и многих других белков, ограничена их коротким периодом полураспада в плазме крови.
Модификация интерферона путем конъюгации белка с полиэтиленгликолем (ПЭГилирование) позволяет существенно увеличить время его персистенции в плазме крови, повысить его стабильность и устойчивость к протеолизу, снизить его иммуногенность и в сумме значительно усилить терапевтический эффект препарата.
К числу препаратов ПЭГилированных белков, получивших в настоящее время наибольшее признание, относятся производные интерферона альфа. «Пэгинтрон» (PEGINTRON™ - peginterferon alfa-2b производства Schering-Plough Corporation) представляет собой монозамещенный интерферон--2b с ковалентно пришитой линейной молекулой полиэтиленгликоля с молекулярной массой 12000 Да. «Пегасис» (PEGASYS® - peginterferon alfa-2a производства Hoffmann-La Roche Inc.,) - монозамещенное производное интерферона--2а с остатком полиэтиленгликоля с молекулярной массой 40000 Да разветвленной структуры. Общим для данных двух препаратов является способ пришивки к аминогруппам молекулы белка посредством активной гидроксисукцинимидной группы. Имеются сведения о получении эффективных дериватов интерферона--2а разветвленной трехцепочечной молекулой полиэтиленгликоля с молекулярной массой 43000 Да (Long-acting interferon-alpha 2а modified with a trimer-structured polyethylene glycol: preparation, in vitro bioactivity, in vivo stability and pharmacokinetics. - Int. J.Pharm., 2006), а также избирательно модифицируемого полиэтиленгликолями интерферона, благодаря замене одного аминокислотного остатка глютамина в пятом положении на цистеин (А long-lasting, highly potent interferon alpha-2 conjugate created using site-specific PEGylation. - Bioconjug. Chem., 2005, Jan-Feb). Ранее предпринимались попытки получить производные интерферона альфа пролонгированного действия за счет его модификации ПЭГами с молекулярным весом до 5000 Да, которые не привели к желаемому результату несмотря на многоточечные множественные модификации.
Не менее важным фактором, влияющим на успешность получения эффективных и биосовместимых ПЭГ-производных, является выбор методов активации полимера. Для этих целей были использованы ацетальдегидные, пропиональдегидные, сукцинимидилкарбонатные, сукцинимидилсукцинатные, триазиновые, N-гидроксисукцинимидные, мезилатные, трезилатные и другие активные группы. Способы активации, направленные на модификацию иных, нежели аминогруппы, в данном случае нами не рассматриваются, т.к. более удобных для модификации свободных сульфгидрильных групп интерферон-альфа не содержат. Несмотря на некоторые преимущества, например, альдегидных групп в некоторой избирательности в отношении альфа аминогрупп, множественная модификация, а также некоторые побочные реакции не позволяют считать их идеальным выбором. Нестабильность сукцинимидилсукцинатных и сукцинимидилкарбонатных производных, а также способность последних образовывать лабильные связи с остатками гистидина существенно ограничивают перспективы их использования.
Прототипом для настоящего изобретения является патент RU 2298560 С2, в котором описывается получение конъюгатов интерферона альфа с двухцепочечными разветвленными молекулами полиэтиленгликоля с молекулярными массами цепей от 7500 до 35000 Да, активированных молекулой триазина.
Основным и существенным недостатком такой молекулы является ее способность к модификации помимо аминогрупп имидазольного кольца гистидина. Такая реакция является обратимой, что приводит к высвобождению активированных молекул ПЭГа, способных вступать в реакцию с другими биомолекулами и клеточными структурами организма.
Задачей изобретения являлось получение конъюгата, представляющего собой модифицированный полиэтиленгликолем интерферон альфа, имеющий сравнимые с интерфероном фармакологические свойства, но имеющий отличия как по структуре, так и по технологии получения и не имеющий указанных недостатков.
Задача решается новым лекарственным средством, представляющим собой конъюгат с активностью интерферона альфа, соединенного с молекулой разветвленного полиэтиленгликоля общей формулы:
где: INF - полипептид интерферона альфа;
R - радикалы 2-аминоэтанола -HN-CH2-CH2-O-,
3-аминопропанола -HN-CH2-CH2-CH2-O-, гомосерина -HN-CH(COOH)-CH2-CH2-O-;
n и n1 - одинаковые или различные =50-170,
в котором с аминогруппами полипептида интерферона альфа ковалентно связаны остатки разветвленного полиэтиленгликоля (ПЭГа) с молекулярной массой 5000-15000 Да.
Под - INF (-интерферон) понимают природный или рекомбинантный полипептид, обладающий активностью интерферона альфа, предпочтительно человеческий, получаемый из любого обычного источника, такого как ткани, путем химического синтеза протеина из культуры клеток с использованием нативных и рекомбинантных клеток. Способы получения интерферона альфа из природных или рекомбинантных источников хорошо известны (Pestka, Sci. Am., 249, 36 (1983); Европейский патент 43980).
Остатки полиэтиленгликоля образуют ковалентные связи с аминогруппами интерферона. В частности, с рекомбинантным интерфероном альфа-2-иммуномодуляторным белком, состоящим из полипептидной цепи, включающей 165 аминокислот с двумя дисульфидными связями, образованными 4 цистеиновыми остатками. В его состав входят 10-11 остатков лизина, несущих доступные для модификации эпсилонаминогруппы, 1 свободная концевая альфа-аминогруппа, а также 3 остатка гистидина, имидазольное кольцо которого также доступно для модификации.
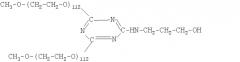
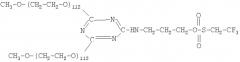
Для осуществления настоящего изобретения была выбрана наиболее эффективная структура разветвленной молекулы ПЭГа со средним значением молекулярной массы 5000-15000 Да, имеющая активную трезилатную группу, способную подобно гидроксисукцинимидным группам модифицировать в мягких условиях исключительно аминогруппы белка.
Результирующая структура активированного ПЭГа выглядит следующим образом:
где значения R, n и n1 - как указано выше.
Известную сложность при модификации белков полиэтиленгликолями представляет свойство последних «высаливать» (осаждать из раствора) белковые молекулы при концентрациях ПЭГа выше 5%, которые недостаточны для полной модификации белка, что приводит к низким выходам целевого продукта. При получении прототипа данное обстоятельство обходилось с помощью многократного добавления активированного ПЭГа к раствору белка по мере убывания его концентрации вследствие вступления в реакцию.
В данной работе задача повышения молярного соотношения модифицирующего агента к белку решается путем использования твердофазного носителя, адсорбирующего белок перед модификацией. В качестве такого носителя была выбрана ионообменная смола. Для модификаций белка, требующих слабощелочных значений рН 7-10, использовали анионообменные смолы, в частности Q-Sepharose Fast Flow, упакованную в хроматографическую колонку. После нанесения раствора белка и его адсорбции ионообменной смолой к сорбенту с помощью перистальтического насоса добавляли раствор ПЭГа при различных значениях рН и в объеме, равном объему хроматографической колонки. После определенного времени инкубации реакционной смеси через колонку прокачивали следующую аналогичную порцию свежего раствора ПЭГа. Количество циклов добавления реагента определялось по необходимой степени модификации интерферона.
Анализ результатов экспериментов показал, что использование твердофазного процесса модификации приводит не только к повышению степени модификации белка, но и существенно повышает ее избирательность. Выход моно- и дипэгилированного продукта значительно повышается, а доля примесей более высокой степени модификации уменьшается. К такому же результату, в смысле уменьшения гетерогенности модифицированного интерферона, приводит использование в реакции модификации более низких значений рН, близких к нейтральным.
По окончании процесса модификации избыток ПЭГа удаляют промывкой сорбента нужным буферным раствором. Элюция модифицированного продукта производится линейным градиентом нейтральной соли, в частности хлористого натрия. При этом достигается фракционирование различной степени модифицированных молекул белка.
Эффективность модификации белка различными производными двуцепочечного ПЭГа существенно возрастает в ряду 2-аминоэтанол-<3-аминопропанол-<гомосерин-трезильных производных. Равные выходы монозамещенных производных (свыше 40%) достигались при 100, 40, и 20-кратных весовых избытках ПЭГа соответственно. Более высокая активность аминопропанольного и гомосеринового производных позволяет проводить эффективную модификацию белка также и в растворе без использования твердофазного носителя. Кроме того, наличие отрицательно заряженной карбоксильной группы в гомосериновом производном помимо обеспечения экспонированности активной трезилатной группы в водную фазу и повышения тропности к аминогруппам белка привносит определенные сложности для проведения реакции на анионообменной твердой фазе, благодаря ионному взаимодействию с ней и появившимися конкурентным отношениям с белковой молекулой за связывание с сорбентом.
Хотя анионообменный сорбент обеспечивает отделение белков от избытка реагента и частичное разделение продуктов модификации, более эффективное фракционирование различной степени модифицированных производных и немодифицированного белка обеспечивает катионообменная хроматография, например, на SP- или CM-Sepharose FF. Использование линейного, ступенчатого или более сложной формы градиентов нейтральной соли, например хлористого натрия, или слабокислых буферных растворов, например ацетата аммония или натрия, позволяет достичь высокой степени чистоты ПЭГилированных препаратов интерферона. Для достижения гомогенности препарата, а также в качестве конечной стадии приготовления фармакопейной субстанции препарата катионообменная хроматография может быть дополнена гель-фильтрационной, например, на колонке Superdex 75.
Конъюгаты согласно изобретению могут быть использованы для лечения в виде фармацевтических композиций для парэнтерального введения, таких как растворы для инъекций, суппозитории, приготовленных известными в химико-фармацевтической области способами. В качестве приемлемых вспомогательных носителей могут быть указаны: вода для инъекций, буферные растворы, например, ацетатный, фосфатный, цитратный, хлориды натрия, калия, лимонная кислота, ПАВ, сахара, сахарные спирты, такие как трегалоза, маннитол, сорбитол и др.
Пример 1. Синтез разветвленных полиэтиленгликолей.
Синтез линейных полиэтиленгликолей заданной молекулярной массы с концевыми функциональными группами осуществляют методом анионной полимеризации окиси этилена (см. пример 1 патента РФ 2298560).
Синтез разветвленного полиэтиленгликоль-аминопропанол-трезила с молекулярной массой 10000 Да общей формулы:
проводят в три стадии.
Стадия синтеза №1. Синтез разветвленного полиэтиленгликоль-триазин-монохлорида общей формулы:
В трехгорлую колбу объемом 200 мл вносят 15,0 г (0,003 г·моль) ПЭГ-5000 с одной гидроксильной группой на конце цепи, 52 мл безводного 1,2-дихлорэтана и при перемешивании получают 25% раствор олигомера. При 20°С в колбу при перемешивании вносят 0,44 мл (0,003 2 г-моль) триэтиламина; после 10 минут взаимодействия ПЭГ с катализатором реакции в колбу вносят 0,28 г (0,0015 г·моль) цианурхлорида. Реакционную массу нагревают до температуры кипения 1,2-дихлорэтана (84°С) и ведут реакцию в течение 2 часов. Далее реакционную массу охлаждают до комнатной температуры и выливают при слабом перемешивании в 150 мл серного эфира. Выпавший осадок отфильтровывают, помещают в стакан, заливают 150 мл свежего серного эфира, перемешивают суспензию 20 минут и заново отфильтровывают промытый олигомер. Полученный порошок (12,7 г) сушат 1 сутки на воздухе, растворяют в 30 мл 1,2-дихлоэтана и высаждают продукт в 150 мл серного эфира. Осадок отфильтровывают, промывают (как указано выше) в 150 мл серного эфира, сушат 1 сутки на воздухе, а затем 2 суток в вакуумном шкафу при 20°С. Выход продукта после переосаждения составляет 6,9 г (46% от теоретического выхода).
Стадия синтеза №2. Синтез разветвленного полиэтиленгликоль-триазин-аминопропанола общей формулы:
В трехгорлую колбу объемом 200 мл вносят 0,320 г карбоната натрия, 60 мл дистиллированной воды, 18,0 г (0,0018 г·моль) разветвленного полиэтиленгликоль-триазин-монохлорида, включают ток аргона, магнитную мешалку и обогрев; при температуре силиконовой бани 50-60°С и перемешивании получают опалесцирующий раствор без осадка. Подключают вакуум от водоструйного насоса (7-10 мм рт.ст) и медленно повышают температуру бани до 105-110°С. Реакционная масса закипает и одновременно с протеканием реакции идет отгонка воды, температура паров воды в верхней части насадки составляет 55-60°С. Реакцию при указанных температуре и вакууме ведут 4 часа и полностью отгоняют воду. Получают расплав продукта реакции при температуре бани 110°С. Вакуум стравливают аргоном и охлаждают колбу с продуктом реакции до комнатной температуры в токе инертного газа.
Стадия синтеза №3. Синтез разветвленного полиэтиленгликоль-аминопропанол-трезила со средней молекулярной массой 10000 Да общей формулы:
При комнатной температуре в колбу с продуктом стадии №2 вносят 35 мл очищенного 1,2-дихлорэтана, растворяют вещество при перемешивании с помощью магнитной мешалки и получают мутный от кристалликов солей (карбонат натрия, хлористый натрий) раствор. Соли отфильтровывают с помощью фильтра Шотта пористостью 4 мкм, фильтр промывают 35 мл 1,2-дихлорэтана. Полученный светлый раствор переливают в новую трехгорлую колбу для синтеза, охлаждают до комнатной температуры и вносят 0,33 мл (0,0024 г·моль) триэтиламина. Через 10 минут реакции с помощью микрошприца в колбу добавляют 0,30 мл (0,0027 г·моль) 2,2,2-трифторэтансульфонилхлорида и ведут реакцию 2 часа. Затем реакционный раствор выливают при слабом перемешивании в 150 мл серного эфира. Выпавший осадок отфильтровывают, помещают в стакан, заливают 150 мл серного эфира, перемешивают суспензию 20 минут и заново отфильтровывают промытый олигомер. Далее порошок (14,5 г) сушат 1 сутки на воздухе, растворяют в 30 мл 1,2-дихлорэтана и высаждают продукт в 150 мл серного эфира. Осадок отфильтровывают, промывают (как указано выше) в два приема 250 мл серного эфира, сушат 1 сутки на воздухе, а затем 2 суток в вакуумном шкафу при 20°С. Выход продукта после переосаждения составляет 8,2 г (45% от теоретического выхода).
Аналогичным способом были получены продукты с n, n1=50 и n, n1=170.
Строение синтезированных продуктов подтверждено данными ЯМР-спектроскопии и гельпроникающей хроматографии.
На ЯМР спектрах соотношение интегральных интенсивностей сигналов протонов от протонов -O-СН3 групп и -СН2-СF3 групп, равное 2,5, близко к расчетному соотношению этих протонов 6:2=3.
Определение молекулярной массы и молекулярно-массового распределения синтезированных продуктов проводили с помощью хроматографа фирмы «Уотерс» со стирогелевыми колонками пористостью 20, 50 и 100 нм. Исследования проводили при 30°С с использованием в качестве элюента тетрагидрофурана. Результаты гельпроникающей хроматографии для исходного ПЭГ-5000 и синтезированных активированных олигомеров приведены в таблице.
| Таблица. | |
| Молекулярно-массовые характеристики полиэтиленгликолей с n=n1=112. |
| № | R | MW | Mn | Mw/Mn |
| 1 | Исходный ПЭГ-5000 c n=112 | 7100 | 4700 | 1,51 |
| 2 | -HN-CH2-CH2-O- | 12600 | 8300 | 1,53 |
| 3 | -HN-CH2-CH2-CH2-O- | 12200 | 8200 | 1,49 |
| 4 | -HN-CH(COOH)-CH2-CH2-O- | 13100 | 8300 | 1,58 |
Как видно из таблицы, величины средневесовых (Mw) и среднечисловых (Mn) молекулярных масс разветвленных активированных производных полиэтиленгликолей (пп.2-4) близки к теоретической величине 10000 Да. Кроме того, величины молекулярно-массового распределения (Mw/Mn) для разветвленных продуктов реакции невелики и сравнимы с распределением макромолекул в исходном ПЭГ-5000.
Пример 2. Твердофазнын синтез ПЭГ-ИФН.
Субстанция интерферона разводилась деионизованной водой, рН доводился до 7.5 и сорбировались на твердой фазе в объеме из расчета 1.5 мг интерферона на 1 мл Q-Sepharose Fast Flow, предварительно уравновешенных 20 мМ натрий-фосфатным буфером рН 7.5.
После завершения сорбции сорбент упаковывался в колонку, промывался 20 мМ натрий-фосфатным буфером рН 7.5, затем на колонку наносился раствор активированного трезилхлоридом аминопропанольного производного ПЭГ в том же буфере в 50-кратном избытке по отношению к интерферону. После инкубации в течение 12 часов при +4°С колонка промывалась уравновешивающим буфером для удаления избытка ПЭГа, а белок элюировался буферным раствором, содержащим 250 мМ хлористого натрия. Продукты реакции анализировали электрофорезом.
Пример 3. ПЭГилирование интерферона альфа 2б в растворе.
Субстанцию интерферона доводили до рН раствора 7.5. К раствору интерферона добавляли раствор активированного трезилхлоридом гомосеринового производного ПЭГ в 20 мМ натрий-фосфатном буфером, рН 7.5, затем инкубировали 12 часов при комнатной температуре на ротационном миксере. Продукты реакции анализировали электрофорезом.
Пример 4. Хроматографическое фракционирование ПЭГ-ИФН.
Растворы модифицированного интерферона разводили в три раза деионизованной водой для понижения ионной силы и доводили рН до 4.5. Раствор наносили на колонку CM-Sepharose Fast Flow (или SP-XL-Sepharose, Pharmacia) с соотношением диаметр/высота=1:8, уравновешенную 40 мМ буферным раствором ацетата аммония рН 4.5, содержащим 0.02% твина 20. Для элюции белка использовали градиент концентрации хлористого натрия в диапазоне 0-350 мМ. Отбирали фракции, соответствующие пикам белка. Фракции подвергали анализу электрофорезом в полиакриламидном геле.
Пример 5. Токсичность полученных ПЭГ-производных.
Эксперименты по изучению токсичности выполнялись на белых нелинейных мышах. Испытание проводили на здоровых животных обоего пола. За 2 часа до проведения испытаний мышей лишали корма и воды. Животных взвешивали и отбирали особей с массой тела 20±1 г. Количество мышей, которые будут использованы для испытания на токсичность одного образца, определяется из расчета 5 мышей на каждый путь введения препарата. Для испытания токсичности производных интерферона альфа были выбраны внутривенный и внутрибрюшинный способы введения каждого образца. Раствор препарата, подлежащего испытанию, подогревали в термостате до 37°С в течение 3-5 мин и вводили со скоростью 0,1 мл/с. Тестовые дозы для каждого образца составляли - 1 млн ME производных интерферона альфа в 0,5 мл раствора натрия хлорида 0,9% для инъекций на мышь.
Сразу после введения раствора препарата отмечают возможные признаки интоксикации и проводят непрерывный мониторинг в течение 30 минут. Последующее наблюдение за состоянием животных ведут в течение 48 часов. Препарат считают выдержавшим испытание на токсичность, если в течение предусмотренного срока наблюдения не погибнет ни одна из подопытных мышей.
При использовании указанных доз производных интерферона альфа летальных эффектов не наблюдалось.
Пример 6. Противовирусная активность ПЭГ-ИФН in vitro.
Противовирусную активность определяли стандартным методом (Европейская фармакопея 5.3, статья интерферон альфа) в культуре перевиваемых линий клеток MDBK (АТСС №CCL22), свободных от микробиологического загрязнения, чувствительных к интерферону альфа типа, против вируса везикулярного стоматита, штамм «Индиана» (ГКВ ГУ НИИ Вирусологии им. Д.И.Ивановского РАМН №600) в дозе, соответствующей 100 ТИД50 в 0,1 мл. Активность интерферона альфа определяли, сравнивая эффект защиты клеток от цитопатического действия вируса, испытуемого образца и стандарта (WHO International Standard INTERFERON ALPHA).
1. Исходный интерферон альфа фирмы ООО "Фармапарк", Москва, Россия, раствор - 10 мкг/мл.
2. Пэгилированный интерферон альфа Pegasys, Хоффманн-Ля Рош, Швейцария, раствор - 50 мкг/мл.
3. Конъюгат по примеру 2 раствор - 20 мкг/мл.
4. Конъюгат по примеру 3 раствор - 25 мкг/мл.
Биологическое тестирование дало следующие результаты:
| Препа-рат | Биоактивность, млн. МЕ/мл | Удельная биоактивность, млн. МЕ/мг | % сохранения активности |
| 1 | 1,900 | 190±10 | 100% |
| 2 | 0,065 | 1,3±0,1 | 0,7% |
| 3 | 0,960 | 48±3 | 25% |
| 4 | 1,825 | 73±5 | 38% |
Таким образом, все модифицированные препараты сохраняют значительную противовирусную активность интерферона альфа.
Пример 7. Антипролиферативная активность in vitro
Антипролиферативную активность интерферона оценивали с помощью колориметрического теста с МТТ [3-(4,5-Dimethylthiazol-2-yl)-2,5-Diphenyltetrazolium Bromide], как описано в (Takemoto и др., 2004) на линии клеток Daudi, лимфома Буркитта (АТСС №CCL-213). Человеческие клетки линии поддерживали в виде суспензионных культур в среде RPMI 1640, дополненной 10%-ной фетальной бычьей сывороткой и 2 мМ глютамином. Клетки (1,5×104) добавляли в лунки планшетов для микротитрования (Costar, MA) с 100 мкл среды. Различные концентрации интерферона стандарта (WHO International Standard INTERFERON ALPHA) и конъюгата формулы I, полученного в примере 3, добавляли в лунки объемом 100 мкл. Планшеты инкубировали при 37°С в 5% СО2 в течение 72 часов. Результаты измерений:
| Концентрация интерферона в среде, (МЕ/мл) | Относительное количество живых клеток, (%). Стандарт | Относительное количество живых клеток, (%). Конъюгат |
| 0 | 99 | 99 |
| 250 | 90 | 90 |
| 1000 | 75 | 60 |
| 4000 | 50 | 30 |
Таким образом, конъюгат формулы I оказывал выраженное антипролиферативное действие на клетки лимфомы Буркитта в стандартном тесте (Hirai и др., 1987).
Пример 8. Фармакокинетика препаратов.
Для изучения фармакокинетики средства конъюгат по примеру 2 вводили крысам внутривенно единократно в количестве 1 мкг в объеме по 0,5 мл/крыса.
В качестве препарата сравнения использовали пэгилированное производное интерферона (Pegasys) в той же дозе.
У каждой крысы через определенные промежутки времени после введения из хвостовой вены брали по 0,5 мл крови. Для этого скальпелем отсекали 1,5-2 мм плоти хвоста. Кровь собирали в пробирки типа Eppendorf. Пробирки помещали в термостат и инкубировали 30 минут при 37°С. Стеклянным капилляром отделяли образовавшийся тромб от стенок пробирки. Пробирки помещали в холодильную камеру и инкубировали 4-6 часов при +4°С. Автоматической пипеткой отсасывали сыворотку и для удаления клеток крови центрифугировали при 5000 об/мин в течение 5 минут. Для стерилизации образцов сыворотки крови супернатанты переносили в системы фильтрации Ultrafree-MC (Amicon) и центрифугировали при 2000 об/мин в течение 10 минут. Образцы для тестирования хранили при +4°С.
Измерения проводили с помощью набора для иммуноферментного анализа (Alpha-IFN ELISA kit, Bender Med Systems). Результаты измерения уровня интерферона за период 14 дней показали, что концентрация препарата сравнения через 7 суток составила в сыворотке менее 50% от пиковой, через 14 суток - менее 20%, а концентрация исследуемого средства через 7 суток составила в сыворотке около 60%, а через 14 суток - порядка 30% от пиковой концентрации.
Таким образом, новое средство обладает значительным пролонгированным эффектом.
Пример 9. Фармацевтическая композиция.
Состав для инъекций:
| ПЭГ-INT по примеру 2 | 10-200 мкг |
| Хлористый натрий | 1-8 мг |
| Ацетат натрия | 1-3 мг |
| Уксусная кислота | 0,1-100 мкг |
| Полисорбат 80 | 50-100 мкг |
| Декстран 40 | 20-60 мг |
| ЭДТА | 10-75 мкг |
| рН | 5,0-7,0 |
| Вода для инъекций | до 1 мл |
1. Лекарственное средство с активностью интерферона альфа, характеризующееся тем, что оно представляет собой конъюгат с молекулой разветвленного полиэтиленгликоля общей формулы где INF - полипептид интерферона альфа;R - радикалы 2-аминоэтанола -HN-CH2-CH2-O-, -аминопропанола -HN-CH2-CH2-CH2-O-, гомосерина -HN-CH(COOH)-CH2-CH2-O-;n и n1 - одинаковые или различные =50-170, в котором с аминогруппами полипептида интерферона альфа ковалентно связаны остатки разветвленного полиэтиленгликоля с молекулярной массой 5000-15000 Да.
2. Лекарственное средство по п.1, в котором INF - полипептид интерферона альфа-2b.