Способ высокоэффективного извлечения серы из потока кислого газа
Иллюстрации
Показать всеИзобретение может быть использовано в химической и нефтехимической промышленности. Кислые газы, содержащие H2S, сжигают в печи в присутствии кислорода. Образовавшийся поток газов сгорания, содержащий H2S и SO2, направляют на каталитическую стадию обработки, в результате которой в условиях реакции Клауса образуются реакционные газы, содержащие серу. Из реакционных газов конденсацией выделяют серу, а поток хвостовых газов процесса Клауса подают на стадию извлечения серы путем непосредственного восстановления на катализаторе восстановления. После выделения серы хвостовые газы непосредственного восстановления, содержащие главным образом H2S и небольшое количество SO2, подают на стадию биологического извлечения серы. Стадия биологического извлечения серы включает в себя блок поглощения, блок биологического окисления и блок выделения серы. Хвостовые газы в блоке поглощения контактируют с ненасыщенным растворителем, в результате чего получают обессеренные хвостовые газы и обогащенный растворитель. Обогащенный растворитель подают на биологическое окисление с кислородом и серными бактериями, классифицированными в пределах родов Beggiatoa, Thiothrix, Thiobacillus, для получения серы. Технический результат - повышение эффективности извлечения серы, снижение затрат. 14 з.п. ф-лы, 3 ил, 3 табл.
Реферат
Данная заявка основана на предварительной заявке US 60/549686, поданной 3 марта 2004 г.
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу извлечения серы из потока кислого газа, который содержит сероводород. В одном аспекте осуществления это изобретение относится к способу извлечения серы, который включает как каталитическое, так и биологическое превращение сероводорода с образованием продукта в виде серы и потока газа, имеющего низкую концентрацию сероводорода.
Удаление серы из технологических газовых потоков может быть желательным и даже необходимым по многим причинам, таким как, например, необходимость удаления соединений серы из технологических потоков химических и нефтехимических технологических установок, для того, чтобы соответствовать постановлениям правительства.
Уровень техники
Процесс Клауса является хорошо известным способом, который используют для обработки определенных технологических потоков, содержащих сероводород, с целью извлечения элементарной серы. Процесс Клауса является двухстадийным процессом, который включает термическую стадию с последующей каталитической стадией. На термической стадии сероводород в сырьевом потоке частично окисляется за счет сгорания в кислороде с образованием газообразных продуктов сгорания, содержащих диоксид серы. Химическую реакцию на термической стадии можно представить следующим уравнением
Непрореагировавший сероводород и образовавшийся диоксид серы, содержащиеся в газообразных продуктах сгорания, могут быть вовлечены в реакцию Клауса, где они реагируют с образованием элементарной серы в соответствии со следующим уравнением
Кроме того, в процессе Клауса непрореагировавший сероводород и диоксид серы в газообразных продуктах сгорания подвергают каталитическому взаимодействию в соответствии с реакцией Клауса по уравнению (2) за счет пропускания газообразных продуктов сгорания над катализатором Клауса, что обеспечивает протекание реакции Клауса при пониженной температуре. В процессе Клауса также предусмотрено извлечение образовавшейся элементарной серы в качестве продукта и удаление хвостовых газов процесса Клауса.
Хотя процесс Клауса является весьма эффективным, обеспечивая извлечение основной части серы из сырьевого потока, в этом способе с двухслойным каталитическим реактором Клауса все же предусматривается извлечение серы приблизительно только до 94-96 процентов. Реакторы Клауса с тремя или более каталитическими слоями могут обеспечить дополнительное улучшение степени извлечения серы, однако практически верхний предел извлечения серы на одной установке Клауса составляет приблизительно от 97 до 98 процентов. Однако хвостовые газы из процесса Клауса можно обрабатывать дополнительно, чтобы обеспечить превращение остаточного сероводорода и диоксида серы и дополнительное извлечение серы. С использованием обработки хвостовых газов процесса Клауса, например, в процессе SCOT суммарное извлечение серы может достигать приблизительно от 99 до 99,8 процентов.
Существует возрастающая потребность в усовершенствованных способах извлечения серы, которые обеспечивают высокую степень извлечения серы и повышенную эффективность эксплуатации, предпочтительно с меньшими капитальными затратами. При возрастающей жесткости стандартов на выбросы серы также имеется потребность в способах извлечения серы, которые обеспечивают еще более высокую степень извлечения серы из технологических потоков, содержащих соединения серы, по сравнению с традиционными системами извлечения серы, которые включают в себя установку Клауса в сочетании с установкой обработки хвостовых газов Клауса.
Раскрытие изобретения
Таким образом, целью способа согласно изобретению является обеспечение высокой степени извлечения серы из технологических потоков, содержащих соединения серы.
Другой целью этого изобретения является разработка эффективного способа извлечения серы из технологических потоков, содержащих соединения серы.
Соответственно, в одном варианте воплощения изобретение представляет собой способ, который заключается в том, что газовый поток, содержащий некоторое количество H2S и SO2, направляют на стадию непосредственного восстановления, обеспечивая прямое восстановление хвостовых газов, и на биологическую обработку хвостовых газов непосредственного восстановления с образованием обессеренного газа и серного продукта.
В другом варианте это изобретение включает в себя способ извлечения серы, который заключается в пропускании хвостовых газов процесса Клауса, содержащих H2S и SO2, в реакционную зону непосредственного восстановления, эксплуатируемую в условиях процесса непосредственного восстановления и получения хвостовых газов непосредственного восстановления, содержащих H2S. Хвостовые газы непосредственного восстановления пропускают в систему биологического обессеривания газа, эксплуатируемую с целью получения серного продукта и обессеренного газа.
В еще одном варианте изобретение включает в себя способ извлечения серы, в котором поток кислого газа, содержащего сероводород, подают в качестве сырья в систему извлечения серы процесса Клауса, работающую таким образом, чтобы получить первый серный продукт и хвостовые газы процесса Клауса, содержащие сероводород. Хвостовые газы процесса Клауса пропускают в реакционную зону непосредственного восстановления, эксплуатируемую в условиях процесса непосредственного восстановления, с целью получения реакционных газов непосредственного восстановления, содержащих серу. Из реакционных газов непосредственного восстановления извлекают серу, чтобы получить хвостовые газы непосредственного восстановления с некоторой концентрацией сероводорода. Затем хвостовые газы непосредственного восстановления подают в систему биологического обессеривания газа, в которой получают второй серный продукт и обессеренный газ, содержащий менее 100 об. ч/млн сероводорода.
В еще одном варианте воплощения этого изобретения разработан способ, который заключается в том, что хвостовые газы стадии извлечения серы процесса Клауса направляют на стадию непосредственного восстановления с последующей стадией биологического извлечения серы, чтобы получить обессеренный газовый поток, имеющий очень низкую концентрацию сероводорода и диоксида серы. Поток кислых газов взаимодействует с кислородом в таких условиях окисления, чтобы получить газообразные продукты сгорания, содержащие сероводород и диоксид серы. Газообразные продукты сгорания взаимодействуют в условиях реакции Клауса с образованием реакционных газов, содержащих серу. Из реакционных газов извлекают серу, чтобы получить серный продукт и хвостовые газы процесса Клауса, содержащие сероводород и диоксид серы. Эти хвостовые газы процесса Клауса взаимодействуют в условиях реакции непосредственного восстановления, чтобы получить реакционные газы непосредственного восстановления, содержащие серу. Из реакционных газов непосредственного восстановления извлекают серу, чтобы получить хвостовые газы непосредственного восстановления, содержащие H2S. Хвостовые газы непосредственного восстановления контактируют с ненасыщенным поглотителем с целью удаления из хвостовых газов непосредственного восстановления части содержащегося в них сероводорода с получением обессеренного газа и обогащенного растворителя, содержащего растворенный сероводород. Обогащенный растворитель направляют на стадию биологического окисления, на которой обогащенный растворитель контактирует с кислородом в зоне биореакции, в условиях биологического окисления, при котором серные бактерии биологически окисляют растворенный сероводород в обогащенном растворителе до элементарной серы.
Другие объекты, преимущества и варианты воплощения этого изобретения станут очевидными из следующего подробного описания и прилагаемой формулы изобретения.
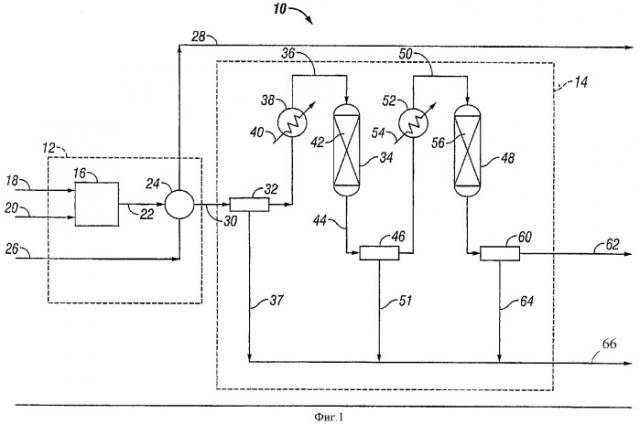
Фигура 1 представляет собой принципиальную схему, отражающую определенные стороны системы процесса Клауса и технологической стадии извлечения серы процесса Клауса согласно изобретению.
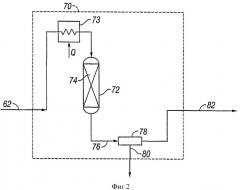
Фигура 2 является принципиальной схемой, представляющей определенные стороны системы непосредственного восстановления и технологической стадии извлечения серы процесса Клауса согласно изобретению.
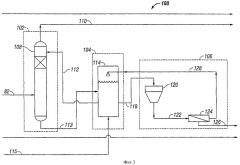
Фигура 3 является принципиальной схемой, представляющей определенные стороны системы биологического обессеривания газа и технологической стадии биологического превращения в способе извлечения серы согласно изобретению.
Способ согласно изобретению обеспечивает высокую эффективность извлечения серы из потока кислого газа и, таким образом, глубокое удаление сероводорода из газового потока, содержащего сероводород. Вариант широкого воплощения способа согласно изобретению включает в себя обработку газового потока с определенной концентрацией H2S и SO2 на стадии непосредственного восстановления, чтобы получить хвостовые газы непосредственного восстановления, причем хвостовые газы непосредственного восстановления обрабатывают на стадии биологического обессеривания газа, чтобы получить обессеренный газ и серный продукт. Газовый поток, который подвергается обработке на стадии непосредственного восстановления, может быть хвостовыми газами процесса Клауса. Таким образом, один признак способа согласно изобретению включает в себя компоновку технологической системы извлечения серы в сочетании с системой непосредственного восстановления и технологической системой биологического обессеривания газа. Эта компоновка предусматривает обработку потока кислого газа и высокую эффективность извлечения серы из потока кислого газа, таким образом обеспечивая серный продукт и поток обессеренного газового продукта, имеющего очень низкую концентрацию сероводорода и диоксида серы.
Способ извлечения серы согласно изобретению включает в себя подачу потока кислого газа, который содержит сероводород (H2S), в систему извлечения серы процесса Клауса. Эта система извлечения серы процесса Клауса может быть любой подходящей технологической системой для обработки потока кислого газа, чтобы получить серный продукт и хвостовые газы процесса Клауса, содержащие некоторые количества H2S и SO2. Способ извлечения серы процесса Клауса является известным процессом извлечения серы из потока кислых газов, и он может обеспечить достаточно высокую степень извлечения серы. Однако в тех случаях, когда желательной или необходимой является очень высокая степень извлечения серы, способ или система Клауса для извлечения серы не может обеспечить экономически целесообразный процесс извлечения серы. Таким образом, согласно изобретению систему Клауса сочетают с системой биологического обессеривания газа, в которой перерабатывают хвостовые газы процесса Клауса, чтобы обеспечить дополнительное улучшение степени удаления серы из хвостовых газов процесса Клауса с образованием обессеренных хвостовых газов, имеющих существенно пониженную концентрацию H2S по сравнению с хвостовыми газами процесса Клауса и чтобы обеспечить улучшение общей степени извлечения серы из потока кислого газа.
Таким образом, обессеренные хвостовые газы из биологической системы обессеривания газа могут иметь концентрацию H2S, которая меньше, предпочтительно значительно меньше, чем концентрация H2S в хвостовых газах процесса Клауса. Следовательно, способ согласно изобретению обеспечивает особенно глубокое удаление H2S из кислых газов за счет получения обессеренных хвостовых газов, которые обычно имеют концентрацию H2S меньше, чем приблизительно 2000 объемных частей на миллион (об. ч/млн), однако желательно, чтобы концентрация H2S в обессеренных хвостовых газах составляла ниже 100 об. ч/млн. В способе согласно изобретению возможно даже достижение предпочтительной концентрации H2S в обессеренных хвостовых газах, которая может составлять вплоть до 50 об. ч/млн и менее, наиболее предпочтительно, концентрация H2S в обессеренных хвостовых газах составляет менее 10 об. ч/млн и даже меньше, чем 5 об. ч/млн или 1 об. ч/млн. Практически нижний предел концентрации H2S в обессеренных хвостовых газах составляет около 100 объемных частей на миллиард (ч/млд) или 10 ч/млд.
Система Клауса для извлечения серы может включать в себя средство сжигания и реакционное устройство, которые соответственно предоставляют термическую стадию и каталитическую стадию процесса Клауса, таким образом, получается серный продукт и хвостовые газы процесса Клауса. Это средство сжигания может включать в себя печь, оборудованную горелками, или любым другим подходящим средством для сжигания, которая принимает кислый газ и кислородсодержащий газ, такой как воздух, и обеспечивает сжигание или сгорание части H2S, содержащегося в кислых газах, до диоксида серы (SO2) в соответствии с уравнением (1), приведенным выше. Таким образом, средство сжигания определяет зону сгорания или термическую зону, в которой H2S в кислых газах частично окисляется с образованием потока газов сгорания, который содержит сероводород и диоксид серы.
Кислые газы, подаваемые в средство сжигания процесса Клауса, могут быть газами из любого источника, поскольку используемый в этом изобретении термин «кислый газ» относится к текучей среде, которая обычно имеет значительный уровень концентрации H2S. Кроме того, подаваемый кислый газ может содержать другие компоненты, такие как, например, диоксид углерода, или азот, или углеводороды, или аммиак, или комбинации одного или нескольких из указанных компонентов. Состав подаваемого кислого газа может изменяться в зависимости от источника и других факторов. Обычным источником кислых газов является система традиционной очистки природных газов, которая применяется для удаления сероводорода из потоков среды, содержащей H2S.
Обычно концентрация H2S в сырьевом кислом газе может изменяться приблизительно от 5 объемных процентов от суммарного объема сырьевого потока кислых газов до 98 объемных процентов. Однако типичная концентрация H2S в сырьевом потоке кислых газов находится в диапазоне от 50 до 95 объемных %, и более типично, от 80 до 94% по объему. В следующей таблице 1 приведен типичный состав и диапазон концентраций для различных компонентов в потоке кислого газа.
| Таблица 1 | |
| Типичный состав сырьевого потока кислых газов, поступающих в установку Клауса | |
| Компонент | Диапазон концентраций (объем. %) |
| Сероводород (H2S) | от 5 до 98 |
| Диоксид углерода (CO2) | от 1 до 90 |
| Углеводороды | от 0,1 до 2 |
| Азот (N2) | от 0,1 до 1 |
| Аммиак (NH3) | вплоть до 50 |
| Прочие | от 0,1 до 1 |
Поток газов сгорания поступает в реакционное устройство процесса Клауса, которое может включать реактор Клауса, в котором находится подходящий катализатор Клауса, и конденсационный аппарат для серы. Реакционное устройство процесса Клауса определяет каталитическую реакционную зону процесса Клауса, содержащую катализатор Клауса, такой как активированный оксид алюминия, и зону конденсации серы. Реакционное устройство процесса Клауса обеспечивает взаимодействие H2S и SO2 из газообразных продуктов сгорания в соответствии с уравнением (2), приведенным выше. Кроме того, в реакционном устройстве процесса Клауса предусмотрено извлечение серного продукта процесса Клауса и образуются хвостовые газы процесса Клауса.
Типичные хвостовые газы процесса Клауса содержат H2S, а также SO2. В стандартном режиме работы установки Клауса обычно желательно, если это возможно, чтобы газообразные продукты сгорания в реакционной секции процесса Клауса имели молярное соотношение H2S к SO2 как можно ближе к стехиометрическому соотношению 2:1, которое следует из уравнения (2). Это приведет к достижению максимального извлечения серы и к минимизации количества суммарной серы в виде H2S и SO2, которое уходит с хвостовыми газами процесса Клауса.
В следующей ниже таблице 2 приведен типичный состав и диапазон концентраций для различных компонентов потока хвостовых газов в установке Клауса, работающей в стандартных технологических условиях. Однако настоящее изобретение не ограничивается установкой Клауса, которая работает в стандартных или обычно желательных технологических условиях, и, следовательно, хвостовые газы процесса Клауса согласно изобретению, которые вовлекаются в стадию обработки путем непосредственного восстановления, могут иметь широкий диапазон концентраций H2S и SO2. Например, в способе согласно изобретению концентрация H2S в хвостовых газах процесса Клауса может быть в диапазоне от 0,1 до 3 объемных процентов, причем объемный процент рассчитывается на суммарный объем хвостовых газов процесса Клауса, и концентрация SO2 может быть в диапазоне от 0,05% (500 об. ч/млн) до 1 объемного процента, причем объемный процент рассчитывается на суммарный объем хвостовых газов процесса Клауса. Более типично, хвостовые газы процесса Клауса могут иметь концентрацию SO2 в диапазоне от более 0,08 объемных % (800 об. ч/млн) до 1 объемного процента, и наиболее типично, концентрация SO2 находится в диапазоне от более 0,1 объемного % (1000 об. ч/млн) до 0,5 объемного %. Что касается концентрации H2S в хвостовых газах процесса Клауса, более типично она может быть в диапазоне от 0,15 до 2,5 объемных %, и наиболее типично, от 0,2 до 2 объемных %.
| Таблица 2 | |
| Типичный состав хвостовых газов процесса Клауса при работе традиционной установки Клауса | |
| Компонент | Диапазон концентраций (объем. %) |
| Сероводород (H2S) | от 0,2 (2000 об. ч/млн) до 2 (20000 об. ч/млн) |
| Диоксид серы (SO2) | от 0,1 (1000 об. ч/млн) до 0,5 (5000 об. ч/млн) |
| Монооксид углерода (СО) | от 0,5 до 2 |
| Водород (Н2) | от 1 до 3 |
| Азот (N2) | от 20 до 80 |
| Диоксид углерода (CO2) | от 20 до 80 |
| Вода (H2O) | от 10 до 35 |
| Аргон (Ar) | от 0,5 до 1 |
| Другие сернистые соединения | от 0,12 до 1,2 |
Способ согласно изобретению может включать в себя подачу газового потока, содержащего SO2 и имеющего некоторые количества SO2 и H2S, которые указаны выше для хвостовых газов процесса Клауса, т.е. имеющего некоторое количество SO2 и H2S, в систему непосредственного восстановления для прямого превращения SO2 в газовом потоке, содержащем SO2, в элементарную серу, и необязательно, для удаления элементарной серы из реакционного газа, образовавшегося при непосредственном восстановлении, чтобы получить хвостовые газы непосредственного восстановления, которые имеют меньшую концентрацию SO2, предпочтительно, существенно меньше, чем концентрация SO2 в газовом потоке, содержащем SO2. Газовый поток, содержащий SO2, может быть любым газовым потоком, который содержит SO2 и H2S, включая, например, хвостовые газы процесса Клауса. Система непосредственного восстановления может быть любой подходящей технологической системой, которая обеспечивает непосредственное восстановление SO2, содержащегося в газовом потоке, имеющем некоторую концентрацию SO2 и концентрацию H2S, до элементарной серы, и, кроме того, система может включать в себя устройство для извлечения серы из газа непосредственного восстановления, который содержит элементарную серу, образовавшуюся при восстановлении SO2.
В предпочтительном варианте воплощения изобретения система непосредственного восстановления включает в себя реактор непосредственного восстановления и, необязательно, установку для извлечения серы. Реактор непосредственного восстановления определяет реакционную зону непосредственного восстановления, содержащую катализатор непосредственного восстановления, и обеспечивает реакционное устройство непосредственного восстановления путем контактирования газового потока, содержащего SO2, с катализатором непосредственного восстановления в условиях, подходящих для реакции непосредственного восстановления, чтобы непосредственно превратить, по меньшей мере, часть SO2 в газовом потоке, содержащем SO2, обычно путем восстановления водородом или монооксидом углерода, в элементарную серу и чтобы получить или реакционные газы непосредственного восстановления, или хвостовые газы непосредственного восстановления, или, в зависимости от того, выделяется ли сера из реакционных газов непосредственного восстановления или не выделяется, как реакционные газы непосредственного восстановления, так и хвостовые газы непосредственного восстановления, причем в этих газах концентрация SO2 ниже концентрации SO2 в газовом потоке, содержащем SO2.
Используемый в этом изобретении термин "хвостовые газы непосредственного восстановления" относится или к газу непосредственного восстановления, полученному в реакторе непосредственного восстановления по способу согласно изобретению и включающему в себя H2S, элементарную серу и SO2, концентрация которого меньше, чем концентрация SO2 в газовом потоке, содержащем SO2, или к хвостовым газам непосредственного восстановления, образовавшимся при извлечении или удалении, по меньшей мере, части элементарной серы, содержащейся в газе непосредственного восстановления, полученном в реакторе непосредственного восстановления. В способе согласно изобретению хвостовые газы непосредственного восстановления подают в систему биологического обессеривания газа для извлечения из него серы.
Как отмечено выше, хвостовые газы непосредственного восстановления имеют концентрацию SO2 меньше, чем концентрация SO2 в газовом потоке, содержащем SO2; однако, для того, чтобы реализовать максимальную выгоду от способа настоящего изобретения, желательно минимизировать концентрацию SO2 в хвостовых газах непосредственного восстановления, и, таким образом, эта концентрация может иметь значение меньше, чем 0,1 объемный процент (1000 об. ч/млн), причем объемный процент рассчитан на суммарный объем хвостовых газов непосредственного восстановления. Более конкретно, концентрация SO2 в хвостовых газах непосредственного восстановления составляет менее 800 об. ч/млн. Однако предпочтительно, чтобы концентрация SO2 в хвостовых газах непосредственного восстановления была меньше 500 об. ч/млн, и наиболее предпочтительно, чтобы концентрация SO2 была меньше 250 об. ч/млн или даже меньше, чем 100 об. ч/млн.
Катализатор непосредственного восстановления, используемый в системе непосредственного восстановления, представляет собой любую подходящую композицию, которая может обеспечить прямое каталитическое превращение SO2 в газовом потоке, содержащем SO2, в элементарную серу. Примеры возможных подходящих композиций для использования в качестве катализатора непосредственного восстановления согласно изобретению включают в себя углеродистые или содержащие углерод материалы, например древесный уголь, такие угли как антрацит, и кокс, как описано в патентах США № 4,428,921 и № 4,452,772, которые оба включены в это изобретение как ссылки, и катализаторы, которые описаны в патенте США № 6,297,189 В1, включенном в это изобретение как ссылка. Катализатор непосредственного восстановления может включать в себя такие каталитические композиции, как боксит-бентонитный катализатор, катализатор NiO/Al2O3, катализатор СО3О4/Al2O3, смешанные оксидные катализаторы, включающие металлоксидные катализаторы, нанесенные на оксид алюминия, в которых оксид металла выбран из оксидов следующих металлов: хрома, молибдена, меди, кобальта и никеля и катализаторов - сульфидированных оксидов металлов, которые все описаны в упомянутом выше патенте США № 6,297,189 В1.
Одна особенно предпочтительная каталитическая композиция для использования в качестве катализатора непосредственного восстановления включает в себя каталитическую композицию, полученную путем пропитки носителя раствором соединения металла, с последующим сульфидированием подложки, пропитанной соединением металла, чтобы превратить оксидную форму соединения металла в сульфидную форму. Носитель может быть алюминийоксидной подложкой оксида алюминия любого типа, в том числе, например, α-оксид алюминия, β-оксид алюминия или γ-оксид алюминия. Пропитывающий раствор соединения металла, в принципе, представляет собой раствор подходящей соли металла или солей металлов, которые будут входить в окончательный состав желательной композиции катализатора. Соли металлов могут представлять собой нитраты, или менее предпочтительной формой могут быть карбонаты или нитриты металлов. Таким образом, катализатор непосредственного восстановления может представлять собой сульфидированный алюминийоксидный носитель, пропитанный соединением металла. Полученная таким образом каталитическая композиция может быть использована в качестве катализатора непосредственного восстановления.
Конкретные способы получения предпочтительного катализатора непосредственного восстановления и конкретные композиции подробно описаны в упомянутом выше патенте США № 6,297,189 В1. Например, катализатор непосредственного восстановления может содержать смесь сульфидированных металлов, которые выбирают из группы, состоящей из металлов VIII группы и металлов из других групп. Металлы VIII группы могут быть выбраны из железа (Fe), кобальта (Со) и никеля (Ni), и металлы из других групп могут быть выбраны из молибдена (Мо), марганца (Mn), меди (Cu), вольфрама (W), ванадия (V) и хрома (Cr). Кроме того, катализатор непосредственного восстановления может включать соединение, имеющее следующую формулу:
FeaCobNicCrdMneMofVgCuhWiOxSy
где каждый индекс а, b, с, d, e и f независимо представляет собой целое число (в том числе нуль) в диапазоне от 0 до 30;
каждый g и h независимо представляет собой целое число (в том числе нуль) в диапазоне от 0 до 10;
i - целое число (в том числе нуль) в диапазоне от 0 до 5;
по меньшей мере, один из а, b, с не является нулем, и, по меньшей мере, один из d, e, f, g, h и i не является нулем; и
сумма x+y определяется балансом зарядов в этой формуле.
Условия реакции непосредственного восстановления, в которых газовый поток, содержащий SO2, контактирует с катализатором непосредственного восстановления, могут представлять собой любые подходящие технологические условия, которые обеспечивают превращение, по меньшей мере, части SO2 в элементарную серу; однако подразумевается, что подходящие технологические условия будут широко изменяться в зависимости от того, какой конкретный катализатор непосредственного восстановления будет использован. Таким образом, температура процесса непосредственного восстановления может находиться в диапазоне приблизительно от 200°С до 1000°С, давление процесса непосредственного восстановления может находиться в диапазоне от атмосферного вплоть до 1000 фунтов/кв. дюйм (6,89 МПа), и объемная скорость подачи газа (при стандартных условиях) может находиться в диапазоне вплоть до 20000 час-1.
Стадию непосредственного восстановления осуществляют путем введения газового потока, содержащего SO2, в реакционную зону непосредственного восстановления и контактирования этого потока с катализатором непосредственного восстановления в условиях, подходящих для процесса непосредственного восстановления. Восстанавливающий газ может быть добавлен внутрь или введен вместе с газовым потоком, содержащим SO2, в реакционную зону непосредственного восстановления для того, чтобы обеспечить необходимый реагент, облегчающий восстановление и превращение SO2 в элементарную серу. В случае, когда газовый поток, содержащий SO2, представляет собой хвостовые газы процесса Клауса, количество водорода и монооксида углерода, которые обычно содержатся в хвостовых газах процесса Клауса, должно быть достаточно для обеспечения необходимых восстанавливающих агентов, чтобы могла протекать реакция восстановления SO2. Следовательно, в предпочтительном варианте воплощения изобретения никакие дополнительные восстанавливающие агенты не добавляют к хвостовым газам процесса Клауса, которые подают на стадию непосредственного восстановления.
Хвостовые газы непосредственного восстановления подают в биологическую систему обессеривания газа, которая представляет собой технологическую стадию для удаления H2S из хвостовых газов непосредственного восстановления, чтобы получить обессеренные хвостовые газы, и для превращения удаленного H2S, чтобы получить серный продукт в биореакторе. Биологическая система обессеривания газа может быть любой подходящей технологической системой, предоставляющей биологический способ обработки текучей среды, содержащей некоторую концентрацию H2S, чтобы удалить из этого потока H2S и чтобы получить серный продукт в биореакторе. Одним примером такого подходящего способа биологического обессеривания газа является процесс фирмы Shell-Paques для извлечения серы из текучей среды, содержащей H2S.
В предпочтительном варианте воплощения изобретения биологическая система обессеривания газа включает в себя компоновку поглощающего устройства, биологического реактора и устройства извлечения серы, сочетание которых обеспечивает удаление H2S из хвостовых газов непосредственного восстановления и их превращение, чтобы получить продукт - элементарную серу и обессеренные хвостовые газы, имеющие очень низкую концентрацию серы, как например, крайне низкие концентрации H2S и SO2. Поглощающее устройство биологической системы обессеривания газа может включать, например, емкость для контактирования, такую как абсорбер, или любое другое подходящее устройство для контактирования, которое определяет зону контактирования или зону абсорбции, в которой хвостовые газы непосредственного восстановления контактируют с ненасыщенным растворителем, чтобы получить обессеренные хвостовые газы и обогащенный растворитель, содержащий растворенный сероводород.
Ненасыщенный растворитель биологической системы обессеривания газа может включать любой растворитель, который обеспечивает соответствующую мокрую очистку хвостовых газов непосредственного восстановления от H2S, предпочтительно с помощью гидроксидных ионов, которые могут взаимодействовать с H2S в хвостовых газах непосредственного восстановления, с образованием сульфидных ионов, которые переходят в раствор в образовавшемся обогащенном растворителе. Таким образом, ненасыщенным растворителем может быть щелочной раствор, такой как раствор, содержащий гидроксид натрия или гидроксид калия, или смесь обоих гидроксидов, то есть предпочтительно водный раствор. Таким образом, щелочной раствор может содержать водный раствор или гидроксида натрия, или гидроксида калия, или их смесь. Желательно, чтобы ненасыщенный растворитель представлял собой буферный щелочной раствор гидроксида натрия, или щелочи, и чтобы ненасыщенный растворитель имел значение pH выше 7, например в диапазоне от выше 7 до 14. Предпочтительно pH ненасыщенного растворителя находится в диапазоне приблизительно от 7,5 до 12, и наиболее предпочтительно, от 8 до 10. Буферные соединения могут включать карбонаты, бикарбонаты, фосфаты и смеси из двух или более таких соединений. Предпочтительным буферным агентом является карбонат натрия, или бикарбонат натрия, или их сочетание.
Ненасыщенный растворитель контактирует с хвостовыми газами непосредственного восстановления в таких условиях, подходящих для поглощения, чтобы обеспечить получение обессеренных хвостовых газов и обогащенного растворителя. Затем обогащенный растворитель пропускают в биореактор, который определяет зону биологической реакции и предоставляет устройство для биологического окисления растворенного сероводорода, содержащегося в обогащенном растворителе, до элементарной серы. Зона биологической реакции работает в условиях, подходящих для биологического окисления в присутствии кислорода, для того чтобы серные бактерии, находящиеся в этом растворе, превращали сульфид, содержащийся в обогащенном растворителе, в элементарную серу и гидроксидные ионы, таким образом обеспечивая регенерацию обогащенного растворителя, с получением ненасыщенного растворителя. В результате биологического окисления ненасыщенный растворитель может содержать элементарную серу, обычно в виде частиц серы.
В зоне биологической реакции могут быть использованы любые серные бактерии, которые подходят для превращения растворенного сероводорода, содержащегося в обогащенном растворителе, в элементарную серу. Возможные виды и штаммы серных бактерий могут быть выбраны из тех, которые классифицированы в пределах родов Beggiatoa, Thiothrix и Thiobacillus. Источник этих серных бактерий не имеет значения, и могут быть использованы любые подходящие серные бактерии, чтобы биологически окислить H2S в обогащенном растворителе; при условии, что используемые серные бактерии осуществляют указанную выше желательную функцию превращения H2S в элементарную серу. Многие подходящие виды серных бактерий встречаются в природе и могут быть обнаружены в окружающей среде, в том числе в промышленной и естественной окружающей среде, где присутствуют сера или сернистые соединения, такие как горячие сернистые источники, и в среде, окружающей эти источники. Предпочтительным родом, из которого выбирают вид серных бактерий для использования в биореакторе согласно изобретению, является Thiobacillus.
Для извлечения серы, образовавшейся на стадии биологического превращения, часть ненасыщенного растворителя, содержащего серу, направляют в устройство извлечения серы для извлечения серы из части ненасыщенного растворителя и чтобы получить второй серный продукт, т.е. серный продукт в биореакторе, и ненасыщенный растворитель с низким содержанием серы. Один способ извлечения частиц серы из ненасыщенного растворителя включает его пропускание в устройство для осаждения серы. Это устройство для осаждения серы может включать в себя емкость, такую как отстойник серы, который определяет зону осаждения. Зона осаждения обеспечивает время пребывания ненасыщенного растворителя, которое позволяет осадиться частицам серы в этом растворителе. Таким образом, устройство для осаждения серы обеспечивает выделение частиц серы, содержащихся в ненасыщенном растворителе, и образуется суспензия, содержащая частицы серы. Затем частицы серы в суспензии могут быть выделены с помощью любого подходящего из известных способов, таких как, например, способы центрифугирования и декантирования, чтобы обеспечить получение серного продукта биологического превращения и ненасыщенный растворитель с низким содержанием серы, имеющий концентрацию элементарной серы ниже концентрации в ненасыщенном растворителе, который может быть возвращен в устройство биологического превращения.
Важным признаком способа согласно изобретению является его работа в таком режиме, чтобы свести к минимуму количество SO2, которое содержится в газообразном сырье, подаваемом в биологическую систему обессеривания. Обычно нежелательно, чтобы газообразное сырье, которое вводится в абсорбер биологической системы обессеривания газа, имело значительную концентрацию SO2 из-за взаимодействия SO2 со щелочью в ненасыщенном растворителе. Действительно, существует прямая связь между концентрацией SO2 в газообразном сырье, которое контактирует со щелочью ненасыщенного растворителя, и потреблением щелочи. Следовательно, для снижения потребления щелочи при работе стадии биологиче