Адъювант на основе полиинозиновой кислоты - полицитидиловой кислоты
Иллюстрации
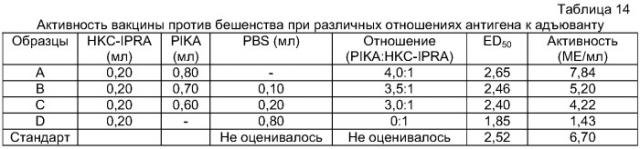
Показать всеИзобретение касается полинуклеотидной адъювантной композиции на основе полирибоинозиновой-полирибоцитидиловой кислоты (PIC) и способам ее применения для индукции иммунного ответа. Настоящее изобретение также относится к набору для иммуногенной композиции и иммуногенной композиции, включающей полинуклеотидную адъювантную композицию вместе с антигеном (например, в качестве вакцины). Адъювантные композиции (варианты) по изобретению имеют особые физические свойства (например, молекулярную массу, концентрацию и pH), которые удовлетворяют потребность в безопасном адъюванте для вызывания усиленного иммунного ответа. Изобретение, кроме того, относится к способу получения иммуногенной композиции и применению иммуногенных адъювантных композиций, в частности, при индукции иммунного ответа на антигенное соединение. Адъювантные композиции по изобретению безопасны и эффективны при обеспечении желаемого иммуногенного эффекта у людей. 11 н. и 14 з.п. ф-лы, 2 ил., 15 табл.
Реферат
Область, к которой относится изобретение
Изобретение в целом относится к адъювантным композициям и способам их применения при усилении иммунного ответа, конкретнее к соединениям, вакцинам и способам усиления иммуногенности антигена, а конкретнее к полинуклеотидным адъювантным композициям, вакцинам, включающим полинуклеотидные адъювантные композиции, и к способам применения указанных полинуклеотидных адъювантных композиций и вакцин для усиления иммунного ответа у хозяина.
Предпосылки изобретения
1. Описание предшествующего уровня техники
Иммунная система может проявлять как специфический, так и неспецифический иммунитет. В целом, В- и Т-лимфоциты, которые проявляют специфические рецепторы для данного антигена на их клеточной поверхности, обеспечивают специфический иммунитет. Иммунная система может реагировать на различные антигены двумя путями: 1) гуморально опосредованный иммунитет, который включает стимуляцию В-клеток и продукцию антител или иммуноглобулинов, представляющие антиген клетки (APCs) и Т-клетки хелперы (Th1 и Th2), и 2) клеточно-опосредованный иммунитет (CMI), который в целом вовлекает Т-клетки, включая цитотоксические Т-лимфоциты (CTLs), хотя в генерирование реакции CTL также вовлечены другие клетки (например, клетки Th1 и/или Th2 и APCs).
Неспецифический иммунитет охватывает различные клетки и механизмы, наряду с другими, такие как фагоцитоз (поглощение инородных частиц или антигенов) макрофагами или гранулоцитами и активность клеток-натуральных киллеров (NK). Неспецифический иммунитет основан на механизмах, менее эволюционно продвинутых, и не проявляет приобретенной природы специфичности и памяти, которые представляют собой иллюстративные вехи специфического иммунного ответа. Ключевые различия между специфическим и неспецифическим иммунитетом основаны на специфичности В- и Т-клеток. Эти клетки преимущественно приобретают свою реактивность после активации специфическим антигеном и имеют механизмы для проявления памяти в случае будущего контакта с этим специфическим антигеном. В результате вакцинация (вовлекающая специфичность и память) является эффективным протоколом для защиты против вредных патогенов.
Адъюванты в целом представляют собой соединения, которые при введении с антигеном (или смешанные с антигеном, или введенные перед введением антигена) усиливают или модифицируют иммунный ответ на этот определенный антиген.
Примеры адъювантов, которые использовались для усиления иммунного ответа, включают соединения алюминия (все в целом именуемые “Alum”), эмульсии масла в воде (полный адъювант Фрейнда (CFA) представляет собой эмульсию масла в воде, содержащую высушенные, убитые нагреванием организмы Mycobacterium tuberculosis), сапонин (выделенный из коры Quillaja Saponoria, адъювантно активный компонент, известный как Quile A), CpG ODN (синтетический олигодеоксинуклеотид, содержащий неметилированные динуклеотиды CpG), MPL (полученные из полисахарида Salmonella Minnesota Re595), липосомы (обычно изготовленные из биологически разлагаемых материалов, таких как фосфолипиды) и микрочастицы биологически разлагаемых полимеров (изготовленные из разнообразных полимеров, таких как PLGA, полифосфазен и полиангидриды). Оценивались адъювантные свойства этих соединений, причем каждый адъювант проявил преимущества и недостатки.
Самой большой проблемой применения адъювантов для человеческих вакцин, в частности для обычных детских вакцин, является токсичность и побочные эффекты большинства адъювантных препаративных форм. Применение новых технологий при разработке вакцин ведет к получению очищенных субъединичных и синтетических антигенов, которые имеют тенденцию к низкой иммуногенности. Разработка новых адъювантов для повышения иммуногенности/эффективности и снижения побочных эффектов представляет одну из главных проблем исследования и разработки вакцин.
Полинуклеотидные комплексы исследовали в плане их различных видов применения, включая действие в качестве адъювантов. Двухнитевые РНК ((dsRNAs) представляют собой очень активные биологические модификаторы, которые в наномолярных концентрациях могут оказывать глубокое влияние на клетки. Модулирующие эффекты dsRNA включают широкий спектр видов действия на молекулярном и клеточном уровне.
На молекулярном уровне dsRNAs могут вызвать биологические эффекты, такие как синтез интерферона, индукция протеин-киназы, усиление антигена тканевой совместимости и ингибирование метаболизма. А на клеточном уровне dsRNAs могут вызвать биологические эффекты, такие как пирогенность, митогенность, активация макрофагов, активация клеточно-опосредованного иммунитета и индукция противовирусного состояния. Один перспективный потенциал dsRNAs состоит в их иммуномодулирующем эффекте при способах противомикробного лечения. В патенте США № 4124702 раскрыто, что двухнитевые полинуклеотиды вызывали индукцию интерферона в клетках живых животных. В патенте США № 3906092 раскрыто, что реакция антител на вакцину адъювантного типа усиливалась включением в вакцину полинуклеотида или комплекса полинуклеотидов. Houston et al. установили PICLC (комплекс полиинозиновой кислоты, полицитидиловой кислоты, поли-L-лизинкарбоксиметилцеллюлозы) как сильнодействующий адъювант увеличением первичной реакции антител без содействия дополнительного адъюванта (Houston et al., Infection and Immunity, 14:318-9, 1976C). Было обнаружено, что миковирусная dsRNA значительно усиливает гемагглютинирующую реакцию антител на бараньи эритроциты (sRBC) (Wright and Adler-Moore, Biochemical and Biophysical Research Communications, 131:949-45, 1985).
Однако PIC (полиинозиновая кислота, полицитидиловая кислота) проявляет тяжелую токсичность при применении у животных. Например, Phillips et al. сообщили, что тяжелые токсические проявления были вызваны у собак после субхронического введения PIC в дозе 2,0 мг/кг. Токсичность характеризовалась сниженной спонтанной активностью, плохой координацией, рвотой, анорексией, потерей массы тела, гематологическими изменениями, отражающими сниженный гематопоэзиз, сниженной активностью щелочной фосфатазы и трансаминазы, дегенерацией тимуса, деструкцией костного мозга, расширением печеночных синусоидальных капилляров в центрально-долевых областях, некрозом клеток печени, коллапсом структур печени и генерализованным артритом (см. Phillips et al., Toxicology and Applied Pharmacology, 18:220-30, 1971).
PIC, один из наиболее изученных полинуклеотидных комплексов, был неэффективен при использовании у обезьян и людей ввиду его неустойчивости в организме после введения. Таким образом, PIC был модифицирован множественными путями для преодоления одного или другого недостатка. Например, комплекс полирибоинозиновой-полирибоцитидиловой кислоты с поли-L-лизингидробромидом примерно в 5-15 раз устойчивее к гидролизу панкреатической рибонуклеазой, чем материнский PIC. Другим примером является полиICLC dsRNA, или сокращенно PICLC, который, как было обнаружено, высоко эффективен в качестве противовирусного или противоопухолевого средства. PICLC представляет собой синтетическую dsRNA, составленную из нитей полирибоинозиновой и полирибоцитидиловой кислот (PIC). Хотя PICLC представляет собой перспективный иммуностимулятор, который имеет большой потенциал при способах противомикробного и противоракового лечения, было показано, что он вызывает серьезные побочные эффекты у людей, особенно при введении препарата во множественных, высоких дозах. Некоторые из отмеченных побочных эффектов включают лихорадку, гипотонию, лейкопению, миалгию, тромбоцитопению и полиартралгию. Присущую проблему токсичности необходимо преодолеть для придания PICLC безопасности с целью применения у людей. Кроме того, терапевтическая эффективность поли ICLC ограничена устойчивостью in vivo.
Противовирусное средство, состоящее из полиинозиновой кислоты-полицитидиловой кислоты (поли I:C), канамицина и кальция (Av-PICKCa), используется для лечения вирусных инфекций. Было показано, что Av-PICKCa способен индуцировать продукцию интерферона и интерлейкина-2. Av-PICKCa, введенный отдельно в качестве противовирусного препарата, стимулирует неспецифический иммунный ответ, т.е. стимулирует форму интерферона, которая не специфична для любого конкретного антигена. Эта противовирусная реакция глубоко отлична от специфического для антигена иммунного ответа, генерированного при введении адъюванта в сочетании с антигеном.
Важнее то, что автор настоящего изобретения обнаружил, что у Av-PICKCa были свойства адъюванта, т.е. способность вызывать специфический иммунный ответ при введении с антигеном. Далее, автор изобретения, кроме того, обнаружил, что Av-PICKCa был эффективным адъювантом при применении вместе с антигенами бешенства и геморрагической лихорадки.
Lin et al. описали, что Av-PICKCa можно применять в качестве адъюванта (Lin, et al., A new immunostimulatory complex (PICKCa) in experimental rabies: antiviral and adjuvant effects, Arch Virol, 131:307-19, 1993; и патент Китая № 93105862.7). В патенте Китая № 93105862.7 раскрыто применение общей композиции поли I:C, канамицина и кальция (PICKCa) в качестве адъюванта в вакцине для применения у людей и млекопитающих.
Образцы Av-PICKCa являются гетерогенными в отношении размера и массы молекул. Av-PICKCa описан в литературе с точки зрения среднего или диапазона величин коэффициента осаждения, по данным измерения Svedberg S. Противовирусный препарат Av-PICKCa существует в одном варианте осуществления от 5S до 8S (источник А), см. Zhung J.C., Research recollection of polyinosinic-polycytidylic acid (PIC). Доклад, представленный на 5-й Китайской конференции “fifth Chinese interferon conference in clinical application and theory”, Siam 1985, pp.23-28. В других вариантах осуществления Av-PICKCa существует с коэффициентом осаждения от 4S до 12S при среднем коэффициенте 6S (источник В) или от 5S до 12S при среднем коэффициенте 7S (источник С), или от 8S до 10S (источник D), см. Hu Q.G., Tianjin Av-PICKCa's laboratory research and clinical application, Fujian Medical Journal, 1983.12; (6) 28-30 and Hu Q.G. Chinese Medical and Pharmaceutical Industry Journal, 1983 (9) 3134.
Коэффициент осаждения этой гетерогенной коллекции молекул в Av-PICKCa можно перевести в эквивалентную молекулярную массу (мм в дальтонах) с использованием формулы перевода мм = 1,100×S2,2 Su B.X. et al.; Introduction of Biochemical Technology, 1st Edition, Zhongshan University, 1978, 356-357). Результаты перевода в дальтоны представлены ниже в таблице.
| Таблица АХарактеристики Av-PICKCa | ||||||
| Источник Av-PICKCa | Коэффициент осаждения S | Молекулярная масса в дальтонах | ||||
| Минимальный | Максимальный | Средний | Минимальный | Максимальный | Средний | |
| А | 5 | 8 | ∗ | 38,000 | 107,000 | ∗ |
| В | 4 | 12 | 6 | 23,000 | 260,000 | 57,000 |
| C | 5 | 12 | 7 | 38,000 | 260,000 | 79,000 |
| D | 8 | 10 | ∗ | 107,000 | 174,000 | ∗ |
Оригинальное исследование Av-PICKCa в качестве адъюванта Lin et al. проводилось с образцом, имеющим молекулы, которые имели свойства, аналогичные источнику А, т.е. коэффициент осаждения от 5S до 8S, то есть эквивалентную молекулярную массу молекул в диапазоне от 38000 дальтон до 107000 дальтон (см. Lin et al. выше).
Считалось, что все формы PICKCa одинаково безопасны и эффективны при условии, что Av-PICKCa представляет собой по существу форму PICKCa, и, кроме того, при условии традиционного применения Av-PICKCa в качестве противовирусного препарата. Однако оказалось, что это не так. Исследование, проведенное автором изобретения, демонстрирует, что эффективность и токсичность PICKCa при использовании в качестве адъюванта в комбинации с антигеном, в действительности, варьируется в зависимости от различной молекулярной массы. Автор изобретения обнаружил, что Av-PICKCa не обеспечивает оптимальный профиль эффективности/безопасности для применения в качестве адъюванта и что PICKCa в определенных условиях вызывает неприемлемые, неблагоприятные побочные эффекты. Таким образом, остается потребность в адъюванте, который более подходит для применения у людей и который безопасен и эффективен при обеспечении желаемого иммуногенного эффекта. Настоящее изобретение направлено на эту потребность и предоставляет другие преимущества, которые будут очевидны при ссылке на подробное описание.
Литература
Интерес могут представлять следующие ссылки:
Патент Японии 1093540А2;
Патент США № 4124702;
Патент США № 3692899;
Патент США № 3906092;
Патент США № 4389395;
Патент США № 4349538;
Патент США № 4024241;
Патент США № 3952097;
Houston et al., Infection and Immunity, 14: 318-9, 1976C;
Wright and Adler-Moore, Biochemical and Biophysical Research Communications, 131: 949-45, 1985;
Phillips et al., Toxicology and Applied Pharmacology, 18: 220-30, 1971;
Lin, et al., A new immunostimulatory complex (PICKCa) in experimental rabies: antiviral and adjuvant effects, Arch Virol, 131: 307-19, 1993;
China Patent 93105862.7;
Zhung J.C., Research recollection of polyinosinic-polycytidylic acid (PIC). The paper of fifth Chinese interferon conference in clinical application and theory, Siam 1985, pp.23-28;
Hu Q.G., Tianjin Av-PICKCa's laboratory research and clinical application, Fujian Medical Journal, 1983,12; (6): 28-30;
Hu Q.G. Chinese Medical and Pharmaceutical Industry Journal, 1983 (9) 3134;
Su B.X. et al; Introduction of Biochemical Technology, 1st Edition, Zhongshan University, 1978, 356-357;
Gupta R.K. et al., Adjuvants - a balance between toxicity and adjuvanticity, Vaccine, 11:293-306, 1993;
Arnon, R. (Ed.) Synthetic Vaccines 1:83-92, CRC Press, Inc., Boca Raton, Fla., 1987;
Sela, M., Science 166:1365-1374 (1969);
Патент США № 6008200;
Ellouz et al., Biochem & Biophy. Res. Comm., 59:1317, 1974;
Патент США № 4094971;
Патент США № 4101536;
Патент США № 4153684;
Патент США № 4235771;
Патент США № 4323559;
Патент США № 4327085;
Патент США № 4185089;
Патент США № 4082736;
Патент США № 4369178;
Патент США № 4314998;
Патент США № 4082735;
Патент США № 4186194;
Патент США № 6468558;
New Trends and Developments in Vaccines, edited by Voller et al., University Park Press, Baltimore, Md., USA, 1978;
Klein, J., et al., Immunology (2nd), Blackwell Science Inc., Boston (1997);
Gupa R.K. and Siber G.R., Adjuvants for human vaccines-current status, problems and future prospects, Vaccine, 13 (14): 1263-1276, 1995;
Richard T., Kenney et al., Meeting Report - 2nd meeting on novel adjuvants currently in/close to human clinical testing, Vaccine 20 2155-2163, 2002;
Laboratory Techniques in Rabies Edited by F.X.Meslin, M.M.Kaplan, H.Koprowski 4th Edition ISBN 92 4 1544 1.
Краткое описание сущности изобретения
Настоящее изобретение относится к полинуклеотидной адъювантной композиции и способам ее применения при индукции иммунного ответа. Настоящее изобретение также относится к иммуногенной композиции, включающей композицию полинуклеотидного адъюванта вместе с антигеном (например, в качестве вакцины). Адъювантные композиции по изобретению имеют определенные физические свойства (например, молекулярную массу, размер, концентрацию и рН), которые направлены на удовлетворение потребности в эффективном и безопасном адъюванте для индукции усиленного иммунного ответа. Настоящее изобретение, кроме того, относится к способам применения таких адъювантных композиций, в частности, при индукции иммунного ответа на антигенное соединение.
В одном варианте осуществления изобретение относится к полинуклеотидной адъювантной композиции, включающей полирибоинозиновую-полирибоцитидиловую кислоту (PIC), антибиотик и положительный ион, где антибиотик может представлять собой канамицин, а положительный ион может представлять собой двухвалентный ион, такой как кальций. Настоящее изобретение также относится к иммуногенной композиции, включающей полинуклеотидную адъювантную композицию вместе с антигеном или вакциной.
Настоящее изобретение служит для углубления накопленных знаний путем определения новой композиции, которую можно безопасно и эффективно использовать в качестве адъюванта для усиления и/или модификации иммунного ответа у хозяина-животного или человека. Хотя в предшествующих описаниях демонстрируется применение противовирусного препарата Av-PICKCa для применения в качестве адъюванта, эта форма PICKCa, по наблюдениям, вызывала ограниченный специфический иммунный ответ при введении с антигеном. Кроме того, было обнаружено, что PICKCa в определенных условиях вызывает неприемлемые неблагоприятные побочные эффекты.
Настоящее изобретение направлено на решение этих проблем предоставлением адъювантной композиции, в целом именуемой здесь “PIKA”, которую можно наиболее эффективно и безопасно вводить в качестве адъюванта у животных, включая людей.
PIKA представляет собой композицию, включающую полинуклеотид, антибиотик и положительный ион, который был специально разработан в качестве адъюванта. В изобретение включены композиции, имеющие необычные свойства продукта, которые делают его наиболее подходящим для применения в качестве адъюванта в иммуногенной композиции, подлежащей введению животным и/или людям.
Конкретнее - настоящее изобретение относится к полинуклеотидной адъювантной композиции, включающей полинуклеотид, антибиотик и положительный ион, где полинуклеотид может представлять собой полирибоинозиновую-полирибоцитидиловую кислоту (PIC), антибиотик представляет собой канамицин, антрациклин, бутирозинсульфат, гентамицин, гигромицин, амикацин, дибекацин, небрамицин, метрзамид, неомицин, пуромицин, стрептомицин или стрептозоцин и ион представляет собой кальций, кадмий, литий, магний, церий, цезий, хром, кобальт, дейтерий, галлий, йод, железо или цинк.
Конкретнее - настоящее изобретение относится к спецификации, включающей молекулярную массу, концентрацию и рН, композиции, включающей полинуклеотид, антибиотик и положительный ион, которая направлена на удовлетворение потребности в безопасном адъюванте, который вызывает максимальный желаемый иммунный ответ.
Настоящее изобретение также относится к иммуногенной композиции, включающей полинуклеотидную адъювантную композицию и антиген или вакцину.
В определенных вариантах осуществления настоящее изобретение представлено в форме набора, включающего полинуклеотидный адъювант и иммуногенное соединение.
Кроме того, настоящее изобретение относится к способу усиления иммунного ответа на антигенное соединение введением хозяину иммуногенной композиции. Хозяин может представлять собой человека или животное. Введение можно осуществлять инъекцией, такой как внутримышечная, внутрибрюшинная, внутривенная или подкожная инъекция, или ингаляцией. В других вариантах осуществления иммуногенную композицию можно доставлять ректально, вагинально, интраназально, перорально, в глаза, местно, трансдермально или интрадермально.
Соответственно, настоящее изобретение относится к адъюванту и иммуногенной композиции, которую можно безопасно применять у людей и животных.
Соответственно, в одном аспекте изобретение характеризует полинуклеотидную адъювантную композицию, включающую полирибоинозиновую-полирибоцитидиловую кислоту (PIC), антибиотик и положительный ион, где композиция содержит молекулы адъюванта, гетерогенные по молекулярной массе, причем молекулярная масса составляет примерно от 66000 до 1200000 дальтон.
В родственных вариантах осуществления молекулы полинуклеотидной адъювантной композиции гетерогенны по молекулярной массе, причем молекулярная масса составляет примерно от 300000 до 1200000 дальтон, или примерно от 66000 до 660000 дальтон, или примерно от 300000 до 660000 дальтон, или примерно от 300000 до 2000000 дальтон, или примерно от 300000 до 4000000 дальтон, или примерно от 500000 до 1000000 дальтон, или примерно от 1000000 до 1500000, или примерно от 1500000 до 2000000 дальтон, или примерно от 2000000 до 2500000 дальтон, или примерно от 2500000 до 3000000 дальтон, или примерно от 3000000 до 3500000 дальтон, или примерно от 3500000 до 4000000 дальтон, или примерно от 4000000 до 4500000 дальтон, или примерно от 4500000 до 5000000 дальтон.
В родственных вариантах осуществления молекулы полинуклеотидной адъювантной композиции в композиции имеют среднюю молекулярную массу, равную или больше чем 150000 дальтон, или равную или больше чем 250000 дальтон, или равную или больше чем 350000 дальтон, или равную или больше чем 500000 дальтон, или равную или больше чем 650000 дальтон, или равную или больше чем 750000 дальтон, или равную или больше чем 1000000 дальтон, или равную или больше чем 1200000 дальтон, или равную или больше чем 1500000 дальтон, или равную или больше чем 2000000 дальтон.
Соответственно, в одном аспекте изобретение характеризует полинуклеотидную адъювантную композицию, включающую полирибоинозиновую-полирибоцитидиловую кислоту (PIC), антибиотик и положительный ион, где композиция содержит молекулы адъюванта, гетерогенные по размеру молекул, имеющих коэффициент осаждения в Svedbergs (сведбергах) (S) примерно от 6,43S до 24,03S.
В родственных вариантах осуществления молекулы полинуклеотидной адъювантной композиции гетерогенны по молекулярному размеру, причем молекулярный размер составляет примерно от 12,8S до 24,03S, или примерно от 6,43S до 18,31S, или примерно от 12,8S до 18,31S, или примерно от 12,8S до 30,31S, или примерно от 12,8S до 41,54S, или примерно от 13,5S до 18,31S, или примерно от 13,5S до 24,03S, или примерно от 16,14S до 22,12S, или примерно от 22,12S до 26,6S, или примерно от 26,6S до 30,31S, или примерно от 30,31S до 35,55S, или примерно от 33,55S до 36,45S, или примерно от 36,45S до 39,1S, или примерно от 39,1S до 41,54S, или примерно от 41,54S до 43,83S, или примерно от 43,83S до 45,95S.
В других родственных вариантах осуществления полинуклеотидная адъювантная композиция имеет средний коэффициент осаждения (в сведбергах) больше чем 9, или больше чем 12, или больше чем 13,5, или больше чем 15, или больше чем 16, или больше чем 17, или больше чем 18, или больше чем 19, или больше чем 20, или больше чем 21, или больше чем 22, или больше чем 25, или больше чем 30.
В родственном варианте осуществления антибиотик в композиции представляет собой канамицин, неомицин, антрациклин, бутирозин сульфат, гентамицин, гигромицин, амикацин, дибекацин, небрамицин, метрзамид, пуромицин, стрептомицин или стрептозоцин.
В еще одном родственном варианте осуществления адъювантная композиция, кроме того, включает источник ионов кальция.
В другом родственном варианте осуществления положительный ион в композиции представляет собой кальций, кадмий, литий, магний, церий, цезий, хром, кобальт, дейтерий, галлий, йод, железо или цинк. Положительный ион может быть представлен в форме неорганических солей или органических комплексов.
Источник ионов кальция может быть обеспечен, например, хлоридом кальция, карбонатом кальция, фторидом кальция, гидроксидом кальция, фосфатом кальция или сульфатом кальция.
В одном аспекте, представляющем особый интерес, изобретение относится к полинуклеотидной адъювантной композиции, включающей полирибоинозиновую-полирибоцитидиловую кислоту (PIC), канамицин и кальций, причем композиция включает молекулы адъюванта, гетерогенные по молекулярной массе, составляющей примерно от 66000 до 1200000 дальтон.
В родственных вариантах осуществления молекулы полирибоинозиновой-полирибоцитидиловой кислоты (PIC), канамицина и кальция имеют молекулярную массу примерно от 300000 до 1200000 дальтон, или примерно от 66000 до 660000 дальтон, или примерно от 300000 до 660000 дальтон, или примерно от 300000 до 2000000 дальтон, или примерно от 300000 до 4000000 дальтон, или примерно от 500000 до 1000000, или примерно от 1000000 до 1500000 дальтон, или примерно от 1500000 до 2000000 дальтон, или примерно от 2000000 до 2500000 дальтон, или примерно от 2500000 до 3000000 дальтон, или примерно от 3000000 до 3500000 дальтон, или примерно от 3500000 до 4000000 дальтон, или примерно от 4000000 до 4500000 дальтон, или примерно от 4500000 до 5000000 дальтон.
В других родственных вариантах осуществления молекулы полирибоинозиновой-полирибоцитидиловой кислоты (PIC), канамицина и кальция адъюванта, гетерогенного по молекулярной массе, имеют молекулярную массу, равную или больше чем 150000 дальтон, равную или больше чем 250000 дальтон, или равную или больше чем 350000 дальтон, или равную или больше чем 500000 дальтон, или равную или больше чем 650000 дальтон, или равную или больше чем 750000 дальтон, или равную или больше чем 1000000 дальтон, или равную или больше чем 1200000 дальтон, или равную или больше чем 1500000 дальтон, или равную или больше чем 2000000 дальтон.
В одном аспекте, представляющем особый интерес, изобретение относится к полинуклеотидной адъювантной композиции, включающей полирибоинозиновую-полирибоцитидиловую кислоту (PIC), канамицин и кальций, причем композиция включает молекулы адъюванта, гетерогенные по молекулярному размеру, имеющие коэффициент осаждения в Svedbergs (сведбергах) (S) примерно от 6,43S до 24,0S.
В родственных вариантах осуществления молекулы полинуклеотидной адъювантной композиции являются гетерогенными по молекулярному размеру, причем молекулярный размер составляет примерно от 12,8S до 24,03S, или примерно от 6,43S до 18,31S, или примерно от 12,8S до 18,31S, или примерно от 12,8S до 30,31S, или примерно от 12,8S до 41,54S, или примерно от 13,5S до 18,31S, или примерно от 13,5S до 24,03S, или примерно от 16,14S до 22,12S, или примерно от 22,12S до 26,6S, или примерно от 26,6S до 30,31S, или примерно от 30,31S до 3,55S, или примерно от 33,55S до 36,45S, или примерно от 36,45S до 39,1S, или примерно от 39,1S до 41,54S, или примерно от 41,54S до 43,83S, или примерно от 43,83S до 45,95S.
В других родственных вариантах осуществления полирибоинозиновая-полирибоцитидиловая кислота (PIC), канамицин и кальций имеют средний коэффициент осаждения больше чем 9, или больше чем 12, или больше чем 13,5, или больше чем 15, или больше чем 16, или больше чем 17, или больше чем 18, или больше чем 19, или больше чем 20, или больше чем 21, или больше чем 22, или больше чем 25, или больше чем 30.
В некоторых вариантах осуществления изобретение относится к полинуклеотидной адъювантной композиции, включающей полирибоинозиновую-полирибоцитидиловую кислоту (PIC), канамицин и кальций, причем может быть предпочтительно, чтобы из композиции были исключены молекулы, в частности, в такой степени, чтобы такие исключенные молекулы не оказывали значимого иммуногенного эффекта, причем исключенные молекулы имеют молекулярную массу примерно или меньше чем 30000 дальтон, примерно или меньше чем 40000 дальтон, примерно или меньше чем 50000 дальтон, примерно или меньше чем 60000 дальтон, примерно или меньше чем 70000 дальтон, примерно или меньше чем 80000 дальтон, примерно или меньше чем 90000 дальтон, примерно или меньше чем 100000 дальтон, примерно или меньше чем 150000 дальтон, примерно или меньше чем 200000 дальтон, примерно или меньше чем 300000 дальтон, примерно или меньше чем 350000 дальтон, примерно или меньше чем 400000 дальтон, примерно или меньше чем 450000 дальтон, примерно или меньше чем 500000 дальтон, примерно или меньше чем 600000 дальтон, примерно или меньше чем 700000 дальтон, примерно или меньше чем 800000 дальтон, примерно или меньше чем 900000 дальтон, примерно или меньше чем 1000000 дальтон.
В некоторых вариантах осуществления изобретение относится к полинуклеотидной адъювантной композиции, включающей полирибоинозиновую-полирибоцитидиловую кислоту (PIC), канамицин и кальций, причем может быть предпочтительно, чтобы из композиции были исключены молекулы, в частности, в такой степени, чтобы такие исключенные молекулы не оказывали значимого иммуногенного эффекта, причем исключенные молекулы имеют молекулярный размер примерно или меньше чем 4,49S, примерно или меньше чем 5,12S, примерно или меньше чем 5,67S, примерно или меньше чем 6,16S, примерно или меньше чем 6,6S, примерно или меньше чем 7,02S, примерно или меньше чем 7,4S, примерно или меньше чем 7,77S, примерно или меньше чем 9,34S, примерно или меньше чем 10,64S, примерно или меньше чем 11,78S, примерно или меньше чем 12,8S, примерно или меньше чем 13,73S, примерно или меньше чем 14,59S, примерно или меньше чем 15,39S, примерно или меньше чем 16,14S, примерно или меньше чем 17,54S, примерно или меньше чем 18,81S, примерно или меньше чем 19,99S, примерно или меньше чем 21,09S, примерно или меньше чем 22,12S.
В одном аспекте, представляющем особый интерес, изобретение относится к иммуногенной композиции для усиления антигенности антигенного соединения, включающего полинуклеотидную адъювантную композицию.
В родственных вариантах осуществления иммуногенная композиция включает полинуклеотидный адъювант и антиген.
В родственных вариантах осуществления источником антигена является человеческий антиген, антиген животного, отличного от человека, растительный антиген, бактериальный антиген, грибковый антиген, вирусный антиген, паразитарный антиген или раковый антиген.
В родственных вариантах осуществления иммуногенная композиция включает полинуклеотидную адъювантную композицию и антиген бешенства.
В определенных вариантах осуществления антигены могут быть очищены из натурального источника, синтезированы посредством твердофазного синтеза или могут быть получены посредством рекомбинантной генетики. Антиген может включать белковый фрагмент, включающий одну или более иммуногенных областей молекулы. Антигены могут также быть предоставлены цельными клетками или микроорганизмами (например, цельными вирусными частицами), которые могут быть живыми, ослабленными или усеченными, или убитыми.
В других вариантах осуществления антигены включают один или несколько антигенов из инфекционных агентов, растительного антигена, ракового антигена, аллергенных агентов и другой человеческий антиген, такой как для развития аутоиммунных заболеваний. В других вариантах осуществления антигены включают один или несколько инфекционных агентов из любого из вируса, бактерии, микобактерии, грибов и паразитов.
Полинуклеотидная адъювантная композиция по настоящему изобретению может также использоваться для усиления иммунного ответа против антигенов, продуцируемых применением вакцин ДНК. Последовательности ДНК в этих вакцинах, кодирующие антиген, могут быть или «голыми», или содержащимися в системе доставки, такой как липосомы.
В еще одних вариантах осуществления антиген бешенства выбран из вакцины человеческих диплоидных клеток (HDCV), или очищенной вакцины против бешенства, инактивированной почечными клетками хомячка (HKC-IPRV), или неочищенной вакцины против бешенства, инактивированной почечными клетками хомячка (HKC-ICRV), или очищенной вакцины против бешенства из клеток vero (PVRV), или очищенных клеток куриного эмбриона (РСЕС), или очищенной вакцины утиного эмбриона (PDEV), или очищенного антигена бешенства, инактивированного почечными клетками хомячка (HKC-IPRA), или неочищенного антигена бешенства, инактивированного почечными клетками хомячка (HKC-ICRA).
В одном аспекте, представляющем особый интерес, изобретение относится к иммуногенной композиции для усиления антигенности антигенного соединения, включающего полинуклеотидную адъювантную композицию, которая способна вызвать специфический для антигена клеточно-опосредованный иммунный ответ.
В одном аспекте, представляющем особый интерес, изобретение относится к иммуногенной композиции для усиления антигенности антигенного соединения, включающего полинуклеотидную адъювантную композицию, которая способна вызвать специфический для антигена В клеточный иммунный ответ.
В одном аспекте, представляющем особый интерес, изобретение предоставляет иммуногенную композицию для усиления антигенности антигенного соединения, включающего полинуклеотидную адъювантную композицию, которая способна вызвать комбинированный специфический для антигена Т- и В-клеточный иммунный ответ.
В одном аспекте, представляющем особый интерес, изобретение относится к иммуногенной композиции для усиления антигенности соединения, включающего полинуклеотидную адъювантную композицию и очищенный антиген бешенства, инактивированный почечными клетками хомячка, где присутствие антигена бешенства должно достигать минимального количества, такого как более чем 1 Международной Единицы (МЕ).
В родственных вариантах осуществления иммуногенная композиция включает полинуклеотидную адъювантную композицию и очищенный антиген бешенства, инактивированный почечными клетками хомячка, где присутствие антигена бешенства должно достигать минимального количества, такого как более чем 0,25 Международных Единиц, более чем 0,5 Международных Единиц, более чем 1,2 Международных Единиц, более чем 1,4 Международных Единиц, более чем 1,6 Международных Единиц, более чем 1,8 Международных Единиц, более чем 2,0 Международных Единиц, более чем 2,2 Международных Единиц, более чем 2,4 Международных Единиц, более чем 2,6 Международных Единиц, более чем 2,8 Международных Единиц, более чем 3,0 Международных Единиц, более чем 3,2 Международных Единиц, более чем 3,4 Международных Единиц, более чем 3,6 Международных Единиц, более чем 3,8 Международных Единиц или более чем 4,00 Международных Единиц.
В одном аспекте, представляющем особый интерес, изобретение относится к иммуногенной композиции для усиления антигенности соединения, включающего полинуклеотидную адъювантную композицию и очищенный антиген бешенства, инактивированный почечными клетками хомячка, где адъювант и антиген бешенства присутствуют в соотношении примерно 1:1.
В родственных вариантах осуществления иммуногенная композиция включает полинуклеотидную адъювантную композицию и очищенный антиген бешенства, инактивированный почечными клетками хомячка, где адъювант и антиген бешенства присутствуют в соотношении менее чем 1:10, примерно 1:9, примерно 1:8, примерно 1:7, примерно 1:5, примерно 1:4, примерно 1:3, примерно 1:2, примерно 2:1, примерно 3:1, примерно 4:1. примерно 5:1, примерно 6:1, примерно 7:1, примерно 8:1, примерно 9:1, примерно 10:1, более чем 10:1.
В одном аспекте, представляющем особый интерес, изобретение относится к адъювантной композиции или к иммуногенной композиции, где иммуногенная композиция или адъювантная композиция, содержащаяся в иммуногенной композиции, представлена в твердой или жидкой форме или в растворе, или в суспензии.
В одном аспекте, представляющем особый интерес, изобретение относится к адъювантной композиции или к иммуногенной композиции, включающей адъювантную композицию, где адъювантная композиция или иммуногенная композиция лиофилизирована.
В родственных вариантах осуществления изобретение относится к набору, включающему адъювантную композицию и антигенное соединение.
В одном аспекте, представляющем особый интерес, изобретение относится к применению полинуклеотидной адъювантной композиции для получения лекарственного средства для усиления иммуногенной реакции хозяина.
В одном аспекте, представляющем особый интерес, изобретение относится к способу усиления иммунных ответов на антигенное соединение, включающему введение хозяину иммуногенной композиции для усиления антигенности антигенного соединения, включающего полинуклеотидную адъювантную композицию.
В родственных вариантах осуществления способ введения хозяину иммуногенной композиции может осуществляться одним путем, выбранным из группы, включающей парентеральную инъекцию, внутримышечную инъекцию, внутрибрюшинную инъекцию, внутривенную инъекцию, подкожную инъекцию, ингаляцию, ректальную доставку, вагинальную доставку, интраназальную доставку, пероральную доставку, внутриглазную доставку, местную доставку, трансдермальную доставку или интрадермальную доставку.
В одном аспекте, представляющем особый интерес, изобретение относится к способу усиления иммунных ответов на антигенное соединение, включающему введение хозяину иммуногенной композиции для усиления антигенности антигенного соединения, включающего полинуклеотидную адъювантную композицию, где хозяин представляет собой человека.
В одном аспекте, представляющем особый интерес, изобретение относится к способу усиления иммунных ответов на антигенное соединение, включающему введение хозяину иммуногенной композиции для усиления антигенности антигенного соединения, включающего полинуклеотидную адъювантную композицию, где хозяин представляет собой животное.
Эти и другие признаки и преимущества изобретения станут очевидны из следующего подробного описания предпочтительных вариантов его осуществления в связи с сопровождающими чертежами.
Краткое описание чертежей
На фиг.1 показана относительная молекулярная масса для образцов Av-PICKCa и PIKA.
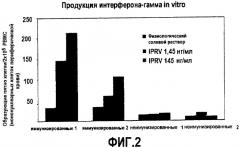
На фиг.2 показано, что PIKA вызывает зависимую от дозы продукцию специфического цитокина интерферона-гамма.
Подробное описание иллюстративных вариантов осуществления изобретения
Настоящее изобретение можно легче понять при ссылке на следующее подробное описание определенных вариантов осуществления изобретения и включенные сюда примеры.
По описанию при ссылке на публикации описания этих публикаций полностью включены сюда в качестве ссылки для более полного описания состояния области, к которой относится изобретение.
Перед дальнейшим описанием настоящего изобретения следует понимать, что это изобретение не ограничивается конкретными описанными вариантами осуществления, поскольку они, конечно, могут варьироваться. Следует также понимать, что используемая здесь терминология предназначена только для цели описания определенных вариантов осуществления, а не предназн