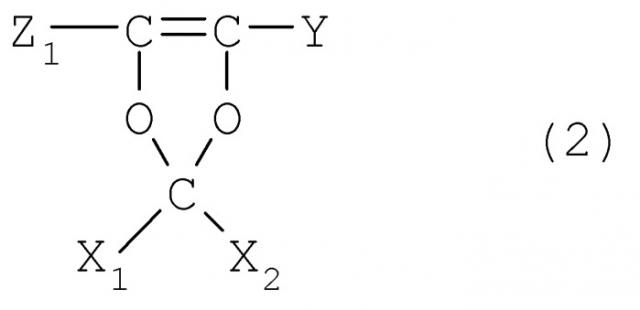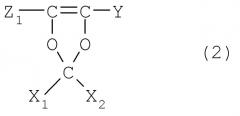Фторэластомеры
Иллюстрации
Показать всеОтверждаемые фторэластомеры, основанные на винилиденфториде VDF, имеющие Tg ниже -35°С и колличество концевых -COF групп ниже чем 0,05 ммоль/кг. Фторэластомеры содержат (А) от 1% до 99% мономера формулы CF2=CFOCF2OCF3 и (В) от 1% до 99% одного или более перфторированных сомономеров, имеющих по меньшей мере одну ненасыщенность этиленового типа. Причем указанные один или более сомономеров (В) содержат винилиденфторид (VDF) в количестве от 1% до 85% по отношению к полным молям мономеров. Изделия из фторэластомеров обладают улучшенной комбинацией механических свойств и остаточной деформацией при сжатии в широком пределе как низких, так и высоких температур. 5 н.п. ф-лы, 1 табл.
Реферат
Данное изобретение относится к фторэластомерам, основанным на винилиденфториде VDF, имеющим Tg (температура стеклования) ниже -35°С и улучшенную комбинацию механических свойств и остаточной деформации при сжатии в широком пределе температур, как при высоких, так и при низких температурах.
Более конкретно данное изобретение относится к фторэластомерам, имеющим Tg ниже -35°С и существенно свободным от концевых -COF групп, причем эти группы не улавливаются рассмотренным ниже способом. Фторэластомеры в соответствии с данным изобретением имеют улучшенную молекулярную массу, что показывает улучшенная собственная вязкость, которые изготавливаются с помощью процесса полимеризации, имеющего повышенную производительность.
Хорошо известно, что фторэластомеры представляют собой полимеры, широко использующиеся в аэрокосмической, нефтяной, химической и электронной промышленностях благодаря комбинации их механических свойств и остаточной деформации при сжатии.
Однако требуется, чтобы эти полимеры имели комбинацию указанных выше свойств в широких пределах температур, как при высоких, так и при низких температурах.
В уровне техники предлагались различные фторэластомеры с комбинацией указанных выше свойств, которые особенно востребованы пользователями фторэластомеров. Однако значение концевых -COF групп во фторэластомерах не указывалось в уровне техники. Заявитель на основании глубоких исследований установил, что в том случае, когда в результате полимеризации получают полимеры, имеющие концевые -COF группы, фторэластомеры не имеют высоких механических свойств и не обладают высокой эластичностью.
Различные фторэластомеры, у которых температура стеклования указывается, известны из уровня техники. Однако с помощью известных из уровня техники решений не получают фторэластомеров с комбинацией низкой Tg и улучшенными механическими свойствами и эластичностью при высоких и низких температурах.
В патенте US 3132123 описывается получение перфторалкилвиниловых эфиров, их гомополимеров и сополимеров с TFE (тетрафторэтилен). Гомополимеры получают в экстремальных экспериментальных условиях, используя давление при полимеризации от 4000 до 18000 атм. Описываемые виниловые эфиры имеют следующую общую формулу:
CF2=CFOR0 F,
где R0 F - перфторалкильный радикал преимущественно с 1-5 атомами углерода. Исследования, проведенные заявителем, показали, что Tg гомополимера не очень низка и находится в пределе -6°С.
Патент US 3450684 относится к виниловым эфирам формулы:
CF2=CFO(CF2CFX0O)n'CF2CF2X0,
где Х0=F, Cl, CF3, H и n' может принимать значение от 1 до 20.
Сообщается также о гомополимерах, полученных УФ-поляризацией. Примеры сополимеров не характеризуются их механическими свойствами и эластичностью при низких температурах.
Патент US 3635926 относится к эмульсионной сополимеризации перфторвиниловых эфиров с TFE. Подчеркивается, что присутствие концевых -COF групп делает полимеры нестабильными. Об этом уже сообщалось в US 3085083 в отношении полимеризационных систем перфторвиниловых эфиров в растворителе.
Патент US 3817960 относится к получению и полимеризации перфторвиниловых эфиров формулы:
CF3O(CF2O)n"CF2CF2OCF=CF2,
где n" может изменяться от 1 до 5. Синтез винилового эфира сложен. Не приводится данных, характеризующих свойства полученного продукта.
Патент US 3896179 относится к выделению "первичных" изомеров фторвиниловых эфиров, например CF3CF2CF2OCF=CF2, из соответствующих "вторичных", менее устойчивых полимеров CF3(CF3)CFOCF=CF2. Последние являются нежелательными продуктами в отношении получения и низких характеристик получаемых полимеров.
Патент US 4487903 относится к получению фотоэластомерных сополимеров с использованием перфторвиниловых эфиров формулы:
CF2=CF(OCF2CFY0)n0OX2,
где n0 может принимать значение от 1 до 4; Y0=F, Cl, CF3, H; X2 может быть C1-С3 перфторалкил, C1-С3 ω-гидроперфторалкил, C1-С3 ω-хлорперфторалкил. Полимер содержит блок фторвиниловых эфиров в пределе от 15 до 50% молярных. Эти виниловые эфиры формируют сополимеры, имеющие при низких температурах свойства, которые выше, чем свойства указанных перфторэластомеров PVE (перфторпропилвиниловый эфир) и MVE. В этом патенте указывается на тот факт, что для достижения хороших свойств при низкой температуре требуется присутствие, по меньшей мере, двух эфирных связей в боковой цепи, примыкающих к двойной связи. Кроме того, в этом патенте для значений n0 более 4 трудно очистить мономеры, и эффект снижения Tg уменьшается. Кроме того, реактивность описанных виниловых эфиров очень низка, и трудно получать полимеры, имеющие большую молекулярную массу и способные обладать эластичностью для указанных назначений. Приводится пример сополимера TFE/перфторвиниловый эфир (n0=2), 31/69% по массе, с Tg -32°С. Однако этот полимер получают за очень долгий промежуток времени протекания реакции (96 часов полимеризации). В этом случае также не приводятся характеристические данные отвержденного эластомера.
В ЕР 130052 описывается полимеризация перфторвинилового полиэфира (PVPE), в результате которой получают аморфные перфторполимеры, имеющие Tg в пределах от -15°С до -100°С. В этом патенте описываются сополимеры и тройные полимеры TFE и MVE с виниловыми эфирами (PVPE) формулы:
где n′′′ находится в пределе от 3 до 30, a R0 f' является перфторалкилом. В связи с трудностями очистки использующиеся виниловые эфиры являются смесью виниловых эфиров с различными значениями n′′′. В соответствии с этим патентом наибольший эффект снижения Tg достигается в тех случаях, когда n′′′ равен или более 3, преимущественно более 4. В соответствии с примерами полимеризации, описанными в указанном патенте, конечная масса полимера, кроме обработки нагревом и в вакууме, должна затем промываться фреоном ® TF для того, чтобы удалить весь непрореагировавший мономер (PVPE). Судя по этому примеру, реактивность всех описанных мономеров (PVPE) низкая.
Патент US 4766190 относится к полимеризации перфторвиниловых полиэфиров (PVPE), аналогичных тем, которые рассматриваются в US 4487903 с TFE и небольшим в процентном отношении содержании перфторпропена для улучшения механических свойств получаемых полимеров.
Патент US 5401818 относится к получению перфторвиниловых эфиров формулы:
R1 f(OCF2CF2CF2)m'-OCF=CF2,
(где R1 f является C1-С3 перфторалкильным радикалом и m' - целое число от 1 до 4) и соответствующих сополимеров, имеющих улучшенные свойства при низких температурах. Получение указанных перфторвиниловых эфиров проходит через 7 стадий, из которых некоторые имеют очень низкий выход, а также включают фторирование элементарным F2. Тем не менее реактивность указанных перфторвиниловых эфиров остается низкой.
Другие проблемы, отмеченные в документах из уровня техники, относятся к низкой реактивности перфторвиниловых эфиров, в связи с чем необходимо извлекать из полученных продуктов непрореагировавшие мономеры (английский патент GB 1514700), а также решать проблемы стабильности полимеров, имеющих концевые -C(O)F группы (US 3635926). Последние могут далее трансформироваться с помощью подходящих реагентов с целью повышения стабильности полимеров (ЕР 178935).
Перфтороксиалкилвиниловые эфиры используются также для придания резинам требующихся свойств при низких температурах и, в частности, для снижения температуры стеклования.
При увеличении перфтороксиалкиленовых блоков снижается Tg аморфных сополимеров, но в то же время реактивность винилового эфира значительно понижается, и получение полимеров с достаточно большой молекулярной массой и хорошими свойствами становится очень трудно или вообще невозможно. Отмеченные ранее проблемы удаления непрореагировавших мономеров из полученных полимеризацией продуктов или из самого полимера остаются (US 4487903 - ЕР 130052).
Аморфные TFE сополимеры с перфторметилвиниловым эфиром имеют Tg около 0°С или немного ниже (Maskornik, M. et al. "ECD-006 Fluoroelastomer - A high performance engineering material", Soc. Plast. Eng. Tech. Pao. (1974), 20, 675-7).
Экстраполированное значение Tg для гомополимера MVE составляет около -5°С (J.Macromol. Sci.-Phys., B1 (4), 815-830, Dec. 1967).
Известны другие патенты, описывающие виниловые эфиры для получения фторэластомеров. См. патенты US 6255536, ЕР 1117710, WO 99/48939 и US 6696216.
Более детально, известны фторэластомерные сополимеры, пригодные для изготовления уплотнительных колец, основанные на мономерных блоках, полученных из винилиденфторида (VDF), гексафторпропена (HFP), перфторалкилвиниловых эфиров (PAVE), как, например, метилвиниловый эфир, и, необязательно, тетрафторэтилен (TFE), который способен ионно отверждаться, имеют хорошие эластомерные свойства при низких и высоких температурах и хорошую способность к обработке, как, например, извлечение из формы после отверждения (см. US 5260393). Однако указанные фторэластомеры имеют температуру стеклования (Tg) выше -35°С. Поэтому они непригодны для использования при температурах ниже -35°С, так как теряют их эластомерные свойства.
Патентная заявка ЕР 1308467 описывает перфторэластомеры, содержащие фторалкоксивиниловые эфиры формулы CFXA=CXAOCF2ORA, где XA=F, H; RA - С2-С6 перфторалкил, перфтороксиалкил или C5-C6 циклический (пер)фторалкил. В частности, описываются следующие перфторалкоксивиниловые эфиры: CF2=CFOCF2OCF2CF3 (MOVE 1) и CF2=CFOCF2OCF2CF2OCF3 (MOVE 2). В Примерах описываются перфторэластомеры, содержащие не более 40% указанных перфторалкоксивиниловых эфиров. MOVE перфторэластомеры с TFE содержат концевые -COF группы. См. сравнительные Примеры. Для приготовления полимерных композиций, содержащих TFE в количестве, ниже или равном 60% в молярном отношении, необходимо проводить полимеризацию в течение длительного времени. С промышленной точки зрения это представляет собой недостаток, так как производительность ухудшается.
В ЕР 1304341 описываются фторэластомеры, содержащие фторалкоксивиниловые эфиры формулы CFXA=-CXAOCF2ORA, где ХА=F, H; RA - С2-С6 перфторалкил, перфтороксиалкил или C5-C6 циклический (пер)фторалкил. В частности, описаны следующие перфторалкоксивиниловые эфиры: CF2=CFOCF2OCF2CF3 (MOVE 1) и CF2=CFOCF2OCF2CF2OCF3 (MOVE 2). В Примерах приводятся фторэластомеры, содержащие не более 19% указанных перфторалкоксивиниловых эфиров. Тесты, проведенные заявителем, показали, что указанные фторэластомеры имеют концевые -COF группы, которые, как указывалось, ухудшают механические свойства при высоких температурах и термостойкость указанных полимеров.
Ощущается потребность в получении основанных на VDF фторэластомеров, имеющих следующую комбинацию свойств:
- Tg ниже -35°С, преимущественно ниже -40°С, более преимущественно ниже -45°С;
- существенно свободные от концевых -COF групп, причем указанные группы не улавливаются способом, указанным ниже;
- улучшенная молекулярная масса, определяемая по более высокой внутренней вязкости;
- улучшенные механические свойства и остаточная деформация при сжатии в широких пределах как высоких, так и низких температур;
- улучшенная производительность процесса получения фторэластомеров, выраженная через величину (масса полимера в кг/час × литр воды).
Заявитель неожиданно и к его удивлению открыл фторэластомеры, имеющие удивительно улучшенную комбинацию рассмотренных выше качеств.
Целью данного изобретения являются отверждаемые VDF-base фторэластомеры, имеющие температуру стеклования ниже -35°С, преимущественно ниже -40°С, более преимущественно ниже -45°С, и имеющие количество концевых -COF групп ниже, чем уровень чувствительности описанного ниже метода; в конце полимеризации полимер изолируется коагуляцией с помощью замораживания и последующего размораживания; он промывается дважды деминерализованной водой и высушивается в печи до достижения постоянного веса; концевые -COF группы определяются ФТ-ИК-спектроскопией, когда на полимерной пленке, имеющей толщину от 50 до 300 микрон, проводится сканирование между 4000 см-1 и 400 см-1, пленка выдерживается в течение 12 часов в атмосфере, насыщенной парами аммиака, и после этого ведется запись ИК-спектра в тех же условиях, в которых получался первоначальный ИК-спектр; обрабатываются оба спектра, вычитая из сигналов спектра необработанного образца (первоначальный спектр) соответствующие сигналы спектра образца после обработки парами аммиака, получают спектр "различия", нормализованный следующим уравнением:
измеряются оптические плотности, относящиеся к концевым -COF группам, прореагировавшим с парами аммиака; оптические плотности преобразовываются в ммоль/кг полимера, используя коэффициент удаления, указанный в таблице страница 73 отчета М.Pianca и др. "End groups in fluoropolymers", J. Fluorine Chem. 95 (1999), 71-84 (использован здесь в качестве ссылки); полученные значения выражают концентрацию остаточных концевых -COF групп в ммолях концевых -COF групп на 1 кг полимера: в спектре фторэластомера не отслеживается линий, относящихся к концевым -COF группам (1900-1830 см-1) при пределе чувствительности метода 0.05 ммоль/кг.
Более точно, количество концевых -COF групп в полимере определяется на ФТ-ИК оборудовании Nicolet® Nexus (256 сканирований, разрешение 2 см-1).
Фторэластомеры в соответствии с данным изобретением содержат также блоки, извлекаемые из бис-олефинов общей формулы:
где R1, R2, R3, R4, R5, R6, равные или отличающиеся друг от друга, представляют Н или C1-C5 алкилы;
Z представляет С1-С58 линейный или разветвленный алкилен или циклоалкиленный радикал, необязательно содержащий атомы кислорода, преимущественно, по меньшей мере, частично фторированный, или (пер)фторполиоксиалкиленный радикал, как тот, который описан в патенте ЕР 661304, выданном на имя заявителя.
Количество бис-олефинов обычно составляет от 0.01 до 1.0% молярных, преимущественно от 0.03 до 0.5% молярных и еще более преимущественно от 0.05 до 0.2 молей на 100 молей приведенных выше мономерных блоков, составляющих основную структуру фторэластомера; полная сумма мономеров составляет 100%.
В формуле (I) Z преимущественно является С4-С12, более преимущественно С4-С8, перфторалкиленовый радикал, в то время как R1, R2, R3, R4, R5, R6 являются преимущественно водородом; когда Z является (пер)фторполиоксиалкиленом, он может включать блоки, выбранные из следующих:
-CF2CF2O-, -CF2CF(CF3)O-, -CFX1O-, где X1=F, CF3, -CF2CF2CF2O-, -CF2-CH2CH2O-, -C3F6O-.
Преимущественно Z выражается формулой:
где Q является C1-С10 алкиленовым или оксиалкиленовым радикалом; p=0 или 1; m и n - такие числа, что отношение m/n находится в пределе между 0.2 и 5, и молекулярная масса указанного (пер)фторполиоксиалкиленового радикала находится в пределах 500-10000, преимущественно 700-2000.
Преимущественно Q выбирается из
-CH2OCH2-; -CH2O(CH2CH2O)sCH2-, где s=1-3.
Бис-олефины формулы (I), где Z является алкиленом или циклоалкиленом, могут получаться в соответствии с описанием в литературе, например, у И.Л.Кнуньянц и др. в Изв. Акад. наук СССР, сер. Химия, 1964(2), стр.384-6. Бис-олефины, содержащие структуры (пер)фторполиоксиалкилена, описаны в патенте US 3810874.
Более преимущественно бис-олефины имеют формулу:
CH2=CH-(CF2)t0-CH=CH2
где t0 - целое число от 6 до 10.
Бис-олефины формулы:
являются особенно преимущественными.
Фторэластомеры в соответствии с данным изобретением отверждаются пероксидным путем. Когда фторэластомеры по данному изобретению отверждаются пероксидным путем, они содержат преимущественно йод и/или бром, более преимущественно йод, в количествах, обычно находящихся в пределах от 0.001% до 5% по массе, преимущественно в пределах от 0.01% до 2.5% по массе в отношении к полной массе полимера. Атомы йода могут находиться внутри цепи и/или в концевом положении.
Для введения атомов йода и/или брома в цепь проводится сополимеризация основных мономеров фторэластомера с подходящими фторированными сомономерами, содержащими йод и/или бром (мономеры при отверждении), см., например, патенты US 4745165, US 4831085, US 4214060, EP 683149. Указанный фторированный сомономер, содержащий йод, может выбираться, например, из следующих соединений:
(a) йодо(пер)фторалкил-перфторвиниловый эфир формулы:
где Rf-C1-C12 (пер)фторалкилен, необязательно содержащий хлор и/или атомы кислорода эфира;
например: ICF2-O-CF=CF2, ICF2CF2-O-CF=CF2, ICF2CF2CF-O-CF=CF2, CF3CFICF2-O-CF=CF2 и подобные им;
(b) йод-(пер)фторолефины формулы:
где R′f - C1-C12 (пер)фторалкилен, необязательно содержащий атомы хлора; например: йодтрифторэтилен, 1-йод-2,2-дифторэтилен, йод-3,3,4,4-тетрафторбутан-1, 4-йодперфторбутан-1 и подобные им;
(c) йод-(пер)фторолефины формулы:
где Ro=Н или -СН3; Zo-C1-C-18 линейный или разветвленный (пер)фторалкилен, необязательно содержащий один или более атомов кислорода, или (пер)фторполиоксиалкилен, определенный выше.
Другими йодированными сополимерами при отверждении являются йодфторалкилвиниловые эфиры, см. патенты US 4745165 и US 4564662.
Кроме или в дополнение к йодированным сомономерам, фторэластомер может содержать атомы йода в концевой позиции, получаемые из подходящего йодированного цепного трансферного агента, вводимого в реакционную среду во время приготовления полимера, как описано в патенте US 4501869. Указанные трансферные агенты имеют формулу RA f(I)x, где RA f - радикал C1-C-12 (пер)фторалкил, необязательно содержащий атомы хлора, а х=1 или 2.
Указанный трансферный агент может выбираться, например, из CF2I2, I(CF2)6I,
I(CF2)4I, CF2ClI, CF3CFICF2I и им подобных.
Для йода, вводимого в качестве цепной концевой группы путем добавления йодированного цепного трансферного агента, как упомянутый выше, см., например, US 4243770 и US 4943622.
Возможно также использовать в качестве цепных трансферных агентов йодиды щелочных или щелочноземельных металлов в соответствии с патентной заявкой ЕР 407937.
В комбинации с цепными трансферными агентами, содержащими йод, могут использоваться другие известные в уровне техники цепные трансферные агенты, как этилацетат, диэтилмалонат и т.п.
Количество йода в концевой позиции фторэластомера обычно составляет между 0.001% и 3%, преимущественно между 0.01% и 1% по массе в отношении к массе фторэластомера. См. US 4035565 и US 4694045.
Кроме того, отвержденные фторэластомеры могут также содержать, кроме йода или в комбинации с ним, бром в цепи или в концевой позиции. Бром может вводиться в цепь с помощью известной технологии, см., например, US 4035565, US 4745165, EP 199138; или как концевой бром, как описывается в US 4501869.
Преимущественно перфторэластомер содержит атомы йода в цепи и/или в концевой позиции.
Необязательно перфторэластомеры по данному изобретению содержат в смеси полукристаллический (пер)фторполимер в количестве в процентах по массе, соотнесенных с полной сухой массой смеси фторэластомер + полукристаллический (пер)фторполимер, от 0% до 70%, преимущественно от 0% до 50%, еще более преимущественно от 2% до 30% по массе.
Под понятием полукристаллический (пер)фторполимер имеется в виду (пер)фторполимер, который имеет не только температуру стеклования Tg, но и, по меньшей мере, одну температуру плавления кристаллов.
Полукристаллический (пер)фторполимер составляется из тетрафторэтиленовых (TFE) гомополимеров или TFE сополимеров с одним или более мономерами, содержащими, по меньшей мере, одну ненасыщенность этиленового типа, в количестве от 0.01% до 10% молярных, преимущественно от 0.05% до 7% молярных.
Указанные сомономеры, имеющие этиленовую ненасыщенность, могут быть как гидрированного, так и фторированного типа. Среди гидрированных можно указать этилен, пропилен, акриловые мономеры, например метилметакрилат, (мет)акриловая кислота, бутилакрилат, гидроксиэтилгексилакрилат, стироловые мономеры.
Среди фторированных сомономеров можно назвать:
- С3-С8 перфторолефины, как гексафторпропен (HFP), гексафторизобутан;
- С2-С8 гидрированные фторолефины, как винилфторид (VF), винилидинфторид (VDF), трифторэтилен, перфторалкилэтилен CH2=CH-Rf, где Rf - C1-C6 перфторалкил;
- С2-С8 хлор- и/или бром- и/или йод-фторолефины, как хлортрифторэтилен (CTFE);
- CF2=CFORf (пер)фторалкилвиниловые эфиры (PAVE), где Rf - C1-C6 (пер) фторалкил, например CF3, C2F5, C3F7;
- CF2=CFOX (пер)фтороксиалкилвиниловые эфиры, где Х=C1-C12 алкил или C1-C12 оксиалкил или C1-C12 (пер)фтороксиалкил, имеющий одну или более эфирных групп, например перфтор-2-пропоксипропил; фтордиоксолы, преимущественно перфтордиоксолы.
PAVEы, в частности перфторметил-, этил-, пропилвиниловый эфир и фтордиоксолы, преимущественно перфтордиоксолы, являются преимущественными сомономерами.
Когда фторэластомеры по данному изобретению содержат полукристаллические (пер)фторполимеры, проводится смешивание в желательном соотношении латекса перфторэластомера с латексом полукристаллического перфторполимера, а затем проводится сокоагуляция полученной смеси так, как описано в US 6395834 и US 6310142.
В другом варианте полукристаллический (пер)фторполимер может полимеризироваться, а затем фторэластомер полимеризируется на частицах (пер)фторполимера. Таким образом получают структуру, состоящую из ядер и оболочек.
Заявитель обнаружил, что когда концевые -COF группы во фторполимере после полимеризации существенно отсутствуют при обнаружении изложенным выше методом анализа, получается наилучшая комбинация механических свойств и остаточной деформации при сжатии в широком диапазоне температур, как при высоких, так и при низких температурах.
Другим объектом данного изобретения являются композиции, которые включают:
- фторэластомеры по данному изобретению, имеющие концевые -COF группы в количестве менее чем 0.05 ммоль/кг и Tg, как она была определена выше,
и
- фторэластомеры, получаемые из полимеров, содержащих концевые -COF группы в количестве более 0.05 ммоль/кг при условии, что количество перфторэластомера по данному изобретению составляет, по меньшей мере, 5-10% по массе, преимущественно 20-40% по массе, более преимущественно 50% по массе в отношении полной массы фторэластомеров в композиции.
Эти композиции могут быть получены различными путями. Например, когда мономеры, привносящие концевые -COF группы, используются в полимеризации для получения улучшенных свойств в соответствии с данным изобретением, проводится частичная полимеризация мономеров в отсутствие тех мономеров, которые привносят концевые -COF группы, чтобы получить определенное количество полимера, существенно свободного от концевых -COF групп, что позволяет получить комбинацию с указанными выше свойствами. Например, полимер, полученный при такой полимеризации части исходного материала, проведенной в отсутствие мономеров, дающих концевые -COF группы, должен составлять, по меньшей мере, 5-10% по массе, преимущественно 20-40% по массе, более преимущественно 50% по массе в отношении окончательной массы полимера. В альтернативном процессе полимеры по данному изобретению, существенно свободные от концевых -COF групп, смешиваются с полимерами, содержащими концевые -COF группы в указанных выше отношениях.
Фторэластомеры, содержащие концевые -COF группы в количестве, более 0.05 ммоль/кг, содержат сомономеры, выбранные из следующих соединений:
- перфтордиоксолы, преимущественно имеющие следующую формулу:
где Y=F, ORf1, Rf1, являющийся C1-C5 перфторалкилом, преимущественно Rf1=CF3;
X1 и Х2, одинаковые или отличающиеся друг от друга, выбираются из F и CF3, преимущественно F;
Z1 выбирается из F, Cl, преимущественно F;
- перфторалкилвиниловые эфиры формулы CF2=CFORf, где Rf является С3 перфторалкилом;
- CF2=CFOXa перфтороксиалкилвиниловые эфиры, где Ха является С3-С12 перфтороксиалкилом, имеющим одну или более эфирных групп, например перфтор-2-пропоксипропил;
- перфторвиниловые эфиры (MOVE) общей формулы , где RAI - С2-С6 линейная, разветвленная или C5-C6 циклическая перфторалкильная группа или С2-С6 линейная или разветвленная, когда это возможно, перфторалкильная группа, содержащая от одного до трех атомов кислорода; когда RAI является фторалкилом или фтороксиалкилом, как определяется выше, он может содержать от 1 до 2 атомов, одинаковых или различных, выбранных из Н, Cl, Br, I; XAI=F; соединения общей формулы: , где YAI=F, OCF3; XAI преимущественно как указан выше, в частности (MOVE 1) и (MOVE 2) .
Отверждаемые фторэластомеры в соответствии с данным изобретением преимущественно содержат следующие мономеры (в молярных процентах):
A) от 1% до 99%, преимущественно от 5% до 99%, мономера формулы:
B) один или более перфорированных сомономеров, имеющих, по меньшей мере, одну ненасыщенность этиленового типа, от 1% до 99%, преимущественно от 1 до 95%;
указанные один или более сомономеров содержат VDF (VDF) в количестве от 1% до 85% по отношению к полной молярной массе мономеров для того, чтобы полимер был фторэластомерным; сумма молярных процентов мономеров равна 100%; количество концевых -COF групп является таким, как указано выше.
Когда полимер не содержит других мономеров В), кроме VDF, количество мономера формулы (а) должно быть не менее 15% молярных для того, чтобы получать фторэластомерные полимеры.
Указанные фторэластомеры преимущественно содержат один бис-олефин.
Более точно количество концевых -COF групп в полимере определяется с использованием ФТ-ИК прибора Nicolet® Nexus (256 сканирований, разрешение 2 см-1).
Эластомерные полимеры в соответствии с данным изобретением представляют собой полимеры, которые при использовании DSC (дифференциальная сканирующая калориметрия) не показывают пиков плавления, так как кристаллическая часть существенно отсутствует.
Когда кроме VDF присутствуют другие сомономеры (В), они выбираются из следующих соединений:
- С2-С8 перфторолефины, например TFE, гексафторпропен, гексафторизобутен;
- перфторалкилвиниловые эфиры формулы CF2=CFORf, где Rf является C1-C2 перфторалкилом, преимуществонно Rf=CF3.
Тетрафторэтилен (TFE) и/или перфторметилвиниловый эфир (MVE) являются преимущественными сомономерами В).
Преимущественными композициями (в молярных %) являются следующие, причем сумма молярных процентов мономеров равна 100%; более преимущественно указанные композиции содержат бис-олефин:
мономер формулы (а): 15-40%, VDF: 60-85%; преимущественно мономер формулы (а): 15-40% VDF: 60-85%, бис-олефин формулы (b): 0.01%-1%;
мономер формулы (а): 15-40%, VDF: 60-85%; TFE: 5-40%; преимущественно мономер формулы (а): 15-40%, VDF: 60-85%; TFE: 5-40%, бис-олефин формулы (b): 0.01%-1%;
мономер формулы (а): 5-40%, MVE: 5-30%; VDF: 50-85%; преимущественно мономер формулы (а): 5-40%, MVE: 5-30%; VDF: 50-85%; бис-олефин формулы (b): 0.01%-1%;
мономер формулы (а): 5-40%, MVE: 5-30%, VDF: 50-85%; TFE: 5-40%; преимущественно мономер формулы (а): 5-40%, MVE: 5-30%, VDF: 50-85%; TFE: 5-40%, бис-олефин формулы (b): 0.01%-1%;
мономер формулы (а): 40-99%; VDF: 1-60%; преимущественно мономер формулы (а): 40-99%, VDF: 1-60%; бис-олефин формулы (b): 0.01%-1%;
мономер формулы (а): 40-99%, MVE: 0-30%, VDF: 1-60%; преимущественно мономер формулы (а): 40-99%, MVE: 0-30%, VDF: 1-60%; бис-олефин формулы (b): 0.01%-1%;
мономер формулы (а): 40-99%, MVE: 0-30%, VDF: 1-60%; TFE: 5-40%; преимущественно мономер формулы (а): 40-99%, MVE: 0-30%, VDF: 1-60%; TFE: 5-40%; бис-олефин формулы (b): 0.01%-1%.
Как уже было сказано, фторэластомеры по данному изобретению имеют улучшенную комбинацию указанных выше свойств.
Фторэластомеры по данному изобретению показывают высокую эластичность при низких температурах, как, например, определяется значениями TR10 и TR70 (ASTM D 1329).
Фторэластомеры по данному изобретению по сравнению с фторэластомерами, известными в уровне техники, имеют Tg ниже -35°С, при сравнении, проводящемся с известными фторэластомерами, имеющими такую же Tg, показывают улучшенные механические свойства и остаточную деформацию при сжатии и более высокую устойчивость при высоких температурах. При сравнении, проведенном с фторэластомерами, основанными на перфторметилвиниловых эфирах, представляющими наиболее широко продающиеся фторэластомеры для использования при низких температурах, фторэластомеры по данному изобретению показали более низкую Tg и улучшенные свойства при низких температурах, что подтверждается значениями TR.
Заявитель обнаружил, что фторэластомеры по данному изобретению получаются с высокой полимеризационной кинетикой, и потому возможно получать гомополимеры и сополимеры, имеющие большую молекулярную массу. Фторэластомеры по данному изобретению могут производится с большим выходом, и потому извлечение непрореагировавших мономеров в конце полимеризации не имеет смысла. Это позволяет упростить конструкцию производящей установки, т.к. нет необходимости применять дорогие способы извлечения непрореагировавших мономеров.
Получение фторэластомеров по данному изобретению осуществляется полимеризацией мономеров в водной эмульсии в присутствии эмульсии, дисперсии или микроэмульсии перфторполиоксиалкиленов в соответствии с патентами US 4789717 и US 4864006. Преимущественно синтез проводится в присутствии микроэмульсии перфторполиоксиалкиленов.
В соответствии с хорошо известными в уровне техники способами используются радикалы-инициаторы, например персульфаты, перфосфаты, пербораты или перкарбонаты щелочи или аммония, необязательно в комбинации с солями железа, меди или серебра или других легко окисляющихся металлов. В реакционной среде необязательно также присутствуют поверхностно-активные вещества различных типов, среди которых особым преимуществом обладают фторированные поверхностно-активные вещества формулы:
где R3 f - цепь C5-C16 (пер)фторалкила или (пер)фторполиоксиалкила, Xk - представляет - СОСТ- или -SO3 -, M+ выбирается из Н+, NH4 + или иона щелочного металла. Среди наиболее обычно применяемых мы можем привести перфтороктаноат аммония, (пер)фторполиоксиалкилены, заканчивающиеся одной или более карбоксильными группами, и т.п. См. патенты US 4990283 и US 4864006.
Реакция полимеризации обычно проводится при температурах между 25°С и 150°С и при давлении между атмосферным и до 10 МПа.
В замену или в комбинации с цепными трансферными агентами, содержащими йод и/или бром, могут использоваться другие цепные трансферные агенты, известные из уровня техники, такие как этилацетат, диэтилмалонат, этан и т.п.
Как сообщалось ранее, фторэластомеры по данному изобретению отверждаются пероксидным или ионным путем.
При пероксидном отверждении преимущественно фторэластомер содержит в цепи и/или в концевой позиции макромолекулу йода и/или атомы брома.
К отверждающей смеси добавляются следующие компоненты:
- пероксиды, способные выделять радикалы при нагревании, например диалкилпероксиды, в частности дитербутилпероксид и 2,5-диметил1-2,5-ди(тербутилперокси)гексан; диалкиларилпероксиды, как, например, дикумилпероксид; дибензоилпероксид; дитербутилпербензоат; ди[1,3-диметил-3-(тербутилперокси)бутил]карбонат. Другие пероксидные системы описаны, например, в Европейских патентных заявках ЕР 136596 и ЕР 410351.
Количество пероксида обычно составляет от 0.5% до 10% по массе в отношении к массе полимера, преимущественно 0.6%-4% по массе;
- отверждающие соагенты, применяющиеся обычно в количестве между 0.5 и 10%, преимущественно между 1 и 7% по массе в отношении к массе полимера; среди них обычно используются бис-олефины формулы (I); триаллилцианурат, триаллилизоцианурат (TAIC), трис-(диалиламин)-s-триазин; триаллилфосфит; N,N-диаллилакриламид; N,N,N′,N′-тетраллилмалонамид; тривинилизоцианурат; 4,6-тривинилметилтрисилоксан и т.п.; особенно преимущественны TAIC и бис-олефин формулы:
CH2=CH-(CF2)6-СН=СН2;
необязательно
- соединение металла в количестве от 1 до 15%, преимущественно от 2 до 10% по массе в отношении к массе полимера, которое выбирается из оксидов или гидроксидов двухвалентных металлов, например, Mg, Zn, Са или Pb, необязательно комбинируется с солью слабой кислоты, как стеараты, бензоаты, карбонаты, оксалаты или фосфиты Ва, Na, K, Pb, Са;
- другие обычные добавки, как минеральные наполнители, полукристаллические фторполимеры в порошке, пигменты, антиоксиданты, стабилизаторы и т.п.
Когда отверждение осуществляется ионным путем, добавляются отверждающие и ускоряющие процесс агенты, известные из уровня техники. В этом случае фторэластомер преимущественно содержит блоки, получаемые из HFP.
Количество ускоряющего агента находится в пределах 0.05-5 ч/100 ч (частей на 100 частей полимера), отверждающего агента в пределах 0.5-15 ч/100 ч, преимущественно 1-6 ч/100 ч.
В качестве отверждающих агентов могут применяться полигидрооксилированные, ароматические или алифатические соединения или их производные, как излагается в патентах ЕР 335705 и US 4233427. Среди них мы, в частности, отмечаем следующие соединения: ди-, три-, тетра-гидроксибензолы, нафталины или антрацены; бисфенолы, у которых два ароматических кольца соединены друг с другом алифатическим, циклоалифатическим или ароматическим бивалентным радикалом или одним атомом кислорода или серы, или также карбонильной группой. Ароматические кольца могут замещаться одним или более атомами хлора, фтора, брома или карбонилами, алкилами, ацилами. В частности, преимущественным является бисфенол AF.
Ускоряющими агентами могут быть, например, четвертичные аммониевые или фосфоновые соли (см., например, ЕР 335705 и US 3876654); аминофосфоновые соли (см., например, US 4259463); фосфораны (см., например, US 3752787); иминовые соединения, описанные в ЕР 182299 и ЕР 120462 и т.д.
Преимущественными являются четвертичные фосфоновые соли и аминофосфоновые соли.
Взамен использования ускоряющего и отверждающего агентов можно использовать от 1 до 5 ч/100 ч (преимущественно 2-4.5) объединенного продукта ускоряющего агента и отверждающего агента в молярном отношении 1:2-1:5, преимущественно 1:3-1:5, причем ускоряющий агент является одним из ониум-органических соединений, имеющих положительный заряд, как указано выше, отверждающий агент, выбирающийся из упомянутых выше соединений, в частности ди- или полигидроксил или ди- или политиол; объединенный продукт получается плавлением реакционного продукта с ускоряющим агентом и отверждающим продуктом в указанном молярном отношении или плавлением смеси объединенного продукта 1:1 с добавлением отверждающего агента в указанных количествах. Необязательно ускоряющий агент может присутствовать в избытке по отношению к тому количеству, которое содержится в объединенном продукте, обычно от 0.05 до 0.5 ч/100 ч.
Для получения объединенного продукта особенно преимущественными являются катионы: 1,1-дифенил-1-бензил-N-диэтилфосфоранамин и тетрабутилфосфониум; из анионов: бисфенольные соединения, где два ароматических кольца соединены двухвалентным радикалом