Способ формирования группы риска опухолевой патологии молочной железы
Иллюстрации
Показать всеИзобретение относится к области медицины в частности к способу формирования группы риска опухолевой патологии молочной железы (ОП МЖ). Способ формирования группы риска ОП МЖ путем подготовки пробы мочи к анализу, качественного и количественного определения в моче следующих нуклеозидов: ксантозина, 2-дезоксиуридина, 5-метилцитидина, расчет прогнозирующей функции, и оценку вероятности наличия ОП МЖ. 9 з.п. ф-лы, 3 ил., 1 табл.
Реферат
Изобретение относится к медицине, в частности к способам исследования или анализа биологических материалов, а именно мочи, и может быть использовано для выявления патологии молочной железы (далее - МЖ) и формирования группы риска больных, в том числе опухолевыми заболеваниями МЖ.
Чрезвычайная актуальность проблемы диагностики раковых заболеваний на ранних стадиях развития болезни ни у кого не вызывает сомнений. В последнее время в литературе встречается большое количество работ, в которых показана принципиальная возможность использования ряда измененных и неизмененных нуклеозидов, присутствующих в моче, в качестве маркеров для ранней диагностики и контроля протекания онкологических заболеваний. Однако ни в одной из работ не представлен полный законченный цикл исследований, касающийся, в частности, диагностики рака МЖ, достоверно подтверждающих такую возможность и алгоритм проведения диагностического исследования.
Наиболее близким к заявляемому изобретению по способу и назначению является способ определения повреждений ДНК (US 20060105384 A1, 18.05.2006, Detection of DNA damage), с помощью которого можно предположить о вероятности риска развития раковых заболеваний. Известный способ включает сбор и анализ внутриклеточных и внеклеточных материалов, их анализ на предмет высоких уровней свободных нуклеотидов и нуклеозидов, причем внеклеточный материал может являться мочой. Принят в качестве прототипа. Однако в известном способе-прототипе показано, что высокий уровень свободных нуклеотидов и нуклеозидов в моче является индикатором целого ряда заболеваний, в том числе раковых. В связи с этим способ-прототип не может быть использован как диагностический аппарат для выполнения специфической задачи - диагностики патологии МЖ. Кроме того, в способе-прототипе отсутствует математический аппарат интерпретации полученных результатов, позволяющий оценить степень вероятности наличия опухолевой патологии (далее - ОП).
Заявляемое изобретение направлено на решение задачи выявления совокупности признаков, позволяющих провести диагностику и сделать вывод о возможном наличии или отсутствии у пациентки ОП МЖ и необходимости проведения инструментального обследования.
Использование в клинической практике заявляемого способа позволяет достичь нескольких технических результатов:
- возможность оценки вероятности наличия патологии МЖ, в том числе опухолевого заболевания, путем качественного и количественного определения содержания нуклеозидов в пробе мочи;
- возможность обследования широкого круга лиц в доклинических условиях неинвазивным методом в форме доставки проб мочи в замороженном виде к месту расположения исследовательских центров, обладающих необходимой аппаратурой;
- повышение точности качественного и количественного определения содержания нуклеозидов в пробе мочи за счет усовершенствования технологии пробоподготовки и метода высокоэффективной жидкостной хроматографии;
- простота и доступность клиницистам математического аппарата обсчета результатов количественного определения содержания нуклеозидов в пробе мочи для отнесения каждой конкретной пациентки к определенной группе риска.
Указанные технические и лечебные результаты при осуществлении изобретения достигаются за счет того, что так же, как в известном способе, наличие ОП МЖ определяют с помощью сбора внеклеточного материала и его анализа на предмет высоких уровней свободных нуклеозидов, причем внеклеточный материал является мочой.
Особенность заявляемого способа заключается в том, что формирование группы риска ОП МЖ включает стадию качественного и количественного определения в моче следующих нуклеозидов: ксантозин (X1), 2-дезоксиуридин (Х2), 5-метилцитидин (Х3) и стадию оценки вероятности наличия ОП МЖ, при этом подготовку пробы мочи к анализу осуществляют путем проведения высокоселективной твердофазной экстракции, идентификацию нуклеозидов и количественное определение содержания нуклеозидов проводят методом высокоэффективной жидкостной хроматографии на гидрофильной колонке с градиентным элюированием с масс-спектрометрическим детектированием, оценку вероятности наличия ОП МЖ рассчитывают путем определения значения прогнозирующей функции F по формуле: F=f1(X1)+f2(Х2)+f3(Х3)+22,45, где:
- Xn - площадь хроматографического пика соответствующего нуклеозида на масс-хроматограмме в пробе мочи;
- fn - идентификационная функция;
- F - прогнозирующая функция.
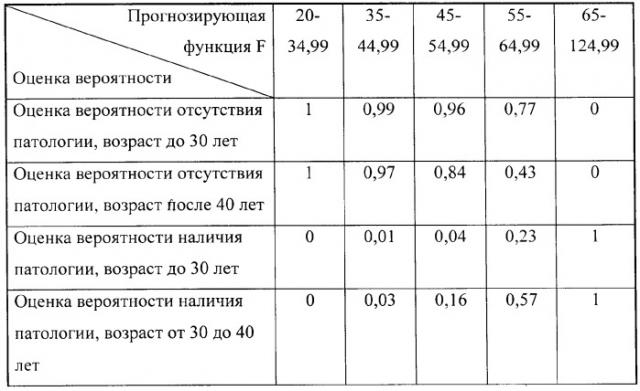
Формирование групп риска осуществляют следующим образом: при значении прогнозирующей функции F менее 34,99 независимо от возраста пациентки наличие ОП МЖ маловероятно и проведение инструментальных исследований не показано, при значении прогнозирующей функции F от 35 до 44,99 оценка вероятности ОП МЖ при возрасте до 30 лет составляет 0,01, а при возрасте более 40 лет - 0,03 и проведение инструментальных исследований показано, при значении прогнозирующей функции F от 45 до 54,99 оценка вероятности ОП МЖ при возрасте до 30 лет составляет 0,04, а при возрасте более 40 лет - 0,16 и проведение инструментальных исследований показано, при значении прогнозирующей функции F от 55 до 64,99 оценка вероятности ОП МЖ при возрасте до 30 лет составляет 0,23, а при возрасте более 40 лет - 0,57 и проведение инструментальных исследований показано, при значении прогнозирующей функции F более 65 оценка вероятности ОП МЖ при любом возрасте составляет 1 и проведение инструментальных исследований является обязательным.
При этом на стадии подготовки пробы мочи к анализу высокоселективную твердофазную экстракцию осуществляют с использованием сорбента с привитыми фенилборонатными группами с помощью системы стабилизированной подачи растворов реагентов с постоянным объемным расходом. Система стабилизированной подачи растворов реагентов с постоянным объемным расходом снабжена полуавтоматическим устройством на основе шприцевого насоса.
Качественное и количественное определение содержания нуклеозидов в пробе мочи методом высокоэффективной жидкостной хроматографии осуществляют на гидрофильной колонке с градиентным элюированием с масс-спектрометрическим детектированием, сорбентом в которой является силикагель с привитыми углеводородными цепями, дополнительно содержащими гидрофильные функциональные группы.
Идентификацию каждого из выбранных нуклеозидов осуществляют в режиме селективного детектирования по времени хроматографического удерживания и масс-спектрометрическим характеристикам: интенсивностям сигналов по двум выделенным ионам для каждого соединения и отношения интенсивностей сигналов в точке максимума хроматографического пика для нуклеозидов, регистрируемых по двум ионам. Определение количества каждого из выбранных нуклеозидов осуществляют путем измерения площади хроматографического пика соответствующего нуклеозида.
Идентификационная функция f1 для нуклеозида ксантозин имеет следующее значение:
- f1=0 при 0<X1≤8971,3;
- f1=(X1-8971,3)-0,0017525 при 8971,3<X1≤27435,4;
- f1=32,359 при 27435,4<X1.
Идентификационная функция f2 для нуклеозида 2-дезоксиуридин имеет следующее значение:
- f2=0 при 0<X2≤1313,3;
- f2=(X2-1313,3)-0,0357 при 1313,3<X2≤1989,1;
- f2=24,093 при 1989,1<X2.
Идентификационная функция f3 для нуклеозида 5-метилцитидин имеет следующее значение:
- f3=0 при 0<Х3≤94243,8;
- f3=(Х3-94243,8)-0,00000929 при 94243,8<Х3≤39998103,5;
- f3=36,279 при 39998103,5<Х3.
Сущность изобретения заключается в следующем.
В результате проведенных исследований авторами изобретения установлено, что наиболее информативным для оценки риска наличия у пациентки ОП МЖ является количественное содержание в пробе мочи следующих нуклеозидов: ксантозина, 2-дезоксиуридина, 5-метилцитидина. Установлено также, что вероятность наличия ОП МЖ согласуется с тенденцией увеличения количественного содержания в моче указанных нуклеозидов, а именно: монотонно возрастает (точнее, не убывает) при увеличении количества каждого из них.
Авторами изобретения разработана методика оценки вероятности наличия ОП МЖ путем определения значения прогнозирующей функции F по формуле: F=f1(X1)+f2(X2)+f3(Х3)+22.45, где:
- Xn - площадь хроматографического пика соответствующего нуклеозида в пробе мочи;
- fn - идентификационная функция;
- F - прогнозирующая функция.
Авторами также установлено, что при значении прогнозирующей функции F менее 34,99 независимо от возраста пациента наличие ОП МЖ маловероятно и проведение инструментальных исследований не показано. При значении прогнозирующей функции F от 35 до 44.99 оценка вероятности ОП МЖ при возрасте до 30 лет составляет 0,01, а при возрасте более 40 лет - 0,03. При значении прогнозирующей функции F от 45 до 54.99 оценка вероятности ОП МЖ при возрасте до 30 лет составляет 0,04, а при возрасте более 40 лет - 0,16. При значении прогнозирующей функции F от 55 до 64.99 оценка вероятности ОП МЖ при возрасте до 30 лет составляет 0,23, а при возрасте более 40 лет - 0,57. В этих случаях целесообразно проведение инструментальных исследований. При значении прогнозирующей функции F более 65 оценка вероятности ОП МЖ в любом возрасте составляет 1 и проведение инструментальных исследований является обязательным.
Представленные закономерности обнаружены на основании достоверного обследования пациенток в возрасте от 16 до 72 лет, представленных тремя группами:
- контрольная группа - практически здоровые женщины (отсутствие патологии МЖ),
- женщины с верифицированной мастопатией и фиброаденомой (отсутствие злокачественных новообразований МЖ),
- женщины с диагностированным раком МЖ: опухоли в стадиях рака in situ (базальная мембрана не имеет повреждений), Т 1 (размер опухоли до 2 см) и Т 2 (размер опухоли от 2 до 5 см).
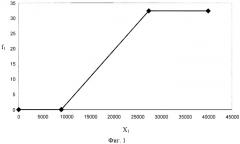
Зависимости величины указанных идентификационных функций (fn) от количественного содержания соответствующего нуклеозида в пробе мочи (Хn) (площади хроматографического пика) проиллюстрированы следующими графиками:
- фиг.1 - Значение идентификационной функции f1 для нуклеозида ксантозин в зависимости от площади хроматографического пика X1,
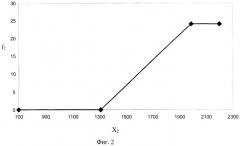
- фиг.2 - Значение идентификационной функции f2 для нуклеозида 2-дезоксиуридин в зависимости от площади хроматографического пика Х2,
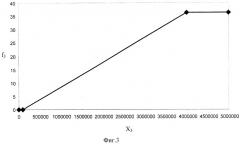
- фиг.3 - Значение идентификационной функции f3 для нуклеозида 5-метилцитидин в зависимости от площади хроматографического пика Х2.
Оценку вероятности наличия или отсутствия заболевания с учетом возраста пациентки осуществляют с помощью таблицы 1.
При проведении качественного и количественного анализа нуклеозидов в литературе рекомендуется использовать наиболее широко распространенные хроматографические колонки, сорбентом в которых является силикагель с привитыми углеводородными радикалами. Однако, как показал опыт, такие колонки малоэффективны для разделения гидрофильных соединений одного класса в силу ряда недостатков:
- недостаточная селективность при анализе сложных систем, содержащих большое количество компонентов одного класса с близкими физико-химическими свойствами,
- недостаточная химическая устойчивость сорбента при работе с подвижными фазами, содержащими большое количество воды, приводящая к нестабильным временам удерживания определяемых соединений.
Авторами изобретения усовершенствована методика подготовки пробы мочи к хромато-масс-спектрометрическому анализу. Пробоподготовка включает получение конечного экстракта нуклеозидов путем проведения высокоселективной твердофазной экстракции на концентрирующем полимерном патроне. Для извлечения нуклеозидов из мочи используют сорбент Affi-gel 601® с привитыми фенилборонатными группами. Для равномерной подачи используют систему стабилизированной подачи растворов реагентов с постоянным объемным расходом с использованием полуавтоматического устройства на основе шприцевого насоса.
Для повышения точности качественного и количественного определения широкого спектра нуклеозидов путем хроматографического анализа проб мочи была использована колонка, в которой сорбентом является силикагель с привитыми углеводородными цепями, дополнительно содержащими гидрофильные функциональные группы. В качестве такой колонки оптимальной была выбрана Synergi Polar RP 250×2 мм. Использование хроматографической колонки с указанным сорбентом позволяет работать с подвижными фазами, содержащими большое количество воды. В ходе работы установлено, что ее селективность по отношению к исследуемым нуклеозидам выше, чем селективность хроматографических колонок, в которых сорбентом является силикагель с привитыми углеводородными радикалами. Это позволило проводить разделение нуклеозидов за меньший промежуток времени. Также ввиду химической устойчивости неподвижной фазы к действию подвижных фаз с большим содержанием воды метрологические характеристики для данной хроматографической колонки такие, как дрейф времен удерживания, дрейф коэффициентов селективности, лучше, чем для колонок, в которых сорбентом является силикагель с привитыми углеводородными радикалами. В частности, при использовании колонки Synergi Polar RP 250×2 мм наблюдалось уменьшение дрейфа времени выхода исследуемых нуклеозидов в 3-4 раза.
Способ осуществляют следующим образом.
1. Получение образцов мочи: произвольно собранную порцию мочи как можно раньше после ее получения и доставки в лабораторию охлаждают при 4-7°С максимум 24 часа и затем глубоко замораживают при -20°С. До замораживания в моче проводят определение концентрации креатинина (мкмоль/л) по методу Яффе тест-наборами фирмы «R
oche» на автоматическом биохимическом анализаторе «Hitachi-902». Кроме того, определяют содержание белка, нитритов и лейкоцитов при помощи тестовой полоски для мочи (Combi-Screen).
2. Идентификацию ксантозина (X1), 2-дезоксиуридина (Х2), 5-метилцитидина (Х3) выполняют по времени удерживания, являющемуся качественной характеристикой, с помощью диодно-матричного спектрофотометрического детектора, и масс-спектрометрическим данным.
3. Конечный экстракт нуклеозидов получают путем высокоселективного выделения с использованием фенилборонатного геля, полуавтоматического устройства на основе шприцевого насоса. Разделение нуклеозидов происходит в хроматографической колонке путем прямого детектирования компонентов с масс-спектрометрическим квадрупольным детектором в режиме сканирования выбранных ионов (SIM), с точностью определения m/z - 0.1 а.е.м. и записи сигнала детектора в цифровом формате.
4. Количественное определение проводят с использованием калибровочных графиков, построенных с использованием метода построения истинных калибровочных на реальной матрице мочи в диапазоне концентраций от 0 до 200 мкг/мл нуклеозида в экстракте пробы после проведения процедуры пробоподготовки.
5. Данные процедуры выполняют на ВЭЖХ системе Agilent 1100 (Agilent, США), оснащенной диодно-матричным детектором, термостатом колонки, градиентным элюированием, автоматической системой ввода пробы или любой другой, обеспечивающей подобные или лучшие характеристики. Сбор и обработку информации о составе анализируемых проб проводят с помощью программного обеспечения Chemstation®.
6. Оценку вероятности наличия патологии МЖ осуществляют следующим образом:
- измеряют площади хроматографических пиков каждого из исследуемых нуклеозидов X1, Х2, Х3;
- в соответствии с изложенной выше методикой вычисляют значение прогнозирующей функции F;
- в соответствии с полученным числовым значением прогнозирующей функции F определяют вероятность наличия ОП МЖ.
Примеры диагностики
1. Пациентка А47, контрольная группа.
Значения площади хроматографических пиков нуклеозидов:
| X1 - ксантозин | 6532,7 |
| Х2 - 2-дезоксиуридин | 0 |
| Х3 - 5-метилцитидин | 699801,3 |
Значения идентификационных функций (fn):
f1(X1=6532,7)=0
f2(X2=0)=0
f3(Х3=699801,3)=(699801,3-94243,8)-0,00000929=5,6
Значение прогнозирующей функции F=f1(X1)+f2(X2)+f3(X3)+22,45=0+0+5,6+22,45=28,1.
При любом возрасте пациентки А47 оценка вероятности ОП равна 0 (т.е. риск заболевания отсутствует).
2. Пациентка А27, мастопатия.
Значения площади хроматографических пиков нуклеозидов:
| X1 - ксантозин | 21360,7 |
| Х2 - 2-дезоксиуридин | 0 |
| Х3 - 5-метилцитидин | 914454,3 |
значения идентификационных функций (fn):
f1(X1=21360,7)=(21360,7-8971,3)-0,0017525=21,7
f2(X2=0)=0
f3(Х3=914454,3)=(914454,3-94243,8)-0,00000929=7,6
Значение прогнозирующей функции F=f1(X1)+f2(X2)+f3(X3)+22,45=21,7+0+7,6+22,45=51,8.
Если возраст пациентки А27 меньше 30 лет, то оценка вероятности ОП составляет 0,04 (т.е. риск заболевания составляет 4%), при возрасте более 40 лет оценка вероятности заболевания 0,16 (риск заболевания 16%).
3. Пациентка В28, фиброаденома.
Значения площади хроматографических пиков нуклеозидов:
| X1 - ксантозин | 2077,7 |
| Х2 - 2-дезоксиуридин | 15287,6 |
| Х3 - 5-метилцитидин | 1475819,6 |
значения идентификационных функций (fn):
f1(X1=2077,7)=0
f2(X2=15287,6)=24,1
f3(Х3=1475819,6)=(1475819,б-94243,8)-0,00000929=12,8
Значение прогнозирующей функции F=f1(X1)+f2(X2)+f3(X3)+22,45=0+24,1+12,8+22,45=59,4.
Если возраст пациентки В28 меньше 30 лет, то оценка вероятности ОП составляет 0,23 (т.е. риск заболевания составляет 23%), при возрасте более 40 лет оценка вероятности заболевания 0,57 (риск заболевания 57%).
4. Пациентка А43, РМЖ 1-я стадия.
Значения площади хроматографических пиков нуклеозидов:
| Х1 - ксантозин | 11979,6 |
| X2 - 2-дезоксиуридин | 4066,1 |
| Х3 - 5-метилцитидин | 1546016,1 |
значения идентификационных функций (fn):
f1(X1=11979,6)=(11979,6-8971,3)·0,0017525=5,3
f2(X2=4066,1)=24,1
f3(Х3=1546016,1)=(1546016,1-94243,8)·0,00000929=13,5
Значение прогнозирующей функции F=f1(X1)+f2(X2)+f3(Х3)+22,45=5,3+24,1+13,5+22,45=65,3.
При любом возрасте пациентки А43 оценка вероятности ОП равна 1 (т.е. риск заболевания составляет 100%).
5. Пациентка А29, РМЖ 2-я стадия.
Значения площади хроматографических пиков нуклеозидов:
| X1 - ксантозин | 31777,8 |
| Х2 - 2-дезоксиуридин | 0 |
| Х3 - 5-метилцитидин | 2153955 |
значения идентификационных функций (fn):
f1(X1=31777,8)=32,4
f2(X2=0)=0
f3(Х3=2153955)=(2153955-94243,8)·0,00000929=19,1
Значение прогнозирующей функции F=f1(X1)+f2(X2)+f3(Х3)+22,45=32,4+0+19,1+22,45=74.
При любом возрасте пациентки А29 оценка вероятности ОП равна 1 (т.е. риск заболевания составляет 100%).
6. Пациентка А36, РМЖ 3-я стадия.
Значения площади хроматографических пиков нуклеозидов:
X1 - ксантозин 29158
X2 - 2-дезоксиуридин 1494,6
Х3 - 5-метилцитидин 2471996,3
значения идентификационных функций (fn):
f1(X1=29158)=32,4
f2(X2=1494,6)=(1494,6-1313,3)·0,0357=6,5
f3(Х3=2471996,3)=(2471996,3-94243,8)·0,00000929=22,1
Значение прогнозирующей функции F=f1(X1)+f2(X2)+f3(Х3)+22,45=32,4+6,5+22,1+22,45=83,4.
При любом возрасте пациентки A36 оценка вероятности ОП равна 1 (т.е. риск заболевания составляет 100%).
Достоверность предлагаемого способа формирования групп риска ОП МЖ подтверждают следующие статистические данные. Контроль выполнен на группе из 106 пациенток: 17 человек - контрольная группа; 16 - группа с мастопатией; 13 - группа с фиброаденомой; 15, 24, 18 и 3 человека - группы с РМЖ в порядке возрастания стадии заболевания от 1 до 4.
Выборка пациенток была разделена на две группы: контрольная группа (17 человек) и группа с заболеваниями (89 человек). При классификации с помощью заявляемого диагностического алгоритма было выявлено 5 ошибок: 1 пациентка из группы с заболеваниями (пациентка имела 2 степень РМЖ) попала в контрольную группу, 4 пациентки из контрольной группы попали в группу с заболеваниями. Уровень ошибок распознавания составляет для контрольной группы 23,5%, а для группы с патологией - 1,1%.
Таким образом, использование совокупности перечисленных существенных признаков позволило усовершенствовать методику высокоэффективной жидкостной хроматографии пробы мочи и сформировать группы с различной вероятностью риска наличия ОП МЖ. Заявляемый способ обладает значительными преимуществами и отвечает критериям патентоспособности.
1. Способ формирования группы риска опухолевой патологии молочной железы (ОП МЖ), характеризующийся тем, что включает стадию качественного и количественного определения в моче следующих нуклеозидов: ксантозина, 2-дезоксиуридина, 5-метилцитидина и стадию оценки вероятности наличия ОП МЖ, при этом подготовку пробы мочи к анализу осуществляют путем проведения высокоселективной твердо-фазной экстракции, идентификацию нуклеозидов и количественное определение содержания нуклеозидов проводят методом высокоэффективной жидкостной хроматографии на гидрофильной колонке с градиентным элюированием с масс-спектрометрическим детектированием, оценку вероятности наличия ОП МЖ рассчитывают путем определения значения прогнозирующей функции F по формуле:F=f1(X1)+f2(X2)+f3(X3)+22,45, гдеХn - площадь хроматографического пика соответствующего нуклеозида на масс-хроматограмме в пробе мочи, X1 - для ксантозина, Х2 - для 2-дезоксиуридина, Х3 - для 5-метилцитидина;fn - идентификационная функция анализируемого нуклеотида, f1 - для ксантозина, f2 - для 2-дезоксиуридина, f3 - для 5-метилцитидина;F - прогнозирующая функция;и при значении прогнозирующей функции F более 34,99 независимо от возраста пациентки формируется группа риска ОП МЖ.
2. Способ по п.1, отличающийся тем, что идентификационная функция f1 для нуклеозида ксантозин имеет следующее значение:f1=0 при 0≤X1≤8971,3;f1=(X1-8971,3)·0,0017525 при 8971,3≤X1≤27435,4;f1=32,359 при 27435,4<Х1.
3. Способ по п.1, отличающийся тем, что идентификационная функция f2 для нуклеозида 2-дезоксиуридин имеет следующее значение:f2=0 при 0≤Х2≤1313,3;f2=(X2-1313,3)·0,0357 при 1313,3<Х2≤1989,1;f2=24,093 при 1989,1<Х2.
4. Способ по п.1, отличающийся тем, что идентификационная функция f3 для нуклеозида 5-метилцитидин имеет следующее значение:f3=0 при 0≤Х3≤94243,8;f3=(X3-94243,8)·0,00000929 при 94243,8<Х3≤39998103,5;f3=36,279 при 39998103,5<Х3.
5. Способ по п.1, отличающийся тем, что высокоселективную твердо-фазную экстракцию осуществляют с использованием сорбента с привитыми фенилборонатными группами.
6. Способ по п.1, отличающийся тем, что высокоселективную твердо-фазную экстракцию осуществляют с помощью системы стабилизированной подачи растворов реагентов с постоянным объемным расходом.
7. Способ по п.6, отличающийся тем, что система стабилизированной подачи растворов реагентов с постоянным объемным расходом снабжена полуавтоматическим устройством на основе шприцевого насоса.
8. Способ по п.1, отличающийся тем, что качественное и количественное определение каждого из выбранных нуклеозидов осуществляют с помощью колонки для жидкостной хроматографии, сорбентом в которой является силикагель с привитыми углеводородными цепями, дополнительно содержащими гидрофильные функциональные группы.
9. Способ по п.1, отличающийся тем, что идентификацию каждого из выбранных нуклеозидов осуществляют в режиме селективного детектирования по времени хроматографического удерживания и масс-спектрометрическим характеристикам: интенсивностям сигналов по двум выделенным ионам для каждого соединения и отношения интенсивностей сигналов в точке максимума хроматографического пика для нуклеозидов, регистрируемых по двум ионам.
10. Способ по п.1, отличающийся тем, что определение количества каждого из выбранных нуклеозидов осуществляют путем измерения площади хроматографического пика соответствующего нуклеозида.