Каталитические композиции и процесс оксихлорирования
Иллюстрации
Показать всеИзобретение относится к каталитическим композициям для оксихлорирования углеводородов. Описана каталитическая композиция для оксихлорирования углеводородов, включающая каталитически эффективное количество катализатора оксихлорирования и разбавитель, включающий частицы алюмосиликата, в которой средний размер частиц катализатора и разбавителя составляет от около 5 микрон до около 300 микрон. Описана каталитическая композиция для оксихлорирования углеводородов, включающая: (а) каталитически эффективное количество катализатора оксихлорирования, имеющего площадь поверхности более чем 25 м2/г, в которой катализатор оксихлорирования включает материал носителя, имеющий распределенную на нем активную солевую композицию; и (b) разбавитель, имеющий площадь поверхности от около 0,1 м2/г до около 25 м2/г, в которой материал носителя и разбавителя являются различающимися химически, и средний размер частиц катализатора и разбавителя составляет от около 5 до около 300 микрон. Также описан способ оксихлорирования углеводорода, включающий стадию контактирования реагентов, включающих углеводород, источник хлора и источник кислорода, с каталитической композицией для оксихлорирования, в условиях способа, с получением хлорированного углеводорода. Также описан способ оксихлорирования углеводорода, включающий стадию контактирования реагентов, включающих углеводород, источник хлора и источник кислорода, с одной из вышеописанной каталитической композицией, включающей каталитически эффективное количество катализатора оксихлорирования и инертный разбавитель, в условиях способа, с получением хлорированного углеводорода, в котором способ проводится при Topt(2) - оптимальной рабочей температуре способа, которая является, по меньшей мере, примерно на 1°С более высокой, чем Topt(1) - оптимальная рабочая температура способа, использующего тот же реактор, те же реагенты, количество загрузки реактора, нормы производительности и катализатор оксихлорирования, но без инертного разбавителя. Технический эффект - достижение более высоких реакционных температур без ущерба для других важных параметров процесса оксихлорирования. 4 н. и 27 з.п. ф-лы, 11 табл., 8 ил.
Реферат
Эта заявка претендует на приоритет Предварительной Патентной Заявки США с серийным номером 60/736524, поданной 14 ноября 2005 года.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение касается каталитических композиций для оксихлорирования, предназначенных для каталитического оксихлорирования углеводородов до хлорированных углеводородов, в особенности композиций, включающих катализатор оксихлорирования и разбавитель, и их применения в процессах оксихлорирования.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Композиции катализаторов оксихлорирования для производства хлорированных углеводородов путем оксихлорирования хорошо зарекомендовали себя в течение многих лет. Оксихлорирование представляет собой реакцию углеводорода, такого как этилен или пропилен, с хлороводородом и кислородом с образованием воды и соответствующих хлорированных углеводородов, таких как 1,2-дихлорэтан (EDC, ДХЭ) или 1,2-дихлорпропан, преимущественно в присутствии катализатора оксихлорирования. Реакция оксихлорирования применяется во всем мире для крупномасштабного промышленного производства. Например, только одно превращение этилена в 1,2-дихлорэтан (ДХЭ) путем оксихлорирования в настоящее время достигает уровня в миллионы тонн ежегодно.
Один конкретный способ оксихлорирования представляет собой парофазную реакцию углеводорода, такого как этилен или пропилен, со смесью хлороводорода (HCl) и источника кислорода (такого как высокоочищенный кислород, получаемый из воздуха на установке для разделения воздуха, где для удаления инертных компонентов применяются абсорбция при переменном давлении или криогенное разделение, или разбавленный поток кислорода, такой как воздух или смесь кислорода и по меньшей мере инертного газа) внутри псевдоожиженного слоя катализатора, включающего катализатор оксихлорирования. Типичный катализатор оксихлорирования может включать соль металла, такую как хлорид меди, и, необязательно, по меньшей мере соль щелочных металлов, щелочноземельных металлов или редкоземельных металлов, нанесенную на или скомбинированную с материалом носителя или инертным носителем, таким как частицы оксида кремния, оксида алюминия, кизельгура, фуллеровой земли, глин и алюмосиликатов (или называемых силикатами алюминия). Для применения в катализе в псевдоожиженном слое материал носителя должен легко переходить в псевдотекучее состояние и иметь должную плотность частиц, устойчивость к истиранию и гранулометрический состав, пригодный для процесса без чрезмерных потерь катализатора из реакционной зоны. Необязательно, каталитическая композиция может включать разбавитель, который включает каталитически и химически инертные частицы, такие как оксид алюминия и оксид кремния, имеющие низкую площадь поверхности.
В оксихлорировании углеводорода (например, этилена) желательно, чтобы каталитическая композиция для оксихлорирования обеспечивала высокий выход желаемого хлорированного продукта (например, 1,2-дихлорэтана, ДХЭ) и малое количество побочных продуктов, таких как диоксид углерода, монооксид углерода и прочие хлорированные материалы. В крупномасштабном промышленном производстве 1,2-дихлорэтана (ДХЭ) небольшое повышение эффективности конверсии этилена в ДХЭ может дать значительную экономию затрат. Далее, повышение эффективности или селективности превращения этилена в ДХЭ может снизить количество образуемых побочных продуктов, связанные с этим расходы для их правильной утилизации и потенциальные опасности для окружающей среды. Селективность превращения этилена в ДХЭ (то есть, селективность превращения этилена) представляет собой число молей чистого 1,2-дихлорэтана (ДХЭ), полученного на 100 молей этилена, израсходованного или превращенного (то есть, конверсия этилена) в ДХЭ, плюс любых побочных продуктов, тогда как эффективность превращения этилена определяется как произведение селективности превращения этилена на конверсию этилена. Подобным же образом, селективность превращения HCl в ДХЭ (то есть, селективность превращения HCl) представляет собой число молей чистого 1,2-дихлорэтана (ДХЭ), полученного на 200 молей HCl, израсходованного или превращенного (то есть, конверсия HCl) в ДХЭ, плюс любых побочных продуктов, тогда как эффективность превращения HCl определяется как произведение селективности превращения HCl на конверсию HCl. Подобным же образом, селективность превращения кислорода в ДХЭ (то есть, селективность превращения кислорода) представляет собой число молей чистого 1,2-дихлорэтана (ДХЭ), полученного на 50 молей кислорода, израсходованного или превращенного (то есть, конверсия кислорода) в ДХЭ, плюс любых побочных продуктов, тогда как эффективность превращения кислорода определяется как произведение селективности превращения кислорода на конверсию кислорода.
Также желательно по экономическим и экологическим причинам, чтобы каталитическая композиция для оксихлорирования обеспечивала высокую конверсию HCl, используемого в реакции. Непрореагировавший HCl нуждается в нейтрализации основанием, а полученная в результате соль должна быть утилизирована. Кроме того, высокие уровни содержания непрореагировавшего HCl в процессе в общем ведут к высокой степени «прорыва» HCl ниже по ходу потока в реактор, что может создать проблемы коррозии. Тем самым является желательным эксплуатировать реактор при оптимальной температуре для обеспечения высокой конверсии HCl. В промышленных вариантах применения наиболее желательной является комбинация высокой конверсии HCl и высокой эффективности превращения этилена или селективности превращения этилена в 1,2-дихлорэтан (ДХЭ).
Далее, является желательным повысить оптимальную рабочую температуру катализатора оксихлорирования без ущерба производительности катализатора, поскольку наиболее экономически выгодным путем было бы повышение производительности существующего реактора для оксихлорирования. В общем повышение рабочих температур увеличивает разность температур между псевдоожиженным слоем катализатора и барабаном парового котла, который используется для утилизации теплоты реакции и поддержания контролируемой температуры. Поэтому повышение рабочей температуры может увеличить силу тяги для выведения теплоты и обеспечения роста производительности реактора. Оптимальная рабочая температура для катализатора в реакторах, где большая часть продуваемого газа возвращается обратно в реактор путем рециркуляции, представляет собой точку, где конверсия HCl и селективность превращения этилена являются оптимизированными. Для однопроходных реакторов с воздушным питанием оптимальная рабочая температура представляет собой точку, где оптимизированы конверсия HCl и эффективность превращения этилена. Например, для реактора, ограниченного давлением в барабане парового котла на уровне 211 psig (то есть, 1455 кПа) и/или температурой 200°С, повышение оптимальной рабочей температуры каталитической композиции для оксихлорирования от 230°С до 240°С имело бы результатом рост производственной мощности этого реактора на 33%. Поэтому всегда есть потребность в каталитических композициях для оксихлорирования, которые могут работать при более высоких оптимальных рабочих температурах, тем самым обеспечивая эффективный путь повышения производственной мощности существующего реактора оксихлорирования.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Здесь раскрываются каталитические композиции для оксихлорирования, которые могут повысить оптимальную рабочую температуру процессов оксихлорирования без ущерба эффективности катализатора.
В одном аспекте, каталитические композиции для оксихлорирования включают каталитически эффективное количество катализатора оксихлорирования и разбавителя, включающего частицы алюмосиликата.
В еще одном аспекте каталитические композиции для оксихлорирования включают:
(а) каталитически эффективное количество катализатора оксихлорирования, имеющего площадь поверхности более чем 25 м2/г, где катализатор оксихлорирования включает материал носителя, имеющий распределенную на нем активную солевую композицию; и
(b) разбавитель, имеющий площадь поверхности от около 0,1 м2/г до около 25 м2/г, в которых материал носителя и разбавитель являются различающимися химически, и средний размер частиц катализатора и разбавителя варьирует от около 5 до около 300 микронами.
Здесь раскрываются также способы оксихлорирования с использованием каталитических композиций для повышения оптимальной рабочей температуры процессов оксихлорирования без ущерба эффективности катализатора.
В одном аспекте способы оксихлорирования включают стадию контактирования реагентов, включающих углеводород, источник хлора и источник кислорода, с каталитической композицией для оксихлорирования в условиях процесса для получения хлорированного углеводорода. В некоторых вариантах осуществления каталитическая композиция для оксихлорирования включает каталитически эффективное количество катализатора оксихлорирования и разбавитель, включающий частицы алюмосиликата. В других вариантах исполнения каталитическая композиция для оксихлорирования включает (а) каталитически эффективное количество катализатора оксихлорирования, имеющего площадь поверхности более чем 25 м2/г, где катализатор оксихлорирования включает материал носителя, имеющий распределенную на нем активную солевую композицию; и (b) разбавитель, имеющий площадь поверхности от около 0,1 м2/г до около 25 м2/г, в которой материал носителя и разбавитель являются различающимися химически, и средний размер частиц катализатора и разбавителя варьирует от около 5 до около 300 микронами.
В еще одном аспекте способы оксихлорирования включают стадию контактирования реагентов, включающих углеводород, источник хлора и источник кислорода, с каталитической композицией для оксихлорирования, включающей каталитически эффективное количество катализатора оксихлорирования и инертный разбавитель, в условиях способа получения хлорированного углеводорода, в котором процесс протекает при оптимальной рабочей температуре процесса Topt(2), которая по меньшей мере примерно на 1°С выше, чем оптимальная рабочая температура способа Topt(1), в котором используют тот же реактор, те же реагенты, нормы производительности и катализатор оксихлорирования, но без инертного разбавителя. В некоторых вариантах осуществления процессы оксихлорирования проводятся при наиболее экономически выгодных условиях процесса.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
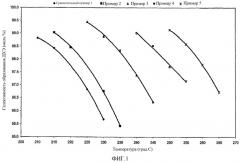
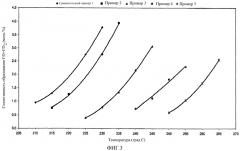
Фиг.1 изображает селективность образования 1,2-дихлорэтана (ДХЭ) как функцию температуры и каталитической композиции в раскрытых здесь Примерах 1-5.
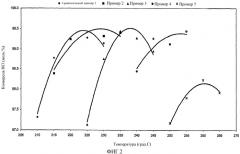
Фиг.2 изображает конверсию HCl как функцию температуры и каталитической композиции в раскрытых здесь Примерах 1-5.
Фиг.3 изображает селективность образования оксида углерода как функцию реакционной температуры и каталитической композиции в раскрытых здесь Примерах 1-5.
Фиг.4 изображает селективность образования 1,1,2-трихлорэтана как функцию реакционной температуры и каталитической композиции в раскрытых здесь Примерах 1-5.
Фиг.5 изображает селективность образования 1,2-дихлорэтана (ДХЭ) как функцию температуры и каталитической композиции в раскрытых здесь Примерах 6-9.
Фиг.6 изображает конверсию HCl как функцию температуры и каталитической композиции в раскрытых здесь Примерах 6-9.
Фиг.7 изображает селективность образования оксида углерода как функцию реакционной температуры и каталитической композиции в раскрытых здесь Примерах 6-9.
Фиг.8 изображает селективность образования 1,1,2-трихлорэтана как функцию реакционной температуры и каталитической композиции в раскрытых здесь Примерах 6-9.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В нижеследующем описании все числа, здесь раскрытые, являются приближенными значениями, независимо от того, применяется ли в связи с ними слово «около» или «приблизительно». Они могут варьировать на 1 процент, 2 процента, 5 процентов или, иногда, 10 и 20 процентов. Всякий раз, когда раскрывается численный диапазон с нижним пределом, RL, и верхним пределом, RU, любое число, попадающее в пределы диапазона, является конкретно представленным. В частности, следующие числа внутри диапазона являются конкретно представленными: R=RL+k·(RU-RL), где индекс k представляет собой переменную величину, варьирующую от 1 процента до 100 процентов с однопроцентным приростом, то есть индекс k представляет собой 1 процент, 2 процента, 3 процента, 4 процента, 5 процентов,……, 50 процентов, 51 процент, 52 процента,……, 95 процентов, 96 процентов, 97 процентов, 98 процентов, 99 процентов или 100 процентов. Более того, любой численный интервал, определяемый двумя числами R, как определяемыми выше, также конкретно представлен.
Это изобретение представляет каталитическую композицию для оксихлорирования, включающую каталитически эффективное количество катализатора оксихлорирования и разбавитель, такой как алюмосиликаты (также известные как силикаты алюминия или алюминийсиликаты), стеклянные бусинки, оксид кремния, баллотини (мелкие стеклянные частицы для светоотражающих красок), оксид алюминия, графит или карбид кремния. Каталитическая композиция для оксихлорирования может обеспечивать более высокую оптимальную рабочую температуру без ущерба преимущественным параметрам производительности, присущим неразбавленному катализатору оксихлорирования, таким как высокая селективность образования 1,2-дихлорэтана (ДХЭ), высокая чистота продукта, высокая конверсия HCl и прекрасная текучесть. Как он здесь применяется, термин «каталитически эффективное количество» предполагается означающим любое количество, которое является эффективным в обеспечении повышения производительности образования ДХЭ в реакторе для оксихлорирования по меньшей мере на 1%, предпочтительно по меньшей мере на 10%, более предпочтительно по меньшей мере на 30%, и наиболее предпочтительно по меньшей мере на 50%.
В некоторых вариантах осуществления каталитическая композиция для оксихлорирования включает от около 10 до около 90 процентов по весу катализатора оксихлорирования и от около 90 до около 10 процентов по весу разбавителя. В других вариантах исполнения каталитическая композиция для оксихлорирования включает от около 20 до около 80 процентов по весу катализатора оксихлорирования и от около 80 до около 20 процентов по весу разбавителя. В дальнейших вариантах осуществления каталитическая композиция для оксихлорирования включает от около 30 до около 70 процентов по весу катализатора оксихлорирования и от около 70 до около 30 процентов по весу разбавителя. В особенных вариантах исполнения каталитическая композиция для оксихлорирования включает от около 60 до около 40 процентов по весу катализатора оксихлорирования и от около 60 до около 40 процентов по весу разбавителя.
Некоторые каталитические композиции для оксихлорирования, описываемые здесь, могут быть охарактеризованы селективностью превращения этилена в ДХЭ, составляющей по меньшей мере 96% при температуре 230°С. Другие каталитические композиции для оксихлорирования могут быть охарактеризованы селективностью превращения этилена в ДХЭ, составляющей по меньшей мере 97% при температуре 240°С. Некоторые каталитические композиции для оксихлорирования могут быть охарактеризованы по существу той же или более высокой селективностью превращения этилена в ДХЭ, конверсией HCl и/или более высокими рабочими температурами, чем сравнительный катализатор оксихлорирования без разбавителя, имеющий площадь поверхности менее чем 25 м2/г.
Катализатор оксихлорирования может быть любым катализатором оксихлорирования, известным любому специалисту в этой области технологии. Он может быть также приготовлен любым способом, известным любому специалисту в этой области технологии. Катализатор оксихлорирования может содержать активную солевую композицию, включающую соль меди, такую как хлорид меди, распределенную, нанесенную в виде покрытия, в виде осадка (отложения) или нанесенную на материал носителя. Активная солевая композиция может также содержать активный оксид металла или соль металла, которая является соосажденной вместе с носителем. Альтернативно, активная солевая композиция может быть не нанесенной, а сплавленной с расплавленной солью. В некоторых вариантах осуществления активная солевая композиция дополнительно содержит по меньшей мере одну соль металла или оксид, производные от металла, выбираемого из группы, составленной из щелочных металлов, щелочноземельных металлов (то есть, металлов Группы IIA), редкоземельных металлов и их комбинаций. Анион соли металла может быть любым анионом, известным в технологии, таким как хлорид, бромид, иодид, нитрат, бикарбонат, карбонат и карбоксилаты (например, формиат и ацетат). В некоторых вариантах осуществления активная солевая композиция включает соль меди, по меньшей мере одну соль щелочного металла, по меньшей мере одну соль редкоземельного металла и по меньшей мере одну соль щелочноземельного металла. В других вариантах исполнения активная солевая композиция не содержит соли щелочного металла, соли щелочноземельного металла, соли редкоземельного металла или соли переходного металла, иной чем соль меди. Некоторые неограничивающие примеры применимых катализаторов оксихлорирования, активных солевых композиций и материалов носителя представлены в патентной заявке РСТ №WO 81/01284, Патентах США №№3488398; 4339620; 4446249; 4740642; 4849393; 5292703; 5382726; 5600043; 6872684; 6803342; 6777373; 6759365; и 6174834, и Японской Патентной Публикации №11-090233, которые все включены здесь ссылкой во всей их полноте.
Средний размер частиц и гранулометрический состав частиц катализатора оксихлорирования, материала носителя или разбавителя могут быть измерены с помощью гранулометра. Как они используются или заявляются в данной заявке, значения среднего размера частиц и гранулометрического состава измеряются или могут быть измерены по стандарту ASTM D4460-00, который включен здесь ссылкой, или по методике, описанной ниже. Средний размер частиц и гранулометрический состав могут быть измерены с помощью лазерного гранулометра Honeywell Microtrac X-100, с использованием воды как диспергирующей среды. Образцы для измерения могут быть приготовлены добавлением примерно 5 мл частиц к 10 мл раствора поверхностно-активного вещества (который готовится из 4 мл средства TRITON™ CF-10 (от фирмы Rohm and Haas Company, Philadelphia, PA) и 6 мл средства TRITON™ Х-100 (от фирмы Rohm and Haas Company, Philadelphia, PA), разбавленных водой до объема 1000 мл) в стакане емкостью 50 мл. Смесь перемешивается для смачивания всех частиц в течение от около 10 до 15 секунд с образованием суспензии, которая затем добавляется в резервуар с мешалкой прибора Microtrac X-100, содержащий примерно 2 литра воды. Как только должный уровень концентрации подтверждается с помощью компьютерной программы (примерно от 10 до 20 секунд), начинается измерение. Температура воды поддерживается примерно между 80 и 90°F. Гранулометр Microtrac X-100 использует принцип дифракции лазерного излучения для измерения процентного содержания частиц в диапазоне от 0,04 до 700 микрон. Средний размер частиц соответствует 50% (по объему) образца. Гранулометрический состав формулируется как процентные доли частиц, меньших по величине, чем некоторый конкретный размер в микронах. Альтернативно, средний размер частиц и гранулометрический состав образцов могут быть измерены с помощью эквивалентного прибора или метода, который дает по существу такие же результаты, как полученные с применением лазерного гранулометра Honeywell Microtrac X-100.
Специалист-технолог может признавать, что измерения среднего размера частиц и гранулометрического состава могут быть подвержены погрешностям и/или вариациям, в зависимости от многих факторов, таких как тип гранулометра, использованного для измерения, метода расчета, включающего алгоритм коррекции погрешностей, метода приготовления образца, количества и природы диспергирующей среды, количества и природы поверхностно-активного вещества и тому подобных. Для каталитических композиций для оксихлорирования, представленных здесь, относительные значения средних размеров частиц и гранулометрических составов частиц катализатора оксихлорирования, материала носителя и разбавителя являются настолько же важными, насколько и их абсолютные величины. Относительные значения средних размеров частиц и гранулометрических составов частиц катализатора оксихлорирования, материала носителя и разбавителя могут быть измерены методом, известным специалисту в этой области технологии. Например, относительный средний размер частиц разбавителя или материала носителя к среднему размеру частиц катализатора оксихлорирования могут быть получены по стандарту ASTM D4460-00 или методу, описанному выше или любому подобному методу, известному специалисту в данной области.
Площадь поверхности материала носителя, катализатора оксихлорирования или разбавителя может быть определена по методу БЭТ (Брунауэра-Эммета-Теллера) измерения площади поверхности, как описано авторами S. Brunauer, P.H. Emmett, и E. Teller, Journal of American Chemical Society, том 60, стр.309 (1938), который включен здесь ссылкой. Как они используются или заявляются в данной заявке, значения площади поверхности рассчитываются или могут быть рассчитаны из данных изотермы адсорбции азота при 77°К с использованием метода БЭТ. Материал носителя, катализатор оксихлорирования или разбавитель могут иметь либо высокую площадь поверхности, либо низкую площадь поверхности. Применяемый здесь термин «высокая площадь поверхности» или «высокая-площадь-поверхности» означает площадь поверхности, большую чем 25 м2/г, предпочтительно большую чем около 50 м2/г, более предпочтительно большую чем около 70 м2/г. Далее, применяемый здесь термин «низкая площадь поверхности» или «низкая-площадь-поверхности» означает площадь поверхности, меньшую чем 25 м2/г, предпочтительно меньшую чем около 20 м2/г, более предпочтительно меньшую чем около 16 м2/г.
Любой материал носителя, который известен в технологии, пригодный в качестве носителя для катализатора оксихлорирования, может быть использован в этом изобретении. Неограничивающие примеры применимых материалов носителя включают оксид алюминия, такой как активированный оксид алюминия и микрогель оксида алюминия, оксид кремния, оксид магния, кизельгур, фуллерову землю, глины, алюмосиликаты, пористые галогениды и оксигалогениды редкоземельных элементов и их комбинации. Материал носителя может иметь площадь поверхности между примерно 5 м2/г и примерно 450 м2/г, определяемую методом БЭТ. В некоторых вариантах осуществления площадь поверхности материала носителя составляет от около 25 м2/г до около 300 м2/г. В дальнейших вариантах исполнения площадь поверхности материала носителя составляет от около 70 м2/г до около 200 м2/г. В некоторых вариантах осуществления площадь поверхности материала носителя составляет от около 70 м2/г до около 240 м2/г.
Материал носителя может иметь средний размер частиц, варьирующий от около 5 до около 300 микрон, от около 20 до около 250 микрон, от около 20 до около 200 микрон, от около 20 до около 150 микрон, от около 20 до около 120 микрон, от около 30 до около 100 микрон, или от около 30 до около 90 микрон. Объемная плотность материала носителя в слежавшемся состоянии, или объемная плотность утрамбованного материала, может варьировать от около 0,6 до около 1,6 г/см3, от около 0,7 до около 1,5 г/см3, от около 0,7 до около 1,3 г/см3, или от около 0,8 до около 1,3 г/см3.
В катализаторах оксихлорирования в псевдоожиженном слое является желательным, что материалы носителя имеют высокую площадь поверхности, поскольку материалы носителя с высокой площадью поверхности могут снижать склонность к слипанию катализатора оксихлорирования, так как активная солевая композиция распределяется на большой площади. Слипание катализатора определяется как агломерирование частиц катализатора вследствие подвижности хлорида меди и мостикового связывания частицы с частицей в рабочих условиях процесса. В катализаторах со стационарным слоем материал носителя может иметь либо высокую площадь поверхности, либо низкую площадь поверхности. Предпочтительным каталитическим процессом является катализ в псевдоожиженном слое с использованием материала носителя с высокой площадью поверхности.
Катализатор оксихлорирования, используемый для процесса с катализом в псевдоожиженном слое, может включать активную солевую или оксидную композицию, равномерно распределенную, нанесенную в виде отложения, покрытия, соосажденную или помещенную на материале носителя с высокой площадью поверхности. Материал носителя может быть в форме частиц, имеющих должные размеры частиц, площадь поверхности, пористость, плотность, устойчивость к истиранию и прочие характеристики (а) для обеспечения равномерной флюидизации, хорошей теплопередачи и минимального температурного градиента в слое реактора; (b) для обеспечения адекватного контакта между активной солевой композицией и газообразными реагентами, когда последние проходят через слой; и (с) для сведения к минимуму потери катализатора из-за выноса мелких частиц из реактора с исходящими газами.
В некоторых вариантах осуществления материал носителя, имеющий площадь поверхности, большую чем 50 м2/г, и материал носителя выбирают из группы, составленной из алюмосиликата, оксида кремния, оксида алюминия и их комбинаций. В конкретном варианте исполнения материалы носителя представляет собой оксиды алюминия, имеющие площадь поверхности в диапазоне от около 25 до 250 м2/г, плотность слежавшегося материала в диапазоне от 0,7 до 1,1 г/см3, и средний размер частиц, варьирующий от около 5 до около 300 микрон. Такие материалы носителя на основе оксида алюминия легко создают псевдоожиженный слой, являются относительно стабильными, механически прочными и устойчивыми к истиранию. В некоторых вариантах исполнения материал носителя представляет собой оксид алюминия, имеющий площадь поверхности в диапазоне от около 120 до 240 м2/г и средний размер частиц, варьирующий от около 30 до около 90 микрон.
Является общепризнанным, что некоторых материалы носителя на основе оксида алюминия могут содержать, в дополнение к оксиду алюминия (Al2O3), небольшие количества других металлических соединений, таких как оксиды металлов. Неограничивающие примеры оксидов металлов в оксиде алюминия включают оксид натрия, оксид магния, оксид титана и тому подобные. Эти материалы носителя на основе оксида алюминия являются легко применимыми в этом изобретении. Подобным образом, некоторые материалы носителя на основе алюмосиликатов могут содержать, в дополнение к алюмосиликату, небольшие количества других металлических соединений, таких как силикаты металлов и оксиды металлов. Неограничивающие примеры оксидов металлов в алюмосиликате включают оксид натрия, оксид магния, оксид железа и тому подобные. Эти алюмосиликатные материалы носителя также являются легко применимыми в этом изобретении. Прочие металлические соединения могут присутствовать изначально или быть добавленными как отдельные соединения.
В некоторых вариантах осуществления активная солевая композиция включает соль меди. Соль меди может быть использована в форме водорастворимой соли, предпочтительно в виде хлорид меди. Однако могут быть также использованы оксиды меди или другие соли меди, такие как нитратная соль, карбонатная соль и прочие галогенидные соли типа бромидной соли, которые могли бы быть превращены в хлорид во время процесса оксихлорирования. Количества соли меди и других солей в катализаторе оксихлорирования зависят от желаемой активности и конкретных характеристик формирования псевдоожиженного слоя материалом носителя для применения в качестве катализатора в псевдоожиженном слое. Уровень содержания металлической меди может быть в диапазоне от около 1% по весу до около 15% по весу, в расчете на общий вес катализатора оксихлорирования. В некоторых вариантах осуществления уровень содержания металлической меди составляет от около 2% по весу до около 8% по весу, в расчете на общий вес катализатора оксихлорирования. В других вариантах осуществления количество металлической меди в соли меди варьирует в диапазоне от около 3% до около 6% по весу, в расчете на общий вес катализатора оксихлорирования. В других вариантах осуществления количество металлической меди в соли меди варьирует в диапазоне от около 7% до около 12% по весу, в расчете на общий вес катализатора оксихлорирования.
Активная солевая композиция может также содержать соль или оксид щелочного металла. Щелочный металл в солях щелочных металлов, используемых в настоящем изобретении, может быть выбран из группы, состоящей из натрия, калия, лития, рубидия, цезия и их смесей. Соль щелочного металла может быть в форме водорастворимой соли, такой как хлорид щелочного металла. Однако могут быть также применены другие соли или оксиды щелочных металлов, которые могли бы быть превращены в хлоридные соли во время процесса оксихлорирования, такие как карбонатные соли и прочие галогенидные соли типа бромидных солей. В некоторых вариантах осуществления щелочной металл представляет собой калий, литий или цезий. В еще одном варианте исполнения щелочным металлом является калий. В одном особенном варианте осуществления соль щелочного металла представляет собой хлорид калия. Количество щелочного металла в соли щелочного металла может варьировать в диапазоне от около 0,1% до около 8,0% по весу, в расчете на общий вес катализатора оксихлорирования. В некоторых вариантах исполнения количество щелочного металла в соли щелочного металла может варьировать в диапазоне от около 0,25% до около 5% по весу, в расчете на общий вес катализатора оксихлорирования. В других вариантах исполнения количество щелочного металла в соли щелочного металла может варьировать в диапазоне от около 0,5% до около 2,5% по весу, в расчете на общий вес катализатора оксихлорирования.
В некоторых вариантах осуществления активная солевая композиция включает соль или оксид редкоземельного металла. Редкоземельный металл в солях редкоземельных металлов, используемых здесь, может быть любым из элементов, перечисленных как элементы с 57 по 71 в Периодической Таблице, и псевдоредкоземельными элементами иттрием и скандием. Неограничивающие примеры редкоземельных металлов включают лантан, церий, неодим, празеодим, диспрозий, самарий, иттрий, гадолиний, эрбий, иттербий, гольмий, тербий, европий, тулий, лютеций и их смеси, такие как дидим, который представляет собой смесь празеодима и неодима. Предпочтительными солями редкоземельных металлов являются хлориды редкоземельных металлов. Однако могут быть также применены другие соли или оксиды редкоземельных металлов, которые могли бы быть превращены в хлоридные соли во время процесса оксихлорирования, например, карбонатные соли, нитратные соли и прочие галогенидные соли типа бромидных солей. Количество редкоземельного металла в соли редкоземельного металла может варьировать в диапазоне от около 0,1% до около 9% по весу, в расчете на общий вес катализатора оксихлорирования. В некоторых вариантах исполнения количество редкоземельного металла в соли редкоземельного металла может варьировать в диапазоне от около 0,5% до около 6% по весу, в расчете на общий вес катализатора оксихлорирования. В других вариантах исполнения количество редкоземельного металла в соли редкоземельного металла может варьировать в диапазоне от около 0,5% до около 3% по весу, в расчете на общий вес катализатора оксихлорирования. В других вариантах осуществления соль редкоземельного металла представляет собой хлорид церия или дидимхлорид. В некоторых вариантах исполнения соль редкоземельного металла представляет собой смесь соли лантана и соли церия, в которой процентная доля лантана превышает процентную долю церия. Предпочтительное отношение процентной доли лантана к процентной доле церия составляет по меньшей мере 2,0. В других вариантах осуществления соль редкоземельного металла представляет собой смесь соли лантана и соли церия, в которой процентная доля церия превышает процентную долю лантана.
В некоторых вариантах исполнения активная солевая композиция включает соль или оксид щелочноземельного металла. Щелочноземельные металлы в солях щелочноземельных металлов могут представлять собой магний, кальций, стронций и барий. Предпочтительно щелочноземельными металлами являются магний и барий. Наиболее предпочтительным щелочноземельным металлом является магний. Предпочтительные соли щелочноземельных металлов представляют собой хлориды. Однако могут быть также применены другие соли или оксиды щелочноземельных металлов, которые могли бы быть превращены в хлоридные соли во время процесса оксихлорирования, например карбонатные соли, нитратные соли и прочие галогенидные соли типа бромидных солей. Количество щелочноземельного металла в солях щелочноземельных металлов может варьировать в диапазоне от около 0,05% до около 6% по весу, в расчете на общий вес катализатора оксихлорирования. В некоторых вариантах исполнения количество щелочноземельного металла в соли щелочноземельного металла варьирует в диапазоне от около 0,25% до около 4% по весу, в расчете на общий вес катализатора оксихлорирования. В некоторых вариантах исполнения количество щелочноземельного металла в соли щелочноземельного металла варьирует в диапазоне от около 0,25% до около 3% по весу, в расчете на общий вес катализатора оксихлорирования.
Необязательно, в активной солевой композиции может присутствовать по меньшей мере одна соль или оксид другого металла в относительно небольших количествах. Такие соли других металлов могут быть в форме карбоната, нитрата или галогенида, такого как хлорид и бромид. Неограничивающие примеры таких других металлов включают металлы главных подгрупп, такие как свинец, олово, висмут, галлий и тому подобные, и переходные металлы, такие как железо, цинк, хром, никель, кобальт, скандий, ванадий, титан, марганец, цирконий, серебро, золото, рутений, родий, палладий и тому подобные. В некоторых вариантах осуществления каждый металл в солях или оксидах других металлов может быть представлен в количестве вплоть до около 1 весового процента, в расчете на общий вес катализатора оксихлорирования. В других вариантах осуществления количество каждого металла в солях или оксидах других металлов может составлять вплоть до около 0,5 весового процента, в расчете на общий вес катализатора оксихлорирования. В дальнейших вариантах выполнения ни одна из солей или оксидов других металлов не присутствует в активной солевой композиции.
Любой способ получения катализаторов оксихлорирования, известный квалифицированному специалисту в этой области технологии, может быть применен для приготовления раскрытых здесь каталитических композиций для оксихлорирования. Неограничивающие примеры таких способов описаны в PCT-патентной заявке № WO 81/01284 и в Патентах США №№3488398; 4339620; 4446249; 4740642; 4849393; 5292703; 5382726; 5600043; 6872684; 6803342; 6777373; 6759365; и 6174834, и в Японской Патентной Публикации №11-090233. Активная солевая композиция может быть нанесена на материал носителя путем добавления раствора активной солевой композиции в любом подходящем растворителе, таком как вода, спирты, диметилформамид, диметилсульфоксид, простые эфиры и кетоны. Предпочтительным растворителем является вода. Хотя пригодны любые соли металлов, способные образовывать раствор, предпочтительными солями металлов являются хлоридные соли. Один неограничивающий пример приготовления катализатора оксихлорирования включает стадию растворения в воде активной солевой композиции, включающей один или более хлоридов металлов, таких как хлорид меди, хлориды щелочных металлов, хлориды редкоземельных металлов, хлориды щелочноземельных металлов, хлориды переходных металлов, иные чем хлорид меди, и их комбинации. Раствор может быть медленно набрызган на материал носителя при непрерывном перемешивании (или, альтернативно, материал носителя может б