Способ получения оксида цинка из слабоконцентрированных растворов
Иллюстрации
Показать всеИзобретение относится к гидрометаллургии цинка и может быть использовано для переработки цинксодержащих отходов для получения оксида цинка. Способ получения оксида цинка из цинксодержащего раствора включает осаждение цинксодержащего осадка гидроксидом аммония, обработку раствором карбоната или бикарбоната аммония, сушку и прокалку. Осаждение ведут из слабоконцентрированных цинксодержащих растворов. Выделенный цинксодержащий осадок прокаливают при 125-150°С. Прокаленный осадок подвергают обработке раствором карбоната или бикарбоната аммония. Затем его сушат и вновь прокаливают при 300-750°С. Техническим результатом является снижение энергозатрат при фильтрации, сушке и прокалке, уменьшение расхода реагентов и улучшение экологических характеристик процесса. 2 ил., 4 табл.
Реферат
Изобретение относится к гидрометаллургии цинка и может быть использовано для переработки цинксодержащих отходов для получения оксида цинка.
Известен способ получения оксида цинка осаждением его гидроксидом аммония с последующей прокалкой при температуре 900°С [Евдокимова А.К. и др. О внедрении нового метода производства окиси цинка для нужд лакокрасочной и других отраслей промышленности. Цветные металлы. 1962. №4. С.41-46].
Недостатком способа являются высокая влажность осадка даже после двух- трехкратной отмывки (влажность 400-500%), наличие большого количества водорастворимых примесей, захваченных при осаждении гидроксида с маточником, высокая температура прокалки во вращающейся трубчатой печи 900-950°С.
Наиболее близким техническим решением является способ получения оксида цинка из цинксодержащих продуктов [Абевова Т.А. и др. Способ получения оксида цинка из цинксодержащих продуктов. Патент РФ 2019511, 1994, Бюл. №17], включающий выделение осадка основного сульфата цинка из раствора гидроксидом аммония, его обработку раствором карбоната аммония или бикарбоната аммония, сушку и прокалку.
Недостатком способа является то, что из слабоконцентрированных растворов наряду с основным сульфатом цинка образуется объемный гидрофильный, плохо фильтрующийся аморфный осадок гидроксида цинка, что вызывает затруднения при его дальнейшей обработке карбонатом или бикарбонатом аммония, большой расход этих реагентов, а сушка и прокалка сопровождаются выделением большого количества углекислого газа и аммиака.
Задачей, на решение которой направлено заявленное изобретение, является нахождение оптимальных условий для быстрого и эффективного способа получения оксида цинка из слабоконцентрированных растворов.
Техническим результатом, который может быть достигнут при осуществлении изобретения, является эффективность процесса получения оксида цинка из слабоконцентрированных растворов.
Этот технический результат достигается тем, что в известном способе получения оксида цинка из цинксодержащего раствора, включающем осаждение цинксодержащего осадка гидроксидом аммония, обработку раствором карбоната или бикарбоната аммония, сушку и прокалку, осаждение ведут из слабоконцентрированных цинксодержащих растворов, выделенный цинксодержащий осадок прокаливают при 125-150°С, обработке раствором карбоната или бикарбоната аммония подвергают прокаленный осадок, который сушат и вновь прокаливают при 300-750°С.
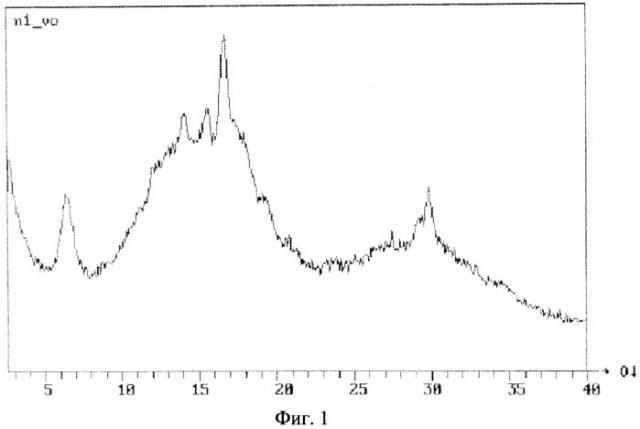
Сущность способа поясняется табл.1-5 и фиг.1 и 2, где даны температуры разложения фазовых составляющих этих осадков, а также по данным рентгенофазового анализа фазового состава осадков, полученных при различных условиях их образования. Рентгенофазовый анализ проводили на установке АРС-5 (Дрон-1); Cu - анод, Θ - углы скольжения, d, Å - межплоскостные расстояния, I/I0, % - интенсивность.
В табл.1 даны температуры разложения ряда соединений цинка и аммония, находящихся в цинксодержащих осадках по реакциям:
Использованы данные следующих источников:
1. Рабинович В.А., Хавин З.Я. Краткий химический справочник. - М.: Химия, Ленинградское отделение. 1977;
2. Рипан Р., Читяну И. Неорганическая химия, ч.2. - М.: Мир. 1972. С.793.
| Таблица 1 | |
| Температуры разложения ряда солей цинка и аммония, содержащихся в цинксодержащих осадках | |
| Соли | Температура, °С |
| (NH4)2SO4 | >218 |
| (NH4)2СО3 | 58 |
| Zn(OH)2 | 125 |
| ZnCO3 | 300 |
| ZnSO4 | >600 |
По прототипу из достаточно концентрированных растворов сульфата цинка, содержащих 100 г/дм3 Zn (II), гидроксидом аммония с концентрацией 25% осаждаются гидроксосульфаты основных солей цинка, например, по реакции:
Даже двухкратная промывка основного сульфата цинка 3Zn(OH)2·ZnSO4 водой сохраняет высокое содержание иона SO4 2- (до 20%), что приводит к увеличению температуры прокалки до 900-950°С. Чтобы избежать такой сложности процесса, выделившийся осадок основных солей сульфата цинка обрабатывают раствором карбоната или бикарбоната аммония с концентрацией 40-100 г/дм3. При этом в результате обменной реакции
содержание сульфат-иона в осадке снижается с 20 до 3% в основном карбонате цинка.
Исходя из данных табл.1 замена сульфат-ионов на карбонат-ионы снижает температуру прокалки. Согласно прототипу при содержании в осадке иона SO4 2- до 3,0% осадок сушили и прокаливали при 750°С.
По предлагаемому способу при осаждении цинка гидроксидом аммония из слабоконцентрированных, разбавленных растворов сульфатов цинка образуется аморфный, гидрофильный, плохо фильтрующийся осадок гидроксида цинка.
Согласно табл.1 прокалка такого осадка при температуре ≥125°С приводит к образованию оксида ZnO по реакции (3), при этом в газовую фазу уходят пары воды и, возможно, в небольших количествах аммиак при разложении захваченного из маточника гидроксида аммония. Образующийся после прокаливания оксид цинка ZnO содержит сульфаты аммония и цинка, имеющие более высокую температуру разложения. Количество последних зависит от исходной концентрации сульфата цинка, числа циклов промывки, времени и температуры сушки и других условий.
При необходимости можно обработать такой осадок растворами карбоната или бикарбоната аммония, расход которых резко снижается по сравнению с прототипом. Кроме того, если учесть, что согласно данным (Абевова Т.А. и др. Цветные металлы. №5, 1993. С.20-22) чем меньше содержание сульфат-ионов в прокаливаемом продукте, тем ниже температура прокалки и содержание водорастворимых примесей в конечном продукте, выше содержание основного вещества и белизна продукта.
Пример конкретного выполнения способа
Стадия 1
Раствор, содержащий 100 мг/дм3 иона Zn (II), нейтрализуют раствором гидроксида аммония до рН 8-9.
В табл.2 и на фиг.1 даны результаты рентгенофазового анализа осадка. Рентгеновский спектр свидетельствует об аморфном состоянии большей части фаз, из которых состоит данный образец. Однозначное решение качественного и количественного анализа такого спектра практически невозможно. Тем не менее, по наличию отдельных кристаллических рефлексов спектра обнаружен Zn(OH)2 - основа и примеси ZnO, ZnSO4, (NH4)2SO4, 3Zn(OH)2·ZnSO4·4H2O, 6Zn(OH)2·ZnSO4·4H2O и др.
| Таблица 2 | ||||||||
| Данные рентгенофазового анализа образца осадка на стадии 1 (фиг.1) | ||||||||
| Θ | d, Å | I/I0 | Θ | d, Å | I/I0 | Θ | d, Å | I/I0 |
| 5,813 | 7,6120 | 12 | 16,337 | 2,7405 | 79 | 25,813 | 1,7704 | 11 |
| 5,963 | 7,4212 | 19 | 16,462 | 2,7203 | 90 | 26,065 | 1,7545 | 13 |
| 6,168 | 7,1754 | 31 | 16,538 | 2,7083 | 97 | 26,331 | 1,7390 | 13 |
| 6,342 | 6,9791 | 36 | 16,656 | 2,6896 | 100 | 26,587 | 1,7224 | 14 |
| 6,513 | 6,7968 | 33 | 16,893 | 2,6529 | 75 | 26,745 | 1,7130 | 15 |
| 6,787 | 6,5226 | 22 | 17,087 | 2,6236 | 66 | 26,983 | 1,6990 | 16 |
| 6,988 | 6,3368 | 12 | 17,242 | 2,6008 | 65 | 27,398 | 1,6752 | 21 |
| 7,267 | 6,0946 | 9 | 17,413 | 2,5761 | 63 | 27,896 | 1,6477 | 17 |
| 7,412 | 5,9754 | 6 | 17,588 | 2,5513 | 60 | 28,161 | 1,6334 | 16 |
| 7,638 | 5,8003 | 6 | 17,863 | 2,5132 | 60 | 28,394 | 1,6211 | 16 |
| 10,919 | 4,0698 | 28 | 18,417 | 2,4401 | 43 | 28,637 | 1,6085 | 16 |
| 11,089 | 4,0080 | 30 | 18,588 | 2,4185 | 39 | 28,887 | 1,5957 | 22 |
| 11,247 | 3,9525 | 31 | 19,084 | 2,3578 | 36 | 29,036 | 1,5883 | 24 |
| 11,969 | 3,7173 | 46 | 19,283 | 2,3343 | 33 | 29,162 | 1,5820 | 24 |
| 12,182 | 3,6532 | 48 | 19,435 | 2,3168 | 33 | 29,317 | 1,5744 | 27 |
| 12,416 | 3,5855 | 50 | 19,610 | 2,2969 | 28 | 29,436 | 1,5686 | 24 |
| 13,043 | 3,4159 | 55 | 20,533 | 2,1979 | 17 | 29,569 | 1,5622 | 30 |
| 13,286 | 3,3545 | 56 | 20,758 | 2,1751 | 19 | 29,637 | 1,5589 | 31 |
| 13,520 | 3,2974 | 56 | 21,038 | 2,1475 | 13 | 29,768 | 1,5527 | 39 |
| 13,633 | 3,2705 | 58 | 21,238 | 2,1282 | 13 | 29,912 | 1,5459 | 31 |
| 13,914 | 3,2057 | 67 | 21,411 | 2,1117 | 12 | 30,037 | 1,5388 | 26 |
| 14,008 | 3,1847 | 68 | 23,181 | 1,9584 | 9 | 30,188 | 1,5318 | 21 |
| 14,113 | 3,1616 | 67 | 23,513 | 1,9323 | 9 | 30,462 | 1,5193 | 18 |
| 14,493 | 3,0804 | 58 | 23,767 | 1,9128 | 10 | 30,755 | 1,5063 | 16 |
| 15,040 | 2,9708 | 61 | 23,953 | 1,8988 | 9 | 31,446 | 1,4765 | 13 |
| 15,288 | 2,9238 | 64 | 24,088 | 1,8888 | 9 | 32,287 | 1,4420 | 8 |
| 15,360 | 2,9103 | 66 | 24,442 | 1,8631 | 8 | 32,823 | 1,4210 | 7 |
| 15,517 | 2,8815 | 66 | 24,708 | 1,8442 | 8 | 34,255 | 1,3684 | 8 |
| 15,621 | 2,8628 | 69 | 24,961 | 1,8267 | 11 | 34,447 | 1,3617 | 9 |
| 16,132 | 2,7745 | 64 | 25,631 | 1,7821 | 10 | 34,763 | 1,3509 | 7 |
Под микроскопом видна шаровидная форма частиц.
Стадия 2
Осадок гидроксида цинка отделяют от раствора, фильтруют и нагревают до 125-150°С.
Под микроскопом видны кристаллы игольчатой формы, характерной для оксида цинка.
В табл.3 и на фиг.2 даны результаты рентгенофазового анализа осадка.
| Таблица 3 | ||||||||
| Данные рентгенофазового анализа образца осадка на стадии 2 (фиг.2) | ||||||||
| Θ | d, Å | I/I0 | Θ | d, Å | I/I0 | Θ | d, Å | I/I0 |
| 5,888 | 7,5154 | 1 | 15,943 | 2,8064 | 100 | 24,888 | 1,8318 | 1 |
| 6,063 | 7,2992 | 2 | 16,593 | 2,6995 | 4 | 25,157 | 1,8134 | 1 |
| 6,188 | 7,1523 | 3 | 16,838 | 2,6614 | 15 | 26,438 | 1,7315 | 1 |
| 6,325 | 6,9974 | 5 | 16,904 | 2,6512 | 16 | 26,613 | 1,7209 | 1 |
| 6,503 | 6,8065 | 4 | 17,292 | 2,5935 | 9 | 26,906 | 1,7035 | 2 |
| 6,953 | 6,3680 | 1 | 17,613 | 2,5477 | 2 | 27,000 | 1,6980 | 2 |
| 10,170 | 4,3659 | 1 | 17,913 | 2,5064 | 3 | 27,841 | 1,6507 | 2 |
| 10,238 | 4,3375 | 1 | 18,193 | 2,4690 | 73 | 27,993 | 1,6424 | 2 |
| 10,688 | 4,1568 | 3 | 18,864 | 2,3842 | 1 | 28,375 | 1,6221 | 43 |
| 10,863 | 4,0906 | 5 | 19,088 | 2,3574 | 2 | 28,788 | 1,6008 | 2 |
| 10,959 | 4,0551 | 6 | 19,317 | 2,3305 | 8 | 29,163 | 1,5820 | 1 |
| 11,381 | 3,9065 | 9 | 19,538 | 2,3051 | 3 | 29,488 | 1,5661 | 1 |
| 11,531 | 3,8563 | 1 | 19,629 | 2,2949 | 2 | 29,645 | 1,5585 | 2 |
| 12,063 | 3,6889 | 1 | 19,725 | 2,2841 | 1 | 30,150 | 1,5336 | 1 |
| 12,313 | 3,6151 | 2 | 19,850 | 2,2703 | 1 | 30,458 | 1,5195 | 1 |
| 12,696 | 3,5075 | 13 | 20,219 | 2,2306 | 1 | 31,288 | 1,4832 | 1 |
| 12,962 | 3,4367 | 3 | 20,915 | 2,1595 | 1 | 31,551 | 1,4720 | 8 |
| 13,180 | 3,3809 | 1 | 21,700 | 2,0849 | 1 | 32,129 | 1,4483 | 1 |
| 13,336 | 3,3422 | 1 | 21,837 | 2,0724 | 1 | 32,513 | 1,4331 | 4 |
| 13,617 | 3,2745 | 2 | 22,092 | 2,0498 | 1 | 32,619 | 1,4289 | 5 |
| 13,728 | 3,2485 | 2 | 22,238 | 2,0370 | 1 | 33,266 | 1,4042 | 7 |
| 13,968 | 3,1937 | 2 | 22,480 | 2,0230 | 2 | 33,691 | 1,3886 | 1 |
| 14,072 | 3,1706 | 2 | 22,993 | 1,9735 | 1 | 33,888 | 1,3815 | 3 |
| 14,181 | 3,1466 | 1 | 23,313 | 1,9479 | 2 | 34,064 | 1,3752 | 15 |
| 14,656 | 3,0468 | 1 | 23,856 | 1,9061 | 8 | 34,625 | 1,3556 | 12 |
| 15,042 | 2,9704 | 1 | 24,163 | 1,8833 | 3 | 34,929 | 1,3453 | 3 |
| 15,412 | 2,9006 | 3 | 24,315 | 1,8722 | 6 | 38,568 | 1,2355 | 2 |
| 15,713 | 2,8466 | 20 | 24,734 | 1,8424 | 1 |
Осадок содержит кристаллические фазы, содержание которых дано в табл.4, указаны также межплоскостные расстояния d, и интенсивности I/I0 этих фаз.
Под микроскопом видна игольчатая форма частиц.
Стадия 3
Для замены сульфат-ионов на карбонат-ионы полученный прокаленный осадок обрабатывают растворами карбоната или бикарбоната аммония.
| Таблица 4 | |||
| Характеристика фаз осадка, полученного на стадии 2 | |||
| Фазы | Содержание фаз в осадке, объемный % | d, Å | I/I0 |
| ZnO | 71,56 | 2,48; 2,82; 2,60 | 100, 71, 56 |
| α - ZnSO4 | 3,98 | 3,44; 2,67; 2,79 | 100, 80, 50 |
| β - ZnSO4 | 2,99 | 3,54; 4,17; 2,65 | 100, 80, 75 |
| ZnO·2ZnSO4 | 2,97 | 2,97; 2,47; 3,67 | 100, 100, 80 |
| 2ZnO·3ZnSO4 | 2,95 | 2,99; 3,71; 3,38 | 100, 95, 95 |
| 3Zn(OH)2·ZnSO4·4Н2О | 2,88 | 10,0; 2,75; 1,58 | 100, 90, 50 |
| (NH4)2Zn(SO4)2 | 2,55 | 4,27; 4,17; 7,51 | 100, 90, 85 |
| (NH4)2SO4 | 2,33 | 4,33; 4,39; 3,06 | 100, 65, 55 |
| (NH4)2Zn(SO4)2·6H2O | 2,29 | 4,15; 3,76; 4,30 | 100, 65, 60 |
| ZnSO4·6H2O | 2,25 | 4,40; 4,05; 2,92 | 100, 53, 27 |
| CaSO4 | 1,75 | 3,50; 2,85; 2,33 | 100, 30, 20 |
| Zn(OH)2 | 1,50 | 6,97; 3,09; 2,97 | 100, 30, 30 |
Из данных табл.1 видно, что карбонаты имеют более низкую температуру разложения, чем соответствующие сульфаты.
Из данных табл.4 видно, что количество сульфатов невелико, поэтому расход карбонатов незначителен, к тому же последующая после сушки прокалка имеет температуру меньше 700°С. В газовую фазу переходят незначительные количества углекислого газа и аммиака.
По мере снижения количества гидроксида цинка и увеличения основных сульфатов цинка и двойных солей сульфатов аммония и цинка осуществляется плавный переход от предлагаемого способа к прототипу.
По сравнению с прототипом снижаются энергозатраты при фильтрации, сушке и прокалке, уменьшается расход реагентов и улучшаются экологические характеристики процесса, так как газовая фаза содержит меньшие количества аммиака и углекислого газа.
Способ получения оксида цинка из цинксодержащего раствора, включающий осаждение цинксодержащего осадка гидроксидом аммония, обработку раствором карбоната или бикарбоната аммония, сушку и прокалку, отличающийся тем, что осаждение ведут из слабоконцентрированных цинксодержащих растворов, выделенный цинксодержащий осадок прокаливают при 125-150°С, обработке раствором карбоната или бикарбоната аммония подвергают прокаленный осадок, который сушат и вновь прокаливают при 300-750°С.