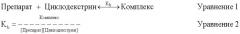Ингаляционная препаративная форма, содержащая простой сульфоалкиловый эфир гамма-циклодекстрина и кортикостероид
Иллюстрации
Показать всеИзобретение относится к медицине. Описана ингаляционная препаративная форма, содержащая SAE-γCD и кортикостероид. Препаративная форма адаптирована для введения субъекту распылением любым известным распылителем, препаративная форма может быть включена в набор. Препаративная форма вводится в виде водного раствора, однако, она может храниться в виде сухого порошка, готового к применению раствора или концентрированной композиции. Препаративная форма используется в усовершенствованной системе распыления для введения кортикостероида путем ингаляции. SAE-γCD, присутствующий в препаративной форме, значительно повышает химическую устойчивость будезонида. Описан способ введения препаративной формы ингаляцией. Препаративную форму можно также вводить обычным прибором для интраназальной доставки. Препаративная форма может включать одно или более дополнительных терапевтических средств для использования в комбинации с кортикостероидом. SAE-γCD особенно полезен для солюбилизации этерифицированных кортикостероидов. 4 н. и 23 з.п. ф-лы, 10 табл., 5 ил.
Реферат
Область изобретения
Настоящее изобретение относится к способу введения и препаративной форме для введения простого сульфоалкилового эфира γ-циклодекстрина и кортикостероида, такого как будезонид, путем ингаляции. Изобретение также относится к способам лечения заболеваний и расстройств легких.
Предпосылки изобретения
Доставка препарата ингаляцией обеспечивает возможность подачи препарата в различные отделы дыхательных путей, например горло, трахею, бронхи и альвеолы. В целом, чем меньше размер частиц, тем дольше частицы будут оставаться суспендированными в воздухе и тем дальше вниз по дыхательным путям может быть доставлен препарат. Кортикостероиды доставляются ингаляторами с использованием распылителей, ингаляторов отмеренной дозы или порошковыми ингаляторами. Принципиальные преимущества распылителей перед другими способами легочной инсталляции состоят в том, что не требуется содействие пациента и легче доставлять более высокие дозы лекарственных средств. Однако основными проблемами, связанными с распылителями, являются их высокая стоимость, недостаточная портативность, неудобство необходимости готовить лекарственное средство заранее и необходимость в увеличенных временных затратах для проведения лечения. Существует потребность в способе, улучшающем введение распылением таких препаратов, как кортикостероиды.
Будезонид ((R,S)-11β,16α,17,21-тетрагидроксипрегна-1,4-диен-3,20-дионциклический 16,17-ацеталь с бутиральдегидом; С25Н34О6; молекулярная масса* 430,5) хорошо известен. Он имеется в продаже в виде смеси двух изомеров (22R и 22S). Будезонид представляет собой противовоспалительный кортикостероид, который проявляет высокую глюкокортикоидную активность. Введение будезонида показано для поддерживающего лечения астмы и в качестве профилактического лечения у детей.
Имеющиеся в продаже препаративные формы будезонида продаются AstraZeneca LP (Wilmington, DE) под торговыми марками ENTOCORTTM EC, PULMICORT RESPULES®, Rhinocort Aqua®, Rhinocort® Nasal Inhaler и Pulmicort Turbuhaler® и под непатентованным наименованием PULMICORT RESPULES®, который представляет собой стерильную водную суспензию микронизированного будезонида и вводится ингаляцией с использованием распылителя, в частности приводимого в действие сжатым воздухом струйного распылителя, который доставляет от 2 до 18% массы препарата, содержащейся в номинальной загрузке. RHINOCORT® NASAL INHALERTM представляет собой устройство для распыления, содержащее дозу суспензии микронизированного будезонида в смеси с вытеснителями. RHINOCORT® AQUATM представляет собой лишенную запаха, аэрозольную препаративную форму, снабженную распылительным устройством для дозированного применения, содержащую суспензию микронизированного будезонида в водной среде. Суспензии не следует вводить ультразвуковым распылителем.
Желательные свойства жидкости для распыления в целом включают: 1) пониженную вязкость; 2) стерильную среду; 3) пониженное поверхностное натяжение; 4) устойчивость в отношении механизма распылителя; 5) умеренный рН (примерно 4-10), 6) способность образовывать капельки при MMAD <5 мкм или предпочтительно <3 мкм; 7) отсутствие раздражающих консервантов и стабилизирующих агентов; 8) подходящую тоничность. С одной стороны, суспензии обладают некоторыми преимуществами, но с другой стороны, вручную приготовленные растворы обладают другими преимуществами.
Smaldone et al. (J. Aerosol Med. (1998), 11, 113-125) описывают результаты исследования определения in vitro вдыхаемой массы и распределения частиц суспензии будезонида. Они делают заключение, что 2-18% загрузки распылителя будезонидом доставлялось из суспензии, это означает, что доставка будезонида была неполной, приводя к значительной потере препарата. В 13 наиболее эффективных устройствах суспензию можно распылить достаточно хорошо для доставки в нижние отделы дыхательных путей.
Другое исследование, кроме того, продемонстрировало высоко вариабельную эффективность распыления от одного распылителя к другому. Barry et al. (J. Allergy Clin. Immunol. (1998), 3230-321) указывают, что эту вариабельность следует принимать во внимание при лечении пациентов распыленным будезонидом. Berg et al. (J. Aerosol Sci. (1998), 19(7), 1101-1104) также сообщают о высоко вариабельной эффективности распыления суспензии PULMICORTTM от одного распылителя к другому. Более того, среднемассовый аэродинамический диаметр (MMAD) распыляемых частиц высоко вариабелен от одного распылителя к другому. В целом, суспензии менее эффективно распыляются, чем растворы (O'Riordan, Respiratory Care (2002), 1305-1313). Ингаляционные кортикостероиды используются при лечении астмы и имеют значительное преимущество, потому что они доставляются непосредственно в участок действия, легкие. Целью использования ингаляционных кортикостероидов является обеспечение локализованного лечения с непосредственным проявлением активности препарата в легких. Ингаляционные кортикостероиды хорошо всасываются из легких. В действительности, можно предположить, что весь препарат, имеющийся в участке рецептора в легких, будет поглощен системно. Однако хорошо известно, что при использовании современных способов и препаративных форм большая часть дозы ингаляционных кортикостероидов проглатывается и становится доступной для орального всасывания, приводя к нежелательным системным эффектам. Для ингаляционных кортикостероидов высокая легочная доступность более важна, чем высокая оральная биологическая доступность, потому что легкие являются органом-мишенью. Продукт с высокой легочной доступностью имеет больший потенциал оказания положительных эффектов в легких. Идеальная препаративная форма ингаляционных кортикостероидов должна обеспечивать минимальную оральную доставку, снижая посредством этого вероятность системных побочных эффектов.
Большая часть дозы кортикостероида, доставленной в легкие, поглощается и доступна системно. Для части ингаляционных кортикостероидов, доставленной орально, биологическая доступность зависит от всасывания из желудочно-кишечного тракта и степени метаболизма первого прохождения в печени. Поскольку этот оральный компонент доставки кортикостероидных препаратов не обеспечивает никакого благоприятного терапевтического эффекта, но может увеличить системные побочные эффекты, желательно, чтобы оральная биологическая доступность ингаляционных кортикостероидов была относительно низкой.
И размер частиц, и препаративная форма влияют на эффективность ингаляционных кортикостероидов. Препаративная форма препарата оказывает значительное воздействие на доставку этого препарата в легкие и поэтому на его эффективность. Наиболее важными при доставке препарата в легкие являются аэрозольный носитель и размер доставляемых частиц. Кроме того, сниженная степень отложения в легких свидетельствует о большей степени ротоглоточного отложения. Ввиду конкретной используемой препаративной формы более вероятно отложение некоторых кортикостероидов в ротовой полости и горле, и они могут вызвать местные побочные эффекты.
Хотя распределение рецепторов представляет собой основной определяющий фактор эффективности бронхолитического средства, размер частиц представляется более важным в определении эффективности ингаляционных кортикостероидов. Самые маленькие дыхательные пути имеют внутренний диаметр 2 микрона (мкм) или менее. Таким образом, ингалятор с частицами, имеющими средний аэродинамический диаметр 1 мкм, должен иметь большую вдыхаемую фракцию, чем ингалятор с частицами, которые имеют средний диаметр от 3,5 до 4 мкм. Для пациентов с обструктивным легочным заболеванием все частицы в идеале должны быть не больше чем 2-3 мкм. Частица, которая мала (менее чем 5 мкм), будет более вероятно ингалированной в мелкие дыхательные пути, таким образом повышая эффективность. Напротив, частицы, которые больше чем 5 мкм, могут откладываться в ротовой полости и горле, снижая пропорцию частиц, которые достигают легких, и потенциально вызывая местные побочные эффекты, такие как кандидоз и охриплость (дисфония). Частицы, имеющие среднемассовый аэродинамический диаметр (MMAD), близкий к 1 мкм, считаются имеющими большую вдыхаемую фракцию на дозу, чем частицы с диаметром 3,5 мкм или более.
Еще одним недостатком распыления суспензий будезонида является необходимость создания очень мелких капелек с MMAD примерно <3 мкм. Поскольку распыленные капельки настолько малы, то микронизированный будезонид должен быть даже меньше или в диапазоне от 0,5 до 2,0 мкм, и частицы должны иметь узкое распределение размера частиц. Создание таких частиц затруднительно.
Даже при этом предпринимались усилия улучшить распыление суспензий бутезонида ультразвуковыми распылителями использованием частиц субмикронного размера (Keller at al. in Respiratory Drug Delivery VIII (2002), 197-206). Суспензию наночастиц (0,1-1,0 мкм) кортикостероида можно использовать для увеличения пропорции вдыхаемых частиц, по сравнению с более грубой суспензией, как в суспензии PULMICORTTM. Улучшение по сравнению с суспензией PULMICORTTM не наблюдалось. Более того, существуют опасения в отношении использования наносуспензий в том, что мелкие частицы (<0,05 мкм) могут вызвать аллергическую реакцию у субъекта. Sheffield Pharmaceuticals, Inc. (St. Louis, MO; "The Pharmacokinetics of Nebulized Nanocrystal Budesonide Suspension in Healthy Volunteers". Kraft et al. в J. Clin. Pharmacol. (2004), 44:67-72) описали получение и оценку UDB (стандартной дозы будезонида), которая представляет собой основанную на суспензии препаративную форму, содержащую наночастицы будезонида, диспергированные в жидкой среде. Этот продукт разрабатывается MAP Pharmaceuticals, Inc. (Mountain View, California).
Известно, что, в отличие от растворенного препарата, ингаляция частиц препарата имеет недостатки. Brain et al. (Bronchial Asthma. 2nd Ed. (Ed. E.B. Weis et al., Little Brown & Co. (1985), pp. 594-603) сообщают, что менее растворимые частицы, которые откладываются на слизистом покрытии, покрывающем легочные дыхательные пути и носовые проходы, перемещаются в направлении глотки ресничками. Такие частицы включали бы более крупные частицы препарата, отложившиеся в верхних дыхательных путях. Слизь, клетки и клеточные фрагменты, поступающие из носовых полостей и легких, встречаются в глотке, смешиваются со слюной и поступают в желудочно-кишечный тракт после заглатывания. По сообщениям, с помощью этого механизма частицы удаляются из легких при периодах полувыведения от минут до часов. Соответственно, отведено мало времени для солюбилизации медленно растворяющихся препаратов, таких как будезонид. Напротив, частицы, отложившиеся в лишенных ресничного эпителия полостях, таких как альвеолы, имеют гораздо более длительные периоды нахождения. Поскольку очень трудно получить очень маленькие частицы будезонида для глубокого отложения в легких, большая часть суспензии после ингаляции, вероятно, была бы обнаружена в дыхательных путях от верхних до средних. Однако гораздо легче получить мелкие капельки из раствора, чем из суспензии твердых веществ. По этим причинам, распыление содержащего будезонид раствора должно быть предпочтительнее, чем распыление суспензии.
O'Riordan (Respiratory Care (2002 Nov), 47(11), 1305-1313) указывает, что препараты можно доставить распылением или растворов, или суспензий, но что в целом распыление раствора предпочтительнее, чем распыление суспензии. Он указывает, что ультразвуковые распылители не следует использовать на суспензиях и их следует использовать только на растворах.
O'Callaghan (Thorax (1990), 45, 109-111), Storr et al. (Arch Dis. Child (1986), 61, 270-273) и Webb et al. (Arch. Dis. Child (1986), 61, 1108-1110) предполагают, что распыление растворов кортикостероидов (в частности, беклометазона) может быть предпочтительнее, чем суспензий, потому что последнее может быть неэффективным, если распыленные частицы слишком велики для попадания в легкие в терапевтически эффективных количествах. Однако данные, представленные O'Callaghan (J. Pharm. Pharmacol. (2002), 54, 565-569) по распылению раствора в сравнении с суспензией флунисолида, показали, что оба функционировали одинаково. Поэтому нельзя обобщенно утверждать, что распыление раствора предпочтительнее, чем распыление суспензии.
Лечение с использованием распылителя в настоящее время сфокусировано на введении более высоких концентраций препарата, использовании раствора, предпочтительно, по возможности, преимущественно растворов на водной основе, в предпочтение не водным или спиртовым не водным спиртовым растворам или суспензиям, минимизации времени лечения, синхронизации распыления с ингаляцией и введении более мелких капелек для отложения препарата глубже в легких.
Содержащие кортикостероиды растворы для распыления известны. Существует ряд различных путей для получения растворов в целях распыления. Их в целом получали добавлением совместного растворителя, поверхностно-активного агента или буфера. Однако совместные растворители, такие как этанол, полиэтиленгликоль и пропиленгликоль, переносятся только в небольших количествах при введении ингаляцией вследствие раздражения дыхательных путей. Существуют пределы для приемлемых уровней этих совместных растворителей в ингаляционных продуктах. Обычно совместные растворители составляют менее чем примерно 35% мас. распыленной композиции, хотя эти пределы определяет общая доза совместного растворителя, а также его концентрация. Пределы устанавливаются склонностью этих растворителей или вызывать местное раздражение легочной ткани, образовывать гиперосмотические растворы, которые притягивали бы жидкость в легкие, и/или вызывать интоксикацию у пациента. Кроме того, большинство потенциальных гидрофобных терапевтических средств недостаточно растворимы в этих смесях совместных растворителей.
Saidi et al. (патент США № 6241969) описывают получение содержащих кортикостероиды растворов для интраназальной и легочной доставки. Растворенные кортикостероиды присутствуют в концентрированной, по существу не водной форме для хранения или в разведенной форме на водной основе для введения.
Lintz et al. (AAPS Annual Meeting and Exposition, 2004) описывают получение жидких препаративных форм, содержащих будезонид, воду, цитрат, хлорид натрия и спирт, пропиленгликоль и/или поверхностно-активный агент, такой как Tween, Pluronic, или фосфолипиды с величинами HLB от 10 до 20.
Подходом, альтернативным введению PULMICORTTM, является введение липосомной препаративной формы. Waldrep et al. (J. Aerosol Med. (1994), 7(2), 135-145) сообщили об успешном получении липосомной препаративной формы будезонида и производных фосфатидилхолина.
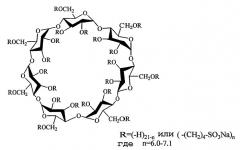
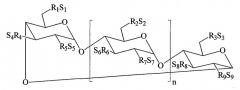
Солюбилизация препаратов циклодекстринами и их производными хорошо известна. Циклодекстрины представляют собой циклические углеводороды, полученные из крахмала. Немодифицированные циклодекстрины отличаются количеством глюкопиранозных единиц, соединенных вместе в цилиндрическую структуру. Материнские циклодекстрины содержат 6, 7 или 8 глюкопиранозных единиц и именуются соответственно α-, β- и γ-циклодекстрином. Каждая субъединица циклодекстрина имеет вторичные гидроксильные группы во 2 и 3 положениях и первичную гидроксильную группу в 6 положении. Циклодекстрины можно изобразить в виде полых, усеченных конусов с гидрофильными наружными поверхностями и гидрофобными внутренними полостями. В водных растворах эти гидрофобные полости обеспечивают приют для гидрофобных органических соединений, которые могут всей или частью их структуры помещаться в эти полости. Этот процесс, известный как образование комплексов включением, может привести к увеличенной видимой водной растворимости и устойчивости для комплексованного препарата. Комплекс стабилизируется гидрофобными взаимодействиями и не участвует в образовании каких-либо ковалентных связей.
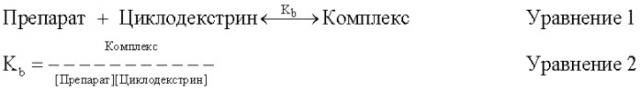
Этот динамический и обратимый процесс обеспечения равновесия можно описать уравнениями 1 и 2, где количество в комплексованной форме является функцией концентраций препарата и циклодекстрина, и равновесие или константа связывания, Kb. Когда препаративные формы циклодекстрина вводятся инъекцией в поток крови, комплекс быстро диссоциируется вследствие воздействий разведения и неспецифического связывания препарата с кровью и тканевыми компонентами.
Константы связывания циклодекстрина и активного агента можно определить методикой равновесия растворимости (T. Higuchi et al. in "Advances in Analytical Chemistry and Instrumentation, Vol. 4; C.N. Reilly ed.; John Wiley & Sons, Inc, 1965, pp. 117-212). В целом, чем выше концентрация циклодекстрина, тем больше процесс равновесия уравнений 1 и 2 сдвигается в сторону образования большего количества комплексов, означая, что концентрация свободного препарата в целом снижается увеличением концентрации циклодекстрина в растворе.
Известно, что недериватизированные, материнские циклодекстрины взаимодействуют с тканями человека и экстрагируют холестерин и другие компоненты мембран, в частности, после накопления в клетках почечных канальцев, приводя к токсическим и иногда фатальным воздействиям на почки.
Материнские циклодекстрины часто проявляют различающийся аффинитет к любому данному субстрату. Например, γ-циклодекстрин часто образует комплексы с ограниченной растворимостью, что приводит к кривым растворимости типа Bs. Это поведение известно для большого количества стероидов, что создает серьезные ограничения в отношении использования γ-циклодекстрина (γ-CD) в жидких препаратах, однако, β-циклодекстрин (β-CD) не достаточно комплексуется с хозяином, относящимся к различным классам соединений. Для β-CD и γ-CD было показано, что дериватизация, например алкилирование, приводит не только к лучшей растворимости производных в воде, по сравнению с материнским CD, но также изменяет тип кривых растворимости от ограничивающего типа Bs к более линейному кривой типа А (Bernd W. Muller and Ulrich Brauns, "Change of Phase-Solubility Behavior by Gamma-Cyclodextrin Derivatization", Pharmaceutical Research (1985) p 309-310).
Химическая модификация материнских циклодекстринов (обычно в положении гидроксилов) привела к получению производных с улучшенной безопасностью, в то же самое время сохраняя или улучшая способность к образованию комплексов. Из многочисленных дериватизированных циклодекстринов, полученных к настоящему времени, только 2 представляются коммерчески жизнеспособными: производные 2-гидроксипропила (HP-CD; нейтральные циклодекстрины, промышленно разрабатываемые Janssen и другими) и производные простого сульфоалкилового эфира, такие как простой сульфобутиловый эфир (SBE-CD; анионные циклодекстрины, разрабатываемые CyDex, Inc.).
Простой сульфобутиловый эфир-β-циклодекстрин (Captisol®)
Однако HP-β-CD все еще обладает токсичностью, которой нет у SBE-CD.
Патенты США № 5376645 и № 5134127, Stella et al., патент США № 3426011, Parmerter et al., Lammers et al. (Reel. Trav. Chim. Pays-Bas (1972), 91(6), 733-742); Staerke (1971), 23(5), 167-171), и Qu et al. (J. Inclusion Phenom. Macro. Chem. (2002), 43, 213-221) раскрывают дериватизированные простым сульфоалкиловым эфиром циклодекстрины. Эти ссылки свидетельствуют о том, что SAE-CD должен подходить для солюбилизации широкого диапазона различных соединений. Однако имеется много исключений, где SAE-CD меньше подходит для солюбилизации соединений, чем HP-β-CD, DM-β-CD, β-CD или γ-CD.
Сульфобутиловые эфирные производные бета-циклодекстрина (SBE-β-CD), в частности производное в среднем примерно с 7 заместителями на молекулу циклодекстрина (SBE7-β-CD), было внедрено в промышленное производство CyDex, Inc. в виде CAPTISOL®. Анионное сульфобутиловое эфирное производное резко улучшает растворение в воде материнского циклодекстрина. Кроме того, присутствие зарядов уменьшает способность молекулы образовывать комплексы с холестерином, по сравнению с гидроксипропиловым производным. Обратимое, не ковалентное образование комплексов препаратов с циклодекстрином CAPTISOL® в целом обеспечивает возможность повышенной растворимости препаратов в водных растворах. Хотя CAPTISOL® представляет собой относительно новый, но известный циклодекстрин, его использование при получении содержащих кортикостероиды растворов для распыления ранее не оценивалось.
Гемолитические анализы в целом используются в области парентеральных препаративных форм для прогнозирования того, вероятна или нет непригодность конкретной препаративной формы для инъекции в поток крови субъекта. Если тестируемая препаративная форма вызывает значительное количество гемолиза, то эта препаративная форма в целом должна считаться неподходящей для введения субъекту. В целом, ожидается, что более высокая осмоляльность связана с более высоким гемолитическим потенциалом. Как изображено на фиг.1 (Thomson, D.O., Critical Reviews in Therapeutic Drug Carrier Systems (1997), 14(1), 1-104), гемолитическое поведение CAPTISOL® сравнивается с гемолитическим поведением материнского β-циклодекстрина, имеющихся в продаже производных гидроксипропила, циклодекстрина ENCAPSINTM (степень замещения ~ 3-4) и циклодекстрина MOLECUSOL® (степень замещения ~ 7-8) и двух других сульфобутиловых эфирных производных, SBE1-β-CD и SBE4-β-CD. В отличие от других производных циклодекстрина сульфоалкиловые эфирные производные, сульфобутиловые эфирные (SAE-CD) производные, в частности, такие как CAPTISOL® (степень замещения - 7) и SBE4-β-CD (степень замещения - 4), по существу не проявляют гемолитического поведения в течение периода времени наблюдения и проявляют по существу более низкий повреждающий мембрану потенциал, чем имеющиеся в продаже гидроксипропиловые производные в концентрациях, обычно используемых для солюбилизации фармацевтических препаративных форм. Диапазон концентраций, изображенный на чертеже (см. источник выше), включает концентрации, обычно используемые для солюбилизации фармацевтических препаративных форм при первоначальном разбавлении в потоке крови после инъекции. После орального введения SAE-CD не подвергается значительному системному всасыванию.
Осмоляльность препаративной формы в целом связана с гемолитическим потенциалом: чем выше осмоляльность (или чем более гипертоничен раствор), тем больше гемолитический потенциал. Zannou et al. ("Osmotic properties of sulfobutyl ether and hydroxypropyl cyclodextrins", Pharma. Res. (2001), 18(8), 1226-1231) сравнили осмоляльность растворов, содержащих SBE-CD и HP-CD. Как изображено на фиг.2, растворы, содержащие SBE-CD, имеют большую осмоляльность, чем растворы, содержащие HP-CD, включающие аналогичные концентрации производного циклодекстрина. Таким образом, удивительно, что SAE-CD проявляет более низкий гемолиз, чем HP-CD в эквивалентных концентрациях, даже хотя HP-CD имеет более низкую осмоляльность.
Были получены метилированные циклодекстрины и оценен их гемолитический эффект на человеческие эритроциты. Было обнаружено, что эти циклодекстрины вызывают гемолиз от умеренного до тяжелого (Jodal et al., Proc. 4 th Int. Symp. Cyclodextrins (1988), 421-425; Yoshida et al., Int. J. Pharm. (1988), 46(3), 217-222).
Введение циклодекстринов в легкие млекопитающего может быть неприемлемым. Действительно, существует литература по потенциалу или наблюдаемой токсичности нативных циклодекстринов и производных циклодекстрина. В химическом каталоге NTP указано, что α-циклодекстрин может быть вреден при ингаляции. Nimbalkar et al. (Biotechnol. Appl. Biochem. (2001), 33, 123-125) предостерегают против легочного применения комплекса HP-β-CD/диацетилдапсона вследствие его первоначального эффекта задержки клеточного роста легочных клеток.
Даже при этом сообщалось о ряде исследований относительно использования циклодекстринов для ингаляции, хотя ни один из них не был доведен до промышленного производства. Эти исследования свидетельствуют о том, что для специфических оптимальных или даже полезных ингаляционных или интраназальных препаративных форм потребуются различные комбинации препарата - циклодекстрина. Предпринимались попытки разработки содержащих циклодекстрин порошков и растворов для буккальной, легочной и/или интраназальной доставки.
В патенте США № 5914122, выданном Otterbeck et al., раскрыто получение устойчивых содержащих будезонид растворов для распыления. Они демонстрируют предпочтительное использование циклодекстрина, такого как β-CD, γ-CD или HP-β-CD, и/или EDTA (этилендиаминтетрауксусная кислота) в качестве стабилизатора. Циклодекстрин также предложен в качестве солюбилизатора для увеличения концентрации будезонида в растворе. В любом случае самый большой химический срок хранения для любой из их препаративных форм, с точки зрения приемлемого удерживании активного ингредиента, о котором они сообщают, составляет лишь от 3 до 6 мес.
Публикация № 20020055496 перед выдачей патента США McCoy et al. раскрывает по существу неводные, вводимые орально препаративные формы, содержащие HP-β-CD. Препаративные формы можно вводить с помощью аэрозоля, распылительного насоса или газа-вытеснителя.
В патенте России № 2180217, выданном Чучалину, раскрыт устойчивый, содержащий будезонид раствор для ингаляции. Раствор включает будезонид, пропиленгликоль, поли(этиленоксид), янтарную кислоту, трилон B, нипазол, тиомочевину, воду и необязательно HP-β-CD.
В публикации Muller et al. (Proceed. Int'l. Symp. Control. Rel. Bioact. Mater. (1997), 24, 69-70) описаны результаты исследования по получению микрочастиц будезонида ASES (аэрозольной системой экстракции растворителя), сверхкритического процесса с использованием двуокиси углерода, для использования в ингаляторе сухого порошка. HP-β-CD предложен в качестве носителя для порошка.
Muller et al. (патент США № 6407079) раскрывает фармацевтические композиции, содержащие HP-β-CD. Они свидетельствуют, что интраназальное введение раствора, содержащего циклодекстрин, возможно.
В данной области признано, что может быть необходимо оценить структурно связанные варианты определенного типа производного циклодекстрина для оптимизации связывания конкретного соединения с этим типом производного циклодекстрина. Однако часто бывает, что нет крайних различий в связывании конкретного соединения с первым вариантом осуществления, по сравнению со вторым вариантом осуществления конкретного производного циклодекстрина. Например, нечасты случаи, когда имеются крайние различия связывания определенного терапевтического средства с первым производным циклодекстрина, в сравнении со структурно связанным вторым производным циклодекстрина. Когда такие ситуации существуют, они являются неожиданными. Worth et al. (24 th International Symposium on Controlled Release of Bioactive Materials (1997)) описывают результаты исследования, оценивающего возможность использования комплексов стероида/циклодекстрина для легочной доставки. При параллельном сравнении β-CD, SBE7-β-CD и HP-β-CD оценивали в соответствии с их способностью образовывать комплексы включения с беклометазондипропионатом (BDP) и его активным метаболитом беклометазонмонопропионатом (BMP). BMP легче солюбилизировался циклодекстрином, и наблюдавшийся порядок способности к солюбилизации был следующий: HP-β-CD (самая большая) > β-CD > SBE7-β-CD. Таким образом, специалист в данной области мог бы ожидать, что производные SAE-CD не очень подходят для использования при солюбилизации таких кортикостероидов, как BMP или BDP. Хотя не были раскрыты результаты, относящиеся к действительной возможности использования в ингаляционных препаративных формах, они свидетельствуют о том, что BMP, а не BDP мог бы быть лучшей альтернативой для разработки распыляемого раствора.
Kinnarinen et al. (11th International Symposium CD (2002), представляют результаты исследования отложения в легких in vitro комплекса включения будезонида/γ-CD для ингаляции сухого порошка. При образовании комплексов с γ-CD преимущество не наблюдалось. Соответственно, с точки зрения солюбилизации кортикостероида, специалист в данной области не мог ожидать никакого преимущества при получении растворимого в воде производного γ-CD. Vozone et al. (11th International Symposium CD (2002)) представляют результаты исследования образования комплекса будезонида с γ-циклодекстрином для использовании при ингаляции сухого порошка. Различия в пределах испускаемых доз комплекса циклодекстрина или физической смеси будезонида и CD не наблюдались. Но различие, наблюдавшееся во фракции мелких частиц обеих препаративных форм, свидетельствовало о том, что использование комплекса циклодекстрина для доставки препарата в легкие может увеличить вдыхаемую фракцию сухого порошка.
Pinto et al. (S.T.P. Pharma Sciences (1999), 9(3), 253-256) описывают результаты исследования по применению HP-β-CD в ингаляционной препаративной форме сухого порошка для беклометазона. HP-β-CD оценивали в виде комплекса или физической смеси с препаратом в исследовании отложения in vitro дозы, подаваемой из ингаляционного устройства MICRO-HALERTM. По сообщениям, количество вдыхаемой фракции препарата было самым высоким при комплексе и самым низким при одном микронизированном препарате.
Rajewski et al. (J. Pharm. Sci. (1996), 85(11), 1142-1169) предоставляют обзор фармацевтических видов применения циклодекстринов. В этом обзоре они приводят исследования, оценивающие использование комплексов циклодекстрина в ингаляционных системах сухого порошка.
Shao et al (Eur. J. Pharm. Biopharm. (1994), 40, 283-288) сообщили об эффективности циклодекстринов в качестве средств, содействующих легочному всасыванию. По данным фармакодинамики, оценивали относительную эффективность циклодекстринов в плане увеличения легочного всасывания инсулина, и относительная эффективность располагалась по ранжиру следующим образом: диметил-β-циклодекстрин > α-циклодекстрин > β-циклодекстрин > γ-циклодекстрин > гидроксипропил-β-циклодекстрин. В связи с этим сообщением специалист в данной области мог бы ожидать, что растворимое в воде производное γ-CD меньше подходит для доставки соединений посредством ингаляции, чем соответствующее производное β-CD, потому что не дериватизированный β-CD больше подходит, чем не дериватизированный γ-CD.
Williams et al. (Eur. J. Pharm. Biopharm. (1999 Mar), 47(2), 145-52) сообщили о результатах исследования по определению влияния методики составления препаративной формы для 2-гидроксипропил-бета-циклодекстрина (HP-β-CD) на устойчивость в ингаляторе (pMDI), содержащем под повышенным давлением отмеренную дозу аспирина в препаративной форме на основе суспензии, содержащей вытеснитель гидрофторалкан (HFA). HP-β-CD был помещен в pMDI в виде лиофилизированного комплекса включения или физической смеси с аспирином. Аспирин в лиофилизированном комплексе включения проявлял самую значительную степень молекулярной деградации во время 6-месячного хранения, хотя один аспирин демонстрировал в pMDI умеренную степень молекулярной деградации. Аспирин, составленный в физическую смесь, проявлял самую низкую степень молекулярной деградации. По сообщениям, HP-β-CD можно использовать для повышения устойчивости химически лабильного препарата, но на устойчивость препарата может воздействовать способ получения препаративной формы.
Gudmundsdottir et al. (Pharmazie (2001 Dec), 56(12), 963-6) описывают результаты исследования, в котором мидазолам был включен в препаративную форму в виде водного буферного раствора сульфобутилэфира-β-циклодекстрина. Интраназальный аэрозоль испытывали у здоровых добровольцев и сравнивали с внутривенно вводимым мидазоламом в открытом перекрестном испытании. По сообщению, интраназальная препаративная форма приближается к внутривенной форме по скорости всасывания, концентрации в сыворотке и клиническому седативному эффекту. Серьезные побочные эффекты не наблюдались.
Srichana et al. (Respir. Med. (2001 Jun), 95(6), 513-9) сообщают о результатах исследования по разработке нового носителя в аэрозолях сухого порошка. Были выбраны 2 типа циклодекстрина: гамма циклодекстрин (γ-CD) и диметил-бета-циклодекстрин (DMCD) в качестве носителей в препаративных формах в виде сухого порошка. Сальбутамол использовали в качестве модельного препарата, и была включена контрольная препаративная форма, содержащая лактозу и препарат. Для оценки эффективности доставки этих препаративных форм в виде сухого порошка использовали двухэтапный импинжер (TSI). По полученным результатам было обнаружено, что препаративная форма, содержащая γ-CD, доставляла препарат на нижнюю стадию TSI (отложение = 65%) гораздо больше, чем обе препаративные формы, содержащие DMCD (50%) и контрольная препаративная форма (40%) (P<0,05). Гемолиз эритроцитов, инкубированных с комплексом DMCD, был выше, чем гемолиз, полученный в комплексе γ-CD. Высвобождение препарата в обеих препаративных формах, содержащих γ-CD и DMCD, было быстрым (более 70% высвобождалось через 5 мин, и почти весь препарат высвобождался в пределах 30 мин.
Van der Kuy et al. (Eur. J. Clin. Pharmacol. (1999 Nov), 55(9), 677-80) сообщают результаты исследования фармакокинетических свойств двух интраназальных препаратов препаративной формы, содержащей дигидроэрготаманмесилат (DHEM), с использованием имеющегося в продаже интраназального препарата. Эти препаративные формы также содержали случайно метилированный β-циклодекстрин (RAMEB). Статистически значимые различия максимальной концентрации в плазме (Cmax), времени до достижения Cmax (tmax), площади под кривой динамики во времени концентрации в плазме (AUC0-8 ч) и Cmax/AUC (t=8 ч) у трех интраназальных препаратов не были обнаружены. Результаты указывают на то, что фармакокинетические свойства интраназальных препаратов значимо не отличаются от имеющегося в продаже интраназального аэрозоля.
Патенты США № 5942251 и 5756483, выданные Merkus, охватывают фармацевтические композиции для интраназального введения дигидроэрготамана, апоморфина и морфина, включающие один из этих фармацевтически активных ингредиентов в комбинации с циклодекстрином и/или дисахаридом и/или полисахаридом и/или сахарным спиртом.
В патенте США № 5955454 раскрыт фармацевтический препарат, подходящий для интраназального введения, содержащий прогестоген и метилированный β-циклодекстрин, имеющий степень замещения от 0,5 до 3,0.
В патенте США № 5977070, выданном Piaza et al., раскрыта фармацевтическая композиция для интраназальной доставки соединений, полезных для лечения остеопороза, включающая эффективное количество физиологически активного усеченного аналога PTH или PTHrp или его соль и усилитель всасывания, выбранный из группы, состоящей из диметил-β-циклодекстрина.
В патенте США № 6436902, выданном Backstrom et al., раскрыты композиции и способы легочного введения паратиреоидного гормона в форме сухого порошка, подходящего для ингаляции, в котором, по меньшей мере, 50% сухого порошка состоит из (а) частиц, имеющих диаметр до 10 мкм, или (b) агломератов таких частиц. Устройство ингалятора сухого порошка содержит препарат, состоящий из сухого порошка, включающего (i) паратиреодиный гормон (PTH) и (ii) вещество, которое усиливает всасывание РТН в нижние дыхательные пути, где, по меньшей мере, 50% (i) и (ii) состоит из первичных частиц, имеющих диаметр до 10 мкм, и где вещество выбрано из группы, состоящей из соли жирной кислоты, желчной соли или его производного, фосфолипида и циклодекстрина или его производного.
В патенте США № 6518239, выданном Kuo et al., раскрыта диспергируемая аэрозольная препаративная форма, включающая активный агент и дипептид или трипептид для аэрозольного введения в легкие. По сообщениям, композиции могут также включать полимерные наполнители/добавки, например поливинилпирролидоны, дериватизированные целлюлозы, такие как гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза и гидроксипропилметилцеллюлоза, фиколлы (полимерный сахар), гидроксиэтилкрахмал, декстраты (например, циклодекстрины, такие как 2-гидроксипропил-β-циклодекстрин и сульфобутилэфир-β-циклодекстрин), полиэтиленгликоли и пектин.
Nakate et al. (Eur. J. Pharm. Biopharm. (2003 Mar), 55(2), 147-54) описывают результаты исследования для определения улучшения легочного всасывания циклопептида FK224 (с низкой растворимостью в воде) у крыс совместным включением его в препаративную форму с бета-циклодекстрином. Целью исследования было изучение воздействия легочной доставки на системное всасывание FK224, в сравнении с другими путями введения, и определение биологической доступности (ВА) FK224 после легочного введения у крыс с использованием различных лекарственных форм. После введения водной суспензии биологическая доступность снизилась до 2,7%, по сравнению с 16,8% для раствора. Однако было обнаружено, что β-циклодекстрин (β-CD)является эффективной добавкой, что касается улучшения растворимости FK224. Биологическая доступность водной суспензии, содержащей β-CD, увеличилась до 19,2%. Наблюдалось, что и C(max), и AUC FK224 увеличивались по мере увеличения количества β-CD. Профили в плазме показали пролонгированное всасывание. Они свидетельствуют о том, что β-CD представляет собой крайне эффективную добавку, что касается улучшения