Дозированная форма немедленного высвобождения, содержащая оболочку с отверстиями
Иллюстрации
Показать всеДозированная (лекарственная) форма немедленного высвобождения содержит, по меньшей мере, один активный ингредиент, имеет твердое ядро и оболочку. Оболочка окружает, по меньшей мере, часть ядра. Ядро имеет плотность около 0,9 г/см3 и пористость менее 40%. Оболочка дозированной формы содержит одно или более отверстий и легко растворима в гастроинтестинальных жидкостях. Дозированная форма по изобретению обеспечивает немедленное высвобождение активного ингредиента после соприкосновения с жидкой средой желудочно-кишечного тракта, сводит к минимуму воздействие на ядро окружающей среды в ротовой полости и увеличивает воздействие растворяющей среды на ядро. 16 з.п. ф-лы, 20 ил.
Реферат
Перекрестная ссылка на родственные заявки
Настоящая заявка представляет собой частичное продолжение совместно рассматриваемой заявки 10/393610, поданной 21 марта 2003 г., которая представляет собой частичное продолжение заявок PCT №№ PCT/US 02/31129, поданной 28 сентября 2002 г.; PCT/US 02/31117, поданной 28 сентября 2002 г.; PCT/US 02/31062, поданной 28 сентября 2002 г.; PCT/US02/31024, поданной 28 сентября 2002 г., и PCT/US 02/31163, поданной 28 сентября 2002 г., которые представляют собой частичные продолжения любой из заявок USSN 09/966939, поданной 28 сентября 2001 г.; USSN 09/966509, поданной 28 сентября 2001 г.; USSN 09/966497, поданной 28 сентября 2001 г.; USSN 09/967414, поданной 28 сентября 2001 г., и USSN 09/966450, поданной 28 сентября, раскрытие сущности каждой из всех перечисленных выше заявок включено сюда во всей полноте посредством ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к дозированной (лекарственной) форме, обеспечивающей немедленное высвобождение активного ингредиента. Дозированная форма состоит из твердого ядра и окружающей ядро оболочки. В оболочке содержится одно или более отверстий.
Уровень техники
Известны некоторые дозированные формы с отверстиями или просечками. Например, в данной области известны дозированные формы с «осмотическим насосом» для введения фармацевтически активных ингредиентов. Обычно они содержат полупроницаемую стенку (оболочку), которая окружает емкость с дозированным препаратом. Стенка является проницаемой для прохождения наружной жидкости, непроницаема для прохождения дозированного препарата и имеет канал в полупроницаемой стенке для доставки дозированного препарата из осмотической системы. Например, в патенте США №4576604 описано осмотическое устройство, содержащее отделение для дозированного препарата, окруженное оболочкой (покрытием), в которой имеется канал. В оболочке может содержаться немедленно высвобождаемая доза дозированного препарата, а во внутреннем отделении для дозированного препарата может содержаться пролонгированно высвобождаемая доза дозированного препарата.
В патенте США №4449983 описано еще одно осмотическое устройство, содержащее два помещенных по отдельности дозированных препарата, которые высвобождаются из устройства по отдельности. Устройство содержит два отделения, по одному для каждого дозированного препарата, разделенные перегородкой. Каждое отделение имеет канал, сообщающийся с наружной стороной устройства.
В патенте США №3823816 описана водорастворимая упаковка в форме капсулы с твердой оболочкой, наполненной порошком, гранулами или т.п. Капсула снабжена отверстиями, а отверстия закрыты водорастворимой защитной пленкой. Пленка является более водорастворимой, чем капсула для того, чтобы, когда упаковка соприкасается с водой, сначала, быстрее чем капсула, растворялась пленка, и таким образом содержимое капсулы подвергалось растворению и/или высвобождению через отверстия, в то время как сама капсула остается нетронутой.
Патент США №5256440 относится к дозированной форме с насечками, содержащей на своей поверхности одну или более очерченных областей. Дозированная форма представляет собой мелкие капли (аэрозоль), покрытые латексным полимером. При размещении в среде для применения латексное покрытие внутри очерченной области удаляется с воспроизводимым результатом, покидая таблетку с покрытым ядром и с заранее определенным отверстием, через которое дискретная часть поверхности ядра подвергается воздействию среды применения.
Один из известных способов получения дозированных форм с желатиновым покрытием основан на способе глазирования, в котором две отдельные пленки, изготовленные из желатинового материала, наносят на противоположные стороны таблетки с помощью пары ротационных матриц, как описано, например, в патентах США №№5146730 и 5459983. В состав пленок для получения гелевых капсул и таблеток с гелевым покрытием, получаемых с помощью способов глазирования, таких как способы, описанные в патентах США №№5146730 и 5459983, обычно входит основанная на воде желатиновая композиция, содержащая приблизительно 45% желатина и приблизительно 9% пластификатора (глицерина и/или сорбита) по массе. Глицерин и сорбит можно применять в виде взятых по отдельности пластификаторов или в сочетании друг с другом. Кроме того, в качестве добавок и пластификаторов можно применять другие сахара и полигидроксисоединения. Если требуемым конечным изделием является медицинская таблетка с защитным желатиновым покрытием, отношение пластификатора к желатину в желатиновой композиции должно находиться в диапазоне приблизительно 1:5.
Еще один традиционный способ формования оболочки (или покрытия) на ядре (или субстрате) представляет собой способ, описанный в заявке WO 01/57144, в котором для формования покрытия используются принципы электростатического осаждения. По меньшей мере, либо ядро, либо оболочка предпочтительно включает в себя один или более «регуляторов заряда», таких как салицилаты металлов, например, салицилат цинка, салицилат магния и салицилат кальция; четвертичные аммониевые соли; хлорид бензалкония; хлорид бензетония; бромид триметилтетрадециламмония (цетримид); и циклодекстрины и их аддукты в количестве приблизительно от 1% до приблизительно 10 мас.% от массы оболочки.
Теперь заявители обнаружили, что можно приготовить дозированную форму немедленного высвобождения, состоящую из твердого ядра и окружающей ядро оболочки, в которой ядро имеет плотность, по меньшей мере, приблизительно 0,9 г/см3 и процент пористости менее 40%, предпочтительно менее 35%, наиболее предпочтительно 30%. Оболочка содержит одно или более отверстий и легко растворима в гастроинтестинальных жидкостях. Оболочку предпочтительно наносят на ядро путем глазирования.
Раскрытие изобретения
В настоящем изобретении предлагается дозированная форма, содержащая, по меньшей мере, один активный ингредиент, которая включает ядро и окружающую ядро оболочку, где ядро имеет плотность, по меньшей мере, приблизительно 0,9 г/см3 и процент пористости менее 40%, предпочтительно менее 35%, наиболее предпочтительно 30%, оболочка содержит одно или более отверстий, оболочка легко растворима в гастроинтестинальных жидкостях, и, после соприкосновения дозированной формы с жидкой средой, дозированная форма обеспечивает немедленное высвобождение, по меньшей мере, одного активного ингредиента.
В изобретении также предлагается дозированная форма, содержащая ядро, имеющее внешнюю поверхность, и оболочку, имеющую внешнюю и внутреннюю поверхности, в которой, по меньшей мере, часть оболочки окружает ядро таким образом, что внутренняя поверхность оболочки в основном плотно прилегает к внешней поверхности ядра; по меньшей мере, часть оболочки содержит одно или более отверстий; размер одного или более отверстий составляет приблизительно от 200 до приблизительно 2000 мкм (микрон) в диаметре или в ширину; по меньшей мере, часть оболочки легко растворима в гастроинтестинальных жидкостях; средняя толщина оболочки находится в диапазоне приблизительно от 100 до приблизительно 400 микрон; оболочка содержит приблизительно менее 50% кристаллизующегося сахара; дозированная форма в значительной степени не содержит регуляторов заряда, и после соприкосновения дозированной формы с жидкой средой дозированная форма обеспечивает немедленное высвобождение, по меньшей мере, одного активного ингредиента.
Краткое описание чертежей
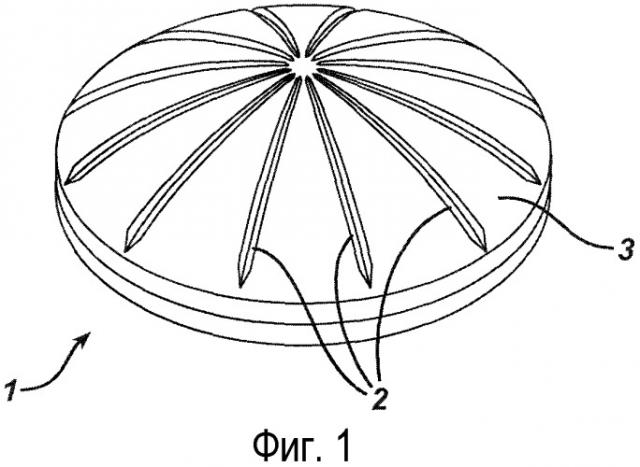
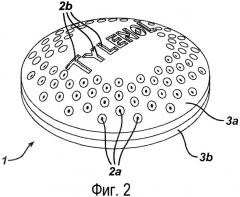
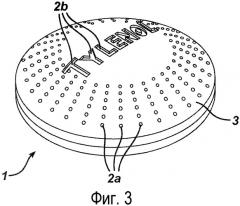
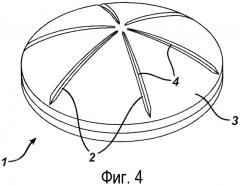
На фигурах 1-5 показаны дозированные формы согласно изобретению.
На фигуре 6 показан один из вариантов осуществления изобретения с отверстиями согласно изобретению.
На фигуре 7 показан способ получения дозированной формы согласно изобретению с помощью способа глазирования.
На фигуре 8 показан еще один способ получения дозированной формы согласно изобретению с помощью способа глазирования.
На фигуре 9 показан дополнительный способ получения дозированной формы согласно изобретению с помощью способа глазирования.
На фигуре 10 показан способ получения дозированной формы согласно изобретению с капсулой, содержащей отверстия, с помощью способа глазирования.
На фигуре 11 показан способ получения дозированной формы согласно изобретению с помощью способа нанесения покрытия путем погружения.
На фигуре 12 показан еще один способ получения дозированной формы согласно изобретению с помощью способа нанесения покрытия путем погружения.
На фигуре 13 показан способ получения дозированной формы согласно изобретению с помощью трансферного способа.
На фигуре 14 показан способ получения отверстия в оболочке дозированной формы согласно изобретению с помощью устройства для шлифования.
На фигурах 15A и 15B показан один из способов получения отверстий в оболочке дозированной формы согласно изобретению с помощью горячих иголок.
На фигурах 16A и 16B показан один из способов получения отверстий в оболочке дозированной формы согласно изобретению с помощью устройства для продавливания.
На фигурах 17А и 17B показан способ получения отверстий в оболочке дозированной формы согласно изобретению путем литьевого формования.
Осуществление изобретения
Применяемый здесь термин «дозированная форма» относится к любому твердому объекту, полутвердой или жидкой композиции, предназначенных для того, чтобы содержать в себе конкретное, заранее заданное количество (дозу) определенного ингредиента, например, активного ингредиента, как указано ниже. Подходящие дозированные формы могут представлять собой системы доставки фармацевтического дозированного препарата, включая системы для перорального введения, трансбуккального введения, ректального введения, системы локальной доставки или доставки через слизистые оболочки, или подкожные имплантаты, или другие имплантируемые системы доставки дозированного препарата; или композиции для доставки минеральных веществ, витаминов и других нутрицевтиков, средств для ухода за полостью рта, корригентов и т.п. Считается, что дозированные формы согласно настоящему изобретению предпочтительно являются твердыми, однако они могут содержать жидкие или полутвердые компоненты. В частности, в предпочтительном варианте осуществления изобретения дозированная форма представляет собой систему для перорального введения, предназначенную для доставки фармацевтически активного ингредиента в желудочно-кишечный тракт человека.
Подходящие для использования в настоящем изобретении активные ингредиенты включают в себя, например, фармацевтические препараты, минеральные вещества, витамины и другие нутрицевтики; средства для ухода за полостью рта, корригенты и их смеси. Подходящие фармацевтические препараты включают в себя анальгетики, противовоспалительные средства, средства против артрита, анестезирующие средства, антигистаминные средства, средства против кашля, антибиотики, противоинфекционные средства, противовирусные средства, антикоагулянты, антидепрессанты, противодиабетические средства, противорвотные средства, антифлатуленты, противогрибковые средства, антиспазматические средства, препараты для подавления аппетита, бронхолитические средства, сердечно-сосудистые препараты, средства для центральной нервной системы, стимуляторы центральной нервной системы, противоотечные средства, пероральные контрацептивы, диуретические средства, отхаркивающие средства, гастроинтестинальные средства, препараты против мигрени, средства против укачивания в транспорте, муколитические средства, мышечные релаксанты, препараты против остеопороза, полидиметилсилоксаны, респираторные средства, вспомогательные средства для сна, средства для лечения мочевыводящих путей и их смеси.
Подходящие средства для ухода за полостью рта включают в себя освежитель для полости рта, средства для отбеливания зубов, противомикробные средства, зубные минерализаторы, ингибиторы зубного кариеса, средства для локальной анестезии, защитные средства для слизистой оболочки и т.п.
Подходящие корригенты включают в себя ментол, мятное масло, мятные ароматизаторы, фруктовые ароматизаторы, шоколад, ваниль, ароматизаторы для жевательной резинки, кофейные ароматизаторы, ароматизаторы со вкусом ликера, их сочетания и т.п.
Примеры подходящих гастроинтестинальных средств включают в себя антациды, такие как карбонат кальция, гидроксид магния, оксид магния, карбонат магния, гидроксид алюминия, бикарбонат натрия, карбонат дигидроксиалюминия и натрия; стимулирующие слабительные, такие как бисакодил, крушина, дантрон, сенна, фенолфталеин, алоэ, касторовое масло, рицинолевая кислота и дегидрохолевая кислота и их смеси; антагонисты H2-рецепторов, такие как фамотидин, ранитидин, циметидин, низатидин; ингибиторы протонового насоса, такие как омепразол или ланзопразол; гастроинтестинальные цитопротекторы, такие как сукралфат и мизопростол; гастроинтестинальные прокинетики, такие как прукалоприд, антибиотики против бактерии H.pylori, такие как кларитромицин, амоксициллин, тетрациклин и метронидазол; противодиарейные средства, такие как дифеноксилат и лоперамид; гликопирролаты; противорвотные средства, такие как ондансетрон; анальгетики, такие как месаламин.
В одном из вариантов осуществления изобретения активный ингредиент можно выбрать из бисакодила, фамотидина, ранитидина, циметидина, прукалоприда, дифеноксилата, лоперамида, лактазы, месаламина, висмута (соединений), антацидов и фармацевтически приемлемых солей, их сложных эфиров, изомеров и смесей.
В еще одном варианте осуществления изобретения активный ингредиент выбран из анальгетиков, противовоспалительных средств и жаропонижающих средств, например, из нестероидных противовоспалительных дозированных препаратов (NSAID), включая производные пропионовой кислоты, например, ибупрофен, напроксен, кетопрофен и т.п.; производные уксусной кислоты, например, индометацин, диклофенак, сулиндак, толметин и т.п.; производные фенамовой кислоты, например, мефенамовая кислота, меклофенамовая кислота, флуфенамовая кислота и т.п.; производные бифенилкарбоновых кислот, например, дифлунизал, флуфенизал и т.п.; и оксикамы, например, пироксикам, судоксикам, изоксикам, мелоксикам и т.п. В одном из конкретных вариантов осуществления изобретения активный ингредиент выбран из NSAID-производного пропионовой кислоты, например, ибупрофена, напроксена, флурбипрофена, фенбуфена, фенопрофена, индопрофена, кетопрофена, флупрофена, пирпрофена, карпрофена, оксапрозина, пранопрофена, супрофена и их фармацевтически приемлемых солей, производных и сочетаний. В еще одном конкретном варианте осуществления изобретения активный ингредиент можно выбрать из ацетаминофена, ацетилсалициловой кислоты, ибупрофена, напроксена, кетопрофена, флурбипрофена, диклофенака, циклобензаприна, мелоксикама, рофекоксиба, целекоксиба и их фармацевтически приемлемых солей, сложных эфиров, изомеров и их смесей.
В еще одном варианте осуществления изобретения активный ингредиент можно выбрать из псевдоэфедрина, фенилпропаноламина, хлорфенирамина, декстрометорфана, дифенгидрамина, астемизола, терфенадина, фексофенадина, лоратадина, деслоратадина, цетиризина, их смесей и фармацевтически приемлемых солей, сложных эфиров, изомеров и их смесей.
Примеры подходящих полидиметилсилоксанов, которые включают в себя диметикон и симетикон, но не ограничиваются ими, представляют собой полидиметилсилоксаны, описанные в патентах США №№4906478, 5275822 и 6103260, содержание каждого из которых в прямой форме включено здесь путем ссылки. Применяемый здесь термин «симетикон» относится к более широкому классу полидиметилсилоксанов, включающему симетикон и диметикон, но не ограничивающемуся ими.
Активный ингредиент или ингредиенты присутствуют в дозированной форме в терапевтически эффективном количестве, представляющем собой количество, которое дает необходимую терапевтическую реакцию после перорального введения и которое специалист в данной области может легко определить. Как известно в данной области, при определении таких количеств должны приниматься во внимание конкретный активный ингредиент, который вводится, характеристики биодоступности активного ингредиента, схема приема дозированного препарата, возраст и вес пациента и другие факторы. Обычно дозированная форма содержит, по меньшей мере, приблизительно 1 мас.%, предпочтительно дозированная форма содержит, по меньшей мере, приблизительно 5 мас.%, например, по меньшей мере, приблизительно 25 мас.% комбинации из одного или более активных ингредиентов. В одном из предпочтительных вариантов осуществления изобретения в ядре содержится в общей сложности, по меньшей мере, приблизительно 50 мас.%, например, по меньшей мере, приблизительно 70 мас.%, допустимо, по меньшей мере, приблизительно 80 мас.% (в расчете на массу ядра) одного или более активных ингредиентов.
Активный ингредиент или ингредиенты могут присутствовать в дозированной форме в любом виде. Например, активный ингредиент может быть диспергирован до молекулярного уровня, например, в расплавленном или растворенном состоянии внутри дозированной формы, или может находиться в виде частиц, которые в свою очередь могут иметь покрытие или не иметь покрытия. Если активный ингредиент находится в виде частиц, частицы (либо с покрытием, либо без покрытия) обычно имеют средний размер приблизительно 1-2000 микрон. В одном из предпочтительных вариантов осуществления изобретения такие частицы представляют собой кристаллы со средним размером приблизительно 1-300 микрон. В еще одном предпочтительном варианте осуществления изобретения частицы представляют собой гранулы или крупинки со средним размером приблизительно 50-2000 микрон, предпочтительно приблизительно 50-1000 микрон, наиболее предпочтительно приблизительно 100-800 микрон.
Ядро может представлять собой любую твердую форму. Ядро можно приготовить с помощью любого подходящего способа, включая, например, прессование или формование. Применяемый здесь термин «ядро» относится к материалу, который, по меньшей мере, частично покрыт или окружен еще одним материалом. Предпочтительно ядро представляет собой самостоятельный единый объект, такой как таблетка или капсула. Обычно ядро содержит твердое вещество, например, ядро может представлять собой прессованную или формованную таблетку, жесткую или мягкую капсулу, суппозиторий или кондитерскую форму, такую как пастилка, нуга, карамель, помадка или композиция на основе масла. В некоторых других вариантах осуществления изобретения ядро или его часть может находиться в готовой дозированной форме в полутвердом или жидком виде. Например, ядро может содержать капсулу, заполненную жидкостью или полутвердый материал в виде помадки. В тех вариантах осуществления изобретения, в которых ядро содержит текучий компонент, такой как совокупность гранул или частиц, или жидкость, для содержания текучего материала ядро предпочтительно дополнительно содержит оболочечный компонент, такой как оболочка капсулы или покрытие. В некоторых конкретных вариантах осуществления изобретения, в которых ядро содержит оболочечный компонент, оболочка или части оболочки настоящего изобретения находятся в непосредственном соприкосновении с оболочечным компонентом ядра, который отделяет оболочку от текучего компонента ядра.
В одном из вариантов осуществления изобретения ядро представляет собой прессованную таблетку с твердостью приблизительно от 2 до приблизительно 30 килопонд/см2 (kp/cm2), например, приблизительно от 6 до приблизительно 25 килопонд/см2. «Твердость» представляет собой термин, применяемый в данной области для описания сопротивления поперечному разрушению либо ядра, либо твердой дозированной формы с покрытием, которое измеряют с помощью традиционного испытательного оборудования для измерения твердости фармацевтических препаратов, такого как измеритель твердости Schleuniger Hardness Tester. Для того чтобы сравнить значения для таблеток разного размера в поперечном направлении, сопротивление разрушению должно нормироваться для области разрушения. Такое нормированное значение, выраженное в единицах килопонд/см2, иногда упоминается в данной области как предел прочности таблетки. Общее обсуждение измерения твердости таблеток описано в публикации Leiberman и др., Pharmaceutical Dosage Forms - Tablets, том 2, 2-е издание, Marcel Dekker Inc., 1990, стр.213-217, 327-329.
Ядро может иметь одну из многочисленных различных форм. Например, ядро может иметь форму полиэдра, такого как куб, пирамида, призма или т.п.; или может иметь геометрию пространственной фигуры с несколькими неплоскими поверхностями, такую как конус, усеченный конус, цилиндр, шар, тор или т.п. В некоторых вариантах осуществления изобретения ядро имеет одну или более больших поверхностей. Например, в вариантах осуществления изобретения, в которых ядро представляет собой прессованную таблетку, поверхность ядра обычно имеет две расположенные друг против друга большие поверхности, образованные при контакте с верхней и нижней поверхностями пуансона в машине для прессования. В таких вариантах осуществления изобретения поверхность ядра обычно дополнительно содержит «хомут», расположенный между двумя большими поверхностями и образованный при контакте со стенками матрицы в машине для прессования. Ядро также может содержать многослойную таблетку.
К типичным формам ядер, которые можно использовать, относятся формы таблеток, образуемые в технологических пресс-формах, описанных в руководстве «The Elizabeth Companies Tablet Design Training Manual» (Elizabeth Carbide Die Co., Inc., p.7 (McKeesport, Pa.) (включенном здесь путем ссылки), которые указаны далее (форма таблетки инверсно повторяет форму оснастки для прессования):
1. Форма с неглубокой вогнутостью.
2. Форма со стандартной вогнутостью.
3. Форма с сильной вогнутостью.
4. Форма со сверхсильной вогнутостью.
5. Форма с модифицированной сферической вогнутостью.
6. Форма со стандартной вогнутостью и насечкой, разделяющей форму пополам.
7. Форма со стандартной вогнутостью и двумя насечками, разделяющими форму пополам.
8. Стандартная европейская форма с вогнутостью и насечкой, разделяющей форму пополам.
9. Форма со стандартной вогнутостью и частичной насечкой, разделяющей форму пополам.
10. Форма с удвоенным радиусом.
11. Заостренная форма & вогнутость.
12. Плоская гладкая форма.
13. Форма с плоской поверхностью и фаской (F.F.B.E.).
14. F.F.B.E. с насечкой, разделяющей форму пополам.
15. F.F.B.E. с двумя насечками, разделяющими форму пополам.
16. Круглая форма.
17. Форма с лунками.
18. Форма эллипса.
19. Овальная форма.
20. Форма капсулы.
21. Прямоугольная форма.
22. Квадратная форма.
23. Треугольная форма.
24. Форма шестигранника.
25. Форма пятигранника.
26. Форма восьмигранника.
27. Форма алмаза.
28. Форма, напоминающая острие стрелы.
29. Пулевидная форма.
30. Форма с неглубокой вогнутостью.
31. Форма со стандартной вогнутостью.
32. Форма с сильной вогнутостью.
33. Форма со сверхсильной вогнутостью.
34. Форма с модифицированной сферической вогнутостью.
35. Форма со стандартной вогнутостью и насечкой, разделяющей форму пополам.
36. Форма со стандартной вогнутостью и двумя насечками, разделяющими форму пополам.
37. Стандартная европейская форма с вогнутостью и насечкой, разделяющей форму пополам.
38. Форма со стандартной вогнутостью и частичной насечкой, разделяющей форму пополам.
39. Форма с удвоенным радиусом.
40. Заостренная форма & вогнутость.
41. Плоская гладкая форма.
42. Форма с плоской поверхностью и фаской (F.F.B.E.).
43. F.F.B.E. с насечкой, разделяющей форму пополам.
44. F.F.B.E. с двумя насечками, разделяющими форму пополам.
45. Круглая форма.
46. Форма с лунками.
47. Форма эллипса.
48. Овальная форма.
49. Форма капсулы.
50. Прямоугольная форма.
51. Квадратная форма.
52. Треугольная форма.
53. Форма шестигранника.
54. Форма пятигранника.
55. Форма восьмигранника.
56. Форма алмаза.
57. Форма, напоминающая острие стрелы.
58. Пулевидная форма.
59. Бочкообразная форма.
60. Форма полумесяца.
61. Форма диска.
62. Форма сердца.
63. Миндалевидная форма.
64. Форма фирмы-производителя/диск фирмы-производителя.
65. Форма параллелограмма.
66. Трапецеидальная форма.
67. Форма гантели/фигура 8.
68. Форма бабочки.
69. Форма неправильного треугольника.
Обычно ядро содержит активный ингредиент и различные инертные наполнители в зависимости от способа, с помощью которого его изготавливают.
В тех вариантах осуществления изобретения, в которых ядро изготавливают прессованием, подходящие инертные наполнители включают в себя наполнители, связующие, дезинтегрирующие агенты, смазки, скользящие вещества и тому подобные наполнители, известные в данной области. В тех вариантах осуществления изобретения, в которых ядро изготавливают прессованием и дополнительно наделяют модифицированным высвобождением содержащегося в нем активного ингредиента, такое ядро предпочтительно дополнительно содержит сжимаемый инертный наполнитель, модифицирующий высвобождение.
Подходящие наполнители, применяемые при изготовлении ядра прессованием, включают в себя водорастворимые, сжимаемые углеводы, такие как сахара, которые включают в себя декстрозу, сукрозу, мальтозу и лактозу, спирты-производные сахаров, которые включают в себя маннит, сорбит, мальтит, ксилит; гидролизаты крахмала, которые включают в себя декстрины и мальтодекстрины и т.п., нерастворимые в воде пластически деформируемые материалы, такие как микрокристаллическая целлюлоза или другие производные целлюлозы, нерастворимые в воде, хрупкие материалы, такие как дикальцийфосфат, трикальцийфосфат и т.п., и их смеси.
Подходящие связующие для изготовления ядра прессованием включают в себя сухие связующие, такие как поливинилпирролидон, гидроксипропилметилцеллюлоза и т.п.; влажные связующие, такие как водорастворимые полимеры, включая гидроколлоиды, такие как гуммиарабик, альгинаты, агар, гуаровая камедь, смола плодоворожкового дерева, каррагинан, карбоксиметилцеллюлоза, таро, аравийская камедь, трагакантовая камедь, пектин, ксантан, желлан, желатин, мальтодекстрин, галактоманнан, пусстулан, ламинарин, склероглюкан, инулин, велан, рамзан, зооглан, метилан, хитин, циклодекстрин, хитозан, поливинилпирролидон, целлюлозы, сукроза, крахмалы и т.п.; их производные и их смеси.
Подходящие дезинтегрирующие агенты для изготовления ядра прессованием включают в себя натрийкрахмалгликолят, поперечно сшитый поливинилпирролидон, поперечно сшитую карбоксиметилцеллюлозу, крахмалы, микрокристаллическую целлюлозу и т.п.
Подходящие смазки для изготовления ядра прессованием включают в себя жирные кислоты с длинной цепью и их соли, такие как стеарат магния и стеариновая кислота, тальк, глицериды и воски.
Подходящие скользящие вещества для изготовления ядра прессованием включают в себя коллоидный диоксид кремния и т.п.
В некоторых вариантах осуществления изобретения ядро или его часть может необязательно содержать инертные наполнители, модифицирующие высвобождение, известные в данной области, например, описанные в переуступленной, совместно рассматриваемой заявке США с регистрационным №10/432488, поданной 28 сентября 2002 г., раскрытие сущности которой включено сюда путем ссылки. Подходящие для изготовления ядра прессованием сжимаемые инертные наполнители, модифицирующие высвобождение, включают в себя способные к набуханию, поддающиеся размыванию гидрофильные материалы; нерастворимые, годные в пищу материалы; pH-зависимые полимеры и т.п.
Подходящие для изготовления ядра прессованием фармацевтически приемлемые вспомогательные вещества включают в себя консерванты; высокоэффективные подсластители, такие как аспартам, ацесульфам калия, сукралоза и сахарин; корригенты; красители; антиоксиданты; поверхностно-активные вещества; смачивающие средства и тому подобное, и их смеси.
В тех вариантах осуществления изобретения, в которых прессованием получают одно или более ядер, можно использовать способ сухого смешения (то есть прямого прессования) или способ мокрой грануляции, известный в данной области. При способе сухого смешения (прямом прессовании) активный ингредиент или ингредиенты вместе с инертными наполнителями смешивают в подходящем смесителе, затем переносят непосредственно в компрессионную машину для прессования таблеток. При способе мокрой грануляции активный ингредиент или ингредиенты, соответствующие инертные наполнители и раствор или дисперсию влажного связующего (например, приготовленную водосодержащую крахмальную пасту или раствор поливинилпирролидона) перемешивают и гранулируют. С другой стороны, в число инертных наполнителей можно включить сухое связующее и гранулировать смесь с водой или другим подходящим растворителем. Подходящие устройства для мокрой грануляции известны в данной области, включая мешалки с малыми сдвиговыми усилиями, например, планетарные мешалки; мешалки с большими сдвиговыми усилиями; и кипящие слои, включая вращающиеся кипящие слои. Полученный гранулированный материал сушат и, необязательно, способом сухого смешения смешивают с дополнительными ингредиентами, например, вспомогательными веществами и/или инертными наполнителями, такими как, например, смазки, красители и т.п. Затем полученную в итоге сухую смесь подвергают прессованию. Способы прямого прессования и способы мокрой грануляции известны в данной области и подробно описаны, например, в публикации Lachman и др., The Theory and Practice of Industrial Pharmacy, глава 11 (3-е издание, 1986).
Порошковые смеси, полученные способом сухого смешения или мокрой грануляции, обычно прессуют в таблетки, применяя роторную машину для прессования, известную в данной области, такую как, например, машина для прессования, доступная для приобретения у фирмы Fette America Inc., Rockaway, NJ, или Manesty Machines LTD, Liverpool, UK. В роторной машине для прессования дозированным объемом порошка заполняют полость матрицы, которая, будучи частью вращающегося «стола с матрицами», перемещается от места загрузки к месту прессования, где порошок прессуется между верхним и нижним пуансоном, до места выталкивания, где полученная таблетка выталкивается из полости матрицы с помощью нижнего пуансона и направляется к спускному желобу с помощью стационарного приемного приспособления.
В одном из необязательных вариантов осуществления изобретения ядро можно приготовить с помощью способов прессования и устройства, описанного в совместно рассматриваемой заявке на патент США №09/966509, стр.16-27, раскрытие сущности которой включено здесь путем ссылки. В частности, ядро изготавливают с помощью роторного модуля для прессования, содержащего в отдельном устройстве зону загрузки, зону запрессовки, зону прямого прессования, зону выталкивания и зону очистки, имеющем конструкцию с двумя рядами матриц, как показано на фигуре 6 заявки на патент США №09/966509. Матрицы модуля для прессования предпочтительно загружают при помощи пониженного давления с применением фильтров, расположенных в каждой матрице или возле нее.
Ядра, изготовленные прессованием, могут представлять собой простые или многослойные таблетки, например, двухслойные таблетки.
Ядра имеют плотность, по меньшей мере, приблизительно 0,9 г/см3, например, по меньшей мере, приблизительно 1,0 г/см3 и процент пористости менее 40%, предпочтительно менее 35%, наиболее предпочтительно 30%. Пористость порошка представляет собой отношение объема пор к общему объему. Объем пор представляет собой объем пространства между частицами, в то время как общий объем представляет собой суммарный занимаемый объем. Процент пористости представляет собой отношение, выраженное в процентах. Указанные значения можно измерить с помощью ртутного порозиметра, такого как порозиметр Autopore IV 9500 V1.05, доступный для приобретения у компании Micrometics Corporation, при давлении заливаемой ртути от 1,32 до 1,33 фунт/кв.дюйм, краевом угле смачивания ртути 130 градусов и поверхностном натяжении 485 дин/см. Типичные ядра включают в себя прессованную полужесткую таблетку весом 385 мг с объемом 0,4 куб.см, и прессованную таблетку весом 586 мг с объемом приблизительно 0,5 куб.см.
Ядра окружены оболочкой. Оболочка содержит одно или более отверстий. Отверстие или отверстия обеспечивают канал для сообщения между ядром и наружной поверхностью дозированной формы. Отверстия могут проходить через всю толщину оболочки до соприкосновения с ядром или только через часть оболочки.
Оболочка может быть в значительной степени едина и непрерывна за исключением имеющихся в ней отверстий, или оболочка может состоять из нескольких частей, например, из первой части оболочки и второй части оболочки. В некоторых вариантах осуществления изобретения оболочка или части оболочки напрямую соприкасаются с ядром. В некоторых других вариантах осуществления изобретения оболочка или части оболочки напрямую соприкасаются с подслоем, который в значительной степени окружает ядро. В тех вариантах осуществления изобретения, в которых оболочка состоит из первой и второй частей, по меньшей мере, в первой части оболочки имеются отверстия.
В некоторых вариантах осуществления изобретения первая часть оболочки и вторая часть оболочки композиционно различаются. Применяемый здесь термин «различаются композиционно» означает наличие свойств, которые легко различимы путем качественного или количественного химического анализа, физического испытания или визуального наблюдения. Например, первая и вторая части оболочки могут содержать разные ингредиенты или разные уровни одних и тех же ингредиентов, или первая и вторая части оболочки могут иметь разные физические или химические характеристики, разные функциональные характеристики, или отличаться визуально. Примеры физических или химических характеристик, которые могут различаться, включают в себя гидрофильность, гидрофобность, гигроскопичность, эластичность, способность деформироваться, предел прочности, степень кристалличности и плотность. Примеры функциональных характеристик, которые могут различаться, включают в себя скорость и/или степень растворения самого материала или активного ингредиента внутри него, скорость разрушения материала, его проницаемость для активных ингредиентов, проницаемость для воды или водной среды и т.п. Примеры визуальных отличий включают в себя размер, форму, рельеф поверхности или другие геометрические свойства, цвет, тон окраски, непрозрачность и блеск.
В одном из вариантов осуществления изобретения дозированная форма согласно изобретению содержит: a) ядро, содержащее в себе активный ингредиент; b) необязательный подслой, который в значительной степени покрывает ядро; и c) оболочку, состоящую из первой и второй частей оболочки, расположенную на поверхности подслоя; первой части оболочки, содержащей одно или более отверстий, и первой части оболочки, легко растворимой в гастроинтестинальных жидкостях. Применяемый здесь термин «в основном покрывает» в отношении оболочки означает, что, по меньшей мере, приблизительно 95% области поверхности ядра покрыто подслоем. Подслой может необязательно содержать красители, такие как красящие вещества, пигменты и их смеси, которые создают матовый, перламутровый или полупрозрачный эффекты.
Применение подслоев хорошо известно в данной области и описано, например, в патенте США №№3185626, который включен сюда посредством ссылки. В качестве подслоя согласно настоящему изобретению можно применять любую композицию, подходящую для покрытия таблетки пленкой. Примеры подходящих подслоев описаны в патентах США №№4683256, 4543370, 4643894, 4828841, 4725441, 4802924, 5630871 и 6274162, все из которых включены сюда посредством ссылки. Дополнительные подходящие подслои включают в себя один или более из следующих ингредиентов: простые эфиры целлюлозы, такие как гидроксипропилметилцеллюлоза, гидроксипропилцеллюлоза и гидроксиэтилцеллюлоза; полиуглеводы, такие как ксантановая камедь, крахмал и мальтодекстрин; пластификаторы, включающие, например, глицерин, полиэтиленгликоль, пропиленгликоль, дибутилсебацат, триэтилцитрат, растительные масла, такие как касторов