Способ блокирования сигнального пути, активируемого tgf-beta фактором vgi в клетках животных
Иллюстрации
Показать всеИзобретение относится к области молекулярной биологии, конкретно к белкам, регулирующим клеточную дифференцировку путем ингибирования белков надсемейства TGF-beta. Предназначено для лечения и профилактики связанных с ортологами VgI человека заболеваний. Вводят белок ноггин2 в ткань, содержащую белок VgI, в количестве, эффективном для ингибирования активности VgI. Изобретение позволяет решить задачу блокирования сигнального пути, активируемого TGF-beta фактором VgI в клетках животных. 2 ил.
Реферат
Изобретение относится к области молекулярной биологии, конкретно к белкам, регулирующим клеточную дифференцировку путем ингибирования белков надсемейства TGF-β, и может найти применение в медицине и клеточных технологиях.
Надсемейство трансформирующего фактора роста β (TGF-β) включает в себя множество факторов роста, обладающих общими структурными мотивами. Данные белки вовлечены в широкий спектр биологических процессов, таких как процессы клеточной и тканевой дифференцировки в ходе эмбрионального развития и заживления ран, восстановление и реконструкции костной ткани во взрослом организме, канцерогенез, воспалительные процессы различной природы и многие другие.
Белки VgI и его ортологи GDF1 и GDF3 образуют одно из семейств факторов из надсемейства TGF-beta (Andersson et al., Dev. Biol. (2007)311 (2):500-11). Используемый здесь и далее термин "ортолог" обозначает полипептид или белок, полученный из одного вида, являющийся функциональной копией полипептида или белка другого вида. Различия последовательностей ортологов являются результатом видообразования. Белки VgI/GDF1/GF3 играют ключевую роль в регуляции формирования мезодермы в эмбриогенезе (Kessler PS, Melton DA., Induction of dorsal mesoderm by soluble, mature VgI protein. Development. (1995)121(7):2155-64), а также в регуляции становления право- левосторонней симметрии органов. Кроме того, различная природа нарушения синтеза этих белков провоцирует развитие некоторых патологий у человека (канцерогенез семенников, аномальное формирование сердца, ожирение) (Caricasole et al., Oncogene (1998) 16(1):95-103; Ezeh et al., Cancer (2005) 104(10):2255-2265; Andersson et al., PNAS (2008) 105 (20): 7252-7256; Roessler et al., Am. J. Hum. Gen. (2008) 83 (1):18-29). В связи с этим важной задачей является поиск регуляторов функционирования белков VgI/GDF1/GF3, в том числе поиск их антагонистов.
Идентифицирован ряд белков межклеточного матрикса, являющихся антагонистами различных представителей надсемейства TGF-β (например, белков костного морфогенеза, BMP) и играющих важную роль в процессах клеточной дифференцировки и развития (Balemans and Van Hul, Dev Biol. (2002) 250(2):231-250; Avsian - Kretchmer and Hsueh, Mol Endocrinol. (2004) 18 (1):1-12). К антагонистам BMP относятся, например, белки хордин, вентроптин, ноггин, церберус и фоллистатин.
Белки церберус и ноггин позвоночных индуцируют формирование структур головы в передней эктодерме эмбрионов позвоночных. Белок ноггин способен так же изменять дифференцировку мезодермальных зачатков из вентральных зачатков, таких как кровь и мезенхима, в дорзальные зачатки, такие как мышца или хорда, или дифференцировку эпидермальных зачатков в нейтральные зачатки. Функции хордина сходны с функциями ноггин1, отражая сходный механизм действия этих белков как антагонистов BMP.
Антагонисты факторов роста из надсемейства TGF-β являются важными фармацевтическими, клиническими и лабораторными инструментами для регуляции клеточной дифференцировки и терапевтического вмешательства.
Известен гомолог белка позвоночных ноггин, названный ноггин2 (Fletcher et al., Gene Expr Patterns. 2004, v.5 (2), pp.225-230; Eroshkin et al., Gene Expr Patterns. 2004, v.6, pp.180-186). Было показано, что ген ноггин2 имеет дифференциальный характер экспрессии в ходе развития Xenopus. Однако функция ноггин2 не исследована.
Известны способы регуляции активности TGF-beta сигнальных каскадов белками семейства ноггин, включающие регуляцию активности семейства TGF-beta факторов - BMP (ADMP, ВМР2, ВМР4, ВМР7, CDF6), с помощью лишь одного представителя семейства белков ноггин - "классического" белка ноггин (ноггин1). При этом введение ноггин1 в ткани организма может производиться либо путем введения матричных ДНК или РНК конструкций, кодирующих данный белок, либо непосредственным введением рекомбинантного белка ноггин1 (Brunet et al. (1998) Science 280, 1455-1457; Lamb et al. (1993) Science 262, 713-718; Slack J.M. & Tannahill, D. (1993). Noggin the dorsalizer. Nature 361, 498-499; US Patent 5,670,481, Dorsal tissue affecting factor (noggin) and compositions comprising same, изобретатели: Harland; Richard M., Smith; William С, дата публикации: September 23, 1997).
Наиболее близкий к заявленному способу описан в McMahon et al., (1998) Genes. Dev. 12, 1438-1452, однако наряду с остальными известными методами он не позволяет осуществлять регуляцию TGF-beta сигнального каскада, активируемого белком VgI.
Изобретение решает задачу блокирования сигнального пути, активируемого TGF - beta фактором VgI в клетках животных.
Поставленная задача решается за счет способа блокирования сигнального пути, активируемого TGF-beta фактором VgI в клетках животных, путем введения белка ноггин2 в ткань, содержащую белок VgI, в количестве, эффективном для ингибирования активности VgI.
Установлено, что ноггин2 способен регулировать дифференцировку эмбриональной мезодермы и является блокатором активности одного из индукторов мезодермальной дифференцировки - TGF-β фактора VgI.
Сущность способа заключается в введении белка ноггин2 в организм, ткань или клетку в количестве, эффективном для блокирования или снижения активности VgI или его ортологов, посредством препятствования связыванию этих факторов со специфическими белковыми рецепторами.
Указанный способ может быть использован для модификации клеточной дифференцировки, где он предусматривает приведение клетки или окружающей клетку среды в контакт с белком ноггин2. При осуществлении способа может быть использована экспрессирующая конструкция, содержащая кодирующую ноггин2 нуклеиновую кислоту под контролем подходящего промотора. В этом осуществлении способ изменения клеточной дифференцировки предусматривает создание экспрессирующей конструкции, содержащей кодирующую ноггин2 нуклеиновую кислоту под контролем подходящего промотора; введение указанной экспрессирующей конструкции в клетку для экспрессии ноггин2, где экспрессия ноггин2 приводит к изменению клеточной дифференцировки.
Указанный способ можно применять для профилактики и лечения связанных с ортологами VgI человека (белки GDF1 и GDF3) заболеваний, например для ингибирования прогрессии определенных опухолей семенников (семеномы) и вызванного неправильной диетой ожирения.
В тексте используются следующие сокращения:
кДНК - ДНК, комплиментарная матричной РНК
мРНК - матричная РНК
пг - пикограмм
ПЦР - полимеразная цепная реакция
Изобретение иллюстрируют графические материалы:
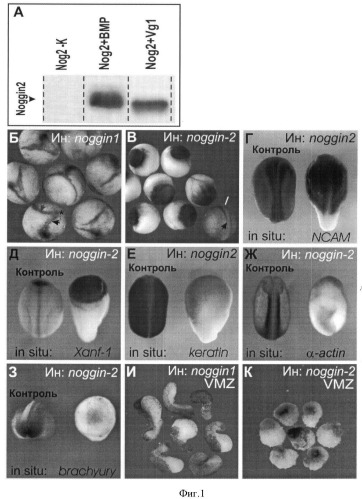
Фигура 1. Связывание белка VgI белком ноггин2 и влияние ноггин2 на дифференцировку нервной и мышечной тканей в эмбрионах Xenopus laevis. (Г-К) сигнал гибридизации in situ показан черным.
А. Белок ноггин2 связывает молекулы костного морфогенетического белка (BMP) и молекулы белка Vg1. Подробное описание приведено в тексте примера 1.
Б, В. Вентральные микроинъекции 40 пг синтетической мРНК гена ноггин1 в зародыши X. laevis на ранних стадиях развития приводят к формированию дополнительной оси тела (черная стрелка указывает основную ось тела, серая стрелка указывает дополнительную ось тела), в то время как микроинъекции такого же количества синтетической мРНК ноггин2 приводят к формированию грибообразного фенотипа.
Г-З. In situ гибридизация контрольных зародышей (слева на каждой из фотографий) и зародышей, микроинъецированных мРНК ноггин2 с пробами мРНК приведенных генетических маркеров, показывает усиление нейральной (Г, Д) и подавление эпидермальной (Е) и мезодермальной (Ж, 3) дифференцировок. Сигнал показан черным.
И. Эксплантаты вентральной маргинальной зоны (VMZ) зародышей, микроинъецированных вентральном РНК ноггин1, удлиняются к концу нейруляции благодаря дифференцировки скелетной мускулатуры.
К. Эксплантаты вентральной маргинальной зоны (VMZ) зародышей, микроинъецированных вентральном РНК ноггин2 к концу нейруляции, сохраняют округлую форму.
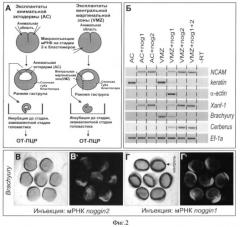
Фигура 2. Влияние ноггин2 на дифференцировку нервной и мышечной тканей в эктодермальных эксплантатах Xenopus laevis и подавление дифференцировки эмбриональной мезодермы с помощью ноггин2.
A. Схема экспериментов с эксплантатами эктодермы анимальной области зародышей (анимальные шапочки - АС) и эксплантатов вентральной маргинальной зоны зародышей (VMZ).
Б. Обратная транскрипция - ПЦР анализ проб тотальной РНК эксплантатов эктодермы анимальной области зародышей и эксплантатов вентральной маргинальной зоны зародышей, микроинъецированных мРНК ноггин1 и ноггин2 с праймерами к нейроэктодермальным (NCAM, Xanf-1), эпидермальным (keratin), мышечным (α-actin), постериорному мезодермальному (brachyury) и эндомезодермальному (cerberus) молекулярным маркерам и Ef-1α в качестве контроля количества мРНК. Ноггин1 и ноггин2 активируют экспрессию нейральных маркеров (NCAM, Xanf-1) и подавляют экспрессию эпидермального (keratin), в то время как мРНК ноггин2, в отличие от мРНК ноггин1, не обнаруживает способность активировать экспрессию мышечного молекулярного маркера α-actin в эксплантатах вентральной маргнальной зоны.
B, В′. Подавление экспрессии мезодермального молекулярного маркера (brachyury) у зародышей, микроинъецированных мРНК ноггин2. В′ - флуоресцентный краситель показывает распределение микроинъецированного материала.
Г, Г′. Экспрессия мезодермального молекулярного маркера (brachyury) у зародышей, микроинъецированных мРНК ноггин1, не обнаруживают изменений по сравнению с контрольным зародышем (стрелка).
Изобретение иллюстрируют примеры.
Пример 1.
Связывание белка VgI белком ноггин2.
Введение белков ноггин2 и VgI в зародыши X. laevis осуществляют путем их экспрессии в составе плазмидных векторов pCS2-3Myc-noggin2 и pCS2-proactivinB-3Flag-Vg1, соответственно.
Для получения вектора pCS2-3Myc-noggin2 нуклеотидную последовательность, кодирующую три аминокислотных последовательности эпитопа белка Мус (EQKLISEEDLEQKLISEEDLEQKLISEEDL), вставляют с помощью ПЦР в кДНК ноггин2 непосредственно на 3′ конец последовательности, кодирующей сигнальный пептид ноггин2. Для этого на первой стадии клонирования получают соответственно 5′ и 3′ перекрывающиеся части кДНК ноггин2 в ПЦР с праймерами 5′-AATTGGATCCGCCACCATGAAGAGGATAAATCTGC-3′ и
5′-GAGGTCTTCCTCCGATATCAGCTTCTGTTCCAGATCCTCTTCAGAGATGAGTTTCT
GCTCATAAGGCTGACAGCACCCCTGA-3′,
5′-GAACAGAAGCTGATATCGGAGGAAGACCTCGAGCAGAAACTCATCTCTGAAGAGGATCT
GCTCAGGCTTAGACCCTCT-3′ и 5′-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3′ соответственно. На второй стадии эти фрагменты кДНК очищают от не включившихся праймеров, смешивают друг с другом, денатурируют нагреванием, отжигают и подвергают второму раунду ПЦР с концевыми праймерами 5′-AATTGGATCCGCCACCATGAAGAGGATAAATCTGC-3′ и 5′-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3′. Полученную полноразмерную кДНК noggin2, содержащую последовательность, кодирующую три аминкислотных последовательности Мус, клонируют в вектор pCS2 по рестриктным сайтам NcoI (тупой)/AgeI (тупой) и XhoI/XhoI.
Вектор pSP64-proactivinB-3Flag-VgI получают путем ряда последовательных клонирований. На первой стадии клонирования нуклеотидную последовательность, кодирующую три аминокислотных последовательности Flag (DYKDDDDKDYKDDDDKDYKDDDDK), вставляют с помощью ПЦР в кДНК непосредственно позади последовательности, кодирующей прорегион белка activin-B Xenopus laevis. Для этого получают 5′ и 3′ перекрывающиеся части кДНК activin-B в ПЦР с праймерами
5′-AATTGGATCCGCCACCATGGCTCTCCTGTTACTGCCTCTG-3′ и
5′-TTTGTCATCATCGTCTTTGTAGTCCTTATCGTCGTCATCCTTGTAATCCTCGAGGCCTCTC
TTACGGA-3′, 5′-GACTACAAAGACGATGATGACAAAGATTACAAGGATGACGACGAT
AAG TGCGATGGACACACAAATT-3′ и 5′-AATGAATTCATGCACAGCCGCACTCGTCCA-3′ соответственно. На второй стадии эти фрагменты кДНК очищают от не включившихся праймеров, смешивают друг с другом, денатурируют нагреванием, отжигают и подвергают второму раунду ПЦР с концевыми праймерами
5′-AATTGGATCCGCCACCATGGCTCTCCTGTTACTGCCTCTG-3′ и
5′-AATGAATTCATGCACAGCCGCACTCGTCCA-3′.
Полученную полноразмерную кДНК activin-B, содержащую последовательность, кодирующую три аминкислотных последовательности эпитопа Flag и содержащую сайт XhoI непосредственно после последовательности, кодирующей три эпитопа Flag, клонируют в вектор pSP64T по рестриктным сайтам HindIII (тупой)/AgeI (тупой) и EcoRI/EcoRI. Получают промежуточный вектор pSP64T-proactivinB-3Flag-activin.
Фрагмент кДНК, кодирующий аминокислотную последовательность VgI, получают на основе геномной ДНК Xenopus laevis методом ПЦР с соответствующими специфическими праймерами к последовательности VgШ: 5′-ATTCTCGAGGATCCAGAGCTCAAGA-3′ и 5′-ATAGAATTCTCACCTGCAGCCACAT-3′.
На заключительной стадии клонирования фрагмент VgI клонируют в вектор pSP64T-proactivinB-3Flag-activin по рестриктным сайтам XhoI и EcoRI. Получают вектор pSP64T-proactivinB-3Flag-VgI.
Анализ способности экспрессированного белка 3Myc-noggin2 связывать молекулы белка 3Flag-VgI проводят методом ко-иммунопреципитации. Для этого 600 pg синтетической мРНК 3Мус-noggin2 и 600 pg синтетической мРНК proactivinB-3Flag-VgI микроинъецируют в развивающиеся зародыши X. laevis на стадии 2-х бластомеров. В дальнейшем эти зародыши инкубируют в растворе 0.1 MMR до стадии ранней гаструлы.
Выделение экспрессированных белков проводят путем лизирования зародышей на стадии ранней гаструлы по методике, описанной в Tanegashima et al., Int.J.Dev.Biol (2004) 48:275-283.
После выделения проводят абсорбцию зрелого белка 3Мус-ноггин2 на смоле Мус-Agarose (Sigma) согласно протоколу производителя. После промывки смолы в соответствии с протоколом производителя наличие на этой смоле связавшегося белка 3Flag-VgI анализируют методом белкового блоттинга с помощью Flag-специфических моноклональных антител (Sigma).
Способность молекул белка ноггин2 связывать молекулы белка VgI показана на Фигуре 1А.
В качестве контроля в эксперименте используют белок 3Flag-ВМР, связываемый белком ноггин2.
Пример 2.
Воздействие ноггин2 на направление развития клеток.
кДНК, содержащую полную кодирующую область ноггин2, реамплифицируют при помощи ПЦР с клона, полученного в работе Eroshkin et al., Gene Expr Patterns. 2004, v.6, pp.180-186, с использованием праймеров 5′-ATTACCGGTGGGAGAACCTTGTTCTTCATT-3′ и 5′-ATTCTCGAGTTAGCATGAACACTTACACTCTG-3′ и клонируют в вектор pCS2 (вектор рСS2-ноггин2).
Полную кодирующую последовательность ноггин1 получают путем ПЦР-амплификации с образца кДНК Xenopus laevis с использованием ноггин1-специфичных праймеров 5′-TATCCATGGCAAGAAATCGGGAGCA-3′ и 5′-ATTCTCGAGTCTCAGCATGAGCATTTGCA-3′ и клонируют в вектор pCS2 (вектор рСS2 - ноггин1).
Синтетические мРНК ноггин2 и ноггин1 получают с применением набора реактивов mMESSAGE MASHINE Kit (Ambion) из векторов pCS2-ноггин2 и вектора рСS2-ноггин1 соответственно, линеаризованных рестрикционной эндонуклеазой EcoRI (Fermentas). Воздействия микроинъекций мРНК ноггин2 на развитие Xenopus laevis сравнивают с ранее описанными воздействиями инъекций vРНК ноггин1 (Smith and Harland, Cell 1992, v.70, pp.829-840; Lamb et al., Science 1993, v.262, pp.713-718; Smith et al., Nature 1993, v.361, pp.547-549). В ходе данных экспериментов мРНК ноггин1 и ноггин2 инъецируют в указанные ниже бластомеры с применением микроинъектора Eppendorf.
Вентральные инъекции 40 пг мРНК ноггин1 в ранние эмбрионы индуцируют вторичную ось тела (Фигура 1 Б, черная стрелка - первичная ось; серая стрелка - вторичная ось), тогда как подобные инъекции мРНК ноггин2 (40 пг) приводят к развитию грибовидных эмбрионов (Фигура 1 В). Таким образом, в отличие от ноггин1 (Dale and Slack, Development 1987, v.100, pp.279-295; Cell 1992, v.70, pp.829-840; Smith et al., Nature 1993, v.361, pp.547-549), ноггин2, несмотря на его способность связывать BMP, не индуцирует вторичную ось тела при инъекции его мРНК в оба вентральных бластомера 8-клеточных эмбрионов. Вместо этого формируются аномальные грибовидные эмбрионы.
Гибридизация in situ на тотальном препарате эмбрионов с инъекцией мРНК ноггин2 с зондами к мРНК нейральных (NCAM, Xanf-1), эпидермальных (ген кератина), мышечных (ген α-актина) генетических маркеров и генетических маркеров поздней мезодермы (brachyury) показывает гигантскую нейрализацию эктодермы и уменьшение мышечной и эпидермальной дифференцировки (Фигура 1Г-З).
Все вместе данные результаты указывают на то, что ноггин2 может нейрализовать эмбриональную эктодерму, но ингибирует дифференцировку дорзальной мезодермы и, таким образом, может препятствовать дорзализующему действию эндогенного ноггин1.
Используют также эксплантаты, полученные из вентральной краевой зоны (VMZ) эмбрионов на стадии ранней гаструлы, для анализа эффектов ноггин2 на дифференцировку мезодермы. Микроинъекция мРНК ноггин1 вызывает сильное удлинение данных эксплантатов, преобразуя характер их вентральной мезодермы в мышечную мезодерму (дорзализация) (Dale and Slack, Development 1987, v. 100, pp.279-295; Cell 1992, v.70, pp.829-840; Smith et al., Nature 1993, v.361, pp.547-549; Фиг.1 И). В отличие от этого, подобно эксплантатам VMZ без инъекции, экспрессирующие ноггин2 или ноггин1 и ноггин2 одновременно, эксплантаты остаются округлыми (Фигура 1 К).
Для анализа влияния белка ноггин2 на тканевую дифференцировку используют также метод обратной транскрипции - ПЦР (ОТ - ПЦР) и сравнение экспрессии различных генетических маркеров в эксплантатах "наивной" эктодермы (анимальные шапочки - АС), извлеченных из эмбрионов на стадии ранней гаструлы, в которые посредством микроинъекции предварительно ввели мРНК ноггин1 или ноггин2 (Фигура 2А, Б). Используют эксплантаты, извлеченные из вентральной краевой зоны (VMZ) эмбрионов на стадии ранней гаструлы, для анализа воздействий ноггин2 на дифференцировку мезодермы (фигура 1 К, Л).
Эксплантаты АС извлекают из эмбрионов, подвергнутых инъекции, с применением микроножа и стеклянной палочки, как ранее описано в Zaraisky et al. Developmental Biology 1992, V. 152, pp.373-382. Все эксплантаты инкубируют в течение ночи в растворе 0,5×MMR. Из десяти эксплантатов каждого типа выделяли общую РНК и проводили ОТ-ПЦР, как описано в Zaraisky et al. Developmental Biology 1992, V.152, pp.373-382. Используют следующие праймеры: ген α-актина: 5′-GCTGACAGAATGCAGAAG и 5′-TTGCTTGGAGGAGTGTGT; brachyury: 5′-GCTGGAAGTATGTGAATGGAG и 5′-TTAAGTGCTGTAATCTCTTCA; церберус: 5′-GCTTTGGTAAATGCATCTCTCTCC и 5′-GGTGACCAGTAAATCATACCTGCT; ген кератина ХK81: 5′-CTGAATAACATGAGAGCTG и 5′-TGGTTCTAGTTGTGGATGT; NCAM: 5′-CCTGCTTATGTGTATCGC и 5′-TTCACAGTACTGGGCTGTGCTT; Xanf-1,
описанные в Groppe et al., 2002.
ОТ - ПЦР на основе тотальной РНК из эксплантатов АС и VMZ эмбрионов, подвергнутых инъекции мРНК ноггин1 или ноггин2, осуществляют с праймерами к маркерам нейроэктодермы (NCAM, Xanf-1), эпидермиса (кератин), мышц (α-актин), поздней мезодермы (brachyury) и энтомезодермы (церберус) и Ef-1-α в качестве контроля (Фигура 2 Б).
Показано, что ноггин1 и ноггин2 активируют экспрессию нейральных маркеров (NCAM, Xanf-1) и ингибируют эпидермальный маркер (кератин), тогда как только ноггин1 активирует экспрессию мышечного маркера (α-актин) в эксплантатах VMZ.
В данном анализе ноггин2 показывает сильную нейтрализующую активность, подобную активности ноггин1 (Smith and Harland, Cell 1992, V.70, pp.829-840; Lamb et al., Science 1993, V.262, pp.713-718), индуцируя экспрессию маркеров передней части нервной системы, но ингибируя эпидермальный маркер.
Способность ноггин2 нейтрализовать эктодерму вкупе с его способностью подавлять дорзализующую активность ноггин1 подтверждает способность ноггин2 связывать помимо молекул BMP и другие факторы, необходимые для дифференцировки мышц.
Пример 3.
Способность белка ноггин2 подавлять дифференцировку эмбриональной мезодермы соответствует его способности блокировать сигнальный путь, активируемый белком VgI.
Известно, что сигнальный путь, активируемый белком VgI играет ключевую роль в дифференцировке эмбриональной мезодермы (Kessler PS, Melton DA., Induction of dorsal mesoderm by soluble, mature VgI protein. Development. (1995)121(7):2155-64).
Способность белка ноггин2 подавлять дифференцировку эмбриональной мезодермы соответствует его способности блокировать активность сигнального пути, активируемого белком VgI через связывание молекул белка VgI (см. Пример 1).
Способность ноггин2 подавлять дифференцировку эмбриональной мезодермы оценивают путем анализа экспрессии универсального маркера ранних стадий развития мезодермы - гена brachyury - на стадии ранней гаструлы Xenopus laevis. Синтетические мРНК ноггин1 и ноггин2, полученные, как описано в Примере 2, инъецируют в экваториальную область одного из вентральных бластомеров на стадии 8 бластомеров в количестве 40 пг с применением микроинъектора Eppendorf.
Микроинъекции мРНК ноггин2 вызывают ингибирование экспрессии гена brachyury в области микроинъекции, что свидетельствует о подавлении в этом месте дифференцировки эмбриональной мезодермы (Фигуры 2 В и В′). Аналогичные микроинъекции мРНК ноггин1 не вызывают ингибирование экспрессии brachyury и, соответственно, подавления развития мезодермы (Фигура 2 Г и Г′).
Таким образом, в отличие от ноггин1, ноггин2 обладает уникальной способностью подавлять дифференцировку эмбриональной мезодермы.
Пример 4.
Блокирование мезодермализующей активности белка VgI с помощью ноггин2.
Способность ноггин2 блокировать мезодермализующую активность белка VgI оценивают по способности ноггин2 подавлять экспрессию основной генетической мишени каскада, активируемого VgI, - гена brachyury - в эксплантатах эмбриональной эктодермы зародышей (АС эксплантаты), микроинъецированных смесью мРНК ноггин2 и мРНК VgI. В качестве контроля, аналогичные опыты проводили с мРНК и ноггин1.
Экспрессию гена brachyury анализируют методом обратной транскрипции - ПЦР мРНК из эктодермальных эксплантатов, как описано в Примере 2.
Установлено, что ноггин2 способен подавлять активацию экспрессии brachyury, индуцируемую VgI. При этом ингибирование brachyury наблюдается только в том случае, если концентрация микроинъецированной мРНК VgI не превышает таковую ноггин2. В отличие от этого, ноггин1 не способен ингибировать активацию гена brachyury в аналогичных тестах.
Способ блокирования сигнального пути, активируемого TGF-beta фактором VgI в клетках животных, путем введения белка ноггин 2 в ткань, содержащую белок VgI, в количестве, эффективном для ингибирования активности VgI.