Способ диагностики заболеваний молочной железы на основании идентификации распределения эффективного атомного номера
Иллюстрации
Показать всеИзобретение относится к медицине, конкретно к способам дифференциальной диагностики доброкачественных и злокачественных заболеваний молочной железы. Способ обеспечивает повышение достоверности диагностики онкологических заболеваний молочных желез за счет совершенствования технологии щадящего режима исследования при повышении чувствительности к изменению эффективного атомного номера тканевой структуры и плотности молочной железы при высокоинформативном контрастном четком рельефном изображении структур молочной железы. Осуществляют получение маммограммы на двух различных энергиях излучения, при этом идентифицируют распределение эффективного атомного номера в молочной железе, для чего вычисляют распределение логарифмов числа фотонов, прошедших молочную железу без взаимодействия с ней на двух различных энергиях излучения с последующим вычислением их отношения, и визуализируют распределение эффективного атомного номера по этому отношению. 9 ил.
Реферат
Способ диагностики заболеваний молочной железы на основании идентификации распределения эффективного атомного номера.
Изобретение относится к медицине, конкретно к способам дифференциальной диагностики доброкачественных и злокачественных заболеваний молочной железы.
Рост числа онкологических заболеваний молочной железы обуславливает расширение арсенала диагностических методов.
Единственно надежным способом борьбы с этим злом является раннее выявление заболевания в его доклинической фазе, когда размеры новообразования не превышают 0.5-1 см (см. Terra Medica, 2002, №2, стр.20-21, М.М.Власова, Обоснование и принципы маммографического скрининга рака молочной железы).
Однако несмотря на значительное число диагностических методов и технических средств ошибки при постановке диагноза по-прежнему очень высоки. Так, частота постановки ложного диагноза о наличии рака составляет более 40%, когда как рак не обнаруживается в 10-15% случаев (см. Department of Health and Human Services, Central Intelligence Agency Brief Russian Health Minister on Their Unique Collaboration to Develop New Breast Imaging Technologies, http://www.womenshealth.gov/news/pr/1996.imaging.htm; Radiology, 1998; p.p. 209, 238, Lewin JM, Hendrick RE, D'Orsi CJ, et al. Clinical evaluation of a full field digital mammography prototype for cancer detection in a screening setting-work in progress).
Наиболее информативным методом диагностики при ранних непальпируемых формах рака является рентгеновская маммография, основанная на принципе различного поглощения рентгеновского излучения разными тканями.
Известен способ диагностики патологии с использованием рентгеновского проникающего излучения (см. патент ЕР №0402802, МПК А61В 06/00, публикация 1990), предусматривающий определение зоны патологического очага, просвечивание молочной железы проникающим излучением и регистрацию прошедшего излучения двухкоординатным позиционно-чувствительным детектором.
Молочная железа содержит только мягкие ткани, слабо различающиеся по коэффициентам поглощения рентгеновских лучей, поэтому изображение имеет слабый контраст, и обнаружение незначительных изменений в тканях на ранних стадиях болезни и выявление опухолей малых размеров являются затруднительными. При проецировании изображения молочной железы на рентгенограмме различные участки тканей накладываются друг на друга, что также искажает общую картину происходящих в тканях изменений.
Раковая опухоль представляет собой звездообразное образование с повышенным эффективным атомным номером. Предвестниками рака являются микрокальцинаты, которые имеют значительно больший эффективный атомный номер (Z=12-14) по сравнению с эффективным атомным номером здоровой ткани (Z=6,5-7,5). Наличие микрокальцинатов является практически достаточным условием образования онкологической опухоли. Особенно опасны мирокальцинаты размером менее 100 микрон, которые не выявляются средствами рентгеновской маммографии.
Традиционные рентгеновские маммограммы визуализируют распределение числа фотонов, прошедших молочную железу без взаимодействия.
N=N0e-µ(E,Z)ρd,
где µ - массовый коэффициент полного поглощения, определяемый эффективным атомным номером Z участка молочной железы и энергией рентгеновского излучения Е,
ρ - плотность участка молочной железы,
d - толщина.
Массовый коэффициент полного поглощения различных областей молочной железы изменяется весьма в широких пределах: от 5 (холестерин) до 12-14 (микрокальцинаты). Однако, учитывая фактические концентрации данных включений в молочной железе, эффективный атомный номер в молочной железе варьируется в диапазоне 6-8, в котором зависимость массового коэффициента полного поглощения может быть принята линейной.
Таким образом, рентгеновский снимок представляет собой нелинейную визуализацию распределения произведения атомного номера (Z) на плотность (ρ) и толщину участка (d) молочной железы. Если толщина молочной железы в процессе исследования постоянна (за исключением периферийных областей), то степень почернения на рентгеновской пленке определяется произведением плотности на эффективный атомный номер соответствующего участка молочной железы. При этом качество визуализации ухудшается за счет попадания на пленку рассеянного молочной железой излучения.
Совместное влияние рассеянного излучения, плотности, атомного номера на степень почернения рентгеновского снимка существенно затрудняет диагностику заболевания на ранней стадии.
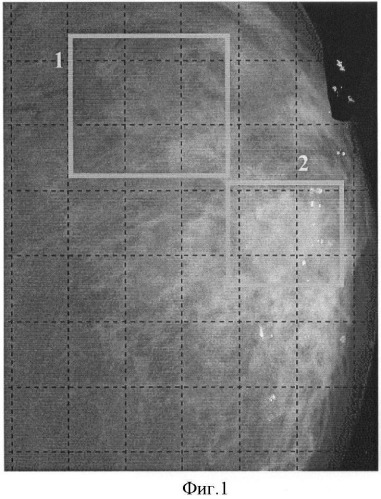
На фиг.1 представлена традиционная молочная железа, на которой прямоугольниками выделены области здоровой ткани (1) и с онкологической опухолью (2).
Известен способ построения маммографического изображения молочной железы на основе двойного облучения рентгеновским излучением двух разных энергий.
Изображение представляет собой разность логарифмов распределений чисел зарегистрированных фотонов на низкой и высокой энергиях:
где - числа зарегистрированных фотонов низкой и высокой энергий, соответственно;
- исходные числа фотонов низкой и высокой энергий, соответственно.
Для повышения контрастности изображения в молочную железу вводят контрастное вещество (ангиография), у которого энергия k-того электрона ниже высокой энергии и выше низкой энергии облучения. Обычно в ангиографии в качестве контрастного вещества используется йод, у которого k-край рентгеновского излучения равен 33.17 кэВ.
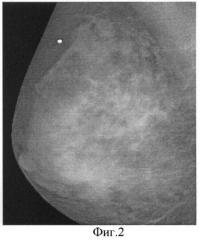
На фиг.2 представлен пример маммограммы, полученной данным способом, заимствованный в работе (см. Radiology, 1998; p.p.209, 238, Lewin JM, Hendrick RE, D'Orsi CJ, et al. Clinical evaluation of a full field digital mammography prototype for cancer detection in a screening setting-work in progress).
Несмотря на повышение резкости изображения, по сравнению с традиционной маммограммой, онкологическая опухоль и микрокальцинаты проявляются не достаточно резко.
Нерезкость изображения вызвана тем, что разность логарифмов пропорциональна произведению эффективного атомного номера на плотность
где k - коэффициент пропорциональности.
Вариации плотности на границах опухоли приводят к размытости изображения ее границ.
Существующие способы не позволяют получить количественные распределения плотности и эффективного атомного номера.
Известен способ обнаружения вещества внутри объектов (см. AC SU №1583806, МПК G01N 23/04, публикация 1990), включающий просвечивание контролируемого объекта рентгеновским излучением, регистрацию прошедшего через объект излучения в двух спектральных областях с различной эффективной энергией и сравнение отношения логарифмов зарегистрированных сигналов разной эффективной энергии с пороговым значением для принятия решения о типе просвеченного вещества.
В данном способе разделение исходного спектра излучения рентгеновской трубки на два спектра с различной эффективной энергией осуществляется путем изменения напряжения на аноде трубки.
Сравнивая отношение логарифмов с определенным пороговым уровнем, можно получить решение о классе вещества: органическое (Z<11) или неорганическое (Z>11).
Недостатком данного способа является невозможность обнаружения конкретных веществ по значению атомного номера Z среди множества других веществ того же класса с близкими значениями Z.
Техническим результатом изобретения является повышение достоверности диагностики онкологических заболеваний молочных желез путем получения численных значений плотности и эффективных атомных номеров биологической ткани молочной железы при выявлении микрокальцинатов размерами менее 100 микрон с четким получением линейных размеров, площади, объема патологических образований.
Технический результат достигается тем, что в способе диагностики заболеваний молочной железы на основании идентификации распределения эффективного атомного номера, предусматривающем облучение биологической ткани молочной железы на двух различных эффективных энергиях рентгеновского излучения, для численной визуализации распределений произведения эффективного атомного номера биологической ткани молочной железы на плотность вычисляют разность логарифмов числа фотонов, зарегистрированных при двух различных эффективных энергиях излучения, а для численной визуализации распределения эффективного атомного номера вычисляют отношение данных логарифмов.
Плотность биологической ткани молочной железы вычисляют по отношению разности логарифмов к логарифму отношения.
Идентификацию микрокальцинатов размером менее 100 микрон вычисляют по отношению логарифмов числа фотонов, зарегистрированных при двух различных эффективных энергиях излучения, за счет смещения двух исходных маммограмм относительно друг друга.
Повышение контрастности изображения эффективного атомного номера получают путем уменьшения разности энергий излучения при его идентификации по сравнению с фактической разностью энергий при облучении молочной железы.
Идентификацию микрокальцинатов размером менее 100 микрон с построением точных границ недоброкачественной опухоли биологической ткани молочной железы осуществляют по отношению логарифмов, полученных при нелинейно преобразованных монотонными функциями исходных чисел зарегистрированных фотонов.
Сущностью предлагаемого технического решения является то, что определяют зону патологического очага путем просвечивания биологической ткани молочной железы проникающим излучением и визуализируют распределение отношения логарифмов числа фотонов на двух разных энергий, прошедших биологическую ткань молочной железы без взаимодействия.
Использование двух различных эффективных энергий фотонов позволяет снизить влияние рассеянного излучения, что приводит к большей резкости получаемых маммограмм, так как распределения угла комптоновского рассеяния для двух различных эффективных энергиях отличаются незначительно.
Визуализация отношения логарифмов позволяет получить распределение эффективного атомного номера инвариантно к изменению плотности.
Другим преимуществом 2-энергетического подхода является возможность повышения чувствительности к изменению эффективного атомного номера, а следовательно, и более надежного выявления микрокальцинатов.
Причем приемлемая точность получения изображений может быть достигнута лишь при реализации алгоритмов компьютерной обработки.
Кроме того, параллельно обеспечивается топометрическая подготовка биологической ткани молочной железы, в ходе которой определяются линейные размеры, площадь, объем патологических образований.
Сравнение предлагаемого решения с известными техническими решениями показывает, что оно обладает новой совокупностью существенных признаков, которые совместно с известными признаками позволяют успешно реализовать поставленную цель.
На фиг.1 представлена традиционная молочная железа, на которой прямоугольниками выделены области здоровой ткани (1) и с онкологической тканью (2); на фиг.2 - маммограмма, полученная при использовании способа прототипа; на фиг.3 - зависимость отношения и разности массовых коэффициентов полного поглощения от эффективного атомного номера; на фиг.4 - традиционная маммограмма; на фиг.5 - визуализация распределения эффективного атомного номера; на фиг.6 - традиционная маммограмма (ТМ), эффективный атомный номер (Z), плотность (ρ) и их произведение (ρZ) онкологической опухоли; на фиг.7 - микрокальцинаты при смещении исходных снимков; на фиг.8 - визуализации распределения идентифицируемого эффективного атомного номера при уменьшении разности энергий излучения; на фиг.9 - визуализации распределения эффективного атомного номера онкологической опухоли при нелинейных преобразованиях исходного распределения числа зарегистрированных фотонов на разной энергии; на фиг.10 - визуализации распределения микрокальцинатов при нелинейных преобразованиях исходного распределения числа зарегистрированных фотонов на разной энергии.
Согласно предлагаемому способу диагностики заболеваний молочной железы обследование пациента осуществляется следующим образом:
- снимается традиционная маммограмма на двух различных энергиях излучения;
- вычисляется распределение логарифмов числа фотонов, прошедших молочную железу без взаимодействия на двух разных энергиях;
- для численной визуализации распределений плотности биологической ткани молочной железы вычисляют отношение разности логарифмов к логарифму отношения числа фотонов, прошедших молочную железу без взаимодействия на двух разных энергиях;
- идентификацию микрокальцинатов размером менее 100 микрон вычисляют отношением логарифмов числа фотонов, зарегистрированных при двух различных эффективных энергиях излучения за счет смещения двух маммограмм на разных энергиях относительно друг друга;
- для численной визуализации эффективного атомного номера уменьшают разность энергий излучения при его идентификации по сравнению с фактической разностью энергий при облучении молочной железы;
- идентификацию микрокальцинатов размером менее 100 микрон с построением точных границ недоброкачественной опухоли биологической ткани молочной железы осуществляют по отношению логарифмов, полученных при нелинейно преобразованных монотонными функциями исходных чисел зарегистрированных фотонов.
Суть предлагаемого изобретения.
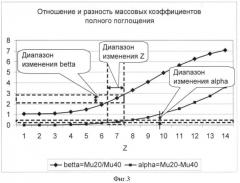
На фиг.3 представлена зависимость разности (α) и отношения (β) массовых коэффициентов поглощения от эффективного атомного номера. Как видно, разность и отношения данных коэффициентов в области их изменения в молочной железе могут быть приняты пропорциональными эффективному атомному номеру:
,
,
где индексы µL, µH - массовые коэффициенты полного поглощения для низкой и высокой энергии, соответственно,
L, Н - соответствуют низкой и высокой энергии;
kα, kβ - коэффициенты пропорциональности.
Разность и отношения коэффициентов могут быть определены как:
Исходное число фотонов может быть определено с помощью размещенной рядом с молочной железой эталонной пластины, известными плотностью, толщиной и атомным номером (например, алюминиевая пластина).
Отсюда эффективный атомный номер и плотность численно определяется как:
где kρ, kz - коэффициенты пропорциональности.
Результаты визуализации эффективного атомного номера и плотности:
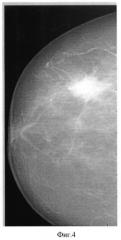
фиг.4 представляет традиционную маммограмму;
фиг.5 представляет идентифицируемое распределение эффективного атомного номера.
Как видно, распределение атомного номера существенно резче и контрастнее традиционной маммограммы.
На фиг.6 представлена традиционная маммограмма раковой опухоли (ТМ), распределения в ней эффективного атомного номера (Z), плотности (ρ) и их произведения (Zρ).
Способы повышения контрастности.
Наличие двух исходных снимков молочной железы позволяет применить нетрадиционные способы обработки изображения, основанные на физике процесса.
Смещение исходных снимков.
Независимость отношения логарифмов от плотности позволяет осуществлять изменение контрастности получаемого изображения путем смещения исходных снимков.
На фиг.7 представлены распределения Z, полученные без смещения и со смещением исходных снимков. Микрокальцинаты на распределении Z, полученном на смещенных снимках, проявляются в виде двух изображений: более темном и более светлом по сравнению с тканью молочной железы.
Это объясняется тем, что первые соответствуют отношению коэффициента поглощения здоровой ткани для низкой энергии (µL,T) к коэффициенту ткани с микрокальцинатом для высокой энергии (µH,Ca). Это отношение существенно выше, чем отношение коэффициентов для здоровой ткани (µL,T/µН,Т), но ниже, чем отношение коэффициентов для ткани с микрокальцинатом (µL,Ca/µН,Са).
Более светлые - отношению ткани с микрокальцинатом на низкой энергии (µL,Са) к коэффициенту здоровой ткани для высокой энергии (µH,T). Это отношение существенно ниже, чем отношение коэффициентов для здоровой ткани (µL,T/µН,Т), но выше, чем отношение коэффициентов для ткани с микрокальцинатом (µL,Ca/µН,Са).
Изменение разности энергий при реконструкции.
Уменьшение разности энергий излучения при реконструкции распределения Z проводит к увеличению чувствительности, к изменению эффективного атомного номера, что делает маммограмму более контрастной (см. фиг.8).
Нелинейные преобразования исходного числа фотонов монотонными функциями также изменяют чувствительность к изменению эффективного атомного номера. Так, на фиг.9 вариация Z в здоровой ткани практически отсутствует, а повышенный атомный номер в раковой опухоли проявляется с высокой контрастностью.
Нелинейные преобразования исходного числа фотонов монотонными функциями позволяют надежно выявлять области с микрокальцинатами, что иллюстрирует фиг.10. На данном распределении видны микрокальцинаты размером менее 60-70 микрон.
Техническо-экономический эффект достигается за счет совершенствования технологии щадящего режима исследования при повышении чувствительности к изменению эффективного атомного номера тканевой структуры и плотности молочной железы при высокоинформативном контрастном четком рельефном изображении структур молочной железы.
Способ проведения диагностики онкологических заболеваний молочной железы, включающий получение маммограммы на двух различных энергиях излучения, отличающийся тем, что идентифицируют распределение эффективного атомного номера в молочной железе, для чего вычисляют распределение логарифмов числа фотонов, прошедших молочную железу без взаимодействия с ней на двух различных энергиях излучения с последующим вычислением их отношения, и визуализируют распределение эффективного атомного номера по этому отношению.