Фармацевтическая гепатопротекторная композиция и способ лечения
Иллюстрации
Показать всеИзобретение относится к области медицины и фармации, а именно к фармацевтической гепатопротекторной композиции для уменьшения оксидативного стресса и ингибирования реакций перекисного окисления липидов, предназначенной для лечения и/или профилактики заболевания печени, выбранного из группы, включающей вирусный гепатит типов А, В, С, D и Е и алкогольный гепатит, содержащей в терапевтически эффективном количестве тиоктовую (альфа-липоевую) кислоту, флаванолигнаны, глицирризиновую кислоту или ее фармацевтически приемлемую соль и фармацевтически приемлемый носитель, отличающейся тем, что дополнительно содержит терапевтически эффективное количество флакозида, селена или его фармацевтически приемлемого производного и акридонуксусной кислоты или ее фармацевтически приемлемой соли, и к способу лечения заболевания, выбранного из группы, включающей вирусный гепатит типов А, В, С, D и Е и алкогольный гепатит, включающему пероральное введение фармацевтической композиции по изобретению с периодичностью 2-3 раза в сутки. 2 н. и 18 з.п. ф-лы, 4 ил., 1 табл.
Реферат
Настоящее изобретение относится к области медицины и фармации, а именно к фармацевтической композиции для лечения и/или профилактики гепатитов вирусной и/или алкогольной этиологии. Более конкретно, изобретение относится к фармацевтической гепатопротекторной композиции для лечения и/или профилактики гепатитов вирусной и/или алкогольной этиологии, содержащей в терапевтически эффективном количестве тиоктовую (альфа-липоевую) кислоту, флаванолигнаны, глицирризиновую кислоту или ее фармацевтически приемлемую соль и фармацевтически приемлемый носитель, отличающейся тем, что дополнительно содержит терапевтически эффективное количество флакозида, селена или его фармацевтически приемлемого производного и акридонуксусной кислоты или ее фармацевтически приемлемого производного, и к способу лечения гепатитов вирусной этиологии, включающему пероральное введение указанной фармацевтической композиции.
Вирусные гепатиты являются одной из ведущих групп заболеваний в структуре инфекционной патологии. Широкая распространенность, высокая заболеваемость, длительность течения с наклонностью к тяжелым формам, зачастую приводящим к осложнениям, нередкое формирование затяжного и хронического течения, а также возможность исхода инфекционного процесса в малигнизацию обусловливают необходимость углубленного изучения вопросов патогенеза, клиники и лечения этой группы заболеваний.
Первостепенное значение в последние десятилетия приобретают вирусные гепатиты с парентеральным путем передачи, этиологическую структуру которых связывают не в последнюю очередь с распространенностью наркомании. Риск заражения вирусными гепатитами среди этого контингента, по данным ВОЗ, составляет от 50 до 90%.
Патологический процесс при вирусных гепатитах и токсических поражениях сопровождается выраженными метаболическими нарушениями и множественной органной патологией, зачастую приводя к развитию фиброза и цирроза печени [1].
Другой важной патологией, также приводящей при хроническом течении к циррозу или фиброзу печени, является алкогольный гепатит.
Термин «алкогольный гепатит» применяется для обозначения острых дегенеративных и воспалительных поражений печени, обусловленных алкоголем и способных в большом числе случаев прогрессировать в цирроз печени. Алкогольный гепатит - один из основных вариантов алкогольной болезни печени, наряду с алкогольным фиброзом считается предвестником или начальной стадией цирроза. Это обозначение лишено указаний на временную протяженность процесса. Целесообразно раздельное рассмотрение острого и хронического алкогольного гепатита. При приеме внутрь около 90% алкоголя метаболизируются в печени с образованием ацетальдегида, вещества, поражающего клетки печени - гепатоциты. Алкоголь и его метаболиты запускают каскад химических реакций в организме, приводящих к гипоксии гепатоцитов и, в конечном итоге, к некрозу клеток печени.
Алкогольный гепатит - диффузный воспалительный процесс в печеночной ткани, являющийся результатом токсического поражения печени алкоголем и продуктами его распада. Это, как правило, хроническое заболевание, развивающееся через 5-7 лет от начала регулярного употребления алкоголя.
Из уровня техники [2] известна биологически активная добавка с гепатопротекторными свойствами на основе компонентов растительного происхождения, предназначенная для снижения алкогольной зависимости и содержащая в качестве компонентов растительного происхождения порошок корня Куджу, экстракт Куджу, корень одуванчика, корень желтокорня канадского, листья алоэ, Готу Кола, силимарин, корень горечавки, дополнительно содержит пантотеновую кислоту или пантотенат кальция, альфа-липоевую кислоту, N-ацетилцистеин и L-глутатион. Указанная добавка является не фармацевтической композицией, а БАД, и не может быть предложена в качестве прототипа настоящего изобретения; кроме того, из описания к указанному патенту не следует, что она может быть использована в комплексном лечении гепатитов, особенно вирусных.
Ранее в уровне техники [3] было показано, что комбинация альфа-липоевой (тиоктовой) кислоты, силимарина и селена может быть успешно использована в лечении гепатита С.
Тиоктовая (альфа-липоевая) кислота (1,2-Дитиолан-3-пентановая кислота) обладает гепатопротекторным, дезинтоксикационным, гипохолестеринемическим, гиполипидемическим, антиоксидантным действием. Является коферментом окислительного декарбоксилирования пировиноградной кислоты и альфа-кетокислот, нормализует энергетический, углеводный и липидный обмены, регулирует метаболизм холестерина. Улучшает функции печени, снижает повреждающее влияние на нее эндогенных и экзогенных токсинов.
После приема внутрь быстро и достаточно полно всасывается, Сmax достигается через 50 мин. Биодоступность составляет около 30% (вследствие пресистемной биотрансформации). В печени окисляется и конъюгирует. Экскретируется почками в виде метаболитов (80-90%) с Т1/2 20-50 мин. Общий плазменный клиренс - 10-15 мл/мин.
На эффективность применения альфа-липоевой кислоты при алкогольном поражении печени указано в работе [4].
Силимарин представляет собой сумму флавоноидов из плодов расторопши пятнистой, обладает гепатопротективным действием. Инактивирует свободные радикалы в печени, прерывает процесс перекисного окисления липидов и препятствует разрушению клеточных структур. В поврежденных гепатоцитах стимулирует синтез структурных и функциональных белков, стабилизирует клеточные мембраны, предотвращает потерю трансаминаз, ускоряет регенерацию клеток печени. Полностью и быстро всасывается из ЖКТ. В печени метаболизируется путем конъюгации. Выводится преимущественно кишечником, куда попадает с желчью, в незначительной степени - с мочой. Не кумулирует.
Улучшает состояние больных с заболеваниями печени, нормализует лабораторные показатели (активность трансаминаз, гамма-глутамилтрансферазы, щелочной фосфатазы, уровень билирубина и др.).
Показан при токсических повреждениях печени, хроническом гепатите (невирусной этиологии), циррозе печени (в составе комплексной терапии), состоянии после перенесенного гепатита, хронических интоксикациях (в т.ч. профессиональных), длительном приеме лекарств, алкоголизме.
Селен представляет собой эссенциальный микроэлемент, необходимый для нормального функционирования клеток. Принимает участие в клеточном дыхании, синтезе нуклеиновых кислот, поддерживает действие антиоксидантов. Селен является структурным компонентом важных ферментов - антиоксидантных и гормоносинтезирующих. В частности - глютатионпероксидазы, мощной «ловушки» свободных радикалов. Селен (в форме селенметионина) потенцирует антиоксидантную активность витамина Е, активирует глутатион и совместно с витамином Е защищает мембраны клеток, митохондрий, микросом и лизосом от перекисного окисления липидов. В рамках настоящего изобретения селен, предпочтительно, применяется в форме селена метионина или селена оксида.
На возможность создания фармацевтической композиции для лечения вирусных гепатитов в форме таблеток или капсул, содержащих тиоктовую кислоту, силимарин и фармацевтически приемлемое производное селена (например, селена метионин) в соотношении 0,9:1,6:0,0004, указывается также в работе автора настоящего изобретения [5]. Однако в источнике [5] не представлено никаких данных относительно эффективности указанной композиции в лечении гепатитов.
Кроме того, было бы полезным повышение эффективности указанного препарата за счет включения в него других компонентов, обладающих противовирусной, гепатопротекторной, антитоксической и антиоксидантной активностью, таких как глицирризиновая кислота, содержащаяся в экстракте корней солодки (Glycyrrhiza glabra, Glycyrrhiza uralensis), и флакозид.
Ранее было показано, что глицирризиновая кислота или ее фармацевтически приемлемые производные могут быть с успехом использованы даже в случаях интерферон-резистентных вирусных гепатитов [6], [7], [8]. Было показано, что глицирризиновая кислота обладает противовирусным и противовоспалительным действием, подавляет репродукцию вирусов в печени и других органах за счет стимуляции продукции интерферонов, повышения фагоцитоза, увеличения активности естественных клеток-киллеров. Оказывает гепатопротекторное действие благодаря антиоксидантной и мембраностабилизирующей активности, в связи с чем на основе комбинации глицирризиновой кислоты и эссенциальных фосфолипидов ранее был разработан и зарегистрирован отечественный препарат «Фосфоглив». Глицирризиновая кислота потенцирует действие эндогенных глюкокортикостероидов, оказывая противовоспалительное и противоаллергическое действие при неинфекционных поражениях печени.
Флакозид представляет собой созданный отечественной компанией «Вилар» противовирусный, антиоксидантный и антигипоксантный, гепатопротекторный препарат растительного происхождения (из листьев бархата амурского, Phellodendron amurensis Rupr., и листьев бархата Лаваля, Phellodendron amurensis var. Lavallei Sprague, сем. рутовых (Rutaceae)).
По химической структуре является 7b Dглюкопиранозид-8(3-метилбут-2-енил)-4', 5, 7-триоксифлаваноном. Оказывает противовирусное, гепатопротекторное, антиоксидантное действие. Стабилизирует мембраны клеток, индуцирует выработку интерферона; известно [9], что флакозид обладает противовирусной активностью в отношении вирусов простого герпеса и вирусных гепатитов А и В. Флакозид показан и при хронических диффузных поражениях печени.
Из уровня техники [10] известна предлагаемая в качестве прототипа настоящего изобретения фармацевтическая композиция для лечения хронической болезни печени (включая цирроз печени и фиброз печени), вирусного гепатита, неалкогольного стеатогепатита, цирроза печени и фиброза печени, содержащая в терапевтически эффективных количествах глицирризин (или его фармацевтически приемлемое производное, включая фармацевтически приемлемую соль), экстракт шизандры, аскорбиновую кислоту, L-глутатион, силимарин, альфа-липоевую (тиоктовую) кислоту и d-альфа-токоферол, и способ лечения указанных заболеваний, включающий парентеральное или пероральное введение указанной композиции в терапевтически эффективном количестве нуждающемуся в этом пациенту. Предпочтительно, указанная композиция содержит от 1000 до 1500 мг глицирризина или его фармацевтически приемлемого производного, от 1500 до 3000 мг экстракта шизандры, от 500 до 10000 мг аскорбиновой кислоты, от 50 до 1000 мг L-глутатиона, от 80 до 1000 мг силимарина, от 150 до 1200 мг альфа-липоевой кислоты, от 200 до 1600 мкг d-альфа-токоферола. Композиция в соответствии с прототипом может быть выполнена как в виде раствора для парентерального введения, так и в виде пероральной лекарственной формы.
Тем не менее, важной остается задача создания новых комбинированных лекарственных средств для лечения гепатитов алкогольной и вирусной этиологии, воздействующих на более широкий круг этиопатогенетических звеньев заболевания.
Известно, что одним из важнейших направлений в терапии вирусных гепатитов является использование иммунокорректоров, в частности индукторов эндогенного интерферона, в частности таких как циклоферон.
Циклоферон (акридонуксусная кислота в форме N-метилглюкаминовой соли), разработанный отечественной компанией «Полисан», представляет собой низкомолекулярный индуктор раннего α-, β- и γ-интерферонов иммунокомпетентными клетками-макрофагами и Т- и В-лимфоцитами. В лейкоцитах периферической крови индуцирует синтез 2500 ЕД/мл интерферона. В тканях и органах, содержащих лимфоидные элементы, циклоферон индуцирует высокие уровни интерферона, который оказывает противовирусный, антипротозойный, антибактериальный, противоопухолевый эффект. Циклоферон способствует коррекции иммунной системы как в случае иммунодефицитов, так и при аутоиммунных состояниях. Циклоферон проявляет высокую эффективность при ревматических и системных заболеваниях соединительной ткани, подавляя аутоимунные реакции и оказывая противовоспалительное и обезболивающее действие.
Циклоферон не обладает пирогенностью. В экспериментальных исследованиях не выявлено мутагенное, терагенное, эмбриотоксическое, канцерогенное действие препарата. Хорошо сочетается с традиционными терапевтическими средствами (антибиотиками, иммунотропными препаратами и т.д.).
Циклоферон показан к применению у взрослых для профилактики и лечения герпетической и цитомегаловирусной и острой респираторной вирусной инфекции, при комплексном лечении ВИЧ-инфекции (СПИД, стадия IIА - IIIВ), при вирусных гепатитах (А, В, С, D) [11], [12], [13], при нейровирусных инфекционных заболеваниях (серозные менингиты клещевой природы, рассеянный склероз и.т.д.), при хламидийных инфекциях (урогенитальные хламидиозы, хламидийные реактивные артриты, венерическая лимфогранулема); при вторичных иммунодефицитах различной этиологии (хронические бактериальные и грибковые инфекции, послеоперационный период, ожоги и др.), при системных заболеваниях соединительной ткани (ревматоидные артриты и др. аутоиммунные заболевания), при дегенеративно-дистрофических заболеваниях суставов (деформирующий остеоартроз и спондилез); у детей - при вирусных гепатитах А, В, С, дельта, GP и ВИЧ-инфекции, при герпетической инфекции (простой герпес, цитомегаловирусная инфекция, инфекционный мононуклеоз и др.).
Неожиданно было установлено в рамках настоящего изобретения, что фармацевтическая композиция, содержащая тиоктовую (альфа-липоевую) кислоту, флаванолигнаны, глицирризиновую кислоту или ее фармацевтически приемлемую соль, а также флакозид, селен или его фармацевтически приемлемое производное и акридонуксусную кислоту (циклоферон), обладает более превосходной, в сравнении с прототипом, гепатопротекторной активностью, что и составляет неожиданный технический результат, в соответствии с настоящим изобретением, и является особенно полезной в лечении гепатитов алкогольной и вирусной этиологии.
Таким образом, в соответствии с настоящим изобретением, заявляются:
- Фармацевтическая гепатопротекторная композиция для лечения и/или профилактики гепатитов вирусной и/или алкогольной этиологии, содержащая в терапевтически эффективном количестве тиоктовую (альфа-липоевую) кислоту, флаванолигнаны, глицирризиновую кислоту или ее фармацевтически приемлемую соль и фармацевтически приемлемый носитель, отличающаяся тем, что дополнительно содержит терапевтически эффективное количество флакозида, селена или его фармацевтически приемлемого производного и акридонуксусной кислоты или ее фармацевтически приемлемой соли, и
- Способ лечения гепатитов вирусной и/или алкогольной этиологии, включающий пероральное введение фармацевтической композиции по любому из п.п.1-15 по 1-2 дозы 2-3 раза в сутки.
Термин «гепатиты вирусной этиологии» здесь и далее означает гепатиты, вызванные вирусами А, В, С, дельта, F и G.
Композицию, в соответствии с настоящим изобретением, применяют в составе комплексной терапии для лечения алкогольного и вирусных гепатитов в количестве 1-2 дозы 3 раза в сутки.
Предпочтительно, отдельные дозы фармацевтической композиции в соответствии с настоящим изобретением могут быть выполнены в форме, пригодной для перорального применения, предпочтительно в виде таблеток, желатиновых капсул (твердых или мягких), раствора или суспензии для внутреннего применения. Предпочтительно, таблетки или капсулы в соответствии с настоящим изобретением изготавливают с использованием носителей и вспомогательных компонентов, традиционных для данной области техники. Фармацевтическая композиция, в соответствии с настоящим изобретением, может быть выполнена и в виде других лекарственных форм, например суппозиториев, с использованием общепринятых для данных лекарственных форм вспомогательных компонентов.
В соответствии с настоящим изобретением, но без ограничения объема испрашиваемых притязаний, предпочтительно фармацевтически приемлемая соль глицирризиновой кислоты представляет собой натрия глицирризинат;
предпочтительно фармацевтически приемлемое производное селена представляет собой селена метионин или селена оксид, фармацевтически приемлемая соль акридонуксусной кислот представляет собой N-метилглюкаминовую соль акридонуксусной кислоты; предпочтительно флаванолигнаны представляют собой силимарин.
Наиболее предпочтительное терапевтически эффективное количество тиоктовой кислоты в одиночной дозе фармацевтической композиции в соответствии с настоящим изобретением составляет от 300 до 600 мг, наиболее предпочтительное терапевтически эффективное количество флаванолигнанов (силимарина) - от 150 до 300 мг, наиболее предпочтительное терапевтически эффективное количество флакозида составляет от 50 до 100 мг, наиболее предпочтительное терапевтически эффективное количество акридонуксусной кислоты составляет от 150 до 300 мг, наиболее предпочтительное терапевтически эффективное количество глицирризиновой кислоты или натрия глицирризината составляет от 75 до 150 мг и наиболее предпочтительное терапевтически эффективное количество селена метионина или селена оксида составляет от 50 до 150 мкг.
Нижеприведенные примеры представлены исключительно для иллюстрации настоящего изобретения, но не для ограничения объема притязаний.
Пример 1. Получение мягких желатиновых капсул
В смеситель засыпают ингредиенты лекарственного средства в следующих соотношениях, в г:
Тиоктовая кислота - 300 г,
Силимарин - 150 г,
Флакозид - 50 г,
Натрия глицирризинат - 75 г,
Селена метионин - 0,068 мг,
Циклоферон (акридонуксусная кислота) - 150 г.
Тщательно перемешивают; полученным составом заполняют мягкие желатиновые капсулы (1000 шт.), в соответствии с традиционными для данной области техники процедурами.
Пример 2. Получение таблеток
В смеситель засыпают ингредиенты лекарственного средства в следующих соотношениях, в г:
Тиоктовая кислота - 600 г,
Силимарин - 300 г,
Флакозид - 100 г,
Натрия глицирризинат - 150 г,
Селена оксид - 0,135 мг,
Циклоферон (акридонуксусная кислота) - 300 г.
Тщательно перемешивают; к полученному составу добавляют в требуемом количестве необходимые для изготовления таблеток вспомогательные вещества, традиционные в данной области техники, тщательно перемешивают и прессуют на таблетировочном прессе в таблетки (1000 шт.), в соответствии с традиционными в данной области техники процедурами.
Пример 3. Получение суспензии для перорального применения
Одна порция водной суспензии для перорального применения содержит: силимарин - 150 мг; тиоктовая кислота - 300 мг; селенметионин или селена оксид (в пересчете на содержание селена) - 50 мкг; глицирризинат натрия - 75 мг; флакозид - 70 мг; циклоферон (соль акридонуксусной кислоты с N-метилглюкамином) - 150 мг; наполнитель (лактоза) - 2400 мг; маннитол - 800 мг; натрия сахаринат -2 мг; ароматизаторы и вкусовые добавки - 30 мг.
Пример 4. Получение суппозиториев
Навески альфа-липоевой (тиоктовой) кислоты (300 г), силимарина (150 г), селенметионина (100 мг), глицирризината натрия (100 г), флакозида (75 г), циклоферона (N-метилглюкаминовой соли акридонуксусной кислоты) (150 г) смешивают, соблюдая правила смешения порошков (Гос. Фармакопея XI, вып.2, стр.150). Полученную смесь растирают с небольшим количеством расплавленной основы, вводят в оставшуюся часть расплавленной основы дробными порциями и перемешивают до получения однородной массы. Полученную суппозиторную массу фильтруют и подают на автомат для изготовления суппозиториев. Массу разливают в ячейки (1000 шт.) из пленки поливинилхлорида при +32-34°С и охлаждают при температуре +5-10°С, получая 1000 шт. суппозиториев, содержащих композицию в соответствии с изобретением.
Нижеприведенные Примеры 5-6 демонстрируют терапевтический эффект заявляемой фармацевтической композиции и подтверждают ее неожиданные преимущества в сравнении с прототипом.
Пример 5
Больной С., 35 лет, поступил 30.05.08 с диагнозом хронический активный гепатит умеренной степени алкогольного генеза. Анамнестически - болен 10 лет, злоупотребляет алкоголем. Ранее гепатопротекторами не лечился. Последнее ухудшение состояния около недели после очередного злоупотребления алкоголем.
Субъективно на момент поступления отмечалась выраженная слабость, тошнота, периодические боли в правом подреберье, потливость, снижение аппетита. Объективно выражена астенизация, субиктеричность склер и кожных покровов, гепатомегалия с уплотнением, умеренно чувствительным при пальпации краем печени (размеры печени по Курлову 12,5×10×10).
В биохимических анализах был выражен цитолитический синдром (ALT - 1,6 мкмоль/лч, AST - 1,2 мкмоль/лч, общий билирубин - 29,4 мкмоль/л, прямой - 5,4 мкмоль/л. Содержание общего белка было в норме - 70 г/л, но отмечалась диспротеинемия: альбумины составляли 52%, гамма-глобулины - 23%). Активация процессов ПОЛ выражалась в повышении содержания уровня МДА до 6,9 мкмоль/л. Серологические маркеры вирусного поражения печени не были выведены. Динамическая гепатобилисцинтиграфия показала увеличение печени в размерах, умеренное нарушение поглотительной и выраженное нарушение экскреторной функции печени. При морфологическом исследовании биоптата - выраженная дистрофия печени, негустая лимфоцитарная инфильтрация портальных полей с умеренным их расширением за счет фиброза. В пограничной пластинке встречались небольшие участки некрозов гепатитов и диффузная интралобулярная лимфоцитарная инфильтрация.
После лечения гепатопротекторной фармацевтической композицией по изобретению (в виде желатиновых капсул), содержащей 300 мг тиоктовой кислоты, 150 мг силибинина, 50 мг флакозида, 75 мг натрия глицирризината, 67,5 мкг селена оксида, и мг акридонуксусной кислоты в виде N-метилглютаминовой соли, принимаемой 2 р/сут до еды, отмечалось исчезновение тошноты, болей в правом подреберье, значительное уменьшение слабости, улучшение аппетита. Размеры печени по Курлову составляли 11х9х9 см. Положительная динамика прослеживалась и в функциональном состоянии печени в виде нормализации следующих биохимических показателей: уменьшения активности AST до 0,2 мкмоль/лч, ALT до 0,6 мкмоль/лч, общего билирубина до 8,4 мкмоль/л, отсутствия прямого билирубина, исчезновения диспротеинемии - альбумины составляли 64%, гамма-глобулины - 14%. Уменьшилась и активность ПОЛ: уровень МДА снизился до 4,7 мкмоль/л. Проведенная в динамике пункционная биопсия печени свидетельствовала о значительном уменьшении лимфоцитарной инфильтрации портальных трактов и внутри долек, также об исчезновении некрозов в пограничной пластинке.
Пример 6
Обследовано 24 пациента (18 мужчин, 6 женщин, средний возраст 33±5,0 лет) с диагнозом: хронический вирусный гепатит С. У всех пациентов в крови были выявлены антитела к HCV и показано наличие вирусной РНК.
Случайным образом пациенты были разбиты на две группы по 12 человек.
Пациенты I группы на протяжении 20 недель лечения получали 3 раза в сутки фармацевтическую композицию в соответствии с прототипом (в форме желатиновых капсул), содержащую: 500 мг глицирризиновой кислоты, 500 мг экстракт шизандры, 2 г аскорбиновой кислоты, 150 мг L-глутатиона, 250 мг силимарина, 150 мг тиоктовой кислоты и 800 мкг d-альфа токоферола.
Пациенты II группы на протяжении 20 недель лечения получали 3 раза в сутки фармацевтическую композицию в соответствии с настоящим изобретением (в форме желатиновых капсул), содержащую: 300 мг тиоктовой кислоты, 250 мг силимарина, 150 мг натрия глицирризината, 100 мг флакозида, 100 мкг селена метионина и 150 мг N-метилглюкаминовой соли акридонуксусной кислоты (циклоферона).
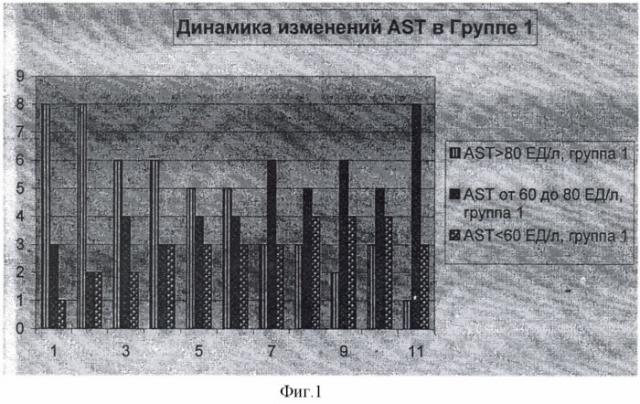
Каждые 2 недели проводился биохимический анализ крови каждого из 24 пациентов, включающий определение ферментов печени (аспартатаминотрансферазы, AST, аланинаминотрансферазы, ALT). Динамика изменений каждого из указанных биохимических показателей в обеих группах по неделям отражена в таблице и на фиг.1-4 (по оси абсцисс - неделя исследования, по оси ординат - количество больных с данным значением биохимического показателя).
| № нед. иссл. | AST, ЕД/л | ALT, ЕД/л | |
| Группа 1 | 0 | >80 - 8 чел., | 120-100 - 9 чел., |
| 60-80 - 3 чел., | 100-80 - 3 чел., | ||
| <60 - 1 чел. | 80-60 - 0 чел., | ||
| <60 - 0 чел. | |||
| 2 | >80 - 8 чел., | 120-100 - 8 чел., | |
| 60-80 - 2 чел., | 100-80 - 4 чел., | ||
| <60 - 2 чел. | 80-60 - 0 чел., | ||
| <60 - 0 чел. | |||
| 4 | >80 - 6 чел., | 120-100 - 7 чел., | |
| 60-80 - 4 чел., | 100-80 - 5 чел., | ||
| <60 - 2 чел. | 80-60 - 0 чел., | ||
| <60 - 0 чел. | |||
| 6 | >80 - 6 чел., | 120-100 - 6 чел., | |
| 60-80 - 3 чел., | 100-80 - 3 чел., | ||
| <60 - 3 чел. | 80-60 - 3 чел., | ||
| <60 - 0 чел. | |||
| 8 | >80 - 5 чел., | 120-100 - 3 чел., | |
| 60-80 - 4 чел., | 100-80 - 3 чел., | ||
| <60 - 3 чел. | 80-60 - 3 чел., | ||
| <60 - 3 чел. | |||
| 10 | >80 - 5 чел., | 120-100 - 2 чел., | |
| 60-80 - 4 чел., | 100-80 - 5 чел., | ||
| <60 - 3 чел. | 80-60 - 2 чел., | ||
| <60 - 3 чел. | |||
| 12 | >80 - 3 чел., | 120-100 - 0 чел., | |
| 60-80 - 6 чел., | 100-80 - 4 чел., | ||
| <60 - 3 чел. | 80-60 - 6 чел., | ||
| <60 - 2 чел. | |||
| 14 | >80 - 3 чел., | 120-100 - 0 чел., | |
| 60-80 - 5 чел., | 100-80 - 4 чел., | ||
| <60 - 4 чел. | 80-60 - 2 чел., | ||
| <60 - 6 чел. | |||
| 16 | >80 - 2 чел., | 120-100 - 0 чел., | |
| 60-80 - 6 чел., | 100-80 - 3 чел., | ||
| <60 - 4 чел. | 80-60 - 2 чел., | ||
| <60 - 7 чел. | |||
| 18 | >80 - 3 чел., | 120-100 - 0 чел., | |
| 60-80 - 5 чел., | 100-80 - 1 чел., | ||
| <60 - 4 чел. | 80-60 - 3 чел., | ||
| <60 - 8 чел. | |||
| 20 | >80 - 1 чел., | 120-100 - 0 чел., | |
| 60-80 - 8 чел., | 100-80 - 1 чел., | ||
| <60 - 3 чел. | 80-60 - 3 чел., | ||
| <60 - 8 чел. | |||
| Группа 2 | 0 | >80 - 11 чел., | 120-100 - 8 чел., |
| 60-80 - 1 чел, | 100-80 - 3 чел., | ||
| <60 - 0 чел. | 80-60 - 1 чел., | ||
| <60 - 0 чел. | |||
| 2 | >80- 10 чел., | 120-100 - 7 чел., | |
| 60-80 - 1 чел., | 100-80 - 3 чел., | ||
| <60 - 1 чел. | 80-60 - 2 чел., | ||
| <60 - 0 чел. | |||
| 4 | >80 - 9 чел., | 120-100 - 7 чел., | |
| 60-80 - 2 чел., | 100-80 - 2 чел., | ||
| <60 - 1 чел. | 80-60 - 3 чел., | ||
| <60 - 0 чел. | |||
| 6 | >80 - 7 чел., | 120-100 - 4 чел., | |
| 60-80 - 5 чел., | 100-80 - 5 чел., | ||
| <60 - 0 чел. | 80-60 - 3 чел., | ||
| <60 - 0 чел. | |||
| 8 | >80 - 5 чел., | 120-100 - 2 чел., | |
| 60-80 - 4 чел., | 100-80 - 7 чел., | ||
| <60 - 3 чел. | 80-60 - 3 чел., | ||
| <60 - 0 чел. | |||
| 10 | >80 - 5 чел., | 120-100 - 1 чел., | |
| 60-80 - 2 чел., | 100-80 - 7 чел., | ||
| <60 - 5 чел. | 80-60 - 2 чел., | ||
| <60 - 2 чел. | |||
| 12 | >80 - 2 чел., | 120-100 - 1 чел., | |
| 60-80 - 5 чел., | 100-80 - 5 чел., | ||
| <60 - 5 чел. | 80-60 - 3 чел., | ||
| <60 - 3 чел. | |||
| 14 | >80 - 2 чел., | 120-100 - 1 чел., | |
| 60-80 - 4 чел., | 100-80 - 2 чел., | ||
| <60 - 6 чел. | 80-60 - 6 чел., | ||
| <60 - 3 чел. | |||
| 16 | >80 - 1 чел., | 120-100 - 0 чел., | |
| 60-80 - 3 чел., | 100-80 - 0 чел., | ||
| <60 - 8 чел. | 80-60 - 6 чел., | ||
| <60 - 6 чел. | |||
| 18 | >80 - 1 чел., | 120-100 - 0 чел., | |
| 60-80 - 2 чел., | 100-80 - 0 чел., | ||
| <60 - 9 чел. | 80-60 - 4 чел., | ||
| <60 - 8 чел. | |||
| 20 | >80 - 0 чел., | 120-100 - 0 чел., | |
| 60-80 - 2 чел., | 100-80 - 0 чел., | ||
| <60 - 10 чел. | 80-60 - 2 чел., | ||
| <60 - 10 чел. |
Вирусная РНК, обнаруживавшаяся в крови в начале исследования в 100% случаев у пациентов обеих групп, к моменту окончания курса лечения выявлялась у 5 пациентов I группы и у 1 пациента II группы.
Представленные данные свидетельствуют о том, что фармацевтическая композиция в соответствии с настоящим изобретением проявляет неожиданно более высокую, в сравнении с прототипом, гепатопротекторную активность при лечении гепатитов алкогольной и вирусной этиологии, воздействуя на различные этиопатогенетические звенья гепатита вирусной и алкогольной этиологии, и оказывается неожиданно высокоэффективной в лечении данных заболеваний, что и составляет неожиданный технический результат настоящего изобретения.
Литература
1. Шульпекова, Ю.О. Острый вирусный гепатит / Ю.О.Шульпекова // Лечащий врач. - 2005. - №2. - С.20-23.
2. Патент РФ №2201247 («БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА ДЛЯ СНИЖЕНИЯ АЛКОГОЛЬНОЙ ЗАВИСИМОСТИ С ГЕПАТОПРОТЕКТОРНЫМИ СВОЙСТВАМИ»), опубл. 27.03.2003.
3. Berskon B.M. A conservative triple antioxidant approach to the treatment of hepatitis C. Combination of alpha lipoic acid (thioctic acid), sylimarin, and selenium - Med. Klin. (Munich), 1999 Oct 15; 94 Suppi 3:84-9 (реферат PubMed).
4. Marshall A.W. et al. Treatment of alcohol-related liver disease with thioctic acid: a six month randomized double-blind trial. - Gut. 1982; 23 [12]: 1088-93 (реферат PubMed).
5. Кожока Т.Г. Лекарственные средства в паразитологии и гастроэнтерологии, проблемы производства и обеспечения населения. - М.: МИЭМП, 2006, стр.99-100.
6. Orient H., Hansen B.E. et al. Biochemical and histological effects of 26 weeks of glycyrrhizin treatment in chronic hepatitis C: a randomized phase II trial. - J Hepatol. 2006 Oct; 45[4]:539-46. Epub 2006 Jim 30 (реферат PubMed).
7. Arase Y. et al. The long term efficacy of glycyrrhizin in chronic hepatitis С patients. - Cancer 1997; 79[8]: 1494-500 (реферат PubMed).
8. Van Rossum T. G. et al. Review article: glycyrrhizin as a potential treatment for chronic hepatitis C. Aliment Pharmacol Ther. 1998; 12[3]: 199-205 (реферат PubMed).
9. http://www.gastroportal.ru/php/content.php?id=706&pr^print
10. Заявка на патент США №2005123628, подана 03.12.2003, опубл. 09.06.2005.
11. Narovlianskii AN, Deriabin PG, Vershinina MIu, Mezentseva MV, Ershov FI. [Effect ofinterferon inductors on infection induced by hepatitis C virus and activity ofmRNA cytokines in cell cultures SW-13 and MT-4] - Vopr Virusol. 2002 Nov-Dec; 47[6]: 17-21 (реферат PubMed).
12. Чуйкова К.И., Гуляева О.М., Ковалева Т.А. Применение циклоферона при вирусном гепатите В и В+С на фоне опийной наркомании. [http://xxt2006.chtd.tpu.m/uploads/pdf/787_864.pdf].
13. H.В.Хомяк Циклоферон - альтернатива интерферон-терапии. -Онлайн-журнал «Провизор», №20, 2000 г. [http://www.provisor.com.ua/archive/2000/N20/cyclopheron.htm].
1. Фармацевтическая гепатопротекторная композиция для лечения и/или профилактики гепатитов вирусной и/или алкогольной этиологии, содержащая в терапевтически эффективном количестве тиоктовую (альфа-липоевую) кислоту, флаванолигнаны, глицирризиновую кислоту или ее фармацевтически приемлемую соль и фармацевтически приемлемый носитель, отличающаяся тем, что дополнительно содержит терапевтически эффективное количество флакозида, селена или его фармацевтически приемлемого производного и акридонуксусной кислоты или ее фармацевтически приемлемой соли.
2. Фармацевтическая композиция по п.1, отличающаяся тем, что гепатит вирусной этиологии представляет собой гепатит, вызванный вирусом гепатита А, или вирусом гепатита В, или вирусом гепатита С, или вирусом гепатита D, или вирусом гепатита Е, или вирусом гепатита G.
3. Фармацевтическая композиция по п.1, отличающаяся тем, что фармацевтически приемлемая соль глицирризиновой кислоты представляет собой натрия глицирризинат.
4. Фармацевтическая композиция по п.1, отличающаяся тем, что фармацевтически приемлемое производное селена представляет собой селена метионин или селена оксид.
5. Фармацевтическая композиция по п.1, отличающаяся тем, что фармацевтически приемлемая соль акридонуксусной кислоты представляет собой N-метилглюкаминовую соль акридонуксусной кислоты.
6. Фармацевтическая композиция по любому из пп.1-5, отличающаяся тем, что терапевтически эффективное количество тиоктовой (альфа-липоевой) кислоты находится в диапазоне от 300 до 600 мг.
7. Фармацевтическая композиция по любому из пп.1-5, отличающаяся тем, что терапевтически эффективное количество флаванолигнанов находится в диапазоне от 150 до 300 мг.
8. Фармацевтическая композиция по п.7, отличающаяся тем, что флаванолигнаны представляют собой силимарин.
9. Фармацевтическая композиция по любому из пп.1-5, отличающаяся тем, что терапевтически эффективное количество глицирризиновой кислоты или ее фармацевтически приемлемой соли находится в диапазоне от 75 до 150 мг.
10. Фармацевтическая композиция по любому из пп.1-5, отличающаяся тем, что терапевтически эффективное количество флакозида находится в диапазоне от 50 до 100 мг.
11. Фармацевтическая композиция по любому из пп.1-5, отличающаяся тем, что терапевтически эффективное количество селена или его фармацевтически приемлемого производного (в пересчете на селен) находится в диапазоне от 50 до 150 мкг.
12. Фармацевтическая композиция по любому из пп.1-5, отличающаяся тем, что терапевтически эффективное количество акридонуксусной кислоты находится в диапазоне от 150 до 300 мг.
13. Фармацевтическая композиция по п.1, отличающаяся тем, что выполнена в виде формы, пригодной для перорального применения.
14. Фармацевтическая композиция по п.13, отличающаяся тем, что выполнена в форме таблеток.
15. Фармацевтическая композиция по п.13, отличающаяся тем, что выполнена в форме суспензии для перорального применения.
16. Фармацевтическая композиция по п.13, отличающаяся тем, что выполнена в форме желатиновых капсул.
17. Фармацевтическая композиция по п.16, отличающаяся тем, что выполнена в форме твердых желатиновых капсул.
18. Фармацевтическая композиция по п.16, отличающаяся тем, что выполнена в форме мягких желатиновых капсул.
19. Фармацевтическая композиция по п.1, отличающаяся тем, что выполнена в форме суппозиториев.
20. Способ лечения гепатитов вирусной и/или алкогольной этиологии, включающий пероральное введение фармацевтической композиции по любому из пп.1-18 по 1-2 дозы 2-3 раза в сутки.