Стерилизация под высоким давлением для заключительной стерилизации фармацевтических препаратов и медицинских изделий
Иллюстрации
Показать всеИзобретение относится к области стерилизации фармацевтических препаратов в виде дисперсии мелких частиц или капель и может быть использовано в фармацевтической промышленности. Способ стерилизации динамической дисперсионной системы, обладающей стабильным состоянием и нестабильным состоянием, включает воздействие на дисперсионную систему малых частиц или капель давления выше 0,25 МПа для повышения температуры системы до температуры выше 100°С в течение периода времени, достаточного для обеспечения стерильности системы, и снятие давления с указанной дисперсионной системы прежде, чем она перейдет в нестабильное состояние. При этом дисперсионная система включает дисперсию микро- и наночастиц в форме малых частиц или капель и имеет стабильное состояние и нестабильное состояние. Частицы или капли указанной дисперсионной системы включают фармацевтически активное соединение, связанное с эксципиентом, включающим поверхностно-активное вещество. Изобретение позволяет обеспечить стабилизацию ассоциатов фармацевтически активного соединения и эксципиента, представленных в виде дисперсионной системы частиц или капель, в процессе стерилизации при повышенной температуре. 2 н. и 35 з.п. ф-лы, 25 ил., 1 табл.
Реферат
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Область техники
В соответствии с настоящим изобретением предлагается способ стерилизации фармацевтических препаратов, например, дисперсии мелких частиц или капель фармацевтически активного соединения с использованием технологий заключительной стерилизации под высоким давлением и изделий из данного соединения.
Уровень техники
Количество органических соединений в рецептурных формах, разработанных для лечебно-терапевтических или диагностических воздействий, которые слабо растворяются или не растворяются в водных растворах, постоянно возрастает. Данные лекарственные средства представляют проблемы для их введения по путям введения, обычно используемым медицинским персоналом. Одним из возможных решений данной проблемы является получение мелких частиц нерастворимого потенциального лекарственного средства путем приготовления из них дисперсий микро- и наночастиц. Преимущества, получаемые от данной рецептуры, могут включать в себя более высокую нагрузку, меньшую токсичность, повышенную степень предельной растворимости и/или растворения лекарственного средства, повышенную эффективность и повышенную стабильность лекарственного средства.
Таким образом, лекарственные средства, которые прежде были непригодны для приготовления рецептуры в системе на водной основе, можно сделать пригодными для введения разными путями. Препараты дисперсий мелких частиц водонерастворимых лекарственных средств можно вводить внутривенным, оральным, пульмональным, местным, интратекальным, офтальмическим, назальным, буккальным, ректальным, вагинальным и трансдермальным путями. Оптимальный диапазон размеров для данных дисперсий обычно зависит от конкретного пути, характеристик частиц и других факторов, например, при внутривенном введении желательно, чтобы размер частиц был меньше, чем приблизительно 7 мкм. Частицы должны быть в данном диапазоне размеров и неагрегированными для безопасного прохода по капиллярам, не вызывая эмболии (Alien et al., 1987; Davis and Taube, 1978; Schroeder et al., 1978; Yokel et al., 1981).
В зависимости от пути введения и других факторов данные дисперсии мелких частиц должны удовлетворять некоторым требованиям стерильности. Одним из полезных способов стерилизации является обычное заключительное автоклавирование дисперсий мелких частиц при 121°C. Хорошо известно, что фармацевтические суспензии предохраняют от роста частиц и/или агрегации во время хранения при нормальных температурах присутствием поверхностно-активных веществ (ПАВ) в рецептурах. Однако даже в присутствии данных стабилизирующих поверхностно-активных вещест суспензии из мелких частиц часто в какой-то степени термочувствительны и не могут выдерживать заключительное автоклавирование. Фармацевтически активный ингредиент, поверхностно-активные вещества и агрегаты лекарственное средство/поверхностно-активное вещество должны оставаться как физически, так и химически стабильными во время всего стерилизационного цикла при 121°C. Как известно, химическая чувствительность дисперсий мелких частиц к заключительному автоклавированию является функцией как времени стерилизации, так и температуры. Способы уменьшения химической нестабильности обычно предусматривают способы высокотемпературной кратковременной стерилизации. В данном случае консервация термолабильных препаратов и деструкция микроорганизмов основаны на различии скоростей, соответственно, химического распада и инактивации. Значительной проблемой данного процесса является обеспечение достаточно быстрой теплопередачи, чтобы равномерная температура была по всему объему изделия во время очень короткого времени воздействия.
Очень сложно также обеспечить физическую стабильность агрегатов лекарственное средство/поверхностно-активное вещество. Мелкие частицы часто агрегируются, растут и/или разлагаются под действием тепла, из-за чего конечная дисперсия становится непригодной для использования. Кроме того, агрегаты поверхностно-активного вещества могут необратимо отделяться от фармацевтически активного соединения. Например, один механизм агрегирования или коалесценции дисперсий из твердых субмикронных частиц может быть непосредственно связан с осаждением стабилизирующего поверхностно-активного вещества в процессе стерилизации при температурах выше точки помутнения поверхностно-активного вещества. Термин «точка помутнения» относится к разделению изотропного раствора поверхностно-активных веществ на одну фазу с высоким содержанием поверхностно-активного вещества и одну фазу с низким содержанием поверхностно-активного вещества. При данных температурах поверхностно-активное вещество часто отделяется от частицы, что вызывает агрегирование и/или рост незащищенных частиц. Поэтому в ряде патентов (например, в патентах США №5298262, 5346702, 5470583 и 5336507) предлагается использование ионных и неионных модификаторов точки помутнения для стабилизации суспензии частиц при автоклавировании. Данные модификаторы повышают точку помутнения поверхностно-активного вещества выше 121°C, что предотвращает отделение поверхностно-активного вещества от частицы лекарственного средства и в результате стабилизируют частицы от роста во время заключительной стерилизации.
В патенте США №6267989 показано также, что наиболее важным для сведения к минимуму роста и нестабильности при автоклавировании является оптимальный диапазон размеров. В патенте №6267989 сообщается, что максимальная стабильность проявляется, когда, по меньшей мере, 50% частиц лекарственного средства, стабилизированных поверхностно-активным веществом, имеют средневесовой размер частиц 150-350 нм.
Поэтому сохраняется потребность в разработке новых и усовершенствованных способов заключительной стерилизации дисперсий мелких частиц в области фармацевтики, и настоящее изобретение направлено на удовлетворение данной потребности.
Системы и растворы, отличные от дисперсий частиц, часто требуют стерилизации перед применением. Примеры включают растворенные фармацевтические растворы, растворы для почечного применения (например, перитонеального диализа) и другие формы фармацевтических препаратов, таких как липидные эмульсии. Другие примеры включают медицинские устройства одноразового пользования, например, пакеты с фармацевтическими препаратами (часто изготовленными из пластифицированного PVC или других пластиков), пакеты с кровью, диализаторы, системы для использования в автоматизированных устройствах (например, устройствах сепарации крови, инфузионных насосах и т.д.). Данные системы могут быть чувствительными к традиционным технологиям стерилизации, например, стерилизации гамма-излучением, стерилизации ETO (этиленоксидом) или автоклавированию. Например, содержащие глюкозу растворы подвержены разложению глюкозы или агрегированию в результате стерилизации по традиционным технологиям. Поэтому существует также потребность в создании усовершенствованных технологий стерилизации, которые обеспечивают надлежащую стерилизацию с небольшим, вплоть до нулевого, риском для стерилизуемой системы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В соответствии с настоящим изобретением предлагается способ стерилизации систем. Данные системы могут представлять собой, но без ограничения нижеследующим, композиции, например дисперсии частиц, и устройства, например контейнеры, которые могут содержать водные растворы, например, фармацевтические препараты. Способ обладает преимуществом обеспечения стерилизации без существенного снижения эффективности данных систем. Изобретение дополнительно обеспечивает стерилизованные фармацевтические препараты. К подходящим контейнерам относится любой контейнер, который стабилен в условиях настоящего способа, включая устройства доставки лекарственных средств, содержащие медицинские растворы.
Способ включает в себя подвод тепловой энергии к системе и поддерживания системы под давлением более 0,25 МПа в течение достаточного периода времени, чтобы сделать систему стерильной. В предпочтительном варианте система будет достигать температуры свыше 70°C. Этапы подвода энергии и давления выполняют одновременно в течение периода времени, по меньшей мере, достаточного для стерилизации системы. Затем системе можно предоставить возможность возврата к температуре и давлению окружающей среды для использования.
Способ можно применять к пустым контейнерам или контейнерам, содержащим любой из широкого множества растворов, включая растворы для парентерального введения, растворы для острого или хронического гемодиализа, гемофильтрационный или гемодиафильтрационный растворы для острого или хронического перитонеального диализа, амбулаторного перитонеального диализа и автоматизированного перитонеального диализа.
Способ особенно полезен при стерилизации растворов, которые содержат глюкозу. Низкая температура, используемая для стерилизации, сводит к минимуму разложение глюкозы, который происходит при более высоких температурах. Таким образом, способ можно использовать для стерилизации растворов, содержащих глюкозу, чтобы глюкоза сохранялась, по существу, без разложения. В предпочтительном варианте более приблизительно 75% глюкозы не разлагается, в более предпочтительном варианте не разлагается более приблизительно 80% глюкозы, еще более предпочтительными являются стерилизованные растворы, в которых не разлагается более приблизительно 85% или более приблизительно 90% или, даже предпочтительнее более приблизительно 95% глюкозы.
Эти и другие аспекты и признаки настоящего изобретения обсуждаются со ссылками на прилагаемые чертежи и описание.
КРАТКОЕ ОПИСАНИЕ ФИГУР
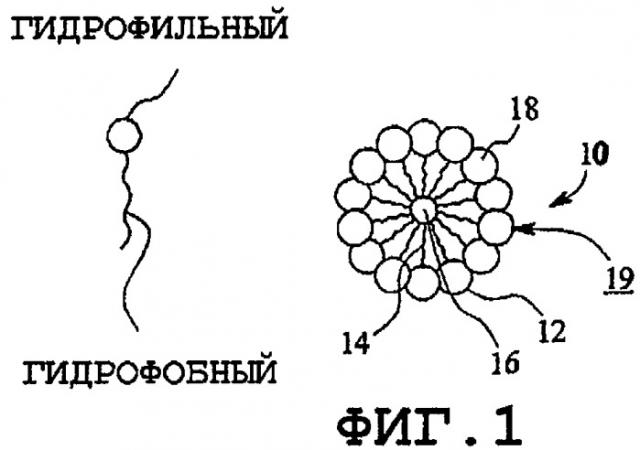
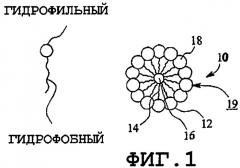
Фиг.1 - мицелла;
фиг.2 - обратная мицелла;
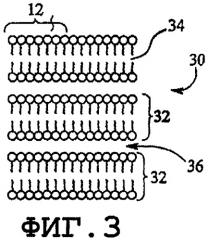
фиг.3 - ламеллярная фаза;
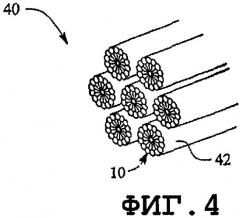
фиг.4 - гексагональная фаза;
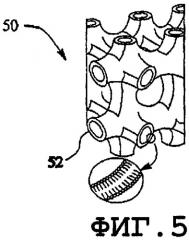
фиг.5 - кубическая фаза;
фиг.6 - график зависимости давления и температуры от времени;
фиг.7 - кривая распределения размеров частиц (пример 1);
фиг.8 - кривая распределения размеров частиц контрольного образца (пример 1);
фиг.9 - стерилизационный цикл высокого давления (пример 1);
фиг.10 - кривая распределения размеров частиц;
фиг.11 - контейнер для текучих материалов;
фиг.12 - многокамерный контейнер со вскрываемым изолирующим слоем;
фиг.13 - однослойная пленка;
фиг.14 - двухслойная пленка;
фиг.15 - трехслойная пленка;
фиг.16 - трехслойная пленка;
фиг.17 - четырехслойная пленка;
фиг.18 - четырехслойная пленка;
фиг.19 - пятислойная пленка;
фиг.20 - шестислойная пленка;
фиг.21 - шестислойная пленка;
фиг.22 - семислойная пленка;
фиг.23 - шприц;
фиг.24 - картридж для устройства введения лекарственного средства; и
фиг.25 - устройства для ввода жидкости.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Хотя осуществление настоящего изобретения возможно в многочисленных различных вариантах, на чертежах изображены и ниже подробно описаны конкретные варианты осуществления настоящего изобретения в предположении, что настоящее описание следует считать иллюстрацией принципов изобретения и нельзя рассматривать как предназначенное для ограничения изобретения конкретными представленными вариантами осуществления.
В соответствии с настоящим изобретением предлагается способ стерилизации системы без существенного снижения пригодности, стабильности и/или эффективности препарата. Согласно изобретению предлагается способ стерилизации динамической системы (т.е. системы, способной к переходу из стабильного состояния в нестабильное состояния), при этом систему подвергают воздействию высокого давления в течение времени, достаточного для стерилизации системы, не вызывая перехода системы из стабильного состояния в нестабильное состояние.
Для целей настоящего описания термин «стерилизация» и его варианты должен означать уничтожение бактерий, вирусов, простейших одноклеточных организмов или других биологических организмов или борьбу с ними в системе, чтобы система обеспечивала снижение риска инфекции при использовании млекопитающими, предпочтительно человеком. Предпочтительные способы по настоящему изобретению должны стерилизовать систему до момента, когда все или почти все биологические организмы убиты или сделаны неспособными к воспроизводству.
В предпочтительном варианте способ используют для стерилизации фармацевтической системы. Фармацевтический препарат может быть приготовлен при помощи многочисленных технологий, известных в данной области техники, и тех, которые еще будут разработаны. Как правило, способ обеспечивает проведение стерилизации системы под высоким давлением. Способ является целесообразным для стерилизации под высоким давлением дисперсий мелких частиц. Согласно изобретению дополнительно обеспечиваются стерилизованные фармацевтические дисперсии.
Технологии стерилизации под высоким давлением согласно настоящему изобретению обеспечивают стерилизацию дисперсий мелких частиц без сопутствующего существенного распада фармацевтически активного соединения, разложения поверхностно-активных веществ или изменения скопления лекарственное средство/поверхностно-активное вещество. Кроме того, теплота передается мгновенно по всей дисперсии по причине быстрого адиабатического нагревания препарата на этапе сжатия. Предполагается, что технологии стерилизации под высоким давлением пригодны для применения ко многим дисперсиям мелких частиц, содержащим различные фармацевтические соединения в контейнерах ряда конфигураций.
В целом, способ обеспечивает проведение стерилизации фармацевтического препарата под высоким давлением. Фармацевтический препарат может быть приготовлен при помощи многочисленных технологий, известных в данной области техники, и тех, которые еще будут разработаны. Технологии стерилизации под высоким давлением хорошо подходят для стерилизации препаратов во многих различных формах, включая фармацевтически эффективное соединение в сухой или порошковой форме, жидкой форме, газообразной форме, или диспергированное до мелких частиц или капель в водной или органической средах. В предпочтительном варианте подлежащая стерилизации система будет содержать некоторое количество воды. Как доказано, присутствие воды обеспечивает особенно эффективное снижение концентрации активных микроорганизмов. Широко известно, что для сообщения фармацевтически активным соединениям устойчивости к агрегированию и изменению размеров используют поверхностно-активные вещества. Поверхностно-активные вещества можно связывать с фармацевтически активным соединением любым из многих способов, широко известных в данной области. Технологии стерилизации под высоким давлением в соответствии с настоящим изобретением обеспечивают стерилизацию, не вызывая распада фармацевтически активного соединения или не вызывая значительного отщепления поверхностно-активных веществ от фармацевтически активного соединения. Способ и изделия по настоящему изобретению не нуждаются в применении химических модификаторов точки помутнения. Термин «точка помутнения» относится к усилению мутности фармацевтического препарата, когда изменение физической характеристики препарата, например, изменение температуры или уровня pH, или другой физической характеристики вынуждает поверхностно-активное вещество отщепляться от фармацевтически активного соединения.
Предполагается, что технологии стерилизации под высоким давлением пригодны к применению со многими органическими соединениями.
I. Фармацевтически активные соединения
Способ согласно настоящему изобретению пригоден для стерилизации фармацевтических препаратов в общем. В предпочтительных способах настоящего изобретения фармацевтически активный ингредиент будет таким, что он ассоциируется с диспергированной гидрофобной областью (например, гидрофобной фазой агрегированного поверхностно-активного вещества, циклодекстриновой полости, капли масла) в водном растворе. Фармацевтически активные соединения могут быть выбраны из терапевтических средств, средств для лечения почек, диагностических средств, косметических средств, пищевых добавок и пестицидов.
Фармацевтически активные средства могут быть выбраны из множества известных классов, например, но без ограничения нижеследующим: анальгетики, анестетики, аналептики, адренергические средства, адреноблокирующие средства, адренолитики, адренокортикоиды, адреномиметики, антихолинергические средства, антихолинэстеразные средства, противосудорожные средства, алкилирующие средства, алкалоиды, аллостерические ингибиторы, анаболические стероиды, препараты для снижения аппетита, антацидные средства, антидиарейные средства, антидоты, антифолические средства, антипиретики, противоревматические средства, психотерапевтические средства, нервноблокирующие средства, противовоспалительные средства, противоглистные средства, антиаритмические средства, антибиотики, антикоагулянты, антидепрессанты, противодиабетические средства, противоэпилептические средства, противогрибковые средства, антигистаминные средства, антигипертензивные средства, мускариновые холиноблокаторы, противомикобактериальные средства, противомалярийные средства, антисептики, антибластомные средства, противопротозойные средства, иммунодепрессанты, иммуностимуляторы, антитиреоидные средства, противовирусные средства, анксиолитические седативные средства, вяжущие средства, бета-адреноблокаторы, рентгеноконтрастные вещества, кортикостероиды, противокашлевые средства, диагностические средства, диагностические визуализирующие средства, мочегонные средства, допаминергические средства, кровоостанавливающие средства, гематологические средства, модификаторы гемоглобина, гормоны, снотворные средства, иммунологические средства, антигиперлипидемические или другие средства регулирования липидного обмена, мускариновые холинорецепторы, миорелаксанты, парасимпатомиметические средства, паратиреоидный кальцитонин, простагландины, радиофармацевтические средства, седативные средства, половые гормоны, противоаллергические средства, раздражители, симпатомиметические средства, тиреоидные средства, сосудорасширяющие средства, вакцины, витамины и ксантины. Антибластомные или противораковые средства, включая, но без ограничения нижеследующим, паклитаксел и производные соединения и другие антибластомные средства, выбранные из группы, состоящей из алкалоидов, антиметаболитов, ингибиторов ферментов, алкилирующих средств и антибиотиков. Лечебное средство может также представлять собой биопрепарат, который содержит, но без ограничения нижеследующим, белки, полипептиды, углеводы, полинуклеотиды и нуклеиновые кислоты. Белок может представлять собой антитело, которое может быть поликлональным или моноклональным.
Диагностические средства включают средства для рентгенологических исследований и рентгеноконтрастные вещества. Примеры средств для рентгенологических исследований включают в себя WIN-8883 (этил-3,5-диацетамидо-2,4,6-трийодбензоат), известный так же, как сложный этиловый эфир диатразоевой кислоты (EEDA), WIN 67722, т.е. (6-этокси-6-оксогексил-3,5-бис(ацетамидо)-2,4,6-трийодбензоат; этил-2-(3,5-бис(ацетамидо)-2,4,6-трийодбензоилокси)бутират (WIN 16318); этилдиатризоксиацетат (WIN 12901); этил-2-(3,5-бис(ацетамидо)-2,4,6-трийодбензоилокси)пропионат (WIN 16923); N-этил-2-(3,5-бис(ацетамидо)-2,4,6-трийодбензоилоксиацетамид (WIN 65312); изопропил-2-(3,5-бис(ацетамидо)-2,4,6-трийодбензоилокси)ацетамид (WIN 12855); диэтил-2-(3,5-бис(ацетамидо)-2,4,6-трийодбензоилоксималонат (WIN 67721); этил-2-(3,5-бис(ацетамидо)-2,4,6-трийодбензоилокси)фенилацетат (WIN 67585); [[3,5-бис(ацетиламино)-2,4,5-трийодбензоил]окси]бис(1-метил)эфир пропандионовой кислоты (WIN 68165); и 3,5-бис(ацетиламино)-2,4,6-трийод-4-(этил-3-этокси-2-бутеноат)эфир бензойной кислоты (WIN 68209). Предпочтительные контрастные вещества включают в себя такие вещества, которые, по расчетам, относительно быстро разлагаются в физиологических условиях, что сводит к минимуму любую воспалительную реакцию, обусловленную частицами. Разложение может происходить в результате ферментативного гидролиза, солюбилизации карбоновых кислот при физиологическом уровне pH или действия других механизмов. Следовательно, предпочтительными могут быть слаборастворимые йодированные карбоновые кислоты, такие как йодипамид, диатризойная кислота и метризойная кислота, вместе с гидролитически нестабильными йодированными продуктами, например, WIN 67721, WIN 12901, WIN 68165 и WIN 68209 или другие.
Другие рентгеноконтрастные вещества включают в себя, но без ограничения нижеследующим, препараты в форме частиц средств для визуализации с помощью ядерного магнитного резонанса, например, хелаты гадолиния или другие парамагнитные контрастные вещества. Примерами данных соединений являются гадопентетат димеглюмин (Magnevist®) и гадотеридол (Prohance®).
Описание данных классов терапевтических средств и диагностических средств и перечни продуктов каждого класса можно найти в публикации Martindale, The Extra Pharmacopoeia, Twenty-ninth Edition, The Pharmaceutical Press, London, 1989, которая включена в настоящее описание путем ссылки и является его частью. Терапевтические средства и диагностические средства имеются в продаже и/или могут быть приготовлены методами, известными в данной области.
Средства для лечения почек включают в себя растворы для непрерывного амбулаторного диализа, автоматизированного перитонеального диализа и гемодиализа.
Косметическое средство представляет собой любой активный ингредиент, способный к косметическому воздействию. Примерами данных активных ингредиентов могут быть, inter alia, мягчители, увлажнители, средства замедления образования свободных радикалов, противовоспалительные средства, витамины, депигментирующие средства, средства от угревой сыпи, противосеборейные средства, кератолитические средства, средства для похудения, тональные средства для кожи и солнцезащитные средства и, в частности, линолевая кислота, ретинол, ретиноевая кислота, сложные алкиловые эфиры аскорбиновой кислоты, полиненасыщенные жирные кислоты, сложные эфиры никотиновой кислоты, токоферол никотинат, неомыляемые вещества риса, соевых бобов или ши, керамиды, оксикислоты, например, гликолевая кислота, производные соединения селена, антиоксиданты, бета-каротин, гамма-оризанол и стеарилглицерат. Косметические средства имеются в продаже и/или могут быть приготовлены методами, известными в данной области.
Примерами пищевых добавок, предполагаемых для использования при практической реализации настоящего изобретения, являются, но без ограничения нижеследующим, белки, углеводы, водорастворимые витамины (например, витамин C, витамины группы B и т.п.), жирорастворимые витамины (например, витамины A, D, E, K и т.п.) и растительные экстракты. Пищевые добавки имеются в продаже и/или могут быть приготовлены методами, известными в данной области.
Следует понимать, что термин пестицид включает в себя гербициды, инсектициды, акарициды, нематоциды, средства против эктопаразитов и фунгициды. Примеры классов соединений, к которым могут принадлежать пестициды по настоящему изобретению, включают в себя мочевины, триазины, триазолы, карбаматы, сложные эфиры фосфорной кислоты, динитроанилины, морфолины, ацилаланины, пиретроиды, сложные эфиры бензиловой кислоты, простые дифениловые эфиры и полициклические галоидзамещенные углеводороды. Конкретные примеры пестицидов в каждом из данных классов перечислены в руководстве Pesticide Manual, 9th Edition, British Crop Protection Council. Пестициды имеются в продаже и/или могут быть приготовлены методами, известными в данной области.
В предпочтительном варианте фармацевтически активные соединения являются слабо растворимыми в воде. Под «слабой растворимостью в воде» понимается растворимость соединения в воде ниже приблизительно 10 мг/мл и, предпочтительно, ниже 1 мг/мл. Данные слаборастворимые в воде средства являются наиболее подходящими для препаратов в форме водных суспензий, поскольку варианты создания рецептур данных средств в водных средах ограничены.
Настоящее изобретение можно также практически осуществить с водорастворимыми фармацевтически активными соединениями в некоторых случаях посредством включения данных соединений в твердую гидрофобную диспергированную фазу (например, в полилактат-полигликолятном сополимере или твердых липидных наночастицах), или инкапсулирования данных соединений в окружающий агрегат поверхностно-активного вещества, который является непроницаемым для фармацевтического соединения. Примеры агрегатов поверхностно-активного вещества включают в себя, но без ограничения, везикулы и мицеллы. Примеры водорастворимых фармацевтических средств включают в себя, но без ограничения нижеследующим, простые органические соединения, белки, пептиды, нуклеотиды, олигонуклеотиды и углеводы.
II. Размер частиц дисперсии и пути введения
Когда фармацевтические средства по настоящему изобретению находятся в форме частиц (т.е. не растворены в растворителе), частицы будут иметь средний эффективный размер частиц, как правило, меньше приблизительно 100 мкм, при измерении с помощью способов динамического светорассеяния, например, фотокорреляционной спектроскопии, дифракции лазерного излучения, малоуглового рассеяния лазерного излучения (LALLS), среднеуглового рассеяния лазерного излучения (MALLS), теневых методов (например, методом Коутлера), реологии или микроскопии (оптической или электронной). Однако частицы могут быть приготовлены с размерами в широком диапазоне, например, от приблизительно 100 мкм до приблизительно 10 нм, от приблизительно 10 мкм до приблизительно 10 нм, от приблизительно 2 мкм до приблизительно 10 нм, от приблизительно 1 мкм до приблизительно 10 нм, от приблизительно 400 нм до приблизительно 50 нм, от приблизительно 200 нм до приблизительно 50 нм или в любом диапазоне или комбинации внутри упомянутых диапазонов. Предпочтительный средний эффективный размер частиц зависит от таких факторов, как предполагаемый путь введения, рецептуры, растворимости, токсичности и биодоступности соединения.
Чтобы частицы были пригодными для парентерального введения, средний эффективный размер частиц должен быть предпочтительно меньше, чем приблизительно 7 мкм, и предпочтительнее меньше, чем приблизительно 2 мкм, или в любом диапазоне или комбинации внутри упомянутых диапазонов. Парентеральное введение включает в себя внутривенную, внутриартериальную, интратекальную, интраперитонеальную, внутриглазную, внутрисуставную, интрадуральную, внутрижелудочковую, интраперикардиальную, внутримышечную, интрадермальную или подкожную инъекцию.
Размеры частиц для лекарственных форм для орального применения могут превосходить 2 мкм. Размеры частиц могут изменяться в диапазоне до приблизительно 100 мкм, при условии, что частицы обладают достаточной биодоступностью и другими характеристиками дозированных форм для орального применения. Лекарственные формы для орального применения включают в себя таблетки, капсулы, таблетки в виде капсулы, капсулы с мягким и плотным гелем или другой носитель для введения лекарственного средства оральным путем.
Кроме того, настоящее изобретение применимо для частиц фармацевтически активного соединения в форме, пригодной для пульмонального введения. Размеры частиц для дозированных форм для пульмонального применения могут превосходить 500 нм и обычно меньше, чем приблизительно 10 мкм. Частицы в суспензии можно аэрозолировать и вводить с помощью распылителя для пульмонального введения. В качестве альтернативы, частицы можно вводить в виде сухого порошка с помощью ингалятора для сухого порошка после удаления жидкой фазы из суспензии, или сухой порошок можно ресуспендировать в неводном пропелленте для введения дозирующим ингалятором. Подходящим пропеллентом является, например, гидрофторуглерод (HFC) типа HFC-134a (1,1,1,2-тетрафторэтан) и HFC-227ea (1,1,1,2,3,3,3-гептафторпропан). В отличие от хлорфторуглеродов (CFC) HFC меньше или совсем не разрушают озоновый слой.
Частицы и капли органических соединений с размерами в вышеприведенных диапазонах далее совокупно именуются мелкими частицами.
Дозированные формы для введения другими путями, например, назальным, местным, глазным, сбуккальным, ректальным, вагинальным, трансдермальным и т.п. также можно готовить из частиц, выполненных в соответствии с настоящим изобретением.
В соответствии с настоящим изобретением можно стерилизовать другие формы растворов. Примеры данных растворов включают в себя фармацевтические препараты для парентерального введения и растворы для почечного диализа, например, растворы для гемодиализа и перитонеального диализа.
III. Препарат из дисперсий мелких частиц
Существует много технологий для приготовления фармацевтических препаратов из мелких частиц фармацевтически активных соединений. Рассмотренные ниже технологии стерилизации пригодны для стерилизации данных фармацевтических препаратов. Ниже приведено краткое описание характерных, но не исчерпывающих примеров методологий для создания мелких частиц фармацевтически активных соединений.
A. Технологии подвода энергии для формирования дисперсий мелких частиц
Способ подготовки дисперсий мелких частиц с помощью технологий подвода энергии обычно содержит этап, состоящий в том, что фармацевтически активное соединение, которое иногда следует называть лекарственным средством, вводят в объеме в подходящий носитель, например, воду или раствор на водной основе, содержащий, по меньшей мере, одно нижеописанное поверхностно-активное вещество, или другую жидкость, в которой фармацевтическое соединение несущественно растворимо для формирования предсуспензии. К предсуспензии подводят энергию для формирования дисперсии частиц. Энергию подводят механическим растиранием, размолом на Бисерной мельнице, размолом на шаровой мельнице, размолом на молотковой мельнице, размолом в струйной мельнице или мокрым измельчением. Данные технологии описаны в патенте США №5145684, который включен в настоящее описание путем отсылки и является его частью.
Технологии подвода энергии дополнительно включают воздействие на предсуспензию больших усилий сдвига, включая кавитацию, сдвиговые или ударные усилия, с использованием микрофлюидизатора. В соответствии с настоящим изобретением дополнительно предлагается подвод энергии в предсуспензию с использованием плунжерного гомогенизатора или противоточного гомогенизатора типа описанных в патенте США №5091188, который включен в настоящее описание путем ссылки и является его частью. Подходящие плунжерные гомогенизаторы продаются под названием EMULSIFLEX фирмой Avestm и French Pressure Cells фирмой Spectronic Instruments. Производителем подходящих микрофлюидизаторов является фирма Microfluidics Corp.
Этап подвода энергии можно также выполнять с использованием технологий обработки ультразвуком. Этап обработки ультразвуком можно выполнять с помощью любого подходящего устройства для обработки ультразвуком, например, Branson Model S-450A или Cole-Panner 500/750 Watt Model. Данные устройства широко известны в промышленности. Обычно устройство для обработки ультразвуком содержит ультразвуковой рупорный излучатель или зонд, который вставляют в предсуспензию для излучения энергии звуковых волн в раствор. Устройство для обработки ультразвуком в предпочтительном варианте осуществления изобретения применяют на частоте от приблизительно 1 кГц до приблизительно 90 кГц и в более предпочтительном варианте от приблизительно 20 кГц до приблизительно 40 кГц или в любом диапазоне или комбинации внутри упомянутых диапазонов. Размеры зонда могут изменяться и, предпочтительно, имеют определенные значения, например, 1/2 дюйма или 1/4 дюйма или что-то подобное.
Независимо от применяемой технологии подвода энергии дисперсия мелких частиц должна удовлетворять соответствующим требованиям по обеспечению стерильности перед использованием. Стерилизацию можно выполнять с использованием нижеописанных технологий стерилизации под высоким давлением.
B. Способы осаждения для приготовления дисперсий субмикронных частиц
Дисперсии мелких частиц можно также приготавливать посредством широко известных технологий осаждения. Ниже представлены технологии осаждения, используемые для получения дисперсий субмикронных твердых частиц.
Способы микроосаждения
Один пример способа микроосаждения предложен в патенте США №5780062, который включен в настоящее описание путем ссылки и является его частью. В патенте США №5780062 приведено описание способа осаждения органического соединения, включающего следующие этапы: (I) растворяют органическое соединение в смешивающемся с водой первом растворителе; (II) приготавливают раствор полимера и амфифильного вещества в водном втором растворителе, при этом органическое соединение, по существу, не растворимо в данном втором растворителе, вследствие чего образуется комплекс полимер/амфифильное вещество; и (III) смешивают растворы с этапов (I) и (II) так, чтобы вызвать осаждение агрегата органического соединения и комплекса полимер/амфифильное вещество.
Другой пример подходящего способа осаждения описан в совместно рассматриваемых и принадлежащих общему владельцу заявках на патенты США №09/874499, 09/874799, 09/874637 и 10/021692, которые включены в настоящее описание путем ссылки и являются его частью. Описанные способы включают следующие этапы: (1) растворяют органическое соединение в смешивающемся с водой первом органическом растворителе для создания первого раствора; (2) смешивают первый раствор со вторым растворителем или водой для осаждения органического соединения, чтобы создать предсуспензию; и (3) подводят энергию к предсуспензии в форме смешивания с большим усилием сдвига или подвода тепла для обеспечения дисперсии мелких частиц. По меньшей мере, один нижеупомянутый возможный модификатор поверхности может быть введен в первый органический растворитель или второй водный раствор.
Способы эмульсионного осаждения
Одна подходящая технология осаждения эмульсии описана в совместно рассматриваемой и принадлежащей общему владельцу заявке на патент США №09/964273, которая включена в настоящее описание путем ссылки и является его частью. При данном подходе способ включает следующие этапы: (1) обеспечивают многофазную систему, содержащую органическую фазу и водную фазу, при этом органическая фаза содержит фармацевтически активное соединение; и (2) обрабатывают систему ультразвуком для выпаривания части органической фазы, чтобы вызвать осаждение соединения в водной фазе для формирования дисперсии мелких частиц. Этап обеспечения многофазной системы содержит следующие этапы: (1) смешивают смешивающийся с водой растворитель с фармацевтически активным соединением для образования органического раствора, (2) приготавливают раствор на водной основе с, по меньшей мере, одним поверхностно-активным соединением и (3) смешивают органический раствор с водным раствором для формирования многофазной системы. Этап смешения органической фазы и водной фазы может включать в себя применение плунжерных гомогенизаторов, коллоидных мельниц, высокоскоростного смесительного оборудования, экструзионного оборудования, ручного оборудования для активации или встряхивания, микрофлюидизатора или другого оборудования или технологий для обеспечения режима с большими усилиями сдвига. Необработанная эмульсия будет содержать масляные капли в воде с размерами приблизительно меньше 1 мкм в диаметре. Необработанную эмульсию обрабатывают ультразвуком для образования более тонкодисперсной эмульсии и, в конечном счете, обеспечения дисперсии мелких частиц.
Другой подход к приготовлению дисперсии мелких частиц описан в совместно рассматриваемой и принадлежащей общему владельцу заявке на патент США №10/183035, которая включена в настоящее описание путем ссылки и является его частью. Способ включает следующие этапы: (1) обеспечивают необработанную дисперсию многофазной системы, содержащей органическую фазу и водную фазу, при этом органическая фаза содержит фармацевтически активное соединение; (2) обеспечивают подвод энергии к необработанной дисперсии для формиро