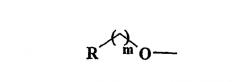Замещенные аминоалкил- и амидоалкилбензопиранпроизводные
Иллюстрации
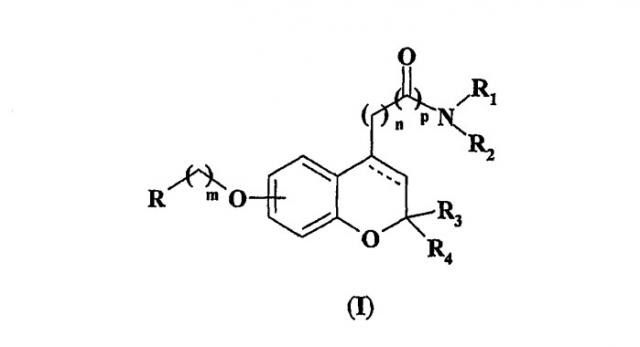
Показать всеДанное изобретение относится к новым аминоалкил- и амидоалкилбензопиранпроизводным следующей общей формулы (I):
в которой группа (а) является заместителем в положении 6 или 7, в которой R является моно- или бициклическим (С6-С10)-арильным радикалом, необязательно замещенным одним или двумя заместителями, выбранными из линейных или разветвленных (С1-С5)-алкилов, линейных или разветвленных (С1-С5)-алкокси, гидрокси, галогена и трифторметила; m является нулем или целым числом 1-3; n, p, R1 и R2 - такие, как показано в описании, и R3 и R4, оба, представляют собой водород или вместе представляют собой кислород, и их фармацевтически приемлемым солям. Эти соединения проявляют себя как селективные и обратимые МАО-В ингибиторы in vitro и in vivo, полезны в качестве лекарственных средств для предупреждения и лечения дегенеративных расстройств ЦНС. Изобретение также относится к фармацевтической композиции на основе этих соединений и способу предупреждения дегенеративных расстройств ЦНС. 3 н. и 10 з.п. ф-лы, 1 табл.
Реферат
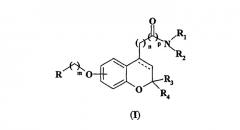
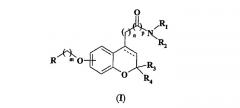
Данное изобретение относится к новым производным аминоалкил- и амидоалкилбензопирана следующей общей формулы (I)
где
группа является заместителем в положении 6 или 7, в которой
R является моно- или бициклическим (C6-C10)-арильным радикалом или моно- или бициклическим 5-10-членным гетероарильным радикалом, причем указанные радикалы являются, необязательно, замещенными одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, линейных или разветвленных (C1-C5)-алкокси, гидрокси, галогена и трифторметила;
m является нулем или целым числом 1-3;
R1 и R2, каждый независимо, представляют собой
водород;
линейный или разветвленный (C1-C5)-алкил, необязательно замещенный фенилом, где соответствующая фенильная группа является необязательно замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
линейный или разветвленный (C2-C5)-алкил, замещенный аминогруппой;
фенил, где фенильная группа является необязательно замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
амино, линейный или разветвленный (C1-C5)-алкил- или диалкиламино;
или R1 и R2 вместе с соседним атомом азота образуют насыщенное 5-7-членное гетероциклическое кольцо, необязательно включающее один или два дополнительных гетероатома или группы, выбранные из O, S и NR5, где R5 представляет собой водород или линейный или разветвленный (C1-C5)-алкил;
n является целым числом 1-3;
p является нулем или 1;
R3 и R4, оба, представляют собой водород или вместе представляют собой кислород;
пунктирная линия указывает на отсутствие или наличие дополнительной связи;
при условии, что
(i) если R, m, n, p, R3, R4 и пунктирная линия соответствуют указанному выше и один из R1 и R2 представляет собой аминогруппу или линейную или разветвленную (C1-C5)-алкиламиногруппу, то другая является водородом или линейной или разветвленной (C1-C5)-алкильной группой;
(ii) если m и пунктирная линия соответствуют указанному выше, n равно 1, p равно нулю, R представляет собой моно- или бициклический (C6-C10)-арильный радикал, необязательно замещенный, как описано выше, R3 и R4, оба, представляют собой водород, и один из R1 и R2 представляет собой водород или линейный или разветвленный (C1-C5)-алкил, то другой может не быть линейным или разветвленным (C2-C5)-алкилом, замещенным фенилом, где фенильная группа может быть необязательно замещена одним или двумя заместителями, как описано выше;
(iii) если m является целым числом 1-3, n, p - такие, как описано выше, пунктирная линия означает дополнительную связь; и
R1 и R2, каждый независимо, представляют собой
водород;
линейный или разветвленный (C1-C5)-алкил, необязательно замещенный фенилом, где фенильная группа является необязательно замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
линейный или разветвленный (C2-C5)-алкил, замещенный аминогруппой;
фенил, где фенильная группа является необязательно замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
или если p равно нулю, R1 и R2 вместе с соседним атомом азота образуют насыщенный 5-6-членный гетероцикл, необязательно содержащий один дополнительный гетероатом или группу, выбранную из O, S и NR5, где R5 является водородом или линейным или разветвленным (C1-C5)-алкилом; и
R3 и R4 вместе образуют кислород; и
представляет собой заместитель в положении 7;
тогда R не может быть незамещенным моно- или бициклическим (C6-C10)-арильным радикалом;
в соответствующем случае, как индивидуальные оптические изомеры или их смеси, и их фармацевтически приемлемые соли.
Данное изобретение включает способ получения соединений формулы (I) и фармацевтические составы, их содержащие, для использования в качестве лекарственных средств для предупреждения и лечения дегенеративных нарушений ЦНС, которые действуют как селективные и обратимые MAO-B ингибиторы in vitro и in vivo.
Термин "производные бензопирана", используемый в настоящем описании и формуле изобретения, включает соединения хромана и 2H-хромена, а также соответствующие 2-оксопроизводные, т.е. производные хроман-2-она и 2H-хромен-2-она (кумарин).
US 5554611 (соответствующий EP 0655242 A) описывает производные кумарина с целью контроля и предупреждения расстройств, которые возникают из-за повышенного уровня NO, в частности, патологических заболеваний, связанных с изменением кровяного давления, что может иметь место при септическом или геморрагическом шоке, при противоопухолевой терапии с использованием цитокинов, или при циррозе печени; воспалений, таких как ревматоидный артрит и, в частности, язвенный колит; инсулинзависимого сахарного диабета; реакций отторжения трансплантата; артериосклероза; постишемического поражения ткани; реперфузионного поражения; миокардита вследствие инфекции, вызванной вирусом Коксаки; кардиомиопатии; форм невритов; энцефаломелита; вирусных нейродегенеративных заболеваний; болезни Альцгеймера; гипералгезии; эпилепсии; мигрени; острой почечной недостаточности и гломерулонефрита; терапии расстройств в желудке и маточном/плацентарном пространстве и подвижности сперматозоидов.
US 5227392 (соответствующий EP 0363796 A) и US 5100914 описывают производные кумарина, обладающие MAO-B ингибирующим действием, в которых заместители пиранового кольца не имеют ни амидо, ни аминогрупп.
M.D. Ennis et al. в Bioorganic & Medicinal Chemistry Letters, 1993, 3, 1131-1136, описывают получение производных 4-аминометилхромана, действующих на 5-HT1A или D-2 рецепторы, в которых бензольное кольцо несет на себе метоксигруппу.
US 4977166 описывает производные бензопирана, обладающие антиаритмическими и антифибрилляторными свойствами, в которых алкоксирадикал, который может быть расположен при бензольном кольце, не предполагает в качестве заместителей моно- или бициклических (C6-C10)-арильных или моно- или бициклических 5-10-членных гетероарильных радикалов.
WO 89/06534 описывает соединения хромана и тиохромана, которые действуют как α-2 адренергические антагонисты, в которых заместители при бензольном кольце не включают моно- или бициклические (C6-C10)-арильные или моно- или бициклические 5-10-членные гетероарильные радикалы.
US 4659737 описывает N-замещенные производные α-аминометилбензопирана, обладающие антигипертензивным действием.
US 4486428 описывает бициклические бензоконденсированные соединения, применимые в качестве анальгетиков, транквилизаторов, противорвотных агентов, диуретиков, антиконвульсантов, противодиарейных средств, противокашлевых средств и применяемые при лечении глаукомы. Указанные бензоконденсированные соединения включают производные бензопирана, несущие два заместителя в положениях 5 и 7.
EP-1318140 A описывает антагонисты C5a рецепторов, которые имеют амидную группу, непосредственно связанную с положением 4 пиранового кольца.
R.A. Geemon et al. в J. Med. Chem., 1982, 25, 393-397, описывают получение производных 6-метокси-4-аминометилхромена и -хромана и их взаимодействий с серотониновыми рецепторами.
Биологический уровень техники
Моноаминоксидаза (MAO) является интегральным белком наружной митохондриальной мембраны и играет важную роль в in vivo инактивации биогенных и получаемых с пищей аминов как в ЦНС, так и в периферических нейронах и тканях. Два MAO энзима различаются в соответствии с их субстратной предпочтительностью и чувствительностью к MAO ингибитору клоргилину:
- MAO тип A (MAO-A) в ЦНС человека ответственна за процесс деаминирования серотонина и норадреналина. Наибольшие MAO-A концентрации наблюдаются в катехоламинергических нейронах locus ceruleus;
- MAO тип B (MAO-B) ответственен главным образом за катаболизм допамина (DA). В отличие от мозга крысы MAO-B является основной изоформой в ЦНС человека и гвинейской свиньи. Наибольшие MAO-B концентрации были найдены в серотонинэргических нейронах ядер шва и заднего отдела гипоталамуса. Nigral MAO-B локализована преимущественно в глиальных клетках.
Активность MAO-B (но не MAO-A) в ЦНС увеличивается с возрастом как у людей, так и у животных, возможно, как результат пролиферации глиальных клеток, ассоциированной с потерей нейронов. Возросший уровень MAO-B в бляшках, характерных для болезни Альцгеймера, ранее сообщался. Сообщалась возросшая MAO-B активность тромбоцитов крови как при болезни Альцгеймера (AD), так и при болезни Паркинсона (PD). MAO-B активность была понижена на 40% в мозге курильщиков: курение табака сопряжено со снижением риска PD.
Большая часть на данный момент исследованных MAO-B ингибиторов представляет собой необратимые ингибиторы. Такое ингибирование является очень продолжительным (недели), поскольку их действие можно преодолеть только посредством синтеза энзима de novo. Интерес к MAO-B ингибированию вначале стимулировался желанием повысить пониженную стриарную концентрацию DA, характерную для PD, так как увеличенная концентрация DA в синаптической щели могла бы ожидаться как первичный эффект лечения селективным MAO-B ингибитором. В случае PD требуется доставить DA предшественник - L-Dopa, золотой стандарт в терапии PD, следует таким образом понижать. Это желательно, так как L-Dopa, несмотря на достигнутые превосходные первичные улучшения, связан в долгосрочном плане лечения с увеличением серьезных побочных эффектов, включая колебания моторной функции, дискинезию и дистонию.
Кроме потери холинергических нейронов, понижается уровень DA, норадреналина и серотонина в мозге AD пациентов. MAO-B ингибиторы могут действовать, понижая образование кислородрадикалов и в то же время предупреждая инактивацию моноаминов и таким образом повышая их уровень в мозге AD пациентов.
Соединения, соответствующие настоящему изобретению, применимы при всех патологиях, вызванных нейродегенеративными процессами, и/или окислительно-метаболической нагрузкой, и/или недостатком биогенных аминов, например, болезнь Паркинсона, двигательных расстройств (например, постэнцефалический паркинсонизм, прогрессирующий супрануклеарный паралич, кортикобазальные дегенеративные процессы), синдром беспокойных ног, эпилепсия, болезнь Альцгеймера и прочие формы слабоумия, такие как старческое слабоумие типа Паркинсона, вазикулярное слабоумие и слабоумие с тельцами Леви, боковой амиотрофический склероз, синдрома Дауна, болезнь Хантингтона, припадки, ишемия, травма ЦНС. Они также полезны для лечения нарколепсии, синдрома Туретта, синдрома дефицита внимания и гиперактивности, негативные симптомы шизофрении, наркомании, при прекращении курения и ожирении.
Яркие примеры в литературе, которые демонстрируют потенциальные терапевтические преимущества MAO-B ингибиторов, можно найти по следующим ссылкам: P.H. Wender J. Clin. Psychiatry, 1998, 59, 76-87; E.J. Houtsmuller et al. Psychopharmacology, 2004, 172, 31; J.E. Rose et al. Nicot. Tob. Res., 2001, 3, 383-388; P. Riederer et al. Curr. Med. Chem., 2004, 11, 2033-43; P. Jenner Neurology, 2004, 63, S13-22; P. H. Yu Gen. Pharmacol., 1994, 25, 1527-39; M. Yamada Neurotoxicology, 2004, 25, 215-21; J.C. Delumeau J. Neural. Transm. Suppl., 1994, 41, 259-66.
Описание изобретения
Данное изобретение относится к новым производным аминоалкил- и амидоалкилбензопирана следующей общей формулы (I)
где
группа является заместителем в положении 6 или 7, в которой
R является моно- или бициклическим (C6-C10)-арильным радикалом или моно- или бициклическим 5-10-членным гетероарильным радикалом, причем указанные радикалы являются, необязательно, замещенными одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, линейных или разветвленных (C1-C5)-алкокси, гидрокси, галогена и трифторметила;
m является нулем или целым числом 1-3;
R1 и R2, каждый независимо, представляют собой
водород;
линейный или разветвленный (C1-C5)-алкил, необязательно, замещенный фенилом, где соответствующая фенильная группа является необязательно замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
линейный или разветвленный (C2-C5)-алкил, замещенный аминогруппой;
фенил, где фенильная группа является необязательно замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
амино, линейный или разветвленный (C1-C5)-алкил- или диалкиламино;
или R1 и R2 вместе с соседним атомом азота образуют насыщенное 5-7-членное гетероциклическое кольцо, необязательно включающее один или два дополнительных гетероатома или группы, выбранные из O, S и NR5, где R5 представляет собой водород или линейный или разветвленный (C1-C5)-алкил;
n является целым числом 1-3;
p является нулем или 1;
R3 и R4, оба, представляют собой водород или вместе представляют собой кислород;
пунктирная линия указывает на отсутствие или наличие дополнительной связи;
при условии, что
(i) если R, m, n, p, R3, R4 и пунктирная линия соответствуют указанному выше и один из R1 и R2 представляет собой аминогруппу или линейную или разветвленную (C1-C5)-алкиламиногруппу, то другая является водородом или линейной или разветвленной (C1-C5)-алкильной группой;
(ii) если m и пунктирная линия соответствуют указанному выше, n равно 1, p равно нулю, R представляет собой моно- или бициклический арильный (C6-C10)-радикал, необязательно замещенный, как описано выше, R3 и R4, оба, представляют собой водород и один из R1 и R2 представляют собой водород или линейный или разветвленный (C1-C5)-алкил, то другой может не быть линейным или разветвленным (C2-C5)-алкилом, замещенным фенилом, где фенильная группа может быть, необязательно, замещена одним или двумя заместителями, как описано выше;
(iii) если m является целым числом 1-3, n, p - такие, как описано выше, пунктирная линия означает дополнительную связь; и
R1 и R2, каждый независимо, представляют собой
водород;
линейный или разветвленный (C1-C5)-алкил, необязательно, замещенный фенилом, где фенильная группа является, необязательно, замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
линейный или разветвленный (C2-C5)-алкил, замещенный аминогруппой;
фенил, где фенильная группа является необязательно замещенной одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C5)-алкилов, гидрокси, линейных или разветвленных (C1-C5)-алкокси, галогена и трифторметила;
или если p равно нулю, R1 и R2 вместе с соседним атомом азота образуют насыщенный 5-6-членный гетероцикл, необязательно содержащий один дополнительный гетероатом или группу, выбранную из O, S и NR5, где R5 является водородом или линейным или разветвленным (C1-C5)-алкилом; и
R3 и R4 вместе образуют кислород; и
представляет собой заместитель в положении 7;
тогда R не может быть незамещенным моно- или бициклическим (C6-C10)-арильным радикалом;
в соответствующем случае, как индивидуальные оптические изомеры или их смеси, и их фармацевтически приемлемые соли.
Данное изобретение относится к способу получения соединений формулы (I) и подобных соединений, и фармацевтическим составав, их содержащих, для использования в качестве лекарственных средств для предупреждения и лечения дегенеративных нарушений ЦНС, которые действуют как селективные и обратимые MAO-B ингибиторы in vitro и in vivo.
В описании и формуле изобретения "моно- или бициклический (C6-C10)-арильный радикал" представляет собой радикал - производное от моно- или бициклической ароматической циклической системы, соответственно, с 6, 9 или 10 атомами углерода, такой как бензол, инден и нафталин, а также включая индан и тетрагидронафталин.
"Моно- или бициклический 5-10-членный гетероарильный радикал" является радикалом - производным от моно- или бициклической гетероароматической циклической системы, соответственно, 5-, 6-, 9- или 10-членной, которая включает один или два гетероатома, выбранных как N, O и S. Примерами указанных радикалов являются фурил, тиенил (возможно тиофенил), пирролил, имидазолил, пиридил, индолил, изоиндолил, хинолил, изохинолил, бензофуранил и бензопиранил.
Термин "галоген" означает хлор, фтор, бром или йод, предпочтительно, хлор, фтор или бром, более предпочтительно, хлор или фтор.
Возможные заместители, описанные выше как "арил" и "гетероарил" радикалы, обозначенные символом R, и при фенильной группе, если присутствуют в R1 и/или R2, то могут находиться в любом положении. Фармацевтически приемлемые соли соединений формулы (I) включают аддукты с неорганическими кислотами, например, хлористоводородной, бромистоводородной, серной и фосфорной, или с органическими кислотами, например, уксусной, пропионовой, бензойной, коричной, миндальной, салициловой, гликолевой, молочной, щавелевой, яблочной, малеиновой, малоновой, фумаровой, винной, лимонной, п-толуолсульфоновой, метансульфоновой кислотой и подобными.
В соответствии с одним аспектом настоящего изобретения группа предпочтительных соединений (I), как описано выше, представляется соединениями формулы (I), в которой
R является фенилом, замещенным одним или двумя заместителями, выбранными из линейных или разветвленных (C1-C4)-алкилов, линейных или разветвленных (C1-C4)-алкокси, галогена и трифторметила, или R является пиридилом;
m равно нулю, 1 или 2;
R1 и R2, каждый независимо, представляют собой водород, линейный или разветвленный (C1-C4)-алкил или фенил-(C1-C2)-алкил; или один из R1 и R2 является аминогруппой, а другой водородом или линейным или разветвленным (C1-C4)-алкилом; или R1 и R2 вместе с соседним атомом азота образуют насыщенный 5-6-членный гетероцикл, необязательно содержащий дополнительный гетероатом, выбранный из O, S и линейного или разветвленного N(C1-C4)-алкила;
n равно 1, 2 или 3;
p равно нулю или 1;
R3 и R4, вместе, образуют кислород;
пунктирная линия указывает на отсутствие или наличие дополнительной связи.
В соответствии с другим аспектом настоящего изобретения группа наиболее предпочтительных соединений формулы (I), как описано выше, представляет собой соединения формулы (I), в которой
R является фенилом, замещенным одним заместителем, выбранным из линейного или разветвленного (C1-C3)-алкила, линейного или разветвленного (C1-C3)-алкокси, фтора, хлора и трифторметила, или R является пиридилом;
m равно 1;
R1 и R2, каждый независимо, представляют собой водород, линейный или разветвленный (C1-C3)-алкил или бензил; или один из R1 и R2 является аминогруппой, а другой водородом или линейным или разветвленным (C1-C3)-алкилом; или R1 и R2 вместе с соседним атомом азота образуют насыщенный 5-6-членный гетероцикл, включающий дополнительный гетероатом, выбранный из O, S и N линейного или разветвленного (C1-C3)-алкила;
n равно 1 или 2;
p равно нулю или 1;
R3 и R4 вместе образуют кислород;
пунктирная линия означает дополнительную связь.
В соответствии с другим аспектом настоящего изобретения группа предпочтительных соединений формулы (I), как описано выше, представляет собой соединения формулы (I), в которой
R является фенилом, необязательно, замещенным одним или двумя заместителями, выбранными как линейные или разветвленные (C1-C4)-алкилы, линейные или разветвленные (C1-C4)-алкокси, галогена и трифторметил, или R представляет собой пиридил;
m равно нулю, 1 или 2;
R1 и R2, каждый независимо, представляют собой водород, линейный или разветвленный (C1-C4)-алкил или бензил; или один из R1 и R2 является аминогруппой и другой водородом или линейным или разветвленным (C1-C4)-алкилом; или R1 и R2 вместе с соседним атомом азота образуют насыщенный 5-6-членный гетероцикл, включающий, необязательно, дополнительный гетероатом, выбранный из O, S и линейного или разветвленного N(C1-C3)-алкила;
n равно 1, 2 или 3;
p равно нулю или 1;
R3 и R4, оба, представляют собой водород;
пунктирная линия означает наличие дополнительной связи или ее отсутствие.
В соответствии с другим аспектом настоящего изобретения группа наиболее предпочтительных соединений формулы (I), как описано выше, представляется соединениями формулы (I), в которой
R является фенилом, необязательно, замещенным одним заместителем, выбранным как линейный или разветвленный (C1-C3)-алкил, линейный или разветвленный (C1-C3)-алкокси, фтор, хлор и трифторметил, или R является пиридилом;
m равно 1;
R1 и R2, каждый независимо, представляет собой водород или линейный или разветвленный (C1-C3)-алкил или бензил; или один из R1 и R2 является аминогруппой и другой водородом или линейным или разветвленным (C1-C3)-алкилом; или R1 и R2 вместе с соседним атомом азота образуют насыщенный 5-6-членный гетероцикл, включающий один дополнительный гетероатом, выбранный из O, S и линейного или разветвленного N(C1-C3)-алкила;
n равно 1 или 2;
p равно нулю или 1;
R3 и R4, оба, представляют собой водород;
пунктирная линия означает наличие или отсутствие дополнительной связи.
Примеры специфических соединений соответствующих изобретению:
4-[(гидразинокарбонил)метил]-7-бензилокси-2H-хромен-2-он;
4-[(аминокарбонил)метил]-7-(3-гидроксибензилокси)-2H-хромен-2-он;
4-[(аминокарбонил)метил]-7-(пиридин-3-ил)метокси-2H-хромен-2-он;
4-[(аминокарбонил)метил]-7-(пиридин-4-ил)метокси-2H-хромен-2-он;
4-[(аминокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(гидразинокарбонил)метил]-6-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(гидразинокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(метиламинокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(бутиламинокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(бензиламинокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(диметиламинокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(N-бутил-N-метиламинокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[[(2-аминоэтил)аминокарбонил]метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(аминокарбонил)метил]-6-(3-фторбензилокси)-2H-хромен-2-он;
4-[(аминокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(гидразинокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(метиламинокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(бензиламинокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(диметиламинокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[2-(гидразинокарбонил)этил]-7-бензилокси-2H-хромен-2-он;
4-[2-(аминокарбонил)этил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(гидразинокарбонил)этил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(метиламинокарбонил)этил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(бензиламинокарбонил)этил]-6-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(бензиламинокарбонил)этил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(диметиламинокарбонил)этил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(аминокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[2-(гидразинокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[2-(метиламинокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[2-(бутиламинокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[2-(бензиламинокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[2-(диметиламинокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(аминокарбонил)метил]-7-бензилокси-2H-хромен;
4-[(гидразинокарбонил)метил]-7-бензилокси-2H-хромен;
4-[(метиламинокарбонил)метил]-7-бензилокси-2H-хромен;
4-[(диметиламинокарбонил)метил]-7-бензилокси-2H-хромен;
4-[(диметиламинокарбонил)метил]-7-(3-хлорбензилокси)-2H-хромен;
4-[(аминокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен;
4-[(гидразинокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен;
4-[(метиламинокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен;
4-[(диметиламинокарбонил)метил]-7-(3-фторбензилокси)-2H-хромен;
4-[2-(аминокарбонил)этил]-6-бензилокси-2H-хромен;
4-[2-(аминокарбонил)этил]-7-бензилокси-2H-хромен;
4-[2-(гидразинокарбонил)этил]-7-бензилокси-2H-хромен;
4-[2-(метиламинокарбонил)этил]-7-бензилокси-2H-хромен;
4-[2-(диметиламинокарбонил)этил]-7-бензилокси-2H-хромен;
4-[2-(аминокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен;
4-[2-(гидразинокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен;
4-[2-(метиламинокарбонил)этил]-7-(3-фторбензилокси)-2H-хромен;
4-[(аминокарбонил)метил]-7-бензилоксихроман;
4-[(гидразинокарбонил)метил]-7-бензилоксихроман;
4-[(метиламинокарбонил)метил]-7-бензилоксихроман;
4-[(аминокарбонил)метил]-7-(3-фторбензилокси)хроман;
4-[(гидразинокарбонил)метил]-7-(3-фторбензилокси)хроман;
4-[(метиламинокарбонил)метил]-7-(3-фторбензилокси)хроман;
4-[2-(гидразинокарбонил)этил]-7-бензилоксихроман;
4-[2-(метиламинокарбонил)этил]-7-бензилоксихроман;
4-[2-(аминокарбонил)этил]-7-(3-фторбензилокси)хроман;
4-[2-(метиламинокарбонил)этил]-7-(3-фторбензилокси)хроман;
4-аминометил-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-(2-аминоэтил)-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(метиламино)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(диметиламино)метил]-6-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(диметиламино)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(метиламино)этил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(этиламино)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[2-(этиламино)этил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(бензиламино)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-[(N-бензил-N-метиламино)метил]-7-(3-хлорбензилокси)-2H-хромен-2-он;
4-аминометил-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(метиламино)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(диметиламино)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[2-(метиламино)этил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(этиламино)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-[(изопропиламино)метил]-7-(3-фторбензилокси)-2H-хромен-2-он;
4-(2-аминоэтил)-7-бензилокси-2H-хромен;
4-[2-(метиламино)этил]-7-бензилокси-2H-хромен;
4-(2-аминоэтил)-7-(3-хлорбензилокси)-2H-хромен;
4-(2-аминоэтил)-7-(3-фторбензилокси)-2H-хромен;
4-(2-аминоэтил)-6-бензилоксихроман;
4-(2-аминоэтил)-7-бензилоксихроман;
4-(3-аминопропил)-7-бензилоксихроман;
4-[(метиламино)метил]-7-бензилоксихроман;
4-[2-(метиламино)этил]-7-бензилоксихроман;
4-[3-(метиламино)пропил]-7-бензилоксихроман;
4-аминометил-7-(3-хлорбензилокси)хроман;
4-(2-аминоэтил)-7-(3-хлорбензилокси)хроман;
4-[(метиламино)метил]-7-(3-хлорбензилокси)хроман;
4-аминометил-7-(3-фторбензилокси)хроман;
4-(2-аминоэтил)-7-(3-фторбензилокси)хроман;
4-[(метиламино)метил]-7-(3-фторбензилокси)хроман;
4-[2-(метиламино)этил]-7-(3-фторбензилокси)хроман;
и их фармацевтически приемлемые соли.
Если соединения, соответствующие настоящему изобретению, содержат асимметрические атомы углерода, они могут существовать в виде индивидуальных оптических изомеров или их смесей (например, во всех случаях, когда пунктирная линия в формуле (I) не означает наличие дополнительной связи или если разветвленный алкил содержит асимметрический атом углерода), в объем данного изобретения включаются все возможные оптические изомеры указанных соединений и их смеси.
Соединения, соответствующие данному изобретению, могут быть получены в соответствии с различными методиками.
Аминометилкумаринпроизводные (аминометил-2H-хромен-2-она производные) получают из 4-(хлорметил)-(6 или 7)-гидрокси-2H-хромен-2-она, который может быть получен из этил 4-хлорацетилацетата и резорцина или гидрохинона посредством классической процедуры фон Пехмана (H. Von Pechmann; C. Duisberg, Chem. Ber., 1883, 16, 2119-2128; N. Nguyen-Hai et al. Bioorganic & Medicinal Chemistry Letters, 2002, 12, 2345-2348), с использованием каталитического количества серной кислоты при нагревании смеси до 120°С или, в качестве альтернативной методики, используя серную кислоту в качестве растворителя, при температуре от -10°С до 10°С.
Вторая стадия представляет собой арил- или гетероарилалкилирование 4-(хлорметил)-(6 или 7)-гидрокси-2H-хромен-2-она соответствующим арил- или гетероарилалкилбромидом в присутствии безводного K2CO3 в кипящем абсолютном спирте, таком как метанол или этанол, или пропанол.
Первичные амины получали посредством синтеза промежуточных азидов кипячением с обратным холодильником различных 6- или 7-арилалкокси или 6- или 7-гетероарилалкокси-4-хлорметил-2H-хромен-2-онов с NaN3 в низших алканолах и восстановлением соответствующих азидопроизводных SnCl2 (S.N. Maiti et al., Tetrahedron Letters, 1986, 13, 1423-1424) в метаноле или этаноле.
Моно- и диалкиламинопроизводные получали реакцией соответствующих 6- или 7-арилалкокси- или 6- или 7-гетероарилалкокси-4-(хлорметил)-2H-хромен-2-онпроизводных с коммерчески доступными или легко получаемыми растворами подходящих первичных или вторичных аминов в ТГФ при 40-65°С или при кипячении с обратным холодильником в низших абсолютных спиртах в присутствии нейтрализаторов HCl, таких как, например, карбонат калия.
Соединения 4-аминокарбонилметил- и 4-(2-аминоэтил)кумарин (и соединения 4-аминокарбонил-(C2-C3)алкил- и 4-(3-аминопропил)алкилкумарин) приготовили из резорцина и диэтил-1,3-ацетондикарбоксилата (и соответствующих гомологов H5C2OOC-(CH2)k-CH2-CO- CH2-COOC2H5, где k равно 1 или 2) в соответствии с классической методикой фон Пехмана (см. выше). Полученные 4-[(этоксикарбонил)метил]-(6- или 7-)гидрокси-2H-хромен-2-он (и соответствующий 4-[2-(этоксикарбонил)этил]- и 4-[3-(этоксикарбонил)пропил]замещенные гомологи) реагировали с аммонием или соответствующим амином при 50-100°С в течение 20-60 ч с получением соответствующих производных 4-[(аминокарбонил)метил]-(6- или 7-)гидрокси-2H-хромен-2-она и соответствующих 4-[2-(аминокарбонил)этил]- и 4-[3- (аминокарбонил)пропил]гомологов).
Конденсация Мицунобу "карбонильных" соединений с соответствующими арил- или гетероарилзамещенными спиртами давала соответствующие 6- или 7-простые эфиры производных 4-[(аминокарбонил)метил]-2H-хромен-2-она. Соответствующие первичные 4-(2-аминоэтил)кумарин и 4-(3-аминопропил)кумарин могли бы быть получены проще, посредством превращения соответствующих 4-аминокарбонилпроизводных формулы (I), где n равно 1 или 2, в нитрилы обработкой ангидридом трифторуксусной кислоты в соответствии с методом, разработанным Каротти (A. Carotti et al. Tetrahedron Letters, 1977, 21, 1813-1816), и восстановлением нитрилов боргидридом натрия в присутствии хлорида кобальта (T. Satoh et al. Tetrahedron Letters, 1969, 52, 4555-4558).
Другие 4-моно- и 4-(дизамещенные-2-аминоэтил- (или 3-аминопропил))кумаринпроизводные лучше получаются посредством 6-12-часовой реакции 4-(2-бромэтил- (или 3-бромпропил))-2H-хромен-2-она 6- или 7-эфирных производных с подходящими первичными или вторичными аминами, в апротонных растворителях, таких как ТГФ или ацетон, или протонных растворителях, таких как низшие алканолы, в присутствии KI и нейтрализатора кислоты, такого как, например, карбонат калия или избытка реакционного амина, при температуре от 30 до 70°С.
4-(2-Бромэтил)-2H-хромен-2-он 6- или 7-эфирные производные получали из 4-[(этоксикарбонил)метил]-(6- или 7-)гидрокси-2H-хромен-2-онов, которые гидролизовались в соответствующие 4-карбоксиметилпроизводные, восстанавливались до 4-(2-гидроксиэтил)спиртов и бромировались системой CBr4/трифенилфосфин в хлористом метилене при 0-35°С. Эти 4-(2-бромэтил)-(6 или 7)-гидроксипроизводные затем трансформировались в соответствующие 6- или 7-простые эфиры. Аналогичные процедуры были применены для получения 4-(3-бромпропил)замещенных гомологов.
Все реакции и реакционные условия, указанные выше, хорошо известны специалистам в данной области.
Производные 2H-хромена получали посредством селективного восстановления соответствующих 2H-хромен-2-онов либо алюмогидридом лития, либо дибораном в апротонных безводных растворителях, таких как ТГФ, при температурах от -20°С до комнатной.
Производные хромана получали селективным восстановлением соответствующих 2H-хроменов Pd/H2 (S. Maki, Tetrahedron Lett. 2003, 44, 3717-3721)
ФАРМАКОЛОГИЯ
Соединения, соответствующие настоящему изобретению, способны к селективному и обратимому ингибированию MAO-B in vitro и in vivo.
Соединения, соответствующие данному изобретению, являющиеся сильными ингибиторами MAO-B (IC50 на субмикромолярном - наномолярном уровне), в общем не обладают никаким значимым действием на MAO-A. MAO-B ингибирование не является времязависимым, что характерно для обратимых ингибиторов. После перорального одноразового применения дозы к мышам соединения проявляют себя как сильные и обратимые, MAO-B ингибиторы короткого действия с возобновлением энзиматической активности MAO-B через 8-16 ч после применения. Соединения, соответствующие настоящему изобретению, применимы для всех расстройств с участием MAO-B энзимов.
Было бы желательно, если бы соединения, соответствующие данному изобретению, могли преимущественно использоваться вместе с одним или более терапевтическими агентами. Примеры подходящих агентов дополнительной терапии включают L-Dopa, и/или агонисты допамина, и/или ингибиторы захвата моноамина; ингибиторы катехин-O-метилтрансферазы; ловушки свободных радикалов; аденазин A2 антагонисты; модуляторы глутамата, такие как ингибитор высвобождения глутамата или NMDA или AMPA антагонисты; ингибиторы NO синтазы (NOS), такие как iNOS или nNOS ингибиторы; блокаторы натриевых и/или кальциевых каналов; антагонисты серотониновых рецепторов; антагонисты P-субстанции (например, NKl антагонист); альфа-1 или альфа-2 адренергические агонисты; агонисты никотиновых рецепторов; ингибиторы α-синуклеарной агрегации; ингибиторы холинэстеразы; агенты, понижающие уровень холестерина (такие как симвастатин, ловастатин, аторвастатин); модуляторы β-секретазы; ингибиторы β-амилйодной агрегации; каннабиноид; габапентин и родственные соединения; трициклические антидепрессанты (например, амитриптилин); нейростабилизирующие антиэпилептические лекарственные средства; ингибиторы матричных металлопротеиназ; ингибиторы выделения TNFα; терапию антителами, такую как терапия моноклональными антителами; антивирусные агенты, такие как ингибиторы нуклеозидов (например, ламивудин) или модуляторы иммунной системы (например, интерферон); анальгетики, такие как ингибиторы циклооксигеназы-2; локальные анастетики; стимуляторы, содержащие кофеин; противоотечные средства (например, фенилэфрин, фенилпропаноламин, псевдоэфедрин, оксиметазолин, эпинефрин, нафазолин); противокашлевые препараты (например, кодеин, гидрокодон, кармифен, карбетапентан или декстраметорфан); диуретические (мочегонные) или седативные или не седативные антигистамины.
Соединения, соответствующие настоящему изобретению, пригодны для лечения человека и в ветеринарии. Следует понимать, что понятие “для лечения” включает как лечение соответствующих симптомов, так и профилактическое лечение, если не оговорено ино