Способ коррекции плотности соединительной ткани
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к кардиологии, и может быть использовано для коррекции плотности соединительной после инфаркта миокарда и перикардотомии. Способ включает трехкратное, через 1,5 и 6 часов и через 3 суток после начала инфаркта или перикардотомии, введение ингибитора полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющей от 100 до 240 аминокислотных остатков. Использование изобретения позволяет изменять структуру формирующейся соединительной ткани за счет изменения концентрации полипептидной последовательности в определенные временные промежутки формирования патологического процесса и таким образом уменьшить фиброз после инфаркта миокарда и перикардотомии. 3 з.п. ф-лы, 2 табл., 5 ил.
Реферат
Предлагаемое изобретение относится к области медицины и биологии.
Известно, что в основе ряда патологических процессов, таких как кардиосклероз, цирроз, спаечная болезнь и другие состояния, лежит формирование чрезмерного количества, а также излишней жесткости вновь образуемой соединительной ткани.
Известен способ заживления ран и стимулирования развития здоровой кожи, включающий применение пептидов, которые происходят из проферментных форм матриксных металлопротеаз и являются их ингибиторами. В известном техническом решении раскрыто применение композиции для изготовления лекарственного средства, способствующего заживлению ран и предотвращению рубцевания. (Противовозрастные и ранозаживляющие составы: пат. 2318873 Рос. Федерация: МПК5 С12N 9/64, 9/99; А61К 38/04, 38/43; А61L 15/32; A61P 43/00 / Кверк С., Мейлик С., Виллануева Ж.М.; заявитель и патентообладатель Кимберли-Кларк Ворлдвайд, Inc. - №2004103071/13; заявл. 15.08.02; опубл. 10.03.08, Бюл. №7. - 76 с.).
Недостатком известного способа является только наружное применение, что ограничивает сферу их использования лечением раневых поверхностей.
Наиболее близким по технической сущности к предлагаемому является способ получения ростовых факторов белковой природы, ростовой фактор белковой природы и ингибитор пролиферации фибробластов (Способ получения ростовых факторов белковой природы, ростовой фактор белковой природы и ингибитор пролиферации фибробластов: пат. 2283654 Рос. Федерация: МКП51 А61К 35/48, 35/54, 35/32, 38/02 / Афанасьев Б.В, Вагемакер Г., Зубаровская Л.С.; заявитель и патентообладатель Афанасьев Б.В., Вагемакер Г., Зубаровская Л.С. - №2005109195; заявл. 30.03.05; опубл. 20.09.06, Бюл. №26. - 13 с.).
Известный способ осуществляют следующим образом. Эмбриональные фибробласты кожи линии В270 культивируют с кондиционированной средой, полученной при культивировании фрагментов эмбриональной костной ткани человека в течение 8-10 недель. Белковую фракцию, обладающую фибробласт- и фиброз-ингибирующей активностью, выделяют обменной хроматографией, гель-фильтрацией и центрифугированием. Полученный ростовой фактор представляет собой очищенный белок, имеющий фибробласт-ингибирующую активность, степень выраженности которой колеблется от 40% до 0%. Ингибирование пролиферации фибробластов обнаруживают по снижению включения радиоактивной метки.
Недостатком известного способа является возможность достижения подавления пролиферации фибробластов только в культуральной среде, низкая вероятность достижения целевого эффекта (от 0 до 40%), узкий диапазон эффективности - отсутствие эффекта при концентрации кондиционированной среды до 0.5%, стимуляция пролиферации фибробластов при концентрации от 1 до 5% и подавление активности при концентрации свыше 20%, а также отсутствие влияния на синтетическую активность фибробластов.
Задачей заявляемого изобретения является разработка способа управления морфогенезом соединительной ткани.
Техническим результатом предлагаемого способа является обеспечение возможности целенаправленного изменения структуры формирующейся соединительной ткани, за счет изменения количественного состава клеток соединительной ткани и плотности коллагеновых волокон.
Технический результат достигается тем, что способ коррекции плотности соединительной ткани проводят путем воздействия на фибробласты.
Отличительные приемы заявляемого способа заключаются в том, что для уменьшения плотности формирующейся соединительной ткани in vivo вводят вещество, блокирующее биологическую активность полипептида, содержащего 3 аминокислотные последовательности -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющего от 100 до 240 аминокислотных остатка трехкратно через 1.5, 6 часов и 3 суток после начала инфаркта миокарда или перикардотомии.
Сопоставительный анализ заявляемого технического решения с прототипом позволяет сделать вывод о соответствии заявляемого технического решения критерию изобретения «новизна».
Авторам заявляемого способа не известно ни одно техническое решение, осуществление которого позволило бы обеспечить заданную плотность коллагеновых волокон в формирующейся соединительной ткани.
Целенаправленное изменение концентрации полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющей от 100 до 240 аминокислотных остатка, в определенные временные промежутки формирования патологического процесса позволило авторам заявляемого способа добиться запрограммированной плотности формирующейся соединительной ткани.
Заявляемый способ обеспечивает достижение усматриваемого заявителем технического результата, а именно - обеспечение возможности целенаправленного изменения структуры формирующейся соединительной ткани, за счет изменения плотности коллагеновых волокон под воздействием искусственно измененной концентрации полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющей от 100 до 240 аминокислотных остатка.
Отличие заявляемого способа также заключается и в том, что производится воздействие на продукцию внеклеточного матрикса клетками соединительной ткани, миграцию и пролиферацию клеток.
Отличительные приемы заявляемого способа заключаются в уменьшении фиброза у индивидуума в миокарде после инфаркта миокарда и перикарде после перикардотомии.
Отличия заявляемого способа от известных авторы усматривают и в том, что для его осуществления используется фармацевтическая композиция, включающая в свой состав ингибиторы полипептидной последовательности с фрагментами -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu-, имеющей от 100 до 240 аминокислотных остатка, а также фармацевтически приемлемый носитель. При этом ингибитор полипептидной последовательности является антителом, полученным от сенсибилизированного животного, либо искусственно синтезированным веществом, обладающим химическим сродством к указанному полипептиду.
Отличительным приемом является и то, что введение фармацевтической композиции проводят нуждающемуся в этом субъекту, состояние или заболевание которого является заболеванием или состоянием сердца (инфаркт миокарда) или серозных оболочек (перикардотомия).
Изложенное позволяет сделать вывод о соответствии технического решения критерию «изобретательский уровень».
Способ, составляющий заявляемое изобретение, предназначен для использования в экспериментальной и клинической медицине и биологии. Возможность его осуществления подтверждена описанными в заявке приемами и средствами.
Вышеизложенное дает основание считать, что заявляемое техническое решение соответствует критерию изобретения «промышленная применимость».
Осуществление заявляемого способа поясняется примерами конкретного выполнения.
Приведенные ниже примеры служат для иллюстрации, но не ограничивают данное изобретение.
Пример 1.
Лабораторным животным - крысам линии Wistar - проводили моделирование инфаркта миокарда путем одномоментного повреждения биполярной диатермокоагуляцией околоконусной артерии сердца в области средней трети. Контроль повреждения миокарда после моделирования осуществляли с использованием электрокардиографии.
Естественную концентрацию полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющей от 100 до 240 аминокислотных остатка, изменяли введением ингибитора, полученного от сенсибилизированного животного (кролика). 40 крысам линии Wistar внутрисердечно проводили инъекцию указанного ингибитора в разовой дозе 2 мкг (объем инъекции 0.1 мл) трехкратно через 1.5, 6 часов и 3-е суток после моделирования инфаркта миокарда (основная группа).
В группе контроля использовали животных (45 крыс), которым предварительно аналогичным способом был смоделирован инфаркт миокарда, а течение патологического процесса происходило естественным путем.
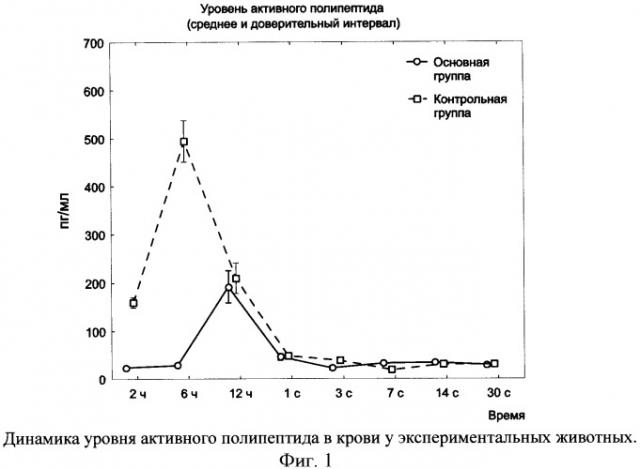
Снижение концентрации активного полипептида в основной группе животных по сравнению с группой контроля подтверждено динамикой его концентрации в крови. Измерения проводили через 2, 6, 12 часов, 1, 3, 7, 14, 30 суток после операции методом иммуноферментного анализа.
Динамика уровня активного полипептида в крови экспериментальных животных показана на фигуре 1 (приложение к описанию по заявке, фиг.1). У животных контрольной группы отмечено значительное повышение уровня активного полипептида с достижением максимума через 6 часов после операции (494.18±58.78 пг/мл), а затем его снижение. У животных основной группы отмечалось закономерное достоверное снижение уровня активного полипептида по сравнению с контрольной группой в сроки 2 часа (24.33±2.59 пг/мл в основной группе по сравнению с 159.75±14.45 пг/мл в группе контроля, р<0.01) и 6 часов (28.58±2.05 и 494.18±58.78 пг/мл соответственно, р<0.01) после операции.
Исследована динамика формирования соединительной ткани в области ишемического повреждения. Так, в основной группе через 30 суток после моделирования инфаркта миокарда в зоне формирующегося постинфарктного кардиосклероза плотность коллагеновых волокон в 2 раза ниже контрольных значений: 19.15±1.22% по сравнению с 41.71±1.30% (M±SE) в группе контроля (р<0.05). Это подтверждается данными, приведенными в таблице 1 и срезами гистологических препаратов зон инфаркта контрольной (фиг.2) и основной (фиг.3) групп животных (окраска по Ван-Гизон, увеличение 600).
| Таблица 1.Относительный объем коллагеновых волокон в области формирования постинфарктного рубца через 30 суток после моделирования инфаркта миокарда | ||
| № | Группа | Относительный объем коллагена, % (медиана, 25%-75% квартили) |
| 1 | Контрольная | 40.51 [40.33-44.30] |
| 2 | Основная | 18.50 [17.42-21.52]*; |
| Примечание: * - р<0.05 по сравнению с контрольной группой |
Из представленных данных следует, что ингибиция активности полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющей от 100 до 240 аминокислотных остатка, привела к снижению плотности формирующейся соединительной ткани в области постинфарктного рубца. Снижение плотности коллагеновых волокон у животных основной группы по сравнению с группой контроля позволило добиться меньшей жесткости левого желудочка (табл.2), что снижает вероятность развития диа-столической сердечной недостаточности.
| Таблица 2.Показатели жесткости миокарда в группах экспериментальных животных на 30 сутки после операции | |||
| Группа | Жесткость, Па/мл (медиана, 25% - 75% квартили) | Межгрупповые различия по тесту Mann-Whitney | |
| Z | P | ||
| Контрольная | 7535.04 [7342.33-7584.95] | - | |
| Основная | 5976.83 [5673.62-6437.64] | Z=-2.19338 | p=0.02828 |
Пример 2.
Лабораторным животным (крысам линии Wistar) проводили торакотомию, рассечение перикарда. Естественную концентрацию активной полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu-, изменяли введением ингибитора. Ингибитор вводили внутрисердечно в дозе 2 мкг (объем инъекции 0.1 мл), трехкратно через 1.5 и 6 часов и через 3-е суток после операции (10 животных основной группы). В качестве группы контроля использовали животных с естественным течением после перикардотомии (12 животных).
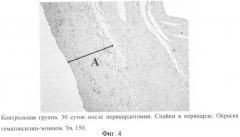
На 14-е и 30-е сутки после перикардотомии оценивали наличие и выраженность спаечного процесса в полости перикарда. Выявлено, что у животных контрольной группы спаечный процесс в полости перикарда зарегистрирован в 66.7% случаев, в основной группе - в 10% (р<0.05) (приложения к описанию по заявке, фиг.4 и 5), при этом его выраженность была значительно меньше. Так, на фиг.4 показан гистологический срез сердца животного контрольной группы на 30-е сутки после операции моделирования. Окраска гематоксилин-эозином, увеличение 150. Спаечный процесс в перикарде (позиция А). На фиг.5 - основная группа, животное на 30-е сутки после перикардотомии, показано отсутствие спаечного процесса в полости перикарда (позиция В). Окраска гематоксилин-эозином, увеличение 150.
Из представленных данных следует, что ингибиция активности полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Lys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющей от 100 до 240 аминокислотных остатка, приводит к торможению формирования соединительной ткани в серозной полости после повреждения серозных оболочек.
Таким образом, предлагаемый способ позволяет проводить коррекцию процесса формирования соединительной ткани за счет целенаправленного изменения характеристик формирующейся соединительной ткани. Данный способ может быть использован в медицине и биологии.
1. Способ коррекции плотности соединительной ткани после инфаркта миокарда или перикардотомии, включающий воздействие на фибробласты, отличающийся тем, что для уменьшения плотности соединительной ткани трехкратно, через 1,5 и 6 ч и через 3 сут после начала инфаркта или перикардотомии вводят ингибитор полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu- и имеющей от 100 до 240 аминокислотных остатков.
2. Способ по п.1, отличающийся тем, что используют фармацевтическую композицию, включающую ингибитор полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu-, имеющей от 100 до 240 аминокислотных остатков, а также фармацевтически приемлемый носитель.
3. Способ по п.2, отличающийся тем, что ингибитор полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu-, имеющей от 100 до 240 аминокислотных остатков, является антителом, полученным от сенсибилизированного животного.
4. Способ по п.1, отличающийся тем, что ингибитором полипептидной последовательности, содержащей фрагменты -Asp-Pro-Lys-Arg-Leu-Tyr-Cys-Asn-Gly-Gly-, -Glu-Arg-Gly-Val-Val-Ser-Ile-Lys-Gly- и -Ala-Asn-Arg-Tyr-Leu-Ala-Met-Lys-Glu-Asp-Gly-Arg-Leu-, имеющей от 100 до 240 аминокислотных остатков, является синтезированное in vitro вещество, обладающее химическим сродством к указанной полипептидной последовательности.