Способ извлечения ионов меди из водного раствора
Иллюстрации
Показать всеИзобретение относится к способу извлечения меди (II) из водного раствора и может быть использовано в области извлечения веществ ионообменными материалами в цветной и черной металлургии, при очистке промышленных и бытовых стоков, а также в сельском хозяйстве и медицине. Способ извлечения ионов меди (II) из водного раствора включает сорбцию меди контактированием исходного раствора с кожицей фасоли. При этом в качестве сорбента используют кожицу фасоли, предварительно обработанную в щелочном растворе, и сорбцию осуществляют при рН 4. Техническим результатом изобретения является нахождение оптимальных условий для быстрого и эффективного способа извлечения Сu (II) из промышленных и бытовых стоков с использованием продуктов сельскохозяйственного производства. 6 ил., 1 табл.
Реферат
Способ извлечения меди (II) из водного раствора относится к области извлечения веществ ионообменными материалами и может быть использован в цветной и черной металлургии, при очистке промышленных и бытовых стоков, а также в сельском хозяйстве и медицине.
Известны способы извлечения ионов меди адсорбцией на катионобменных смолах [Р.Рипан, И.Четяну. Неорганическая химия,т.2. Химия металлов. М.: Мир, 1972.С.687].
Недостатком способа является высокая стоимость сорбентов.
Наиболее близким техническим решением является способ извлечения ионов тяжелых металлов из раствора [RU 2004114538 A, C02F 1/28, опубл. 27.10.2005], включающий сорбцию ионов металла, контактированием раствора с фасолью.
Недостатком способа является то, что не известны оптимальные условия сорбции ионов Cu (II) семенами фасоли и их составными частями.
Задачей, на решение которой направлено заявленное изобретение, является нахождение оптимальных условий для быстрого и эффективного способа извлечения Cu (II) из промышленных и бытовых стоков с использованием продуктов сельскохозяйственного производства.
Техническим результатом, который может быть достигнут при осуществлении изобретения, являются улучшение кинетических характеристик процесса извлечения Cu (II) из водного раствора при одновременной высокой степени его извлечения, снижение расхода реагентов, экономичность процесса за счет использования отходов сельскохозяйственного производства.
Данный технический результат достигается тем, что в известном способе извлечения ионов меди (II) из раствора, включающем сорбцию ионов меди контактированием раствора с кожицей фасоли, в качестве сорбента используют кожицу фасоли, предварительно обработанную в щелочном растворе, и сорбцию осуществляют при рН 4.
Сущность способа поясняется чертежами, где на фиг.1-6 даны результаты сорбции меди (II) из водного раствора. На графиках полученные функциональные зависимости даны также в аналитической форме.
Примеры конкретного выполнения способа.
Для исследования использовали семена фасоли урожая 2007 г. Предварительно сорбент в течение суток выдерживали в 0,1 н растворах H2SО4 или NaOH либо в дистиллированной воде.
Сорбцию меди (II) осуществляли из 100 см3 исходного раствора CuSO4, концентрацию иона металла определяли объемным методом. Массы сорбентов, в г, составили: фасоль 15, кожица 1, семядоли 14.
Сорбцию проводили в статических условиях при непрерывном перемешивании, в процессе сорбции поддерживали заданное значение рН растворов непрерывной нейтрализацией раствора щелочью NaOH или кислотой H2SO4. Коррекцию величины рН до заданного значения осуществляли в пределах двух часов и через сутки от начала сорбции.
Показатели сорбции даны в виде остаточной концентрации иона меди в данный момент времени от начала сорбции С, мг/дм3, рН - постоянной величины рН в процессе сорбции, СОЕ, мг/г, - сорбционной обменной емкости сорбента, в мг сорбата на 1 г сорбента, при достижении системой равновесия и ОЕ, мг/г, - емкости сорбента, в мг сорбата на 1 г сорбента, в данный момент времени τ, мин.
Сорбцию меди (II) осуществляли также из растворов CuCl2, соответственно в этом случае вместо серной использовали соляную кислоту.
Пример 1 (таблица).
В таблице даны результаты сорбции Cu (II) при рН 4 фасолью и ее составными частями, сорбция из раствора CuSO4 (температура 25°С) и сорбция из раствора CuCl2 (температура 70°С).
Исходная концентрация ионов меди (II) составляет 500 мг/дм3.
Лучшие результаты сорбции получены при использовании в качестве сорбента кожицы фасоли, особенно при щелочной обработке сорбента и при нагревании.
| Предварительная обработка сорбента | Время сорбции, мин | Концентрация Си (II), мг/дм3 | СОЕ, мг/г | |
| исходная | остаточная | |||
| Кожица, масса 1 г, 25°С | ||||
| кислая | 60 | 524 | 334 | 19,0 |
| щелочная | 60 | 524 | 262 | 26,2 |
| водная | 60 | 524 | 310 | 21,4 |
| Кожица, масса 1 г, 70°С | ||||
| щелочная | 60 | 517 | 193 | 32,4 |
| водная | 60 | 517 | 278 | 23,9 |
| Семядоли, масса 14 г, 25°С | ||||
| кислая | 50 | 500 | 286 | 1,5 |
| щелочная | 50 | 500 | 95 | 2,9 |
| водная | 50 | 500 | 357 | 1,0 |
| Фасоль, масса 15 г, 25°С | ||||
| кислая | 50 | 500 | 310 | 1,3 |
| щелочная | 50 | 500 | 214 | 1,9 |
| водная | 50 | 500 | 357 | 2,0 |
Через сутки сорбции из раствора CuSO4 при 25°С получены следующие результаты сорбции:
| обработка сорбента | СОЕ, мг/г |
| кислая | 21,4 |
| щелочная | 28,6 |
| водная | 26,2 |
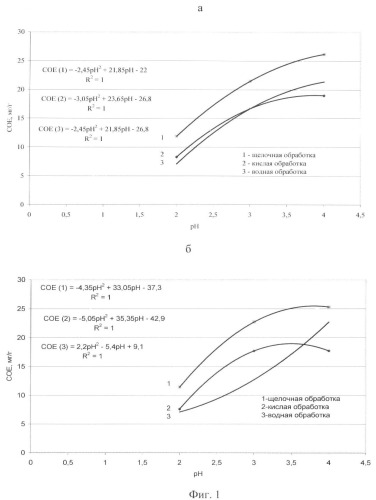
Пример 2 (фиг.1, а, б)
На фиг.1 даны результаты сорбции кожицы фасоли (масса 1 г, время сорбции 1 час) в зависимости от величины рН и предварительной обработки сорбента, сорбция из раствора CuSO4 (фиг.1, a), CuCl2 (фиг.1, б).
Лучшие результаты сорбции получены при щелочной обработке сорбента и рН 4.
Через сутки сорбции при рН 4 получено:
| Раствор CuSO4 | |||
| Обработка сорбента: | кислая (H2SO4) | щелочная | водная |
| СОЕ, мг/г | 21,4 | 28,2 | 26,2 |
| Раствор CuCl2 | |||
| Обработка сорбента: | кислая (HCl) | щелочная | водная |
| СОЕ, мг/г | 19,0 | 25,3 | 24,0 |
Полученные данные свидетельствуют о том, что предварительная обработка сорбента влияет на кинетику сорбции и слабо влияет на СОЕ сорбента.
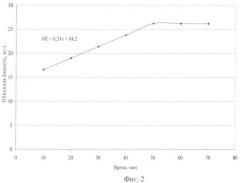
Пример 3 (фиг.2)
Сорбция из раствора CuSO4, температура 25°С, Сисх=500 мг/дм3, масса кожицы 1 г.
На фиг.2 дана зависимость обменной емкости кожицы, мг/г, от времени τ, мин, при рН 4 и щелочной обработке кожицы.
Относительное равновесие достигается за время 50 мин, СОЕ=26,2 мг/г. Кинетическое уравнение имеет вид
ОЕ=0,24τ+14,2 мг/г.
Через сутки сорбции СОЕ=28,6 мг/г.
Результаты сорбции из раствора CuCl2 при Сисх=1750 мг/дм3:
| Время, мин | 50 | 90 |
| СОЕ, мг/г | 45,4 | 50,5 |
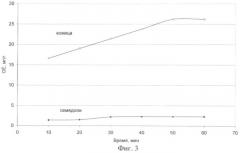
Пример 4 (фиг.3).
Сорбция из раствора CuSO4, температура 25°С, Сисх=500 мг/дм3, масса кожицы 1 г, масса семядолей 14 г.
На фиг.3 дана зависимость обменной емкости ОЕ кожицы и семядолей от времени сорбции при рН 4 и щелочной обработке сорбента.
Из данных фиг.3 видно, что ОЕ кожицы превышает (в 9-12 раз) ОЕ семядолей.
Пример 5 (фиг.4, а, б).
Сорбция из раствора CuSО4, температура 25°С, масса кожицы 1 г.
На фиг.4 дана зависимость остаточной концентрации (фиг.4, а) и обменной емкости ОЕ (фиг.4, б) кожицы от исходной концентрации, мг/дм3, и времени сорбции, мин, при рН 4 и щелочной обработке сорбента. Цифрами указаны исходные концентрации иона меди (II).
Результаты сорбции из раствора CuCl2 при температуре 70°С и времени сорбции 60 мин:
| Обработка сорбента | Сисх, мг/дм3 | ОЕ, мг/г |
| щелочная | 517 | 32,4 |
| водная | 517 | 23,9 |
| щелочная | 1009 | 31,1 |
Как следует из полученных данных, ОЕ кожицы зависит от исходной концентрации, температуры и времени сорбции.
Пример 6 (фиг.5, а, б).
Сорбция из раствора CuSO4, температура 25°С, масса семядолей 14 г. На фиг.4 дана зависимость остаточной концентрации (фиг.5, а) и обменной емкости ОЕ (фиг.5, б) семядолей от исходной концентрации, мг/дм3, времени сорбции, мин, при рН 4 и щелочной обработке сорбента. Цифрами указаны исходные концентрации иона меди (II).
Результаты сорбции из раствора CuCl2 при температуре 70°С и времени сорбции 60 мин:
| Обработка сорбента | Сисх, мг/дм3 | ОЕ, мг/г |
| кислая | 555 | 2,0 |
| щелочная | 555 | 3,1 |
| водная | 555 | 2,3 |
| щелочная | 1110 | 4,3 |
Как следует из полученных данных, ОЕ семядолей слабо зависит от исходной концентрации, температуры и времени.
Пример 7 (фиг.6, а, б)
Сорбция из раствора CuSO4, температура 25°С, масса кожицы 1 г, масса семядолей 14 г.
На фиг.6 дана изотерма сорбции - зависимость СОЕ, мг/г, кожицы (фиг.6, а) и семядолей (фиг.6, б) от равновесной концентрации ионов меди (II) при рН 4 и щелочной обработке сорбента.
Как следует из графиков, СОЕ кожицы в 15 раз превышает СОЕ семядолей.
По сравнению с прототипом показаны возможности быстрого и эффективного извлечения Cu (II) из промышленных и бытовых стоков с использованием продуктов сельскохозяйственного производства.
Способ извлечения ионов меди (II) из водного раствора, включающий сорбцию меди контактированием раствора с кожицей фасоли, отличающийся тем, что в качестве сорбента используют кожицу фасоли, предварительно обработанную в щелочном растворе, и сорбцию осуществляют при рН 4.