Саможелирующиеся альгинатные системы и их применение
Иллюстрации
Показать всеГруппа изобретений относится к медицине, точнее к биосовместимым альгинатным системам, имеющим отсроченный процесс гелеобразования. Предложены наборы и композиции для изготовления саможелирующегося альгинатного геля, содержащие стерильный водорастворимый альгинат и частицы стерильного водонерастворимого альгината с гелеобразующим ионом. Предложены способы дозирования саможелирующейся альгинатной дисперсии для получения саможелирующегося альгинатного геля. Способы могут включать дозирование дисперсии в организм индивидуума. Предложен альгинатный саможелирующийся гель, имеющий толщину более 5 мм и не содержащий один или более из сульфатов, цитратов, фосфатов, лактатов, EDTA или липидов. Предложены имплантируемые устройства, имеющие покрытие из однородного альгинатного геля. Предложены способы улучшения жизнеспособности панкреатических островков или других клеточных агрегатов или ткани после выделения и во время хранения и транспортировки. Группа изобретений обеспечивает создание альгинатной гелеобразующей системы, которая включает альгинат и гелеобразующие ионы, имеющие высокую степень биологической совместимости. Система обеспечивает гелеобразование без изменений pH, связанных с другими системами, и требует минимального количества компонентов. При этом система предусматривает варьирование времени гелеобразования и прочности геля в зависимости от потребностей конкретного применения. 24 н. и 38 з.п. ф-лы, 11 ил. 2 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к альгинатным системам, которые имеют отсроченный процесс гелеобразования, и к компуазозициям, устройствам, наборам и способам изготовления и применения указанных систем.
УРОВЕНЬ ТЕХНИКИ
Данная заявка притязает на приоритет в отношении предварительной заявки США № 60/617852, озаглавленной «Self-Gelling Alginate Systems and Uses Thereof», поданной 12 октября 2004 г., которая включена в настоящий документ в виде ссылки.
Альгинаты представляют собой гидрофильные морские биополимеры, обладающие уникальной способностью образовывать термостабильные гели, которые могут формироваться и отверждаться при физиологически значимых темпуазературах. Альгинаты представляют собой семейство неразветвленных двойных сополимеров остатков β-D-маннуроновой кислоты (М) и α-L-глюкуроновой кислоты (G), соединенных 1-4 гликозидной связью. Относительное количество двух мономеров уроновой кислоты и последовательность их расположения в полимерной цепи широко варьирует в зависимости от природы альгината. Альгинат представляет собой структурный полимер морских бурых водорослей, таких как Laminaria hyperborea, Macrocystis pyrifera, Lessonia nigrescens и Ascophyllum nodosum. Альгинат также вырабатывают некоторые бактерии, такие как Pseudomonas aeruginosa, Azotobacter vinelandii и Pseudomonas fluorescens (WO04011628 A1).
Альгинатные гели образуются, когда двухвалентный катион формирует ионные связи с отрицательно заряженной группой из G остатка каждого из двух различных альгинатных полимеров, в результате чего два полимера оказываются поперечно сшитыми. Образование множества поперечных связей между многочисленными альгинатными полимерами приводит к образованию матрикса, который представляет собой структуру альгинатного геля.
Альгинатные гели могут представлять собой гидрогели, т.е. поперечно сшитые альгинатные полимеры, которые содержат большие количества воды, не растворяясь. Биополимерные гели, такие как альгинатные гидрогели, являются привлекательными кандидатами для тканевой инженерии и других биомедицинских целей. Благодаря этому, а также способности образовывать гели в физиологических условиях, альгинаты широко используются и изучаются для целей инкапсуляции и в качестве биоструктурного материала. Включение клеток в альгинатные гранулы является широко использующейся методикой. Также было показано, что альгинаты представляют собой полезный материал для других типов биологических структур, включая тканевую инженерию, и в качестве каркасов для регенерации нервов.
Существуют различные способы изготовления альгинатных гидрогелей. Наиболее распространенным способом является способ диализа/диффузии, при котором альгинатный раствор желируют диффузией гелеобразующих ионов из внешнего резервуара. Указанный способ обычно используют для изготовления альгинатных гелевых гранул, а также для пищевых целей. Изготовление альгинатных микрогранул представляет собой быстрый процесс, ограничиваемый диффузией гелеобразующих ионов в гелевую сеть. Хотя данный процесс хорошо подходит для заключения клеток в микрогранулы, он менее пригоден для изготовления других форм или структур. Для изготовления гелевых структур больших размеров диффузионные гелеобразующие системы могут иметь ограниченные возможности. Это происходит потому, что быстрый процесс гелеобразования ограничивает время, необходимое для придания формы гелевой структуре.
Задержку процесса гелеобразования можно использовать для инъецирования растворов в организм и/или для примешивания клеток или другого биологического материала к гелевому матриксу до формирования геля. Таким образом, альтернативные способы были разработаны для изготовления других типов биосовместимых альгинатных гелевых структур. Скорость гелеобразования можно уменьшить с помощью действующих изнутри гелеобразующих систем, из которых гелеобразующие ионы высвобождаются внутри формирующегося геля более медленно. Это описывается как затвердевание геля изнутри. Обычно для действующей изнутри гелеобразующей системы кальциевую соль с ограниченной растворимостью или компуазлексированные ионы Са2+ смешивают с альгинатным раствором, в котором ионы кальция медленно высвобождаются. Сульфат кальция используют в носителях для доставки клеток на основе альгината для тканевой инженерии. Высвобождение кальция и кинетику гелеобразования также можно контролировать путем использования кальциевых солей с рН-зависимой растворимостью и добавления медленно действующей кислоты, такой как D-глюконо-δ-лактон (GDL). При изменении рН ионы кальция высвобождаются. Также липосомы, содержащие кальций, используют в качестве контролируемой альгинатной гелеобразующей системы. Альгинатные гелевые системы, основанные на внутреннем гелеобразовании, могут иметь более определенный и ограниченный источник поступления гелеобразующих ионов в противоположность диффузионным системам, в которых ионы кальция диффундируют в альгинатный раствор с образованием насыщенного кальцием геля.
Современные способы изготовления альгинатных гелевых структур имеют ограничения. Некоторые технологии пригодны лишь для изготовления гелей ограниченных размеров и форм. В зависимости от использования могут иметь место проблемы, связанные с контролем кинетики гелеобразования. В некоторых случаях в гелях присутствуют нежелательные материалы, поскольку указанные материалы представляют собой остатки и побочные продукты механизмов гелеобразования, которые контролировались химическими средствами. В некоторых случаях для гелеобразования требуются нефизиологические значения рН, и подобные условия могут представлять ограничения для использования указанных способов. Таким образом существует потребность в других гелеобразующих системах и компуазозициях.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к наборам для изготовления альгинатного геля. Наборы включают в себя первый контейнер, содержащий растворимый альгинат, и второй контейнер, содержащий частицы нерастворимый альгинат/гелеобразующий ион.
Настоящее изобретение относится также к компуазозициям для изготовления альгинатных гелей. Компуазозиции включают непосредственно растворимый альгинат и частицы нерастворимый альгинат/гелеобразующий ион.
Настоящее изобретение относится также к способам дозирования саможелирующейся альгинатной дисперсии. Способы заключаются в формировании дисперсии частиц нерастворимый альгинат/гелеобразующий ион в растворе растворимого альгината и дозировании дисперсии, посредством чего дисперсия формирует альгинатный гелевый матрикс.
Настоящее изобретение относится также к способам дозирования саможелирующейся альгинатной дисперсии индивидууму. Способы заключаются в формировании дисперсии частиц нерастворимый альгинат/гелеобразующий ион в растворе растворимого альгината и дозировании дисперсии индивидууму, посредством чего дисперсия формирует альгинатный гелевый матрикс в теле индивидуума.
Настоящее изобретение относится также к способам дозирования саможелирующейся альгинатной дисперсии индивидууму для применения в качестве материала для увеличения объема ткани, для применения в процедуре эмболизации сосудов, применения для профилактики образования спаек после оперативного вмешательства, для применения в процедуре обработки ран, применения для лечения диабета и применения для лечения артрита.
Настоящее изобретение относится также к способам применения импуазлантируемого альгинатного геля. Способы заключаются в формировании саможелирующегося альгината путем дозирования саможелирующейся альгинатной дисперсии и после образования геля импуазлантирования импуазлантируемого альгинатного геля индивидууму.
Настоящее изобретение относится также к способам изготовления импуазлантируемых устройств.
Настоящее изобретение относится также к альгинатным гелям, имеющим толщину более 5 мм и гомогенную сеть альгинатного матрикса.
Настоящее изобретение относится также к альгинатным гелям, имеющим толщину более 5 мм и не содержащим один или более из сульфатов, цитратов, фосфатов, лактатов, EDTA или липидов.
Настоящее изобретение относится также к импуазлантируемым устройствам, включающим гомогенное альгинатное гелевое покрытие.
Настоящее изобретение относится также к способам пломбирования или восстановления костно-хрящевых дефектов, возникающих в результате остеоартрита, путем дозирования саможелирующейся альгинатной дисперсии, которая содержит хондроциты, в организм индивидуума или путем импуазлантации биологически совместимого матрикса, который содержит хондроциты, в организм индивидуума.
Настоящее изобретение относится также к способам лечения диабета путем дозирования саможелирующейся альгинатной дисперсии, которая содержит инсулинпродуцирующие клетки или многоклеточные агрегаты, в организм индивидуума или путем импуазлантации биологически совместимого матрикса, который содержит инсулинпродуцирующие клетки или многоклеточные агрегаты, в организм индивидуума.
Настоящее изобретение относится также к способам улучшения жизнеспособности панкреатических островков или других клеточных агрегатов или ткани после выделения и во время хранения и транспортировки путем инкорпорирования островков или клеточных агрегатов или ткани в саможелирующуюся альгинатную дисперсию.
Настоящее изобретение относится также к сверхчистым частицам нерастворимый альгинат/гелеобразующий ион и способам их изготовления.
КРАТКОЕ ОПИСАНИЕ ФИГУР
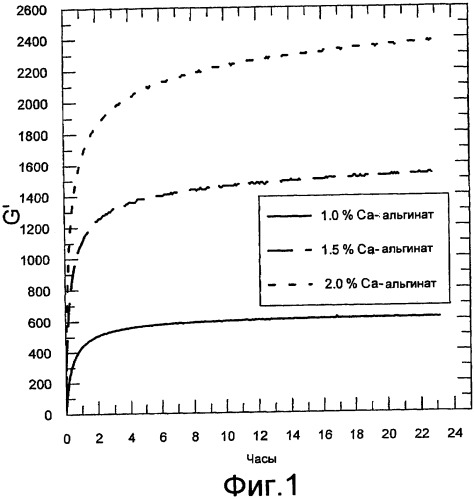
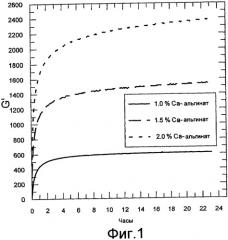
Фигура 1 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей со следующими различными концентрациями альгината кальция (Protaweld TX 120) (концентрации в смеси/геле): 1,0% альгинат кальция, смешанный с 1,0% альгинатом натрия, и 1,5% альгинат кальция, смешанный с 1,0% альгинатом натрия, и 2,0% альгинат кальция, смешанный с 1,0% альгинатом натрия. В качестве альгината натрия использовали Protanal SF 120.
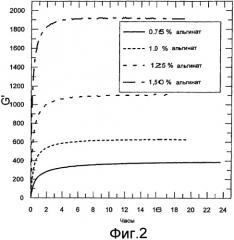
Фигура 2 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, изготовленных смешиванием равных количеств альгината натрия (Protanal SF 120) и альгината кальция (Protaweld TX 120) со следующими концентрациями в геле: 0,75%, 1%, 1,25% или 1,5% альгината натрия и альгината кальция.
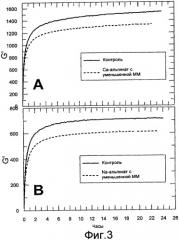
Фигура 3 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, содержащих альгинаты кальция (часть А) и альгинаты натрия (часть В) с различными молекулярными массами. Гели на графике А содержат 1% альгината натрия и 1,5% альгината кальция, а гели на графике В содержат 1% альгината кальция и 1% альгината натрия. В графике А использовали следующие альгинаты: Альгинат кальция: Protaweld TX 120 и Protaweld TX 120, разлагавшийся в течение 33 дней при 60°С. Вязкость (1% раствора при 20°С) двух Са-альгинатов, измеренная как у альгината натрия, составляла 270 и 44 , соответственно. Альгинат натрия: Protanal SF 120. В графике В использовали следующие альгинаты: Альгинат кальция: Protaweld TX 120. Альгинат натрия: Protanal SF 120 и Protanal SF/LF. Вязкость (1% раствора при 20°С) альгинатов натрия составляла 95 и 355 , соответственно.
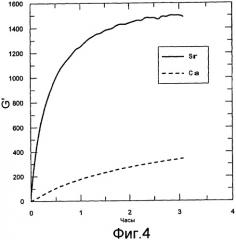
Фигура 4 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, изготовленных с использованием стронция или кальция в качестве гелеобразующих ионов. Количество альгината натрия (Protanal SF 120) и альгината стронция/кальция доводили до 0,75% содержания в геле для каждого. Использовавшийся альгинат кальция получали смешиванием альгиновой кислоты (продукт процесса FMC) (65,2 г) с карбонатом кальция (35,32 г) в лабораторной месилке в течение 1 часа, затем сушкой и размалыванием. Использовавшийся альгинат стронция получали смешиванием альгиновой кислоты (продукт процесса FMC) (65,2 г) с карбонатом стронция (52,10 г) в лабораторной мешалке в течение 1,5 часов, затем сушкой и размалыванием.
Фигура 5 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, содержащих альгинат натрия с высоким и низким содержанием гулуроновой кислоты. На фигуре 5, часть А, количество использовавшихся альгината кальция (Protaweld TX 120) и альгината натрия доводили до 1,0% содержания в геле. Использовали альгинаты натрия Protanal SF 120 (69% G) и Protanal HF 60D (32% G, ММ: 119 000). На фигуре 5, часть В, 5,5% альгината стронция (пример 14) смешивали с 1,25% альгинатом натрия в соотношении 1:4 (конечная концентрация альгината составляла 2,1%). Использовали альгинаты натрия PRONOVA UP 100G (69% G, ММ: 122 000) и PRONOVA UP 100M (46% G, ММ: 119 000). Подбирали как можно более сходные ММ (и вязкость) двух партий альгината натрия. Каждая кривая на фигуре 5, часть В, представляет собой среднее от трех независимых измерений (кривых) со стандартной ошибкой среднего, показанной для каждого пункта.
Фигура 6 показывает стабильность и биоразлагаемость альгинатных гелей, изготовленных с различным содержанием ионов кальция и хранившихся в течение 6 месяцев в физиологических условиях. Гелевые диски изготавливали смешиванием автоклавированной дисперсии альгината кальция (Protaweld TX 120) и стерильного профильтрованного альгината натрия (PRONOVA UP LVG) до конечной концентрации 1,0% каждого альгината и дисперсию желировали в двух чашках Петри. Гелевые диски в одной чашке (маркировка V) промывали 50 мМ хлоридом кальция в течение 10 минут после застудневания, а затем в обе чашки добавляли среду для культивирования клеток (DMEM с добавлением 10% FBS). Чашки хранили в стерильных условиях в СО2-термостате и среду регулярно меняли три раза в неделю. Размеры самого большого гелевого диска в каждой чашке сначала были одними и теми же. Показанные фотографии были сделаны спустя шесть месяцев.
Фигура 7 показывает данные экспериментов с использованием клеток, заключенных в саможелирующийся альгинат. Фигура 7, часть А, показывает мышиные миобласты С2С12 через 45 дней после заключения в саможелирующийся альгинатный гель. Гель изготавливали и хранили, как описано на фигуре 6, но с включенными клетками. Фотография была сделана с использованием флюоресцентного микроскопа после окрашивания клеток кальцеином (Molecular Probes, L-3224) как маркером жизнеспособности клеток. Просветленные области и пятна показывают наличие жизнеспособных клеток. Жизнеспособные клетки располагаются внутри и на поверхности гелевой конструкции. Фигура 7, часть В, показывает человеческие хондроциты, заключенные в саможелирующийся альгинатный гель. Гель изготавливали из 5 мл смешанного саможелирующегося геля PRONOVA SLG 20 и альгината кальция (пример 14), содержавшего человеческие хондроциты. Через три дня после застудневания гели нарезали на 600 мкм среды с использованием вибратома. Гелевые срезы хранили в ростовой среде для клеток в СО2-термостате, а фотография была сделана спустя шесть месяцев. Фотография была сделана с использованием флюоресцентного микроскопа после окрашивания клеток кальцеином (Molecular Probes, L-3224) на предмет жизнеспособности и ясно показывает наличие большого количества жизнеспособных клеток (просветленные участки).
Фигура 8 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, содержащих 1,25% альгината натрия (PRONOVA UP 100G) в смеси с 5,5% альгинатом стронция (пример 14) в соотношении 4:1 (конечная концентрация альгината составляла 2,1%) в присутствии или в отсутствии хлорида натрия или гексаметафосфата натрия. Каждая кривая представляет собой среднее от трех независимых измерений (кривых) со стандартной ошибкой среднего, показанной для каждой точки.
Фигура 9 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, содержащих 1,25% альгината натрия (PRONOVA UP 100G) в смеси с 5,5% альгинатом кальция (пример 14), изготовленным с различными размерами частиц в соотношении 4:1 (конечная общая концентрация альгината составляла 2,1%). Различные размеры частиц получали размалыванием лиофилизированного альгината кальция и просеиванием с получением указанных размеров. Каждая кривая представляет собой среднее от трех независимых измерений (кривых) со стандартной ошибкой среднего, показанной для каждой точки.
Фигура 10 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, содержащих 1,25% альгината натрия (PRONOVA UP LVG) в смеси с 10% альгинатом кальция (пример 14), при различных темпуазературах в соотношении 9:1 (конечная концентрация альгината составляла 2%).
Фигура 11 содержит данные реометрических измерений. Осцилляционные измерения осуществляли с использованием реометра Physica MCR300. Показаны модули хранения в зависимости от времени гелей, содержащих альгинат натрия с различными молекулярными массами. Гель содержит 1,25% альгината натрия (PRONOVA UP 100G), неразложившегося (контроль), или ту же партию альгината, подвергнувшегося разложению. Был изготовлен также гель из разложившегося альгината натрия с концентрацией 2,5% (верхняя кривая). Во всех случаях альгинаты натрия смешивали с 5,5% альгинатом стронция (пример 14) в соотношении 4:1. Каждая кривая представляет собой среднее от трех независимых измерений (кривых) со стандартной ошибкой среднего, показанной для каждой точки.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Разработана альтернативная альгинатная гелеобразующая система. Указанная система используется в многочисленных биомедицинских целях, а также в других областях. Система может включать в себя альгинат и гелеобразующие ионы, которые имеют высокую степень биологической совместимости. Система предусматривает варьирование времени гелеобразования и прочности геля в зависимости от потребностей конкретного применения. Система обеспечивает гелеобразование без изменений рН, связанных с другими системами, и требует минимального количества компуазонентов.
Система включает в себя два компуазонента: один представляет собой растворимый альгинат; другой представляет собой частицы нерастворимый альгинат/гелеобразующий ион. Когда компуазоненты объединяют в присутствии растворителя с получением дисперсии, начинает формироваться альгинатный гель по мере того, как гелеобразующий ион частиц начинает поперечную сшивку альгинатных полимеров из частиц и растворимых альгинатных полимеров в растворе. Два компуазонента можно смешивать путем перемешивания или использования подходящего перемешивающего устройства. Кинетика гелеобразования компуазозиции зависит от нескольких факторов, включая: концентрацию растворимого альгината в растворе, концентрацию частиц нерастворимого альгината в дисперсии, содержание гелеобразующего иона по отношению к альгинату, наличие негелеобразующих ионов или других углеводов, темпуазературу, размер частиц нерастворимый альгинат/гелеобразующий ион, содержание клеток, многоклеточных агрегатов, тканей или других биологических материалов, которые должны быть помещены в гель или присутствуют во время гелеобразования (наличие примесей), и типы использующихся альгинатов, а также процесс изготовления частиц нерастворимого альгината и постпроизводственную обработку альгинатных исходных материалов. Данная альгинатная система, таким образом, может быть широко адаптирована для каждой конкретной цели. Для помещения клеток, многоклеточных агрегатов, тканей или других биологических материалов в формирующийся гель, растворитель, альгинатный раствор или дисперсию можно предварительно смешивать с материалом, который должен быть в него заключен.
Дисперсию можно дозировать индивидууму в виде жидкости/взвеси в тот участок, в котором желательно получить альгинатный гелевый матрикс. Образование альгинатного геля, инициированное, когда растворимый альгинат и частицы нерастворимого альгината/гелеобразующего иона смешали в присутствии растворителя, продолжается и альгинатный гель затвердевает in situ. Используемый в настоящем документе термин «саможелирующийся» относится к процессу гелеобразования, который наблюдается, когда растворимый альгинат и частицы нерастворимый альгинат/гелеобразующий ион смешивают в присутствии растворителя. «Саможелирующийся альгинат» представляет собой альгинатную дисперсию или гель, который включает в себя или образован растворимым альгинатом и частицами нерастворимый альгинат/гелеобразующий ион в растворителе.
Компуазоненты, использующиеся в системе, можно содержать перед употреблением в любой из нескольких форм. Например, растворимый альгинат можно содержать в растворе или в виде порошка. В некоторых вариантах осуществления настоящего изобретения растворимый альгинат можно содержать в виде порошка, который немедленно растворяется, такого как лиофилизированный порошок. Подобно этому частицы нерастворимый альгинат/гелеобразующий ион можно содержать в виде дисперсии или в виде порошка.
Альгинатные полимеры или их комбинации, используемые в растворимом альгинате, могут быть одними и теми же или отличаться от альгинатных полимеров или их комбинаций в частицах нерастворимый альгинат/гелеобразующий ион.
Концентрация альгината, как растворимого альгината, так и альгината в форме частиц нерастворимый альгинат/гелеобразующий ион, в дисперсии по отношению к количеству растворителя влияет на время гелеобразования, порозность, стабильность и биоразлагаемость, прочность и эластичность гелей, и можно изготавливать гели, обладающие конкретными свойствами, с использованием конкретных соотношений растворимого альгината и частиц нерастворимый альгинат/гелеобразующий ион с растворителем. Обычно, чем ниже концентрация альгината (для данного соотношения растворимого альгината и нерастворимого альгината), тем более биоразлагаемым будет гель. В некоторых вариантах осуществления настоящего изобретения можно использовать приблизительно 0,5%, 0,75%, 1%, 1,25%, 1,5%, 2%, 2,5%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10% или более альгината (растворимого альгината и альгината в форме частиц нерастворимый альгинат/гелеобразующий ион).
Относительная концентрация растворимого альгината по отношению к альгинату в форме частиц нерастворимый альгинат/гелеобразующий ион в дисперсии влияет на время гелеобразования, размер пор, прочность и эластичность гелей, а также стабильность и биоразлагаемость, и можно изготавливать гели, обладающие конкретными свойствами, с использованием конкретных соотношений растворимого альгината и частиц нерастворимый альгинат/гелеобразующий ион. В некоторых вариантах осуществления настоящего изобретения концентрация растворимого альгината приблизительно равна концентрации альгината в форме частиц нерастворимый альгинат/гелеобразующий ион (1:1). В некоторых вариантах осуществления настоящего изобретения концентрация альгината в форме частиц нерастворимый альгинат/гелеобразующий ион в два раза превышает концентрацию растворимого альгината (2:1). В некоторых вариантах осуществления настоящего изобретения концентрация альгината в форме частиц нерастворимый альгинат/гелеобразующий ион составляет половину от концентрации растворимого альгината (1:2). В некоторых вариантах осуществления настоящего изобретения концентрация альгината в форме частиц нерастворимый альгинат/гелеобразующий ион относится к концентрации растворимого альгината как 1 к 0,7 (1:0,7). Обычно, чем меньше наличие гелеобразующего иона, тем более биоразлагаемым будет гель. Можно применять уменьшение концентрации нерастворимого альгината/гелеобразующего иона в системе, чтобы создавать гели с более низкой стабильностью и более высокой биоразлагаемостью, связанных с тем, что гелевая сеть является менее насыщенной ионами, обеспечивающими поперечную сшивку. Саможелирование вносит поправку в изготовление гелей с более низкими концентрациями гелеобразующего иона, чтобы получать гели, особенно хорошо подходящие для таких целей, где требуется биологическое разложение. В некоторых предпочтительных вариантах осуществления настоящего изобретения отношения альгинатов в частицах нерастворимый альгинат/гелеобразующий ион и растворимого альгината составляют 5:1, 4:1, 3:1, 2:1, 1:1, 1:2, 1:3, 1:4 или 1:5.
Относительное содержание мономеров G и М в альгинатных полимерах влияет на размер пор, стабильность и биоразлагаемость, прочность и эластичность гелей. Альгинатные полимеры имеют различные вариации общего содержания М и G, и относительное содержание последовательных структур также широко варьирует (G-блоки, М-блоки и MG перемежающиеся последовательности), как и длина последовательностей по ходу полимерной цепи. Обычно, чем ниже содержание G по сравнению с содержанием М в используемых альгинатных полимерах, тем более биоразлагаемым будет гель. Гели с высоким содержанием G в альгинате обычно имеют большие размеры пор и являются более прочными по сравнению с гелями с высоким содержанием М в альгинате, у которых размеры пор меньше, а прочность ниже. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат более 50% α-L-гулуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат более
60% α-L-гулуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат от 60% до 80% α-L-гулуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат от 65% до 75% α-L-гулуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат более 70% α-L-гулуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат более 50% С-5 эпимера β-D-маннуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат более 60% С-5 эпимера β-D-маннуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат от 60% до 80% С-5 эпимера β-D-маннуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат от 65% до 75% С-5 эпимера β-D-маннуроновой кислоты. В некоторых вариантах осуществления настоящего изобретения один или более из альгинатных полимеров альгинатного матрикса содержат более 70% С-5 эпимера β-D-маннуроновой кислоты. Процедуры получения уроновых блоков описаны в патенте США № 6121441. G-блоковые альгинатные полимеры и их применение в качестве модуляторов свойств альгинатных гелей описаны в патенте США № 6407226. Некоторые предпочтительные варианты осуществления настоящего изобретения, 30% G, 35% G, 40% G, 45% G, 50% G, 55% G, 60% G, 65% G, 70% G, 75% G, 80% G или 85% G.
Средняя молекулярная масса альгинатных полимеров влияет на время гелеобразования, размер пор, прочность и эластичность гелей. Альгинатные полимеры могут иметь средние молекулярные массы от 2 до 1000 кДа. Молекулярная масса альгинатов может влиять на гелеобразование и окончательные свойства геля. Обычно, чем ниже молекулярная масса используемого альгината, тем более биоразлагаемым будет гель. Альгинатные полимеры или их комбинации, используемые в компуазонентах растворимого альгината, могут быть одними и теми же или отличаться от полимеров или их комбинаций, используемых в частицах нерастворимый альгинат/гелеобразующий ион. В некоторых вариантах осуществления настоящего изобретения альгинатные полимеры альгинатного матрикса имеют среднюю молекулярную массу от 5 до 350 кДа. В некоторых вариантах осуществления настоящего изобретения альгинатные полимеры альгинатного матрикса имеют среднюю молекулярную массу от 2 до 100 кДа. В некоторых вариантах осуществления настоящего изобретения альгинатные полимеры альгинатного матрикса имеют среднюю молекулярную массу от 50 до 500 кДа. В некоторых вариантах осуществления настоящего изобретения альгинатные полимеры альгинатного матрикса имеют среднюю молекулярную массу от 100 до 1000 кДа. В некоторых вариантах осуществления настоящего изобретения разработаны гели, имеющие высокую степень биоразлагаемости. Соответственно, гели, содержащие меньше альгината, меньше гелеобразующего иона, альгинаты с более низким содержанием G и более низкими молекулярными массами, можно изготавливать с использованием более низких лимитов указанных параметров, как описано в настоящем документе, чтобы получать гели с более высокой степенью биоразлагаемости.
Альгинат может обладать вязкостью в 1% растворе, измеренной при 20 градусах Цельсия, от 25 до 1000 и в некоторых вариантах осуществления настоящего изобретения, предпочтительно, от 50 до 1000 (1% раствор, 20°С).
В некоторых вариантах осуществления настоящего изобретения предпочтительно, чтобы способы изготовления частиц нерастворимый альгинат/гелеобразующий ион обеспечивали продукты со стехиометрическим количеством (100% насыщение) гелеобразующего иона. Использование указанных стехиометрических солей сообщает саможелирующимся альгинатным системам более высокую воспроизводимость. В некоторых вариантах осуществления настоящего изобретения предпочтительно, чтобы способ изготовления частиц нерастворимый альгинат/гелеобразующий ион обеспечивал продукты с субстехиометрическим количеством (< 100% насыщение) указанного гелеобразующего иона. Использование указанных субстехиометрических солей сообщает саможелирующимся альгинатным системам биоразлагаемость.
В некоторых вариантах осуществления настоящего изобретения альгинат представляет собой сверхчистый альгинат. Сверхчистый альгинат является коммерчески доступным, например, из различных морских водорослей, таких как Laminaria Hyperborea. Коммерческие кальциевые соли альгиновой кислоты обычно производят с использованием процессов, при которых кальций добавляют к альгиновой кислоте в твердой фазе простым смешиванием и перемешиванием компуазонентов. Примерами коммерчески доступных кальциевых солей альгиновой кислоты являются Protaweld (от FMC BioPolymer) и Kelset от ISP Corporation. Частицы нерастворимый альгинат/гелеобразующий ион можно изготавливать с использованием сверхчистого альгината путем изготовления альгинатного геля с использованием сверхчистого альгината и гелеобразующего иона, отмывания от натриевых и других ионов, которые присутствовали в сверхчистом альгинате, сушки геля для удаления воды и изготовления частиц из высушенного геля. В некоторых вариантах осуществления настоящего изобретения частицы нерастворимый альгинат/гелеобразующий ион представляют собой стехиометрические соли. Частицы нерастворимый альгинат/гелеобразующий ион предпочтительно имеют высокую чистоту и особое, постоянное и обычно однородное содержание гелеобразующего иона, такого как, например, кальций или стронций, барий, цинк, железо, марганец, медь, свинец, кобальт, никель или их комбинации, таким образом, чтобы скорость гелеобразования и прочность геля можно было обеспечить с более высокой степенью предсказуемости. Нерастворимые соли альгиновой кислоты с щелочноземельными металлами, такие как, например, альгинат кальция или альгинат стронция (в зависимости от используемого гелеобразующего иона), или нерастворимые соли альгиновой кислоты с переходными металлами (такие как соли с гелеобразующими ионами меди, никеля, цинка, свинца, железа, марганца или кобальта) можно изготавливать с использованием известного и заранее определенного количества ионов щелочных металлов путем осаждения из растворов. В некоторых вариантах осуществления настоящего изобретения коммерчески доступный альгинат натрия сначала используют для изготовления раствора альгината натрия. Необязательно, натриевую соль, такую как карбонат натрия, можно включать в раствор альгината натрия. Соль, содержащую желательный гелеобразующий ион для частицы нерастворимый альгинат/гелеобразующий ион, такую как, например, соль кальция или соль стронция, такую как хлорид кальция или хлорид стронция, используют для изготовления раствора. Раствор альгината натрия объединяют, предпочтительно медленно, с раствором гелеобразующего иона. Предпочтительно, объединенные растворы непрерывно перемешивают во время процесса смешивания. Нерастворимый альгинат, такой как, например, альгинат кальция или альгинат стронция (в зависимости от используемого гелеобразующего иона), выпадает в осадок из объединенных растворов. Осажденный нерастворимый альгинат затем следует удалить из раствора и повторно отмывать, например, 2-10 раз очищенной водой, чтобы удалить все растворимые ионы. Удаление растворимых ионов подтверждается, например, тестированием проводимости нерастворимого альгината в очищенной воде по сравнению с проводимостью очищенной воды. После отмывания нерастворимый альгинат можно высушить, например, в условиях вакуума. Высушенный альгинат можно размалывать и в некоторых вариантах осуществления настоящего изобретения сортировать по размеру частиц.
В некоторых вариантах осуществления настоящего изобретения альгинат является стерильным. В некоторых предпочтительных вариантах осуществления настоящего изобретения альгинат представляет собой стерильный сверхчистый альгинат. Условия, которые часто используются для стерилизации материала, могут изменить альгинат, например уменьшить молекулярную массу. В некоторых вариантах осуществления настоящего изобретения стерильный альгинат изготавливают с использованием стерилизационных фильтров. В некоторых вариантах осуществления настоящего изобретения альгинат имеет уровень эндотоксина <25 ЭЕ/грамм.
В некоторых вариантах осуществления настоящего изобретения альгинатный матрикс может быть покрыт поликатионным полимером, подобным полиаминокислотному полимеру или хитозану, после формирования гелевого матрикса. В некоторых вариантах осуществления настоящего изобретения поликатионным полимером является полилизин. В некоторых вариантах осуществления настоящего изобретения полилизин связан с другой частью, и полилизин, таким образом, используется для облегчения связи указанной части с гелем. Примеры частей, связанных с гелем с использованием поликатионных полимеров, включают, например, лекарственные средства, пептиды, контрастные реагенты, лиганды, связывающиеся с рецепторами, или другие детектируемые метки. Некоторые конкретные примеры включают фактор роста эндотелия сосудов (VEGF), фактор роста эпидермиса (EGF), трансформирующий фактор роста (TGF) и морфогенный белок костей (BMP). Лекарственные средства могут включать противораковые химиотерапевтические агенты, такие как таксол, цисплатин и/или другие производные, содержащие платину. Углеводные полимеры могут включать гиалуронан, хитозан, гепарин, ламинарин, фукоидан, хондроитинсульфат. В некоторых вариантах осуществления настоящего изобретения используемые альгинаты представляют собой модифицированные альгинатные полимеры, такие как химически модифицированный альгинат, в котором один или более полимеров связаны с другим альгинатным полимером. Примеры указанных модифицированных альгинатных полимеров можно найти в патенте США № 6642363, который включен в настоящий документ в качестве ссылки.
В некоторых вариантах осуществления настоящего изобретения альгинатный полимер может включать неальгинатную часть, такую как, например, лекарственное средство, пептид, контрастный реагент, лиганд, связывающийся с рецепторами, или другую детектируемую метку. В од