Антагонисты crf-рецепторов и способы, относящиеся к ним
Иллюстрации
Показать всеИзобретение относится к 3-(2-метокси-4-пиразол-1-илфенил)-2,5-диметил-7-(3-метилпиридин-2-ил)пиразоло[1,5-а]пиримидину или его фармацевтически приемлемым солям, сольвату, стереоизомеру, имеющему приведенную ниже структурную формулу, которые являются антагонистами CRF-рецепторов и могут быть применены в лечении разнообразных расстройств, вызывающих гиперсекрецию CRF у теплокровных животных, такую как при внезапном приступе. Также изобретение относится к промежуточным соединениям, фармацевтической композиции на основе указанного соединения и способу лечения расстройства, вызывающего гиперсекрецию CRF у млекопитающего. 9 н. 6 з.п. ф-лы, 14 табл.
Реферат
Перекрестная ссылка на родственную заявку
Данная заявка заявляет приоритет предварительной заявки США с регистрационным номером 60/532031, поданной 12 декабря 2003 г, полное раскрытие которой включено в данную работу посредством ссылки.
Область техники, к которой относится изобретение
Данное изобретение относится в основном к антагонистам CRF-рецепторов и к способам лечения расстройств введением таких антагонистов млекопитающему, нуждающемуся в этом.
Уровень изобретения
Впервые кортикотропинрилизинг-фактор (CRF) был выделен из овечьего гипоталамуса и идентифицирован как 41-аминокислотный пептид (Vale et al., Science 213:1394-1397, 1981). Затем были выделены последовательности CRF человека и крысы и определена их идентичность, но с отличием от овечьего CRF в 7 из 41 аминокислотного остатка (Rivier et al., Proc. Natl. Acad. Sci. USA 80:4851, 1983; Shibahara et al., EMBO J. 2:775, 1983).
Было установлено, что CRF вызывает глубокие изменения в функции эндокринной, нервной и иммунной систем. Полагают, что CRF является главным физиологическим регулятором базального и высвобождаемого при стрессе адренокортикотропного гормона (“АСТН”), β-эндорфина и других пептидов, производных проопиомеланокортина (“РОМC”) из аденогипофиза (Vale et al., Science 213:1394-1397, 1981). Короче, предполагается, что CRF инициирует свои биологические эффекты связыванием с плазменным мембранным рецептором, который, как было установлено, распределен в головном мозге (DeSouza et al., Science 224:1449-1451, 1984), гипофизе (DeSouza et al., Methods Enzymol. 124:560, 1986; Wynn et al., Biochem. Biophys. Res. Comm. 110:602-608, 1983), надпочечниках (Udelsman et al., Nature 319:147-150, 1986) и селезенке (Webster, E.L. and E.B. DeSouza, Endocrinology 122:609-617, 1988). СRF-рецептор сочетается с GTP-связывающим протеином (Perrin et al., Endocrinology 118:1171-1179, 1986), который опосредует CRF-стимулируемое повышение внутриклеточного образования сАМР (Bilezikjian, L.M., and W.W. Vale, Endocrinology 113:657-662, 1983). Рецептор для CRF в настоящее время клонирован от крысы (Perrin et al., Endo 133(6):3058-3061, 1993) и головного мозга человека (Chen et al., PNAS 90(19):8967-8971, 1993; Vita et al., FEBS 335(1):1-5, 1993). Данный рецептор представляет собой протеин из 415 аминокислот, содержащий семь мембранных протяженных доменов. Сравнение идентичности между последовательностями крысы и человека показывает высокую степень гомологии (97%) на аминокислотном уровне.
В дополнение к своей роли в стимулировании образования АСТН и РОМС считается, что CRF координирует многие эндокринные, автономные и поведенческие реакции на стресс и может быть включен в патофизиологию аффективных расстройств. Кроме того, полагают, что CRF является ключевым промежуточным звеном в связи между иммунной, центральной нервной, эндокринной и сердечно-сосудистой системами (Crofford et al., J. Clin. Invest. 90:2555-2564, 1992; Sapolsky et al., Science 238:522-524, 1987; Tilders et al., Regul. Peptides 5:77-84, 1982). В целом, CRF, по-видимому, является одним из основных нейротрансмиттеров центральной нервной системы и играет решающую роль в объединении общего ответа организма на стресс.
Введение CRF непосредственно в головной мозг вызывает поведенческие, физиологические и эндокринные реакции, идентичные реакциям, наблюдаемым у животных под воздействием стрессов в окружающей среде. Например, интрацеребровентрикулярная инъекция CRF приводит к активации поведения (Sutton et al., Nature 297:331, 1982), стойкой активации электроэнцефалограммы (Ehlers et al., Brain Res. 278: 332, 1983), cтимулированию симпатоадреномедуллярного пути (Brown et al., Endocrinology 110:928, 1982), повышению частоты сердечных сокращений и кровяного давления (Fisher et al., Endocrinology 110:2222, 1982), повышению потребления кислорода (Brown et al., Life Sciences 30:207, 1982), изменению активности желудочно-кишечного тракта (Williams et al., Am. J. Physiol. 253:G582, 1987), подавлению потребления пищи (Levine et al., Neuropharmacology 22:337, 1983), изменению сексуального поведения (Sirinathsinghji et al., Nature 305:232, 1983) и иммунной функциональной недостаточности (Irwin et al., Am. J. Physiol. 255:R744, 1988). Кроме того, клинические данные свидетельствуют о том, что CRF может выделяться в повышенных количествах в головном мозге при депрессии, нарушениях, связанных с состояниями тревоги/страха, и анорексии невроза (DeSouza, Ann. Reports in Med. Chem. 25:215-223, 1990). В соответствии с этим клинические данные свидетельствуют о том, что антагонисты CRF-рецепторов могут представлять собой новые антидепрессантные и/или анксиолитические лекарственные средства, которые могут быть применимы в лечении нервно-психических расстройств, проявляющихся из-за гиперсекреции CRF.
Первые антагонисты CRF-рецепторов представляли собой пептиды (см., например, Rivier et al., U.S. Patent No. 4605642; Rivier et al., Science 224:889, 1984). Хотя данные пептиды показали, что антагонисты CRF-рецепторов могут ослаблять фармакологические реакции на CRF, пептидным антагонистам CRF-рецепторов свойственны обычные недостатки пептидных медикаментов, включающие недостаток стабильности и ограниченную пероральную активность. Некоторые из опубликованных патентных документов включают US 6313124, WO 01/23388 и WO 97/29109, все из которых раскрывают пиразолопиримидиновые соединения в качестве CRF-антагонистов. Опубликованная заявка WO 98/54093 описывает некоторые пиразолопиримидиновые соединения в качестве ингибиторов тирозинкиназы.
Благодаря физиологической роли CRF разработка биологически активных малых молекул, обладающих значительной связывающей активностью CRF-рецепторов и способных быть антагонистами CRF-рецепторов, остается актуальной задачей. Такие антагонисты CRF-рецепторов были бы полезны в лечении эндокринных, психических и неврологических состояний или заболеваний, включающих нарушения, связанные со стрессами вообще.
Хотя были сделаны значительные шаги в отношении достижения регулирования CRF путем введения антагонистов CRF-рецепторов, остается потребность в области эффективных малых молекул антагонистов CRF-рецепторов. Существует также потребность в отношении фармацевтических композиций, содержащих такие антагонисты CRF-рецепторов, а также способов, относящихся к их применению, для лечения, например, нарушений, связанных со стрессами. Данное изобретение восполняет указанные потребности и предоставляет другие сопутствующие преимущества.
Сущность изобретения
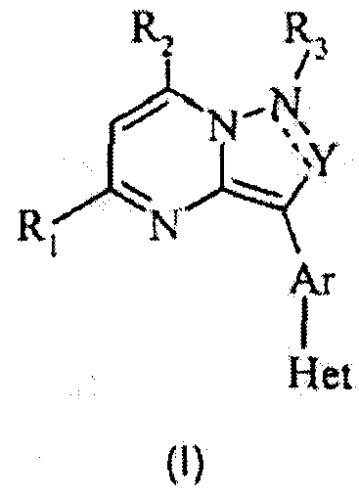
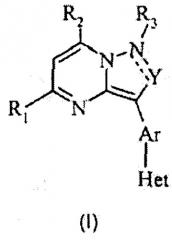
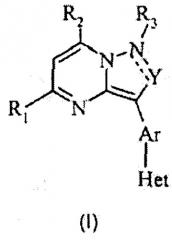
Вкратце, данное изобретение относится к антагонистам CRF-рецепторов и конкретнее к антагонистам CRF-рецепторов, имеющим следующую общую структуру (I):
и их фармацевтически приемлемым солям, эфирам, сольватам, стереоизомерам и пролекарствам, где R1, R2, R3, Y, Ar и Het принимают значения, определенные ниже.
Антагонисты CRF-рецепторов могут найти применение в широком диапазоне терапевтических аппликаций и могут быть использованы для лечения многих расстройств или заболеваний, включающих нарушения, связанные со стрессами. Такие способы включают введение фармацевтически активного количества антагониста CRF-рецепторов, предложенного в данном изобретении, предпочтительно в форме фармацевтической композиции, животному, нуждающемуся в этом. Соответственно в другом варианте осуществления раскрываются фармацевтические композиции, содержащие один или несколько антагонистов CRF-рецепторов, предложенных в данном изобретении, и фармацевтически приемлемый носитель и/или разбавитель.
Данные и другие аспекты изобретения будут очевидными после отсылки к следующему подробному описанию. С этой целью в данной работе приводятся различные ссылки, которые описывают более подробно некоторые процедуры, соединения и/или композиции, и, таким образом, включаются ссылкой полностью.
Подробное описание изобретения
Данное изобретение относится в основном к антагонистам рецепторов кортикотропинрилизинг-фактора (CRF).
В первом варианте осуществления антагонисты CRF-рецепторов, предложенные в данном изобретении, имеют следующую структуру (I):
или представляют собой их фармацевтически приемлемую соль, эфир, сольват, стереоизомер или пролекарство,
где:
“---” представляет вторую связь необязательной двойной связи;
R1 представляет собой водород, алкил, замещенный алкил, гетероарил, замещенный гетероарил, -NH2 или галоген;
R2 представляет собой алкил, замещенный алкил, -С(О)NR7R8, арил, замещенный арил, арилоксиалкил, замещенный арилоксиалкил, гетероарилалкоксиалкил, замещенный гетероарилалкоксиалкил, гетероциклоалкил, замещенный гетероциклоалкил, арилалкил, замещенный арилалкил, гетероарил или замещенный гетероарил, где указанный гетероарил или замещенный гетероарил присоединен к пиримидиновому циклу через углерод-углеродную связь;
R3 отсутствует или представляет собой водород или алкил;
Y представляет собой =(СR4)- или -(С=О)-;
R4 представляет собой водород, алкил, замещенный алкил, тиоалкил, алкилсульфинил или алкилсульфонил;
Ar представляет собой фенил, фенил, замещенный 1 или 2 R5, пиридил или пиридил, замещенный 1 или 2 R5;
R5 в каждом случае представляет собой гидрокси, алкил, замещенный алкил, алкокси, замещенный алкокси, циано, галоген, алкилсульфонил или алкилсульфинил;
Het представляет собой гетероарил, необязательно замещенный 1 или 2 R6;
R6 в каждом случае представляет собой гидрокси, алкил, замещенный алкил, алкокси, замещенный алкокси, циано или галоген; и
R7 и R8 независимо представляют собой водород, алкил, замещенный алкил, арил, замещенный арил, гетероцикл, замещенный гетероцикл, арилалкил, замещенный арилалкил, гетероциклоалкил или замещенный гетероциклоалкил; или
R7 и R8 вместе с азотом, к которому они присоединены, образуют гетероциклическое кольцо или замещенное гетероциклическое кольцо.
Вышеупомянутые термины, использованные в данной работе, имеют следующее значение:
“Алкил” означает углеводород с прямой или разветвленной цепью, ациклический или циклический, насыщенный или ненасыщенный, содержащий от 1 до 10 атомов углерода, хотя термин “низший алкил” имеет то же значение, как и алкил, но содержит от 1 до 6 атомов углерода. Типичные насыщенные алкилы с прямой цепью включают метил, этил, н-пропил, н-бутил, н-пентил, н-гексил и тому подобное; в то время как насыщенные разветвленные алкилы включают изопропил, втор-бутил, изобутил, трет-бутил, изо-пентил и тому подобное. Типичные насыщенные циклические алкилы включают циклопропил, циклобутил, циклопентил, циклогексил, -СН2-циклопропил, -СН2-циклобутил, -СН2-циклопентил, -СН2-циклогексил и тому подобное; в то время как ненасыщенные циклические алкилы включают циклопентенил и циклогексенил и тому подобное. Циклические алкилы, также называемые как “гомоциклические кольца”, включают ди- и полигомоциклические кольца, такие как декалин и адамантил. Ненасыщенные алкилы содержат, по меньшей мере, одну двойную или тройную связь между соседними атомами углерода (называемые как “алкенил” или “алкинил” соответственно). Типичные алкенилы с прямой и разветвленной цепью включают этиленил, пропиленил, 1-бутенил, 2-бутенил, изобутиленил, 1-пентенил, 2-пентенил, 3-метил-1-бутенил, 2-метил-2-бутенил, 2,3-диметил-2-бутенил и тому подобное; в то время как типичные алкинилы с прямой и разветвленной цепью включают ацетиленил, пропинил, 1-бутинил, 2-бутинил, 1-пентинил, 2-пентинил, 3-метил-1-бутинил и тому подобное.
“Алкилиденил” представляет собой дивалентный алкил, для образования которого два атома водорода взяты от одного и того же атома углерода, такой как =СН2, =СНСН3, =СНСН2СН3, =С(СН3)СН2СН3 и тому подобное.
“Арил” означает ароматический карбоциклический фрагмент, такой как фенил или нафтил.
“Арилалкил” означает алкил, содержащий, по меньшей мере, один алкильный атом водорода, замещенный арилом, такой как бензил (т.е. -СН2фенил, -СН2-(1- или 2-нафтил), -(СН2)2фенил, -(СН2)3фенил, -СН(фенил)2 и тому подобное.
“Арилоксиалкил” означает арил, присоединенный через кислородный мостик к алкилу (т.е. арил-О-алкил-), такой как -метил-О-фенил и т.п.
“Гетероарил” означает ароматическое гетероциклическое кольцо из 5-10 членов, содержащее, по меньшей мере, один гетероатом, выбранный из азота, кислорода и серы, и содержащее, по меньшей мере, один атом углерода, включающее как моно-, так и бициклические кольцевые системы. Типичные гетероарилы включают (но без ограничения только ими) фурил, бензофуранил, тиофенил, бензотиофенил, пирролил, индолил, изоиндолил, азаиндолил, пиридил, хинолинил, изохинолинил, оксазолил, изооксазолил, бензоксазолил, пиразолил, имидазолил, бензимидазолил, тиазолил, бензотиазолил, изотиазолил, пиридазинил, пиримидинил, пиразинил, триазинил, циннолинил, фталазинил и хиназолинил.
“Гетероарилалкил” означает алкил, содержащий, по меньшей мере, один алкильный атом водорода, замещенный гетероарилом, такой как -СН2-пиридинил, -СН2-пиримидинил и тому подобное.
“Гетероцикл” (также называемый в настоящей работе как “гетероциклическое кольцо”) означает 5-7-членное моноциклическое, или 7-14-членное полициклическое, гетероциклическое кольцо, которое является либо насыщенным, либо ненасыщенным или ароматическим и которое содержит от 1 до 4 гетероатомов, независимо выбранных из азота, кислорода и серы, и в котором гетероатомы азота и серы могут быть необязательно окисленными, и гетероатом азота может быть необязательно кватернизованным, включающий бициклические кольца, в которых любые из вышеуказанных гетероциклов являются конденсированными с бензольным кольцом, а также трициклическими (и более) гетероциклическими кольцами. Гетероцикл может быть присоединен через гетероатом или атом углерода. Гетероциклы включают гетероарилы, определенные выше. Таким образом, в дополнение к ароматическим гетероарилам, перечисленным выше, гетероциклы также включают (но без ограничения только ими) морфолинил, пирролидинонил, пирролидинил, пиперидинил, пиперазинил, гидантоинил, валеролактамил, оксиранил, оксетанил, тетрагидрофуранил, тетрагидропиранил, тетрагидропиридинил, тетрагидропиримидинил, тетрагидротиофенил, тетрагидротиопиранил и тому подобное.
“Гетероциклоалкил” означает алкил, содержащий, по меньшей мере, один алкильный атом водорода, замещенный гетероциклом, такой как -СН2-морфолинил, и тому подобное.
Термин “замещенный”, используемый в данной работе, относится к любой группе (например, алкилу, арилу, арилалкилу, гетероарилу, гетероарилалкилу, гетероциклу или гетероциклоалкилу), в которой, по меньшей мере, один атом водорода замещен заместителем. В случае кетозаместителя (“-С(=О)-”) замещены два атома водорода. “Заместители” по тексту данного изобретения включают галоген, гидрокси, циано, нитро, амино, алкиламино, диалкиламино, алкил, алкокси, тиоалкил, галогеналкил, гидроксиалкил, арил, замещенный арил, арилалкил, замещенный арилалкил, гетероарил, замещенный гетероарил, гетероарилалкил, замещенный гетероарилалкил, гетероцикл, замещенный гетероцикл, гетероциклоалкил, замещенный гетероциклоалкил, -NRaRb, -NRaC(=O)Rb, -NRaC(=O)NRaRb, -NRaC(=O)ORb, -NRaSO2Rb, -ORa, -C(=O)Ra, -C(=O)ORa, -C(=O)NRaRb, -OC(=O)NRaRb, -SH, -SRa, -SORa, -S(=O)2Ra, -OS(=O)2Ra, -S(=O)2ORa, где Ra и Rb одинаковые или различные и независимо представляют собой водород, алкил, галогеналкил, замещенный алкил, арил, замещенный арил, арилалкил, замещенный арилалкил, гетероарил, замещенный гетероарил, гетероарилалкил, замещенный гетероарилалкил, гетероцикл, замещенный гетероцикл, гетероциклоалкил или замещенный гетероциклоалкил.
“Галоген” означает атом фтора, хлора, брома или иода.
“Галогеналкил” означает алкил, содержащий, по меньшей мере, один атом водорода, замещенный галогеном, такой как трифторметил и тому подобное. Галогеналкил представляет собой конкретный вариант осуществления замещенного алкила, где алкил замещен одним или несколькими атомами галогена.
“Алкокси” означает алкил, присоединенный через кислородный мостик (т.е. -О-алкил), такой как -О-метил, -О-этил, и тому подобное.
“Тиоалкил” означает алкил, присоединенный через серный мостик (т.е. -S-алкил), такой как -S-метил, -S-этил, и тому подобное.
“Алкиламино” и “диалкиламино” означают одну или две алкильные группы, присоединенные через азотный мостик (т.е. -NHалкил или -N(алкил)(алкил)), такие как метиламино, этиламино, диметиламино, диэтиламино, и тому подобное.
“Гидроксиалкил” означает алкил, замещенный, по меньшей мере, одной гидроксигруппой.
“Моно- или ди(циклоалкил)метил” представляет собой метильную группу, замещенную одной или двумя циклоалкильными группами, такой как циклопропилметил, дициклопропилметил и тому подобное.
“Алкилкарбонилалкил” представляет собой алкил, замещенный -С(=О)алкильной группой.
“Алкилкарбонилоксиалкил” представляет собой алкил, замещенный -С(=О)Оалкильной группой или -ОС(=О)алкильной группой.
“Алкоксиалкил” представляет собой алкил, замещенный -О-алкильной группой.
“Алкилтиоалкил” представляет собой алкил, замещенный -S-алкильной группой.
“Моно- или ди(алкил)амино” представляет собой аминогруппу, замещенную одним или двумя алкилами соответственно.
“Моно- или ди(алкил)аминоалкил” представляет собой алкил, замещенный моно- или ди(алкил)аминогруппой.
“Алкилсульфонил или алкилсульфинил” представляет собой алкил, замещенный (-S(=O)2-) или (-S(=O)-) функциональными группами соответственно.
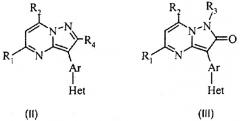
Варианты осуществления данного изобретения даются как пример и не предназначены для ограничения. В первом варианте осуществления изобретения R3 отсутствует и Y означает =(СR4)- в приведенной структуре (II), и в следующем варианте осуществления Y означает -(С=О)- в приведенной структуре (III).
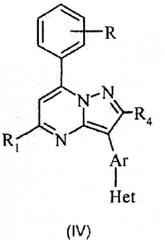
Следующие варианты осуществления относятся к структуре (IV), где R2 означает фенил, R представляет собой необязательный заместитель указанного фенила, и Y означает =(СR4)-.
В следующих вариантах осуществления данного изобретения, где Y означает =(СR4)-, Ar представляет собой фенил, замещенный на 2 R5 в структуре (V), и Het представляет собой пиридил, замещенный на 1 R6 в структуре (VI).
Cоединения данного изобретения, в основном, могут быть применены в виде свободного основания. В альтернативном случае соединения данного изобретения могут быть использованы в виде кислотно-аддитивных солей. Кислотно-аддитивные соли свободно-основных аминосоединений данного изобретения могут быть приготовлены способами, хорошо известными в данной области, и могут быть получены с органическими и неорганическими кислотами. Подходящие органические кислоты включают малеиновую, фумаровую, бензойную, аскорбиновую, янтарную, метансульфоновую, уксусную, щавелевую, пропионовую, винную, салициловую, лимонную, глюконовую, молочную, миндальную, коричную, аспаргиновую, стеариновую, пальмитиновую, гликолевую, глутаминовую и бензолсульфоновую кислоты. Подходящие неорганические кислоты включают хлористоводородную, бромистоводородную, серную, фосфорную и азотную кислоты. Таким образом, термин “фармакологически приемлемая соль” структуры (I) предназначена для охвата любых и всяких фармацевтически приемлемых солевых форм.
Вообще, соединения структуры (I) могут быть сделаны по методикам органического синтеза, известным специалистам в данной области, а также представленными способами, изложенными в примерах. Примеры синтетических процедур, которые могут быть использованы для приготовления соединений по данному изобретению, проиллюстрированы на схемах реакций 1-3.
Схема реакций 1
Функциональная аминогруппа 4-аминобензоата а может конденсироваться с необязательно замещенным малоновым альдегидом, давая соответствующий 4-пиразол-1-илбензоат b. После взаимодействия последнего соединения с LAH, SOCl2 и NaCN с превращением его в пиразолофенилацетонитрильное соединение с, реакция с Na/этиловым эфиром карбоновой кислоты и гидразином приводит к бис-пиразолу d. Взаимодействие с соответственно замещенным сложным β-кетоэфиром дает пиразолопиримидин е, который реагирует с POCl3 с образованием хлорида f. Взаимодействие хлорида f с соответствующим металлоорганическим реагентом R2M в присутствии подходящего катализатора или промотора дает соединение g. Примеры подходящих металлоорганических реагентов и подходящих катализаторов/промоторов включают:
1. (замещенные)алкилреагенты Гриньяра R2MgX (Fe(acac)3промотор);
2. арил, гетероарил или алкенилбороновые кислоты или сложные эфиры (Pd(PhP)4 катализатор); и
3. арил или гетероарил цинксодержащие реагенты (Pd(PhP)4 катализатор).
R2 группы, введенные таким образом, затем могут быть подвержены превращению или взаимодействию при использовании стандартных способов, известных специалистам в данной области (например, окисление/восстановление, гидролиз и тому подобное), для обеспечения следующих примеров данного изобретения.
Схема реакций 2
Многостадийные синтетические пути к пиразолопиримидиновому ядру изобретения являются доступными. По схеме реакций 2 необязательно замещенный галогенбензальдегид h реагирует с тозилметилизоцианидом (TosMIC) с образованием фенилацетонитрила i. Взаимодействие i с NaH и EtOAc дает 3-гидроксибут-2-еннитрил j, который претерпевает замыкание цикла в реакции с гидразином HBr, образуя 3-амино-2-фенилпиразол k. Добавление сложного β-кетоэфира дает пиразоло[1,5-a]пиримидин-7-ол l. Замещение кислорода так же, как по схеме реакций 1, и замещение периферического брома на Het приводит к соединениям по данному изобретению.
Схема реакций 3
Взаимодействие замещенного ацетонитрила m с кетоном n, где R' представляет собой легко удаляемую группу, такую как алкокси, циано, или галоген, и где R'' представляет собой группу, такую как гидрокси или алкокси, дает цианокетон о, который реагирует с гидразином с образованием замещенного пиразола р. Взаимодействие р со сложным β-кетоэфиром q дает пиразолопиримидин r. Реакция с POCl3 приводит к хлориду s, и замещение хлорида на R2 дает соединение t.
Эффективность соединения как антагониста CRF-рецепторов может быть определена различными способами анализа. Подходящие CRF-антагонисты данного изобретения могут быть способны ингибировать специфическое связывание CRF с его рецептором и противодействовать эффектам, связанным с CRF. Соединение структуры (I) может быть оценено по активности в качестве CRF-антагониста одним или несколькими обычно принятыми для данной цели анализами, включающими (но без ограничения только ими) анализы, раскрытые в публикациях DeSouza et al. (J. Neuroscience 7:88, 1987) и Battaglia et al. (Synapse 1:572, 1987). Как упомянуто выше, подходящие CRF-антагонисты включают соединения, которые проявляют сродство к CRF-рецептору. Сродство к CRF-рецептору может быть определено исследованиями связывания, которые измеряют способность соединения ингибировать связывание меченного радиоактивным изотопом CRF (например, [125I]тирозин-CRF) с его рецептором (например, рецепторы, приготовленные из мембран церебрального кортекса крысы). Анализ радиолигандного связывания, описанный DeSouza et al. (см. выше, 1987), обеспечивает количественные данные для определения сродства соединения к CRF-рецептору. Такую активность обычно рассчитывают из IC50, как концентрации соединения, необходимой для замещения 50% меченного радиоактивным изотопом лиганда рецептора, и публикуют в виде “Ki” величины, вычисленной по следующему уравнению:
где L = радиолиганд и KD = cродство радиолиганда к рецептору (Cheng and Prussoff, Biochem. Pharmacol. 22:3099, 1973).
В дополнение к ингибированию связывания CRF-рецепторов активность соединения-антагониста CRF-рецепторов может быть установлена по способности соединения препятствовать активности, связанной с CRF. Например, известно, что CRF стимулируют различные биохимические процессы, включающие активность аденилатциклазы. Поэтому соединения могут быть оценены как CRF-антагонисты по их способности препятствовать СRF-стимулируемой активности аденилатциклазы, например, измерением уровней сАМР. Анализ по оценке СRF-стимулируемой активности аденилатциклазы, описанный Battaglia et al. (см. выше, 1987), обеспечивает количественные данные для определения способности соединения препятствовать CRF-активности. Соответственно активность антагониста CRF-рецепторов может быть определена оценочной методикой, которая обычно включает первоначальное определение связывания (такое, которое описано DeSouza (см. выше, 1987)), сопровождаемое сАМР скрининговым протоколом (таким, как описан Battaglia (см. выше, 1987)).
Что касается сродства к связыванию CRF-рецепторов, то антагонисты CRF-рецепторов, предложенные в данном изобретении, характеризуются величиной Кi менее чем 10 мкМ. В предпочтительном варианте осуществления данного изобретения антагонист CRF-рецепторов имеет Ki менее чем 1 мкМ, и более предпочтительно менее чем 0,25 мкМ (т.е., 250 нМ). Как показано подробнее ниже, величины Кi могут быть оценены способами, данными в примере 27.
Антагонисты CRF-рецепторов, предложенные в данном изобретении, могут проявлять активность в CRF-рецепторном сайте и могут быть применены как терапевтические средства для лечения широкого спектра расстройств и заболеваний, включающих эндокринные, психические и неврологические расстройства или заболевания. Конкретнее, антагонисты CRF-рецепторов, предложенные в данном изобретении, могут быть применимы в лечении физиологических состояний или расстройств, возникающих от гиперсекреции CRF. Так как считается, что CRF является основным нейротрансмиттером, который активирует и координирует эндокринные, автономные и поведенческие реакции на стресс, то антагонисты CRF-рецепторов, предложенные в данном изобретении, могут быть применены для лечения нервно-психических расстройств. Нервно-психические расстройства, которые можно лечить антагонистами CRF-рецепторов, предложенными в данном изобретении, включают аффективные расстройства, такие как депрессия; нарушения, связанные с состояниями тревоги/страха, такие как генерализованное тревожное расстройство, паническое расстройство, обсессивно-компульсивное расстройство, атипичная агрессия, сердечно-сосудистые нарушения, такие как нестабильная стенокардия и реактивная гипертензия; расстройства питания, такие как анорексия невроза, булимия и сидром раздраженной толстой кишки. CRF-антагонисты могут быть также применимы в лечении подавления иммунной системы, вызванного стрессом, связанным с различными болезненными состояниями, а также внезапного приступа. Другие применения CRF-антагонистов данного изобретения включают лечение воспалительных состояний (таких как ревматоидный артрит, увеит, астма, воспалительное заболевание кишечника и воспалительная G.I. перистальтика), боли, болезни Кушинга, младенческих судорог, эпилепсии и других припадков как у младенцев, так и у взрослых, и злоупотребления различными веществами и абстиненции (включая алкоголизм).
В другом варианте осуществления изобретения раскрыты фармацевтические композиции, содержащие один или несколько антагонистов CRF-рецепторов. Для введения соединения данного изобретения могут быть приготовлены фармацевтические композиции. Фармацевтические композиции данного изобретения содержат антагонист CRF-рецепторов, предложенный в данном изобретении (т.е. соединение структуры (I)), и фармацевтически приемлемый носитель и/или разбавитель. Антагонист CRF-рецепторов присутствует в композиции в количестве, эффективном для лечения конкретного расстройства, т.е. в количестве, достаточном для достижения антагонистической активности для CRF-рецепторов, и предпочтительно с приемлемой токсичностью для пациента. Предпочтительно, фармацевтические композиции данного изобретения могут включать антагонист CRF-рецепторов в количестве от 0,1 мг до 250 мг на дозировку, зависящую от пути введения, и более предпочтительно от 1 мг до 60 мг. Соответствующие концентрации и дозировки могут быть легко определены специалистом в данной области.
Фармацевтически приемлемый носитель и/или разбавители известны специалистам в данной области. Для композиций, приготовленных как жидкие растворы, приемлемые носители и/или разбавители включают физиологический раствор и стерильную воду и могут необязательно включать антиоксиданты, буферы, бактериостатики и другие обычные добавки. Композиции также могут быть приготовлены в виде пилюль, капсул, гранул или таблеток, которые содержат, в дополнение к антагонисту CRF-рецепторов, разбавители, диспергаторы, поверхностно-активные вещества, связующие вещества и замасливатели. Специалист в данной области, кроме того, может приготовить антагонист CRF-рецепторов целесообразным способом и в соответствии с приемлемыми методиками, такими как методики, описанные в Remington's Pharmaceutical Sciences, Gennaro, Ed., Mack Publishing Co., Easton, PA 1990.
Кроме того, в охват данного изобретения также включены пролекарства. Пролекарства представляют собой любые ковалентно связанные носители, которые высвобождают соединение структуры (I) in vivo, если такое пролекарство введено пациенту. Пролекарства обычно готовят модификацией функциональных групп таким способом, чтобы модификация расщеплялась, либо рутинной манипуляцией, либо in vivo, с образованием исходного соединения.
Что касается стереоизомеров, то соединения структуры (I) могут иметь хиральные центры и могут существовать как рацематы, рацемические смеси и как индивидуальные энантиомеры или диастереомеры. Все такие изомерные формы включены в данное изобретение, в том числе их смеси. Кроме того, некоторые из кристаллических форм соединений структуры (I) могут существовать в альтернативной кристаллической, аморфной или полиморфной формах как полиморфные модификации, которые все включены в данное изобретение. Кроме того, некоторые из соединений структуры (I) также могут образовывать сольваты с водой или другими органическими растворителями. Такие сольваты также включены в охват данного изобретения.
В другом варианте осуществления данное изобретение относится к способу лечения различных расстройств и заболеваний, включающих эндокринные, психические и неврологические расстройства или заболевания. Такие способы включают введение соединения данного изобретения теплокровному животному в количестве, достаточном для лечения расстройства или заболевания. Такие способы включают системное введение антагониста CRF-рецепторов, предложенного в данном изобретении, предпочтительно в форме фармацевтической композиции. Использованное в данной работе системное введение включает пероральный и парентеральный способы введения. Для перорального введения подходящие фармацевтические композиции антагонистов CRF-рецепторов включают порошки, гранулы, пилюли, таблетки и капсулы, а также жидкости, сиропы, суспензии и эмульсии. Указанные композиции могут также включать корригенты, консерваторы, суспендирующие средства, загустители и эмульгаторы и другие фармацевтически приемлемые добавки. Для парентерального введения соединения данного изобретения могут быть приготовлены в виде водных растворов для инъекций, которые могут содержать, в дополнение к антагонисту CRF-рецепторов, буферы, антиоксиданты, бактериостатики и другие добавки, обычно используемые в таких растворах.
В другом варианте осуществления данное изобретение позволяет проводить диагностическую визуализацию определенных сайтов внутри организма применением радиоактивных или нерадиоактивных фармацевтических средств. Применение соединения данного изобретения может обеспечить физиологическую, функциональную или биологическую оценку пациента или обеспечить выявление болезни или патологии и оценку. Радиоактивные фармацевтические средства применяются в сцинтиграфии, позитронной эмиссионной томографии (РЕТ), компьютерной томографии (СТ) и однофотонной эмиссионной компьютерной томографии (ОЭКТ, SPECT). Для данных применений вводятся радиоизотопы таких элементов, как иод (I), включающий 123I (PET), 125I(SPECT) и 131I, технеций (Tc), включающий 99Тс (РЕТ), фосфор (Р), включающий 31Р и 32Р, хром (Cr), включающий 51Cr, углерод (С), включающий 11С, фтор (F), включающий 18F, таллий (Tl), включающий 201Tl, и подобные эмиттеры позитронного и ионизирующего излучения. Нерадиоактивные фармацевтические средства применяются в магнитно-резонансной томографии (МРТ, MRI), флюороскопии и ультразвуковой диагностике. Для данных применений вводятся изотопы таких элементов, как гадолиний (Gd), включающий 153Gd, железо (Fe), барий (Ba), марганец (Mn) и таллий (Tl). Такие частицы также применимы для идентификации присутствия конкретных целевых участков в смеси и для мечения молекул в смеси.
Как отмечено выше, введение соединения данного изобретения может быть использовано для лечения широкого спектра расстройств и заболеваний. В частности, соединения данного изобретения могут быть введены теплокровному животному для лечения депрессии, тревожного расстройства, панического расстройства, обсессивно-компульсивного расстройства, атипичной агрессии, нестабильной стенокардии, реактивной гипертензии, анорексии невроза, булимии, синдрома раздраженной толстой кишки, подавления иммунной системы, вызванного стрессом, удара, воспаления, боли, болезни Кушинга, младенческих судорог, эпилепсии и злоупотребления различными веществами или абстиненции.
Следующие примеры приведены для иллюстративных целей, а не для ограничения.
Примеры
Антагонисты CRF-рецепторов данного изобретения могут быть получены способами, раскрытыми в примерах от 1 до 26. Пример 27 представляет способ для определения сродства связывания с рецептором, и пример 28 раскрывает оценку скрининговых соединений данного изобретения по активности на CRF-стимулируемой аденилатциклазе.
Аналитический ВЭЖХ-МС (HPLC-MS) метод 1
Платформа: Agilent 1100 серии: оснащенные автопробоотборником, УФ-детектором (220 нМ и 254 нМ), МС детектором (APCI);
ВЭЖХ колонка: YMC ODS AQ, S-5, 5 мк, 2,0 x 50 мм картридж;
ВЭЖХ градиент: 1,0 мл/минута, от 10% ацетонитрила в воде до 90% ацетонитрила в воде в 2,5 минуты, поддерживание 90% в течение 1 минуты. И ацетонитрил, и вода содержит 0,025% TFA.
Аналитический ВЭЖХ-МС (HPLC-MS) метод 2
Платформа: Agilent 1100 серии: оснащенные автопробоотборником, УФ-детектором (220 нМ и 254 нМ), МС детектором (APCI);
ВЭЖХ колонка: Phenomenex Synergi-Max RP, 2,0 x 50 мм колонка;
ВЭЖХ градиент: 1,0 мл/минута, от 5% ацетонитрила в воде до 95% ацетонитрила в воде в 13,5 минут, поддерживание 95% в течение 2 минут. И ацетонитрил, и вода содержит 0,025% TFA.
Аналитический ВЭЖХ-МС (HPLC-MS) метод 3
Платформа: Agilent 1100 серии: оснащенные автопробоотборником, УФ-детектором (220 нМ и 254 нМ), МС-детектором (электрораспыление);
ВЭЖХ колонка: XТerra MS, C18, 5 мк, 3,0 x 250 мм колонка;
ВЭЖХ градиент: 1,0 мл/минута, от 10% ацетонитрила в воде до 90% ацетонитрила в воде в 46 минут, скачок до 99% ацетонитрила и поддерживание 99% ацетонитрила в течение 8,04 минуты. И ацетонитрил, и вода содержит 0,025% TFA.
Аналитический ВЭЖХ-МС (HPLC-MS) метод 4
Платформа: Agilent 1100 серии: снабженные автопробоотборником, УФ-детектором (220 нМ и 254 нМ), МС-детектором (APCI) и Berger FCM 1200 CO2 насосным модулем;
ВЭЖХ колонка: Berger Pyridine, PYR 60A, 6 мк, 4,6 x 150 мм колонка;
ВЭЖХ градиент: 4,0 мл/минута, 120 бар; от 10% метанола в надкритическом СО2 до 60% метанола в надкритическом СО2 в 1,67 минуты, поддерживание 60% в течение 1 минуты. Метанол содержит 1,5% воды. Регулируемое противодавление 140 бар.
Препаративная ВЭЖХ-МС
Платформа: Shimadzu HPLC, снабженный Gilson 215 авто-пробоотборником/коллектором фракций, УФ-детектором и РЕ Sciez API150EX масс-детектором;
ВЭЖХ колонка: ВНК ODS-O/B, 5 мк, 30 x 75 мм;
ВЭЖХ градиент: 35 мл/минута, от 10% а