Применение производных фталида
Иллюстрации
Показать всеИзобретение относится к химико-фармацевтической промышленности и касается производных фталида и их применения при получении сенсибилизаторов или средств реверсии противоопухолевых лекарственных средств. Производные фталида по настоящему изобретению могут преодолеть или ослабить полирезистентность к лекарственным средствам, усилить ингибирование роста, вызываемое химиотерапевтическими лекарственными средствами, в 5-30 раз и также существенно промотировать гибель опухолевых клеток, вызываемую лекарственными средствами. Указанные производные фталида значительно повышают чувствительность опухолевых клеток, вне зависимости от типа противоопухолевых средств. 4 н. и 6 з.п. ф-лы, 6 табл., 4 ил.
Реферат
Изобретение относится к применению производных фталида (РА). Мономеры и димеры таких производных могут усиливать чувствительность резистентных к лекарственному средству опухолевых клеток к химиотерапевтическому лекарственному средству.
Уровень техники
Полирезистентность (MDR) означает, что опухолевые клетки имеют перекрестную резистентность к различным противораковым лекарственным средствам с различной химической структурой, функцией и механизмом действия. Клиническое исследование показывает, что некоторые солидные опухоли, такие как рак толстой кишки, рак почек, гепатокарцинома, немелкоклеточный рак легких, глиома, саркома Капоши и рак предстательной железы, как правило, резистентны к лекарственным средствам, вероятно, даже в то время, когда они только диагностируются, и принадлежат, таким образом, к опухолям с внутренней MDR. В таких опухолевых клетках существуют, как правило, различные механизмы резистентности, совместно провоцирующие широкую резистентность к химиотерапевтическим лекарственным средствам. В то же время некоторые опухоли, такие как острый миелоидный лейкоз, острый лимфоцитарный лейкоз, множественная миелома, лимфома, рак молочной железы, рак яичника и другие опухоли, как правило, чувствительны к химиотерапевтическим средствам в начальной стадии лечения, но постепенно в ходе лечения становятся резистентными к лекарственным средствам, в особенности, во время лечения рецидива, когда резистентность к лекарственным средствам существенно возрастает. Такой тип резистентности к лекарственным средствам называют приобретенной MDR. Терапевтический эффект может заметно снизиться после установления резистентности к лекарственным средствам. MDR приводит к слабому лечебному действию, плохому прогнозу и легкому рецидиву и метастазированию опухоли при обычных химиотерапиях. Примерно 90% случаев смерти среди онкобольных связаны с присущей или приобретенной резистентностью к лекарственным средствам.
Механизмы появления MDR широко исследовались. В целом выяснено, что MDR регулируется одновременно многими факторами и многими механизмами, включая, в основном, отток химиотерапевтических лекарственных средств за счет транспортных белков ABC, усиленную экспрессию антиапоптозных белков, изменение пути обмена веществ и типа регуляции и усиление системы детоксификации.
Поэтому на современном уровне технике срочно требуется химиотерапевтический сенсибилизатор с ощутимым действием.
Раскрытие изобретения
Целью настоящего изобретения являются химиотерапевтические сенсибилизаторы с ощутимой эффективностью и их применение при получении сенсибилизаторов или средств реверсии для противораковой химиотерапии. Указанные сенсибилизаторы представляют собой фталид или его производные формулы (I) (включая мономеры и димеры).
В первом аспекте настоящее изобретение относится к применению фталида или его производного формулы (I) при получении сенсибилизатора или средства реверсии противоопухолевых лекарственных средств.
В формуле (I)
R1 представляет собой водород, гидроксил, С1-С8алкил, C2-C8алкенил, С2-С8алкинил, С3-С8циклоалкил, С1-С8алкоксил, С1-С4карбоксил или галоген;
R2 представляет собой водород, гидроксил, С1-С8алкил, С2-С8алкенил, С2-С8алкинил, С3-С8циклоалкил, С1-С8алкоксил, С1-С4карбоксил или галоген, или R2 отсутствует;
R3 и R4 представляют собой независимо водород, гидроксил, С1-С8алкил, С2-С8алкенил, С2-С8алкинил, С3-С8циклоалкил, С1-С8алкоксил или галоген;
R5 и R8 представляют собой водород, гидроксил, С1-С8алкил, С2-С8алкенил, С2-С8алкинил, С3-С8циклоалкил, С1-С8алкоксил, С1-С4карбоксил, фенил, арил, аралкил, 5-6-членный гетероциклил, содержащий 1-2 атома азота, или галоген;
R6 и R7 представляют собой независимо водород, гидроксил, С1-С8алкил, С2-С8алкенил, С2-С8алкинил, С1-С4карбоксил или галоген; или R6 и R7 соединяются вместе с образованием 5-7-членного цикла;
где алкил, алкенил, алкинил, циклоалкил, алкоксил, фенил, арил, аралкил и гетероциклил замещены 0-3 заместителями, выбранными из группы, состоящей из С1-С3алкила, гидроксила и галогена.
В другом предпочтительном воплощении указанное производное является дигидропроизводным или тетрагидропроизводным фталида формулы (I) или димером фталида формулы (I), его дигидропроизводного или тетрагидропроизводного.
Предпочтительнее, структуру указанного фталида или его производного выбирают из числа
где в указанных формулах R1-R8 имеют значения, указанные выше.
В другом предпочтительном воплощении структуру указанного фталида или его производного выбирают из числа
Предпочтительно, указанные противоопухолевые лекарственные средства выбирают из числа адриамицина; винкристина; таксола, цисплатина; актиномицина; блеомицина; бусульфана; капецитабина; карбоплатина; кармустина; хлорамбуцила; циклофосфамида; цитарабина; даунорубицина; эпирубицина; этопла; вепезида; этопозида; флударабина; флуороурацила; гемцитабина; трастузумаба; гидроксикарбамида; идарубицина; ифосфамида; иринотекана; ломустина; мелфалана; меркаптопурина; метотрексата; митомицина; митоксантрона; дигидроксиантрахинонела; оксалиплатина; прокабазина; метилгидразина; мабтеры; стероида; стрептозоцина; доцетаксела; тиогуанина; тиотепы; ледертепы; теспамина; ралтитрекседа; топотекана; треосульфана; урацила; винбластина; винка алкалоида; виндезина; винорельбина; гливека; гидроксикамптотецина и их производных или смесей.
В другом предпочтительном воплощении указанные противоопухолевые лекарственные средства используют для лечении опухолей, выбранных из группы, состоящей из немелкоклеточного рака легких, рака предстательной железы, рака кишечника, гепатокарциномы, лейкоза, миеломы, лимфомы, рака молочной железы, рака яичника, рака желудка, рака пищевода, рака ободочной кишки или саркомы.
Во втором аспекте настоящее изобретение относится к фармацевтической композиции, которая содержит (а) эффективное количество фталида или его производного формулы (I), (b) безопасное и эффективное количество противоопухолевого лекарственного средства и (с) фармацевтически приемлемый носитель.
Предпочтительно указанное противоопухолевое лекарственное средство выбирают из группы, состоящей из адриамицина; винкристина; таксола; цисплатина; актиномицина; блеомицина; бусульфана; капецитабина; карбоплатина; кармустина; хлорамбуцила; циклофосфамида; цитарабина; даунорубицина; эпирубицина; этопла; вепезида; этопозида; флударабина; флуороурацила; гемцитабина; трастузумаба; гидроксикарбамида; идарубицина; ифосфамида; иринотекана; ломустина; мелфалана; меркаптопурина; метотрексата; митомицина; митоксантрона; дигидроксиантрахинонела; оксалиплатина; прокабазина; метилгидразина; мабтеры; стероида; стрептозоцина; доцетаксела; тиогуанина; тиотепы; ледертепы; теспамина; ралтитрекседа; топотекана; треосульфана; урацила; винбластина; винка алкалоида; виндезина; винорельбина; гливека; гидроксикамптотецина и их производных или смесей.
В третьем аспекте настоящее изобретение относится к применению фталида или его производного формулы (I) при получении композиции для преодоления сверхэкспрессии P-gp или Bcl-2 или сверхактивности глиоксилазы I.
В четвертом аспекте настоящее изобретение относится к способу лечения опухоли, включающему введение млекопитающему, нуждающемуся в таком лечении, безопасного и эффективного количества фталида или его производного формулы (I).
Предпочтительно, указанный способ также включает введение, по меньшей мере, одного из вышеперечисленных противоопухолевых лекарственных средств.
Описание чертежей
Фигура 1 показывает хроматограмму производных фталида.
Фигура 2 показывает результаты анализа методом вестерн-блоттинга экспрессии Bcl-2.
Фигура 3 показывает усиливающее действие производных РА на Adr-индуцированную гибель клеток среди клеток MCF-7/Adr.
Фигура 4 показывает потенциирующее действие производных РА в сочетании с Adr на индуцированный Adr апоптоз клеток MCF-7/Adr, измеренный FACS.
Осуществление изобретения
В результате широкого и интенсивного исследования авторы настоящего изобретения обнаружили, что фталид и его производные формулы (I) являются эффективными сенсибилизаторами противоопухолевых химиотерапевтических средств. На основании такого сенсибилизирующего действия фталид и его производные могут эффективно инвертировать полирезистентность опухолей к противоопухолевым лекарственным средствам. На этой основе осуществлено настоящее изобретение.
Термин "алкил", используемый в данном описании, относится к линейной или разветвленной насыщенной алифатической углеводородной группе, содержащей 1-8 (предпочтительно 1-6) атомов углерода. Указанный алкил может быть разветвленным, и его примерами являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, н-пентил, изопентил, трет-пентил, гексил и т.д. Термин "алкенил" относится к линейной или разветвленной углеводородной группе, содержащей, по меньшей мере, одну С-С двойную связь и 2-8 (предпочтительно 2-6) атомов углерода. Термин "алкинил" относится к линейной или разветвленной углеводородной группе, содержащей, по меньшей мере, одну С-С тройную связь и 2-8 (предпочтительно 2-6) атомов углерода.
Термин "арил", используемый в данном описании, относится к ароматической системе, которая может представлять собой одноядерный цикл или полиядерный арильный цикл, который уже конденсирован или объединен таким образом, что, по меньшей мере, часть конденсированных или связанных колец может образовывать сопряженную ароматическую систему. Арильная группа включает (но не ограничивается перечисленным) фенил, нафтил и тетралил.
Термин "циклоалкил", используемый в данном описании, относится к циклоалкильной группе с 3-8 атомами углерода, такой как циклопропил, циклопентил, циклогексил и циклогептил и т.д.
Термин "алкоксил" относится к алкоксилу с 1-8 атомами углерода, такому как метоксил, этоксил, пропоксил, бутоксил, пентилоксил, гексоксил и т.д.
Термин "гетероциклил" относится к устойчивому 4-7-членному (предпочтительно 5-6-членному) моноциклическому или полициклическому гетероциклилу. Указанный гетероциклил может являться насыщенным, частично ненасыщенным или ненасыщенным и состоит из атомов углерода и 1-4 гетероатомов, выбранных из числа атомов N, О и S. Атомы N и S могут быть окисленными. Гетероциклил также может включать любой полицикл, и любой гетероциклил из числа указанных выше может конденсироваться с арильным циклом.
"Замещенный арил" или "замещенный гетероциклил" означает арильную группу или гетероциклил, который замещен заместителем, выбранным из группы, состоящей из галогена, CN, ОН, NO2, амино, алкила, циклоалкильной группы, алкенила, алкинила, алкоксила, арилокси, замещенного алкоксила, алкилкарбонила, алкилкарбоксила, алкиламино или арилсульфонила. Предпочтительно, заместителем является галоген, С1-С4алкил, алкил или гидроксил.
Термин "галоген", используемый в данном описании, относится к элементу семейства галогенов и обозначает F, О, Br или I.
Активные ингредиенты
Активными ингредиентами по настоящему изобретению являются производные фталида формулы (I).
Термин "производное фталида", используемый в данном описании, относится к фталиду формулы (I), когда производное фталида мономер может содержать атом водорода, присоединенный к фенилу. Данный термин также включает димеры или полимеры (предпочтительно, димеры) фталида формулы (I) или их гидрированные продукты.
Термин "дигидропроизводное", используемый в данном описании, означает, что два атома водорода присоединяются к соседним атомам углерода, соответствующим двойной связи в фенильном цикле фталида. Термин "тетрагидропроизводное" означает, что четыре атома водорода присоединяются к соседним атомам углерода, соответствующим двойным связям в фенильном цикле. Например, соединение формулы (k)' является дигидропроизводным соединения формулы (k); и соединение формулы (k)” является тетрагидропроизводным соединения формулы (k).
Производные фталида по настоящему изобретению можно искусственно синтезировать или выделить из природного источника. Например, мономер и/или димер фталида формулы (I) можно выделить экстракцией из дудника или гирновника влагалищного (ligusticus wallichii franchet) из числа зонтичных растений.
Фармацевтическая композиция
Настоящее изобретение также относится к фармацевтической композиции, которая содержит производное фталида формулы (I) (мономер или димер) в качестве активного ингредиента и один или несколько фармацевтически приемлемых носителей или эксципиентов (таких как растворитель, разбавитель). Фармацевтически приемлемый носитель, который можно использовать в настоящем изобретении, включает обычные твердые и жидкие носители, до тех пор, пока они удовлетворяют свойствам активного ингредиента и желательному определенному способу введения. Например, твердые носители включают крахмал, лактозу, CaHPO4, микрокристаллическую целлюлозу и т.д., а жидкие носители включают стерильную воду, полиэтиленгликоль и т.д.
Фармацевтическую композицию по настоящему изобретению можно получить в различных обычных формах, таких как таблетка, капсула, диспергируемый порошок, гранула, суспензия, сироп (содержащий, например, примерно 10-50% сахара) и эликсир (содержащий примерно 20-50% этанола). Формой фармацевтической композиции также может являться стерильный раствор или суспензия для инъекции (примерно 0,05-5% суспендирующего агента в изотонической среде) для парентерального введения. Например, фармацевтическая композиция может содержать 0,01-99,9 мас.%, предпочтительно, 2,5-90 мас.%, предпочтительнее, 5-60 мас.%, активного ингредиента, смешанного с носителем.
В другом предпочтительном воплощении фармацевтическая композиция также содержит противоопухолевое лекарственное средство. Например, фармацевтическая композиция содержит (а) 0,01-99,9 мас.% (предпочтительно, 0,1-90 мас.%) мономера или димера производного фталида; (b) 0,01-99,9 мас.% (предпочтительно, 0,1-90 мас.%) противоопухолевого лекарственного средства; (с) фармацевтически приемлемый носитель. Как правило, массовое соотношение компонента (а) и компонента (b) составляет 1:100-100:1, предпочтительно 10:1-1:10.
Фармацевтическая композиция также может включать другие добавки, такие как пигмент, консервант и антиоксидант, и т.д.
Эффективная дозировка активного компонента может изменяться в зависимости от схемы введения и тяжести заболевания, от которого лечат. Однако эффект будет удовлетворительным, когда мономер или димер производного фталида вводят в дозировке примерно 0,05-500 мг/кг массы тела (предпочтительно, 0,1-100 мг/кг массы тела) в сутки. Предпочтительно, можно вводить в сутки 2-4 отдельные дозы или вводить в форме с постепенным высвобождением.
Способ лечения
Настоящее изобретение также относится к способу лечения, включающему стадию введения безопасного и эффективного количества мономера или димера производного фталида млекопитающему, нуждающемуся в таком лечении. Предпочтительно, указанный способ также включает стадию совместного введения других противоопухолевых лекарственных средств (таких как, например, противоопухолевое лекарственное средство в качестве субстрата для P-gp) или другие методы лечения (такие как химиотерапия).
Различные опухоли можно лечить введением мономера или димера производного фталида одного или в сочетании с другими средствами. Типичные примеры включают (но не ограничиваются перечисленным) немелкоклеточный рак легких, рак предстательной железы, рак кишечника, гепатокарциному, лейкоз, миелому, лимфому, рак молочной железы, рак яичника, рак желудка, рак пищевода, рак ободочной кишки, саркому и т.д.
Способ введения мономера или димера производного фталида не имеет особого ограничения. Их можно вводить перорально, внутривенно, внутримышечно, локально, внутриопухолево или подкожно и т.д. Предпочтительно, их вводят перорально, внутривенно или внутриопухолево.
Основные преимущества настоящего изобретения заключаются в следующем.
Все мономеры или димеры производных фталида по настоящему изобретению могут в широком интервале повышать чувствительность опухолевых клеток к противоопухолевым лекарственным средствам и реверсировать полирезистентность к лекарственным средствам (MDR), причем посредством этого эффективно усиливается способность противоопухолевых лекарственных средств убивать опухолевые клетки. Как показывают эксперименты, они обладают лучшим реверсивным действием, чем верапамил (VER, ингибитор P-gp), когда комбинируются с противоопухолевыми средствами, такими как адриамицин (Adr), для уничтожения опухолевых клеток, резистентных к лекарственным средствам. Когда их вводят с винкристином (VCR), таксолом или цисплантином (DDP), реверсивный эффект в 2-5 раз выше, чем у верапамила. Такие производные могут снизить резистентность опухолевых клеток к лекарствам в 5-30 раз и заметно усилить апоптоз опухолевых клеток, индуцируемый многими химиотерапевтическими лекарственными средствами.
Настоящее изобретение далее будет поясняться приведенными примерами. Следует иметь в виду, что эти примеры предназначены только для пояснения изобретения, а не для ограничения объема изобретения. В следующих примерах эксперименты, если не указано иное, проводят в общепринятых условиях или в условиях, указанных изготовителем.
Пример 1. Экстракция производных фталида из гирновника влагалищного и дудника
Сушат и измельчают 3 кг лекарственного сырья (гирновника влагалищного или дудника) и просеивают через сито 20 меш. Полученный порошок 3 раза экстрагируют двойным объемом (об./мас.) хлороформа. Хлороформ из вытяжки удаляют, и оставшийся раствор конденсируют до экстрактума (extractum). Затем экстрактум экстрагируют н-гексаном и метанолом. Метанольную фазу повторно пропускают через хроматографическую колонку с силикагелем G254, в качестве элюента используют н-гексан и ацетонитрил (в объемном соотношении от 9:1 до 5: 5), и получают соединения S1-S5, соответствующие пикам 8, 12, 7, 14, 3 на фигуре 1, соответственно. Повторно пропускают фазу н-гексана через хроматографическую колонку с силикагелем G254, с лигроином и этилацетатом (в соотношении от 9:1 до одного этилацетата) в качестве элюента, и получают соединения S6-S8, соответствующие пикам 16, 18, 17 на фигуре 1, соответственно. Каждый из таких мономеров растворяют в подходящей полярной жидкости и перекристаллизовывают путем перенасыщения при комнатной температуре 2-3 раза. Полученные кристаллические вещества идентифицируют ЯМР.
Соединения S1-S5 являются мономерами производных РА, а соединения S6-S8 являются димерами производных РА.
S1:
1Н-ЯМР (CDCl3) δ 4,96 (1H, дд, J=6,5, 4,0, Н-3), 2,45 (4Н, м, Н-4, Н-5) 5,88 (1H, дт, J=10,0, 3,5, Н-6), 6,16 (1Н, дт, J=10,0, 1,0, Н-7), 1,51 (1Н, м, Н-8а), 1,85 (1Н, м, Н-8b), 1,36 (4Н, м, Н-9, Н-10), 0,87 (3Н, т, J=7,5, Н-11).
S2:
1Н-ЯМР (CDCl3) δ 5,52 (1H, дд, J=8,0, 3,2, Н-3), 7,33 (1H, дд, J=7,5, 1,4, Н-5), 7,31 (1Н, т, J=7,5, Н-6), 7,10 (1H, дд, J=7,5, 1,4, Н-7), 2, 31, 1,73 (каждый 1Н, м, Н-8), 1,37 (4Н, м, Н-9, Н-10), 0,89 (3Н, т, J=7,l, Н-11), 9,59 (1H, с, 4-ОН).
13С-ЯМР (CDCl3) δ 171,2 (с, С-1), 80,9 (д, С-3), 136,1 (с, С-3а), 152,4 (с, С-4), 120,2 (д, С-5), 130,3 (д, С-6), 115,9 (д, С-7), 127,8 (с, С-7а), 32,3 (т, С-8), 26,9 (т, С-9), 22,4 (т, С-10), 13,9 (к, С-11).
S3:
1Н-ЯМР δ 2,59 (2Н, м, Н-4), 2,06, 2,14 (каждый 1H, м, Н-5), 4,33 (1 Н, ддд, J=5,5, 3,5, 2,5, Н-6), 4,61 (1Н, ушд, J=2,5, Н-7), 5,36 (1Н, т, J=8,0, Н-8), 2,38 (2Н, м, J=8,0, 7,5, Н-9), 1,58 (2Н, м, J=7,5, 7,5, Н-10), 0,96 (3Н, т, J=7,5, Н-11).
S4:
1Н-ЯМР (CDCl3) δ 2,47 (2Н, м, Н-4), 2,57 (2Н, т, J=13,5, Н-5), 5,96 (1Н, дт, J=9,5, 4,0, Н-6), 6,24 (1H, дт, J=9,5, 1,5, Н-7), 5,19 (1H, т, J=8,0, Н-8), 2,33 (2Н, к, J=7,5, Н-9), 1,47 (2Н, м, Н-10), 0,92 (3Н, т, J=7,5, Н-11).
S5:
1Н-ЯМР (CDCl3) δ 2,01, 1,91 (2H, м, Н-4); 1,92, 1,67 (2Н, м, Н-5); 3,46 (1H, к, Н-5); 3,77 (1H, д, Н-7); 5,13 (1Н, т, Н-8); 1,96 (2Н, м, Н-9); 1,37 (2Н, м, Н-10); 0,96 (3Н, т, Н-11); 2,0 (1H, м, 6-ОН,7-ОН).
S6:
1Н-ЯМР (CDCl3) δ 2,02, 2,08 (каждый 1Н, м, Н-4), 1,54, 1,91 (каждый 1H, м, Н-5), 2,55 (1Н, т, J=7,8, Н-6), 3,25 (1Н, д, J=8,9, Н-7), 5,7 (1Н, т, J=7,8, Н-8), 2,29 (2Н, к, J=7,3, Н-9), 1,46 (2Н, м, Н-10), 0,93 (3Н, т, J=7,3, Н-11), 1,4, 2,03 (1Н, м, Н-4'), 1,30, 1,88 (1Н, м, Н-5'), 2,99 (2Н, м, Н-6'), 7,36 (1Н, д, J=6,6, Н-7'), 5,0 (1Н, т, J=7,6, Н-8'), 2,18 (2Н, м, Н-9'), 1,45 (2Н, м, Н-9'), 0,92 (3Н, т, J=7,3).
13С-ЯМР (CDCl3) δ 168,4 (С-1), 148,1 (С-3), 155,0 (С-3а), 19,8 (С-4), 29,0 (С-5), 38,4 (С-6), 41,6 (а, С-7), 126,6 (С-7а), 112,1 (С-8), 28,0 (С-9), 22,3 (С-10), 13,9 (b, С-11), 164,9 (С-1'), 150,5 (С-3'), 47,6 (С-3'а), 31,1 (С-4'), 25,8 (С-5'), 41,5 (а, С-6'), 142,0 (С-7'), 134,3 (С-7'а), 108,8 (С-8'), 27,5 (С-9'), 22,3 (С-10'), 13,8 (b, С-11').
S7:
1Н-ЯМР (CDCl3) δ 2,02, 2,57 (каждый 1H, м, Н-4), 2,02, 2,17 (каждый 1H, м, Н-5), 2,55 (1H, м, Н-6), 3,47 (1Н, д, J=7,3, Н-7), 5,21 (1Н, т, J=7,8, Н-8), 2,33 (2Н, м, Н-9), 1,50 (2Н, м, Н-10), 0,95 (3Н, т, J=7,6, Н-11), 2,58, 2,74 (каждый 1H, м, Н-4'), 2,47, 2,75 (каждый 1Н, м, Н-5'), 5,93 (1Н, дт, J=9,6, 4,1, Н-6'), 6,17 (1H, дт, J=9,6, 1,8, Н-7'), 2,94 (1H, к, J=7,8, Н-8'), 1,45 (2Н, м, Н-9'), 1,14 (2Н, м, Н-10'), 0,87 (3Н, т, J=7,6, Н-11').
13С-ЯМР (CDCl3) δ 168,5 (С-1), 149,2 (С-3), 154,6 (С-3а), 19,6 (С-4), 26,2 (С-5), 35,0 (с, С-6), 44,0 (С-7), 122,3 (с, С-7а), 112,2 (С-8), 28,0 (С-9), 22,4 (С-10), 13,9 (С-11), 170,3 (С-1'), 92,0 (С-3'), 160,1 (С-3'а), 21,0 (с, С-4'), 20,7 (с, С-5'), 138,7 (С-6'), 117,0 (С-7'), 122,5 (d, C-7'a), 32,3 (с, С-8'), 20,0 (с, С-9'), 22,6 (С-10'), 14,1 (С-11').
S8:
1Н-ЯМР (CDCl3) δ 4,56 (1H, м, Н-3), 1,98, 2,08 (каждый 1Н, м, Н-4), 1,53, 1,90 (каждый 1Н, м, Н-5), 2,54 (1H, м, Н-6), 3,18 (1Н, д, J=8,9, Н-7), 1,38, 1,70 (каждый 1Н, м, Н-8), 1,26 (2Н, м, Н-9), 1,45 (2Н, м, Н-10), 0,93 (3Н, т, J=7,34, Н-11), 1,40, 2,03 (каждый 1H, м, Н-4'), 2,30, 1,87 (каждый 1Н, м, Н-5'), 2,97 (1Н, м, Н-6'), 7,33 (1Н, д, J=6,6, Н-7'), 4,98 (1Н, т, J=7,3), 2,18 (2Н, к, J=7,8, Н-9'), 1,44 (2Н, м, Н-10'), 0,93 (3Н, т, J=7,3, Н-11').
13С-ЯМР (CDCl3) δ 165,0 (C-1), 82,4 (С-3), 47,3 (С-3а), 30,9 (С-4), 25,7 (С-5), 41,6 (С-6), 141,9 (С-7), 134,5 (С-7а), 32,2 (С-8), 26,5 (С-9), 22,3 (С-10), 13,7 (С-11), 171,9 (С-1'), 150,5 (С-2'), 168,1 (С-3а), 22,4 (С-4'), 28,8 (С-5'), 38,3 (С-6'), 41,7 (С-7'), 127,1 (С-7а'), 108,6 (С-8'), 27,4 (С-9'), 22,2 (С-10'), 13,9 (С-11').
Мономеры или димеры производных PA S1-S8, полученные так, как описано выше, используют в последующих экспериментах. Соединения S1-S5 являются мономерами производных РА, а соединения S6-S8 являются димерами производных РА.
Пример 2. Определение резистентности клеточных линий к лекарственным средствам
Используют следующие клеточные линии: К562 (клеточная линия хронического миелоидного лейкоза человека) и K562/Adr (клеточная линия с резистентностью к таким химиотерапевтическим средствам, как адриамицин, вызванной длительным воздействием низкой дозировки адриамицина); KB (клеточная линия эпителия полости рта человека) и KBv200 (клеточная линия с резистентностью к таким химиотерапевтическим средствам, как винкристин, вызванной длительным воздействием низкой дозировки винкристина); MCF-7 (клеточная линия рака молочной железы человека) и MCF-7/Adr (клеточная линия с резистентностью к таким химиотерапевтическим средствам, как адриамицин, вызванной длительным воздействием низкой дозировки адриамицина). Все вышеуказанные клеточные линии покупают в Институте гематологии Китайской медицинской академии.
Полирезистентная к лекарственным средствам клеточная линия K562/Adr характеризируется, главным образом, сочетанием нескольких резистентных механизмов, включая повышенную экспрессию белков семейств P-gp и Bcl-2 и усиленную активность глиоксилазы I, и т.д. K562/Adr в 20 раз более резистентна к адриамицину, чем К562, и перекрестно резистентна к винкристину, дауномицину, митоксантрону, таксолу и т.д.
Полирезистентная к лекарственным средствам клеточная линия KBv200 также характеризируется, главным образом, сочетанием нескольких резистентных механизмов, включая повышенную экспрессию белков семейств P-gp и Bcl-2 и усиленную активность глиоксилазы I и т.д. KBv200 более чем в 100 раз резистентна к винкристину по сравнению с KB и перекрестно резистентна к винкристину, дауномицину, таксолу и т.д.
Подобным образом, полирезистентная к лекарственным средствам клеточная линия MCF-7/Adr также характеризируется, главным образом, сочетанием нескольких резистентных механизмов, включая повышенную экспрессию белков семейств P-gp и Bcl-2 и усиленную активность глиоксилазы I и т.д.
Полуингибирующую концентрацию (IC50) вычисляют с помощью программного обеспечения GraphPad Prism (San Diego, CA). Реакцию на лекарственное средство анализируют с помощью модели нелинейной регрессии Sigmoldal. Используют следующие реагенты и приборы.
Раствор мономера и димера РА: соединение растворяют в ДМСО для получения рабочего раствора 5 мг/мл, и затем для получения рабочего раствора используют среду RPMI 1640. Адриамицин (Adr), винкристин (VIN), таксол, цисплатин (DDP), RPMI 1640, МТТ, сыворотка плода коровы, культуральный планшет, медицинский инкубатор с диоксидом углерода, ферментометр, высокоэффективный жидкофазный хроматограф (ВЭЖХ), клеточный сортер с активацией флуоресценцией (FACS), набор антител UIU2 к P-gp флуоресценции (закупают у Immunotech A Coulter Company, Франция).
1. Экспрессия P-gp, определенная FACS
Клетки в логарифмической фазе роста собирают и два раза промывают PBS. Экспрессию P-gp определяют FACS согласно инструкции к набору UIU2 антител к P-gp флуоресценции. Подсчитывают 10000 клеток на образец.
Результаты
К562: положительная степень экспрессии P-gp составляет 0,22%; K562/Adr: положительная степень экспрессии P-gp составляет 83,6%.
KB: положительная степень экспрессии P-gp составляет 0,37%; KBv200: положительная степень экспрессии P-gp составляет 76,3%.
MCF-7: положительная степень экспрессии P-gp составляет 0,36%; MCF-7/Adr: положительная степень экспрессии P-gp составляет 83,4%.
Полученные результаты показывают, что основной механизм резистентности к лекарственному средству всех испытанных клеточных линий может быть связан с высокой экспрессией P-gp.
2. Измерение активности глиоксилазы I (GLO1)
Клетки замораживают-оттаивают с повторением в PBS, содержащем 1 мМ PMSF, разрушают ультразвуком, центрифугируют при 12000 20 минут, и затем собирают супернатант. Для определения GLO1 используют смесь 7,9 мМ MG, 1 мМ глутатиона, 14,6 мМ MgSO4 и 182 мМ имидазол-HCl (рН 7,0). Величину OD определяют при 240 нм. Результаты показаны в таблице 1.
| Таблица 1 | ||||||
| Клеточная линия | К562 | K562/Adr | KB | KBv200 | MCF-7 | MCF-7/Adr |
| Величина OD | 0,22 | 1,21 | 0,31 | 1,47 | 0,16 | 1,46 |
Результаты показывают, что один из механизмов резистентности к лекарственному средству испытанных клеточных линий связан с повышенной активностью GLO1.
3. Определение экспрессии Bcl-2
Клетки лизируют в растворе для лизиса клеток NP-40 и количественно анализируют ВСА. Белки разделяют в 1,2% геле для SDS-PAGE и переносят на целлюлозонитратные мембраны, когда гель в полусухом состоянии. Добавляют к мембранам первичные антитела (Sigma) против Bcl-2, и осуществляют визуализацию.
Результаты показаны на фигуре 2. Результаты показывают, что один из механизмов резистентности к лекарственному средству испытанных клеточных линий связан с высокой экспрессией Bcl-2.
2. Определение резистентности резистентных к лекарственным средствам клеточных линий к традиционным химиотерапевтическим средствам
Собирают клетки в логарифмической фазе роста и добавляют к среде RPMI-1640 (содержащей 10% сыворотки плода коровы), и получают клеточную суспензию. Затем клеточную суспензию высевают в 96-луночный планшет в количестве 100 мкл на лунку (1×104 клеток/лунку). Добавляют адриамицин, винкристин, таксол, цисплатин в разных концентрациях непосредственно в полусуспензионные клетки (К562 и K562/Adr). Адгезивные клетки культивируют в течение 24 часов после инокуляции, так что клетки могут полностью прилипнуть, и затем добавляют вышеуказанные средства в различных концентрациях. На каждый градиент концентрации приходится шесть параллельных повторных лунок. Среду добавляют в каждую лунку до конечного объема 200 мкл на лунку. Клетки культивируют в условиях 37°С, влажности насыщения и 5% СО2 в течение 68 часов. Добавляют 50 мкл МТТ (2 мг/мл) на лунку. Центрифугируют 96-луночный планшет, и удаляют супернатант. Затем добавляют 120 мкл ДМСО на лунку и обрабатывают вибрацией на виброустройстве. Величину OD измеряют при длине волны 590 нм с помощью ферментометра после того, как кристаллическое вещество полностью растворится.
Метод вычисления:
IC50=концентрация лекарственного средства, когда степень ингибирования составляет 50%.
Фактор резистентности к лекарственному средству (RF)=IC50 клеток, резистентных к лекарственному средству / IC50 чувствительных клеток.
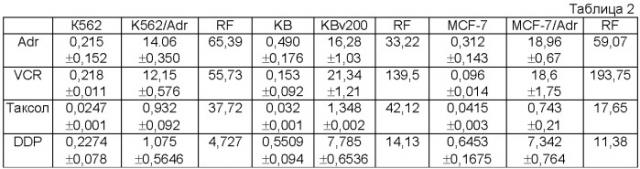
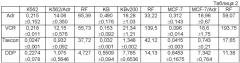
Результаты определения резистентности к лекарственному средству резистентных к лекарственным средствам клеточных линий в отношении традиционных химиотерапевтических средств показаны в таблице 2 (IC50: мкг/мл).
Результаты показывают, что все испытанные резистентные к лекарственным средствам клеточные линии имеют перекрестную резистентность к традиционным химиотерапевтическим средствам, т.е. полирезистентность.
Пример 3. Оценка цитологического действия производных РА - способность ингибировать рост клеточных линий, резистентных к лекарственным средствам
Методы. Инокулируют 1×103 клеток на 96-луночный планшет. К K562/Adr РА добавляют непосредственно, а к KBv200 и MCF-7/Adr после прилипания. Концентрации лекарственных средств составляют 0, 0,1, 0,5, 1,5, 10, 20, 40, 80, 160 мкг/мл. Определяют МТТ согласно методу в примере 2 и рассчитывают IC50. Эксперимент повторяют три раза.
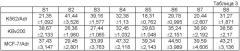
Результаты определения ингибирующего действия РА на рост клеток, резистентных к лекарственным средствам, показаны в таблице 3 (IC50 (мкг/мл)).
Результаты показывают, что производные РА при концентрации примерно 10 мкг/мл не имеют заметного цитотоксического действия.
Пример 4. Оценка цитологического действия производных РА - сенсибилизирующее действие на традиционные химиотерапевтические лекарственные средства
Собирают клетки в логарифмической фазе роста и добавляют к среде RPMI 1640 (содержащей 10% сыворотки плода коровы) для получения клеточной суспензии. Клеточную суспензию добавляют в 96-луночный планшет по 100 мкл на лунку, и число клеток на лунку составляет 2×103 (суспензионные клетки) или 1х103 (адгезивные клетки). После инокуляции перед добавлением лекарственных средств суспензионные клетки адаптируют в течение получаса на планшете, а адгезивные клетки культивируют до прилипания. В контрольные группы клеток (Ctrl) добавляют противоопухолевые средства, но без РА. Концентрация лекарственного средства каждой РА-группы составляет 10 мкг/мл. Концентрация химиотерапевтических средств возрастает от 0,001 мкг/мл до 20 мкг/мл. На каждый градиент концентрации приходится шесть параллельных повторных лунок. RPMI 1640 добавляют до конечного объема 200 мкл на лунку. Клетки культивируют в условиях 37°С, влажности насыщения и 5% СО2 в течение 68 часов. Определяют МТТ и вычисляют IC50 так, как в примере 4.
Формула фактора резистентности:
Фактор резистентности (RF)=IC50 без сенсибилизатора / IC50 с сенсибилизатором
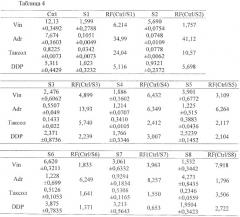
Результаты определения сенсибилизирующего действия РА (10 мкг/мл) на клетки K562/Adr показаны в таблице 4.
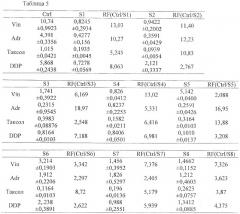
Результаты определения сенсибилизирующего действия РА (10 мкг/мл) на клетки KBv200 показаны в таблице 5.
Результаты определения сенсибилизирующего действия РА (10 мкг/мл) на клетки MCF-7/Adr показаны в таблице 6.
Пример 5. Оценка цитологического действия производных РА - сенсибилизирующее действие в случае гибели клеток, вызванной химиотерапевтическими лекарственными средствами
Инокуляцию клеток и индукцию лекарственных средств осуществляют так, как в примере 2. Через сорок восемь часов добавляют в каждую лунку 5 мкл трипанового синего (4 мг/мл). Через пять минут клетки проверяют под микроскопом. Подсчитывают пятьсот клеток на лунку. Клетки, окрашенные в синий цвет, являются мертвыми клетками. Вычисляют коэффициент выживаемости клеток.
Коэффициент выживаемости клеток (%)=[1-мертвые клетки (синие)/500]·100
Сенсибилизирующее действие производных РА в случае гибели клеток, вызванной адриамицином, показано в таблице 3. Концентрация каждого соединения S1-S8 составляет 10 мкг/мл. Концентрация Adr составляет 2,5 мкг/мл. S1+-S8+ представляет совместное использование S (10 мкг/мл) и Adr (2,5 мкг/мл). Результаты показывают, что производные РА могут заметно усилить гибель клеток, вызванную Adr.
Пример 6. Определение FACS сенсибилизирующего действия производных РА на апоптоз, вызванный химиотерапевтическими лекарственными средствами
Клетки MCF-7/Adr инокулируют на 6-луночный планшет (1×106 клеток/лунку). Клетки культивируют в течение 24 часов, и затем добавляют РА и химиотерапевтические лекарственные средства, как описано выше. Клетки культивируют еще в течение 72 часов. Клетки гидролизуют 0,25% тризином и собирают. Клеточной осадок фиксируют предварительно охлажденным 70% этанолом и хранят при температуре 4°С. Образцы промывают PBS 3 раза, гидролизуют РНКазой (1 г/мл) 15 минут, окрашивают иодидом пропидия (PI, 50 мг/л) в течение 30 минут, затем измеряют с помощью клеточного сортера с активацией флуоресценцией и вычисляют процент погибших клеток.
Результаты показаны на фигуре 4. Концентрация Adr составляет 2,5 мкг/мл. Концентрация РА составляет 10 мкг/мл. S1+-S8+ представляет совместное использование S (10 мкг/мл) и Adr (2,5 мкг/мл). Результаты показывают, что производные РА могут заметно сенсибилизировать гибель клеток, вызванную Adr.
Все документы, цитированные в данном описании, включены в него в качестве ссылок. Кроме того, следует иметь в виду, что в приведенные выше указания специалисты в данной области могут внести различные изменения или модификации по изобретению, но все такие эквивалентные формы входят в объем изобретения, определенный формулой изобретения, прилагаемой к заявке.
1. Применение фталида или его производного формулы (I) при получении сенсибилизатора или средства реверсии противоопухолевых лекарственных средств ,где R1 представляет собой водород, гидроксил, С1-С8 алкил, С2-С8 алкенил, С2-С8 алкинил, С3-С8 циклоалкил, С1-С8 алкоксил, С1-С4 карбоксил или галоген;R2 представляет собой водород, гидроксил, С1-С8 алкил, С2-С8 алкенил, С2-С8 алкинил, С3-С8 циклоалкил, С1-С8 алкоксил, С1-С4 карбоксил или галоген, или R2 отсутствует;R3 и R4 представляют собой независимо водород, гидроксил, С1-С8 алкил, С2-С8 алкенил, С2-С8 алкинил, С3-С8 циклоалкил, С1-С8 алкоксил или галоген;R5 и R8 представляют собой водород, гидроксил, С1-С8 алкил, С2-С8 алкенил, С2-С8 алкинил, С3-С8 циклоалкил, С1-С8 алкоксил, С1-С4 карбоксил, фенил, арил, аралкил, 5-6-членный гетероциклил, содержащий 1-2 атома азота, или галоген;R6 и R7 представляют собой независимо водород, гидроксил, С1-С8 алкил, С2-С8 алкенил, С2-С8 алкинил, С1-С4 карбоксил или галоген; или R6 и R7 соединяются вместе с образованием 5-7-членного цикла;где алкил, аленил, алкинил, циклоалкил, алкоксил, фенил, арил, аралкил и гетероциклил замещены 0-3 заместителями, выбранными из группы, состоящей из С1-С3 алкила, гидроксила и галогена.
2. Применение по п.1, где указанное производное являе