Нейротропное средство, обладающее антиоксидантной, противогипоксической, нейропротекторной, антиамнестической и противоукачивающей активностью и способностью улучшать когнитивные функции
Иллюстрации
Показать всеИзобретение описывает применение 2-этил-6-метил-3-оксипиридиния Н-ацетил-L-глутамината в качестве нейротропного средства с антиоксидантной, противогипоксической, нейропротекторной, антиамнестической и противоукачивающей активностью и способностью улучшать когнитивные функции. Технический результат: получена и соль 2-этил-6-метил-3-оксипиридиния, которая может найти свое применение в лечении острых и хронических нарушений мозгового кровообращения, в том числе ишемического и геморрагического инсульта и других заболеваний, сопровождающихся снижением когнитивных функций и нейродегенерацией. 17 табл.
Реферат
Изобретение относится к медицине, а именно к созданию нейротропного средства, обладающего антиоксидантной, противогипоксической, нейропротекторной, антиамнестической и противоукачивающей активностью и способностью улучшать когнитивные функции, предназначенного, в частности, для лечения острых и хронических нарушений мозгового кровообращения, в том числе ишемического и геморрагического инсульта и других состояний и заболеваний, сопровождающихся снижением когнитивных функций и нейродегенерацией, в том числе при старении.
Одной из актуальных проблем современной медицины является изыскание и разработка новых нейротропных средств, способных эффективно защищать мозг. Актуальность этого определяется, в частности, высокой летальностью при инсульте, а также тем, что применяемые при нем препараты разных фармакологических групп, как правило, не являются средствами патогенетической терапии, малоэффективны и имеют серьезные побочные эффекты [5, 6].
Ближайший аналог заявляемого средства (как по химическому строению, так и по фармакологическим свойствам) - отечественный лекарственный препарат мексидол (этилметилгидроксипиридина сукцинат: 2-этил-6-метил-3-оксипиридина сукцинат), который является производным 3-оксипиридина и обладает нейротропной, нейропротекторной и антиоксидантной активностью, из-за чего его широко используют в неврологии при острой и хронической недостаточности мозгового кровообращения и связанных с ней заболеваниях, в том числе при инсульте и его последствиях [3, 4, 11, 13]. Однако установлено, что в клинике и эксперименте мексидол не всегда эффективен при этой патологии. Например, мексидол давал положительный клинический эффект лишь у 63% больных, который преобладал у пациентов с дисциркуляторной энцефалопатией атеросклеротического генеза [12]. Более того, мексидол обладает недостаточной противогипоксической и ноотропной активностью.
Поэтому необходимо изыскание в ряду производных 3-оксипиридина новых веществ, имеющих широкий спектр фармакологического действия и способных более активно и эффективно, чем мексидол, действовать, в частности, на моделях инсульта в эксперименте.
В связи с изложенным задачей настоящего изобретения является создание нового нейротропного средства, обладающего антиоксидантной, противогипоксической, нейропротекторной, антиамнестической и противоукачивающей активностью и способностью улучшать когнитивные функции.
Поставленная цель достигается применением в качестве нового нейротропного средства 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) в эффективных количествах, имеющего выраженное нейропротекторное действие в сочетании с антиоксидантной, противогипоксической, антиамнестической, противоукачивающей активностью и способностью улучшать когнитивные функции.
Изобретение иллюстрируется следующими ниже примерами. При этом примеры 2-8 иллюстрируют эффективность ЭМОП-АГ в качестве антиоксиданта, противогипоксического, антиамнестического, противоукачивающего и улучшающего когнитивные функции средства в сравнении с ближайшим аналогом мексидолом, а также другими препаратами сравнения.
Пример 1. В трехгорлую колбу, снабженную мешалкой, термометром и холодильником, загружают 30 мл ацетонитрила, затем при перемешивании постепенно добавляют 1,0 г 2-этил-6-метил-3-оксипиридина и 1,38 г кислоты N-ацетил-L-глутаминовой. Реакционную массу нагревают до температуры кипения и выдерживают при перемешивании в течение 1 часа, после чего охлаждают до комнатной температуры, ацетонитрил декантируют, к остатку прибавляют 10 мл диэтилового эфира, тщательно перемешивают и кристаллизуют при температуре 10-15°С.
Получают - 2,1 г белого с кремоватым оттенком кристаллического порошка с Тпл. 95÷97°С, растворимого в воде, в спиртах.
Найдено, %: С 55,19; Н 6,77 N 8,62. C15H22N2O6
Вычислено, %: С 55,24; Н 6,74; N 8,59
ИК-спектр (ν, см-1): 3270 (NH), 2600 (N+), 1720 (C=O), 1600 (C=C, аром), 1560 (NHCO)
Пример 2. Антиоксидантная активность 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) в модельной системе многослойных липосом из липопротеинов желтка куриных яиц (табл.1)
Антиоксидантную (антиокислительную) активность ЭМОП-АГ и препаратов сравнения (отечественный препарат мексидол и эталонный антигипоксант амтизол) оценивали хемилюминесцентным методом в модельной системе многослойных липосом из липопротеинов желтка куриных яиц [2]. Регистрировали все стадии железоиндуцированной хемилюминесценции: быструю вспышку, латентный период и медленную вспышку.
В модельной системе многослойных липосом из липопротеинов желтка куриных яиц ЭМОП-АГ тормозил перекисное окисление липидов на всех стадиях железоиндуцированной хемилюминесценции: уменьшал интенсивность быстрой вспышки и скорость медленной вспышки, увеличивал латентный период. При этом по антиоксидантной активности ЭМОП-АГ превосходил мексидол почти в 2 раза, а также эталонный антигипоксант амтизол в 3 раза (табл.1).
При выполнении экспериментальной части работы (опыты на животных - примеры 3-8) в соответствии с Российскими национальными правилами исследований («Правила лабораторной практики в Российской Федерации»; приказ Минздрава России №267 от 19.06.2003; и др.) и международными требованиями были использованы модели и методы, рекомендованные Фармакологическим комитетом для проведения подобных исследований, утвержденные Министерством здравоохранения и социального развития РФ и соответствующие рекомендациям ВОЗ, касающихся правил надлежащей лабораторной практики (GLP - "Good Laboratory Practice") [10]. Животных получали из Центрального питомника лабораторных животных РАМН («Столбовая», Московская область). Содержание животных соответствовало правилам GLP и осуществлялось в соответствии с нормативным документом «Санитарные правила по устройству, оборудованию и содержанию вивариев», утвержденным Главным государственным санитарным врачом 06.04.1973 г. №1045-73, и приказом МЗ РФ №267 от 19.06.2003.
Пример 3. Противогипоксическое действие 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) на различных моделях острой гипоксии у мышей (табл.2-6)
Исследования выполнены на белых нелинейных мышах-самцах массой 20-28 г по методикам, описанным в «Методических рекомендациях по экспериментальному изучению препаратов, предлагаемых для клинического изучения в качестве антигипоксических средств» [7] и «Руководстве по экспериментальному (доклиническому) изучению новых фармакологических веществ» [10].
Острую нормобарическую гипоксическую гипоксию с гиперкапнией воспроизводили путем помещения мышей (поодиночке) в гермокамеру. Острую гипобарическую гипоксию моделировали у мышей в проточно-вытяжной барокамере; животных поднимали со скоростью 50 м/с до "высоты" 11000 м. Острую гемическую гипоксию воспроизводили путем подкожного (п/к) введения мышам метгемоглобинообразователя натрия нитрита в дозе 300 мг/кг. Острую гистотоксическую гипоксию моделировали путем п/к введения мышам натрия нитропруссида в дозе 20 мг/кг. Регистрировали продолжительность жизни животных. Исследуемые вещества вводили однократно внутрибрюшинно (в/б) за 30 (амтизол) или 60 минут (все остальные вещества) до опыта. Животным контрольных групп вводили в/б 0,9% раствор натрия хлорида (NaCl) в том же объеме.
На модели острой нормобарической гипоксической гипоксии с гиперкапнией (в гермокамере) ЭМОП-АГ в дозах 10 и 30 мг/кг значимо (р<0,05) увеличивал продолжительность жизни мышей на 25% и 30% соответственно, примерно также действовали мексидол (100 мг/кг - на 27%) и эталонный антигипоксант амтизол (30 мг/кг - на 28%) (табл.2).
На модели острой гипобарической гипоксии ЭМОП-АГ в дозах 10 и 30 мг/кг значимо (р<0,05) увеличивал продолжительность жизни мышей на 90% и 121% соответственно, превосходя в дозе 10 мг/кг эталонный антигипоксант амтизол (10 мг/кг, в 1,5 раза, р<0,05), а в дозе 30 мг/кг - мексидол (100 мг/кг, в 2,2 раза, р<0,05) (табл.3).
На модели острой гемической гипоксии ЭМОП-АГ в дозах 10 и 30 мг/кг значимо (р<0,05) увеличивал продолжительность жизни мышей на 26% и 29% соответственно, превосходя в дозе 10 мг/кг эталонный антигипоксант амтизол (10 мг/кг, в 1,2 раза, р<0,05), а в дозе 30 мг/кг - мексидол (100 мг/кг, в 1,2 раза, р<0,05) (табл.4).
На модели острой гистотоксической гипоксии ЭМОП-АГ в дозах 10 и 30 мг/кг значимо (р<0,05) увеличивал продолжительность жизни мышей на 25% и 33% соответственно, превосходя в дозе 10 мг/кг эталонный антигипоксант амтизол (10 мг/кг, в 1,1 раза, р<0,05), а в дозе 30 мг/кг - мексидол (100 мг/кг, в 1,3 раза, р<0,05) (табл.5).
Итак, на разных моделях острой гипоксии ЭМОП-АГ при однократном введении превосходит и/или не уступает эталонному антигипоксанту амтизолу и мексидолу.
Также оценивали противогипоксическое действие ЭМОП-АГ при курсовом введении на модели острой гипобарической гипоксии. Острую гипобарическую гипоксию моделировали у мышей в проточно-вытяжной барокамере; животных поднимали со скоростью 20 м/с до высоты 11000 м. Экспозиция составляла 10 минут, затем в течение 5 минут животных "спускали" до исходных условий. В течение всей экспозиции оценивали состояние и поведение мышей, регистрировали продолжительность жизни животных и количество выживших мышей. ЭМОП-АГ вводили в/б в дозах 5, 10, 20 мг/кг ежедневно в течение 5 суток (сут) в 10 часов утра, последний раз введение осуществляли за 40 минут до опыта. Препарат сравнения мексидол вводили в/б в дозах 150 и 250 мг/кг ежедневно в течение 5 сут в 10 часов утра (последний раз - за 40 минут до опыта). Контрольным животным в течение 5 сут вводили в/б 0,9% раствор NaCl в эквивалентном объеме.
Обнаружено, что ЭМОП-АГ после курсового применения в дозе 10 мг/кг/сут (в течение 5 сут) достоверно (р<0,05) увеличивал продолжительность жизни мышей в условиях острой гипобарической гипоксии в 1,6 раза, а в дозе 20 мг/кг/сут - в 2,3 раза по сравнению с контролем (табл.6). Мексидол оказывал значимое (р<0,05) противогипоксическое действие только в дозе 250 мг/кг, увеличивая продолжительность жизни животных в 1,6 раза. По выраженности действия мексидол в дозе 250 мг/кг/сут уступал ЭМОП-АГ в дозе 20 мг/кг.
После 10-минутного нахождения мышей в барокамере на критической «высоте» 11000 м в контроле погибли все животные (100%). ЭМОП-АГ в дозе 10 мг/кг/сут достоверно (р<0,05) увеличивал количество выживших мышей до 50% по сравнению с контролем, а в дозе 20 мг/кг/сут - до 67% (табл.6). Мексидол в дозе 250 мг/кг/сут также достоверно уменьшал процент гибели животных (до 50%, р<0,05), но по эффекту он уступал ЭМОП-АГ (табл.6).
В условиях острой гипобарической гипоксии у всех контрольных животных наблюдались двигательные нарушения. Так, например, уже на «высоте» 6800 м у мышей появлялся тремор, а в течение времени нахождения на «высоте» 11000 м у контрольных мышей выявлялись четкие эпизоды периодического тремора (средний показатель - 12 эпизодов).
У мышей, получавших ЭМОП-АГ в дозах 5, 10 и 20 мг/кг/сут, тремор появлялся однократно (только при подъеме - на «высоте» 10500 м и не наблюдался на «высоте» 11000 м). Мексидол (250 мг/кг/сут) уменьшал количество эпизодов тремора: на «высоте» 11000 м наблюдалось 4 эпизода. Следовательно, ЭМОП-АГ в отличие от мексидола практически полностью предупреждает возникновение тремора и других двигательных нарушений, возникающих в условиях острой гипобарической гипоксии.
Таким образом, ЭМОП-АГ при курсовом применении в дозах 10 и 20 мг/кг/сут (ежедневно в течение 5 сут) оказывает выраженное противогипоксическое действие при острой гипобарической гипоксии. При этом ЭМОП-АГ существенно увеличивает продолжительность жизни и выживаемость животных, предупреждает возникновение двигательных нарушений, возникающих при подъеме на «высоту», и улучшает общее состояние животных. ЭМОП-АГ значительно превосходит мексидол по противогипоксической активности, давая эффект в значительно (в 25 раз) меньших дозах: одинаковое по выраженности противогипоксическое действие достигается при курсовом введении ЭМОП-АГ в дозе 10 мг/кг/сут, а мексидола - в дозе 250 мг/кг/сут.
Пример 4. Нейропротекторное действие 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) (табл.7-8)
Исследования выполнены на белых нелинейных крысах-самцах массой 220-290 г, содержащихся в виварных условиях, у которых моделировали два вида инсульта - ишемический и геморрагический.
В I серии опытов исследовали нейропротекторное действие ЭМОП-АГ и препаратов сравнения у крыс (массой 220-290 г) с экспериментальной ишемией головного мозга. В качестве препаратов сравнения были выбраны мексидол и семакс, широко используемые сегодня в неврологии при лечении ишемического инсульта, а также эталонный антигипоксант амтизол. Ишемию головного мозга у крыс воспроизводили путем одномоментной перевязки (под эфирным наркозом) обеих общих сонных артерий. У ложнооперированных животных (контрольная группа №1) операция была ограничена этапом доступа к общим сонным артериям. В контрольной группе №2 крысы получали только 0,9% раствор NaCl. В подопытных группах животным вводили в/б различные вещества (ЭМОП-АГ и препараты сравнения) в разных дозах 1 раз в сутки (сут) в течение 7 сут; в первые сутки - через 1, 3 и 6 часов (ч) после операции. Животных после операции наблюдали в течение 2 недель с учетом выживаемости крыс. Неврологический дефицит у животных определяли (слепым методом) по шкале McGraw et al. [18] (в баллах) каждый час в течение 24 ч, а затем 1 раз в сутки. Тяжесть состояния определяли по сумме соответствующих баллов. У ложнооперированных животных неврологический дефицит отсутствовал.
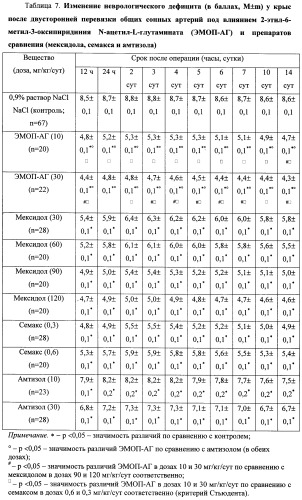
Результаты исследования нейропротекторного действия веществ представлены в табл.7. Из нее видно, что у крыс контрольной группы №2 неврологический дефицит был наиболее выражен (8,8±0,1 балла) через 2 и 3 сут после двусторонней перевязки общих сонных артерий; при этом в контроле погибло 24% (16 крыс из 67) животных.
Было обнаружено, что мексидол оказывает доза-зависимое нейропротекторное действие. Так, например, препарат уменьшал летальность крыс в дозах 30 и 60 мг/кг/сут до 14% и 10% (р>0,05) соответственно, в дозе 90 мг/кг/сут - до 5% (р<0,05), а в дозе 120 мг/кг/сут - даже до 0% (р<0,05). Сходные достоверные изменения происходили под влиянием мексидола и с неврологическим дефицитом.
Семакс оказал наиболее выраженное действие в дозе 0,3 мг/кг/сут: снижал летальность животных до 7% (р<0,05) и уменьшал неврологический дефицит. В более высокой дозе - 0,6 мг/кг/сут - эффект препарата был существенно слабее (летальность составляла 15%; р>0,05).
Амтизол в дозах 10 и 30 мг/кг/сут оказал незначительное благоприятное действие: незначимо (р>0,05) снижал летальность крыс до 22% и 18% соответственно и несколько уменьшал (р<0,05) неврологический дефицит.
Было установлено, что ЭМОП-АГ (в дозах 10 и 30 мг/кг/сут) оказывает выраженное нейропротекторное действие, превосходя по выраженности действия в отношении неврологического дефицита эталонный антигипоксант амтизол (10 и 30 мг/кг/сут), а также другие препараты сравнения (мексидол и семакс) (табл.7). При этом эффект ЭМОП-АГ в дозе 10 мг/кг/сут соответствовал таковому мексидола в дозе 90 мг/кг/сут, а в дозе 30 мг/кг/сут - мексидола в дозе 120 мг/кг/сут. ЭМОП-АГ также превосходил и семакс в дозах 0,3 и 0,6 мг/кг/сут. Уровень летальности при использовании ЭМОП-АГ в дозе 30 мг/кг/сут был достоверно (р<0,05) ниже на 18% по сравнению с амтизолом в аналогичной дозе. Более того, в большинстве сроков наблюдения ЭМОП-АГ по уменьшению неврологического дефицита значимо превосходил мексидол в указанных дозах.
Итак, можно заключить, что наиболее выражено действуют ЭМОП-АГ (30 мг/кг/сут), мексидол (120 мг/кг/сут) и семакс (0,3 мг/кг/сут). При этом ЭМОП-АГ по влиянию на неврологический дефицит значимо превосходит указанные препараты в большинстве случаев наблюдения.
Во II серии опытов у крыс (массой 250-270 г) воспроизводили геморрагический инсульт (ГИ; интрацеребральная посттравматическая гематома). Моделирование локального кровоизлияния в головном мозге - создание ГИ с ишемией мозга (интрацеребральной посттравматической гематомы) проводили по известной методике [17].
Операцию на мозге крыс проводили под наркозом (400 мг/кг хлоралгидрата внутримышечно). У крыс, закрепленных в стереотаксисе, проводили трепанацию черепа, а затем осуществляли деструкцию мозговой ткани в области внутренней капсулы с последующим (через 2-3 минуты) введением в место повреждения крови, взятой из-под языка этого же животного (0,02-0,03 мл). Таким способом достигается локальный аутогеморрагический билатеральный инсульт в области внутренней капсулы (диаметр - 2 мм, глубина - 3 мм) без существенных повреждений вышерасположенных образований мозга, в том числе неокортекса.
Выживших животных с ГИ разделили на 3 группы: 1 - животные с ГИ; 2 - крысы с ГИ, которым вводили ЭМОП-АГ; 3 - животные с ГИ, которым вводили препарат сравнения мексидол. 4-ю группу составили ложнооперированные крысы (их наркотизировали, им проводили трепанацию черепа, но не осуществляли разрушения мозговой ткани), 5-ю группу - интактные животные.
ЭМОП-АГ вводили животным в дозе 20 мг/кг, а мексидол в дозе 150 мг/кг в/б. Схема их введения была следующей: первую инъекцию осуществляли через 2 ч после операции, потом еще 3 раза каждые 4 ч (всего 4 инъекции в первые сутки). Затем ЭМОП-АГ или мексидол вводили ежедневно (в 10 часов утра) однократно в течение 14 сут. Контрольным животным 1-й, 4-й и 5-й групп вводили в/б 0,9% раствор NaCl в эквивалентном объеме по схеме введения препаратов.
Нарушение состояния и поведения крыс в постинсультный период оценивали в течение 14 сут после операции. Для оценки нарушений у крыс с ГИ использовали традиционный комплекс методов. Неврологический дефицит определяли так, как описано выше; также оценивали координацию движений и способность препаратов повышать выживаемость животных.
Среди ложнооперированных крыс ни одна крыса не погибла. В группе контрольных животных с ГИ в течение первых суток погибло 30%, а через 14 сут - 70%.
ЭМОП-АГ (по 20 мг/кг/сут ежедневно в течение 14 сут) предупреждал гибель крыс с ГИ - через 14 сут после операции гибель наблюдалась только у 30% крыс, т.е. в 2,3 раза (р<0,05) меньше по сравнению с нелеченными животными. После курсового введения мексидола в дозе 150 мг/кг/сут гибель наблюдалась также у 30% животных (р<0,05).
При оценке неврологического дефицита у животных через 1 сут после операции было установлено, что у ложнооперированных крыс (без ГИ) легкие неврологические нарушения в виде вялости и замедленности движений наблюдаются у 10-20% животных. Тяжелых неврологических нарушений, проявляющихся в виде манежных движений, парезов/параличей конечностей, у ложнооперированных крыс отмечено не было. У интактных животных неврологических нарушений не выявили.
У контрольных крыс с ГИ через 1 сут после операции у всех (100%) животных были отмечены легкие неврологические нарушения. Тяжелые неврологические нарушения также были выявлены у большого числа животных: манежные движения - у 40%, парезы - у 40%, параличи конечностей - у 30% (р<0,05 по сравнению с ложнооперированными крысами).
ЭМОП-АГ после 4-кратного введения (по 20 мг/кг) при регистрации нарушений через 1 сут после операции на максимуме их выраженности достоверно уменьшал неврологический дефицит. Так, например, после применения ЭМОП-АГ легкие нарушения регистрировали лишь у 50% животных (в контроле у 100%, т.е. в 2 раза чаще, р<0,05). Наряду с этим ЭМОП-АГ значимо (р<0,05) уменьшал число крыс с тяжелыми неврологическими нарушениями: манежными движениями (наблюдали у 0%) и парезом/параличом 1-4 конечностей (у 10-20%).
Мексидол (по 150 мг/кг 4 раза) также значимо (р<0,05) ослаблял легкие неврологические нарушения, в частности вялость и замедленность движений (наблюдали у 60%), а также тяжелые неврологические нарушения в виде манежных движений (у 0%), пареза/паралича конечностей (у 10-20%). Однако по активности мексидол (доза 150 мг/кг) значительно уступает ЭМОП-АГ (доза 20 мг/кг).
Сходным образом в отношении неврологического дефицита действовали оба вещества и в другие сроки наблюдения. Следовательно, ЭМОП-АГ вызывает существенное уменьшение неврологического дефицита у крыс с ГИ в разные сроки наблюдения и по активности значительно превосходит мексидол.
Нарушение координации движений оценивали в тесте вращающегося стержня: крыс помещали на горизонтальный стержень диаметром 4 см, вращающийся со скоростью 3 оборота в минуту; неспособность животных удерживать равновесие на стержне в течение 2 минут рассматривалось как проявление нарушения координации движений [10].
Интактные животные не имели нарушений координации движений, а у ложнооперированных крыс нарушения наблюдали только у 10% (табл.8). У контрольных крыс с ГИ наблюдалось отчетливое нарушение координации движений: на 2-е сутки после операции нарушение координации движений выявили у 64% животных, на 3-й сутки - у 58%, на 7-е - у 50% и на 14-е - у 33% крыс (табл.8).
ЭМОП-АГ (по 20 мг/кг/сут в течение 14 сут) значимо (р:<0,05) восстанавливал нарушенную у крыс в результате ГИ координацию движений на 3-й и 7-е сутки после операции (табл.8). Мексидол (по 150 мг/кг/сут в течение 14 сут) достоверно не изменял этот показатель (табл.8). Следовательно, ЭМОП-АГ в отличие от мексидола обладает способностью восстанавливать нарушенную ГИ координацию движений.
Таким образом, у крыс с ГИ ЭМОП-АГ (по 20 мг/кг/сут в течение 14 сут) вызывает значительное уменьшение неврологического дефицита, улучшает координацию движений и в 2,3 раза уменьшает гибель животных. Препарат сравнения мексидол при аналогичном курсовом применении также уменьшает неврологический дефицит и летальность крыс, но в значительно более высокой дозе - 150 мг/кг/сут. Следовательно, ЭМОП-АГ значительно превосходит мексидол по нейропротекторной активности (по крайней мере в 7,5 раз) на модели ГИ.
Пример 5. Антиамнестическое действие 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) на различных моделях амнезии у мышей и крыс (табл.9-13)
Исследования выполнены на белых нелинейных мышах-самцах массой 20-28 г.Влияние ЭМОП-АГ и препаратов сравнения на процессы обучения и памяти у животных исследовали, используя условную реакцию пассивного избегания (УРПИ) электрокожного раздражения [1]. Выработку УРПИ у мышей производили на основе электрокожного подкрепления по методу Cumin et al. (1982) [16] с учетом рекомендаций Mondadori et al. (1990) [19]. Мышей подвергали воздействию электросудорожного шока (ЭСШ) (50 Гц, 50 мА, 0,3 с, транспиннеально) сразу после обучения УРПИ [10]. У животных контрольной группы вызывали псевдоЭСШ. Для воспроизведения модели скополаминовой амнезии м-холиноблокатор вводили мышам в/б в дозе 1 мг/кг сразу после обучения УРПИ [10]. Острую нормобарическую гипоксическую гипоксию с гиперкапнией воспроизводили путем помещения мышей (поодиночке) в гермокамеру. В качестве комплексного экстремального воздействия использовали плавание мышей в холодной воде (ПМХВ) с одновременным вращением колеса до изнеможения. Исследуемые вещества вводили однократно в/б за 30 (амтизол) или 60 минут (все остальные вещества) до обучения мышей. Животные контрольных групп получали (в/б) в том же объеме 0,9% раствор NaCl. Сохранность УРПИ проверяли через 24 ч после амнезирующего воздействия.
На модели амнезии, вызванной электросудорожным шоком, было обнаружено, что у мышей ЭМОП-АГ (30 мг/кг), препараты сравнения пирацетам (800 мг/кг) и мексидол (100 мг/кг), но не эталонный антигипоксант амтизол, полностью или почти полностью (мексидол, пирацетам) предупреждают развитие амнезии УРПИ (табл.9).
На модели скополаминовой амнезии было обнаружено, что у мышей ЭМОП-АГ (30 мг/кг), препараты сравнения пирацетам (800 мг/кг) и мексидол (100 мг/кг), но не эталонный антигипоксант амтизол, полностью предупреждают развитие амнезии УРПИ (табл.10).
На модели амнезии, вызванной острой нормобарической гипоксической гипоксии с гиперкапнией (в гермокамере), было обнаружено, что у мышей ЭМОП-АГ (30 мг/кг) препараты сравнения оксирацетам (100 мг/кг) и мексидол (100 мг/кг) практически полностью предупреждают развитие амнезии УРПИ (табл.11). Эталонный антигипоксант амтизол (30 мг/кг) был менее эффективным - ослаблял выраженность амнезии в 2 раза (р<0,05).
На модели амнезии, вызванной ПМХВ с одновременным вращением колеса до изнеможения, было обнаружено, что у мышей ЭМОП-АГ (30 мг/кг) препараты сравнения пирацетам (800 мг/кг) и мексидол (100 мг/кг), но не эталонный антигипоксант амтизол полностью предупреждают развитие амнезии УРПИ (табл.12).
Также исследовали антиамнестическую активность ЭМОП-АГ в тесте скополаминовой амнезии у крыс.
Исследование выполнено на белых нелинейных крысах самцах массой 250-270 г с использованием сертифицированной установки "Lafayette Instrument Co" (США). Установка представляет собой темную камеру размером 400×400×400 мм с электродным полом. Темная камера соединена через квадратную гильотинную дверцу размером 60×60 мм с навесной платформой размером 250×70 мм. Навесная платформа освещена лампой 60 Вт, расположенной на высоте 400 мм. Темная камера располагается на лабораторном столе, а платформа висит над полом на высоте 800 мм. Крысу сажали на ярко освещенную платформу хвостом к открытой гильотинной двери, ведущей в темную камеру. Вследствие норкового рефлекса после нахождения входа в темный отсек камеры крыса переходила в темный отсек. Регистрировали латентный период (ЛП) выполнения этого навыка. Затем крысу оставляли на 180 секунд (с) в темной камере с целью ее освоения, и животное почти все время проводило в темной камере. По истечении 180 с осуществляли обучение. С этой целью в момент, когда крыса находилась в темном отделении, отверстие закрывали и наносили животному неизбегаемое электроболевое раздражение через пол (5 ударов, сила обучающего тока 0,45 мА, длительность каждого импульса составляла 1 с, интервал между последовательными импульсами 2 с). После получения болевого раздражения (обучение) крыса выскакивала из темного отсека на освещенную платформу. Следовательно, животное было обучено тому, что в темной камере оно получает болевое раздражение и помнит об этом. Крысу снимали с платформы и помещали в обычную клетку. Тест на воспроизведение обученного проводили через 24 ч после обучения, для чего крысу опять сажали на платформу хвостом к отверстию и регистрировали ЛП захода животного в темное отделение, а также число животных (в течение 180 с), совсем не зашедших в опасный темный отсек и остававшихся на освещенной висячей платформе (крысы, хорошо помнящие ситуацию).
Амнезию вызывали посредством введения м-холиноблокатора скополамина, вызывающего холинергический дефицит. Скополамин (в/б 1,0 мг/кг) вводили за 30 минут до обучения. Исследуемые вещества вводили крысам однократно в/б в объеме 0,2 мл на 100 г массы за 40 минут до обучения. ЭМОП-АГ вводили в дозах 10, 20 и 30 мг/кг, а препарат сравнения мексидол - в дозах 50, 100 и 200 мг/кг.
При помещении на освещенную платформу крысы с коротким ЛП (в среднем по группам от 12 до 17 с) заходили в темную камеру. При воспроизведении рефлекса через 24 ч после обучения крысы без амнезии помнят обученное и при помещении их на освещенную платформу животные остаются там основное время эксперимента (177±13 с) и не заходят в темную опасную камеру, где они накануне получили болевое раздражение (обучение) (табл.13).
Скополамин достоверно укорачивал ЛП захода в темную камеру при воспроизведении (в 2,6 раза, р<0,001) и значимо (р<0,001) уменьшал число животных (с 85% до 20%), совсем не зашедших в темный отсек камеры, т.е. помнящих о нанесенном там накануне аверсивном стимуле (табл.13). Эти показатели характеризуют выраженную амнезию.
ЭМОП-АГ в дозе 10 мг/кг не оказывал достоверного влияния на амнезию, вызванную скополамином (табл.13). ЭМОП-АГ в дозе 20 мг/кг значимо (р<0,05) увеличивал ЛП (в 1,7 раза) захода в темный отсек при воспроизведении и число животных (в 3 раза), не зашедших в темный отсек камеры, т.е. помнящих о нанесенном аверсивном стимуле (табл.13). В дозе 30 мг/кг ЭМОП-АГ оказывал более выраженное антиамнестическое действие: наблюдалось значимое (р<0,05) увеличение ЛП (в 2 раза) захода в темную камеру при воспроизведении и процента животных (в 3,5 раза), не зашедших в темную камеру (табл.13). Эти данные свидетельствуют о выраженном достоверном антиамнестическом эффекте ЭМОП-АГ в дозах 20 и 30 мг/кг.
Мексидол в дозе 50 мг/кг увеличивал ЛП воспроизведения УРПИ в 1,3 раза по сравнению с контролем с амнезией (контроль 2), но недостоверно (табл.13). В дозе 100 мг/кг мексидол достоверно (р<0,05) увеличивал ЛП (в 2,1 раза) захода в темный отсек и число животных (в 3,5 раза), не зашедших в темный отсек камеры, т.е. помнящих о нанесенном аверсивном стимуле (табл.13). В дозе 200 мг/кг мексидол оказывал более выраженное антиамнестическое действие: наблюдалось достоверное (р<0,01) увеличение ЛП (в 2,2 раза) захода в темную камеру при воспроизведении и процента животных (в 4 раза), не зашедших в темную камеру (табл.13). Полученные данные свидетельствуют о выраженном антиамнестическом эффекте мексидола в дозах 100 и 200 мг/кг.
Таким образом, ЭМОП-АГ в дозах 20 и 30 мг/кг оказывает сходное антиамнестическое действие с мексидолом в дозах 100 и 200 мг/кг, что свидетельствует о том, что ЭМОП-АГ по крайней мере в 3 раза превосходит мексидол по активности в тесте скополаминовой амнезии у крыс.
Пример 6. Противоукачивающее действие 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) (табл.14).
Исследования выполнены на крысах-самцах линии Вистар массой 180-200 г.
Моделирование болезни движения (БД) у крыс производили в течение 90 минут на модифицированной установке ПАСА США [15], позволяющей вращать животных в двух перпендикулярных плоскостях с частотой 0,33 Гц. Выраженность БД у крыс оценивали по количеству потребляемой ими пищи за 2 ч после вращения [14].
Исследование противоукачивающих свойств ЭМОП-АГ у крыс показало наличие вестибулопротекторной активности в дозе 30 мг/кг. По выраженности противоукачивающего действия ЭМОП-АГ превосходил эталонный вестибулопротектор скополамин в 1,3 раза (р<0,05). Эталонный антигипоксант амтизол был неэффективен (табл.14).
Пример 7. Способность 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) улучшать когнитивные функции (табл.15-17)
Исследования выполнены на белых нелинейных крысах-самцах массой 250-270 г.
В I серии опытов исследовали влияние ЭМОП-АГ на обучение условному рефлексу пассивного избегания (УРПИ) крыс-недоучек с использованием сертифицированной установки "Lafayette Instrument Co" (США). Описание установки и методики обучения УРПИ приведено выше (см. пример 5). Следует подчеркнуть, что для получения крыс-недоучек сила обучающего тока составляла не 0,45 мА (это обычно требуется для получения хорошей степени обученности), а только 0,3 мА, т.е. обучение было нежестким.
Исследуемые вещества вводили крысам однократно в/б в объеме 0,2 мл на 100 г массы за 40 минут до обучения. ЭМОП-АГ вводили в дозах 20 и 30 мг/кг, а препарат сравнения мексидол - в дозах 100 и 200 мг/кг.
Установлено, что когда крысу впервые помещали на ярко освещенную платформу хвостом к открытой гильотинной двери, ведущей в темную камеру, она вследствие норкового рефлекса с коротким латентным периодом (ЛП) переходила в темный отсек. ЛП выполнения норкового рефлекса в различных контрольных группах колебался от 10 до 18 с. ЭМОП-АГ и мексидол не изменяли ЛП выполнения навыка захода в темную камеру. После этого осуществляли обучение УРПИ, для чего крыса получала в темной камере меньшее (0,3 мА), чем обычно (0,45 мА), болевое раздражение, чтобы получились крысы-недоучки. Контрольные животные-недоучки (контроль 2) при воспроизведении обученного через 24 ч после обучения плохо помнили о раздражении, полученном в темной камере, и заходили туда с гораздо меньшим ЛП (в 2,4 раза, р<0,05), чем хорошо обученные крысы (контроль 1) (табл.15).
ЭМОП-АГ достоверно (р<0,05) увеличивал ЛП воспроизведения УРПИ крысами-недоучками: в дозе 20 мг/кг - в 1,8 раза, а в дозе 30 мг/кг - в 2,2 раза по сравнению с контролем 2 крыс-недоучек (табл.15). Под влиянием ЭМОП-АГ также значительно увеличивалось количество животных, совсем не зашедших в темный отсек камеры: в дозе 20 мг/кг в темную камеру не зашло 30% крыс, в дозе 30 мг/кг - 60% (р<0,05) (табл.15).
Следовательно, ЭМОП-АГ улучшает процесс обучения УРПИ у крыс-недоучек, что выражается в значительном увеличении количества животных, совсем не зашедших в темную камеру, и в достоверном увеличении ЛП захода в темную камеру.
Мексидол в дозах 100 и 200 мг/кг также улучшал обучение крыс-недоучек УРПИ. Он значимо (р<0,05) в дозе 100 мг/кг увеличивал ЛП воспроизведения рефлекса в 2,2 раза, в дозе 200 мг/кг - в 2,4 раза, а также в последней дозе и число крыс (70%), совсем не зашедших в темную камеру (табл.15).
Таким образом, ЭМОП-АГ в дозах 20 и 30 мг/кг обладает способностью улучшать обучение крыс-недоучек и по выраженности это действие ЭМОП-АГ соответствует таковому мексидола в дозах 100 и 200 мг/кг.
Во II серии опытов исследовали влияние ЭМОП-АГ на нарушение когнитивных функций в результате геморрагического инсульта (ГИ). Для оценки нарушений когнитивных функций после операции использовали обучение УРПИ у крыс в установке "Lafayette Instrument Co" (США) так, как описано выше. Описание методики воспроизведения ГИ у крыс приведено выше - см. пример 4. Сила обучающего тока составляла 0,45 мА. Воспроизведение УРПИ осуществляли через 24 ч после обучения, а также через 3, 7 и 14 сут после операции. Испытанные вещества вводили так же, как в примере 4.
Установлено, что интактные и ложнооперированные крысы при помещении их на освещенную платформу быстро (с коротким ЛП) переходили в темную камеру, т.е. осуществляли норковый рефлекс. ГИ не нарушал выполнение природного норкового рефлекса: у контрольных крыс с ГИ было только несколько повышен ЛП выполнения норкового рефлекса. ЭМОП-АГ и мексидол также не изменяли выполнение норкового рефлекса, и ЛП его выполнения не отличался от показателей интактных и ложнооперированных животных.
Среди интактных и ложнооперированных крыс при воспроизведении УРПИ через 24 ч после обучения 70-80% животных помнили об ударе током и не заходили в опасную темную камеру.
У крыс с ГИ (контроль) через 24 ч, 3, 7 и 14 сут после операции память существенно нарушалась. У этих животных при оценке сохранности памятного следа резко уменьшалось количество крыс, помнящих обученное: через 1, 3, 7 и 14 сут только 17-25% животных совсем не зашли в темную камеру, т.е. помнили об ударе током, а у 75-83% крыс память была нарушена и поэтому они заходили в опасную темную камеру. У заходящих в темный отсек крыс достоверно (р<0,05) уменьшался ЛП воспроизведения УРПИ (табл.16-17).
ЭМОП-АГ (курсовое введение) восстанавливал нарушенную ГИ память. ЭМОП-АГ через на 1 и 3 сут после операции увеличивал ЛП выполнения УРПИ в 1,6 раза, но недостоверно (р>0,05). Через 7 и 14 сут отмечалось значимое (р<0,05) улучшение когнитивных функций, что характеризовалось существенным увеличением (в 2,6 и 3,3 раза соответственно) ЛП воспроизведения УРПИ (табл.16) и числа животных (в 3,9 раза), совсем не зашедших в опасную темную камеру (табл.17). Следовательно, действие ЭМОП-АГ на нарушенную ГИ память зависело от времени, прошедшего после операции, и от курса введения вещества. Наибольший эффект ЭМОП-АГ выявлялся после его курсового применения через 7 и 14 сут после операции.
Мексидол (курсовое введение) значимо (р<0,05) восстанавливал нарушенные ГИ когнитивные функции только через 14 сут после операции и не оказывал достоверного влияния на память через 1-7 сут (табл.16-17).
Таким образом, ЭМОП-АГ (курсовое введение) восстанавливает нарушенные ГИ когнитивные функции в тесте УРПИ через 7 и 14 сут после операции. По всем показателям оценки когнитивных функций ЭМОП-АГ превосходит мексидол. При этом ЭМОП-АГ имеет гораздо большую активность (по крайней мере в 7,5 раз выше), поскольку он вызывает эффект в дозе в 7,5 раз меньше дозы мексидола. Следовательно, ЭМОП-АГ превосходит мексидол как по способности восстанавливать нарушенные ГИ когнитивные функции, так и по активности.
Пример 8. Электрофизиологическое исследование действия 2-этил-6-метил-3-оксипиридиния N-ацетил-L-глутамината (ЭМОП-АГ) на переживающих срезах гиппокампа крыс
В настоящее время в качестве объекта нейрофармакологических исследований in vitro для расшифровки механизма действия веществ, влияющих на центральную нервную систему, часто используют переживающие поперечные срезы гиппокампа [центральная структура лимбической системы, участвующая в процессах памяти и обучения и др.], сохраняющие нормально функционирующие внутренние системы с