Способ диагностики эндогенной интоксикации
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к лабораторной диагностике, и может быть использовано для диагностики степени выраженности эндогенной интоксикации. Для осуществления способа каплю смешанной слюны высушивают и осуществляют анализ структуры полученной фации под микроскопом. О низкой степени выраженности эндогенной интоксикации судят по наличию темной пигментации в самом центре центральной зоны фации. О средней степени выраженности эндогенной интоксикации судят по наличию темной пигментации в виде кольца по краю центральной зоны фации. О высокой степени выраженности эндогенной интоксикации судят по наличию темной пигментации по всей центральной зоне фации. Способ прост и доступен в осуществлении. Использование способа позволяет определить степень выраженности эндогенной интоксикации и проводить динамическое наблюдение за уровнем интоксикации в процессе лечения без проведения инвазивных манипуляций. 4 ил., 3 табл.
Реферат
Изобретение относится к медицине, а именно к лабораторной диагностике, и может использоваться для диагностики интоксикации и степени ее выраженности.
Уровень техники
Эндогенная интоксикация представляет собой синдром, характеризующийся накоплением в тканях и биологических жидкостях организма избытка продуктов нормального или извращенного обмена веществ или клеточного реагирования - эндогенных токсических субстанций. Можно выделить несколько механизмов эндогенной интоксикации, включающие в себя избыточную продукцию эндогенных токсических продуктов, резорбцию токсических веществ, накопление продуктов перекисного окисления липидов и других медиаторов воспаления, прежде всего фактора некроза опухолей, транслокацию продуктов жизнедеятельности микроорганизмов и самих тел микробов, с последующими аутоиммунными процессами, и нарушение выделения эндогенных токсических продуктов из организма естественными органами детоксикации [2, 4, 8, 9].
Эндогенную интоксикацию рассматривают как один из универсальных механизмов патогенеза различных заболеваний, который включает выход в кровь из патологического очага токсических продуктов, их распространение по организму с током крови и воздействие на другие органы и ткани. Развитие патологических нарушений в организме при интоксикации зависит от баланса двух противоположно направленных процессов - скорости образования и выхода в кровь эндотоксинов, с одной стороны, и элиминации (детоксикации) этих веществ, осуществляемой защитными системами организма, с другой. Разработка методологии доказательной биохимической оценки тяжести состояния больных в развитии эндотоксикоза - одна из актуальных проблем современной медицины, клинической биохимии. [3]
Интоксикация развивается при многих заболеваниях, в частности, при патологии почек и печени, при онкологических заболеваниях [12, 13]. Эти болезни могут протекать как остро, так и хронически с ремиссиями и обострениями, поэтому возникает проблема оценки степени выраженности интоксикации, контроля состояния пациентов и оценки эффективности лечения. Известные методы биохимического исследования сыворотки крови (определение концентрации молекул средней массы (МСМ), продуктов перекисного окисления липидов, билирубина и т.д.) имеют ряд общих недостатков:
- необходимо брать кровь из вены, то есть производить инвазивную манипуляцию, которая кроме этого может быть затруднена в силу особенностей анатомического строения вен или возраста обследуемого;
- необходимость в специальной биохимической лаборатории, оснащенной сложным оборудованием и обеспеченной реактивами, что делает анализы дорогими и не всегда доступными как для лечебно-профилактических учреждений, так и для пациентов.
Эти недостатки ограничивают количество и частоту этих исследований.
Известен метод клиновидной дегидратации [14], который не требует сложного дорогого оборудования и реактивов. При исследовании сыворотки крови авторами метода обнаружены маркеры интоксикации - морщины и токсические бляшки, которые наблюдаются в фации сыворотки крови независимо от причины интоксикации. Так как для анализа нужно не более 0,1 мл сыворотки, то кровь можно брать из пальца.
Метод клиновидной дегидратации позволяет делать видимой молекулярную организацию биологических жидкостей путем перевода ее на макроуровень. После высыхания капли в стандартных условиях на твердой подложке количество солей увеличивается от периферии к центру, а количество органических веществ - от центра к периферии [14].
В плане исследования степени выраженности интоксикации интересна слюна как биологическая жидкость, которую можно забирать у пациента практически без ограничения количества и частоты. Забор слюны не связан с инвазивными манипуляциями и может осуществляться не только в стенах лечебно-профилактического учреждения, но и на дому. Известно, что кроме пищеварительной функции слюнные железы выполняют гомеостатическую и экскреторную функции. Со слюной могут выделяться желчные кислоты и билирубин, витамины, антибиотики, что указывает на экскреторную функцию слюнных желез [17], Комаровой Л.Г. и Алексеевой О.П. (2006) показано, что гематосаливарный барьер проницаем для пировиноградной кислоты, креатина, холестерина, арахидоновой кислоты и др. [5]. Г.Ф.Коротько (2006) считает, что гематосаливарный барьер не является препятствием для многих токсичных веществ (тяжелые металлы, алкоголь, наркотики, хлорорганические соединения и многие другие) [7].
В работе С.Н.Разумовой детально описаны маркеры, которые появляются в фации ротовой жидкости при различных заболеваниях ротовой полости [10]. С.Н.Шатохина и соавт. [16] указывают, что наличие темной пигментации по краю центральной зоны фации (ЦЗФ) смешанной слюны является маркером интоксикации. Е.В.Агаповой описана темная пигментация кристаллов ЦЗФ смешанной слюны при механической желтухе [1].
За прототип предлагаемого изобретения выбран способ диагностики эндогенной интоксикации и степени ее выраженности по содержанию МСМ в слюне. Для исследования берут надосадочную жидкость, полученную после отстаивания смешанной слюны, собранной в пробирку путем сплевывания [8].
Ход определения: надосадочную жидкость обрабатывают 15% раствором трихлоруксусной кислоты в соотношении 1:0,5. Тщательно перемешивают содержимое пробирок и через 5-7 минут центрифугируют 30 минут при 3000 об/мин. После этого супернатант разводят дистиллированной водой в соотношении 1:9. Затем измеряют оптическую плотность на спектрофотометре при длинах волн 244, 254, 264, 274, 284 и 294 нм.
После осаждения белков в супернатанте остаются молекулы, имеющие молекулярную массу ниже 10 кД, которым приписывают максимальные токсические свойства [86]. Наличие эндогенной интоксикации оценивают путем определения общего уровня молекул средней массы (ΣМСМ), их отдельных составляющих в смешанной слюне. При этом в общем спектре МСМ на длинах волн 244-254 нм выделялся катаболический пул, а 264-294 нм - анаболический.
Недостатком способа-прототипа является необходимость в специальной дорогостоящей аппаратуре (спектрофотометр, центрифуга).
Раскрытие изобретения
Техническим результатом изобретения является удешевление, доступность и простота диагностики эндогенной интоксикации и степени ее выраженности.
Технический результат в заявляемом способе диагностики эндогенной интоксикации по пункту 1, достигается тем, что, как и в способе-прототипе, осуществляют анализ содержания МСМ смешанной слюны. Новым в способе является то, что каплю смешанной слюны на предметном стекле предварительно высушивают, анализ структуры полученной фации осуществляют под микроскопом, а об эндогенной интоксикации судят по наличию и расположению различной степени пигментированного агломерата.
При этом: об отсутствии эндогенной интоксикации судят по отсутствию темной пигментации в центральной зоне фации; о низкой степени выраженности эндогенной интоксикации судят по наличию в самом центре центральной зоны фации пигментированного агломерата; о средней степени выраженности эндогенной интоксикации судят по наличию пигментированного кольца по краю центральной зоны фации; о высокой степени выраженности эндогенной интоксикации судят по наличию темной пигментации по всей центральной зоне фации. Необходимое оборудование:
1) предметные стекла,
2) пипеточный микродозатор,
3) световой микроскоп.
Заявляемый способ имеет основное преимущество в сравнении с прототипом - удешевление (не требуется специальной дорогостоящей аппаратуры и реактивов) и простота технического выполнения анализа.
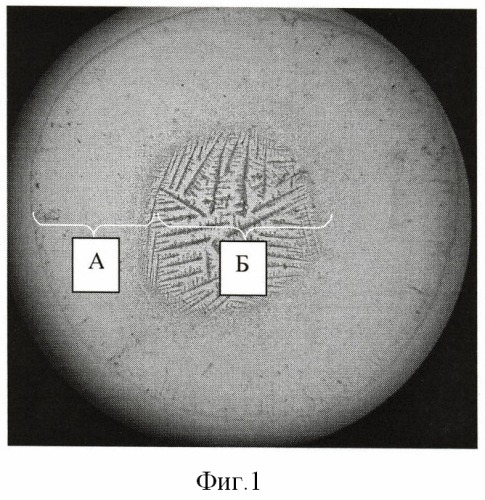
На фиг.1 - 4 представлены характерные фации смешанной слюны гастроэнтерологических обследованных больных. Морфологическая картина смешанной слюны имеет две зоны: аморфную периферическую (А) и центральную, заполненную кристаллами солей в виде дендритов (Б) (показано на фиг.1).
Детальный анализ фаций гастроэнтерологических больных показал, что имелись три варианта распределения темной пигментации в ЦЗФ слюны:
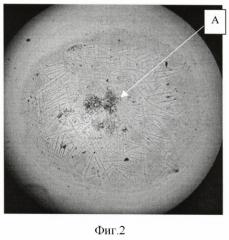
- темная пигментация была сосредоточена только в самом центре ЦЗФ (А на фиг.2),
- темное кольцо по краю ЦЗФ (А на фиг.3),
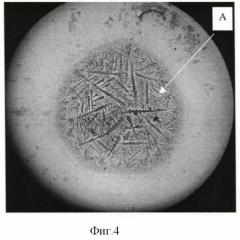
- темная пигментация наблюдалась по всей ЦЗФ (А на фиг.4).
Заявляемый способ осуществляют следующим образом. У обследуемых натощак после тщательного полоскания ротовой полости забирают смешанную слюну путем сплевывания в пробирку, затем ее отстаивают в холодильнике в течение суток. Каплю надосадочной жидкости - смешанной слюны предварительно высушивают на предметном стекле и затем анализируют структуру полученной фации под микроскопом, а об эндогенной интоксикации судят по наличию и расположению различной степени пигментированного агломерата.
При этом: об отсутствии эндогенной интоксикации судят по отсутствию темной пигментации в центральной зоне фации; о низкой степени выраженности эндогенной интоксикации судят по наличию в самом центре центральной зоны фации пигментированного агломерата; о средней степени выраженности эндогенной интоксикации судят по наличию пигментированного кольца по краю центральной зоны фации; о высокой степени выраженности эндогенной интоксикации судят по наличию темной пигментации по всей центральной зоне фации.
Необходимое оборудование: предметные стекла, пипеточный микродозатор, микроскоп с проходящим светом. Никакие реактивы не требуются. Способ дешев и прост в исполнении, не требует специального дорогостоящего оборудования и специально оборудованной лаборатории. Он может применяться для выявления эндогенной интоксикации, определения ее степени и для динамического наблюдения за уровнем интоксикации в процессе лечения.
Для доказательства достоверности заявляемого способа были обследованы 150 больных на базе гастроэнтерологического отделения Нижегородской городской клинической больницы №13, из них 62 мужчины и 88 женщины. Возраст больных был от 30 до 84 лет, медиана 54 года. У всех пациентов была диагностирована сочетанная гастроэнтерологическая патология (гастроэзофагеальная рефлюксная болезнь, хронический гатродуоденит, дисфункция сфинктера Одди, хронический запор). В качестве сопутствующих заболеваний у 53 человек (35,3%) были диагностированы сердечно-сосудистые заболевания (ишемическая болезнь сердца, артериальная гипертензия, хроническое нарушение кровообращения головного мозга), у 20 человек (13,3%) - заболевания печени (цирроз, жировой гепатоз), у 7 человек (4,7%) - хронические бронхолегочные заболевания (бронхиальная астма, хронический бронхит), у 6 человек (4%) - инсулиннезависимый сахарный диабет. Таким образом, у большей части обследованных пациентов наблюдались заболевания, которые могли быть причинами развития эндогенной интоксикации.
При поступлении в стационар и перед выпиской у них забирали кровь из вены и смешанную слюну. Методика сбора слюны: утром натощак до чистки зубов тщательно 2-3 раза прополоскать рот дистиллированной водой, далее сплюнуть 2-3 раза в раковину, после этого в течение 10 минут сплевывать в градуированную пробирку. Во время сбора слюны нужно дышать носом и не разговаривать. После этого собранную жидкость отстаивали в холодильнике в течение суток, в результате клеточные элементы оседали. Для исследования брали надосадочную жидкость.
Сыворотку крови и ротовую жидкость исследовали методом клиновидной дегидратации, а также определяли в них содержание молекул средней массы (МСМ). Дополнительно определяли концентрацию общего билирубина в сыворотке крови с помощью колориметрического фотометрического теста на анализаторе OLIMPUS ().
Статистическая обработка полученных результатов проводилась с использованием программ Microsoft Excel 2000 и Statistica 6.0. Так как большинство распределений в выборках отличались от нормального, то для описания выборок указывали число объектов исследования (n), минимальное и максимальное значения признака, медиану (значение, справа и слева от которого на оси значений признака располагаются равные количества значений признака данной выборки). Для выяснения различий между выборками применялись непараметрический критерий Вилкоксона для парных сравнений и U-критерий Манна-Уитни. Для анализа различий между несколькими выборками (больше двух) использовался метод ANOVA. Критический уровень значимости (р) при проверке статистических гипотез принимался равным 0,05. Во всех таблицах уровень значимости выделялся жирным шрифтом при условии, если р<0,05. Для исследования связи двух признаков использовали непараметрический метод Спирмена. Считалось, что линейная связь между признаками существует при коэффициенте корреляции r≥0,4, уровень значимости р<0,05 [11].
Морфологическая картина смешанной слюны у всех обследованных больных имела две зоны: аморфную периферическую (А) и центральную, заполненную кристаллами солей в виде дендритов (Б) (показано на фиг.1). Темная пигментация в ЗЦФ слюны до лечения была обнаружена у 93 больных. Детальный анализ распределения темной пигментации в ЦЗФ слюны гастроэнтерологических больных показал, что имелись три варианта:
- у 25 человек (27%) темная пигментация была сосредоточена только в самом центре ЦЗФ (А на фиг.2),
- у 50 человек (54%) в фации ротовой жидкости наблюдалось темное кольцо по краю ЦЗФ (А на фиг.3),
- у 18 человек (19%) темная пигментация наблюдалась по всей ЦЗФ (А на фиг.4).
После лечения значительно реже наблюдалась темная пигментация, расположенная по всей ЦЗФ и по краю ЦЗФ, а частота встречаемости проб слюны, в которых темная пигментация располагалась только в центре ЦЗФ или отсутствовала, статистически значимо увеличилась (табл.1).
| Таблица 1Частота встречаемости темной пигментации в центральной зоне фации смешанной слюны до и после лечения | ||
| Темная пигментация в ЦЗФ РЖ | До лечения | После лечения |
| По всей ЦЗФ* | 12% | 2% |
| По краю ЦЗФ* | 33% | 10,5% |
| В центре ЦЗФ* | 17% | 37% |
| Нет темной пигментации* | 38% | 50,5% |
| * - р<0,05 - критический уровень значимости |
Эти данные позволили предположить, что разное расположение темной пигментации в ЦЗФ РЖ зависит от степени выраженности интоксикации, и ввели следующие обозначения: 0 - нет темной пигментации, 1 - темная пигментация сосредоточена в самом центре ЦЗФ, 2 - темная пигментация в виде кольца по краю ЦЗФ, 3 - темная пигментация по всей ЦЗФ.
Как видно из таблицы 2, значения экстинкций сыворотки крови в диапазоне от 244 до 274 нм были выше нормы, что свидетельствует о наличии у обследованных больных эндогенной интоксикации. Особенно сильно были повышены уровни МСМ катаболического пула. Он включает продукты катаболизма белковых молекул и такие низкомолекулярные метаболиты, как мочевина, креатин, креатинин, мочевая кислота, продукты пуринового обмена и др., а также нуклеотиды и их производные - метаболиты обмена нуклеопротеидов [8]. Такое смещение основного максимума в сторону катаболической составляющей спектра МСМ характерно для четвертого варианта метаболического ответа организма на эндогенную интоксикацию по классификации Т.В.Копытовой [6]. Вариант может быть обозначен как «катаболический ответ по нуклеопротеидному типу».
Корреляционный анализ показал наличие статистически значимой положительной корреляции спектрограмм сыворотки крови и смешанной слюны по всему изучаемому спектру МСМ кроме 244 нм. Кроме этого, значения экстинкций на длинах волн 264 и 274 нм статистически значимо не отличались в сыворотке крови и смешанной слюне.
| Таблица 2Содержание МСМ в плазме крови и смешанной слюне до лечения и их корреляционные связи | ||||||
| МСМ, усл. ед. | ||||||
| 244 нм | 254 нм | 264 нм | 274 нм | 284 нм | 294 нм | |
| Сыворотка крови | 0,1-0,81, медиана 0,64* | 0,26-0,68, медиана 0,34* | 0,2-0,63, медиана 0,3* | 0,23-0,67, медиана 0,34* | 0,23-0,63, медиана 0,35 | 0,14-0,42, медиана 0,22 |
| Смешанная слюна | 0,18-2,2, медиана 1,02 | 0,07-0,96, медиана 0,49 | 0,06-0,73, медиана 0,32 | 0,05-0,67, медиана 0,31 | 0,05-0,57, медиана 0,26 | 0,04-0,41, медиана 0,2 |
| Отличия по критерию Вилкоксона | р=0,0004 | р=0,0006 | р=0,057 | р=0,08 | р=0,001 | р=0,01 |
| Корреляция | r=-0,03, р=0,8 | r=0,45, р=0,04 | r=0,69, р=0,002 | r=0,69, р=0,0005 | r=0,7, р=0,0005 | r=0,71, p=0,0003 |
| * - значения медианы выше нормы. |
Из этих данных можно заключить, что МСМ выводятся слюнными железами. Отличие значений экстинкции на длинах волн 244 и 254 нм (катаболический пул МСМ) можно объяснить патологическими процессами, происходящими в ротовой полости.
Корреляционный анализ связи выявил статистически значимые положительные связи степени выраженности темной пигментации в ЦЗФ (от 0 до 3) со всеми видами МСМ в смешанной слюне: 244 нм - r=0,63, 254 нм - r=0,56, 264 нм - r=0,53, 274 нм - r=0,46, 284 нм - r=0,46, 294 нм - r=0,46. Наибольшие коэффициенты корреляции наблюдались для катаболического пула МСМ. Во всех случаях р<0,05.
Сравнение значений экстинкции на разных длинах волн при различной морфологической картине смешанной слюны продемонстрировало в большинстве случаев статистически значимые отличия (табл.3).
Анализ таблиц показал, что впервые показаны положительные корреляции темной пигментации в ЦЗФ с содержанием МСМ в смешанной слюне, что позволяет проводить неинвазивную диагностику эндогенной интоксикации предлагаемым способом.
| Таблица 3Содержание МСМ в ротовой жидкости при различной морфологической картине ее фации | ||||||
| МСМ, усл. ед. | ||||||
| 244 нм | 254 нм | 264 нм | 274 нм | 284 нм | 294 нм | |
| Нет ТП (0) | 0,08-0,67, медиана 0,26 | 0,07-0,32, медиана 0,15 | 0,06-0,22, медиана 0,12 | 0,05-0,17, медиана 0,11 | 0,05-0,14, медиана 0,09 | 0,04-0,1, медиана 0,075 |
| ТП в самом центре ЦЗФ (1) | 0,66-1,35, медиана 0,94 | 0,33-0,84, медиана 0,44 | 0,17-0,53, медиана 0,28 | 0,13-0,44, медиана 0,26 | 0,09-0,36, медиана 0,24 | 0,05-0,28, медиана 0,16 |
| ТП по краю ЦЗФ (2) | 0,79-1,27, медиана 1,02 | 0,39-0,82, медиана 0,5 | 0,2-0,58, медиана 0,31 | 0,15-0,57, медиана 0,3 | 0,09-0,54, медиана 0,27 | 0,07-0,4, медиана 0,2 |
| ТП по всей ЦЗФ (3) | 0,78-2,2, медиана 1,31 | 0,39-0,96, медиана 0,74 | 0,22-0,73, медиана 0,53 | 0,15-0,67, медиана 0,38 | 0,11-0,57, медиана 0,31 | 0,08-0,42, медиана 0,22 |
| Сравнение по методу ANOVA | р=0,0002 | р=0,015 | р=0,046 | р=0,005 | р=0,005 | р=0,26 |
| ТП - темная пигментация |
В качестве иллюстрации работоспособности заявляемого способа неинвазивной диагностики эндогенной интоксикации приводим примеры, подтверждающие практическое применение данного способа.
Пример 1. Больной С., 65 лет, поступил в гастроэнтерологическое отделение с жалобами на боли и тяжесть в эпигастрии и правом подреберье постоянного характера, изжогу, отрыжку воздухом, горечь во рту, тошноту, вздутие живота, запоры (стул 2 раза в неделю).
В течение 10 лет неоднократно лечился по поводу хронического панкреатита, 5 лет назад впервые диагностирован цирроз печени токсического генеза. Ухудшение состояния в течение месяца после очередного злоупотребления алкоголем. Хронические запоры - в течение 15 лет.
При поступлении состояние средней степени тяжести. Сознание ясное. Иктеричность кожи и склер, пальмарная эритема. В легких рассеянные сухие хрипы, дыхание жестковатое. Тоны сердца ритмичные, приглушенные, ЧСС 96 уд/мин, АД 150/95 мм рт.ст. Живот несколько напряжен и болезнен при пальпации в верхней половине. Печень выступает из подреберья на 4-5 см, плотная, бугристая. Пальпируется увеличенная селезенка.
Результаты обследования: Показатели общего анализа крови: гемоглобин - 108 г/л, эритроциты - 3,6×1012/л, лейкоциты 9,2×109/л, СОЭ-26 мм/час, тромбоциты - 160×109/л. Биохимический анализ крови: АЛТ - 5N (в 5 раз выше нормы), ACT-8N, билирубин - 102 ммоль/л, щелочная фосфатаза - 4N, общий белок - 63 г/л.
ФГДС: Эрозивный рефлюкс-эзофагит. Варикозное расширение вен пищевода II степени, портальная гастропатия.
УЗИ: Печень увеличена (переднезадний размер 14,8 см), структура крупнозернистая, эхогенность снижена. Диаметр воротной вены 14 мм. Холедох 4 мм. Желчный пузырь 8,4×3,2 см, стенка уплотнена. Поджелудочная железа с неровными контурами, эхогенность повышена, размер головки 3,4 см. Селезенка 13×5 см.
Ректороманоскопия: Внутренний геморрой вне обострения.
Ирригоскопия: патологии не выявлено.
Исследование морфологической картины ротовой жидкости: узкая периферическая зона с сетью трехлучевых трещин и большим количеством кристаллических включений в виде зерен разных размеров, центральная зона с большим количеством мелких дендритов, частично разрушенных, с черной пигментацией по всей зоне. Заключение: эндогенная интоксикация высокой степени.
Клинический диагноз: Цирроз печени токсической этиологии, класс А по Чайльд-Пью с явлениями портальной гипертензии (варикозное расширение вен пищевода, спленомегалия) и начальными проявлениями печеночной недостаточности. Потральная гастропатия. Хронический рецидивирующий панкреатит в стадии умеренного обострения. ГЭРБ: эрозивный рефлюкс-эзофагит. Хронический функциональный запор. Артериальная гипертензия II, риск 2.
Проведенное лечение: внутрь омепразол 20 мг/сут, мезим 10000 ЕД×3 раза в сут, дицетел 50 мг×3 раза в сут, дюфалак 30 мл/сут; инъекции платифиллина, цефатаксима, эссенциале, реамберина, витаминов группы В.
Через 3 недели лечения боли в верхней половине живота и диспепсический синдром ликвидировались, уменьшилась желтуха, нормализовался стул. Улучшились биохимические показатели крови: АЛТ- 2N, ACT-2N, билирубин - 46 ммоль/л, щелочная фосфатаза - 3N, общий белок - 64 г/л.
По данным ФГДС эрозии в пищеводе эпителизировались.
Исследование морфологической картины ротовой жидкости: узкая периферическая зона с небольшим количеством кристаллических включений в виде мелких зерен, центральная зона с большим количеством мелких дендритов с черной пигментацией по краю зоны. Заключение: эндогенная интоксикация средней степени.
Пример 2. Больной И., 51 года, поступил в гастроэнтерологическое отделение с жалобами на изжогу, возникающую через час после приема пищи, воздушную отрыжку, болезненное прохождение пищи по пищеводу, чувство тяжести в эпигастрии после еды, запоры.
Болен в течение 10 лет. Периодически принимал антациды и обволакивающие препараты с хорошим положительным эффектом. В течение последнего полугода изжога стала упорной, появились боли по ходу пищевода во время еды.
При поступлении состояние удовлетворительное. Нормального питания. В легких дыхание везикулярное. Тоны сердца ритмичные, ЧСС-76 уд. в минуту. АД-110/70 мм рт.ст. Язык влажный, обложен у корня белым налетом. Живот мягкий, болезненный в эпигастрии и правом подреберье. Печень - по краю реберной дуги, безболезненная.
Проведенное обследование: Показатели общего и биохимического анализов крови - без отклонения от нормальных значений.
При рентгенологическом исследовании: пищевод свободно проходим для жидкого бария, эластичность стенок его сохранена. Кардия полностью не смыкается. Грыжа пищеводного отверстия диафрагмы. Гастроэзофагеальный рефлюкс. Признаки хронического гастродуоденита. Гипермоторная дискинезия луковицы двенадцатиперстной кишки.
ФГДС: Слизистая пищевода светло-розовая, в нижней трети отечная, белесоватая, рыхлая, с единичными рассеянными белесоватыми пятнами (очагами гликогенного акантоза) и сглаженным сосудистым рисунком. В нижней трети перед Z-линией (переходом пищеводного эпителия в желудочный) на слизистой имеются множественные дефекты слизистой, соединяющиеся между собой, распространяющиеся на 2 и более складок, занимающие менее 75% окружности пищевода. Кардия зияет. Диафрагмальный жом смещен дистальнее Z-линии на 2 см. Слизистая желудка умеренно гиперемирована, отечная. Луковица двенадцатиперстной кишки обычной формы. Слизистая бледно-розовая. Заключение: Эрозивный рефлюкс-эзофагит, степень С. Диафрагмальная грыжа. Хронический диффузный антральный гастрит с распространением на тело желудка. Тест на пилорический хеликобактер - положительный.
УЗИ органов брюшной полости: эхопризнаки хронического бескаменного холецистита. Диффузные структурные изменения печени и поджелудочной железы по типу жировой дистрофии.
ФКС: хронический геморрой вне обострения.
Исследование морфологической картины ротовой жидкости: узкая периферическая зона без трещин и кристаллических включений, центральная зона с большим количеством длинных тонких дендритов, с темной пигментацией по краю зоны. Заключение: эндогенная интоксикация средней степени.
Клинический диагноз: Гастроэзофагеальная рефлюксная болезнь: эрозивный рефлюкс-эзофагит. Грыжа пищеводного отверстия диафрагмы. Хронический гастродуоденит, ассоциированный с пилорическим хеликобактером. Хронический бескаменный холецистит. Стеатоз печени. Хронический функциональный запор.
Проведено лечение: внутрь омепразол 40 мг/сут, дицетел 150 мг/сут, маалокс 1 ст. ложка 3 раза в день, флемоксин 2,0 г/сут 10 дней, фромилид 1,0 г/сут 10 дней; инъекции церукала, витамины группы В.
В течение 10 дней лечения состояние больного улучшилось: ликвидировалась изжога, отрыжка, чувство тяжести в эпигастрии, нормализовался стул.
При контрольном эндоскопическом исследовании эрозии в пищеводе эпителизировались.
Исследование морфологической картины ротовой жидкости: широкая периферическая зона без трещин, с малым количеством кристаллических включений в виде мелких зерен, центральная зона с большим количеством длинных тонких дендритов и пигментированным агломератом в самом центре зоны. Заключение: эндогенная интоксикация низкой степени.
Заявляемое изобретение как обладающее простотой, дешевизной, доступностью, а также неинвазивностью может широко использоваться в медицине, в лабораторной диагностике и для диагностики интоксикации и степени ее выраженности. Он может применяться для выявления эндогенной интоксикации, определения ее степени и для динамического наблюдения за уровнем интоксикации в процессе лечения.
Источники информации
1. Агапова Е.В. Морфологическое и биохимическое исследование ротовой жидкости при заболеваниях пищеварительного тракта у лиц среднего и пожилого возраста. - Автореф. дис. к.м.н. - М.: 2007. - 24 с.
2. Дьяченко П.К., Желваков Н.М. Эндотоксикоз в хирургии // Вестник хирургии. - 1987. - №7. - С.129-135.
3. Иванова В.Н., Обедин А.Н., Первушин Ю.В., Бондарь Т.П., Марченко Л.А. Лабораторная оценка тяжести синдрома эндогенной интоксикации и выбор метода детоксикации у хирургических больных // Клиническая лабораторная диагностика. - 1999. - №11. - С.33.
4. Карпищенко А.И. Медицинская лабораторная диагностика (программы и алгоритмы). - СПб: Интермедика. - 1997. стр.246-265.
5. Комарова Л.Г., Алексеева О.П. Саливалогия. - Н.Новгород: Изд-во НижГМА, 2006. - 180 с.
6. Копытова Т.В. Механизмы эндогенной интоксикации и детоксикации организма в норме и при морфофункциональных изменениях в коже: Автореф. дис. д.б.н. - Н.Новгород, 2007. - 40 с.
7. Коротько Г.Ф. Секреция слюнных желез и элементы саливадиагностики. - М.: Издательский дом «Академия естествознания», 2006. - 192 с.
8. Малахова М.Я. Метод регистрации эндогенной интоксикации. Пособие для врачей. - СПб: СПбМАПО, 1995. - 33 с.
9. Оболенский С.В., Малахова М.Я., Ершов А.Л. Диагностика стадий эндогенной интоксикации и дифференцированное применение методов эфферентной терапии // Вестник хирургии. - 1991. - №3. - С.95-100.
10. Разумова С.Н. Диагностические и прогностические критерии стоматологической патологии по морфологической картине ротовой жидкости у пациентов разных возрастных групп: Автореф. дис. д.м.н. - М.: 2007. - 42 с.
11. Реброва О.Ю. Статистический анализ медицинских данных. Применение прикладных программ STATISTICA. - М.: МедиаСфера, 2002. - 312 с.
12. Саакян М.А. Биохимическая оценка опухолевых заболеваний толстой кишки, осложненной перитонитом. Клин. лаб. диагностика. 1992, 7-8, 43-45.
13. Салихова Н.Н., Ахмеджанов Р.И., Мухамадиева Ш.Г. Количественный метод определения среднемолекулярных пептидов в сыворотке крови больных с хронической почечной недостаточностью. Лаб. дело, 1989, 3, 48-52.
14. Шабалин В.Н., Шатохина С.Н. Аутогенные ритмы и самоорганизация биологических жидкостей // Бюллетень экспериментальной биологии и медицины. - 1996. - Т. 122, №10. - С.364-371.
15. Шабалин В.Н., Шатохина С.Н. Морфология биологических жидкостей человека. - М.: Хризостом, 2001. - 304 с.
16. Шатохина С.Н., Разумова С.Н., Шабалин В.Н. Морфологическая картина ротовой жидкости - диагностические возможности // Стоматология. - 2006. - №6.
17. Burgen A.S.V., Emmelin N.G. Salivary glands. - London, 1961.
Способ диагностики степени выраженности эндогенной интоксикации, отличающийся тем, что каплю смешанной слюны высушивают, осуществляют анализ структуры полученной фации под микроскопом, при этом о низкой степени выраженности эндогенной интоксикации судят по наличию темной пигментации в самом центре центральной зоны фации, о средней степени выраженности эндогенной интоксикации судят по наличию темной пигментации в виде кольца по краю центральной зоны фации, о высокой степени выраженности эндогенной интоксикации судят по наличию темной пигментации по всей центральной зоне фации.