Фармацевтическая композиция для лечения диспластических процессов шейки матки
Иллюстрации
Показать всеИзобретение относится к области медицины, фармацевтической промышленности и касается новых средств, используемых для лечения диспластических процессов шейки матки и слизистой прямой кишки. Лекарственное средство для лечения диспластических процессов шейки матки и слизистой прямой кишки в форме суппозитория, характеризующееся тем, что содержит 3,3'-дииндолилметан, эпигаллокатехин-3-галлат, а также катализатор ингибирующей активности эпигаллокатехин-3-галлата в отношении ДНК-метилтрансфераз, представляющий собой катионы Mg2+ в виде фармацевтически приемлемой соли магния, липофильную основу, содержащую твердый жир, поливинилпирролидон и бутилгидроксианизол и/или бутилгидрокситолуол. Средство оказывает эффективное действие при тяжелых формах диспластических поражений. 3 з.п. ф-лы, 3 ил., 2 табл.
Реферат
Изобретение относится к области медицины, фармацевтической промышленности и касается новых средств, используемых для лечения диспластических процессов шейки матки и слизистой прямой кишки.
Дисплазии шейки матки (ДШМ), или цервикальные интраэпителиальные неоплазии (CIN), относят к предраковым заболеваниям. Дисплазия - это атипия эпителия шейки матки с нарушением ее "слоистости", но без вовлечения в процесс поверхностного слоя и стромы. Для эпителиальных дисплазий характерно отклонение от нормы размножения, развития, дифференцировки клеток плоского многослойного эпителия, покрывающего шейку матки. Выделяют три основные формы дисплазий: легкую (CIN I), умеренную (CIN II) и тяжелую (CIN III).
К группе риска по ДШМ относятся женщины, имеющие в анамнезе:
1) раннее начало половой жизни (до 16 лет - эпителий шейки матки истончен и легко раним, что может привести к травмированию и развитию патологического процесса);
2) частая смена половых партнеров;
3) воспалительные заболевания и заболевания, передающиеся половым путем (ЗППП), наличие хронических вирусных инфекций генитального тракта (в частности, вирус герпеса второго типа);
4) травматизация во время абортов, родов, диагностических выскабливаний;
5) пристрастие к курению.
К патогенетическим факторам ДШМ относят наличие воспалительных процессов, нарушение баланса половых гормонов и перенесенные травмы шейки матки.
Однако главным фактором патогенеза ДШМ считается инфицирование вирусом папилломы человека (ВПЧ). ДНК ВПЧ высокой степени онкогенного риска (преимущественно 16 и 18 типов) обнаруживают в более чем 80% образцов умеренной и тяжелой дисплазии плоского эпителия шейки матки.
Папилломавирусная инфекция (ПВИ) является наиболее распространенным инфекционным заболеванием, передающимся половым путем. Согласно статистике более 50% сексуально активного населения в течение жизни инфицируется ВПЧ. Повышенный биологический и медицинский интерес к ПВИ объясняется тем, что она относится к опухолеродным инфекциям, способным вызвать доброкачественную гиперплазию, а некоторые типы ПВИ - инициировать развитие злокачественных опухолей аногенитальной области: рак шейки матки, вульвы, влагалища и пр. ДНК ВПЧ высокой степени онкогенного риска (преимущественно 16 и 18 типов) обнаруживают в 90% случаев инвазивного рака.
Рак шейки матки (РШМ) занимает второе место по распространенности среди злокачественных новообразований у женщин. Ежегодно в мире регистрируется около полумиллиона новых случаев данного заболевания и 270000 из них заканчивается смертельным исходом. Стандартизированный показатель заболеваемости и смертности от РШМ составляет 16,2 и 9 на 100000 населения соответственно. В России от РШМ (что составляет 4,8% от всех злокачественных заболеваний у женщин) ежегодно умирает более 6 тыс. больных (в возрастной категории от 20 до 40 лет РШМ является основной причиной смерти), показатель заболеваемости - приблизительно вдвое выше.
Не меньшей по значимости медицинской проблемой являются доброкачественные проявления ПВИ, к которым относятся экзофитные и эндофитные поражения различных участков эпителия вульвы, влагалища и шейки матки, а также окружающих кожных покровов и слизистых оболочек, включая анальное отверстие.
Экзофитные формы (генитальные кондиломы) включают в себя разнообразные по внешнему виду и размеру остроконечные, папиллярные и папулообразные образования, нередко осложняющиеся присоединением вторичной бактериальной инфекции и сопровождающиеся не только психологическими, но и физическими страданиями пациента. Частота генитальных кондилом (генитальных бородавок), являющихся следствием инфицирования доброкачественными ВПЧ-типами, по данным Минздрава РФ (2001 г.) составляет 26 на 100000 населения.
Эндофитные формы (субклиническая ПВИ) представляют собой различные морфологические изменения плоского эпителия без наружных разрастаний.
Генитальные кондиломы являются также причиной возвратного респираторного папилломатоза у детей, что обусловлено вертикальной трансмиссией вируса от инфицированной матери к ребенку.
Следует отметить, что в последние годы значительно увеличилось количество диагнозов рака прямой кишки, также обусловленного вирусами папилломы человека. Особенное распространение этот вид патологии получил среди мужчин с нетрадиционной сексуальной ориентацией. В большинстве случаев онкологической патологии предшествует образование кондилом слизистой прямой кишки, которое сопровождается кровотечениями при акте дефекации, воспалительными процессами и трещинами анального отверстия.
Основными методами лечения генитальных кондилом и предраковых неопластических заболеваний, обусловленных ВПЧ, в настоящее время являются химическая деструкция, хирургическое иссечение или аблация. Данные методы нередко сопровождаются осложнениями, требуют применения дорогостоящего медицинского оборудования и далеко не всегда оказываются эффективными. При этом огромное число молодых женщин с невыраженной клинической картиной вагинального кондиломатоза, не подлежащих деструктивному лечению, являются носителями инфекции и представляют опасность для половых партнеров и будущего ребенка.
При инфицировании эпителиальных тканей вирус папилломы использует целый набор механизмов, подчиняющих своим интересам жизнедеятельность инфицированной клетки. Известно, что ДНК ВПЧ кодирует синтез двух белков Е6 и Е7, индуцирующих переход дифференцированных клеток в S-фазу клеточного цикла. На стадии активной репродукции вируса экспрессия генов Е6 и Е7 регулируется белковым продуктом гена Е2 - репрессором транскрипции этих генов. Ключевым событием в малигнизации клеток является интеграция вируса в геном клетки-хозяина, которая сопровождается делецией гена Е2.
Контроль клеточного цикла и дифференцировки осуществляется посредством онкогенных белков Е6 и Е7, инактивирующих "ключевые" белки-регуляторы пролиферативной активности клеток - проапоптотический белок р53 и белок ретинобластомы (pRB). Установлено, что белок Е7 способен образовывать стабильный комплекс с белком pRB, вызывая его деградацию, что приводит к высвобождению транскрипционного фактора E2F, который стимулирует транскрипцию генов, необходимых для репликации ДНК в S-фазе клеточного цикла. Кроме того, Е7 влияет на активность целого ряда других белков-регуляторов клеточного цикла, таких как А- и Е-циклины, сdk2-киназа и ингибиторы циклин-зависимой киназы р21 и р27 (Киселев В.И. Вирусы папилломы человека в развитии рака шейки матки. Монография, М.: Димитрейд График Групп®, 2004).
Известно, что в патогенезе вирусной инфекции, приводящей к повышению пролиферативной активности инфицированных клеток доброкачественного характера (а иногда и с их злокачественным перерождением), значительную роль играет уровень и активность женских половых гормонов - эстрогенов (Киселев В.И., Дмитриев Г.А., Кубанова А.А. Взаимосвязь вирусных инфекций, передаваемых половым путем, и онкологических заболеваний урогенитального тракта. Вестник дерматологии и венерологии, 2000, №6, стр.20-23).
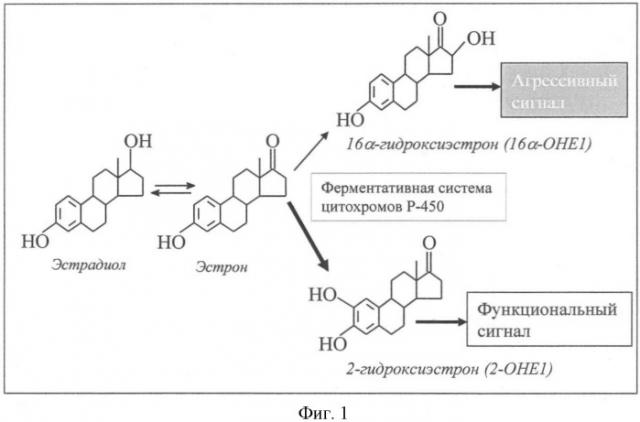
При этом относительное постоянство пролиферативной клеточной активности в эстроген-чувствительных тканях контролируется с помощью специальных метаболических механизмов, конвертирующих эстрадиол (наиболее активный эстроген) в биологически активные его производные. Основной пул эндогенного эстрогена утилизируется посредством локализованной в печени монооксигеназной системы цитохромов Р-450, катализирующей образование его гидроксипроизводных, что облегчает их растворимость и последующее выведение из организма через почки и желчевыводящие пути. Ферментативная система цитохромов P-450 обеспечивает конверсию эстрадиола в два основных метаболита: 16α-гидроксиэстрон (16α-ОНЕ1) и 2-гидроксиэстрон (2-ОНЕ1) (фиг.1).
16α-ОНЕ1 относится к категории "агрессивных" гормонов, вызывающих длительный канцерогенный эффект (Schneider J., Kinne D., Fracchia A., Pierce V. et al. Abnormal oxidative metabolism of esradiol in women with breast cancer, Proc. Natl. Acad. Sci. USA, 1982, v.79, p.3047-3051). Показано, что этот эффект обусловлен образованием прочных ковалентных связей 16α-ОНЕ1, являющегося агонистом эстрогена, с ядерными эстрогеновыми рецепторами (Swaneck G.E., Fishman J., Covalent binding of the endogenous estrogen 16 alphahydroxyestrone to estradiol receptor in human breast cancer cells: characterization and intranuclear localization, Proc. Natl. Acad. Sci. USA, 1988, v.85 (21), p.7831-7835).
2-ОНЕ1 обладает умеренными функциями и, в отличие от 16α-ОНЕ1, напротив, нормализует клеточный рост. При повышении уровня 2-ОНЕ1 наблюдается тенденция к гибели опухолевых клеток и профилактике их дальнейшего образования.
Изучение функций этих двух метаболитов позволило выявить однозначную связь между уровнем 16α-ОНЕ1 и риском развития опухолей в эстроген-зависимых тканях и заключить, что соотношение 2-ОНЕ1 к 16α-ОНЕ1 является одновременно универсальным биомаркером и надежным диагностическим критерием при определении риска и прогноза развития эстроген-зависимых опухолей.
Давно было отмечено, что тканевые изменения в цервикальном канале, вызванные ВПЧ, локализованы главным образом в эстроген-чувствительных зонах. Более того, было установлено, что там, где наблюдается активная экспрессия белков ВПЧ, отмечен высокий уровень синтеза 16α-ОНЕ1, сравнимый с таковым в раковых клетках молочной железы.
Следует подчеркнуть, что в норме эпителиальные клетки шейки матки не способны обеспечивать превращение эстрадиола в 16α-гидроксиэстрон. Таким образом, активная репродукция ВПЧ индуцирует образование "агрессивного" метаболита в инфицированных клетках (Киселев В.И. Вирусы папилломы человека в развитии рака шейки матки. Монография, М.: Димитрейд График Групп®, 2004).
В то же время было показано, что ВПЧ-инфицированные кератиноциты человека проявляют пролиферативную активность in vitro, но при этом не имеют опухолевого фенотипа при микроскопическом исследовании. Добавление в культуральную среду экзогенного 16α-ОНЕ1 превращает клетки в типично раковые (Aubom К., Woodworth G., DiPaolo J., Bradlow L. The interaction between HPV infection and estrogen metabolism in cervical carcinogenesis. Int. J. Cancer, 1991, v.49, p.867-869).
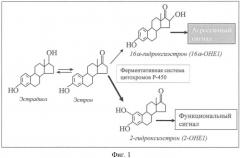
Таким образом, формируется «порочный круг», при котором вирус через образование "агрессивной" формы эстрадиола создает благоприятные условия для развития опухоли, стимулируя синтез онкобелка Е7. В свою очередь, онкобелок Е7, с одной стороны, активирует механизмы патологической пролиферации клеток, а с другой - блокирует противовирусную иммунологическую защиту (фиг.2).
Еще одним важным свойством белка Е7 является его способность индуцировать экспрессию циклооксигеназы 2-го типа (ЦОГ-2) (Subbaramaiah К. and Dannenberg A.J. Cyclooxygenase-2 transcription is regulated by human papillomavirus 16 E6 and Е7 oncoprotein: Evidence of corepressor/coactivator exchange. Cancer Res., 2007, 67(8), 3976-3985). В последние годы доказана исключительно важная роль этого фермента в малигнизации эпителиальных клеток шейки матки (Kulkarni S., Rader J.S. et al. Cyclooxigenase-2 is overexpressed in human cervical cancer, Clinical Cancer Research, 2001, vol.7, p.429-434), (By Ferrandina G., Lauriola L. et al. Increased Cyclooxigenase-2 expression is associated with chemotherapy resistence and poor survival in cervical cancer patients, J. of Clinical Oncology, 2002, v.20, 4, p.973-981). Однако многолетние клинические наблюдения показывают, что вирусная инфекция - необходимый, но недостаточный элемент в развитии опухолевых процессов шейки матки. По разным данным лишь от 1% до 4% случаев ВПЧ инфекции эпителия шейки матки развиваются по пути малигнизации и приводят к раку. Это означает, что для индукции канцерогенеза необходимы еще какие-то метаболические нарушения эпителия, инфицированного ВПЧ.
В последние годы накапливаются данные о том, что гиперметилирование генов-супрессоров опухолевого роста может служить благоприятным фоном для инициации канцерогенеза (Momparler RL, Cancer epigenetics, Oncogene, 2003, 22, 6479-6483). Дело в том, что онкогенного потенциала ВПЧ недостаточно для инициации необратимых процессов канцерогенеза эпителия шейки матки, если вирус инфицирует здоровый эпителий, не имеющий признаков генетических нарушений. Этим и объясняется тот факт, что в большинстве случаев инфицирования наблюдаются умеренные процессы дисплазии (CIN I) и (CIN II), которые с большой вероятностью разрешаются спонтанно, без врачебного вмешательства. В случае если вирусная инфекция поражает эпителий с определенными генетическими нарушениями, например дефектами в экспрессии генов - супрессоров опухолевого роста, то процессы малигнизации приобретают злокачественный характер, что приводит к развитию рака in situ (Кекеева Т.В., Жевлова А.И. и др. Аномальное метилирование генов - супрессоров опухолевого роста и микросателлитная нестабильность в предраковых состояниях шейки матки, Молекулярная биология, 2006, том.40, №2, с.224-230).
Для формирования необратимой неоплазии необходимы:
1) индукция метаболических механизмов конверсии эстрадиола в 16α-ОНЕ1, играющего ключевую роль в раковом перерождении ВПЧ-инфицированных клеток;
2) активная экспрессия онкогенов Е6 и Е7 вируса, стимулируемая взаимодействием комплекса гормон-рецептор с промотором ДНК ВПЧ;
3) индукция множественных повреждений хромосомной ДНК в инфицированной клетке, завершающая процесс опухолевой трансформации;
4) гиперметилирование генов-супрессоров опухолевого роста, в результате которого нарушается их экспрессия и утрачивается механизм контроля над процессами малигнизации эпителиальных клеток.
В связи с появлением вирусной концепции цервикального канцерогенеза принципиально изменились и подходы к лечению диспластических процессов шейки матки и прилегающих областей.
В частности, было разработано средство на основе композиции для профилактики и лечения дисплазий и рака шейки матки и папилломатоза гортани, включающей индол-3-карбинол (I3С) в эффективном количестве и подходящий фармацевтический носитель в виде вагинальных свечей (патент РФ 2196568, опубл. 2003.01.20).
Соединение I3С обладает широким спектром противоопухолевой активности. Однако индол-3-карбинол является нестабильным соединением. Поэтому более перспективным представляется дииндолилметан (DIM), представляющий собой димер, образующийся из индол-3-карбинола (I3С) в кислой среде. Экспериментально доказано, что практически все механизмы, индуцируемые I3С in vitro и in vivo, характерны и для DIM.
В одном из последних экспериментальных исследований была показана способность DIM вызывать апоптоз цервикальных ВПЧ-инфицированных кератиноцитов человека в условиях in vitro. При этом на одной из трех исследованных клеточных линий цервикального рака DIM демонстрировал в несколько раз большую эффективность, чем I3С. Величина LD50 составляла 50-60 мкМ для DIM и 200 мкМ для I3С.Но так же, как и его метаболический предшественник - I3С, DIM не вызывал апоптотических изменений в нормальных (нетрансформированных) кератиноцитах (Chen D.Z., Qi M., Auborn К., Carter Т.Н. Indole-3-Carbinol and diindollylmethane induce apoptosis of human cervical cancer cells and in murine HPV16-transgenic preneoplastic cervical epithelium, J. Nutrit., 2001, 131, 3294-3302).
Недавно также было описано еще одно важное свойство DIM - его иммуномодулирующая активность. Было показано, что в условиях in vitro в опухолевых клетках DIM стимулирует IFNγ-зависимые сигнальные каскады посредством активации экспрессии рецепторов IFNγ, а также других IFN-респонсивных регуляторных белков (Riby J.E., Xue L., Chatterji U., Bjeldanes E.L. et al. Activation and potentiation of interferon-γ signaling by 3,3'-diindolylmethane in MCF-7 breast cancer cells, Mol. Phannacol, 2006, 69, 430-439).
Имея в виду высокую противовирусную и противоопухолевую активность IFNγ, данное свойство может иметь большое клиническое значение при использовании DIM для лечения цервикальных дисплазий, обусловленных ВПЧ.
В качестве ближайшего аналога может быть указано решение, касающееся лекарственной формы в виде вагинальных суппозиториев, содержащих в качестве активной субстанции метиндол (3,3'-дииндолилметан), липофильную основу, включающую твердый кондитерский жир, поливинилпирролидон и бутилгидроксианизол, взятые в определенном соотношении (Патент РФ №2318510, опубл. 2008.03.10). Средство предназначено для лечения генитальных кондилом и неопластических заболеваний репродуктивных органов. Клинические исследования показали его эффективность при CIN I и CIN II. Морфологические и клинические признаки цервикальных дисплазий исчезали при двухнедельном курсе препарата (по 1 свече 1 раз в день). Положительная динамика сопровождалась иррадикацией ДНК ВПЧ в пробах цервикального эпителия анализируемого полимеразной цепной реакцией (ПЦР).
Однако в процессе клинических испытаний было установлено, что вагинальные суппозитории, содержащие DIM, обладали недостаточной эффективностью у пациенток с тяжелой дисплазией (CIN III). По мнению авторов это обусловлено более глубокой степенью малигнизации клеток, которая уже в меньшей степени зависит от экспрессии генов вируса папилломы человека и приобретает необратимый характер за счет нарушений клеточного генома, в основном благодаря эпигенетическим механизмам инактивации генов-супрессоров опухолевого роста, наступающей вследствие гиперметилирования промоторных областей этих генов.
Таким образом, задачей настоящего изобретения являлся поиск более эффективного средства на основе дииндолилметана.
Ключевым механизмом эпигенетической регуляции является метилирование ДНК. Оно заключается в ковалентном присоединении метильной группы по С5-положению цитозина в составе динуклеотида CpG (цитозин-фосфор-гуанозин). Динуклеотидные сочетания CpG могут быть локализованы как в регуляторных (промоторных) участках генов, так и на всем остальном протяжении молекул ДНК. Примерно 50% генов млекопитающих в составе своих промоторов содержат динуклеотид CpG. Если CpG находится в неметилированном состоянии, наблюдается активная экспрессия соответствующего гена. Присоединение метильной группы к цитозину CpG, напротив, подавляет экспрессию генов и переводит их в статус "молчащих". Метилирование цитозинов в составе пары CpG осуществляется при помощи специального фермента - ДНК-метилтрансферазы (DNMT), а точнее, семейства из трех изоферментов - DNMT1, DNMT3a, DNMT3b. Показано, что в условиях in vitro и in vivo уровень экспрессии и активность DNMT1 специфично повышены при многих злокачественных опухолях (Fang J.Y., Cheng Z.H., Chen Y.X. et al. Expression of Dnmtl, demethylase, MeCP2 and methylation of tumor-related genes in human gastric cancer, World J. Gastroenterol, 2004, 10, 3394-3398), (Mizuno S., Chijiwa Т., Okamura T. et al. Expression of DNA methyltransferases DNMT1, 3А, and 3B in nirmal hematopoiesis and in acute and chronic myelogenous leukemia, Blood, 2001, 97, 1172-1179), (Patra S.K., Patra A., Zhao H., Dahiya R. DNA metyltransferase and demethylase in human prostate cancer, Mol. Carcinog, 2002, 33, 163-171).
Повышенный уровень DNMT-опосредованного ДНК-метилирования связывается с повышенной опухолеобразующей (малигнизирующей) активностью клеток млекопитающих. Напротив, ингибирование DNMT (особенно изоформы DNMT1) блокирует гиперметилирование вновь синтезированных ДНК-цепей, в результате чего происходит снижение общего уровня метилирования генома и реэкспрессия "молчащих" генов (Clark S.J., Melki J. DNA methylation and gene silencing in cancer: which is the guilty party, Oncogene, 2002, 21, 5380-5387).
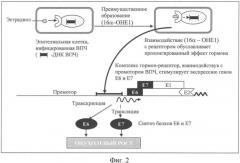
В 2003 г. было показано, что эпигаллокатехин-3-галлат (EGCG) - самый активный из катехинов зеленого чая - является эффективным ингибитором фермента ДНК-метилтрансферазы, основного клеточного фермента, осуществляющего метилирование остатков цитозина в молекуле ДНК (Fang M.Z., Wang Y., Ai N. et al. Tea polyphenol (-)-epigallocatechin-3-gallate inhibits DNA methyltransferase and reactivates methylation-silenced genes in cancer cell lines, Cancer Res, 2003, 63, 7563-7570). EGCG (5-50 мкМ) дозозависимым образом эффективно подавляет активность ДНК-метилтрансферазы, в результате чего происходит деметилирование CpG-динуклеотидов и реактивация метилированных "молчащих" (транскрипционно неактивных) генов, вовлеченных в процессы канцерогенеза, а именно гена-супрессора опухолевого роста р16, гена ретиноидных рецепторов (RAR), гена метилгуанин-метилтрансферазы (MGMT) и гена hMLH1, ответственного за репарацию ДНК (фиг.3).
EGCG не только является деметилирующим агентом, но также ингибирует ЦОГ-2, о важной роли которой в развитии дисплазий шейки матки упоминалось ранее (Peng G., Dixon D.A. et. al. Green tea polyphenol- Epigallocatechin-3-gallate inhibits cyclooxygenase-2 expression in colon carcinogenesis, Molecular carcinogenesis, 2006, 45, 309-319].
Авторами неожиданно было обнаружено, что ингибирующую активность EGCG в отношении ДНК-метилтрансфераз можно на порядок усилить добавлением катиона Mg2+.
Таким образом, вышеуказанная задача была решена новым лекарственным средством для лечения диспластических процессов шейки матки и слизистой прямой кишки. Новое средство выполнено в виде суппозитория вагинального или ректального, содержащего в качестве активных субстанций 3,3'-дииндолилметан и эпигаллокатехин-3-галлат, а также катализатор ингибирующей активности эпигаллокатехин-3-галлата в отношении ДНК-метилтрансфераз, представляющий собой катионы Mg2+в виде фармацевтически приемлемой соли магния, липофильную основу, содержащую твердый жир, поливинилпиролидон и бутилгидроксианизол и/или бутилгидрокситолуол при следующем содержании, мас.%:
| 3,3'-Дииндолилметан | 1,0-10,0 |
| Эпигаллокатехин-3-галлат | 1,0-8,0 |
| Поливинилпирролидон | 0,5-1,2 |
| Бутилгидроксианизол и/или | |
| бутилгидрокситолуол | 0,3-0,5 |
| Соль магния | 0,1-2,0 |
| Липофильная основа | остальное |
В качестве липофильной основы, содержащей твердый жир, могут быть использованы любые известные в области фармации основы данного типа: бутирол, сплав масло какао с гидрогенизированным маслом и парафином, кулинарный жир в смеси с парафином, витепсол и т.п.
В качестве катализатора ингибирующей активности эпигаллокатехин-3-галлата в отношении ДНК-метилтрансфераз могут быть использованы фармацевтически приемлемые соли магния, такие как магния аспарагинат, магния фумарат, магния сукцинат и др. Предпочтительно использование магния хлорида, особенно предпочтительно магния хлористого 6-водного.
Бутилгидроксианизол и бутилгидрокситолуол проявляют эффективное антиоксидантное действие и являются известными консервантами. Введение их в суппозиторную массу дает дополнительный эффект воздействия на пораженную слизистую.
Включение ПВП в липофильную основу обеспечивает также благоприятное действие на слизистую оболочку.
Способ приготовления суппозиториев заключается в том, что расплавляют компоненты липофильной основы, часть ее отдельно растирают с действующим веществом до получения гомогенной взвеси, к охлажденной оставшейся части основы добавляют поливинилпирролидон (ПВП) и бутилгидроксианизол и/или бутилгидрокситолуол и затем полученную взвесь перемешивают до однородного состояния и формуют свечи методом выливания в формы.
Предпочтительно дииндолилметан содержится в количестве 0,01-0,6 г на свечу, эпигаллокатехин-3-галлат - 0,01-0,4 г, магния соль - 0,01-0,02 г.
Изобретение поясняется следующими чертежами:
Фигура 1 - метаболизм эстрадиола,
Фигура 2 - роль эстрогенов в канцерогенезе эпителиальных клеток шейки матки, инфицированных ВПЧ,
Фигура 3 - эпигенетическая регуляция активности генов.
Изобретение может быть проиллюстрировано следующими примерами.
Пример 1.
Состав фармацевтической композиции в виде вагинальных суппозиториев, в мас.%.
| Дииндолилметан | 2,0 |
| Эпигаллокатехин-3-галлат | 10,0 |
| Поливинилпирролидон | 1,2 |
| Бутилгидроксианизол | 0,3 |
| Магний хлористый | 2,0 |
| Твердый жир типа А | остальное |
Пример 2.
Состав фармацевтической композиции в виде вагинальных суппозиториев, в мас.%.
| Дииндолилметан | 10,0 |
| Эпигаллокатехин-3-галлат | 2,0 |
| Поливинилпирролидон | 1,0 |
| Бутилгидроксианизол | 0,5 |
| Магний хлористый | 0,1 |
| витепсол | остальное |
Пример 3.
Состав фармацевтической композиции в виде вагинальных суппозиториев, в мас.%.
| Дииндолилметан | 3,0 |
| Эпигаллокатехин-3-галлат | 3,0 |
| Поливинилпирролидон | 0,5 |
| бутилгидрокситолуол | 0,3 |
| Магний аспарагинат | 1,0 |
| Основа из кулинарного жира и парафина 1:1 | остальное |
Пример 4.
Исследование клинической эффективности разработанной фармацевтической композиции у пациенток с дисплазией шейки матки.
Для клинических исследований были отобраны две группы пациенток с диагнозом дисплазии шейки матки. В первую группу отбирали пациенток с легкой (CIN I) и умеренной (CIN II) формами дисплазий (таблица 1), во вторую группу - пациенток с тяжелой формой дисплазий (CIN III) (таблица 2).
| Таблица 1 | |||||||
| Количество пациентов с диагнозом CIN I-CIN II | Назначение: вагинальные суппозитории, содержащие | Результаты лечения (количество пациентов) | |||||
| Клиника | Морфология | ПЦР ДНК ВПЧ | |||||
| Норма | Патология | Норма | Патология | Норма | Патология | ||
| 10 | DIM | 8 | 2 | 8 | 2 | 7 | 3 |
| 10 | DIM+EGCG | 9 | 1 | 9 | 1 | 8 | 2 |
| 10 | DIM+EGCG+Mg | 10 | 0 | 10 | 0 | 10 | 0 |
| Таблица 2 | |||||||
| Количество пациентов с диагнозом CIN III | Назначение: вагинальные суппозитории, содержащие | Результаты лечения (количество пациентов) | |||||
| Клиника | Морфология | ПЦР ДНК ВПЧ | |||||
| Норма | Патология | Норма | Патология | Норма | Патология | ||
| 10 | DIM | 2 | 8 | 2 | 8 | 3 | 7 |
| 10 | DIM+EGCG | 9 | 1 | 9 | 1 | 9 | 1 |
| 10 | DIM+EGCG+Mg | 10 | 0 | 10 | 0 | 10 | 0 |
Все диагнозы были подтверждены морфологическими исследованиями. У всех пациенток в цервикальных соскобах были обнаружены методом ПЦР вирусы папилломы человека высокого онкогенного риска, типы 16 или 18.
Каждая из групп делилась на три подгруппы, одной из которых назначалось лечение вагинальными суппозиториями, содержащими DIM, другая подгруппа применяла для лечения суппозитории, содержащие DIM в комбинации с EGCG, и третья - свечи по примеру 2. Курс лечения продолжался в течение 14 дней по одной свече через день.
Через месяц после начала лечения пациенток обследовали с помощью кольпоскопии, провели морфологические исследования клеток шейки матки и лабораторный анализ ПЦР на наличие ДНК ВПЧ 16 и 18 типов.
Пример 5.
Исследование клинической эффективности применения предлагаемой фармацевтической композиции для лечения пациентов с диагнозом кондиломы прямой кишки.
Для клинического исследования были отобраны 20 пациентов проктологического отделения с диагнозом "рецидивирующие кондиломы прямой кишки". Пациенты предъявляли жалобы на боли при акте дефекации, следы крови в стуле. При визуальном осмотре слизистой прямой кишки выявлены кондиломы размером 0.2-0.5 см, слизистая воспалена. У некоторых больных обнаружены трещины анального отверстия. Пациентам назначена монотерапия ректальными суппозиториями по примеру 1, по 1 свече утром и вечером в течение 14 дней. После проведенного курса лечения у 16 пациентов наступило полное клиническое выздоровление, которое сопровождалось исчезновением кондилом и всех признаков воспалительного процесса. У 4 пациентов после проведенного лечения наблюдалось уменьшение числа кондилом и отсутствие признаков воспаления.
1. Лекарственное средство для лечения диспластических процессов шейки матки и слизистой прямой кишки в форме суппозитория, характеризующееся тем, что содержит 3,3'-дииндолилметан, эпигаллокатехин-3-галлат, а также катализатор ингибирующей активности эпигаллокатехин-3-галлата в отношении ДНК-метилтрансфераз, представляющий собой катионы Mg2+ в виде фармацевтически приемлемой соли магния, липофильную основу, содержащую твердый жир, поливинилпирролидон и бутилгидроксианизол и/или бутилгидрокситолуол при следующем содержании, мас.%:
| 3,3'-Дииндолилметан | 1,0-10,0 |
| Эпигаллокатехин-3-галлат | 1,0-8,0 |
| Поливинилпирролидон | 0,5-1,2 |
| Бутилгидроксианизол | 0,3-0,5 |
| Соль магния | 0,1-2,0 |
| Липофильная основа | остальное |
2. Лекарственное средство по п.1, характеризующееся тем, что указанный суппозиторий представляет собой вагинальный суппозиторий.
3. Лекарственное средство по п.1, характеризующееся тем, что указанный суппозиторий представляет собой ректальный суппозиторий.
4. Лекарственное средство по любому из пп.1-3, характеризующееся тем, что катализатор ингибирующей активности эпигаллокатехин-3-галлата в отношении ДНК-метилтрансфераз представляет собой магний хлористый.