Новые поверхностно-активные вещества и их применение
Иллюстрации
Показать всеНастоящее изобретение относится к новым поверхностно-активным соединениям формулы III и их использованию для получения наночастиц, служащих в качестве векторов для биологически активных ингредиентов.
где R3 выбран из групп IV или V; Y - атом серы или -NH-CO-(CH2)n-X-; Х - атом серы или -СН2-; n и y целые числа от 0 до 10; R - углеводород, фторированный углеводород или тиоалкил; W - группа -NH- или -СН2-; p - целое число от 1 до 50; m - целое число от 0 до 9; и если Х=СН2, тогда 0<m+n<6; x - целое число от 0 до 30; R1 - выбран из следующих радикалов:
где R' представляет собой Н или полигидроксилированный углеводород; R2 - группа распознавания, обладающая сродством к биологической мишени; Z - спейсерная группа. Технический результат - разработка новых поверхностно-активных соединений и наночастиц на их основе. 4 н. и 18 з.п. ф-лы, 2 табл., 9 ил.
Реферат
Настоящее изобретение относится к новым поверхностно-активным веществам типа теломеров и к их использованию для получения метастабильных надмолекулярных систем. Эти стабильные надмолекулярные системы или наночастицы могут представлять собой липосомы или мицеллярные системы. Изобретение также относится к атипичным липосомам и наночастицам, полученным из данных поверхностно-активных веществ, и к их использованию в качестве векторов для активных ингредиентов, в особенности для терапевтически активных ингредиентов.
Некоторые амфифильные молекулы, природные фосфолипиды, обладают свойством ассоциироваться в воде с образованием метастабильных надмолекулярных образований сферической формы, называемых липосомами, которые содержат внутренний водный компартмент. Такие липосомы способны содержать терапевтически активные агенты внутри указанного внутреннего компартмента и могут, таким образом, быть использованными для транспортировки указанных активных агентов к клеткам-мишеням или тканям-мишеням. Исследование этих специфических векторов представляло собой предмет многочисленных публикаций, в которых были широко рассмотрены проблемы, а также потенциальные возможности (Barenholz, Curr. Opin. in Coll. And Int. Sci. 6 (2001) 66-77).
Однако использование липосом для транспортировки терапевтически активных ингредиентов имеет несколько основных недостатков.
Данные наноструктуры обычно обладают сравнительно низкой стабильностью с течением времени, так как они сливаются в среде, в которой они диспергированы, с образованием более крупных объектов, которые впоследствии быстро осаждаются. Это поведение в значительной степени ограничивает их стабильность и сохраняемый объем.
Биологическая стабильность данных векторов, т.е. время их удержания в кровотоке, непосредственно связана с их размером, который должен составлять менее 200 нм, для того, чтобы они могли достичь потенциальной мишени (Nagayasu et al., Adv. Drug Del. Rev. 40 (1999) 75-87). Однако кандидаты, наиболее эффективные с этой точки зрения, а именно однослойные липосомы небольших размеров, обладают недостатком, состоящим в том, что они имеют соотношение инкапсулированный медицинский продукт/липид меньшее по сравнению с однослойными липосомами больших размеров (Vernuri et al., Pharm. Acta Helv. 70 (1995) 95-111). Липиды, образующие указанные наноструктуры, обычно имеют высокую стоимость производства. Таким образом, низкая способность к инкапсулированию активных ингредиентов некоторых из этих липосом представляет собой экономическую проблему.
Наконец, необходима возможность обеспечить вектор, который может высвобождать свое содержимое постепенно и непрерывно. Такие свойства требуют использования высокоорганизованных и непроницаемых мембран, которые состоят из сложных и дорогостоящих липидных составов.
Несмотря на эти трудности, в настоящее время в продаже или на клинической фазе испытаний имеется определенное число фармацевтических препаратов на основе липосом. Наиболее существенное преимущество этих препаратов состоит в их превосходной переносимости по сравнению с использованием свободного активного ингредиента. В то же время их эффективность при эквивалентной дозе лишь незначительно выше. Это наблюдается в случае инкапсулированного в липосомы амфотерицина В (Ambisome®). Его инкапсулирование в липидных составах в значительной степени увеличивает его терапевтический индекс (Andres et al., Rev. Med. Interne, 22 (2001) 141-150).
Для того, чтобы уменьшить их быстрое удаление ретикулоэндотелиальной системой, были разработаны системы защиты липосом. Наиболее эффективная состоит в использовании фосфолипидов, замещенных полиэтиленгликолями, имеющими молекулярную массу в диапазоне от 1000 до 5000 в пропорции от 5 до 10% от общей смеси фосфолипидов. «Невидимые» липосомы, также называемые стелс-липосомами, образованные таким образом (продаваемые под торговым наименованием Stealth liposomes®), имеют большее время удержания в кровотоке по сравнению с традиционными липосомами (45 ч по сравнению с диапазоном от нескольких минут до нескольких часов). Увеличение времени циркуляции указанных липосом в крови способствует их аккумулированию в раковых тканях, которые особенно омываются (кровью), и их использование особенно пригодно для транспортировки противораковых составов (Gabizon et al., Cancer Res. 54 (1994) 987-992). В настоящее время на рынке представлены составы Stealth liposomes® на основе доксорубицина (Doxil®, Alza Corp.) для борьбы с синдромом Капоши. Однако определенные составы, состоящие из очень мелких (50 нм) липосом могут также рассматриваться как препараты длительной циркуляции. Примером этого является антираковый препарат даунорубицин (дауномицин), представленный на рынке NeXstar (DaunoXome®).
Для того, чтобы гарантировать механическую стабильность липосом как в ходе их хранения, так и при их использовании in vivo, можно представить себе несколько стратегий, включающих использование полимеров:
полимеризация поверхностно-активных веществ, составляющих мембрану липосомы, после ее образования (Bader et al., Adv. Polym. Sci. 64 (1985) 1-62 и Hotz et al., Adv. Mater. 10 (1998) 1387-1390);
взаимодействие амфифильных и неамфифильных ионных полимеров на поверхности внешней мембраны липосом (Hayashi et al., Biochem. Biophys. Acta, 1280 (1996) 120-126, Ishishara et al., Coll. And Surf., B: Biointerfaces 25 (2002) 325-333);
наконец, полимеризация гидрофильного мономера внутри внутренней водной полости липосомы представляет собой способ, который очень слабо изучен и был кратко описан Torchilin et al. (Makromol. Chem., Rapid communication, 8 (1987) 457-460). Его использовали в качестве инструмента для получения полимеризованного молекулярного отпечатка в патенте США (Perrot et al., патент США № 6217901, 17 апреля 2001).
Значительное ограничение, связанное с использованием полимеров для стабилизации липосом, представляет собой потенциальная токсичность, вызванная их аккумуляцией в лизосоме или собственной токсичностью неполимеризованного гидрофильного мономера (в случае акриламида). Для того, чтобы ограничить это явление, необходимо использовать полимеры с низкой молекулярной массой, которые более легко поддаются биологическому разрушению.
Использование мицелл, стабилизированных с использованием полимеризованных амфифильных соединений, комбинирующих гидрофильные и гидрофобные блоки, для транспортировки терапевтически активных агентов, которые в значительной степени нерастворимы в воде, представляло собой предмет многочисленных научных исследований (G.S. Kwon et al., Adv. Drug. Deliver. Rev., 16 (1995) 295-309, M. Jones et al., Eur. J. Pharm. Biopharm., 48 (1999) 101-111, V.P. Torchilin, J. Control. Release, 73 (2003) 137-172). Указанные векторные системы делают это возможным, в особенности для транспортировки и растворения определенного числа активных антираковых агентов, в особенности полициклических производных. Как общее правило, последние характеризуются очень низкой биологической доступностью при пероральном введении, а их внутривенные инъекции приводят из-за агрегации к эмболии кровеносных сосудов и к местной токсичности, связанной с твердыми отложениями (A.N. Lukyanov et al., Adv. Drug. Deliver. Rev., (2004) доступно в сети Интернет, Science Direct). Использование липосом, микроэмульсий или циклодекстринов представляет собой многообещающее решение, но все еще демонстрирующее слишком много ограничений, в частности слишком высокую вариабельность в растворении этих сравнительно нерастворимых активных ингредиентов, которое в значительной степени зависит от их структуры. Развитие малых полимерных мицеллярных систем, таким образом, представляет собой благоприятную альтернативу таким технологиям, в которых были заинтересованы заявители.
Благодаря особенно низкой ККМ (критической концентрации мицелообразования) полимерные поверхностно-активные вещества, составляющие указанные мицеллы, придают им в особенности высокую термодинамическую стабильность и чрезвычайно высокую способность к удержанию инкапсулированных активных агентов. Очень небольшой размер указанных наночастиц (менее чем 100 нм) придает им превосходную стабильность in vivo, а также пассивное нацеливание на в особенности хорошо снабжаемые (кровью) опухолевые участки.
Активное нацеливание указанных векторов можно осуществлять путем покрывания их поверхности нацеливающими молекулами, такими как антитела, пептиды, лектины, сахара, гормоны или специфические синтетические соединения.
В литературе упоминается большое число полимеров, которые являются амфифильными по своей природе. Они представляют собой обычно полимеры двухблочного типа, состоящие из различных гидрофильных и гидрофобных мономеров (M. Jones et al., Eur. J. Pharm. Biopharm., 48 (1999) 101-111, V.P. Torchilin, J. Control. Release, 73 (2001) 137-172). Также были исследованы другие амфифильные агенты, полученные из фосфолипидов и из полимеров полиэтиленгликоля и поливинилпирролидона (A.N. Lukyanov et al., Adv. Drug Deliver. Rev., (2004) доступно в Internet, Science Direct).
Первая цель настоящего изобретения состоит в развитии наноразмерных векторов, которые имеют низкую стоимость производства и имеют способность к транспортировке внутри своей внутренней полости большого семейства гидрофильных активных агентов. Наноразмерные векторы по изобретению позволяют инкапсулировать, удерживать и высвобождать вещества, которые можно дозировать. Заданные применения включают транспортировку активных ингредиентов, в особенности терапевтических активных ингредиентов, эпидермальную доставку косметических веществ и медицинскую диагностику; в частности транспортировку противораковых активных агентов, активных агентов для использования на основе вакцин, генетического материала, ферментов, гормонов, витаминов, сахаров, белков и пептидов, липидов или органических и неорганических молекул.
Эта цель достигнута посредством разработки и синтеза новых поверхностно-активных веществ, которые делают возможным получение наноразмерных векторов или липосом, которые имеют благоприятные свойства по сравнению с липосомами по предшествующему уровню техники.
Вторая цель настоящего изобретения состоит в разработке наноразмерных векторов, имеющих очень низкую стоимость производства и обладающих способностью транспортировать внутри своей гидрофобной полости или липидного слоя очень большое семейство гидрофобных активных агентов. Наноразмерные векторы по изобретению позволяют инкапсулировать, удерживать и высвобождать вещества, которые можно дозировать. Заданные применения включают транспортировку активных ингредиентов, в особенности терапевтических активных ингредиентов, эпидермальную доставку косметических веществ и медицинскую диагностику; в частности транспортировку противораковых активных агентов, активных агентов для использования на основе вакцин, генетического материала, ферментов, гормонов, витаминов, сахаров, белков и пептидов, липидов или органических и неорганических молекул.
Эта цель достигнута при помощи разработки и синтеза новых поверхностно-активных веществ теломерного типа, которые делают возможным получение мицелл и эллипсоидальных наночастиц или липосом, которые имеют благоприятные свойства по сравнению с полимерными мицеллами по предшествующему уровню техники.
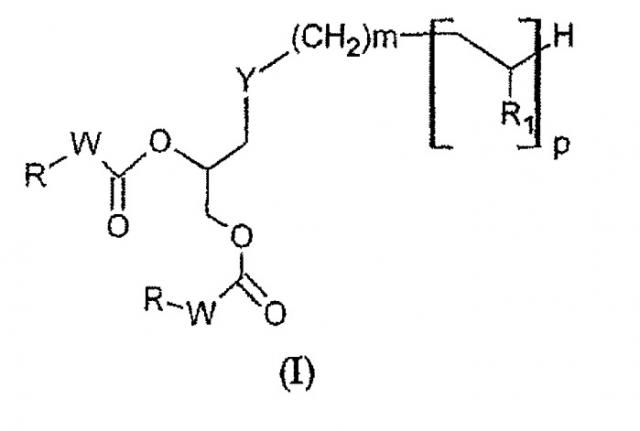
Предметом настоящего изобретения являются соединения, имеющие формулу (I):
в которой:
• Y представляет собой атом серы или группу
Причем Х выбирают из групп S и СН2, n представляет собой целое число, изменяющееся в диапазоне от 0 до 10, такое как, например, 0, 1, 2, 3, 4, 5 или 6;
• m представляет собой целое число, изменяющееся в диапазоне от 0 до 9, такое как, например, 0, 1, 2, 3, 4, 5 или 6;
и если Х=СН2, тогда 0 < m+n < 6;
• W представляет собой группу -NH- или группу -CH2-;
• р представляет собой целое число, изменяющееся в диапазоне от 0 до 50;
• R1 представляет собой группу, выбранную из следующих радикалов:
в которых R' представляет собой Н или гидрофильную группу, такую как, например, С4-С24 полигидроксилированное соединение на основе углеводорода; в частности, R' может быть выбрана из сахаров, таких как, например, галактоза, глюкоза, манноза или сиаловая кислота, связанных через их аномерный атом углерода;
• R представляет собой группу, выбранную из: С4-С24 радикалов на основе углеводорода; С4-С24 фторированных радикалов на основе углеводорода; С4-С24 тиоалкильных радикалов.
Группа R может быть, в частности, выбрана из следующих радикалов:
- тиооктильного радикала,
- С4-С24 радикалов на основе углеводорода, таких как н-бутил, трет-бутил, изобутил, н-пентил, изопентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил, н-додецил, н-тридецил, н-тетрадецил, н-пентадецил, н-гексадецил, н-гептадецил, н-октадецил или фитильный радикал
(CH3[CH(CH3)(CH2)3]3CH(CH3)CH2CH2)),
С4-С24 фторированных радикалов на основе углеводорода, таких как радикалы, отвечающие формуле -(СН2)t-(CF2)rF, в которой r и t оба представляют собой целые числа при условии 24 ≥ r+t ≥4, такие как, например:
-(CF2)4F; -(CF2)5F; -(CF2)6F; -(CF2)7F; -(CF2)8F; -(CF2)9F;
-(CF2)10F; -(CF2)11F; -(CF2)12F; -(CF2)13F; -(CF2)14F; -CH2-(CF2)3F;
-CH2-(CF2)4F; -CH2-(CF2)5F; -CH2-(CF2)6F; -CH2-(CF2)7F; -CH2-(CF2)8F; -CH2-(CF2)9F; -CH2-(CF2)10F; -CH2-(CF2)11F; -CH2-(CF2)12F; -CH2-(CF2)13F; -(CH2)2-(CF2)2F; -(CH2)2-(CF2)3F; -(CH2)2-(CF2)4F; -(CH2)2-(CF2)5F; -(CH2)2-(CF2)6F; -(CH2)2-(CF2)7F; -(CH2)2-(CF2)8F; -(CH2)2-(CF2)9F; -(CH2)2-(CF2)10F; -(CH2)2-(CF2)11F; -(CH2)2-(CF2)12F; -(CH2)3-(CF2)1F; -(CH2)13-(CF2)F; -(CH2)4-(CF2)6F; -(CH2)4-(CF2)8F;
-(CH2)4-(CF2)10F; -(CH2)10-(CF2)6F; -(CH2)10-(CF2)8F; -(CH2)10-(CF2)10F; и т.д.
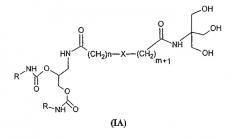
Согласно первому предпочтительному варианту предметом настоящего изобретения являются соединения, имеющие формулу (IA):
в которой:
Х представляет собой атом S или группу -СН2-;
n представляет собой целое число, изменяющееся в диапазоне от 0 до 10, такое как, например, 0, 1, 2, 3, 4, 5 или 6;
m представляет собой целое число, изменяющееся в диапазоне от 0 до 9, такое как, например, 0, 1, 2, 3, 4, 5 или 6;
и если Х=СН2, тогда 0 < m+n < 6;
R представляет собой группу, выбранную из: С4-С24 радикалов на основе углеводорода; С4-С24 фторированных радикалов на основе углеводорода; С4-С24 тиоалкильных радикалов.
Предпочтительными цепями R являются цепи, которые способствуют тому, чтобы температура фазового перехода поверхностно-активного вещества формулы (I) была выше 37°С. В действительности, когда подобные поверхностно-активные вещества используют для получения липосом, такие поверхностно-активные вещества, которые имеют кристаллическую структуру при физиологической температуре, придают мембране липосомы бульшую жесткость и более высокую степень удержания растворенных веществ, инкапсулированных во внутреннем водном компартменте. Предпочтительно, R представляет собой цепь на основе углеводорода С12-С24 или цепь на основе фторированного углеводорода С8-С24.
Предпочтительно выполняются одно или несколько следующих условий: X=S; n=2, m=1.
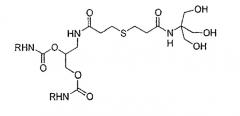
Предпочтительными соединениями формулы (IA) являются соединения, отвечающие формуле А, в которой R имеет то же определение, что и описано выше, n=2, X=S, m=1:
Формула А
Среди этих соединений в особенности предпочтительным соединением является соединение А1, представленное ниже:
Соединение А1
Синтез молекул формулы (I) можно легко проводить при использовании традиционных способов органического синтеза. Несколько примеров синтеза проиллюстрировано в экспериментальной части.
Другой предмет изобретения состоит в использовании молекул формулы (I), преимущественно молекул формулы (IA) для получения липосом. Стенки липосом по предшествующему уровню техники в основном состоят из фосфолипидов.
Липосомы очень легко получают из поверхностно-активных веществ формулы (I), предпочтительно формулы (IA), на основе пленочного способа (Liposomes, a practical approach, R.R.C. New, Ed., Oxford University Press, New York, 1990). Этот способ может быть суммирован следующим образом.
Раствор поверхностно-активного вещества (I) или (IA), растворенного в метаноле или в хлороформе, медленно испаряют в круглодонной колбе для того, чтобы образовать тонкую пленку на стенке круглодонной колбы. Добавляют дистиллированную воду при 65°С, для того, чтобы повторно гидратировать пленку, с концентрацией 2,5 мг/мл. Полученный раствор затем подвергают обработке ультразвуком в течение 30 минут на ультразвуковой бане при температуре выше температуры фазового перехода диспергированного поверхностно-активного вещества, до тех пор, пока не будет получен голубоватый прозрачный раствор. В последней стадии также возможно заменить обработку ультразвуком повторной экструзией раствора через два поликарбонатных фильтра с размером пор 200 нм, установленных последовательно. Также можно представить себе двойную обработку ультразвуком и экструзией.
Для получения липосом по изобретению можно использовать другие традиционные способы получения липосом. В этом контексте в качестве ссылки можно указать S. Vernuri and C.T. Rhodes, Pharmaceutics Acta Helvetiae 70, (1995), 95-111.
Неожиданно наблюдается образование везикул удлиненной формы, такие везикулы носят название трубчатые везикулы из-за их размера, который составляет несколько десятков нанометров, и из-за их формы, которая напоминает трубу, закрытую с ее обеих концов.
Размер и механическую стабильность частиц, полученных в растворе, в зависимости от времени измеряли после фильтрации при помощи динамической дифракции света (High Performance Particle Sizer, Malvern). Природу полученных частиц исследовали при помощи просвечивающей электронной микроскопии после негативного окрашивания образца или после замораживания-скалывания (Фиг.4).
Измерения формы и размера, определенные путем рассматривания электронной микрофотографии, дали возможность продемонстрировать образование липосом удлиненной формы, называемых трубчатыми везикулами, замкнутыми с концов, среднее поперечное сечение которых составляет от 20 до 80 нм и средняя длина которых составляет от 200 до 500 нм (Фиг.3). Анализ способом замораживания-скалывания подтвердил образование указанных трубчатых везикул и их морфологические характеристики, а именно наличие внутренней водной полости, изолированной от внешней среды (Фиг.5).
Для заданного поверхностно-активного вещества формулы (IA) размер частиц является в значительной степени гомогенным: он изменяется в пределах диапазона ±10% от значения, предпочтительно ±5% вокруг центрального значения длины и диаметра.
Эти трубчатые везикулы имеют относительно высокую стабильность, поскольку не наблюдается изменения размера частиц после года хранения, тогда как липосомы, образованные из фосфатидил-холина яичного желтка, показывают изменение всего после лишь 5 дней хранения.
Доказательство наличия внутренней водной полости было получено опосредованно при помощи спектрофлуориметрических измерений кинетики инкапсулирования и высвобождения гидрофильного флуоресцентного зонда - карбоксифлуоресцеина. Измерения напрямую показывают более медленную кинетику высвобождения флуоресцентного зонда по сравнению с традиционным инкапсулированием в смеси фосфатидил-холина яичного желтка (Фиг.1).
Заявители смогли продемонстрировать, что внутримолекулярные водородные связи между поверхностно-активными веществами, составляющими трубчатые везикулы, являются причиной их морфологии и их специфической стабильности. Действительно, спиртовые функции трис(гидроксиметил)аминометана, а также карбаматные функции обладают способностью генерировать сеть водородных связей между поверхностно-активными веществами, составляющими мембрану, таким образом стабилизируя трубчатые везикулы. Оказалось возможным продемонстрировать это при использовании инфракрасной спектроскопии жидкой фазы на основе преобразования Фурье (в CCl4). Увеличение интенсивности полосы при 1691 см-1, отвечающее карбонильным функциям, связанным с атомом водорода, фактически отмечается в спектре при увеличении концентрации поверхностно-активного вещества в растворе за счет его несвязанного гомолога (Фиг.2).
Здесь следует отметить, что замещение в поверхностно-активном веществе формулы (IA) карбаматной связи на сложно-эфирную связь между жирной цепочкой и звеном глицерина, как проиллюстрировано в структуре В, приводит к образованию в воде липосом традиционного строения, механическая стабильность которых составляет всего несколько часов, таким образом подтверждая выдвигаемую гипотезу, что трубчатые везикулы стабилизированы и организованы благодаря установлению специфических водородных связей (Фиг.6).
Структура В
Предмет настоящего изобретения составляют также липосомы, или водная дисперсия везикул, отличающаяся тем, что они включают одно или несколько соединений формулы (I), преимущественно формулы (IA) в качестве компонента их стенок.
Эти липосомы демонстрируют оригинальные структурные характеристики, которые придают им неожиданные свойства, в частности улучшенную стабильность по сравнению с липосомами по предшествующему уровню техники. Липосомы по изобретению также демонстрируют способность к высвобождению активного ингредиента в течение длительного периода времени по сравнению с липосомами по предшествующему уровню техники.
Согласно второму предпочтительному варианту предмет настоящего изобретения представляет собой соединения, отвечающие формуле (IB):
в которой:
Y представляет собой атом серы или группу -NH-CO-CH2CH2S-;
W представляет собой группу -NH- или группу -CH2-;
р представляет собой целое число, изменяющееся в диапазоне от 1 до 50;
R1 представляет собой группу, выбранную из следующих радикалов:
в которых R' представляет собой Н или гидрофильную группу, такую как, например, С4-С24 полигидроксилированное соединение на основе углеводорода. В частности, R' может быть выбрана из сахаров, таких как, например, галактоза, глюкоза, манноза или сиаловая кислота, связанных через их аномерный атом углерода;
R представляет собой группу, выбранную из: С4-С24 радикалов на основе углеводорода; С4-С24 фторированных радикалов на основе углеводорода; С4-С24 тиоалкильных радикалов.
Предпочтительными цепями R являются цепи, которые способствуют тому, чтобы критическая концентрация мицеллообразования (ККМ) поверхностно-активного вещества формулы (IB) составляла менее 10-5 М. В действительности, низкая ККМ придает наночастице термодинамическую стабильность, а также способность к удержанию растворов, инкапсулированных во внутреннем гидрофобном компартменте. Предпочтительно, R представляет собой цепь на основе углеводорода С12-С24 или цепь на основе фторированного углеводорода С8-С24.
Синтез молекул формулы (IB) можно легко проводить с использованием традиционных способов органического синтеза. Несколько примеров синтеза проиллюстрировано в экспериментальной части.
В качестве краткого обобщения, молекулу формулы (IB) синтезируют с группой R тиоалкильного типа, указанную молекулу используют в качестве агента-переносчика в реакции теломеризации в присутствии гидрофильного полимеризуемого реагента (типа трис- (гидроксиметил)акриламидометана или его производных, или винилпирролидона) и свободно-радикального инициатора, такого как α,α'-азобисбутиронитрил (AIBN) в растворе в метаноле, ТГФ (THF) или в ацетонитриле, доведенном до точки кипения. Изначальное соотношение полимеризуемого мономера и агента-переносчика делает возможным осуществление контроля степени полимеризации теломера и, таким образом, растворимости продукта. Последний получают осаждением из простого эфира.
Предпочтительными соединениями формулы (IB) являются соединения, в которых Y представляет собой S.
Другой предпочтительный вариант представляет собой такой, в котором р представляет собой целое число в диапазоне от 5 до 15.
Еще более преимущественно, предпочтение отдается соединениям, отвечающим формуле С ниже, в которой R определен так же, как указано выше, р представляет собой целое число в диапазоне от 5 до 15 и W=CH2:
Соединение С
Среди указанных соединений в особенности предпочтительным соединением является С1, представленное ниже:
Соединение С1
Другим предметом изобретения является использование соединений формулы (I), преимущественно соединений формулы (IB), для получения наночастиц с гидрофобной полостью, а также полученные таким образом наночастицы. Наночастицы получают из поверхностно-активных веществ формулы (I) или (IB), чрезвычайно легко, при использовании пленочного способа, который хорошо известен специалистам в данной области техники и который описан в работе Liposomes, a practical approach, R.R.C. New, Ed., Oxford University Press, New York, 1990. Способ проводят, как описано выше для соединения формулы (IA).
Неожиданно, при использовании соединений с общей формулой (IB), в которых величина р составляет менее чем 15 и где R представляет собой цепь на основе углеводорода, включающую по крайней мере 12 атомов углерода, наблюдалось образование наночастиц удлиненной формы, называемых эллипсоидами из-за их формы, напоминающей форму зерен риса (Фиг.7а).
Исследование эллипсоидных частиц, полученных при использовании соединений структуры (IB)
Действительно, при использовании производных соединений с общей формулой (IB), в которых р составляет в диапазоне от 5 до 15, наблюдалось образование оригинальных частиц (Фиг.8), форма которых напоминала зерно риса и размер которых уменьшался с увеличением р. В том случае, если р составляет более 15, размер полученных объектов составляет менее 10 нм и природа образуемых агрегатов в значительной степени является мицеллярной.
Размер и механическую стабильность с течением времени частиц, полученных в растворе, измеряли после фильтрации при помощи динамической дифракции света (High Performance Particle Sizer, Malvern). Природу полученных частиц исследовали при помощи просвечивающей электронной микроскопии (ТЕМ) после негативного окрашивания образца или после замораживания-скалывания. Критическую концентрацию агрегации этих поверхностно-активных веществ определяли тензиометрией или спектрофлуометрией при использовании способа флуоресцентной метки. Кроме того, способ тензиометрии по Wilhelmi сделал возможным определение максимальных поверхностных натяжений и площади полярной головки на границе раздела вода-воздух (Фиг.8). Эти соединения демонстрируют сравнительно низкие ККМ порядка 10-5 М. ККМ этих поверхностно-активных веществ фактически не изменяется как функция от р (Фиг.8). Для того, чтобы вызвать уменьшение или увеличение этой величины, необходимо соответственно увеличивать или уменьшать длину цепей на основе углеводородов. Температуру фазового перехода этих поверхностно-активных веществ определяли поляризационной спектрофлуриметрией и рассеянием света (Фиг.9). Температура фазового перехода фактически не изменяется для постоянных длин цепи при увеличении р (41°С<Tm<44°С).
Гидродинамический диаметр (D H) надмолекулярного образования изменяется обратно пропорционально изменению средней степени полимеризации теломеров: чем больше относительный объем полярного компонента, тем больше кривизна мембран (Фиг.8). Этот результат был подтвержден электронной микроскопией. За пределами р=20 все микрофотографии показывают мицеллярные растворы (Фиг.7b). С другой стороны, ниже этой величины они демонстрируют надмолекулярные образования, напоминающие продолговатые объекты в форме рисового зерна, которые не демонстрируют наличия внутренней водной полости при ТЕМ исследованиях после негативного окрашивания (Фиг.7а).
При использовании калибровки частиц оказывается, что для соединения структуры (С) с р=5 и R=C17H35 гидродинамический диаметр полученных частиц составляет 148 нм. Эти объекты демонстрируют чрезвычайно высокую стабильность с течением времени, которая увеличивается пропорционально величине р (от 2 недель для р=5 до нескольких месяцев для р=25).
Данные эллипсоидные частицы демонстрируют оригинальные структурные характеристики, и их средний гидродинамический диаметр можно легко изменять, варьируя р, т.е. число мономерных единиц, составляющих полимерную частицу. Частицы по изобретению также продемонстрировали способность инкапсулировать гидрофобные активные агенты. Это включение можно проводить при использовании технологических способов, хорошо известных специалистам в данной области техники. Например, инкапсулирование можно проводить растворением активного агента в предварительно полученном растворе эллипсоидов или мицелл, процедурой “масло в воде” или диализом. Терапевтические соединения, которые могут быть инкапсулированы, представляют собой все соединения, предпочтительно гидрофобные соединения, которые могут быть стабильно включены в эти мицеллярные или эллипсоидные образования. При использовании указанных объектов различные семейства слабогидрофильных или гидрофобных активных ингредиентов могут быть инкапсулированы или растворены, включая противораковые агенты, антибиотики, иммуномодуляторы, стероиды, противовоспалительные препараты или нуклеотиды. Могут также быть инкапсулированы или векторизированы гидрофильные соединения, способные образовывать комплекс с полярной частью наночастиц. Дозу активного агента, эффективно инкапсулированного в указанных наночастицах, определяют после фильтрации неинкапсулированного активного агента при использовании ВЭЖХ (HPLC), УФ (UV) или флуоресцентной спектрометрии, а также 1Н ЯМР.
В дополнение к соединению формулы (I) мицеллярные, эллипсоидальные или липосомные наночастицы по изобретению могут также предпочтительно содержать по крайней мере одно соединение, отвечающее формуле (II) ниже:
в которой:
- Y представляет собой атом серы или группу
-NH-CO-(CH2)n-X-, в которой Х представляет собой атом серы S или группу -CH2-, n представляет собой целое число в интервале от 0 до 10;
- W представляет собой группу -NH- или -CH2-;
- x представляет собой 0 или целое число в диапазоне от 1 до 30;
- y представляет собой 0 или целое число в диапазоне от 1 до 10;
- R1 представляет собой гидрофильную группу, выбранную из следующих радикалов:
в которых R' представляет собой Н или гидрофильную группу, такую как, например, C4-С24 полигидроксилированное соединение на основе углеводорода; в особенности R' может быть выбрана из сахаров, таких как, например, галактоза, глюкоза, манноза или сиаловая кислота, связанных через их аномерный атом углерода;
- R2 представляет собой группу распознавания, которую выбирают в соответствии с клеточной мишенью; предпочтительно ее выбирают из групп, обладающих заметным сродством к биологической мишени активного ингредиента, транспортируемого в наночастице.
R2 может представлять собой сахарид по своей природе (для определения в качестве объекта специфических мембранных пектинов, которые находятся в специфических тканях и которые специфическим образом распознают либо галактозу - в случае печени, кости, определенных раковых опухолей; либо маннозу - в случае макрофагов, сердца; либо сиаловую кислоту - в случае эритроцитов, и т.д.), небольшие молекулы-эффекторы (небольшая молекула, концентрация которой регулирует активность молекулы определенного белка путем взаимодействия со специфическим участком связывания на молекуле белка и изменения его структуры (Айала Ф., Кайгер Дж. «Современная генетика». Том 3, стр.318)), быть гормональным по природе (как, например, стероиды), быть синтетическим по природе, как, например, Gleevek для определения в качестве объектов киназ, специфические антитела, фрагменты антител, антиген, биотин, который связывает определенные специфические белки, и, в более общем случае, представлять собой любой субстрат, для которого предшествующие исследования показали распознаваемую специфичность. Среди пептидов, которые могут быть использованы в настоящем изобретении, можно упомянуть, например, RGD-последовательность, известную благодаря своему сродству к αVβ3 интегринам.
Можно представить, что та же самая молекула формулы (II) содержит одну или несколько идентичных групп распознавания R2 или больше различных групп распознавания R2, которые дают возможность направлять частицы к нескольким отдельным биологическим мишеням.
- R группа подчиняется тем же правилам, что и определены выше для структуры соединения формулы (I).
Z представляет собой «ножку» (spacer arm), которая соединяет группу распознавания R2 с полимерной цепью. Z связана с R2 при помощи связи, которая может быть выбрана из функций
-О-СО-, -СО-NH-, -NH-CO-NH-, -NH-CO-O-, O-CO-O-, -O-, -CH=N- или -S- или за счет образования комплекса с атомом никеля (WoodleChikh et Lasical., Biochim. Biophys. Acta, 1113 (1992) 171-1999, Acta, 1567 (2002) 204-212). Последний может связываться, во-первых, с полигистидиновой меткой, присоединенной к агенту, определяющему объект, и, во-вторых, - с поликислотой типа NTA, присоединенной к полимерной цепи.
«Ножка» Z может состоять из белковой цепи. Последняя может быть присоединена к олигомерной цепи при помощи концевой аминогруппы боковой цепи или основной цепи. Эта «ножка» включает от 1 до 5 аминокислот, предпочтительно от 1 до 3 аминокислот.
Аминокислоты, составляющие «ножку» Z, выбирают из природных аминокислот, таких как аланин, аргинин, аспарагин, аспарагиновая кислота, цистеин, глутамин, глутаминовая кислота, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин или валин, или синтетических аминокислот, таких как гидроксипролин, норлейцин, орнитин, цитруллин или циклогексилаланин. Эта «ножка» Z может состоять из тирозинового остатка, который дает возможность отслеживать вектор in vivo после введения метки с 125I или 131I.
В качестве группы Z можно также предположить использование Ω-аминокислот, таких как 3-аминопропионовая кислота и 4-аминомасляная кислота, а также этаноламина, 3-пропаноламина или диаминов формулы -NH-(CH2)r NH-, в которых r представляет собой целое число в диапазоне от 2 до 6.
Или Z-R2 группа представляет собой группу NTA, и, если происходит связывание за счет образования комплекса с атомом никеля, Z-R2 группа состоит из группы NTA формулы:
Согласно первому варианту изобретения, который касается липосом, полученных из молекул формулы (IA), предпочтительные соединения формулы (II) представляют собой соединения формулы (IIA) ниже:
в которой X, n, z, y, R, R1 и R2 имеют те же значения, что и выше в формуле (II);
- предпочтительно x и y не представляют собой ноль одновременно;
- п