Способ получения синтез-газа и продуктов органического синтеза из диоксида углерода и воды
Иллюстрации
Показать всеИзобретение относится к области химии. Диоксид углерода выделяют из исходной газовой смеси и концентрируют в абсорбере 9 жидкими поглотителями на основе аминов, которые регенерируют сухими парами воды с температурой 170…190°С в десорбере 12. Десорбированный диоксид углерода осушают конденсацией паров воды. Полученную воду в жидкой фазе подают в электролизер 20 для получения кислорода на аноде и водорода на катоде. После осушки диоксид углерода смешивают с полученным водородом в мольном соотношении Н2:CO2=(2,1…3,2) и восстанавливают диоксид углерода водородом при температуре от 600 до 800°С в аппарате 27 до получения синтез-газа состава Н2:СО=2…2,3 и паров воды. Полученный синтез-газ осушают конденсацией паров воды и затем подвергают абсорбционной очистке от остаточного диоксида углерода в аппарате 29, добавляют в него водород и проводят экзотермическую реакцию каталитической конверсии, например, типа Фишера-Тропша при температуре от 170 до 190°С в аппарате 31 для получения газообразных углеводородных продуктов и жидкого моторного топлива. Теплоту реакции конверсии синтез-газа отводят и утилизируют для испарения воды и генерации сухих паров, которые направляют на регенерацию абсорбента в процессе концентрирования диоксида углерода из исходной газовой смеси. Полученные товарные продукты - газообразные углеводородные продукты, жидкое моторное топливо и электролизный кислород направляют потребителю. Изобретение позволяет увеличить производительность процесса, сократить себестоимость процесса, расширить область применения за счет утилизации диоксида углерода из промышленных газовых выбросов и из окружающей атмосферы. 2 з.п. ф-лы, 7 ил.
Реферат
1. Изобретение относится к области химических технологий получения синтез-газа и синтетических углеводородных продуктов и, в частности, к способам получения синтез-газа с использованием в качестве исходного сырья продуктов окисления (сгорания) углеводородных веществ - диоксида углерода и воды.
Известны способы получения синтез-газа для дальнейшего производства продуктов органического синтеза и углеводородного топлива, включающие в себя конверсию исходных углеводородных веществ (природного газа, нефтепродуктов, углей) водяным паром или парокислородную конверсию [1], [2].
Общим недостатком этих способов является необходимость расходования в качестве исходного сырья естественных углеводородных запасов, являющихся невозобновляемым природным ресурсом. Но, кроме того, данные способы являются источниками выбросов в атмосферу диоксида углерода, который образуется частично как в самих реакциях, так и при сжигании топлив и генерации тепловой энергии, необходимой для осуществления указанных сильно эндотермических процессов. Например, при получении синтез-газа переработкой метана СН4 для энергообеспечения реакции (-57,2 Вт·ч/моль):
СН4+H2O⇔СО+3H2-57,2 Вт·ч/моль
требуется сжигание топлива в количестве, дающем удельный выброс CO2 в атмосферу до 0,7 кг СО2 на 1 кг переработанного СН4.
Ограничение промышленных выбросов СО2 в атмосферу («парниковых» газов) является в настоящее время основной задачей международных соглашений по Киотскому протоколу к рамочной Конвенции ООН «Об изменении климата», подписанному Россией. При этом выбросы CO2 в атмосферу промышленными источниками строго квотируются в ряде развитых стран. Наряду с этим рядом международных экоохранных проектов ставятся задачи создания технологий извлечения и утилизации накопленных в земной атмосфере запасов избыточного диоксида углерода (около 500 млрд т), находящегося в сильно разбавленном состоянии (0,034…0,038% объемных), а также экологические задачи очистки локально загрязненных атмосфер промышленных зон, мегаполисов, производственных объектов и помещений, содержащих диоксид углерода в концентрациях до 0,3…0,6%.
2. Указанный недостаток устраняется в известном способе [3] получения синтез-газа, в котором в качестве исходного сырья используют окисленные продукты сгорания (переработки) углеродосодержащих веществ - диоксид углерода и воду, представляющими собой «парниковые» газы атмосферы.
Технология способа включает две основные стадии: извлечение диоксида углерода из промышленных газовых выбросов (дымовых газов) с содержанием СО2 не менее 7% объемных методом мембранного газоразделения с выделением его в среду паров воды (либо вакуумной откачкой), создание парогазовой смеси с составом «пары воды/диоксид углерода» в диапазоне 1,0…2,3, и вторую стадию процесса: электрохимическое восстановление парогазовой смеси в газофазном высокотемпературном электролизере с твердым оксидным электролитом при температуре 1120…1220°К до получения на катоде электролизера синтез-газа с заданным составом Н2/СО в диапазоне 1,0…2,3, а на аноде электролизера - чистого кислорода. Полученный синтез-газ направляют потребителю на синтез углеводородов.
3. Однако данный способ и используемые в его стадиях технические средства реализации способа имеют существенные недостатки, значительно затрудняющие практическое промышленно-масштабное внедрение способа и связанные с высокими технологическими сложностями создания промышленного аппаратурного оформления способа и с высокими капитально-стоимостными затратами на реализацию способа, которые рассматриваются ниже.
3.1. Стадия выделения диоксида углерода
В данной стадии капитально-стоимостные затраты связаны в основном со стоимостью газоселективных мембран и определяются удельной поверхностью газоразделительных мембран, необходимой для выделения единицы объема концентрированного диоксида углерода в час - f, м2/м3 СО2·ч-1.
Энергозатраты в способе на откачивание диоксида углерода из подмембранного пространства водяным паром как при атмосферном давлении, так и при пониженном давлении вакуумной откачки, прямо пропорциональны удельным расходам пара на обеспечение концентрирования из исходной смеси единицы объема диоксида углерода vп, м3 пара/м3 СО2.
Указанные величины, имея приемлемые значения в зоне средних концентраций СО2, характерных для промышленных газовых (дымовых) выбросов (более 7%), как показывает анализ, гиперболически возрастают при переходе в зону низких концентраций СО2. (0,1…1%), имеющих место в целом ряде практически важных задач по очистке локально загрязненных производственных и экологически неблагоприятных атмосфер промышленных зон, мегаполисов и т.п.
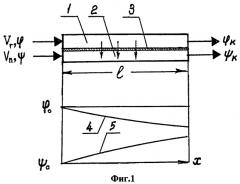
Количественно этот вывод следует из анализа процессов мембранной сепарации диоксида углерода. Этот процесс описывается уравнениями:
- баланса массы по СО2. в надмембранном потоке исходной газовой смеси:
- баланса массы по СО2. в подмембранном паровом потоке:
- интегрального баланса по CO2. в надмембранной и подмембранной полостях:
при краевых условиях:
где (см. фиг.1)
1 - надмембранный канал;
2 - подмембранный канал;
3 - газоселективная мембрана;
4 - объемная концентрация СО2 в потоке газовой смеси над мембраной φ;
5 - концентрация СО2 в потоке водяного пара под мембраной ψ;
vг - общий расход исходной газовой смеси над мембраной, м3 ч-1;
φ0, φк - начальная и конечная объемная концентрация CO2. в исходной смеси;
vп - расход пара в подмембранном канале, м3 ч-1;
ψО, ψк - начальная и конечная концентрация сепарированного CO2. в паровом потоке;
h, l - ширина и длина канала разделения (h·l = F - площадь поверхности мембраны);
Po - общее давление смеси;
k - коэффициент проницаемости мембраны по СО2, м3/м2 ч-ат.
Решение уравнений дает выражения для удельной величины поверхности мембран f=F/ΔvCО2 и удельного расхода пара vп=vп/ΔvCО2, где ΔvCО2=vг(φо-φк) - объемный расход сепарированного диоксида углерода:
где η=(φк-Ψк)/(φо-Ψo)=(1+vг/vп)(φо-φк)/φо - степень использования потенциала переноса СО2 через мембрану, т.е. разницы парциальных давлений СО2 на мембране по ходу потоков (фиг.1).
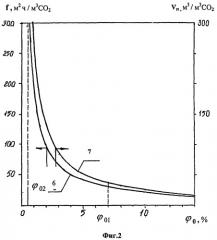
Зависимости (5), (6) приведены на фиг.2 для средних значений величин параметров:
k=1 м3 CO2/м2·ч·aт; Po=1 ат = 0,1 МПа; vп\vг=2; η=0,8.
Из анализа зависимостей (5), (6) следует, что если в диапазоне исходных концентраций СО2 в газовой смеси φо≥7% объемных требующаяся удельная поверхность газоразделительных мембран f, м2/м3 CO2-ч-1 и удельный расход пара vп, м2/м3 CO2-ч-1 относительно невелики, то с переходом в зону концентраций диоксида углерода в исходной смеси φо≤1% эти показатели экономических затрат процесса гиперболически возрастают (в 10…15 раз).
Данная особенность процесса выделения диоксида углерода в способе-прототипе ограничивает область практического применения способа газовыми выбросами промышленности (топливно-энергетического, химического и металлургического комплексов), т.е. концентрированными сырьевыми источниками CO2.
3.2. Стадия восстановления СО2 и Н2О
Существенные недостатки имеет вторая стадия способа - высокотемпературное электрохимическое восстановление диоксида углерода и воды. Процесс проводят в газофазном электролизере с элементами на основе твердого окисно-циркониевого (керамического) электролита, имеющими каталитически активные газодиффузионные электроды - катод и анод, которые выполняют в виде тонкопленочных дисперсно-пористых покрытий из платины, наносимых на поверхности твердого электролита [5], [6].
Особенностями электрохимических элементов данного типа, выполняемых обычно в виде тонкостенных керамических колец и трубок, являются низкие физико-механические свойства (хрупкость) элементов и чувствительность к термоудару (при попадании капельной воды).
Низкая электропроводность дисперсно-пористых электродов вдоль поверхности принципиально ограничивает размеры рабочей поверхности единичных элементов величиной от нескольких см2 до десятков см2 и требует для достижения промышленных мощностей (куб. метры газов в час) количества элементов до нескольких тысяч в одной батарее электролиза с соответствующим количеством электронно-проводящих, «биполярных» стыков между ними. Указанные «биполярные» стыки должны быть полностью герметичны, разделяя полости со взрывоопасными компонентами (кислород - водород), и с учетом высокой рабочей температуры (+850°С) и окислительной среды должны выполняться из металлов платиновой группы.
Данные особенности определяют высокую технологическую сложность и трудоемкость изготовления электролизеров данного типа, выдвигают проблемы надежности, взрыво- и пожаробезопасности, ресурса, требуют повышенного расхода драгметаллов на изготовление (до 120 мг платины на см2 рабочей поверхности электролизеров [5], [6]) и приводят к себестоимости изготовления высокотемпературных электролизеров, на порядки превышающей данные показатели для существующих промышленных электролизеров.
Рассмотренные конструкторско-технологические и технико-экономические недостатки средств реализации способа значительно затрудняют его промышленное внедрение и являются основной причиной того факта, что существующие в мировой практике разработки в области высокотемпературных газофазных электролизеров ограничиваются стадией создания отдельных экспериментальных образцов и до настоящего времени не получили промышленного освоения.
4. С целью устранения указанных недостатков предлагается:
1. Способ получения синтез-газа и продуктов органического синтеза на основе переработки окисленных продуктов - диоксида углерода и воды, включающий выделение и концентрирование диоксида углерода из исходных газовых смесей - сырьевых источников диоксида углерода и восстановление окисленных продуктов до синтез-газа с использованием электрохимических процессов, отличающийся тем, что диоксид углерода выделяют из исходной газовой смеси и концентрируют методом абсорбции жидкими поглотителями на основе аминов, которые регенерируют парами воды с использованием тепловой энергии экзотермических процессов способа с температурным уровнем 170…190°С, десорбированный диоксид углерода осушают конденсацией паров воды; окисленные продукты восстанавливают в раздельных, последовательно осуществляемых процессах; воду электрохимически восстанавливают в жидкой фазе процессом низкотемпературного электролиза до получения кислорода на аноде и водорода на катоде, выделенный диоксид углерода смешивают с полученным водородом в мольном соотношении с избытком водорода Н2:CO2=(2,1…3,2) и проводят в полученной смеси реакцию химико-каталитического восстановления диоксида углерода водородом при температуре от 600 до 800°С до получения синтез-газа с составом Н2:СО=2…2,3 и паров воды, полученный синтез-газ осушают конденсацией паров воды, регулируют по составу в заданном диапазоне путем абсорбционной очистки от остаточного диоксида углерода и добавления водорода и проводят в нем экзотермическую реакцию каталитической конверсии, например, типа Фишера-Тропша на температурном уровне от 170 до 190°С до получения углеводородных продуктов и жидкого моторного топлива, при этом теплоту реакции конверсии синтез-газа отводят и утилизируют путем испарения воды и генерации сухих паров, которые направляют на регенерацию абсорбентов в процессе концентрирования диоксида углерода из исходной газовой смеси, полученные товарные продукты - углеводородные продукты, жидкое моторное топливо и электролизный кислород направляют потребителю.
2. Способ по п.1, отличающийся тем, что диоксид углерода выделяют из исходной газовой смеси, которую забирают из промышленных газовых выбросов в атмосферу с содержанием диоксида углерода от 7 до 90% объемных и производственно загрязненных атмосфер с содержанием диоксида углерода от 0,25 до 0,35% объемных, выделение и концентрирование диоксида углерода осуществляют процессом абсорбции жидкими поглотителями на основе этаноламинов, например моноэтаноламина, при температурах от 20 до 30°С, а процесс десорбции диоксида углерода проводят на температурном уровне от 110 до 130°С.
3. Способ по п.1, отличающийся тем, что диоксид углерода выделяют из исходной газовой смеси, которую забирают из окружающей воздушной атмосферы с содержанием диоксида углерода от 0,034 до 0,038% объемных, выделение и концентрирование диоксида углерода осуществляют процессом абсорбции жидкими поглотителями на основе полиаминов, например диамина, при температурах от 30 до 40°С, процесс десорбции диоксида углерода проводят на температурном уровне от 140 до 150°С и доочищают диоксид углерода диффузией через газоселективные мембраны.
5. Существо изобретения
5.1. Целью изобретения является устранение рассмотренных в п.3.1, п.3.2 недостатков прототипа, затрудняющих его промышленную реализацию - снижение температурного уровня электрохимических процессов и обеспечение простоты конструкции и технологии средств реализации способа, повышение их надежности и эксплуатационной безопасности, сокращение расхода драгоценных металлов в конструкции и себестоимости изготовления средств способа, а также расширение диапазона применения способа.
Указанные цели достигаются в изобретении на основе предлагаемых особенностей осуществления предлагаемого способа в его последовательных стадиях концентрирования и переработки диоксида углерода и воды, которые составляют совокупность существенных признаков способа, излагаемых ниже.
5.2. Существенные признаки изобретения
5.2.1. В отличие от прототипа диоксид углерода (СО2) из исходной газовой смеси извлекают процессом селективной абсорбции с помощью жидких регенерируемых поглотителей на основе аминов [4].
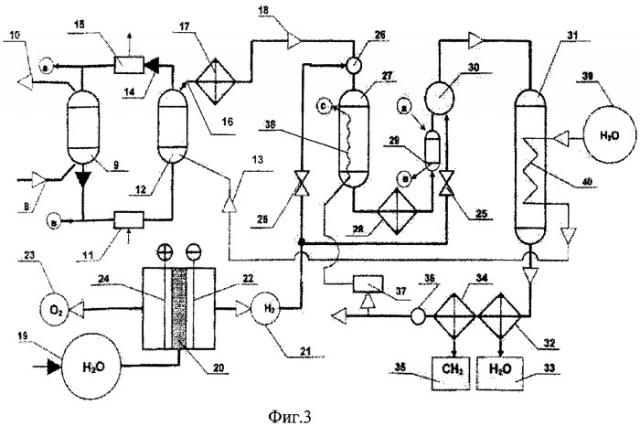
а) Процесс осуществляют по циклу «абсорбция-десорбция CO2» (фиг.3):
- исходную газовую смесь (8) при атмосферном давлении непрерывно пропускают через зону контактного массообмена с абсорбентом в абсорбере (9) при температуре абсорбции ta, обедненную по содержанию СО2 исходную газовую смесь выбрасывают в атмосферу (10);
- насыщенный диоксидом углерода абсорбент нагревают (11) до температуры десорбции tд>ta и направляют на десорбцию (12), которую осуществляют путем продувки абсорбента и контактного массообмена его с сухим водяным паром (13);
- регенерированный абсорбент (14) охлаждают до температуры абсорбции ta (15) и возвращают на процесс абсорбции диоксида углерода (9).
В процессе регенерации абсорбента и концентрирования СО2 парциальное давление СО2 доводят до величины не менее атмосферного давления.
Десорбированный диоксид углерода 16 подвергают осушке 17 путем конденсации паров воды при температурах теплоотвода в наружную среду (например, воздушным охлаждением при 30…40°С) и направляют на переработку в последующую стадию способа.
Отличительной особенностью способа является то, что тепловую энергию, необходимую для генерации сухих паров воды и осуществления процесса десорбции CO2 и составляющую 1700…1800 ккал/нм3СО2 (38…40 ккал/моль СО2) - см.[4], в способе получают утилизацией тепловой энергии с температурным потенциалом 170…190°С, которая выделяется в экзотермической реакции переработки СО2 в конечные органические продукты (см. ниже п.5.2.3), т.е. процесс осуществляют без затрат внешней тепловой энергии.
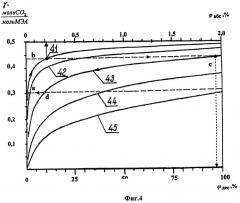
Принципиальный цикл процесса выделения и концентрирования диоксида углерода приведен на диаграмме фиг.4 в виде зависимостей степени карбонизации абсорбента γ (т.е. содержания растворенного СО2 в абсорбенте γ, моль СО2/моль абсорбента) от парциального давления диоксида углерода в газовой смеси р над поверхностью жидкого абсорбента.
На фиг.4 парциальные давления даны в виде отношения к общему давлению Ро смеси φ=(р/Ро), т.е. соответствуют объемному (процентному) содержанию диоксида углерода в газовой смеси, при этом:
- верхняя шкала соответствует содержанию диоксида углерода в исходной газовой смеси φо и относится к изотермам абсорбции (41, 42) - φабс=(рабс/Ро)·100%,
- нижняя шкала соответствует содержанию диоксида углерода в парогазовой смеси после десорбции и относится к изотермам десорбции (43, 44, 45) - φд=pд/Ро·100%.
Здесь рабс, рд - равновесные парциальные давления СО2 над поверхностью жидкого абсорбента соответственно при температуре абсорбции ta (кривая 41) и температуре десорбции tд (кривая - 43), а Ро=105 Па - общее давление газовой смеси, равное атмосферному.
Участки цикла на фиг.4:
ab - насыщение абсорбента диоксидом углерода в процессе абсорбции от начального состояния с γа до степени карбонизации γb, равновесной с объемной концентрацией (парциальным давлением) диоксида углерода в исходной газовой смеси φb=φо;
bc - процесс нагревания абсорбента от температуры абсорбции tабс до температуры десорбции tд при постоянной карбонизации γс=γb;
cd - процесс десорбции СО2 из абсорбента сухим водяным паром при постоянной температуре tд с уменьшением карбонизации абсорбента от γс до γd и равновесного парциального давления СО2 над абсорбентом от рс до pd; при противотоке фаз абсорбент - пар в десорбере 12 точка с на диаграмме фиг.4 соответствует параметрам парогазовой смеси на выходе из десорбера - парциальному давлению рс и объемному содержанию диоксида углерода φс=pc/P0 в смеси;
da - охлаждение абсорбента до температуры t=tабс абсорбции с понижением равновесного парциального давления и объемной концентрации СО2 в газовой смеси над поверхностью абсорбента до φа.
В процессе нагревания абсорбента на основе аминов от температуры абсорбции tабс до температуры десорбции tд, например на (tабс-tд)=100°С, достигается повышение парциального давления от исходного рс/pb в 250…350 раз [4], что обеспечивает концентрирование СО2 до давления рс не менее атмосферного.
Полученный на выходе десорбера 12 влажный диоксид углерода 16 нагнетают на осушку в теплообменнике-конденсаторе 17 путем конденсации паров воды при температурах воздушного охлаждения (30…40°С) и направляют на переработку в последующую стадию способа - восстановление диоксида углерода.
5.2.2. Принципиальной особенностью предлагаемого способа является то, что восстановление исходных окисленных продуктов - диоксида углерода и воды - осуществляют в двух раздельных, последовательно проводимых процессах (фиг.3):
а) воду 19 электрохимически восстанавливают в жидкой фазе процессом низкотемпературного электролиза 20 (при температурных уровнях данного типа электролиза +40…+70°С) до получения водорода 21 на катоде 22 и кислорода 23 на аноде 24:
(здесь nэл - удельный расход электроэнергии на электролиз, который составляет 7,0…7.2 кВт·ч/кг кислорода в случае использования низкотемпературных электролизеров с жидким щелочным электролитом и 6.5…6,7 кВт·ч/кг кислорода для более экономичных электролизеров с твердым полимерным электролитом [6], [7], [8]);
б) очищенный диоксид углерода 18 смешивают с полученным водородом 21 в мольном соотношении с коэффициентом избытка водорода:
и в полученной смеси проводят реакцию химического восстановления диоксида углерода 27 при температурах 600…800°С в присутствии катализатора с подводом 38 тепловой энергии до получения оксида углерода и воды (в стехиометрической записи):
(25 - кран-регулятор подачи водорода);
в) основные режимные параметры процесса восстановления СО2: коэффициент стехиометрического избытка водорода в исходной смеси и температурный уровень реакции (9) TP устанавливают, исходя из:
- минимизации остаточного содержания диоксида углерода в продуктах реакции φСО2=рСО2/Po, т.е. достижения максимальной степени конверсии kкон диоксида углерода в реакции (9):
kкон=(pCO2(o)-pCO2)/pCO2(o)=1-φCO2/φCO2(o)=1-φCO2(1+∝);
- получения смеси продуктов реакции - (СО+Н2), т.е. синтез-газа, с заданным составом рН2/рСО, необходимым для дальнейшего синтеза углеводородных продуктов [1], [2]:
где
рН2(о), pCO2(о) - парциальные давления водорода и диоксида углерода в исходной газовой смеси;
рН2, рСО2 - равновесные парциальные давления H2 и СО2 в продуктах реакции (8);
φCO2(о)=pCO2(о)/Ро и φCO2=рСО2/Ро - объемные доли СО2 в исходной смеси и в продуктах реакции;
Po - общее давление газовой смеси.
Равновесный состав продуктов реакции (8) определяется из условий:
- условия равновесия реакции (8):
- условия постоянства общего давления смеси газов:
- нормирующего условия - соотношения «водород-кислород» [Н:O] в смеси реагирующих газов, которое задают составом исходной смеси ∝:
- нормирующего условия по соотношению кислорода и углерода, заданного стехиометрией молекулы СО2:
где
- k(Tp) - константа равновесия реакции (9) - стандартная функция температуры реакции;
- рСО, рСО2, рН2, рН2О - равновесные парциальные давления продуктов реакции (9).
Состав продуктов реакции (9) приведен на фиг.5 в виде зависимостей остаточной концентрации диоксида углерода φСО2 (47) и соотношения «водород-оксид углерода» β=рН2/рСО (46) в продуктах реакции от режимных параметров реакции:
- коэффициента начального избытка водорода в исходной смеси
α - в диапазоне от 1,0 до 4,0;
- температурного уровня реакции tp в диапазоне от 500°С до 900°С.
Зависимости показывают, что остаточное содержание СО2 в синтез-газе интенсивно снижается и глубина конверсии диоксида углерода kкон возрастает с увеличением коэффициента начального избытка водорода α и с увеличением температуры реакции tP (9).
В способе рабочий диапазон режимных параметров ограничивают условием (10) получения синтез-газа заданного состава β и условием минимизации в полученном синтез-газе примесей остаточного диоксида углерода φCO2, содержание которого, как инертного газа, в последующем процессе синтеза углеводородов в способе ограничивается.
Рабочий диапазон режимных параметров способа выделен на фиг.5 и ограничен:
- по нижнему пределу температурным уровнем реакции tp(min)=600°С и коэффициентом избытка водорода αmin=2,1, поскольку при более низких значениях этих параметров существенно снижается глубина конверсии kкон и возрастает содержание остаточного СО2 φСО2;
- по верхнему пределу температуры величиной tp(max)=800°С, поскольку дальнейшее повышение температуры tр уже не дает заметного приращения глубины конверсии СО2, но приводит к существенному возрастанию термоконструкционных нагрузок химреакторов и оборудования;
- по верхнему пределу α коэффициентом αmax=3,2, поскольку превышение его будет приводить к получению синтез-газа с более высоким, чем βmax=2,3 содержанием водорода, и к бесполезным потерям избытка электролизного водорода в последующих реакциях способа.
При этом внутри рабочего диапазона зона температур реакции (9) 600…800°С граничные значения режимного параметра избытка водорода αmin(tp), αmax(tp) устанавливают для выбранного конкретного температурного уровня tp проведения реакции (8), исходя из условия (9) получения синтез-газа необходимого состава:
βmin=2, βmax=2,3.
Граничные значения αmin(tp), αmax(tp) вытекают из данных фиг.5 в виде линеаризированных зависимостей (см. фиг.6):
Например, для температурного уровня реакции tp=700°С рабочий диапазон составляет αmin=2,4, αmax=2,78 (см. фиг.6 и фиг.5).
г) Реакция (9) идет без изменения объема реагирующих газов и величина общего давления Ро газовой смеси не влияет на ее характеристики. В практическом проектировании конструкций реактора величину общего давления выбирают из общих проектно-технологических соображений (сокращения объема и металлоемкости реактора, увеличения удельной объемной нагрузки реактора и т.п.) и устанавливают в диапазоне умеренных давлений - 0,5…1,5 МПа. В состав нормируемых режимных параметров способа данная технологическая величина общего давления Ро не входит.
д) Полученный синтез-газ осушают конденсацией паров воды 28 (при температурах промышленного, воздушного охлаждения +30…+40°С); окончательно кондиционируют по составу 30 в заданном диапазоне β добавлением электролизного водорода 25 и абсорбцией остаточного диоксида углерода 29 (аналогично основной операции 9), и направляют на дальнейшую переработку. Регенерированный абсорбент на операцию очистки 29 от остаточного диоксида углерода отбирают от входа а в абсорбер 9 и возвращают на вход b десорбера 12 контура концентрирования СО2.
5.2.3. В завершающей стадии способа синтез-газ конвертируют в продукты органического синтеза:
а) Конверсию осуществляют, например, в жидкие углеводороды и синтетическое топливо процессом Фишера-Тропша [2], который проводят 31 (фиг.3) в присутствии катализатора при температуре +170…+190°С до получения предельных углеводородов по экзотермической реакции:
а также непредельных углеводородов:
При этом в продуктах реакции около 80…85% весовых составляют жидкие фракции углеводородов и около 15…18% - газообразные углеводороды (метан, частично этан, этилен и т.п.).
Пары воды 33 отделяют конденсацией 32, жидкие фракции 35 отделяют конденсацией 34.
Часть газообразных углеводородов 36 отбирают на сжигание с воздухом 37 для компенсации 38 затрат тепловой энергии в слабо эндотермической реакции (9): CO2+Н2⇔СО+Н2О - 10 ккал/моль. Сжигание происходит по экзотермической реакции с тепловым эффектом 192 ккал/моль:
Количество сжигаемых газообразных углеводородов (метана) в расчете по тепловому балансу на 1 моль СО2, переработанного в реакции (9), при этом составляет:
(СН4/CO2)=(10/192)=0,05 моля CH4 на моль переработанного CO2, т.е. не более 5% от общего количества углеводородов по реакциям (16) и не более 35…40% от образующихся газообразных углеводородов; при этом относительное количество выделяемого диоксида углерода в реакции (17) составляет соответственно не более 5% от количества исходного, перерабатываемого в способе CO2.
С учетом относительно невысоких затрат тепловой энергии на реакцию (9) - около 7% от основных затрат на электролиз воды, в качестве альтернативного варианта подогрева в способе данные затраты компенсируют электроподогревом реактора 66.
Теплоту экзотермических реакций (16) отводят путем испарения охлаждающей воды 39, которую пропускают по каналам парогенератора 40 через реакционную зону 31 с регулируемыми расходом и давлением, обеспечивающими заданный температурный уровень реакций (16). Полученный сухой пар 16 направляют на процесс 12 десорбции диоксида углерода и регенерации абсорбента для обеспечения данного процесса необходимой тепловой энергией - 38…40 ккал/моль СО2 [4].
Основным конечным продуктом данного, завершающего процесса способа является жидкое моторное топливо, в частности высокоцетановое дизельное топливо, отвечающее европейским стандартам качества, а также автомобильный бензин.
б) Стадия конверсии синтез-газа в способе может также осуществляться по альтернативному варианту процесса - конверсии в жидкие кислородосодержащие органические продукты, например метанол и другие спирты.
Процесс проводят при высоком давлении 6…7 МПа и на температурном уровне 280…360°С в присутствии катализатора [2] с выходом (до 90…95%) метанола:
Метанол является альтернативным видом жидкого моторного топлива и интермедиатом для производства серии продуктов органической химии.
Аналогично осуществляют вариант процесса - синтез диметилэфира - наиболее экологичного вида синтетического жидкого моторного топлива:
5.3. Способ осуществляют со следующими особенностями в частных областях его применения:
5.3.1. Исходную газовую смесь 8 (фиг.3) забирают из промышленных газовых выбросов диоксида углерода (топливно-энергетической, металлургической и химической промышленности) с высокой концентрацией φо от 7% до 95%, а также из загрязненных атмосфер производственных помещений, промышленных зон, мегаполисов, имеющих содержание диоксида углерода φо от 0,25% до 0.35% объемных, близкое к уровню или на уровне предельно допустимых концентраций (ПДК) диоксида углерода φПДК=0,79%.
Выделение диоксида углерода из исходной газовой смеси осуществляют процессом абсорбции 9 жидкими регенерируемыми поглотителями на основе этаноламинов, например моноэтаноламина (МЭА) [4], при температурах 20…30°С, а процесс десорбции 12 и концентрирования диоксида углерода проводят на температурном уровне от 110 до 130°С. Примеры равновесных кривых для МЭА даны на фиг.4, где 41 - 30°С, 42 - 40°С (изотермы абсорбции СО2), 43 - 100°С, 44 - 120°С, 45 - 140°С (изотермы десорбции СО2) [4].
На изотерме абсорбции +20°С начальной а и конечной b точкам процесса поглощения СО2 абсорбентом при степени карбонизации МЭА γ=0,45 моль CO2/моль МЭА соответствуют парциальные давления диоксида углерода ра=7,4 Па и pb=200 Па, что позволяет извлекать диоксид углерода из исходной газовой смеси с содержанием φо=pb/P0 от 0,2% объемных и выше.
На изотерме +30°С (поз.41 на фиг.4) парциальные давления составляют соответственно ра=13 Па и pb=333 Па, что позволяет извлекать диоксид углерода из исходной газовой смеси с содержанием φCO2(о) от 0,33% объемных и выше.
Температурный диапазон процесса абсорбции (20…30°С) устанавливают, исходя из возможностей промышленного градирно-воздушного охлаждения потоков абсорбента и исходной газовой смеси.
Процесс десорбции диоксида углерода осуществляют на температурном уровне от tд=+110°С до +130°С, что соответствует равновесному парциальному давлению рс диоксида углерода на выходе из десорбера 12 (фиг.3) при противотоке фаз «абсорбент - сухой пар» в десорбере (см. точка с на фиг.4) от 0,139 до 0,4 МПа, т.е. обеспечивает необходимое концентрирование диоксида углерода до давления не менее атмосферного (0,1 МПа). Этим условием определяют нижний предел температуры десорбции 110°С.
Верхний предел tд=130°С определяют температурным уровнем источника тепловой энергии - реакции (15), составляющим 170…190°С, и необходимым запасом перепада температур на перегрев водяного пара в парогенераторе 40 реактора 31 (фиг.3), а также неоправданным повышением парциального давления паров МЭА и уносом его с диоксидом углерода при дальнейшем повышении температуры десорбции.
При использовании исходных газовых смесей, из промышленных газовых выбросов с высокой концентрацией диоксида углерода от 7% объемных и выше степень карбонизации абсорбента γ при температурах абсорбции 20…30°С составляет до 0,5 моль СО2/моль МЭА, а равновесное давление рс диоксида углерода на изотермах десорбции 110…130°С достигает 0.24…0.5 МПа, т.е. заведомо превышает атмосферное и удовлетворяет условию концентрирования СО2.
Полученный диоксид углерода осушают конденсацией паров воды в теплообменнике 17 и направляют на дальнейшую переработку в способе.
В качестве варианта абсорбента в указанном процессе могут также использоваться амины - диэтаноламин и триэтаноламин с более высокой молекулярной массой и несколько большим равновесным давлением СО2.
5.3.2. Исходную газовую смесь забирают из окружающей воздушной атмосферы с естественным содержанием диоксида углерода φСО2(о) от 0,034 до 0,038% объемных.
Выделение диоксида углерода из исходной газовой смеси осуществляют процессом абсорбции 9 жидкими регенерируемыми поглотителями на основе полиаминов, например диамина [4], при температурах от 30 до 40°С, а процесс десорбции 12 и концентрирования диоксида углерода проводят на температурном уровне от 140 до 150°С.
Данный тип поглотителей имеет в 6 раз меньшее равновесное давление диоксида углерода при тех же температурах абсорбции по сравнения с этаноламинами.
Абсорбцию СО2. осуществляют диамином при температурах 30…40°С, при этом давление диоксида углерода в конце процесса абсорбции (точка b фиг.4) составляет от 13 до 30 Па [4], что соответствует объемной концентрации диоксида углерода над поверхностью диамина 0,013…0,03% и позволяет извлекать диоксид углерода из воздушной атмосферы.
Равновесное давление диоксида углерода в конце процесса десорбции при назначенных температурах 140…150°С составляет от pc=0,079 до 0,12 МПа [4].
Полученную, обогащенную диоксидом углерода парогазовую смесь нагнетают на осушку от паров воды, подвергают доочистке и дополнительному концентрированию диффузионным пропусканием через газоселективные мембраны (см. ниже фиг.8).
При этом следует отметить, что в силу абсорбционного концентрирования диоксида углерода диамином от φо=0,034…0,038% до уровня не ниже φ2=pc/P0=79% требующаяся рабочая поверхность газоразделительных мембран в предлагаемом способе в отличие от операции прямого мембранного газоразделения в способе-прототипе принципиально сокращается как минимум на два порядка (ср. φ2=0,03% и φ1=79% на фиг.2).
В качестве альтернативного абсорбента в данной операции могут также использоваться полиамины - гексаметилендиамин или диэтилентриамин, имеющие несколько более высокую (на 10…15%) абсорбционную емкость по сравнению с диамином [4].
Режимные параметры процесса - температурный уровень процесса абсорбции tабс=30…40°С устанавливают, исходя из возможностей промышленного воздушного охлаждения потоков абсорбента и исходной газовой смеси. Верхний предел температуры десорбции определяют температурным уровнем источника тепловой энергии - реакции (15) способа (170…190°С) и необходимым запасом перепада температур 20…40°С на перегрев водяного пара в реакторе 40 (фиг.3).
5.4. Показатели экономической эффективности способа
Все конечные продукты способа - жидкое углеводородное (моторное) топливо и кислород - являются прямой товарной рыночной продукцией, что позволяет непосредственно оценить конкретные показатели экономической эффективности предлагаемого способа при внедрении в промышленное производство.
Источником прибыли при эксплуатации внедренного способа является разность стоимости реализуемых продуктов (выручки В) и стоимости затрат на