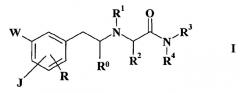
2-фенилэтиламинопроизводные в качестве модуляторов кальциевых и/или натриевых каналов
Иллюстрации
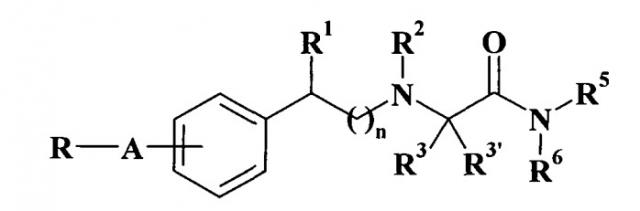
Показать всеИзобретение относится к новым 2-фенилэтиламинозамещенным производным карбоксамидов формулы (I)
где J, W, R, R0, R1, R2, R3 и R4 имеют значения, такие, как определено в п.1 формулы изобретения, и их фармацевтически приемлемым солям, фармацевтическим композициям, содержащим их в качестве модуляторов натриевых и/или кальциевых каналов для предупреждения, ослабления и лечения широкого спектра патологий, включающих неврологические, психические, сердечно-сосудистые, воспалительные, офтальмологические, урологические и желудочно-кишечные заболевания. 2 н. и 20 з.п. ф-лы, 1 ил., 10 табл.
Реферат
Настоящее изобретение относится к фенилэтиламинопроизводным, их фармацевтически приемлемым солям, фармацевтическим композициям, содержащим такие производные, и к их применению в качестве модуляторов натриевых и/или кальциевых каналов.
Фенилэтиламинопроизводные, являясь объектом настоящего изобретения, действуют как активные модуляторы кальциевых и/или натриевых каналов и, следовательно, применимы для предупреждения, ослабления и лечения широкого круга патологий, включающих, но без ограничения, неврологические, психические, сердечно-сосудистые, воспалительные, офтальмологические, мочеполовые и желудочно-кишечные заболевания, где вышеупомянутые механизмы описаны как играющие патологическую роль.
Соединения по настоящему изобретению по существу не обладают никаким ингибирующим действием в отношении МАО (моноаминоксидазы) или проявляют значительно уменьшенное ингибирующее действие на МАО в дозах, которые являются терапевтически эффективными для предупреждения, ослабления и/или лечения вышеуказанных заболеваний.
УРОВЕНЬ ТЕХНИКИ
Уровень техники (химия)
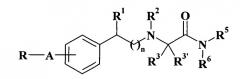
Патентная заявка WO 90/14334 описывает монозамещенные N-фенилалкил-альфа-аминокарбоксамидные производные общей формулы
где
R представляет собой (C1-C8)алкил, (C3-C8)циклоалкил, фурил, тиенил, пиридил или фенильное кольцо, необязательно замещенное 1-4 заместителями, независимо выбранными из галогена, (C1-C6)алкила, (C1-C6)алкокси и трифторметила; A представляет собой -(CH2)m-, -(CH2)p-X-(CH2)q-группу, в которой m является целым числом от 1 до 4, один из р и q равен нулю, а другой равен нулю или представляет собой целое число от 1 до 4, Х представляет собой -O-, -S- или -NR4-группу, в которой R4 представляет собой водород или (C1-C4)алкил; n равно 0 или 1; каждый из R1 и R2 независимо представляет собой водород или (C1-C4)алкил; R3 представляет собой водород, (C1-C4)алкил, необязательно замещенный гидроксилом или фенилом, необязательно замещенным, как указано выше; R3' представляет собой водород или R3 и R3' вместе образуют (C3-C6)циклоалкильное кольцо; каждый из R5 и R6 независимо представляет собой водород или (C1-C6)алкил; и их применение в качестве противоэпилептических, антипаркинсонических, нейропротекторных, антидепрессивных, противоспазматических и/или снотворных средств.
Соединение 2-[2-[4-(3-хлорбензилокси)фенил]этиламино]ацетамид и его гидрохлоридная соль и их получение конкретно описаны в вышеупомянутой патентной заявке (см. также P. Pevarello and al., J. Med. Chem., 1998, 41, 579-590).
В WO 90/14334 упомянуты, но не охарактеризованы соединения (S)-2-[2-[4-бензилоксифенил]этиламино]ацетамид, (S)-2-[2-[4-(2-хлорбензилокси)фенил]этиламино]ацетамид, 2-[2-(4-бензилфенил)этиламино]ацетамид и 2-[2-(4-бензиламинофенил)этиламино]ацетамид.
В патентной заявке WO 04/089353 описаны способ и комбинированная терапия для лечения болезни Паркинсона с помощью сафинамида ((S)-(+)-2-[4-(3-фторбензилокси)бензиламино]пропанамида), производного сафинамида или ингибитора MAO-B вместе с антипаркинсоническими средствами. Соединение 2-[2-[4-(3-хлорбензилокси)фенил]этиламино]ацетамид приводится в качестве примера в этой заявке.
Вышеупомянутое соединение также получено и описано в качестве противосудорожного средства (Pevarello P., Bonsignori A., Dostert P., Heidempergher F., Pinciroli V., Colombo M., McArthur R.A., Salvati P., Post C., Fariello R.G., Varasi M.J. Med. Chem. (1998) 41: 579-590).
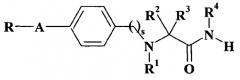
Патентная заявка WO 99/35125 описывает альфа-аминоамидные производные общей формулы
где R представляет собой фурил, тиенил, пиридил или фенильное кольцо; A представляет собой -(CH2)m-, -(CH2)n-X- или -(CH2)v-O- группу, в которой m представляет собой целое число от 1 до 4, n равно нулю или целому числу от 1 до 4, X представляет собой -S- или -NH- и v равно нулю или целому числу от 1 до 5; s равно 1 или 2; R1 представляет собой водород или (C1-C4)алкил; один из R2 и R3 представляет собой водород, а другой представляет собой водород или (C1-C4)алкил, необязательно замещенный гидрокси или фенилом; или R2 и R3 вместе образуют (C3-C6)циклоалкильное кольцо; или R2 и R3, оба, представляют собой метил; R4 представляет собой водород или (C1-C4)алкил; и их применение в качестве анальгетических средств.
В вышеуказанной патентной заявке упоминается соединение 2-[2-[4-(3-хлорбензилокси)фенил]этиламино]пропанамид.
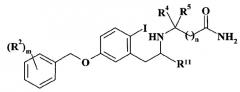
Патентная заявка WO 03/091219 описывает 5-(бензилокси)-2-(йодфенил)этиламинопроизводные (см. формулу XII), которые используют как промежуточные соединения при получении изохинолинов в качестве ингибиторов моноаминоксидазы В, применяемых против болезни Альцгеймера и сенильной деменции:
где, в частности, m равно 1, 2 или 3; R2 выбран из галогена, галоген(C1-C6)алкила, циано, (C1-C6)алкокси или галоген-(C1-C6)алкокси; R11 представляет собой водород; n равно 0, 1 или 2; R4 и R5 независимо выбраны из водорода, (C1-C6)алкила, -(CH2)р-OR8, -(CH2)р-SR8 или бензила, где p равно 1 или 2 и R8 представляет собой водород или (C1-C6)алкил.
В WO 99/26614 раскрываются замещенные 2-(бензиламино)ацетамиды и их применение для лечения нарушений, реагирующих на блокаду каналов ионов натрия, включающего предотвращение или облегчение невропатической боли.
WO 03/037865 относится к соединениям, применяемым в лечении рака, общей формулы
в которой обозначения R1, R2, R3, X, U и Y могут принимать широкий ряд значений. Хотя некоторые комбинации указанных широких родовых значений могли бы включать фенетиламинопроизводные, ни одно из соединений, описанных в настоящей заявке, в действительности не раскрывается в WO 03/037865.
Патент США № 5366982 (WO 92/01675) относится к соединениям, обладающим свойствами селективного антагониста лейкотриена B4 (LTB4), охватываемым общей формулой
в которой обозначения R, R', R2, R3, R4, X, Y, Z, W, n, m и Q могут принимать широкий ряд значений. Несмотря на то, что некоторые комбинации указанных родовых значений могли бы охватывать также фенетиламинопроизводные, в действительности ни одно из соединений, описанных в настоящей заявке, не раскрывается в патенте США № 5366982.
В WO 98/35957 раскрываются производные ацетамида, активные в качестве антагонистов нейропептидного Y рецептора, в частности, применяемые для лечения ожирения, общей формулы
в которой обозначения R1, R2, R3, R4 и R5 могут принимать широкий ряд значений. В действительности ни одно из соединений, описанных в настоящей заявке, не раскрывается в WO 98/35957.
В EP 1588704A описаны альфа-аминоамидные производные, включающие (S)-(+)-2-[4-(2-фторбензилокси)бензиламино]пропанамид, т.е. ралфинамид, для применения в лечении синдрома усталых ног.
WO 2005/018627 раскрывает альфа-аминоамидные производные, включая ралфинамид, для применения в качестве терапевтических противовоспалительных средств.
Уровень техники (биология)
Кальциевые каналы представляют собой мембранные, состоящие из многих субъединиц белки, которые делают возможным регулируемый вход кальциевых ионов в клетки из внеклеточной жидкости. Как правило, кальциевые каналы являются потенциалзависимыми и называются потенциалзависимыми кальциевыми каналами (VGCC). Каналы VGCC находят по всей нервной системе млекопитающих, где они регулируют внутриклеточные уровни ионов кальция, которые важны для жизнеспособности и функций клеток. Внутриклеточные концентрации ионов кальция тесно связаны с рядом жизненных процессов у животных, таких как высвобождение нейротрансмиттеров, мышечные сокращения, двигательная активность и секреция гормонов. Все «чувствительные к раздражению» клетки у животных, такие как нейроны центральной нервной системы (ЦНС), периферические нервные клетки и мышечные клетки, включая клетки скелетных мышц, сердечных мышц и клетки гладких мышц вен и артерий, имеют потенциалзависимые кальциевые каналы.
Кальциевые каналы представляют собой большое семейство с множеством подтипов, отличающихся генетически, физиологически и фармакологически. На основании биофизических свойств кальциевых токов, зарегистрированных от отдельных нейронов, описаны два суперсемейства: высокопороговые (с высоким High Voltage Activated (HVA) и низкопороговые Low Voltage Activated (LVA) кальциевые каналы. Кальциевые токи, которые называют токами L-типа, P-типа, Q-типа, N-типа, R-типа, представляют собой HVA, а токи T-типа представляют собой LVA. Конкретно, термин «L-тип» был первоначально применен к каналам с высокой проводимостью одиночных каналов и длительным временем открытия, и термин «T-тип» применяют к каналам с очень низкой проводимостью одиночных каналов и переходным временем открытия. Дальнейшее исследование многообразия функциональных кальциевых каналов выявило канал «N-типа», экспрессированный в нейронах, и канал «P-типа», который представляет собой доминирующий тип, экспрессированный в мозжечковых нейронах Пуркинье и фармакологически устойчивый к известным блокаторам кальциевых каналов L-типа и N-типа. Исходя из молекулярного родства, десять отличающихся подтипов кальциевых токов выявлены, клонированы, экспрессированы и сгруппированы в три семейства: семейство Cav1 (Cav 1.1, 1.2, 1.3, 1.4) функционально относится к Ca току L-типа; семейство Cav2 (Cav 2.1, 2.2, 2.3) функционально относится к токам P/Q, N, R-типа, и семейство Cav3 (Cav 3.1, 3.2, 3.3) функционально относится к току T-типа.
Считается, что кальциевые каналы имеют отношение к некоторым болезненным состояниям. Полагают, что ряд соединений, применимых для лечения различных сердечно-сосудистых заболеваний у млекопитающих, включая человека, оказывают полезное действие путем модуляции функций потенциалзависимых кальциевых каналов, присутствующих в сердечных и/или сосудистых гладких мышцах. Соединения с активностью, направленной против кальциевых каналов, также непосредственно связаны с лечением боли. Конкретно кальциевые каналы N-типа (Cav2.2), ответственные за регуляцию высвобождения нейротрансмиттера, играют значительную роль в ноцицептивной трансмиссии, как полагают, вследствие их распределения в тканях и на основании результатов нескольких фармакологических исследований. Активированные кальциевые каналы N-типа были обнаружены в ипсилатеральном спинном роге на моделях невропатической боли при повреждениях (Cizkova D., Marsala J., Lukacova N., Marsala M., Jergova S., Orendacova J., Yaksh T.L. Exp. Brain Res. (2002) 147: 456-463). Специфические блокаторы кальциевых каналов N-типа, как показано, являются эффективными средствами для уменьшения болевых реакций на моделях невропатической боли (Mattews E.A., Dickenson A.H. Pain (2001) 92: 235-246), в фазе II формалинового теста (Diaz A., Dickenson A.H. Pain (1997) 69: 93-100) и при гипералгезии, вызванной воспалением коленного сустава (Nebe J., Vanegas H., Schaible H.G. Exp. Brain Res. (1998) 120: 61-69). Показано, что мыши-мутанты, не имеющие кальциевых каналов N-типа, обладают пониженной реакцией на постоянную боль, что видно по уменьшению болевой реакции во время фазы II формалинового теста (Kim C., Jun K., Lee T., Kim S.S., Mcenery M.W., Chin H., Kim H.L, Park J.M., Kim D.K., Jung S.J., Kim J., Shin H.S. Mol. Cell Neurosci. (2001) 18: 235-245; Hatakeyama S., Wakamori M, Ino M., Miyamoto N., Takahashi E., Yoshinaga T., Sawada K., Imoto K., Tanaka I., Yoshizawa T., Nishizawa Y., Mori Y., Nidome T., Shoji S. Neuroreport (2001) 12: 2423-2427), а также на невропатическую боль, оцениваемую по уменьшению механической аллодинии и термической гипералгезии на модели лигирования спинального нерва. Интересно, что упомянутые мыши показали также пониженные уровни тревожности по сравнению с мышами немутантного типа (Saegusa H., Kurihara T., Zong S., Kazuno A., Matsuda Y., Nonaka T., Han W., Toriyama H., Tanabe T., EMBO J. (2001) 20: 2349-2356). Участие кальциевых каналов N-типа в боли дополнительно подтверждено в клинике зиконотидом, пептидом, полученным из яда морского моллюска Conus Magnus. Ограничение в терапевтическом использовании указанного пептида состоит в том, что его приходится вводить человеку интратекально (Bowersox S.S. и Luther R. Toxicon (1998) 36: 1651-1658).
Натриевые каналы играют важную роль в нейронной сети, быстро передавая электрические импульсы по всем клеткам и клеточным сетям, координируя таким образом высшие психические процессы, начиная от локомоторных до познавательных. Указанные каналы представляют собой большие трансмембранные белки, которые способны переключать различные состояния, чтобы обеспечить селективную проницаемость для ионов натрия. Для этого процесса требуется действие потенциала для деполяризации мембраны, и поэтому такие каналы являются потенциалзависимыми. В последние несколько лет разработано намного лучшее объяснение взаимодействия натриевых каналов и лекарственных средств.
Потенциалзависимые натриевые каналы первоначально систематизировали по их чувствительности к тетродотоксину от низкой наномолярной (тетродотоксин-чувствительные TTXs) до высокой микромолярной (тетродотоксин-устойчивые, TTXr). Пока 10 различных альфа-субъединиц натриевых каналов идентифицированы и систематизированы как Nav1.1 и до Nav1.9. Субъединицы Nav1.1-Nav1.4, Nav1.6 и Navl.7 представляют собой TTXs, тогда как Nav.1.5, Nav.1.8 и Nav.1,9 представляют собой TTXr с различными степенями чувствительности. Nav1.1-Nav1.3 и Nav1.6 экспрессированы главным образом в ЦНС, тогда как Nav1.4 и Nav1.5 экспрессированы в основном в мышцах (скелетных и сердечных соответственно), а Nav1.8 и Nav1.9 экспрессированы преимущественно в небольших DRGs.
Стало понятно, что ряд лекарственных средств, включая местные анестетики, антиаритмические средства I класса и противосудорожные средства с неизвестным механизмом действия, на самом деле действуют путем модуляции проводимости натриевых каналов. Блокаторы нейрональных натриевых каналов нашли применение для лечения эпилепсии (фенитоин и карбамазепин), биполярных расстройств (ламотригин), предотвращения нейродегенерации и для ослабления невропатической боли. Различные противоэпилептические лекарственные средства, которые стабилизируют нейрональную возбудимость, эффективны при невропатической боли (габапентин, карбамазепин).
Кроме того, наблюдается также увеличение экспрессии или активности натриевых каналов на некоторых моделях воспалительной боли, заставляя предположить роль натриевых каналов в воспалительной боли.
Все вместе эти данные указывают, что соединения, приводящие к блокаде натриевых и/или кальциевых каналов, обладают высоким терапевтическим потенциалом для предупреждения, ослабления и лечения широкого спектра патологий, включающих неврологические, психиатрические, сердечно-сосудистые, воспалительные, офтальмологические, мочеполовые и желудочно-кишечные заболевания, где вышеупомянутые механизмы описаны как играющие патологическую роль.
Имеется множество статей и патентов, в которых описаны модуляторы или антагонисты натриевых и/или кальциевых каналов для лечения или модуляции плеторы заболеваний, например, их применение в качестве местных анестетиков, антиаритмических и противорвотных средств, антиманиакальных антидепрессантов, средств для лечения однополюсной депрессии, сердечно-сосудистых заболеваний, энуреза, диареи, воспаления, эпилепсии, нейродегенеративных состояний, гибели нервных клеток, невропатической боли, мигрени, острой гипералгезии и воспаления, заболевания почек, аллергии, астмы, бронхоспазма, дисменореи, спазма пищевода, глаукомы, нарушений мочевыводящих путей, нарушений моторики желудочно-кишечного тракта, преждевременных родов, ожирения. Неисчерпывающий список таких статей и патентов/патентных заявок, описывающих блокаторы натриевых и/или кальциевых каналов и виды их применения, включает ссылки, представленные ниже.
C. Alzheimer в Adv. Exp. Med. Biol. 2002, 513, 161-181, описывает натриевые и/или кальциевые каналы в качестве мишеней нейропротективных веществ.
Vanegas e Schaible (Pain 2000, 85, 9-18) обсуждают действие антагонистов кальциевых каналов по спинальным механизмам боли, гипералгезии и аллодинии.
Патент США № 5051403 относится к способу уменьшения нейронального повреждения, связанного с ишемическим состоянием, таким как удар, путем введения связывающего/ингибирующего омега-конотоксин пептида, где пептид характеризуется специфическим ингибированием потенциалзависимых токов кальциевых каналов избирательно в нейрональных тканях.
Патент США № 5587454 относится к композициям и способам для получения обезболивания конкретно в лечении боли и невропатической боли.
Патент США № 5863952 относится к антагонистам кальциевых каналов для лечения ишемического инсульта.
Патент США № 6011035 относится к блокаторам кальциевых каналов, применимым для лечения таких заболеваний, как удар и боль.
Патент США № 6117841 относится к блокаторам кальциевых каналов и их применению в лечении инсульта, церебральной ишемии, боли, травмы головы или эпилепсии.
Патент США № 6362174 относится к блокаторам кальциевых каналов N-типа в лечении инсульта, церебральной ишемии, боли, эпилепсии и травмы головы.
Патент США № 6380198 относится к применению блокатора кальциевых каналов флунаризина для местного лечения глаукомы.
Патенты США № 6420383 и № 6472530 относятся к новым блокаторам кальциевых каналов, применимым для лечения и профилактики ряда заболеваний, таких как гиперчувствительность, аллергия, астма, бронхоспазм, дисменорея, спазм пищевода, глаукома, преждевременные роды, заболевания мочевыводящих путей, нарушения моторики желудочно-кишечного тракта и сердечно-сосудистые заболевания.
Патент США № 6458781 относится к соединениям, которые действуют, блокируя кальциевые каналы, и их применению для лечения инсульта, церебральной ишемии, боли, травмы головы или эпилепсии.
Патент США № 6521647 относится к применению блокаторов кальциевых каналов в лечении заболеваний почек у животных, главным образом хронической почечной недостаточности.
WO 97/10210 относится к трициклическим гетероциклическим производным и их применению в терапии, конкретно в качестве антагонистов кальциевых каналов, например для лечения ишемии, конкретно ишемического инсульта.
WO 03/018561 относится к соединениям хинолина в качестве антагонистов кальциевых каналов N-типа и способам применения таких соединений для лечения или профилактики боли или ноцицепции.
WO 03/057219 относится к блокаторам кальциевых каналов, применимым в качестве средств для лечения или модуляции нарушений центральной нервной системы, таких как невропатическая боль, воспалительная боль, боль, связанная с воспалением или эпилепсия.
В WO 99/14199 описаны замещенные 1,2,3,4,5,6-гексагидро-2,6-метано-3-бензазоцин-10-олы в качестве сильных блокаторов кальциевых каналов, применимых для лечения нескольких заболеваний, таких как удар, нейродегенеративные расстройства, болезнь Альцгеймера, болезнь Паркинсона и сердечно-сосудистые заболевания.
WO 01/74779 раскрывает новые аминопиридиновые блокаторы натриевых каналов и их применение в качестве противосудорожных средств, местных анестетиков, в качестве антиаритмических средств для лечения или предотвращения нейродегенеративных состояний, таких как боковой амиотрофический склероз (ALS), для лечения или предотвращения как острой, так и хронической боли и для лечения или предотвращения диабетической нейропатии.
В WO 04/087125 описаны производные аминокислот в качестве ингибиторов натриевых каналов млекопитающих, применимых для лечения хронической и острой боли, звона в ушах, заболеваний кишечника, дисфункции мочевого пузыря и демиелинизирующих заболеваний.
Моноаминоксидаза (MAO) представляет собой фермент во внешней митохондриальной мембране нейрональных и не нейрональных клеток. Существуют две изоформы MAO: MAO-A и MAO-B. Ферменты MAO ответственны за окислительное деаминирование эндогенных и ксенобиотических аминов и имеют различные предпочтительные субстраты, специфичность ингибиторов и распределение в тканях. Для MAO-A предпочтительными субстратами являются серотонин, норадреналин и адреналин, а клоргилин представляет собой селективный ингибитор MAO-A; тогда как для MAO-B в качестве субстрата предпочтителен β-фенилэтиламин, и она почти селективно ингибируется селегилином. Допамин, тирамин и триптамин окисляются как MAO-A, так и MAO-B, конкретно в мозге человека допамин деаминирован ферментом MAO-B на 80%.
Ингибирование MAO позволяет эндогенным и экзогенным субстратам накапливаться и, возможно, при почти полном ингибировании (>90%) изменять динамику нормальных моноаминных медиаторов. MAO регулирует концентрации в мозгу наиболее важных нейромедиаторов, таких как норадреналин, серотонин и допамин, которые связаны с эмоциями, тревожностью и движением.
Таким образом, полагают, что MAO тесно связана с различными психиатрическими и неврологическими заболеваниями, такими как депрессия, тревожные расстройства и болезнь Паркинсона (PD).
Ингибиторы MAO-A используют главным образом в психиатрии для лечения большой, рефракторной и атипичной депрессии как следствия их способности увеличивать пониженные уровни серотонина и норадреналина. Позже ингибиторы MAO-A стали использовать для лечения пациентов с тревожными расстройствами, такими как социальная фобия, расстройства панического типа, посттравматические стрессовые расстройства и обсессивно-компульсивные расстройства.
Ингибиторы MAO-B используют в основном в неврологии для лечения PD.
Имеются также последние данные и интерес к роли MAO-B в других патологических состояниях, таких как болезнь Альцгеймера (AD). До настоящего времени нет сообщений, свидетельствующих о вовлечении MAO-B в метаболизм сомедиаторов, таких как колецистокинин, вещество Р, соматостатин и нейротензин, которые участвуют в модуляции болевой чувствительности. По этой причине не имеется разумного научного объяснения для применения ингибиторов MAO-B в болевых синдромах.
Сообщают о негативных реакциях на лекарственные средства во время клинической практики с ингибиторами MAO. Первое поколение неселективных и необратимых ингибиторов MAO, таких как транилципромин и фенелзин, имеет серьезные побочные эффекты, включающие гепатотоксичность, ортостатическую гипотензию и наиболее важно гипертонический криз, который имеет место после глотания пищи, содержащей тирамин (Cooper A.J. Tyramine and irreversible monoamine oxidase inhibitors in clinical pratice.- Br. J. Psych. Suppl. 1989: 38-45).
Когда используют упомянутые неселективные и необратимые ингибиторы MAO, необходимо соблюдать строгую диету с пониженным содержанием тирамина. Прессорная чувствительность в отношении тирамина нормализуется в течение 4 недель после прекращения транилципроминовой терапии и более 11 недель после прекращения терапии фенелзином.
Селегилин, почти избирательный и необратимый ингибитор MAO-B, особенно при использовании в комбинации с леводопой, может вызывать анорексию/тошноту, сухость во рту, дискинезию и ортостатическую гипотензию у пациентов с PD, причем последняя является наиболее проблематичной (Volz H.P. and Gleiter C.H.- Monoamine oxidase inhibitors. A perspective on their use in the elderly.- Drugs Aging 13 (1998), pp. 341-355).
При монотерапии у пациентов, получавших селегилин, чаще имели место анорексия/тошнота, скелетно-мышечные поражения и сердечная аритмия, по сравнению с больными, получавшими плацебо. Кроме указанных негативных эффектов, отмечались увеличенные показатели повышенных уровней AST и ALT в сыворотке крови. Наиболее часто описываемыми отрицательными эффектами моклобемида, селективного и обратимого ингибитора MAO-A, являются нарушения сна, повышенная тревожность, дисфория и головная боль.
Комбинация селективных ингибиторов обратного захвата серотонина (SSRIs) и моклобемида обладает высокой эффективностью в случаях не поддающейся лечению депрессии, но идут споры о том, возникают ли в результате такой комбинации токсические побочные эффекты, такие как серотонергический синдром (Baumann P.- Pharmacokinetic-pharmacodynamic relationship of the selective serotonin reuptake inhibitors. Clin. Pharmacokinet. 31 (1996), pp. 444-469). Из-за сердечной аритмии и повышенных уровней ферментов следует регулярно проверять электрокардиограмму и данные лабораторных анализов.
Множество видов физиологических изменений, которые происходят с возрастом, влияют на фармакодинамику и фармакокинетику ингибиторов MAO. Действительно, фармакокинетические переменные заметно отличаются у пожилых пациентов от переменных у молодых пациентов. Указанные переменные, включающие всасывание, распределение, метаболизм и экскрецию, приходится принимать во внимание, чтобы избежать или свести к минимуму некоторые негативные неблагоприятные эффекты взаимодействий лекарственное средство-лекарственное средство. Пожилые больные обычно более чувствительны к побочным эффектам, включая неблагоприятные реакции на лекарства, чем молодые. У пожилых пациентов чаще, чем у молодых, может происходить гипертонический криз, так как сердечно-сосудистая система пожилых людей уже нарушена с возрастом.
Применение симпатомиметических лекарственных средств в комбинации с ингибиторами MAO может также повышать кровяное давление. Кроме того, по сравнению с плацебо при применении фенелзина значительно чаще имеет место дремота, тремор, дискинезия, диарея, затрудненное мочеиспускание, ортостатические эффекты и неблагоприятные дерматологические эффекты. Интересно отметить, что во время лечения моклобемидом, как сообщают, у пожилых пациентов головная боль имеет место чаще, чем у более молодых пациентов (Volz H.P. и Gleiter C.H.- Monoamine oxidase inhibitors. A perspective on their use in the elderly. Drugs Aging 13 (1998), pp. 341-355).
Ингибиторы MAO иногда прописывают при депрессии. Из-за потенциального риска суицида, неблагоприятные побочные реакции и токсичность, обусловленная передозировкой, являются важными факторами, рассматриваемыми при выборе антидепрессанта. Кроме того, когда ингибиторы MAO используют в больших дозах, неблагоприятные сердечно-сосудистые эффекты, по-видимому, значительно возрастают, и, так как селективность MAO теряется при таких высоких дозах, тирамин может вызывать потенциально опасные гипертензивные реакции. Сильная передозировка ингибиторами MAO вызывает ажитацию, галлюцинации, гиперпирексию, гиперрефлексию и судороги. Аномальное кровяное давление также является признаком токсичности, и может потребоваться промывание желудка и поддержание пневмокардиальной функции. Передозировка традиционных неселективных и необратимых ингибиторов MAO является достаточно опасной и иногда смертельной (Yamada and Richelson, 1996. Pharmacology of antidepressants in the elderly. In: David J.R., Snyder L., editors. Handbook of pharmacology of aging. Boca Raton: CRC Press 1996).
В лечении заболеваний, в которых механизм(ы) натриевых и кальциевых каналов играет(ют) патологическую роль, и, конкретно, в лечении болевых синдромов (или невропатического, или воспалительного типа) ингибирование MAO ферментов бесполезно (невыгодно). Наиболее активные в клинике антиноцицептивные лекарственные средства не обладают способностью ингибировать MAO. Наоборот, побочные эффекты, ингибирующие MAO, могут налагать по меньшей мере два типа негативных ограничений.
1) Диетические: употребление пищи с высоким содержанием тирамина может вызвать серьезное, даже угрожающее жизни, повышение системного кровяного давления (так называемый «сырный эффект»).
2) Фармакологические: боль часто лечат комбинацией лекарственных средств, таких как опиоидные производные и трициклические антидепрессанты. Такая комбинация в сочетании с ингибиторами MAO опасна, так как она может вызвать серотонинергический синдром (возбуждение, тремор, галлюцинации, гипертермию и аритмию).
Следовательно, устранение или значительное уменьшение ингибирующей MAO активности в лекарственных средствах, действующих в качестве модуляторов натриевых и/или кальциевых каналов, применимых для предупреждения, облегчения и излечения широкого спектра патологий, в которых указанный(е) механизм(ы) играет(ют) патологическую роль, включающих неврологические, психические, сердечно-сосудистые, воспалительные, офтальмологические, мочеполовые и желудочно-кишечные заболевания, является неожиданным и существенным улучшением для терапии по сравнению с соединениями, имеющими аналогичную эффективность, но обладающими вышеупомянутыми побочными эффектами. Указанное улучшение является особенно желательным для лекарственных средств, действующих в качестве модуляторов натриевых и/или кальциевых каналов, применимых, в частности, для лечения болевых синдромов.
Принимая во внимание эти данные по ингибиторам MAO, конкретно отсутствие каких-либо доказательств о роли MAO-B в патологических поражениях, подобных боли, мигрени, сердечно-сосудистым, воспалительным, мочеполовым и желудочно-кишечным заболеваниям, можно допустить, что ингибирование MAO-B не должно быть существенным признаком для соединений, указанных для вышеупомянутых патологий, не допускающих побочных эффектов во время хронического и/или длительного лечения.
Предпочтительное решение описанной выше проблемы состояло бы в создании лекарственных средств, которые «избирательно действуют как модуляторы натриевых и/или кальциевых каналов» или применимы для «избирательного лечения» повреждений, расстройств или заболеваний, в которых механизм(ы) натриевых и/или кальциевых каналов играет(ют) патологическую роль. Это выражение подразумевает лекарственные средства, которые при введении пациенту, нуждающемуся в лечении, в количествах, эффективных для лечения вышеуказанных болезней, где вышеупомянутые механизм(ы) играет(ют) патологическую роль, не проявляют какой-либо ингибирующей активности в отношении MAO или проявляют значительно сниженную ингибирующую активность в отношении MAO, таким образом, в результате не допускают побочных эффектов, обусловленных накоплением эндогенных и экзогенных моноаминных медиаторов.
Основная задача настоящего изобретения состоит в применении фенилэтиламинопроизводных для изготовления лекарственных средств, активных в качестве модуляторов натриевых и/или кальциевых каналов, для лечения патологий, в которых вышеуказанные механизм(ы) играет(ют) патологическую роль, причем указанные лекарственные средства по существу не обладают ингибирующей активностью в отношении MAO или обладают значительно сниженной ингибирующей активностью в отношении MAO и, следовательно, возможности нежелательных побочных эффектов уменьшены. Указанное применение обеспечивает повышенный селективный ресурс для предупреждения, ослабления и/или излечения вышеуказанных патологических поражений.
Описание изобретения
Авторы настоящего изобретения обнаружили новый класс фенилэтиламинопроизводных, высокоэффективных в качестве модуляторов натриевых и/или кальциевых каналов, по существу не обладающих ингибирующей активностью в отношении MAO или обладающих значительно сниженной ингибирующей активностью в отношении MAO и, следовательно, имеющих потенциально сниженные побочные эффекты, для предупреждения, ослабления и излечения широкого спектра патологий, включающих, но без ограничения, нейрогенные, психиатрические, сердечно-сосудистые, воспалительные, офтальмологические, мочеполовые и желудочно-кишечные заболевания, в которых, как сообщается, вышеупомянутые механизмы играют патологическую роль.
В настоящем описании и формуле изобретения выражение «модулятор(ы) натриевых и/или кальциевых каналов» обозначает соединения, способные блокировать натриевые и/или кальциевые токи потенциалзависимым способом.
Следовательно, задача настоящего изобретения состоит в обеспечении соединения общей формулы I
где
(a)
J представляет собой группу A-[(CH2)n-O]r- в пара-положении по отношению к этиламиновому фрагменту,
в которой
n равно нулю или 1, и
r равно 1;
A представляет собой трифторметил; или фенил, необязательно замещенный галогеном;
W представляет собой (C1-C4)алкокси;
R представляет собой водород;
R0 представляет собой водород или (C1-C2)алкил;
R1 представляет собой водород; (C1-C4)алкил, необязательно замещенный гидроксигруппой; циклопропилметил; 2-пропин-1-ил; бензил, необязательно замещенный одной или двумя (C1-C2)алкоксигруппами в бензольном кольце; тиазолил; 5-6-членный насыщенный гетероциклил, содержащий атом азота, необязательно замещенный (C1-C2)алкильной группой; или гетероциклилметил, в котором гетероциклическая группа представляет собой 5-6-членный гетероциклил, содержащий 1-3 гетероатома, выбранных из азота, кислорода и серы, необязательно замещенный одной или двумя группами, выбранными из (C1-C2)алкила, гидроксиметила и (C1-C2)алкокси;
R2 представляет собой водород; (C1-C4)алкил или фенил;
R3 представляет собой водород или (C1-C4)алкил; и
R4 представляет собой водород; (C1-C4)алкил, необязательно замещенный группой, выбранной из амино, (C1-C4)алкиламино, ди(C1-C4)алкиламино, имидазолила и пирролидинила, причем имидазолильная и пирролидинильная группы необязательно замещены (C1-C2)алкильной группой; или бензил; или
R3 и R4 вместе с соседним атомом азота образуют пирролидинильное, морфолинильное или пиперазинильное кольцо, необязательно замещенное (C1-C2)алкильной группой;
или
(b)
J представляет собой водород;
W представляет собой группу A-[(CH2)n-O]r-,
в которой
n равно нулю, 1 или 2; и
r равно нулю или 1;
A представляет собой (C1-C4)алкил, трифторметил; циклопропил; циклопентил; фенил, необязательно замещенный группой, выбранной из галогена, метила, метокси, трифторметила, ацетиламино и диметиламинометила; тиенил, необязательно замещенный хлором; фуранил; изоксазолил, необязательно замещенный одной или двумя метильными группами; пиперидинил; морфолинил; пиридинил или пиримидинил, причем пиридинильное и пиримидинильное кольца необязательно замещены одной или двумя метоксигруппами;
R представляет собой водород или фтор;
R0 представляет собой водород или (C1-C2)алкил;
R1 представляет собой циклопропилметил, фуранилметил, тетрагидрофуранил или тетрагидрофуранилметил;
R2 представляет собой водород или (C1-C4)алкил;
R3 представляет собой водород или (C1-C4)алкил; и
R4 представляет собой водород, (C1-C4)алкил, необязательно замещенный группой, выбранной из (C1-C2)алкокси, амино, (C1-C4)алкиламино и ди(C1-C4)алкиламино; или гетероциклил, где гетероциклил выбран из изоксазолила, пиразолила, имидазолила, тиазолила и 1,3,4-тиадиазолилила и может быть необязательно замещен (C1-C2)алкильной группой; или
R3 и R4 вместе с соседним атомом азота образуют пирролидиновое кольцо;
при условии, что когда A представляет собой (C1-C4)алкил, трифторметил, циклопропил или циклопентил, тогда r равен 1;
в определенных случаях либо в виде индивидуального энантиомера или диастереоизомера, либо в виде их смеси, и его фармацевтически приемлемые соли.
Tермин «(C1-C4)алкильная» или «(C1-C4) алкильная» группа в других заместителях (например, в терминах «алкокси», «моно- и диалкиламино»), используемый в настоящем описании и формуле изобретения, когда не указано иное, обозначает линейный или разветвленный алкильный радикал или группу; примеры указанных радикалов или групп включают соответственно метил, этил, пропил, изопропил, бутил, изобутил и трет-бутил или метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и трет-бутокси.
Tермин «галоген», когда не указано иное, обозначает радикал атома галогена, такого как фтор, хлор, бром и йод.
Термин «гетероцикл» и «гетероциклил», когда в настоящем описании не указано иное, означает полностью ненасыщенный, частично ненасыщенный или насыщенный моноциклический 5- или 6-членный гетероцикл, содержащий от 1 до 3 гетероатомов, выбранных из азота, кислорода и серы. Примеры моноциклического 5- или 6-членного полностью ненасыщенного гетероцикла, содержащего от 1 до 3