Способ получения n-фенилпиразол-1-карбоксамидов
Иллюстрации
Показать всеИзобретение относится к способу получения соединений формулы (I), который включает взаимодействие соединений формул (II) и (III) и сульфонилхлорида в подходящем органическом растворителе в присутствии основания с образованием соединения формулы (I), причем растворитель или/и основание объединяется с соединениями формул (II) и (III). Описаны также соединения формулы (III), которые применимы в качестве исходных соединений для этого способа. Радикалы R1-R6 имеют значения, указанные в формуле изобретения. Технический результат - разработка менее дорогого и более эффективного, гибкого и удобного в работе способа получения соединений формулы (I). 2 н. и 11 з.п. ф-лы, 2 табл.
Реферат
Данное изобретение относится к способу получения N-фенилпиразол-1-карбоксамидов связыванием карбоновых кислот с антраниламидами и к соединениям антраниламидов, пригодным для способа.
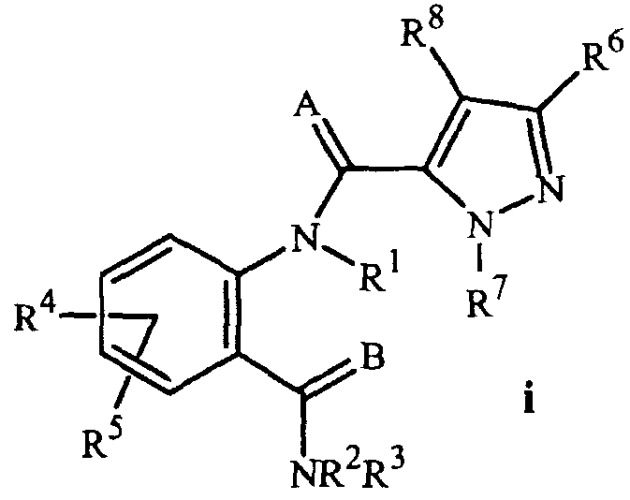
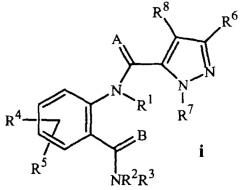
Патентная публикация PCT WO 03/015518 раскрывает использование в качестве антроподицитов N-ацил производных антраниловой (о-аминобензойной) кислоты формулы i
где A и B независимо представляют O или S; R1 представляет H; R2 представляет H, C1-C6 алкил, C2-C6 алкоксикарбонил или C2-C6 алкилкарбонил; R3 представляет, наряду с прочим, H или C1-C6 алкил; R4 представляет, наряду с прочим, H или C1-C6 алкил; R5 представляет Н, C1-C6 алкил или галоген; R6 представляет Н, C1-C6 алкил, C1-C6 галогеналкил, галоген, CN, C1-C4 алкокси или C1-C4 галогеналкокси; R7 представляет, наряду с прочим, кольцо фенила, кольцо бензила, 5- или 6-членное гетероароматическое кольцо, кольцевую систему нафтила, каждое кольцо или кольцевая система необязательно замещены 1-3 заместителями; и R8 представляет, наряду с прочим, H. Этот документ раскрывает различные способы получения соединений формулы i. Однако остается потребность в новых способах, менее дорогих, более эффективных, более гибких или более удобных для работы.
Сущность изобретения
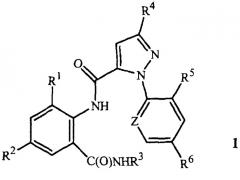
Данное изобретение относится к способу получения соединения формулы 1
где R1 означает CH3 или Cl;
R2 означает Br, Cl, I или CN;
R3 означает H или C1-C4 алкил;
R4 означает Cl, Br, CF3, OCF2H или OCH2CF3;
R5 означает F, Cl или Br;
R6 означает Н, F или Cl;
Z означает CR7 или N и
R7 означает Н, F, Cl или Br.
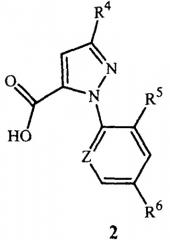
Способ включает объединение (1) соединения карбоновой кислоты формулы 2
(2) соединения анилина формулы 3
и (3) сульфонилхлорида с получением соединения формулы 1.
Данное изобретение также относится к соединению анилина формулы 3, где
R1 представляет CH3 или Cl;
R2 представляет Br, Cl, I или CN и
R3 представляет H или C1-C4 алкил,
при условии, что
(a) когда R1 и R2 представляют Cl, тогда R3 не является H, CH2CH3 или CH(CH3)CH2CH3;
(b) когда R1 представляет CH3 и R2 представляет Cl, Br или CN, тогда R3 не является CH3 или CH(CH3)2;
(c) когда R1 представляет Cl и R2 представляет Cl или Br, тогда R3 не является CH3 или CH(CH3)2, и
(d) когда R1 представляет CH3 и R2 представляет CN, тогда R3 не является H.
Подробное описание изобретения
Используемые в описании термины "содержит", "содержащий", "включает", "включающий", "имеет", "имеющий" или любые другие их вариации предназначаются для охвата неэксклюзивного добавления. Например, состав, процесс, способ, изделие или аппарат, который содержит перечень элементов, не должен ограничиваться только этими элементами, но может включать другие элементы, четко не перечисленные или свойственные такому составу, процессу, способу, изделию или аппарату. Далее, если четко не указано противоположного, "или" относится к инклюзивному или, а не к эксклюзивному или. Например, условие А или В удовлетворяет одному из следующего: А является истинным (или присутствует) и В является ложным (или отсутствует), А является ложным (или отсутствует) и В является истинным (или присутствует), и оба А и В являются истинными (или присутствуют).
Объединение реагентов относится к взаимодействию их друг с другом.
К тому же неопределенные артикли "а" и "an" перед элементом или компонентом изобретения предполагают неограничительное рассмотрение числа отдельных примеров (т.е. случаев) элемента или компонента. Поэтому "a" или "an" следует понимать как включающие один или по меньшей мере один, и единственное число слова, обозначающего элемент или компонент, также включающие множественное число, если число явно не должно быть единственным.
Радикал на основе углерода относится к одновалентному молекулярному компоненту, содержащему атом углерода, который соединяет радикал с остальной химической структурой через одинарную связь. Радикалы на основе углерода необязательно могут содержать насыщенные, ненасыщенные и ароматические группы, цепи, кольца и кольцевые системы и гетероатомы. Хотя радикалы на основе углерода не подвергаются какому-либо конкретному ограничению по размеру, в контексте данного изобретения они обычно содержат от 1 до 16 атомов углерода и от 0 до 3 гетероатомов. Предпочтительными являются радикалы на основе углерода, выбранные из C1-C6 алкила, C1-C4 галогеналкила и фенила, необязательно замещенных 1-3 заместителями, выбранными из C1-C3 алкила, галогена и нитро.
В перечислениях в описании сокращение "Ph" означает фенил. Алкил может быть с прямой или разветвленной цепью. Термин "галоген", или один, или в сложных словах, таких как "галогеналкил", включает фтор, хлор, бром или йод. К тому же при использовании в сложных словах, таких как "галогеналкил", указанный алкил может быть частично или полностью замещенным атомами галогена, которые могут быть одинаковыми или разными. Примеры "галогеналкила" включают F3C, ClCH2, CF3CH2 и CF3CCl2.
Варианты воплощения данного изобретения включают:
Вариант воплощения M1. Способ, где молярное отношение соединения формулы 2 к соединению формулы 3 от около 1,2:1 до около 1:1,2.
Вариант воплощения M2. Способ по варианту воплощения M1, где молярное отношение соединения формулы 2 к соединению формулы 3 от около 1:1 до около 1:1,2.
Вариант воплощения M3. Способ по варианту воплощения M2, где молярное отношение соединения формулы 2 к соединению формулы 3 около 1:1,1.
Вариант воплощения M4. Способ, где молярное отношение сульфонилхлорида к соединению формулы 2 по меньшей мере около 1:1.
Вариант воплощения M5. Способ по варианту воплощения M4, где молярное отношение сульфонилхлорида к соединению формулы 2 от около 1:1 до около 2,5:1.
Вариант воплощения M6. Способ по варианту воплощения M5, где молярное отношение сульфонилхлорида к соединению формулы 2 от около 1,1:1 до около 1,4:1.
Вариант воплощения M7. Способ по варианту воплощения M6, где когда R2 представляет Br, Cl или I, тогда молярное отношение сульфонилхлорида к соединению формулы 2 около 1,2:1.
Вариант воплощения M8. Способ по варианту воплощения М6, где когда R2 представляет CN, тогда молярное отношение сульфонилхлорида к соединению формулы 2 около 1,4:1.
Вариант воплощения M9. Способ, где сульфонилхлорид представлен формулой 4
R8S(O)2Cl,
где R8 представляет углеродсодержащий радикал.
Вариант воплощения M10. Способ по варианту воплощения M9, где R8 представляет C1-C4 алкил, C1-C2 галогеналкил или фенил, необязательно замещенные 1-3 заместителями, выбранными из группы, состоящей из галогена, C1-C3 алкила и нитро.
Вариант воплощения M11. Способ по варианту воплощения M10, где R8 представляет C1-C2 алкил, CF3, фенил или 4-метилфенил.
Вариант воплощения M12. Способ по варианту воплощения M11, где R8 представляет C1-C2 алкил, фенил или 4-метилфенил.
Вариант воплощения M13. Способ по варианту воплощения M12, где R8 представляет CH3.
Вариант воплощения M14. Способ, где карбоновую кислоту формулы 2, анилин формулы 3 и сульфонилхлорид объединяют при температуре между около -70 и 100°С.
Вариант воплощения M15. Способ по варианту воплощения M14, где температура между около -20 и 40°С.
Вариант воплощения M16. Способ по варианту воплощения MI5, где температура между около -10 и 20°С.
Вариант воплощения M17. Способ, где карбоновую кислоту формулы 2 объединяют с анилином формулы 3, чтобы получить смесь, и затем смесь объединяют с сульфонилхлоридом.
Вариант воплощения M18. Способ по варианту воплощения M17, где основание объединяют со смесью или до, или после объединения с сульфонилхлоридом.
Вариант воплощения M19. Способ по варианту воплощения M17, где основание объединяют с соединениями формул 2 и 3, чтобы получить смесь, до объединения с сульфонилхлоридом.
Вариант воплощения M20. Способ, где основание объединяют с соединениями формул 2 и 3 и сульфонилхлоридом.
Вариант воплощения M21. Способ по любому из вариантов воплощения M18-M20, где количество основания равно по меньшей мере приблизительно 2 эквивалентам по отношению к сульфонилхлориду.
Вариант воплощения M22. Способ по варианту воплощения M21, где количество равно по меньшей мере приблизительно 2,1 эквивалента по отношению к сульфонилхлориду.
Вариант воплощения M23. Способ по варианту воплощения M22, где количество основания равно от около 2,1 до 2,2 эквивалента по отношению к сульфонилхлориду.
Вариант воплощения M24. Способ по любому из вариантов воплощения M18-M20, где основание выбрано из третичных аминов (включая необязательно замещенные пиридины).
Вариант воплощения M25. Способ по варианту воплощения M24, где основание выбрано из необязательно замещенных пиридинов и их смесей.
Вариант воплощения M26. Способ по варианту воплощения M25, где основание выбрано из 2-пиколина, 3-пиколина, 2,6-лутидина, пиридина и их смесей.
Вариант воплощения M27. Способ по варианту воплощения M26, где основанием является 3-пиколин.
Вариант воплощения M28. Способ, где растворитель объединяют с соединениями формул 2 и 3 и сульфонилхлоридом.
Вариант воплощения M29. Способ по варианту воплощения M17, где растворитель объединяют с соединениями формул 2 и 3 с получением смеси перед объединением с сульфонилхлоридом.
Вариант воплощения M30. Способ по варианту воплощения M28 или M29, где растворитель выбран из нитрилов (например, ацетонитрил, пропионитрил), сложных эфиров (например, метилацетат, этилацетат, бутилацетат), кетонов (например, ацетон, метилэтилкетон, метилбутилкетон), галогеналканов (например, дихлорметан, трихлорметан), простых эфиров (например, этиловый простой эфир, метил-трет-бутиловый простой эфир, тетрагидрофуран, п-диоксан), ароматических углеводородов (например, бензол, толуол, хлорбензол, дихлорбензол), третичных аминов (например, триалкиламины, диалкиланилины, необязательно замещенные пиридины) и их смесей.
Вариант воплощения M31. Способ по варианту воплощения M30, где растворитель выбран из третичных аминов (например, триалкиламины, диалкиланилины, необязательно замещенные пиридины) и их смесей.
Вариант воплощения M32. Способ по варианту воплощения M30, где растворитель выбран из нитрилов (например, ацетонитрил, пропионитрил), сложных эфиров (например, метилацетат, этилацетат, бутилацетат), кетонов (например, ацетон, метилэтилкетон, метилбутилкетон), галогеналканов (например, дихлорметан, трихлорметан), простых эфиров (например, этиловый простой эфир, метил-трет-бутиловый простой эфир, тетрагидрофуран, п-диоксан), ароматических углеводородов (например, бензол, толуол, хлорбензол, дихлорбензол) и их смесей.
Вариант воплощения M33. Способ по варианту воплощения M32, где растворителем является ацетонитрил.
Вариант воплощения C1. Соединение формулы 3, где R1 представляет CH3.
Вариант воплощения C2. Соединение формулы 3, где R2 представляет Br или Cl.
Вариант воплощения C3. Соединение формулы 3, где R2 представляет I.
Вариант воплощения C4. Соединение формулы 3, где R2 представляет CN.
Вариант воплощения C5. Соединение формулы 3, где R3 представляет H или CH3.
Вариант воплощения С6. Соединение формулы 3, где R3 представляет CH3.
Достойны внимания соединения формулы 3, где R1 представляет CH3, R2 представляет Cl и R3 представляет H, CH2CH3, CH2CH2CH3, CH2CH2CH2CH3, CH2CH(CH3)2, CH(CH3)CH2CH3 или C(CH3)3. Следует отметить также соединения формулы 3, где R1 представляет CH3, R2 представляет Br и R3 представляет Н, CH2CH3, CH2CH2CH3, CH2CH2CH2CH3, CH2CH(CH3)2, CH(CH3)CH2CH3 или C(CH3)3. Также значительными являются соединения формулы 3, где R1 представляет CH3, R2 означает I и R3 представляет Н, CH3, CH2CH3, CH2CH2CH3, CH(CH3)2, CH2CH2CH2CH3, CH2CH(CH3)2, CH(CH3)CH2CH3 или C(CH3)3. Также значительными являются соединения формулы 3, где R1 представляет CH3, R2 представляет CN и R3 представляет CH2CH3, CH2CH2CH3, CH2CH2CH2CH3, CH2CH(CH3)2, CH(CH3)CH2CH3 или C(CH3)3. Также значительными являются соединения формулы 3, где R1 представляет Cl, R2 представляет Cl и R3 представляет CH2CH2CH3, CH2CH2CH2CH3, CH2CH(CH3)2 или C(CH3)3. Также значительными являются соединения формулы 3, где R1 представляет Cl, R2 представляет Br и R3 представляет Н, CH2CH3, CH2CH2CH3, CH2CH2CH2CH3, CH2CH(CH3)2, CH(CH3)CH2CH3 или C(CH3)3. Также значительными являются соединения формулы 3, где R1 представляет Cl, R2 представляет I и R3 представляет Н, CH3, CH2CH3, CH2CH2CH3, CH(CH3)2, CH2CH2CH2CH3, CH2CH(CH3)2, CH(CH3)CH2CH3 или C(CH3)3. Также значительными являются соединения формулы 3, где R1 представляет Cl, R2 представляет CN и R3 представляет Н, CH3, CH2CH3, CH2CH2CH3, CH(CH3)2, CH2CH2CH2CH3, CH2CH(CH3)2, CH(CH3)CH2CH3 или C(CH3)3.
На следующих схемах значения R1, R2, R3, R4, R5 и R6 в соединениях нижеследующих формул 1-34 являются такими же, как указано выше в разделе "Сущность изобретения" и описании вариантов воплощения, если не указано иначе.
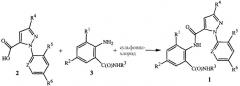
Как показано на схеме 1, данное изобретение относится к способу получения соединений формулы 1 путем взаимодействия карбоновых кислот формулы 2 с антраниламидами формулы 3 с использованием сульфонилхлорида, обычно в присутствии основания и растворителя.
Схема 1
Таким образом, в данном способе пиразолкарбоновую кислоту формулы 2, анилин формулы 3 и сульфонилхлорид объединяют (т.e. взаимодействуют) с получением соответствующего N-фенил-5 пиразол-1-карбоксамида формулы 1.
Возможен широкий диапазон отношений реагентов, однако обычно используют молярное соотношение соединения формулы 3 к соединению формулы 2, составляющее от около 0,9 до 1,1, и предпочтительно около 1,0, так что оба соединения могут быть полностью израсходованы. Данный способ может быть осуществлен в широком диапазоне температур, но обычно его проводят при температурах в пределах от -70°С до +100°С. Предпочтительными являются температуры от -20°С до +40°С. Наиболее пригодны для удобства работы, благоприятной скорости и селективности реакции и высокого выхода процесса температуры от -10°С до +20°С.
Соединение сульфонилхлорида используют в качестве реагента для облегчения связывания карбоновой кислоты с антраниламидом, чтобы получить N-фенилпиразол-1-карбоксамид. Обычно молярное соотношение сульфонилхлорида к соединению формулы 2 составляет от около 1,0 до 2,5 и предпочтительно от около 1,1 до 1,4, при этом побочная реакция циклизации, описанная ниже, происходит в незначительной степени (т.e. 0-10%). Сульфонилхлориды представлены, в основном, формулой R8S(O)2Cl (формула 4), где R8 представляет радикал на основе углерода. Обычно для данного способа R8 представляет C1-C4 алкил, C1-C2 галогеналкил или фенил, необязательно замещенные 1-3 заместителями, выбранными из группы, состоящей из галогена, C1-C3 алкила и нитро. Соединения сульфонилхлорида, предпочтительные для данного способа, вследствие их коммерческой доступности, включают метансульфонилхлорид (R8 представляет CH3), пропансульфонилхлорид (R8 представляет (CH2)2CH3), бензолсульфонилхлорид (R8 представляет Ph) и п-толуолсульфонилхлорид (R8 представляет 4-CH3-Ph). Метансульфонилхлорид является наиболее предпочтительным вследствие низкой стоимости, легкости присоединения и/или снижения отходов.
В данном способе сульфонилхлорид объединяют с пиразолкарбоновой кислотой формулы 2 и анилином формулы 3. Реагенты могут быть объединены в разных последовательностях, таких как объединение сульфонилхлорида с карбоновой кислотой формулы 2 для получения смеси и последующее объединение смеси с анилином формулы 3. Однако для получения конкретных N-фенилпиразол-1-карбоксамидов формулы 1 наиболее предпочтительным является объединение карбоновой кислоты формулы 2 с анилином формулы 3 с получением смеси и последующее объединение сульфонилхлорида со смесью (например, добавление сульфонилхлорида к смеси соединений формул 2 и 3), потому что такой порядок добавления позволяет удобно контролировать процесс связывания. Скорость реакции легко регулируют простым регулированием скорости добавления соединения сульфонилхлорида. Поэтому предпочтительный вариант воплощения данного способа включает последовательные стадии (1) объединения карбоновой кислоты формулы 2 и анилина формулы 3 с получением смеси и (2) последующее объединение смеси с сульфонилхлоридом. Хотя при добавлении сульфонилхлорида к смеси, содержащей анилин формулы 2, потенциально могут присходить нежелательные побочные реакции, было обнаружено, что конкретные стереоэлектронные профили соединений формул 2 и 3 позволяют достичь удивительно высоких выходов соединений формулы 1 при использовании данного способа.
Соединение формулы 1 получают, когда исходные соединения формул 2 и 3 и сульфонилхлорид взаимодействуют друг с другом в объединенной жидкой фазе, в которой каждый из них по меньшей мере частично растворим. В частности, так как исходные реагенты формул 2 и 3 обычно являются твердыми веществами при обычных температурах окружающей среды, способ наиболее успешно проводят, используя растворитель, в котором исходные соединения хорошо растворяются. Так, обычно способ осуществляют в жидкой фазе, содержащей растворитель. В некоторых случаях карбоновая кислота формулы 2 может иметь только слабую растворимость, но ее соль с присоединенным основанием может иметь более хорошую растворимость в растворителе. Подходящие для этого способа растворители включают нитрилы, такие как ацетонитрил и пропионитрил; сложные эфиры, такие как метилацетат, этилацетат и бутилацетат; кетоны, такие как ацетон, метилэтилкетон (MEK) и метилбутилкетон; галогеналканы, такие как дихлорметан и трихлорметан; простые эфиры, такие как этиловый простой эфир, метил-трет-бутиловый простой эфир, тетрагидрофуран (THF) и п-диоксан; ароматические углеводороды, такие как бензол, толуол, хлорбензол и дихлорбензол; третичные амины, такие как триалкиламины, диалкиланилины и необязательно замещенные пиридины; и их смеси. Представляющие интерес растворители включают ацетонитрил, пропионитрил, этилацетат, ацетон, MEK, дихлорметан, метил-трет-бутиловый простой эфир, THF, п-диоксан, толуол и хлорбензол. Особо предпочтительным в качестве растворителя является ацетонитрил, так как он часто обеспечивает продукты с превосходным выходом и/или чистотой.
Так как в результате реакции в способе по данному изобретению образуется в качестве побочного продукта хлорид водорода, который иначе мог бы связываться с имеющими основный характер центрами на соединениях формул 1, 2 и 3, способ наиболее удовлетворительно осуществляют в присутствии по меньшей мере одного добавленного основания. Основание может также облегчать конструктивное взаимодействие карбоновой кислоты с соединением сульфонилхлорида и антраниламидом. В результате взаимодействия добавленного основания с карбоновой кислотой формулы 2 образуется соль, которая может иметь более хорошую растворимость, чем карбоновая кислота, в реакционной среде. Хотя основание и может быть добавлено одновременно, с чередованием или даже после добавления сульфонилхлорида, обычно основание добавляют перед добавлением сульфонилхлорида. Некоторые растворители, такие как третичные амины, также служат в качестве оснований и, когда их используют в качестве растворителей, они должны быть в большом стехиометрическом избытке в качестве оснований. Когда основание не используют в качестве растворителя, номинальное молярное соотношение загруженного основания к загруженному сульфонилхлориду обычно составляет от около 2,0 до 2,2 и предпочтительно от около 2,1 до 2,2. Предпочтительными основаниями являются третичные амины, включая замещенные пиридины. Более предпочтительные основания включают 2-пиколин, 3-пиколин, 2,6-лутидин и пиридин. Особо предпочтительным основанием является 3-пиколин, так как его соли с карбоновыми кислотами формулы 2 часто являются высокорастворимыми в растворителях, таких как ацетонитрил.
Признаки данного способа обеспечивают эффективное получение N-фенилпиразол-1-карбоксамида формулы 1, в то же время ограничивая количества карбоновой кислоты, сульфонилхлорида и антраниламида, которые расходуются во время образования N-фенилпиразол-1-карбоксамида, и уменьшение отходов. Данный способ позволяет удобно регулировать процесс соединения и обеспечивает способ с вовлечением меньшего числа и более простых операций по сравнению с ранее известными процессами получения N-фенилпиразол-1-карбоксамидов, таких как представленные формулой 1.
Предпочтительный вариант воплощения данного способа объединяет пиразолкарбоновую кислоту формулы 2, антраниловую кислоту формулы 3 и подходящее основание в подходящем растворителе с последующим добавлением соединения сульфонилхлорида (или одного, или в смеси с подходящим растворителем).
Полученные N-фенилпиразол-1-карбоксамиды формулы 1 могут быть выделены из реакционных смесй способами, известными специалистам в этой области, включая кристаллизацию, фильтрование и экстракцию. Как показано на схеме 2, в некоторых случаях в условиях реакции взаимодействия происходит частичная циклизация амидов 1 до иминобензоксазинов формулы цикло-1.
Схема 2
В таких случаях часто предпочтительно превращать соединение формулы цикло-1 обратно в амид формулы 1 перед выделением продукта реакции. Такое превращение может быть осуществлено обработкой реакционной смеси водной кислотой. В качестве варианта, смесь иминобензоксазина формулы цикло-1 и амида формулы 1 может быть выделена и эта смесь затем может быть превращена в амид формулы 1, например, обработкой разбавленной водной кислотой необязательно в присутствии подходящего органического растворителя.
В предпочтительных условиях этого процесса побочная реакция циклизации, превращающая желательный продукт формулы 1 в соединение формулы цикло-1, обычно происходит только до незначительной степени, если вообще происходит, в таких случаях предпочтительные соотношения сульфонилхлорида и основания являются достаточными для завершения реакции соединения. Однако для некоторых пиразолкарбоновых кислот формулы 2, антраниловых кислот формулы 3 (таких, где R2 представляет CN) и условий реакции (например, с использованием стерически затрудненных замещенных пиридинов, таких как 2,6-лутидин, в качестве оснований) превращение желательного продукта формулы 1 в соединение формулы цикло-1 может происходить до более значительной степени или может быть доминирующей реакцией. В таких случаях применение более высоких соотношений сульфонилхлорида и основания может облегчить завершение реакции взаимодействия. Побочная реакция циклизации стехиометрически потребляет эквивалент сульфонилхлорида дополнительно к эквиваленту сульфонилхлорида, израсходованному на реакцию взаимодействия. Поэтому если бы происходила 100% циклизация, стехиометрически было бы необходимо молярное соотношение 2:1 сульфонилхлорида к соединению формулы 2 для достижения полного расходования исходных реагентов, и обычно было бы использовано молярное соотношение вплоть до около 2,5:1 сульфонилхлорида к соединению формулы 2 в сравнении с молярным соотношением около 1,4:1 сульфонилхлорида к соединению формулы 2, когда циклизация происходит только на 5-10% (как это происходит обычно с большинством оснований, когда R2 представляет CN) и молярным соотношением около 1,2:1 сульфонилхлорида к соединению формулы 2, когда побочная реакция циклизации незначительная (как это происходит обычно с большинством оснований, когда R2 представляет Br, Cl или I). Дополнительные количества сульфонилхлорида и основания могут быть добавлены в течение реакции, если наблюдается реакция циклизации.
Вышесказанное показывает ценный признак этого процесса, который заключается в том, что дополнительные количества любого из компонентов процесса могут быть добавлены в любое время, как требуется для завершения превращения. Другое пояснение ценности этого признака касается ситуации, когда или компонент формулы 2, или компонент формулы 3 непредумышленно недогружен в реакционную смесь. Эта недогрузка может быть определена анализом реакционной смеси с использованием любого из разнообразных методов, которые широко известны и доступны, включая ЖХВР и ЯМР. При обнаружении недогрузка может быть скорректирована дополнительным добавлением соответствующего компонента к реакционной смеси. Это может быть особенно ценно для производства в больших масштабах, так как позволяет исправить ошибку при загрузке и предотвратить отходы дорогостоящего промежуточного соединения, которые иначе могли бы образовываться.
Пиразолкарбоновые кислоты формулы 2 могут быть получены с использованием методов гетероциклического синтеза, известных в литературе, включая ссылки, находящиеся в следующем списке: Rodd's Chemistry of Chemistry of Carbon Compounds, Vol. IVa to IVl, S. Coffey editor, Elsevier Scientific Publishing, New York, 1973; Comprehensive Heterocyclic Chemistry, Vol.1-7, A.R. Katritzky и C.W. Rees editors, Pergamon Press, New York, 1984; Comprehensive Heterocyclic Chemistry II, Vol.1-9, A.R.Katritzky, C.W. Rees, и E.F. Scriven editors, Pergamon Press, New York, 1996; и серии The Chemistry of Heterocyclic Compounds, E.C. Taylor, editor, Wiley, New York. Разнообразные гетероциклические кислоты (включая пиразолкарбоновые кислоты) и общие способы их синтеза находятся в патентной публикации PCT WO 98/57397.
Один особенно используемый способ получения пиразолкарбоновых кислот формулы 2a показан на схеме 3
Схема 3
Взаимодействие пиразола формулы 6 с 2-галогенпиридином формулы 7 позволяет получить высокие выходы 1-пиридинилпиразола формулы 8 с хорошей специфичностью в отношении желательной региохимии. Металлирование соединения формулы 8 диизопропиламидом лития (LDA) с последующим гашением соли лития диоксидом углерода дает 1-(2-пиридинил)пиразолкарбоновую кислоту формулы 2a. Приводимая ссылка на этот способ: см. патентную публикацию PCT WO 03/015519.
Как показано на схеме 4, пиразолкарбоновые кислоты формулы 2b могут быть получены посредством 3+2 циклоприсоединения соответствующим образом замещенного иминогалогенида формулы 9, или с замещенными пропиолатами формулы 10, или с акрилатами формулы 11.
Схема 4
Циклоприсоединение с акрилатами требует дополнительного окисления промежуточного пиразолина до пиразола. Гидролиз сложного эфира формулы 12 дает пиразолкарбоновые кислоты формулы 2b. Предпочтительные иминогалогениды для этой реакции включают трифторметилиминохлорид формулы 9a и иминодибромид формулы 9b. Соединения, такие как представленные формулой 9a, известны (J. Heterocycl. Chem. 1985, 22(2), 565-8). Другие соединения формулы 9, такие как соединения формулы 9b, доступны известными способами (Tetrahedron Letters 1999, 40, 2605).
Другой способ получения пиразолкарбоновых кислот формулы 2b показан на схеме 5.
Схема 5
Пиразолы формулы 13 могут быть конденсированы с арилиодидами с использованием способов, таких как те, о которых сообщалось A. Klapars, J.C. Antilla, X. Huang и S.L. Buchwald, J. Am. Chem. Soc. 2001, 123, 7727-7729, или с арилбороновыми кислотами с использованием способов, таких как те, о которых сообщалось P.Y.S. Lam, C.G. Clark, S. Saubern, J. Adams, M.P. Winters, D.M.T. Chan и A. Combs, Tetrahedron Lett. 1998, 39, 2941-2944. Полученные аддукты формулы 15 могут быть окислены окислителями, такими как перманганат калия, до образования пиразолкарбоновых кислот формулы 2b.
Исходные пиразолы формул 6 и 13 являются известными соединениями или могут быть получены согласно известным способам. Например, пиразол формулы 6a (соединение формулы 6, где R4 представляет CF3) может быть получен путем описанных в литературе процедур (J. Fluorine Chem. 1991, 55(1), 61-70). Пиразолы формулы 6b (соединения формулы 6, где R4 представляет Cl или Br) могут быть получены путем процедуры, описанной в Chem. Ber. 1966, 99(10), 3350-7.
Применимый альтернативный способ получения соединения формулы 6b изображен на схеме 6.
Схема 6
Металлирование сульфамоилпиразола формулы 16 н-бутиллитием с последующим непосредственным галогенированием аниона или гексахлорэтаном (для R4, обозначающего Cl), или 1,2-дибромтетрахлорэтаном (для R4, обозначающего Br) дает галогенированные производные формулы 17a. Удаление сульфамоилгруппы трифторуксусной кислотой (TFA) при комнатной температуре происходит четко и с хорошим выходом с образованием пиразолов формулы 6c. Специалисту в этой области будет понятно, что формула 6c является таутомером формулы 6b.
Пиразолкарбоновые кислоты 2 могут быть также получены окислением пиразолина формулы 18 до получения пиразола формулы 19 с последующим гидролизом до карбоновой кислоты, как показано на схеме 7.
Схема 7
Окислителем может быть пероксид водорода, органические пероксиды, персульфат калия, персульфат натрия, персульфат аммония, моноперсульфат калия (например, Oxone®) или перманганат калия. Такое окисление может быть проведено в присутствии растворителя, предпочтительно простого эфира, такого как тетрагидрофуран, п-диоксан и тому подобное, органического сложного эфира, такого как этилацетат, диметилкарбонат и тому подобное, или полярного апротонного органического соединения, такого как N,N-диметилформамид, ацетонитрил и тому подобное.
Галогенпиразолины 18, где R4 представляет Cl или Br, могут быть получены из пиразолонов формулы 20 обработкой соответствующим галогенирующим агентом, как показано на схеме 8.
Схема 8
Галогенирующие реагенты, которые могут быть использованы, включают оксигалогениды фосфора, тригалогениды фосфора, пентагалогениды фосфора, тионилхлорид, дигалогентриалкилфосфораны, дигалогентрифенилфосфораны, оксалилхлорид и фосген. Предпочтительны оксигалогениды фосфора и пентагалогениды фосфора. Типичные растворители для этого галогенирования включают галогенированные алканы, такие как дихлорметан, хлороформ, хлорбутан и тому подобное, ароматические растворители, такие как бензол, ксилол, хлорбензол и тому подобное, простые эфиры, такие как тетрагидрофуран, п-диоксан, диэтиловый простой эфир и тому подобное, и полярные апротонные растворители, такие как ацетонитрил, N,N-диметилформамид и тому подобное. Необязательно может быть добавлено органическое основание, такое как триэтиламин, пиридин, N,N-диметиланилин или тому подобное. Возможно также добавление катализатора, такого как N,N-диметилформамид.
В альтернативном случае соединения формулы 18, где R4 представляет галоген, могут быть получены обработкой соответствующих соединений формулы 18, где R4 представляет другой галоген (например, Cl для получения соединения формулы 18, где R4 представляет Br) или сульфогруппу, такую как метансульфонат, бензолсульфонат или п-толуолсульфонат, бромистым водородом или хлористым водородом соответственно. Этим способом галоген или сульфозаместитель R4 исходного соединения формулы 18 замещают на Br или Cl от бромистого водорода или хлористого водорода соответственно. Исходные соединения формулы 18, где R4 представляет Cl или Br, могут быть получены из соответствующих соединений формулы 20, как уже описано. Исходные соединения формулы 18, где R4 представляет сульфогруппу, могут быть получены подобным образом из соответствующих соединений формулы 20 стандартными способами, такими как обработка сульфонилхлоридом (например, метансульфонилхлоридом, бензолсульфонилхлоридом или п-толуолсульфонилхлоридом) и основанием, таким как третичный амин (например, триэтиламин), в подходящем растворителе, таком как дихлорметан.
Пиразолкарбоновые кислоты формулы 2c, где R4 представляет OCHF2 или OCH2CF3, могут быть получены способом, охарактеризованным в общих чертах на схеме 9.
Схема 9
В этом способе вместо галогенирования, как показано на схеме 8, соединение формулы 20 окисляют до соединения формулы 21. Условия реакции для этого окисления являются такими, как уже описано для превращения соединения формулы 18 в соединение формулы 19 на схеме 7. Соединение формулы 21 может быть затем алкилировано, чтобы получить соединение формулы 22 путем контактирования с дифторкарбеном, полученным in situ из CHClF2 в присутствии основания. Соединение формулы 21 также может быть алкилировано, чтобы получить соединение формулы 24, путем контактирования с алкилирующим агентом CF3CH2Lg в присутствии основания. Реакцию алкилирования обычно проводят в растворителе, который может содержать простые эфиры, такие как тетрагидрофуран или диоксан, и полярные апротонные растворители, такие как ацетонитрил, N,N-диметилформамид, и тому подобное. Основание может быть выбрано из неорганических оснований, таких как карбонат калия, гидроксид натрия или гидрид натрия. Предпочтительно реакцию проводят, используя карбонат калия с N,N-диметилформамидом или ацетонитрилом в качестве растворителя. В алкилирующем агенте CF3CH2Lg Lg представляет нуклеофуг (т.e. уходящую группу), такой как галоген (например, Br, I), OS(O)2CH3 (метансульфонат), OS(O)2CF3, OS(О)2Ph-п-CH3 (п-толуолсульфонат) и тому подобное. Продукт формулы 22 может быть выделен обычными техническими приемами, такими как экстракция. Сложные эфиры могут быть затем превращены в карбоновые кислоты формулы 2c способами, уже описанными для превращения формулы 12 в формулу 2b на схеме 4.
Соединения формулы 20 могут быть получены из соединений формулы 25, как показано в общих чертах на схеме 10.
Схема 10
В этом способе соединение гидразина формулы 25 приводят в контакт с соединением формулы 26 (может быть использован сложный эфир фумаровой кислоты (фумарат), или сложный эфир малеиновой кислоты (малеат), или их смесь) в присутствии основания и растворителя. Основанием обычно является соль алкоксид металла, такая как метоксид натрия, метоксид кали