Иммуногенная композиция и способ разработки вакцины, основанной на вич, инактивированном псораленом
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, вирусологии и медицины. Раскрыта иммуногенная композиция предварительно определенных инактивированных штаммов вируса иммунодефицита человека (ВИЧ). Инактивацию проводят с помощью псоралена и ультрафиолетового излучения. Композицию делают более эффективной удалением структуральных особенностей ВИЧ, которые мешают иммунному ответу. В частности, сиаловую кислоту удаляют для усиления иммунного распознавания композиции и для ослабления связывания комплиментарного Фактора Н. Также для предотвращения связывания комплиментарного Фактора Н удаляют CD55 и CD59. Определение штаммов для инактивации можно осуществлять с помощью иммунотерапевтического генотипирования или вероятностной оценки риска заражения. Изобретение может быть использовано в медицине. 3 н. и 27 з.п. ф-лы, 3 ил.
Реферат
ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Данная заявка испрашивает приоритет по заявке США с временным номером 60/513827, дата подачи 23.10.2003.
ПРЕДПОСЫЛКИ ДАННОГО ИЗОБРЕТЕНИЯ
Область данного изобретения
[0002] Данное изобретение касается области вирусологии и иммунологии. В частности, но не исключительно, оно касается способа индуцирования иммунного ответа на ВИЧ с использованием композиции инактивированного псораленом ВИЧ и субстанции для достижения этого.
Описание известного уровня техники
Вирус Иммунодефицита человека
[0003] Вирус иммунодефицита человека (ВИЧ) является ретровирусом медленной или лентивирусной группы и вызывает Синдром Приобретенного Иммунного Дефицита (СПИД). Некоторые ретровирусы, которые поражают иммунную систему, такие как ВИЧ-1, являются вариабельными и быстро мутируют, образуя много штаммов варьирующей генетической композиции, что затрудняет попытки разработать эффективное лечение. Эти штаммы, которые можно разделить на группы или подтипы, обладают индивидуальными биологическими свойствами. Последовательности в подтипе можно разделить на генетические кластеры или сходства, которые иногда показывают их общее происхождение. Однако вариации в скорости эволюции могут вызвать различия среди мутаций даже в пределах подтипа. Кроме того, тенденция ретровирусов рекомбинироваться с родственными ретровирусами усложняет вирусный геном.
[0004] ВИЧ использует свою РНК как матрицу для образования вирусной ДНК в клетках-мишенях путем обратной транскрипции, затем вирусная ДНК может объединиться с ДНК инфицированного хозяина. ВИЧ инфицирует клетки, имеющие поверхностный CD4, такие как лимфоциты, моноциты, дендритные клетки и макрофаги, и разрушает CD4+ хелперные Т-лимфоциты. Этот процесс, в частности, касается двух гликопротеинов ВИЧ. Этими гликопротеинами являются gp120 (Env гликопротеин, компонент связывания внешнего рецептора) и связанный нековалентной связью партнер gp41 (Env трансмембранный гликопротеин). Gp120 и gp41 объединены в трехмерную единицу, причем три молекулы gp120 выступают на поверхности вириона и соединены с тремя молекулами gp41 в вирусной липидной мембране. Gp 120 связывается с рецептором CD4 на поверхности хелперных Т-клеток. Это связывание обычно является высокоаффинным и может также усиливаться высоким содержанием сиаловой кислоты на поверхности вируса; сиаловая кислота снижает пороговое значение энергии связывания, необходимое для преодоления отталкивающих электростатических сил. Затем вирус начинает сливаться с Т-клеткой, производя структуральные или конформационные изменения и оголяя другие рецепторы. При слиянии фрагмент gpl20 отшелушивается, оголяя эктодомен gp41 в процессе, который также изменяет конформацию. Тогда Gp41 становится доступным для построения пептидных доменов слияния для связывания с клеткой-мишенью. Это приводит к проникновению ВИЧ и инфицированию клетки-мишени.
[0005] Оболочка ВИЧ начинает формирование с плазматической мембраны клетки хозяина, когда вирус прорастает сквозь клеточную мембрану. Таким образом, оболочка включает липидные и белковые компоненты клетки-хозяина (Frank, Ines, Heribert Stoiber, et al., Vol.10, pp.1611-20 (1996); Stoiber, Heribert, etal., Vol.15, pp.649-74 (1997)). Некоторые вирусы с оболочкой используют белки шипов для имитации молекул хозяина для связывания с рецепторами клетки хозяина и проникновения в другие клетки-мишени. Однако эти шипы могут также являться антигенными поверхностями для распознавания иммунной системой. Однако ВИЧ пытается защититься. В дополнение к вариабельности конформационных изменений gp120 обеспечивает другие особенности поверхности, которые маскируют его от иммунного выявления и разрушения, такие как покрытие гликопротеинов, ковалентно связанные остатки сиаловой кислоты или пространственная помеха (Haurum, John, Treffen Thiel, et al., Vol.7(10), pp.1307-13 (Oct. 1993); Sande, Merle, et al.. The Medical Management of Aids, (6th ed. 1999); Cohen, P.Т., The AIDS Knowledge Base, (3rd ed. Feb 1999)).
[0006] Ядро вириона ВИЧ функционирует как руководящий центр. Внутри вирион ВИЧ представляет собой капсидную комбинацию вирусных белков р24 (СА). Капсид также имеет две отдельные цепи РНК, каждая цепь обеспечивает копирование девяти генов ВИЧ, которые кодируют 15 белков. Три гена из девяти (gag, pol и env) считаются основными. В геноме из 9 тысяч пар нуклеотидов РНК обнаружены шесть дополнительных генов (vif, vpu, vpr, tat, rev и nef). Более детально, ген env содержит информацию или код об образовании gp160, который распадается на gp120 и gp41. Подобным образом, ген gag кодирует матрицу (р17 или МА), капсид (р24 или СА), нуклеокапсид (р9 или NC) и р6. Ген pol обеспечивает генетическую информацию о продуцировании вирусом фермента обратной транскриптазы, а также интегразы и фермента RNAseH. Остальные шесть генов (vif, vpu, vpr, tat, rev и nef) являются регуляторными и управляют механизмами инфицирования и репликации. Среди прочих, ген nef содержит информацию об эффективной репликации, в то время как vpu содержит информацию о регулировании высвобождения новых вирусных частиц из инфицированной клетки хозяина. В конце концов, для того чтобы ВИЧ инфицировал клетку-мишень, он должен ввести генетический материал в цитоплазму клеток-мишеней.
[0007] Как отмечено выше, полагают, что ген nef помогает эффективной репликации ВИЧ. Образование новой вирусной частицы происходит в мембране клетки хозяина. Обнаружили, что nef воздействует на среду инфицированной клетки путем, который оптимизирует репликацию. Вирусные белки собираются около мембраны клеток хозяина, прорастают наружу из мембраны и отслаиваются. Эти белки являются тремя структуральными белками (gp160, gp120, gp41), плюс два других внутренних предшествующих полипротеина (Gag и Gag-Pol). Белок Gag-Pol несет две цепочки положительной РНК в выпячивании, тогда как протеаза вырезается свободно. После прорастания вируса протеаза свободно вырезается и разрезает остальные белки Gag или Gag-Pol, высвобождая различные структуральные белки и обратную транскриптазу. Вирусные белки не являются функциональными до тех пор, пока они не отделятся протеазой. Таким образом, протеаза отвечает за расщепление Gag-Pol и меньшего полипротеина Gag на структуральные белки. Высвобожденные белки р24, р7 и р6 образуют новый капсид, в то время как основой липидной мембраны является р24. В этом процессе gp160 распадается на gp120 и gp41 действием фермента хозяина.
[0008] Большинство вакцин ВИЧ используют части гликопротеинов оболочки (gp160, gp120 и gp41) при попытке индуцировать образование нейтрализующих антител против шипов оболочки вируса (Johnston, et al., 2001). Некоторые попытки в продуцировании высокого титра нейтрализующих антитела были успешны. Идея этого подхода заключается в том, что антитела, которые связываются с этими гликопротеинами, нейтрализовали бы вирус и предотвратили инфекцию. Затем функционирующая иммунная система могла бы активировать систему комплемента, которая каскадно лизировала бы и разрушала вирус. Система комплемента представляет собой ряд циркулирующих белков, который "комплементирует" роль антител. Компоненты системы комплемента последовательно активируются или разворачиваются, что является каскадом комплемента. Завершением комплемента является протеиновый мембраноатакующий комплекс (МАК), который стремится прикрепиться к поверхности проникающего организма и разрушить его прокалыванием клеточной мембраны.
[0009] Однако ВИЧ предусматривает дополнительную защиту от гуморального иммунного ответа. ВИЧ будет активировать системы комплемента человека даже при отсутствии специфических антител. Эта активация была бы вредной для вируса, если бы комплемент оставался свободным для достижения МАК, запускающего лизис вируса. Однако ВИЧ избегает лизис вируса, включая в свою структуру различные молекулы (например, CD55, CD59), которые регулируют комплемент. ВИЧ включает эти молекулы клеточной мембраны в вирусную мембрану при прорастании из инфекционных клеток или присоединением к gp41 и gp120. Комплементарный Фактор Н может включаться в структуры gp41 и gp120. Фактор Н ингибирует активность С3b, молекулы, которая является центральной для каскада комплемента. Это взаимодействие с компонентами комплемента позволяет ВИЧ использовать активацию комплемента для усиления инфективности, фолликулярной локализации и расширения диапазона клеток-мишеней.
Вакцинная терапия и предшествующий уровень техники
[0010] Иммунотерапия включает использование или стимулирование иммунной системы в отношение условия или чувствительности. Вакцины являются формой иммунотерапии. В 1955 году доктор Солк ввел полиовирусную вакцину; для того чтобы эту вакцину ввести пациентам, вирус убивали или делали его неинфективным или неактивным путем химической обработки формальдегидом (формалином). В 1961 году доктор Сэбин ввел вакцину живого аттеньюированного относительно авирулентного полиовируса. Вакцина Сэбина в основном составлена из вирусных мутантов, способных элиситировать иммунный ответ, но не способных к значительной активной репликации или вирулентности, и поэтому считалась относительно безопасной при использовании для человека.
[0011] Существовали эффективные вакцины против ретровирусов у животных. Одна вакцина предпочтительна против ретровируса иммунодефицита кошачьих (или FIV) (т.е. Fel-O-Vax); вторым примером является вакцина против вируса инфекционной анемии у лошадей (или EIAV, т.е. EIAV(UK)deltaS2), серьезной ретровирусной инфекции лошадей. Эти вакцины надежно свидетельствуют о том, что вакцины могут работать против ретровирусов, хотя ни одна болезнь не является идеальной моделью ВИЧ у людей (Beyer, 2003).
[0012] Однако трудно получить вакцину против ВИЧ. Подавляющее большинство вакцин при исследовании, изучении или опытах включает или "живые" аттеньюированные вирусные частицы, или целые инактивированные вирусные частицы. Использование и изучение рекомбинантной технологии, аденовирусные векторы, вакцины на основе ДНК или их комбинации установили границы иммунологии, возлагая некоторые надежды на применение к ВИЧ. Такие иммуногенные композиции применяют в следующих целях:
- для усиления иммунной системы индивидуума, который уже инфицирован системным заболеванием;
- для предупреждения заражения индивидуума болезнью после воздействия;
- для предупреждения заражения индивидуума болезнью до воздействия; на сегодня это наиболее общее применение вакцины;
- для предупреждения заражения пациента различными штаммами ВИЧ, особенно у пациентов, не поддающихся лечению, или иммуносупрессивных;
- для предотвращения вертикальной передачи от матери плоду или от матери новорожденному; для облегчения протекания ВИЧ заболевания у ВИЧ-отрицательного пациента, если он впоследствии заразится этой болезнью;
- для изучения потенциальных композиций и способов для достижения любой определенной выше цели.
К сожалению, медицина нуждается в определении иммунности к ВИЧ (Gonsalves, Gregg, Basic Science (2000); Cohen, 1999). Это фундаментальная проблема с важным последствием: не известно ни одного коррелята защиты от ВИЧ. Однако существуют хорошо охарактеризованные корреляты развития болезни, такие как вирусные нагрузки и подсчет CD4. Кроме того, нет доказательства, что любая из современных кандидатных вакцин может вызывать ответы у ВИЧ-положительных пациентов, которые улучшили бы эти параметры (вирусные нагрузки и подсчеты CD4) в течение длительного периода (Beyrer, Chris, "The HIV/ATOS Vaccine Research: An Update." The Hopkins Report (Jan. 2003)). Кроме того, в то время как наблюдали улучшение у некоторых животных моделей, не существует подтвержденной системы животной модели для испытания вакцин-кандидатов, очевидно ограничение при работе с высоколетальным патогеном, таким как ВИЧ (Beyrer, 2003). Обычная продолжительность жизни после заражения ВИЧ составляет приблизительно 10-15 лет. Усовершенствованием была бы даже вакцина, которая не в состоянии предотвратить передачу, но удлиняющая продолжительность жизни зараженного пациента.
[0013] В исследовании и медицинской практике применяются инактивированные вирусы. Фактически, большинство успешных раннее созданных вакцин основывались на инактивированном вирусе. Инактивация делает вирус неинфективным, но который все же индуцирует иммунный ответ, основанный на его остаточных свойствах. Инактивированный вирус обычно образуется из групп вирулентного штамма, выращенных в культуре клеток или в животных. Затем потенциально вирулентный штамм делают неинфективным или инактивированным химической обработкой. Вирусы по определению являются нежизнеспособными объектами; они не потребляют кислород и питательные вещества, не образуют продукты обмена веществ; они реплицируются с помощью их хозяина, как описано выше для ВИЧ. Вирусам не присуща метаболическая активность, и они не образуют аденозин трифосфат (АТФ). Однако вакцина из живых вирусов способна к репродукции, в то время как вакцина из убитых вирусов не способна. В общем, '"живые" вакцины более эффективны, чем "убитые" вакцины.
[0014] Если вирус инактивирован, иммуногенная композиция, основанная на инактивированном вирусе, чтобы быть полезной, должна сохранять его антигенность. Процесс инактивации должен сохранить пространственную структуру вируса, в то же время устраняя его вирулентность. Для инактивации или "убивания" вируса подходят многие способы, но большинство разрушают или изменяют пространственную структуру вириона, нарушая его антигенные свойства. Первоначально использовали обработку формальдегидом (формалином); например, полиовирусная вакцина Солка была получена инактивированием формалином трех вирусных серотипов. Несмотря на широкое применение в ранних вакцинах, формалин тяжело удаляется и поэтому создается опасность остаточной токсичности. В последнее время для химической инактивации вируса обычно применяют β-проприолактон, так как остаточные количества реагента можно легко гидролизовать в нетоксичный продукт. Hearst и др. в патенте США №4169204 для инактивации вирусов при производстве вакцин предложили использовать псоралены с облучением. Псоралены привлекают из-за их способности инактивировать вирус без повреждения структуры и без вредного остатка (Hanson, C.V., Bloodcells, Vol.18(1), pp.7-25 (1992)). Псоралены в природе встречаются в растениях, включая липу и сельдерей, которые используют псоралены для защиты от насекомых и грибов.
[0015] Как отмечено выше, известно общее понятие использования псоралена для инактивации вируса. Например, в патенте США №5106619 раскрыта псораленовая инактивация живого вируса для получения вакцин. Это изобретение касается обработки или инактивации вирионов с помощью фурокумаринов, включая 4'-аминометил-4,5',8-триметилпсоралена гидрохлорид (АМТ), и ультрафиолета в среде с ограниченным кислородом. Инактивация направлена на вирусы с двойной и одинарной цепочкой ДНК, вирусы с двойной и одинарной цепочкой РНК и вирусы с оболочкой и без оболочки. Это описание было общим, и конкретно не рассматривало ВИЧ.
[0016] Некоторые изобретатели рассматривают применение псоралена в ВИЧ вакцине или композиции. В патенте США №6107543 раскрыт иммуноген целой частицы ВИЧ, который предпочтительно инактивирован гамма-радиацией; также раскрыты, однако являются разновидностью альтернативной инактивации, способы, включающие псорален, формалин, β-проприолактон и т.д. Целую частицу обрабатывают для удаления внешних белков оболочки gp120 или gp160, сохраняя остаток структуры. В альтернативном варианте осуществления редуцированный иммуноген, включающий оставшиеся очищенные продукты гена, такие как кодируемые генами gag, генами ро1, трансмембранный белок gp41 или оставшиеся гены генома ВИЧ.
[0017] Патенты США №6383806 и №6503753 раскрывают композицию и способ разработки ВИЧ вакцины, основанной на псораленовой фотоинактивации обратной транскриптазы (RT). Другими словами, целью этого изобретения является создание условий для иммунного ответа, основанного на инактивации отдельного фермента ВИЧ. Сохранение остатка частицы, как считают, усиливает иммунный ответ на композицию.
[0018] Хотя псорален описывается изобретателями для использования в иммуногене ВИЧ или вакцине, ни один не рассматривал определенное структурное сохранение продуктов, присущих псораленовой инактивации ВИЧ. Например, ВИЧ является высокоиммуногенным, часто изменяющим структуры в процессе обратной транскрипции. Мутация может предусматривать средства для избежания штаммом ВИЧ иммунного ответа, вызванного вакциной (Cohen, 1999). Кроме того, сохранение структуры ВИЧ может привести к сохранению компонентов, которые нарушают иммунный ответ.
[0019] Последние попытки не сосредотачивали внимание на проблемах мутации. ВИЧ является высокомутагенным ретровирусом, который с помощью обратной транскриптазы преобразовывает свою РНК в ДНК. Обратная транскриптаза склонна к ошибкам, что приводит к мутации. Кроме того, быстрая репликация усиливает мутацию. Высокий уровень геномного разнообразия у ВИЧ усложняет диагноз, лечение и санитарный контроль развития болезни. В частности, это разнообразие проявляется в биологических особенностях, характеризующих инфективность, заразность и иммуногенность. Дивергенция вирусных генотипов ВИЧ внесла свой вклад в полиморфизм, эффективность передачи и историческое эпидемиологическое развитие ВИЧ. Разнообразие подтипов и под-подтипов, каждый из которых имеет специфическую пространственную структуру, может привести к тому, что вакцина из подтипа неэффективна для пациента, инфицированного другим подтипом. Высокая скорость мутации ВИЧ, как полагают, усложняет селекцию соответствующего иммуногена.
[0020] Сохранение структурных компонентов ВИЧ может представлять сложность. Как и в патенте США №5106619, в патентах №№6383806 и 6503753 сохраняются целые частицы. Более поздние изобретения направлены на инактивацию только RT. Сохранение антигенной структуры предназначается для использования преимущества широкого диапазона иммуногенов. Это сохранение корректной антигенной конформации считается важным для проникновения в цитоплазму посредством микропиноцитоза или поглощения дендритными клетками, опосредованного маннозным рецептором. Патент США №6107543 раскрывает способ с инактивацией псораленом, для которого, наоборот, необходимо удаление гликопротеинов оболочки gp120 и gp160 (а не gp41), потому что антитела к этим гликопротеинам могут облегчить поглощение вируса клетками. Фактически, известно, что ВИЧ может связывать и использовать C3b как лиганды, чтобы позволить инфекционным иммунным комплексам связываться с дендритными клетками и В-лимфоцитами. Антитела к gp160 или gp120 иногда приводят к накоплению вируса в лимфатических узлах и селезенке. Подход патента '543, как и других патентов, сохраняет трансмембранный белок gp41 и часть или всю вирусную мембрану.
[0021] Во всяком случае, эта сохраненная вирусная структура может привести к непредусмотренным последствиям. Во-первых, как описано выше, gp160, gp120 и gp41 обеспечивают участки связывания комплементарного Фактора Н (Pinter, Claudia et al. Aids Research and Human Retroviruses, Vol.11(5), pp.577-88 (1995); Pinter, Claudia, et al., Aids Research and Human Retrovinises, Vol.11(8) (1995); Stoiber, Heribert, et al., Immunobiology. Vol.193, pp 98-113 (1995)).Следовательно, сохранение этих структур означает, что Фактор Н будет мешать гуморальному иммунному ответу после вакцинации. Удаление gp120 и gp160 в патенте США №6107543 может до некоторой степени смягчить этот эффект; однако сохранение участка связывания Фактора Н на gp41 работало бы против иммуногенности композиции. Во-вторых, оба подхода молчат относительно клеточной плазматической мембраны и сохраняют часть или всю вирусную мембрану, включая определенные связанные белки, которые мешают иммунному ответу. Как и собирающаяся, реплицирующаяся частица ВИЧ прорастает сквозь плазматическую мембрану инфицированной клетки, мембрана обогащена CD55 (фактором ускорения диссоциации) и CD59 (гомологичным фактором рестрикции), которые регулируют комплемент. Эти молекулы включаются в вирусную мембрану при прорастании из инфицированных клеток. Сохранение некоторых или всех этих особенностей или структур могло мешать активации комплемента и гуморальному ответу (Saifuddm, 1995). В-третьих, компоненты поверхности ВИЧ несут сиаловую кислоту, которая могла остаться на сохраненной структуре инактивированного ВИЧ. Сиаловые кислоты обычно находят на белках хозяина и клеточных структурах; высокое содержание сиаловой кислоты у вируса, даже если вирус был инактивирован, ограничило бы способность хозяина распознавать вирус и должным образом отвечать. Важно, что остатки сиаловой кислоты также используются в связывании Фактора Н (Meri, Seppo, et al., "Discrimination Between Activator and Nonactivators of the Alternative Pathway of complement Regulation: Regulation Via a Sialic acid/Polyanion binding site on Factor Н." Proc. Natl. Acad. Sci., USA, Vol.87(10), pp.3982-6 (May 1990); Blackmore, Т.К., et al., J. of Immunology, Vol.157(12), pp.5422-7 (Dec. 1997); Kuhn, S., et al., Eur. J. Immunol., Vol.26 (10), pp.2383-7 (Oct 1996); Pangbum, M.K., et al., J. of Immunology, Vol.164 (9) (May 2000)). [0022] Данное изобретение направлено на иммуногенную композицию, которая обращена на эти проблемы. Предполагают, что создание композиций, предназначенных для различных подтипов и аспектов ВИЧ, продвинет вперед лечение и исследование. В конечном счете, существует надежда увеличить выживаемость и улучшить качество жизни инфицированных индивидуумов.
[0023] ВИЧ относится к вирусам, чувствительным к инактивации псораленом. Во время процесса инактивации псораленом сохраняется вирусная структура. Это сохранение выгодно для образования обширного ответа, основанного на антигене. В данном изобретении структура инактивированного вируса модифицирована для удаления или нейтрализации выбранных особенностей, которые мешали бы иммунному ответу. В частности, сиаловая кислота и определенные участки связывания комплементарного Фактора Н нейтрализованы; в некоторых случаях может быть удалена внешняя клеточная плазматическая мембрана. Первичный эффект этой обработки должен устранить помеху иммунному гуморальному ответу комплементарным Фактором Н человека и другими регуляторами активности комплемента (RCA). Кроме того, удаление сиаловой кислоты показывает иммунной системе, что компоненты вируса отличны от компонентов хозяина
[0024] Данное изобретение приспособлено к генотипу представленного вируса. ВИЧ легко реплицируется и легко мутирует с помощью обратной транскриптазы и рекомбинации. Каждая группа, подтип, под-подтип и циркулирующий рекомбинант ВИЧ-1 и ВИЧ-2 уникальны по строению. Отсутствие подтипа может нести серьезные последствия. Для того чтобы иммуногенная композиция была эффективной, необходимо принимать во внимание не только вмешательство сохраненной структуры, но и каждой вирусной группы, подтипа, под-подтипа и т.д., представляющих интерес при данных обстоятельствах. Таким образом, вакцина может быть приспособлена к вирусному штамму (штаммам), имеющемуся у хозяина. Соответственно композиция предпочтительно может быть получена из генетически релевантного образца; например, в случае композиции, предназначенной для вакцинации инфицированного хозяина, релевантный образец может быть выделен из индивидуума-хозяина или подобран ему. В случае композиции, предназначенной для вакцинации неинфицированного человека или животного, релевантный образец может основываться на вероятностной оценке риска контакта с источником заражения для этого человека или животного.
[0025] Соответственно данное изобретение является композицией, способной вызывать иммунный ответ, в которой предварительно определенные штаммы ВИЧ, релевантные для применения в композиции, выделены и инактивированы с помощью псоралена и воздействия ультрафиолета. Кроме того, данное изобретение характеризуется удалением из инактивированного ВИЧ определенных особенностей, которые ослабляют иммунный ответ. Композиция также может включать фармакологические носители, стабилизаторы или наполнители.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
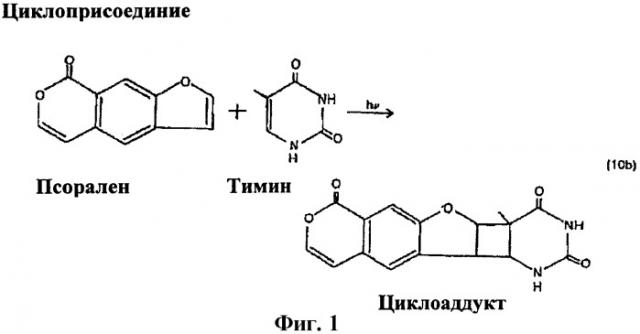
[0026] На Фиг.1 показано образование фотопродукта псоралена с нуклеиновой кислотой после облучения ультрафиолетом.
[0027] На Фиг.2 показана зависимость усиления иммуногенности от увеличения длины полисахарида максимум до 16 моносахаридов.
[0028] Фиг.3 представляет схематический рисунок, на котором показаны структуры цепей С3, CVF и их взаимосвязь.
ОПИСАНИЕ ДАННОГО ИЗОБРЕТЕНИЯ
[0029] Как отмечено выше, известно общее использование псоралена в инактивации ВИЧ для получения композиции или вакцины. Однако изменчивость ВИЧ и его способность мешать иммунному ответу могут снижать эффективность предшествующих мероприятий. Данное изобретение является иммуногенной композицией и способом, направленными на решение проблем, возникших в связи с сохраненными особенностями вирусной структуры, высокой скоростью мутации ВИЧ и устойчивости ВИЧ к иммунному ответу. Данное изобретение относится к иммунотерапии, в которую включено использование или стимулирование иммунной системы при определенном условии или чувствительности. Интересующая иммунная система может быть иммунной системой человека или любого животного, такого как шимпанзе или мышь. Как используется в данном описании, иммунотерапия охватывает приспособление иммуногенной композиции к оптимальной эффективности в условиях высокоизменчивого генотипа совместно с активным влиянием вируса на иммунный ответ. Подразумевается, что улучшения диагностических методик и исследований по данному изобретению вызывают иммунный ответ у животных. Предполагают, что, учитывая разработку эффективной иммуногенной композиции, вакцину можно разработать и ввести с помощью композиции для продуцирования иммунозащитных факторов у пациента.
[0030] Соответственно одним из аспектов данного изобретения является композиция, способная вызывать иммунный ответ, в которой предварительно определенные штаммы ВИЧ, релевантные для применения в композиции, выделены и инактивированы псораленом и воздействием света, а также в которой особенности ВИЧ, ослабляющие иммунный ответ, удалены из инактивированного ВИЧ. Композиция также может включать фармакологически приемлемые носитель, стабилизатор или наполнитель.
[0031] В дополнительном варианте осуществления, предназначенном для применения в качестве вакцины для инфицированного животного, вакцина может включать штаммы, присутствующие у животного на время выделения образца, согласуясь с генотипом вакцины, к той же инфекции. В противном случае профилактическая вакцина может включать интересующие штаммы, основываясь на вероятности заражения. Вакцину можно обработать для удаления особенностей ВИЧ, которые ослабляют иммунный ответ.
[0032] Другим аспектом данного изобретения является способ приготовления иммуногенной композиции, включающий определение штаммов ВИЧ, релевантных для использования в композиции, при инактивировании штаммов используют псорален и воздействие светом, удаляя или модифицируя особенности ВИЧ, которые ослабляют иммунный ответ. В частности, эти особенности или компоненты могут включать участки связывания комплементарного Фактора Н gp160, gp120 и gp41, удаление остатков сиаловой кислоты и необязательно, внешнюю клеточную плазматическую мембрану. Следовательно, способ по данному изобретению получения иммуногенной композиции включает:
1. определение штаммов ВИЧ, вызывающих беспокойство;
2. выделение и культивирование штаммов, вызывающих беспокойство;
3. отделение вируса от культуральной среды;
4. необязательное удаление внешней клеточной плазматической мембраны;
5. добавление псоралена и агента, блокирующего ферменты, репарирующие ДНК;
6. облучение ультрафиолетом;
7. удаление или нейтрализация CD55 и CD59;
8. десиалирование инактивированного вируса.
[0033] Таким образом, данное изобретение является иммуногенной композицией, содержащей подобранную комбинацию подтипов инактивированных псораленом ВИЧ, и способом получения и применения данной композиции.
Определение релевантных штаммов
[0034] Определение штаммов ВИЧ будет зависеть от варианта осуществления и применения данного изобретения. Существует широкий спектр применений для иммуногенных композиций; следовательно, следующее следует рассматривать как пример, а не как ограничение. Определение релевантных штаммов ВИЧ можно разделить на три категории примеров: (i) исследовательские, связанные с разработкой, аналитические; (ii) терапевтические; и (iii) профилактические.
[0035] В одной категории вариантов осуществления иммуногенную композицию можно рассматривать для использования в исследовании или клиническом анализе. Для исследования интересующие штаммы будут определены целями научного поиска. Таким образом, получение, выделение и культивирование вируса ВИЧ будут согласовываться с исследовательским проектом и целями. Определение релевантных штаммов для медицинского исследования может, вероятно, проводиться параллельно какой-либо предусмотренной терапевтической или профилактической потребности, такой как разработка вакцины. Чисто теоретическое исследование может охватить аспекты, такие как разработка исследовательских инструментов или расширение сведений о штаммах, не вызывающих эпидемию ВИЧ. Иммуногенная композиция может также применяться в изучении иммунного ответа, эволюции вируса, эпидемиологии и анализе поведения вируса.
[0036] В следующей категории вариантов осуществления иммуногенная композиция может быть предназначена для введения ВИЧ-инфицированному человеку (или животному или хозяину) возможно как терапевтическая вакцина. В общем, мультивалентные иммуногенные композиции должны быть способны индуцировать иммунный ответ против различных вирусных изолятов; ранее эта мультивалентность включала комбинацию инактивированных вирусных частиц от различных интересующих штаммов. Однако ВИЧ у отдельного хозяина редко является статическим и продолжает эволюционировать посредством генетической мутации и рекомбинации. Прошлые попытки выявить известные штаммы или варианты в мультивалентной вакцине ВИЧ опираются на макроскопические показатели здравоохранения и консервативные образцы штаммов ВИЧ. В данном изобретении штаммы ВИЧ могут быть генотипированы и выделены из образца, полученного у инфицированного человека или животного. То есть мононуклеары периферической крови (РВМС) или другой образец можно выделить для идентификации присутствия ВИЧ у инфицированного человека или животного. Можно использовать любой способ типирования, соответствующий обстоятельствам, включая диагностическое типирование на основании последовательности, анализ гетеродуплексной изменчивости (НМА), генотипирование с помощью реактивов для качественного анализа, молекулярные диагностики, определение продуктов гена и определение продуктов на основании пробы ДНК. Затем вакцину можно составить из штаммов, присутствующих у человека во время выделения образца. Таким образом, в одном варианте осуществления ВИЧ у человека (или животной модели) генотипировали, а информацию использовали для создания сложной вакцины, составленной из исходных компонентов, полученных от инактивированного вируса для каждого из идентифицированных штаммов. Как описано ниже, эта альтернатива может включать вакцину, полученную из вируса, культивированного в человеке РВМС in vitro, или другого образца, выделенного из индивидуума (или животного), который затем подвергается процессу псораленовой инактивации перед повторным введеним этому индивидууму или животному в качестве иммуногена. Таким образом, иммунотерапия приспособлена к генотипу вируса данного хозяина. Методика данного изобретения рассматривает множество образцов для идентификации и направленных изменений в доминировании штамма или композиции в течение длительного времени и, в ответ, облегчает изменения при лечении. После разрушения доминирующего штамма может появиться непохожий, но относительно устойчивый вариант, что потребует дальнейшей иммунотерапии.
[0037] В следующей категории вариантов осуществления иммуногенная композиция может быть предназначена для введения неинфицированному человеку возможно как профилактическая вакцина. В прошлом профилактическая композиция и введение были подобны используемым терапевтическим мультивалентным композициям; такие композиции могли быть основаны на комбинированном использовании вирусных частиц из широкого спектра штаммов, предназначенных для индуцирования обширного иммунного ответа. Такой подход описан как один вариант осуществления данного изобретения в форме профилактики.
[0038] Альтернативно данное изобретение в профилактическом варианте осуществления может также основываться на вероятностной оценке риска заражения для данного индивидуума. Примечательно, что патент США №6503753 описывает персональные профилактические вакцины в случаях, когда риск передачи, прежде всего, исходил из определенного индивидуума; следовательно, инактивированные штаммы можно получать из образца, выделенного от данного инфицированного индивидуума. Такие персональные вакцины могли использоваться как вариант осуществления данного изобретения. Аналогично, лаборанты или работники здравоохранения могут подвергаться усиленному риску профессионального заражения определенными известными штаммами и могут воспользоваться усиленным иммунным ответом на эти определенные штаммы. Альтернативно определение штамма для персональных вакцин может основываться на поведенческих и демографических факторах риска инфекции ВИЧ в интересующих географических областях. Такой анализ мог учитывать поведенческие модели в рамках исторических, эпидемиологических и географических данных, подтверждающих анализ вероятности заражения. В географических областях, где эпидемия распространялась вне групп с поддающимися учету факторами риска, мультивалентная профилактика могла отразить все известные штаммы интересующей географической области.
Получение и приготовление для облучения
[0039] Следующие варианты осуществления считаются примерами, а не ограничениями, поскольку являются признанными способами получения, выделения и культивирования вирусов. Фактически, существующий вирус можно получить различными способами. Можно выбрать индивидуумы, зараженные штаммами ВИЧ, и ВИЧ можно выделить, очистить, культивировать и типировать, используя методики, известные в данной области и частично раскрытые ниже. Такие образцы можно выделить из РВМС или других жидкостей, таких как слюна, или тканей, таких как релевантные слизистые оболочки; однако, как известно в данной области, РВМС будет предпочтительной для включения иммунных компонентов в зависимости от нанесения. Альтернативно, ВИЧ можно приобрести в виде существующих образцов известных коммерческих вирусных стандартов или лабораторных изолятов. Вирусные частицы можно также получить преобразованием клеток вирусными кодирующими векторами, которые поглощаются клеткой как чужеродный генетический материал. Преобразование обычно достигается физическими средствами, такими как совместное осаждение ДНК с нерастворимым хлоридом кальция (Nicholls, Desmond, An Introduction of Genetic Engineering (2nd ed. Feb 2002)). Преобразованная ДНК может находиться в клетке как эписомальный (экстра хромосомный) элемент или объединиться с ядерным геномом. Эффективность переноса ДНК в клетки зависит от используемых специальных методов. Нижеприведенные описания могут быть общими для различных категорий вариантов осуществления, если не указано обратное.
[0040] Данное изобретение рассматривает различные предпочтительные культуральные среды. Первой культуральной средой является РВМС, выделенные из ВИЧ инфицированного хозяина. В этом варианте осуществления клетки реплицировали бы ВИЧ в сохраненной in vitro среде хозяина. Такая среда может быть более безопасной и более простой для последующего введения хозяину. Однако многие культуральные среды, такие как клетки человека или дрожжей, включают ферменты, репарирующие ДНК, которые могут обратить действие псоралена. Эти фермент могут репарировать ДНК или РНК с помощью транскрипции и глобальной геномной репарации. Таким образом, культивирование в РВМС или дрожжевых клетках можно улучшить ингибированием каких-либо ферментов, имеющих тенденцию восстанавливать ДНК и РНК после обработки псораленом и ультрафиолетом. В предпочтительном варианте осуществления такую среду можно обработать ингибиторами репарирующих ферментов, такими как новобиоцин, афидиколин