Способ определения гуминовых кислот в водных средах
Иллюстрации
Показать всеИзобретение относится к количественному анализу питьевых, природных и сточных вод. Способ включает окисление гуминовых кислот и детектирование продуктов их окисления, причем в качестве окислителя применяется молекулярный бром в количестве 0.05-0.25% от массы водной пробы, а детектирование осуществляют методом капиллярной газовой хроматографии. Достигается повышение чувствительности и надежности анализа. 2 табл., 6 ил.
Реферат
Изобретение относится к аналитической химии органических соединений и может быть использовано для определения количественного содержания гуминовых кислот в питьевых, природных и сточных водах.
Наиболее близким по технической сущности к заявляемому решению является метод проточно-инжекционного анализа гуминовых кислот в присутствии N-бромсукцинимида с детектированием хемилюминесценции [J.Michałowski, P.Hałaburda, A. Kojło. Determination of humic acid in natural waters by flow injection analysis with chemiluminescence detection // Analytica Chimica Acta. - 2001. - Vol.438. - P.143-148.]. Недостатками прототипа являются высокий предел обнаружения гуминовых кислот и зависимость результатов количественного анализа от присутствия в воде различных фенольных соединений (фенол, крезолы, хлорфенолы). Следует отметить, что соединения этого класса, как правило, всегда содержатся в природных, питьевых и сточных водах [Елин Е.С. Фенольные соединения в биосфере. - Новосибирск: Изд-во Сибирского отделения Российской академии наук, 2001 - 386 с.].
Задачей изобретения является разработка более эффективного способа, позволяющего снизить предел обнаружения и исключить влияние фенольных соединений на результаты количественного анализа гуминовых кислот в водных средах. В этом состоит технический результат.
Решение поставленной задачи достигается тем, что в способе определения гуминовых кислот в водных средах, включающего окисление гуминовых кислот и детектирование продуктов их окисления, новым является то, что в качестве окислителя применяется молекулярный бром в количестве 0.05-0.25% от массы водной пробы, а детектирование осуществляют метом капиллярной газовой хроматографии.
Согласно современным представлениям гуминовые кислоты относят к полиэлектролитам со слабо выраженными кислотными свойствами и проявляющими высокую реакционную способность, связанную с наличием в их структуре большого числа карбоксильных и фенолгидроксильных групп.
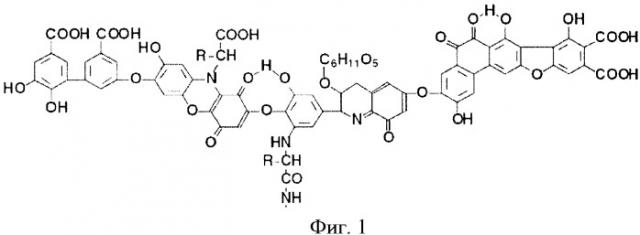
На фиг.1 приведена гипотетическая формула гуминовой кислоты (по Стивенсону).
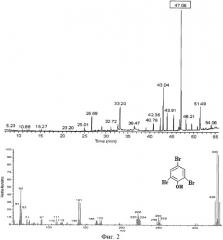
В присутствии сильного окислителя - молекулярного брома происходит окисление гуминовых кислот с образованием различных низкомолекулярных органических соединений. На фиг.2 приведена хроматограмма экстракта природной воды, предварительно обработанной молекулярным бромом и масс-спектр соединения с временем удерживания 47.06 мин. Этот пик является самым интенсивным на хроматограмме и принадлежит 2,4,6-трибромфенолу.
Таким образом, фенол выбран нами в качестве вещества, на котором основан способ косвенного определения гуминовых кислот в воде. Присутствие в экстракте фенола в виде 2,4,6-трибромфенола неслучайно, поскольку он легко взаимодействует с молекулярным бромом в воде по реакции электрофильного замещения с количественным образованием трибромпроизводного [Нейланд О.Я. Органическая химия. - М.: Высш. шк., 1990. - 751 с.].
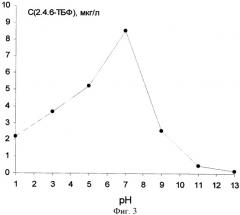
Оптимальное значение pH водного раствора, при котором происходит наиболее эффективное окисление гуминовых кислот, соответствует нейтральной среде (фиг.3). Это связано, на наш взгляд, с одновременным присутствием в воде двух сильных окислителей Br2 и HBrO [Ксензенко В.И., Стасиневич Д.С. Химия и технология брома, йода и их соединений. - М.: Химия, 1995. - 432 с.]:
Br2+H2O⇔Н++Br-+HBr.
Снижение окислительной активности в кислой и щелочной среде связано с тем, что в результате смещения равновесия гидролиза в кислой среде окислителем выступает преимущественно молекулярный бром, а в щелочной - HBrO.
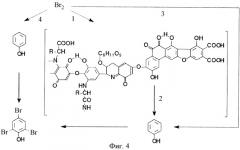
Процессы, происходящие в водном растворе гуминовых кислот в присутствии молекулярного брома, показаны на фиг.4: 1 - окисление гуминовых кислот бромом; 2 - образование фенола при окислении гуминовых кислот; 3 - бромирование фенола, образовавшегося при окислении гуминовых кислот; 4 - бромирование нативного фенола, присутствующего в воде до окисления гуминовых кислот.
Для учета нативного фенола бромирование одной и той же пробы проводят дважды: в нейтральной среде и сильнокислой (pH 1). В этом случае прирост концентрации 2,4,6-трибромфенола в нейтральной среде по сравнению кислой будет связан только с фенолом, образовавшимся при окислении гуминовых кислот, и пропорционален их содержанию в анализируемой пробе воды.
Способ определения гуминовых кислот в водных средах включает три этапа:
1) Окисление гуминовых кислот - обработка исследуемого водного образца молекулярным бромом. Одновременно с окислением гуминовых кислот протекает процесс бромирования образующегося при их окислении фенола. При комнатной температуре (20±5°С) реакция бромирования фенола завершается в течение 3 мин с количественным образованием 2,4,6-трибромфенола.
2) Жидкостная экстракция 2,4,6-трибромфенола. Эта стадия предназначена для перевода 2,4,6-трибромфенола в более удобную для последующего газохроматографического анализа органическую фазу, повышения его концентрации в экстракте и отделения мешающих компонентов.
Химическая модификация фенола в 2,4,6-трибромфенол значительно снижает его растворимость в воде, что приводит к его эффективному извлечению из водной фазы в органический растворитель (до 98%).
3) Анализ экстракта методом газовой хроматографии. Полученный экстракт 2,4,6-трибромфенола анализируют методом капиллярной газовой хроматографии с детектором электронного захвата (ДЭЗ). Галогенселективный ДЭЗ обеспечивает максимально возможное по чувствительности газохроматографическое определение 2,4,6-трибромфенола.
Определение гуминовых кислот выполняют по следующей методике. В мерную колбу помещают 1000 см3 анализируемой пробы. Исходный объем пробы делят на две равные части, одну из которых подкисляют раствором серной кислоты до значения pH 1. В обе части пробы добавляют бромную воду; расчетное содержание молекулярного брома в пробе 0.05-0.25%. Бромирование проводят в течение 3 мин. После завершения бромирования избыток брома удаляют раствором тиосульфата натрия; расчетная концентрация в пробе - 0.01 моль/дм3. Затем в обе части пробы вводят внутренний стандарт (2,4,6-трихлорфенол); расчетная концентрация в пробе - 0.5 мкг/дм3 и проводят экстракцию образовавшегося 2,4,6-трибромфенола 11 см3 толуола в течение 10 минут. После расслаивания фаз отбирают по 10 см3 экстракта, вводят 0.5 мл раствора щелочи (0.1 М) и реэкстрагируют 2,4,6-трибромфенол в течение 3 мин. После расслаивания фаз удаляют 9.5 см3 экстракта, нейтрализуют реэкстракт раствором серной кислоты до pH 2-3 и повторно экстрагируют в течение 3 мин. Полученные экстракты анализируют на газовом хроматографе с ДЭЗ.
Условия газохроматографического определения: температура детектора 320°С, испарителя 320°С, термостата колонок 200°С; кварцевая капиллярная колонка 30 м × 0.25 мм × 0.25 мкм со слабополярной неподвижной жидкой фазой (SE-30, SE-52, SE-54), скорость потока газа-носителя (азот, ос.ч.) через колонку 1.0 см3/мин, поддув детектора 20 см3/мин, деление потока 1:30. Хроматограмма экстракта, полученная при анализе стандартного раствора гуминовых кислот с концентрацией 10 мкг/дм3, приведена на фиг.5 (ВС - 2,4,6-трихлорфенол (внутренний стандарт); 2,4,6-ТБФ - 2,4,6-трибромфенол).
Идентификацию 2,4,6-трибромфенола в анализируемой пробе воды проводят по относительному времени удерживания tx*:
tx*-tx/tcт,
где tx и tcт - исправленные времена удерживания компонентов анализируемой пробы и внутреннего стандарта соответственно.
Относительные времена удерживания компонентов анализируемой пробы сравнивают с относительным временем удерживания 2,4,6-трибромфенола, полученного для стандартного раствора: tх*(2,4,6-трибромфенол)=2.981.
На основе полученных хроматограмм находят приращение фенола:
ΔS(фенол)=S(фенол/pH 7)-S(фенол/pH 1)
где S(фенол/pH 1) - отношение площадей пика 2,4,6-трибромфенола и внутреннего стандарта на хроматограмме той части пробы, бромирование которой поводили при значении pH 1;
S(фенол/pH 7) - отношение площадей пика 2,4,6-трибромфенола и внутреннего стандарта на хроматограмме той части пробы, бромирование которой поводили без добавления кислоты.
Массовую концентрацию гуминовых кислот в анализируемой пробе воды рассчитывают по уравнению, полученному на основе градуировочного графика для стандартных растворов гуминовых кислот (таблица 1):
С(ГК)=160.79ΔS(фенол)-0.11(R2=0.9986)
| Таблица 1 | |
| Результаты газохроматографического анализа стандартных растворов гуминовых кислот | |
| С (ГК), мкг/дм3 | ΔS (фенол) |
| 10 | 0.052 |
| 30 | 0.189 |
| 45 | 0.287 |
| 75 | 0.48 |
| 125 | 0.768 |
На фиг.6 приведена градировочная зависимость массовой концентрации гуминовых кислот (стандартные растворы) от приращения фенола ΔS (фенол). Стандартные растворы гуминовых кислот были приготовлены на основе препарата фирмы Aldrich (Humic acid, sodium salt, technical grade, cat: H1, 675-2). Аналогичный препарат применяется и в способе, выбранном в качестве прототипа.
Примеры осуществления способа
Пример 1
В мерную колбу помещают 1000 см3 анализируемой пробы. Исходный объем пробы делят на две равные части, одну из которых подкисляют раствором серной кислоты до значения pH 1. В обе части пробы добавляют бромную воду; расчетное содержание молекулярного брома в пробе 0.0005%. Бромирование проводят в течение 3 мин. После завершения бромирования избыток брома удаляют раствором тиосульфата натрия; расчетная концентрация в пробе - 0.01 моль/дм3. Затем в обе части пробы вводят внутренний стандарт (2,4,6-трихлорфенол); расчетная концентрация в пробе - 0.5 мкг/дм3 и проводят экстракцию образовавшегося 2,4,6-трибромфенола 11 см3 толуола в течение 10 минут. После расслаивания фаз отбирают по 10 см экстракта, вводят 0.5 мл раствора щелочи (0.1 М) и реэкстрагируют 2,4,6-трибромфенол в течение 3 мин. После расслаивания фаз удаляют 9.5 см3 экстракта, нейтрализуют реэкстракт раствором серной кислоты до pH 2-3 и повторно экстрагируют в течение 3 мин. Полученные экстракты анализируют на газовом хроматографе с ДЭЗ.
Способ неосуществим, так как предел обнаружения гуминовых кислот при содержании брома в пробе 0.0005% составляет 480 мкг/дм3, что выше, чем по прототипу.
Пример 2.
Содержание брома в пробе - 0.005%. Анализируют, как указано в примере 1. Предел обнаружения - 150 мкг/дм3. Способ неосуществим, так как предел обнаружения гуминовых кислот выше, чем по прототипу.
Пример 3.
Содержание брома в пробе - 0.05%. Анализируют, как указано в примере 1. Предел обнаружения - 5.0 мкг/дм3. Способ осуществим.
Пример 4.
Содержание брома в пробе - 0.10%. Анализируют, как указано в примере 1. Предел обнаружения - 5.0 мкг/дм3. Способ осуществим.
Пример 5.
Содержание брома в пробе - 0.15%. Анализируют, как указано в примере 1. Предел обнаружения - 5.0 мкг/дм3. Способ осуществим.
Пример 6.
Содержание брома в пробе - 0.20%. Анализируют, как указано в примере 1. Предел обнаружения - 5.0 мкг/дм3. Способ осуществим.
Пример 7.
Содержание брома в пробе - 0.25%. Анализируют, как указано в примере 1. Предел обнаружения - 5.0 мкг/дм3. Способ осуществим.
Результаты определения гуминовых кислот в воде предлагаемым способом приведены в табл.2.
| Таблица 2 | |||
| Примеры осуществления способа | |||
| № примера | Содержание брома по отношению к массе пробы, % | Достигаемый предел обнаружения, мкг/дм3 | Возможность осуществления заявляемого способа |
| По прототипу | - | 14 | - |
| 1 | 0.0005 | 480 | неосуществим |
| 2 | 0.005 | 150 | неосуществим |
| 3 | 0.05 | 5.0 | осуществим |
| 4 | 0.10 | 5.0 | осуществим |
| 5 | 0.15 | 5.0 | осуществим |
| 6 | 0.20 | 5.0 | осуществим |
| 7 | 0.25 | 5.0 | осуществим |
Из примеров 1-7 и табл.2 следует, что предлагаемый способ определения гуминовых кислот осуществим в диапазоне концентраций брома 0.05-0.25% по отношению к массе пробы. Дальнейшее увеличение концентрации брома нецелесообразно, поскольку не оказывает влияния на предел обнаружения гуминовых кислот. При содержании брома менее 0.05% образуется недостаточное количество фенола при окислении гуминовых кислот.
По сравнению с прототипом предлагаемое техническое решение имеет следующие преимущества:
1) Более низкий предел обнаружения гуминовых кислот в воде: 5 мкг/дм3; по прототипу - 14 мкг/дм3.
2) Применение хроматографии на этапе инструментального определения продуктов окисления гуминовых кислот обеспечивает большую селективность их определения; по прототипу - хроматографического разделения не проводиться.
3) Применение более доступного реагента для окисления гуминовых кислот - молекулярный бром; по прототипу - N-бромсукцинимид.
Способ определения гуминовых кислот в водных средах, включающий окисление гуминовых кислот и детектирование продуктов их окисления, отличающийся тем, что в качестве окислителя применяется молекулярный бром в количестве 0,05-0,25% от массы водной пробы, а детектирование осуществляют методом капиллярной газовой хроматографии.