Стабильные фармацевтические составы, которые содержат интерфероны гамма и альфа в синергичных соотношениях
Иллюстрации
Показать всеИзобретение относится к медицине и фармакологии и представляет собой стабильный фармацевтический состав для парентерального применения, который содержат в одном резервуаре фиксированные дозы рекомбинантных интерферонов гамма и альфа 2b для лечения патологических явлений, характеризующихся доброкачественным нефизиологическим или злокачественным клеточным ростом тканей или органов, и который дополнительно содержат фармацевтически приемлемые наполнители или носители. Изобретение обеспечивает повышенную эффективность лечения опухолей за счет синергетического воздействия компонентов состава, а также стабильность составов. 2 н. и 16 з.п. ф-лы, 19 табл., 9 ил.
Реферат
Область техники
Настоящее изобретение относится к биотехнологии и медицине, в частности к стабильным фармацевтическим составам, которые содержат рекомбинантные интерфероны гамма и альфа в синергичных соотношениях, для подавления роста клеток в различных тканях и органах людей.
Предпосылки изобретения
Разнообразие эффектов интерферонов I типа (IFNs) создает широкий терапевтический потенциал по их применению. Применение IFNs является благоприятным для лечения различных видов рака, включая лейкемии (US 5830455), базально-клеточную эпителиому (US 5028422), плоскоклеточную карциному (US 5256410), рак молочной железы (US 5024833), опухоли желудочно-кишечного тракта (US 5444064; 5814640) и старческий кератоз (US 5002764). Различные типы клеток проявляют разную чувствительность к IFNs, и ингибирующие их рост концентрации могут варьировать в широких пределах (Borden E., et al. (1981) Progress in Hematology. vol XII, Brown EB., editor, 299-339) для IFNs, для которых показаны различия в их способности ингибировать рост клеток (Dahl H. (1983). Human interferon and cell growth inhibition. VII. Reversibility of interferon activities. J Interferon Animal, 3:327-332; Willson J.K.V., Bittner G., et al. (1984) Antiproliferative activity of human interferons against ovarian cancer cells grown in human tumor stem cell assay. J Interferon Animal, 4:441-447; Hu R., Gan Y., et al. (1993) Evidence for multiple binding sites for several components of human lymphoblastoid interferon-alpha. J. Biol. Chem., 268:12591-12595), and to the activity antitumoral (Quesada J.R., Talpaz M., et al. (1986) Clinical toxicity of interferons in cancer patients: to review. J. Clin. Oncol, 4:234-243). Применение IFNs при лечении рака не оправдало ожиданий, основанных на исследованиях in vitro и на свойствах, которыми обладают эти сильнодействующие биологические молекулы. Были проверены различные схемы лечения без отчетливых благоприятных эффектов и импульсов (Strander H., and Oberg K., (1992) Clinical use of interferons. Solid tumors INTERFERON. Principles and Medical Applications. Publishing Baron S., Coppenhaver D.H., Dianzani F., Fleischmann WR., Jr. Hughes T.K., Jr. Klimpel G.R., Niesel D.W., Staton G.J., and Tyring S.K., 533-561).
С целью достижения лучших эффектов при лечениях IFNs применяли в увеличенных дозах, однако благоприятный потенциальный ожидаемый ответ не проявлялся из-за различных факторов, среди которых побочные действия, вызываемые указанными дозами (Lane H. С (1990) Interferon-alpha in patients with asymptomatic human immunodeficiency virus (HIV) infection. A randomized, placebo-controlled trial. Annals of internal Medicate, 112:805-811).
Кроме того, IFNs применяли в комбинированном виде, используя их синергичные эффекты. Комбинация IFN альфа и IFN гамма была описана в исследованиях in vitro с культурами келоидных фибробластов (Tredget Е.Е., Wang R., et al. (2000) Transforming growth factor-beta mRNA and protein in hypertrophic scar tissues and fibroblasts: antagonism by IFN-alpha and IFN-gamma in vitro and in vivo. J. Interferon Cytokine Animal, 20:143-151). В этой работе отмечено совместное использование IFNs альфа и гамма, однако приводимые данные получены из экспериментов in vitro и на клетках, происходящих из келоидов у детей. Эти авторы не проводили никакого клинического испытания и не оценивали эффект сочетания IFNs на клетки келоидов взрослых, которые слабо реагируют на интерфероны.
Патент EP 0107498 демонстрирует комбинацию интерферонов альфа и гамма на линии клеток меланомы Hs294T, но не описывает его действие на другие виды клеток типа первичной культуры базально-клеточной эпителиомы, или глиобластомы (GL-5), или ларенгиальной карциномы (HEp-2).
Также было описано альтернативное использование натурального IFN альфа и рекомбинантного IFN гамма для лечения ренальных и легочных метастазов (Fujii A., Yui-In K., et al. (1999) Preliminary results of the alternating administration of natural interferon-alpha and recombinant interferon-gamma for metastasic renal cell carcinoma BJU Int.; 84:399-404). Комбинация IFN альфа2, или альфа4 или гибрида δ4 альфа2 Bgl II альфа1 с IFN гамма была описана на клеточной линии RT4 (карцинома цисты) и на A2182 (аденокарцинома легкого) и обладала большим антипролиферативным эффектом, чем IFNs I типа или IFN гамма по отдельности (Hubbell H.R., Craft J.TO., et al. (1987) Synergistic antiproliferative effect of recombinant alpha-interferons with recombinant gamma-interferon. J Biol Response Mod, 6:141-153). Синергичный эффект IFN гамма (1000 IU/мл) и IFN альфа 2 (1000 IU/мл) был продемонстрирован на линии клеток A459 (альвеолярная опухоль) (Martyre M. C., Beaupain R., et al. (1987) Potentiation of antiproliferative activity by mix of human recombinant IFN-alpha 2 and -gamma on growth of human cancer nodules maintained in continuous organotypic culture. Eur J. Cancer Clin Oncol, 23:917-920), а также на линиях клеток, полученных из немелкоклеточной анапласической карциномы легких (Hand A., Pelin K., et al. (1993) Interferon-alpha and interferon-gamma combined with chemotherapy: in vitro sensitivity studies in non-small cell lung-cancer cell lines. Anticancer Drugs, 4:365-368).
Комбинация IFN альфа и IFN гамма была описана при исследовании линии клеток HepG2 ((Mizukoshi E., Kaneko S., et al. (1999) Up-regulation of type I interferon receptor by IFN-gamma. J Interferon Cytokine Animal, 19:1019-1023) и на линии клеток AVA5 (Okuse C, Rinaudo J. A., et al. (2005) Enhancement of antiviral activity against hepatitis С virus in vitro by interferon combination therapy. Antiviral Animal, 65:23-34). Эти авторы не выявили ни антипролиферативного эффекта, ни более эффективных соотношений при сочетании интерферонов альфа и гамма на линии клеток HepG2. Кроме того, синергичный эффект был изучен для TNF альфа и IFN гамма на линии клеток Hepa1-6 гепатомы мыши (Sasagawa Т., Hlaing M., et al. (2000) Synergistic induction of apoptosis in murine hepatoma Hepa1-6 cells by IFN-GAMMA and TNF-alpha. Biochem Biophys Common Animal, 272:674-680).
В патенте US 5190751 описано ингибирование роста лейкемийных линий клеток типа В и типа T комбинацией IFN альфа и гамма. Ни для одной из исследованных линий T клеток не наблюдался эффект усиления ингибирования роста, и при определенных экспериментальных условиях эффекты комбинаций были противоположными. В патенте EP 010749 и в публикации (Czarniecki С. W., Fennie C. W., et al. (1984) Synergistic antiviral and antiproliferative activities of Escherichia coli-derived human alpha, beta, and gamma interferons. J Virol. 49:490-496) также показано, что комбинация IFNs альфа и гамма не всегда является синергичной и может быть антагонистической. Отмечена эффективность комбинаций в очень широком диапазоне, однако это не приведено.
Эти данные свидетельствуют о том, что использование комбинаций IFN альфа и гамма следует оценивать для экспериментального определения, которое позволяет идентифицировать, какое из условий подходит для установления оптимальной комбинации для лечения нарушенного роста клеток в определенных тканях и органах. По этой причине для выбора лечения и соответствующей дозировки следует проводить оценку в экспериментах in vitro и в контролируемых клинических испытаниях.
В исследовании с линиями клеток глиом IFN гамма оказывал влияние на параметры злокачественного новообразования, такие как пролиферация и перемещение исследуемых опухолевых клеток (Knupfer M. M., Knupfer H., et al. (2001) Interferon-gamma inhibits growth and migration of A172 human glioblastoma cells. Anticancer Animal, 21:3989-3994). С другой стороны, сообщалось об отрицательных результатах применения IFN гамма при лечении глиом (Mahaley M. S., Bertsch L., Jr. et al. (1988) Systemic gamma-interferon therapy for recurrent gliomas. J. Neurosurg, 69:826-829). Одновременное использование IFN гамма и IFN β оказалось эффективным для ингибирования роста линии клеток GBM-18 астроцитомы с множественной устойчивостью (Reddy P. G., et al. (1991) Systemic gamma-interferon therapy for recurrent gliomas. J. Natl Cancer Inst, 83:1307-1315). Кроме того, была описана комбинация IFN гамма с альфа-дифторметилорнитином (DFMO) для лечения таких опухолей (US 4499072). В патенте US 5002879 описана сходная терапия с использованием DFMO после киллерных клеток, активированных лимфокинами и IL-2. Что касается IFN альфа, то его комбинации с другими лекарственными средствами не оказывали благоприятных эффектов при лечении глиом и обладали токсичностью (Buckner J. C, Burch P. A., et al (1998) Phase II trial of recombinant interferon-alpha-2a and eflornithine in patients with recurrent glioma. J Neurooncol. 36:65-70; Chang S. M., Barker F. G., et al. (1998) High dose oral tamoxifen and subcutaneous interferon alpha-2a for recurrent glioma. J Neurooncol, 37:169-176). Затем лечению этого типа опухоли может способствовать комбинированное применение IFN альфа и IFN гамма, исходя из соответствующего подбора соотношений их комбинаций, основанных на экспериментах in vitro и на клинических испытаниях.
Гортань является вторым из наиболее часто встречающихся после полости рта участком рака верхнего отдела дыхательных путей и пищеварительного тракта. Карцинома гортани представляет собой наиболее часто встречающуюся опухоль головы и шеи, и наиболее распространенным раком гортани является плоскоклеточная карцинома (95% всех случаев). Выживаемость при случаях опухолей гортани T3 и T4 составляет только 5 лет у приблизительно 30% больных, подвергшихся ларингектомии (Djordjevic V., Milovanovic J., et al. (2004) Radical surgery of the malignant laryngeal tumors. Minutes Chir Lugosl, 51:31-35). Было показано, что лучевая терапия и химиотерапия для лечения этой карцинома (Chen W., Guo X., et al. (2004) Long-term follow-up observation of clinical therapy for laryngeal carcinoma recurrence and cervical metastasis Lin Chuang Er Bi Yan Hou Ke Za Zhi. 18:536-537).
Тем не менее, полихимиотерапия совместно с применением IFN альфа оказались благотворными при лечении рака гортани (Mantz C. A., Vokes E. E., (2001) Sequential induction chemotherapy and concomitant chemoradiotherapy in the management of locoregionally advanced laryngeal cancer Ann Oncol, 12:343-347). Комбинация IL-2 и IFN альфа оценивалась в фазе II исследования в качестве терапии карциномы гортани, однако результаты были удовлетворительными (Clayman G. L, Young G., et al. (1992) Detection of regulatory factors of lymphokine-activated killer cell activity in head and neck cancer patients treated with interleukin-2 and interferon alpha. Ann Otol Rhinol Laryngol, 101:909-915). В терапии опухолей гортани достигнуты незначительные успехи. Комбинированное применение IFNs альфа и гамма может способствовать улучшению существующих методов лечения для борьбы с этим типом опухолей.
Патент US 5503828 описывает композицию интерферонов, характеризующуюся содержанием не менее 50% аллелей IFN альфа 2 и IFN альфа 8 и одним или несколькими дополнительными видами IFNs группы, образованной IFN альфа 4, альфа 7, альфа 10, альфа 16, альфа 17 и альфа 21. В то же время патент US 4503035 демонстрирует изготовление некоторых видов IFN альфа, но которые не включают альфа 1, альфа 5, альфа 14, и al IFN омега. Эти патенты не описывают состав, образуемый комбинацией рекомбинантных IFN гамма и IFN альфа 2.
Патент US 5762923 подробно описывает жидкую композицию интерферона, растворенного в воде с неионным детергентом и бензиловым спиртом в количестве, достаточном для стабилизирования IFN альфа, которая, кроме этого, содержит кислый буфер. С другой стороны, патент US 4847079 описывает фармацевтическую композицию интерферона и тимерозала, тогда как патент US 4675184 демонстрирует состав интерферона с многоатомным спиртом и органическим буфером в качестве стабилизатора и типового носителя или разбавителей с pH 3-6. Композиция может дополнительно иметь анионный сурфактант и/или альбумин в качестве стабилизатора. В патентах US 5236707 и US 5431909 описаны амины в качестве стабилизаторов (алифатические первичные амины) и органические соли лития, которые предохраняют интерферон от деградации и стабилизируют его.
Патент US 4496537 относится к жидким стабильным составам интерферона-альфа, которые содержат композицию сывороточного альбумина человека, и аланин или глицин, воду и буферную систему, способную поддерживать pH между 6,5 и 8,0.
Патент US 5935566 описывает стабильные составы интерферона альфа, которые содержат в своей композиции буферную систему, способную поддерживать pH в диапазоне от 4,5 до 7,1, полисорбат 80 в качестве стабилизатора, EDTA в качестве хелатирующего агента, хлорид натрия в качестве изотонизирующего агента и м-крезол в качестве противомикробной защиты.
Патент US 0170207 описывает стабильные составы интерферона альфа, которые содержат в своей композиции буферную систему, способную поддерживать pH в диапазоне от 4,5 до 9,0, стабилизирующее вещество, неионный сурфактант и регулятор осмотического давления.
В заявке WO 89/04177 описаны жидкие фармацевтические составы интерферона гамма, которые содержат буферный раствор, поддерживающий pH в диапазоне от 4,0 до 6,0, полигидроксильный сахар в качестве стабилизатора и неионный детергент. Патент US 4895716 относится к композициям и способам стабилизации интерферона гамма лактобионовой кислотой в буферном глицин/ацетатном растворе.
Патент US 5676942 описывает фармацевтические композиции, образованные подтипами интерферонов I типа, полученных из натуральных источников, но без комбинации с интерфероном гамма и не определяет соотношения этих комбинаций, только описывает эти комбинации для вирусных инфекций и не для лечения опухолей. Ни в одном из описанных ранее сообщений не применяли, характеризовали или упоминали фармацевтический состав, который одновременно содержит рекомбинантные IFNs гамма и альфа2 в синергичных комбинациях. Потенциальные возможности в комбинированном использовании существуют для IFN гамма и IFNs I типа, когда они смешаны в определенных пропорциях для лечения клеточного роста различной степени устойчивости к установленным методам лечения и/или их комбинациям.
Принимая во внимание эти предпосылки, необходимо разработать стабильные фармацевтические составы, которые содержат эти IFNs в соотношениях, которые позволят их безопасное, эффективное, простое и широкое применение у индивидуумов с доброкачественными или злокачественными опухолевыми образованиями. Это позволит более оптимально использовать комбинации и сделает более плодотворным применение в терапии больных, зависящих от этих лечений.
Пояснение изобретения
Настоящее изобретение разрешает ранее поставленную проблему, предоставляя стабильные фармацевтические составы для применения парентеральным (жидкие или лиофилизированные) или местным способом (гель, мазь или крем). Они содержат различные количества рекомбинантных интерферонов гамма и альфа в синергичных соотношениях для лечения патологических явлений, которые предполагают нефизиологический доброкачественный или злокачественный рост ткани или органов и которые, кроме этого, содержат фармацевтически приемлемые наполнители или носители.
Эти составы представляют собой результат анализов in vitro линий клеток с различной чувствительностью к IFNs и клинических испытаний с различными вариантами опухолей, а также оценки биологической и физико-химической устойчивости рекомбинантных IFNs гамма и альфа2 в присутствии различных фармацевтически приемлемых наполнителей или носителей.
Лиофилизированные стабильные фармацевтические составы состоят их рекомбинантных IFN гамма и альфа2, смешанных в буферном растворе, способном поддерживать pH между 4,9 и 7,5, который может быть ацетатом аммония или натрия, сукцинатом натрия, фосфатом натрия и/или калия или цитратом/фосфатом натрия.
Такие составы также состоят, по меньшей мере, из компонента, выбранного из соединений невосстанавливающих сахаров, аминокислот, сурфактантов и стабилизирующих полимеров. Невосстанавливающие сахара могут представлять собой сахарозу или трегалозу; аминокислоты могут представлять собой глицин, гистидин или лейцин; в то время как сурфактанты характеризуются полисорбатом 20 или полисорбатом 80 и в качестве стабилизирующего полимера - полиэтиленгликолем, декстраном или гидроксиэтилкрахмалом.
Осуществление изобретения определяло, что буферный раствор следует применять в диапазоне концентраций между 10 и 20 мМ. Сахарозу или трегалозу следует использовать в концентрации от 5 до 100 мг/мл; глицин, гистидин или лейцин следует применять в диапазоне концентраций между 1 и 20 мг/мл. Полисорбат следует применять в концентрации от 0,01 до 1 мг/мл, что касается полиэтиленгликоля, декстрана, и гидроксиэтилкрахмала, их применяют в диапазоне концентраций между 5 и 50 мг/мл.
Некоторые осуществления изобретения описывают лиофилизированные стабильные фармацевтические составы, которые содержат рекомбинантный IFN гамма в диапазоне концентраций между 5,6×108 IU и 1,4×108 IU и рекомбинантный IFN альфа2 в диапазоне концентраций между 6,8×108 IU и 1,7×108 IU. Или рекомбинантный IFN гамма в диапазоне концентраций между 2,0×108 IU и 0,5×108 IU и рекомбинантный IFN альфа2 в диапазоне концентраций между 12,0×108 IU и 3,0×108 IU. Или рекомбинантный IFN гамма в диапазоне концентраций между 4,0×108 IU и 1,0×108 IU и рекомбинантный IFN альфа2 в диапазоне концентраций между 80×108 IU и 20×108 IU. Cоставы дополнительно содержат 0,0802 г фосфорнокислого калия, 0,249 г 2-водного фосфорнокислого динатрия, 4 г сахарозы, 0,8 г глицина, 0,03 г Tween 20, 1 г полиэтиленгликоля 6000 и воду для инъекций в достаточном количестве по 100 мл и по 0,5 мл, 1 мл, 5 мл и 10 мл в соответствующих эквивалентных пропорциях.
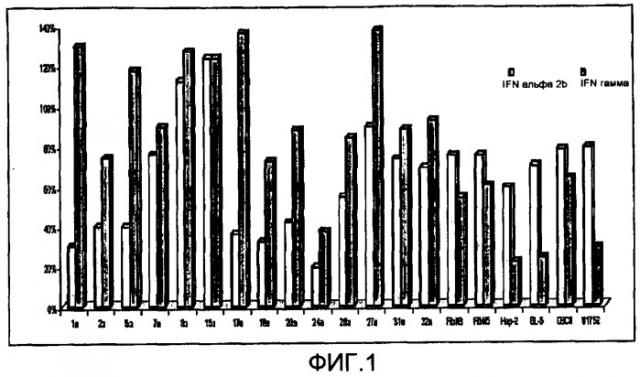
Определение смешивать рекомбинантные IFN гамма и IFN альфа в диапазоне определенной комбинации было получено после изоболограммного анализа. Концентрация рекомбинантного IFN гамма между 5,6×108 IU и 1,4×108 IU и рекомбинантного IFN альфа2 в диапазоне концентраций между 6,8×108 IU и 1,7×108 IU в одном из лиофилизированных стабильных фармацевтических составов была выявлена из анализа изучения ингибирования роста первичной культуры, полученной из келоидов (Kel 5a, Kel 17a) и из CBC III. В результате изоболограммного анализа была выявлена комбинация из 100 IU/мл (10 нг/мл) рекомбинантного IFN гамма со 100 IU/мл (0,5 нг/мл) рекомбинантного IFN альфа 2b, которая уменьшает рост клеток in vitro на 21%, 43% и 47%, соответственно, (см. примеры 1, 2 и 3, фиг. 1, Таблица 1).
Смесь рекомбинантного IFN гамма в диапазоне концентраций между 2,0×108 IU и 0,5×108 IU и рекомбинантного IFN альфа2 в диапазоне концентраций между 12,0×108 IU и 3,0×108 IU для состава была определена при помощи клинического испытания и на основании выписки из истории болезни с облегчением. Рандомизированным, контролируемым, проведенным в трех повторностях вслепую клиническим испытанием оценивали эффективность лечения введением внутрь пораженных тканей (I.L.) больных базально-клеточной эпителиомой определенного выше устойчивого лиофилизированного состава (см. примеры 7, таблицы 9, 10, 11 и 12).
По выписке из истории болезни с облегчением, которая также способствовала определению этих соотношений, подвергались лечению больные с плоскоклеточным раком (больной 1) и больной с множественными рецидивирующими плоскоклеточными раками и с предварительными прививками (больной 2) (см. пример 8 фиг. 5 b, c, d; больной 1, и фиг. 6 b, c; больной 2, соответственно).
Состав, который содержит рекомбинантный IFN гамма в диапазоне концентраций между 4,0×108 IU и 1,0×108 IU и рекомбинантный IFN альфа2 в диапазоне концентраций между 80×108 IU и 20×108 IU, был определен по анализу результатов исследования ингибирования роста клеток глиобластомы (GL-5) при помощи 50 IU/мл (5 нг/мл) рекомбинантного IFN гамма с 100 IU/мл (0,5 нг/мл) рекомбинантного IFN альфа 2b. Таким образом, достигнуто ингибирование роста на 55% (пример 3). Кроме того, был учтен анализ исследования с линией клеток HEp-2. В этом случае количества IFNs составляют 5 IU/мл (0,5 нг/мл) рекомбинантного IFN гамма с 75 IU/мл (0,375 нг/мл) рекомбинантного IFN альфа 2b. При этом достигнута оптимальная комбинация для уменьшения клеточного роста in vitro на 76% (см. примеры 1, 2 и 3).
Кроме того, были разработаны фармацевтические стабильные жидкие составы. В этих составах соотношения рекомбинантных IFNs гамма и альфа поддерживались, как описано для лиофилизированных составов, однако их фармацевтические составляющие варьировали для достижения большей устойчивости этих смесей IFNs.
Как следствие этой работы, осуществление изобретения описывает жидкие стабильные фармацевтические составы, которые содержат буферный раствор и, по меньшей мере, компонент, выбранный из невосстанавливающих сахаров, аминокислот, сурфактантов, стабилизирующих полимеров, антиоксидантов/хелатирующих компонентов и изотонизирующих веществ. В этих составах применяют водные растворители, которые могут содержать или не содержать консерванты, такие как смесь метил- и пропилпарабена.
Другое осуществление изобретения создает условия для определения жидких стабильных фармацевтических составов, в которых применяют буферный раствор, способный поддерживать pH между 4,9 и 6,5. Этот буфер может быть ацетатом аммония или натрия, сукцинатом натрия, фосфатом натрия и/или калия, цитратом/фосфатом. В этих составах в качестве сурфактантов можно применять полисорбат 20 или полисорбат 80; в качестве антиоксиданта/хелатирующего вещества - EDTA или ацетилцистеин; тогда как в качестве аминокислот можно включать гистидин, L-аргинин, L-аланин, глицин или лизин. В качестве стабилизирующего полимера установлено применение гидроксиэтилкрахмала или декстрана, а в качестве изотонизирующего вещества - хлорид натрия, хлорид калия, пропиленгликоль, маннит, глицерин, сахарозу или трегалозу.
Осуществление изобретения позволяет сделать вывод, что в жидких стабильных фармацевтических составах применяют буферный раствор в диапазоне концентраций между 10 и 100 мМ. В этом составе полисорбат применяют в диапазоне концентраций между 0,01 и 1 мг/мл; EDTA или ацетилцистеин применяют в диапазоне концентраций между 0,01 и 1 мг/мл. Аминокислоты гистидин, L-аргинин, L-аланин, глицин или лизин - в концентрации между 1 и 20 мг/мл; гидроксиэтилкрахмал и декстран применяют в диапазоне концентраций между 5 и 50 мг/мл и изотонизирующие вещества присутствуют в количестве, достаточном для получения изотонического раствора.
Другие осуществления разъясняют количества всех фармацевтических ингредиентов жидких стабильных фармацевтических составов, необходимых для физико-химической и биологической устойчивости описанных ранее смесей рекомбинантных IFNs гамма и альфа. Эти жидкие составы содержат, кроме IFNs, 0,708 г натрия ацетат, 0,079 мл уксусной кислоты, 0,01 г Tween 20, 5 г маннита и воду для инъекций в достаточном количестве по 100 мл и по 0,5 мл, 1 мл, 5 мл и 10 мл в соответствующих эквивалентных пропорциях.
Данное изобретение определяет соотношения смесей IFNs гамма и альфа, которые могут быть эффективны для лечения доброкачественного или злокачественного чрезмерного роста клеток. Это должно способствовать применению меньших доз, меньшему времени лечения и поддержанию неизменных терапевтических эффектов или достижению эффектов, превосходящих те, которые были достигнуты к настоящему времени с применением интерферонов при лечении опухолей или других аберрантных событий клеточного роста. Снижение дозы позволит ожидать уменьшения побочных эффектов или ослабления их интенсивности, что приведет к улучшению качества жизни больных и позволит им получить пользу от применения этих сильнодействующих лекарственных средств. Изобретение характеризует составы смесей рекомбинантных IFN гамма и IFN альфа2, которые не были описаны ранее, которые облегчают менеджмент и клиническое применение этой терапевтической комбинации и их коммерциализацию.
Лиофилизированные и жидкие стабильные фармацевтические составы, которые содержат описанные в изобретении смеси рекомбинантных IFNs гамма и альфа2 в синергичных соотношениях для ингибирования пролиферации, обладают широким спектром клинического применения. При использовании этих составов in vivo показано, что при значительных онкологических заболеваниях эффективно одновременное и внутриопухолевое применение комбинации рекомбинантных IFN гамма и IFN альфа2.
Эта комбинация способна оказывать равные лечебные эффекты на опухоли за более короткое время и с большим эстетическим эффектом по сравнению с эффектами, полученными для ее отдельных компонентов. Применение этих комбинаций позволит охватывать большие терапевтические возможности для борьбы с раком. Это накоплено в осуществлении изобретения, в котором раскрыто, что лиофилизированные или жидкие составы можно применять при лечении однородных доброкачественных или злокачественных опухолей, использовать в независимых формах или сочетать с химиотерапией, лучевой терапией или комбинацией обеих.
Использование этих составов в комбинации с другими терапевтическими веществами подтверждено результатами, полученными при лечении больного с гигантской базально-клеточной опухолью комбинацией рекомбинантных IFN гамма и IFN альфа2 вместе с цисплатином (см. пример 10 и фиг. 9).
В изобретении описано, как комбинированное применение интерферонов гамма и альфа2 позволяет уменьшить и/или вылечить опухоли с крайне неблагоприятным прогнозом и искажающими эстетическими проявлениями.
На основании характерных особенностей некоторых доброкачественных и онкологических нарушений, у которых преобладает неконтролируемый рост клеток, они могут быть восприимчивы к лечению этими составами. Среди них имеются: опухоли клеток из гематопоэтической ткани, такие как острая или хроническая миелоидная лейкемия, острый или хронический лимфолейкоз, а также лейкемии T или В клеток и лимфома центральной нервной системы. Также можно лечить карциномы гортани, папиломатоз гортани, липому, эпидермоид и интрадермальную цисту, липосаркому, нейробластому и жировую гиперплазию. Может быть полезно применение этих фармацевтических составов при опухолях периферической и центральной нервной системы, как, например, астроцитомы, полиморфные глиобластомы, эпендимомы, ганглионевромы, пилоцитарные астроцитомы, разнородные глиомы, олигодендроглиомы, глиомы зрительного нерва, эмбриональные эктодермальные опухоли, акустические нейромы, кордомы, краниофарингиомы, медулабластомы, менингиомы, нейрофиброматоз, ложные опухоли головного мозга, туберозные уплотнения, метастазирующие опухоли мозга. Другие чувствительные к лечению опухоли представляют собой кавернозные гемангиомы, гепатоцеллюлярные аденомы, очаговую узелковую гиперплазию, пинеальные опухоли, аденомы гипофиза, васкулярные опухоли, менингиальный карциноматоз, вишнеподобные ангиомы, жировую гиперплазию лимфатических узлов. Опухоли кожи, как, например, базально-клеточная эпителиома, плоскоклеточная карцинома, дерматофиброма, пиогенная гранулема, невоидная опухоль кожи, а также себорейный и актиничный квератоз могут иметь благоприятное воздействие при лечении этими фармацевтическими составами.
Другое осуществление изобретения описывает, что эти составы также можно применять для лечения пролиферативных явлений, как, например, фиброз, дисплазия и гиперплазия.
На основании результатов клинических испытаний, проведенных и описанных в примерах 7, 8 и 10, в качестве осуществления изобретения определены внутримышечные, внутриопухолевые и околоопухолевые способы применения составов. Другие осуществления описывают применение местных стабильных фармацевтических составов, которые содержат IFN гамма в диапазоне концентраций между 0,32×106IU и 0,08×106 IU и al IFN альфа2 в диапазоне концентраций между 2,0×106 IU и 0,5×106 IU на грамм полутвердого состава. Составы представляют собой крем, состоящий из 2,2% IFN гамма, 0,58% IFN альфа, 4% цетилового спирта, 10% вазелина, 2% Tween 60 и 0,2% метилпарабена, пропилпарабена. Кроме того, композиция мази была определена как 2,2% IFN гамма, 0,58% IFN альфа, 60% белого твердого вазелина, 10% вязкого жидкого вазелина, 3% span 20, и 0,2% метилпарабена и пропилпарабена. Наконец, состав геля состоит из 2,2% IFN гамма, 0,58% IFN альфа, 0,5% Carbopol 940, 0,2% метилпарабена и пропилпарабена, 0,2% гидрохлорида натрия, 0,01% динатрийэтилендиаминотетраацетата кальция и 2% этанола.
Все эти составы стабильны к колебаниям температуры, что полезно для производства продукта, его транспортировки и хранения. Они препятствуют агрегации интерферонов и поэтому представляют уменьшенный риск получения аллергии во время длительного применения продукта. Полутвердые составы больные могут применять самостоятельно в неинвазивной и безопасной форме. В качестве другого осуществления изобретения было определено применение этих местных стабильных составов при лечении солидных доброкачественных или злокачественных опухолей кожи или слизистых оболочек, используемых в независимых формах или в сочетании с химиотерапией, лучевой терапией или комбинацией обеих.
Другое осуществление изобретения описывает, что местные стабильные фармацевтические составы можно применять для лечения липомы, эпидермоидной и интрадермальной цисты, липосаркомы, нейробластомы, жировой гиперплазии, гемангиом, очаговой узелковой гиперплазии, эпендимом, ганглионевром, пилоцитарных астроцитом, менингиом, пинеальных опухолей, аденом гипофиза, васкулярных опухолей, менингиального карциноматоза, нейрофиброматоза, вишнеподобных ангиом, гиперплазии сальных желез, базально-клеточной эпителиомы, плоскоклеточной карциномы, дерматофибромы, пиогенной гранулемы, родимых пятен на коже, себорейного и актиничного квератоза и кондилом.
Другое осуществление изобретения описывает устройство набора, который содержит ампулу с рекомбинантным IFN гамма, ампулу с рекомбинантным IFN альфа в описанных выше концентрациях и соотношениях, ампулы с достаточным количеством воды для инъекций, разведения и/или растворения IFNs. Набор содержит шприцы и соответствующие иглы для одновременного введения IFNs, предварительно смешиваемых в одной из ампул, которая содержат один из IFNs.
Краткое описание фигур:
Фиг. 1. Ингибирование роста первичной культуры клеток фибробластов, происходящей из биопсии келоидов взрослых больных, 1000 IU/мл рекомбинантного IFN гамма или IFN альфа2.
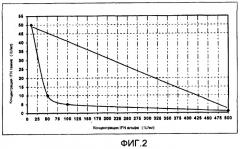
Фиг. 2. Изоболограмма ингибирования роста клеток комбинацией рекомбинантных IFN гамма и IFN альфа 2b на первичной культуре клеток фибробластов из келоидов (Kel5a).
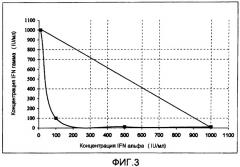
Фиг. 3. Изоболограмма ингибирования роста клеток комбинацией рекомбинантных IFN гамма и IFN альфа 2b на первичной культуре клеток фибробластов из келоидов (Kel17a).
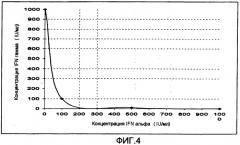
Фиг. 4. Изоболограмма ингибирования роста клеток комбинацией рекомбинантных IFN гамма и IFN альфа 2b на первичной культуре клеток фибробластов из базально-клеточной эпителиомы (CBC III).
Фиг. 5. Изоболограмма ингибирования роста клеток комбинацией рекомбинантных IFN гамма и IFN альфа 2b на клеточной линии глиобластомы GL-5.
Фиг. 6. Изоболограмма ингибирования роста клеток комбинацией рекомбинантных IFN гамма и IFN альфа 2b на клеточной линии HEp-2 гортани.
Фиг. 7. Больной эпидермоидальной карциномой, подвергавшийся лечению комбинацией рекомбинантных IFN гамма и IFN альфа 2b.
Фиг. 8. Больной с рецидивирующей базально-клеточной эпителиомой, подвергавшийся лечению комбинацией рекомбинантных IFN гамма и IFN альфа 2b.
Фиг. 9. Больной с рецидивирующей базально-клеточной эпителиомой, подвергавшийся лечению комбинацией рекомбинантных IFN гамма и IFN альфа 2b и цисплатина. A: до лечения, B: после 1 года лечения.
Подробное изложение способов выполнения/Примеры
Пример 1. Ингибирование роста клеток рекомбинантными IFNs гамма или альфа в первичной клеточной культуре.
Биопсии кожи были получены из нормальной кожи и от больных, у которых развивались базально-клеточная эпителиома или келоиды, последние явились результатом повреждения, полученного при хирургической операции или ожогов. Образец ткани был немедленно помещен в среду DMEM и фрагментирован для получения первичной культуры способом эксплантации. Для оценки антипролиферативного эффекта рекомбинантных IFNs гамма и альфа оценивали следующие первичные культуры: первичная культура фибробластов (CPF) из келоидов (1, 2, 5, 7, 8, 15, 17, 19, 20, 24, 26, 27, 31, 32), CPF из базально-клеточной эпителиомомы (CBC III) и CPF из нормальной кожи (FibN3 и FibN5). CPF наращивали в смеси культуральных сред RPMI-1640/DMEM, которая содержала гентамицин (50 мкг/мл) и 12% сыворотки теленка (CBS). Все культуры инкубировали при 37°C в CO2-инкубаторе при 5% влажности. Для определения антипролиферативного эффекта IFNs клетки засевали с концентрацией 5×104 клеток/мл в 96-микролуночный планшет. Их синхронизировали путем замены среды на свежую через 24 часа после посева. В конце 96 часов инкубации в присутствии различных концентраций IFNs была определена жизнеспособность 3 повторностей оцениваемых экспериментальных условий способом окрашивания кристаллическим фиолетовым при помощи измерения поглощения при 580 нм и использования планшетов для ридера. Результаты были определены как % роста, основанный на числе жизнеспособных клеток:
% роста=(AT72h-AC0h/AC72h-AC0h)×100.
AT72h = Поглощение клеток, обработанных 72 часа.
AC72h = Поглощение контрольных клеток, обработанных 72 часа.
AC0h = Поглощение клеток до обработки IFN.
На фиг. 1 показано антипролиферативное действие рекомбинантного IFNs гамма или альфа на рост келоидных CPF. Как можно видеть, IFN гамма или альфа 2b ингибирует клеточную пролиферацию у различных первичных культур, в то время как у других они стимулируют их рост. В качестве контрольных оценивались первичные культуры FibN3 и FibN5, а также первичная культура из биопсии линий клеток CBCIII, и HEp-2, U1752 и GL-5.
Пример 2: Ингибирование клеточного роста рекомбинантами рекомбинантных IFNs гамма или альфа у определенных линий клеток.
Были исследованы линии клеток человека: Jurkat (ATCC, TIB-152), GL-5 (Perea S. and., et al. (1993) Minutes Cient Venez, 44:22-27), HEp-2 (ATCC, CCL23). Клетки GL-5 культивировали в DMEM, а HEp-2 - в MEM-CANE, содержащей гентамицин (50 мкг/мл) и 10% CBS. Клетки Jurkat инкубировали в среде RPMI с гентамицином и 10% CBS. Все культуры инкубировали при 37°C в CO2 инкубаторе при 5% влажности. Для оценки антипролиферативного эффекта клетки GL-5 и HEp-2 засевали при концентрации 3×104 клеток/мл. В случае клеток Jurkat засев проводили при концентрации 105 клеток/мл. После 72 часов инкубации в присутствии различных концентраций IFNs выживаемость оценивали способом окрашивания кристаллическим фиолетовым при помощи измерения поглощения при 580 нм и использования планшетов для ридера. Результаты были определены как % роста, основанный на подсчете жизнеспособных клеток, как описано в примере 1. Как видно из Таблицы 1 и на фигуре 1, линии клеток HEp-2 (карцинома гортани) и GL-5 (из глиобластомы) являются очень чувствительными к IFN гамма и не чувствительными к IFN альфа.
| Таблица 1Ингибирование клеточного роста 1000 IU/мл IFN гамма или IFN альфа 2b на линиях клеток | |||||
| IFNs | Среднее | Стандартное отклонениеSD | Коэффициент вариации VariacionCV | Повторности | Пробы |
| HEp-2 | |||||
| IFN альфа2 | 65% | 13,68% | 0,211 | 6 | 2 |
| IFN гамма | 18% | 6,26% | 0,357 | 6 | 2 |
| GL-5 | |||||
| IFN альфа2 | 71% | 20,26% | 0,287 | 6 | 2 |
| IFN гамма | 24% | 10,21% | 0,421 | 4 | 2 |
| HepG2 | |||||
| IFN альфа2 | 103% | 13,17% | 0,128 | 6 | 1 |
| IFN гамма | 106% | 21,67% | 0,204 | 6 | 1 |
| Jurkat | |||||
| IFN альфа2 | 60% | 5,28% | 0,088 | 3 | 1 |
| IFN гамма | 107% | 16,89% | 0,157 | 3 | 1 |
В Таблице 1 подмечено, что линия HepG2 (Гепатома) не чувствительна к этим IFNs и что для линии клеток Jurkat (лимфома T) IFN альфа является наиболее эффективным, результат, который согласуется с успешным применением IFN альфа2 при лечении опухоли лимфоидной ткани.
Пример 3: Комбинации рекомбинантных IFNs гамма и альфа с наиболее эффективным антипролиферативным воздействием на первичную культуру и линии клеток.
С использованием CBC-III и келоидных (Kel-5a и Kel-17a) CPF и линий клеток HEp-2 и GL-5 проводили изучение комбинаций рекомбинантных IFNs гамма и альфа 2b для определения оптимальной смеси с синергичной активностью ингибирования клеточного роста. Полученные в исследовании данные были проанализированы построением изоболограмм. Из исследования изоболограмм CPF, полученных из биопсии келоидов (kel 5a и kel 17a) взрослых было определено, что оптимальная синергичная комбинация для ингибирования роста должна составлять 100 IU/мл (10 нг/мл) IFN гамма и 100 IU/мл (0,5 нг/мл) IFN альфа 2b. С этой комбинацией рост клеток уменьшается in vitro на 21% (Kel 5a) и на 43% (kel 17a) (фиг. 2 и 3).
На изоболограмме фиг. 4 показано, что комбинация 100 IU/мл (10 нг/мл) IFN гамма с 100 IU/мл (0,5 нг/мл) IFN альфа 2b является синергичной и является наиболее эффективной при уменьшении роста клеток in vitro для CBC III на 47%.
В соответствии с изоболограммой, представленной на фигуре 5, оптимальная синергичная комбинация для ингибирования роста клеток GL-5 составляет 50 IU/мл (3 нг/мл) IFN гамма с 600 IU/мл (5 нг/мл) IFN альфа 2b. С этой комбинацией рост клеток in vitro уменьшается на 55%.
На изоболограмме, представленной на фигуре 6, показана оптимальная синергичная комбинация IFN гамма и альфа для достижения наилучшего антипролиферативного эффекта на клетках HEp-2. Количества IFNs составляют 5 IU/мл (0,5 нг/мл) IFN гамма и 75 IU/мл (0,375 нг/мл) IFN альфа 2b. С этой оптимальной комбинацией достигается уменьшение роста клеток in vitro на 76%.
Пример 4: Эффект pH, видов ионов и концентрации буферного раствора на устойчивость смеси интерферонов альфа 2b и гамма в водном растворе.
Для исследования устойчивости жидких и лиофилизированных составов синергичных композиций рекомбинантных интерферонов гамма и альфа IFNs разведены из их соответствующего Активного Фармацевтические Ингредиента (IFA) в различных пробных составах: буферные растворы, смесь буферных растворов с отдельными наполнителями и смесь буферных растворов с различными наполнителями. Характерные образцы ампул с различными составами были представлены для различных обработок дл