Ранозаживляющее средство
Иллюстрации
Показать всеИзобретение относится к области медицины, а именно к ранозаживляющим средствам. В качестве антисептического компонента средство содержит хлорид поли-(4,9-диоксадодекангуанидина) (ПДДГ), или фосфат (ПДДГ), или сукцинат (ПДДГ). Средство содержит гидроксиэтилцеллюлозу, поливинилпирролидон (Полидон), глицерин, альгинат натрия и воду при определенном соотношении компонентов. Изобретение позволяет снизить токсичность и аллергенность. 2 табл.
Реферат
Изобретение относится к области медицины, а именно к средствам, включающим полимерные материалы, используемые в хирургии для лечения ран, ожогов, повреждений кожи различной степени тяжести.
Местное лечение ран различной этиологии, в том числе инфицированных и гнойных, остается актуальной проблемой современной медицины.
В качестве лекарственных антибактериальных средств для лечения ран используют антибиотики (патент РФ №2034572, кл. А61L 15/31, опубл. 10.05.95), ферменты (патент РФ №2085218, кл. А61L 15/00, опубл. 27.07.97; патент РФ №2074709, кл. А61К 9/06) или противоспалительные фармакологические субстанции, например облепиховое масло, люцерон (а.с. РФ №602185, кл. А61L 15/01, патент РФ №2143925, А61L 15/32).
Многочисленность факторов патогенеза ран, язв и абсцессов (особенно инфицированных с вялотекущим процессом заживления), особенности их анатомии предопределяют необходимость применения широкого арсенала лекарственных средств и многоэтапность их лечения. Поэтому обосновано применение комплексных лекарственных средств, включающих лекарственные субстанции, действующие на разные звенья патогенетического процесса. Однако применение многих лекарственных средств, содержащих комбинации лекарственных препаратов, до настоящего времени не всегда дает положительный эффект из-за их несовместимости в одном препарате, что сопровождается побочными реакциями в виде жжения, гиперемии или аллергических проявлений. Все это ограничивает использование известных средств.
Известно средство для лечения ран, содержащее природный краситель шиконин, обладающий антимикробным действием (патент РФ №2071788, кл. А61L 15/32, опубл. 20.01.97, Бюл.№2).
Недостатком известного средства является ограниченность лечебного воздействия на раневой процесс, обусловленная только его антисептическими свойствами, а также отсутствие пролонгированного эффекта,
Наиболее близким по сущности и достигаемому эффекту к предлагаемому изобретению является состав для обработки рук медицинского персонала, гнойных ран, инъекционных и операционных полей, изложенный в пат. РФ №2122865, кл. А61L 2/16, Бюл. №34, 1998 г.
В составе содержится антисептическое средство на основе полигуанидина - фосфат полигексаметиленгуанидина (ПГМГ).
Используемые составы сохраняют свои антисептические свойства длительное время.
Однако используемый при производстве фосфата ПГМГ гексаметилендиамин является аллергеном и эти аллергенные свойства передает фосфату ПГМГ.
Техническая задача, решаемая изобретением, - снижение токсичности и аллергенности средства, кроме того, расширяется область применения средства.
Техническая задача решается за счет того, что в ранозаживляющем средстве, включающем соединение полигуанидина и воду, в качестве соединения полигуанидина используют хлорид поли-(4,9-диоксадодекангуанидина), или фосфат поли-(4,9-диоксадодекангуанидина), или сукцинат поли-(4,9-диоксадодекангуанидина) и дополнительно гидроксиэтилцеллюлозу, Полидон, глицерин и альгинат натрия при следующем соотношении компонентов в мас.%:
| соединение полигуанидина | 0,2-1,0 |
| гидроксиэтилцеллюлоза | 0,5-1,5 |
| Полидон | 20,0-30,0 |
| глицерин | 2,0-5,0 |
| альгинат натрия | 0,1-0,5 |
| вода | остальное |
Сущность изобретения поясняется следующим образом.
Используемые в составе ранозаживляющего средства высокоэффективные соединения поли-(4,9-диоксадодекангуанидина) обладают широким спектром биоцидной активности с пролонгированным эффектом: антибактериальной, фунгицидной и вирулицидной. Эти соединения малотоксичны и не являются аллергенами.
В качестве соединений полигуанидина используют хлорид поли-(4,9-диоксадодекангуанидина (ПДДГ) «ЭКОСЕПТ», фосфат поли-(4,9-диоксадодекангуанидина (ПДДГ) «ЭКОСЕПТ» и сукцинат ПДДГ.
Эти соединения выпускает РОО «Институт эколого-технологических проблем» (ИЭТП). Товарный знак «ЭКОСЕПТ» принадлежат РОО ИЭТП.
Наиболее предпочтительно применение сукцината ПДДГ.
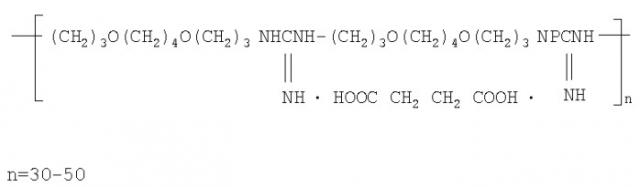
Сукцинат поли-(4,9-диоксадодекангуанидина) (двузамещенный) имеет следующую структурную формулу:
Следует отметить, что янтарная кислота, входящая в состав сукцината ПДДГ является биоактивным природным соединением. Она присутствует в организме человека и поэтому соль янтарной кислоты необходима человеку. Сукцинат ПДДГ увеличивает пролонгированный антисептический эффект состава и является наиболее предпочтительным в применении.
Гидроксиэтилцеллюлоза представляет собой водорастворимое производное целлюлозы и применяется в составе ранозаживляющего средства в качетве гелеобразующего компонента. Это порошок белого цвета с содержанием основного компонента не менее 97% мас. (ТУ 6-05-1857-87).
Глицерин - обволакивающий и вяжущий компонент. Глицерин (ГОСТ 6259-75) представляет собой прозрачную вязкую жидкость с содержанием основного вещества не менее 99% мас. Глицерин способствует проникновению активных веществ в пораженный участок кожи, а также оказывает смягчающее и вяжущее действие.
Альгинат натрия (ВФС 42-1680-87) представляет собой мелкодисперсный порошок белого цвета, относится к полисахаридам, легко растворим в воде, гигроскопичен. Альгинат натрия эффективно стимулирует регенерацию клеток, способствует остановке кровотечений, устранению воспалительных явлений и ускорению процессов заживления, а также обладает сорбирующими свойствами, что особенно важно при раневом процессе. Сочетание альгината натрия с полимерными компонентами состава ранозаживляющего средства обеспечивает образование дополнительного полимерного слоя, что делает рану микробонепроницаемой.
Полидон - предствавляет собой водно-полимерную композицию высокомолекулярного поливинилпирролидона в виде прозрачного геля. Полидон выпускается ООО «Оргполимерсинтез СПб», г.Санкт-Петербург по ТУ 9365-002-46270704-2001, используют Полидон (модификации А или В-1) с вязкостью 3000-25000 сПз. Полидон в сочетании с соединением полигуанидина образует комплексы, обладающие пониженной токсичностью, а также способствует повышению стабильности и гомогенности состава ранозаживляющего средства.
Вода используется в качестве основы по ГОСТ 6709-72 (дистиллированная).
Количественное содержание компонентов ранозаживляющего средства является оптимальным и выбрано на основании многочисленных экспериментов.
В табл.1 представлены данные, подтверждающие оптимальность заявленных пределов.
Альтернативные признаки п.1 формулы изобретения обеспечивают тот же технический результат, что и приведенные в табл.1.
Процесс приготовления ранозаживляющего средства имеет следующие стадии. Первая стадия - диспергируют во взвешенном количестве воды глицерин, гидроксиэтилцеллюлозу, альгинат натрия в течение 30 минут при температуре 35-40°С с периодическим перемешиванием массы. Режим перемешивания и конструктивные особенности реактора должны препятствовать пенообразованию.
Вторая стадия - последовательно вводят при перемешивании в полученную дисперсию остаточное количество воды, Полидон и соединение полигуанидина. Далее смесь перемешивают при температуре 25-30°С в течение 1-2 час до получения однородного вязкого раствора.
Полученное ранозаживляющее средство фасуют в индивидуальную герметичную упаковку, стерилизуют радиационным методом дозой 2,0±0,5 Мрад.
В примерах конкретного выполнения содержание компонентов ранозаживляющего средства представлено в мас.%.
Пример №1
| хлорид ПДДГ | 0,2 |
| гидроксиэтилцеллюлоза | 1,0 |
| Полидон | 20,0 |
| глицерин | 5,0 |
| альгинат натрия | 0,3 |
| вода | остальное |
Полученный состав стимулирует процессы регенерации, способствует элиминации раневого отделяемого и микрофлоры, ускоряя заживление поражений. Применяется для лечения инфицированных ран, в том числе острых и хронических.
Пример №2
| фосфат ПДДГ | 1,0 |
| гидроксиэтилцеллюлоза | 1,5 |
| Полидон | 23,0 |
| глицерин | 3,0 |
| альгинат натрия | 0,1 |
| вода | остальное |
Полученный состав может применяться для лечения гнойных ран, пролежней, язв трофических, венозных и язвенных дефектов при синдроме диабетической стопы. Ранозаживляющее средство стимулирует развитие репаративных процессов, способствует очищению и быстрой эпителизации ран.
Например, при лечении пролежней, лечение которых происходит длительно с повторными некротомиями, сменой препаратов, большого количества антибиотиков, отмечен такой случай. Больной Р. 26 лет находился в отделении ГКБ№20 г.Москвы 7 месяцев после тяжелой травмы, развившегося сепсиса и с множественными пролежнями. После лечения ран тампонами с предлагаемым ранозаживляющим средством через 3 недели произошла санация ран, и, казалось бы, безнадежный больной выписан в удовлетворительном состоянии.
Пример №3.
| сукцинат ПДДГ | 0,6 |
| гидроксиэтилцеллюлоза | 0,5 |
| Полидон | 30,0 |
| глицерин | 2,0 |
| альгинат натрия | 0,5 |
| вода | остальное |
Полученный состав может применяться для лечения ожогов, оказывает пластифицирующее воздействие на ожоговую рану, создает на ране влажную среду, оптимальную для течения процессов регенерации, ускорения эпителизации, предотвращает проникновение микробов.
Остальные примеры сведены в табл.1.
Клинические испытания предлагаемого ранозаживляющего средства проводили в Подольской городской клинической больнице, отделении гнойной хирургии ГКБ №15 им. О.М.Филатова г.Москвы, на кафедре госпитальной хирургии №1 Российского государственного медицинского университета г.Москвы.
В исследование были включены 243 больных, из них 195 больных с инфекционными и воспалительными заболеваниями кожи и мягких тканей: острые, хронические, послеоперационные (нагноившиеся) раны, пролежни, язвы (трофические, венозные, СДС), а также 48 больных с ожогами туловища и конечностей.
Площадь раневых дефектов составляла от 2,0 до 100 см.2 Раны находились в I-III стадиях раневого процесса.
Перед нанесением ранозаживляющего средства рана обрабатывалась физиологическим раствором и тщательно осушалась.
Обработку проводили ежедневно при наличии воспаления в области раны.
При стихании перифокального воспаления, уменьшении экссудации и появлении краевой эпителизации рану обрабатывали ранозаживляющим средством не реже 1 раза в 2 суток.
Опытная группа составляла 122 больных, в комплексе терапии которых было применено предлагаемое ранозаживляющее средство, и 121 пациент, составившие контрольную группу, получали стандартную терапию.
Все больные в возрасте от 19 до 67 лет. Пациенты контроля были сопоставимы с опытными группами по характеру патологии и возрасту.
Клинические испытания показали, что за счет лечебных свойств состава предлагаемое ранозаживляющее средство обеспечивает пластифицирующее воздействие на ткани раны, стимулирует аутолиз и позволяет быстро очистить рану от некротических масс, фибринозного налета и клеточного детрита, ускоряя процесс грануляции. Положительная динамика в течение раневого процесса, который отличался ускоренными темпами очищения раны от некрозов, нарастания грануляционной ткани и краевой эпителизации, позволила сократить сроки госпитализации больных.
Медико-биологические испытания, проведенные в Испытательной лаборатории НИИ трансплантологии и искусственных органов Росмедтехнологий показали отсутствие цитотоксичности на суспензионной кратковременной культуре подвижных клеток (семя крупного рогатого скота) и на культуре фибробластов мыши линии L-929. Испытания в условиях in vivo на животных показали, что предлагаемое ранозаживляющее средство не вызывает аллергического, сенсибилизирующего действия, не токсично.
Испытания по определению антимикробной активности средства проводились двумя способами. По первому способу определяли зоны подавления микроорганизмов при диффузии исследуемого вещества в плотную питательную среду (Федоров Ю.А., Корень В.Н. «Микробиологические методы исследования зубных гигиенических средств» в кн. «Основы гигиены полости рта». Л., «Медицина», 1973 г., с.3-215).
Для этого на поверхность твердой питательной среды в чашке Петри (объемом 20 мл) наносили по 1 мл 24-часовую микробную взвесь тест-микроорганизмов с концентрацией 5×105 КОЕ/мл. Подсушивали в течение 30 мин, а затем в питательной среде делали лунки диаметром 6 мм, в которые помещали пробы предлагаемого ранозаживляющего средства. Количество лунок не превышало 6 на чашку Петри. В течение 30 мин чашки Петри выдерживали при комнатной температуре (20°С), затем их помещали в термостат на 24-48 часов при температуре 37°С и по истечении указанного срока учитывали зоны угнетения микробного роста, включая диаметр лунок. По размерам зон угнетения судили об антимикробном действии исследуемого состава. При этом следует учитывать, что скорость диффузии полимерных антисептических средств ниже скорости диффузии низкополимерных антисептических средств.
Для получения достоверных результатов все опыты проводили с трехкратной повторностью, время тестирования - 48 часов. Данные эксперимента обрабатывались статистически.
В табл.2 представлены результаты испытаний антимикробной активности образцов ранозаживляющего средства по примерам 1, 2 и 3, а также для сравнения образца средства, выполненного по составу прототипа (1%-ный водный раствор ПГМГ).
Предложенные ранозаживляющие средства образовывали зоны задержки роста от 20 до 40 мм, что соответствует достаточно высокой антимикробной активности, в то время как средство, выполненное с использованием фосфата полигексаметиленгуанидина (по прототипу), показывало зоны задержки роста от 18 до 24 мм.
Второй способ испытания антимикробной активности состоит в определении минимального времени, необходимого для полного подавления роста и развития тест-микроорганизмов.
В испытываемое вещество добавляли суспензию тест-микроорганизмов в количестве 105 КОЕ/мл, для этого в пробирки наливали по 1 мл испытываемого вещества. Пробирки встряхивали и через промежутки времени 2-5-10 и 30 минут делали посевы на плотные питательные среды. Чашки Петри помещали на 24-48 часов в термостат при 37°С. После истечения указанного срока подсчитывали число выросших колоний и по этому показателю судили о бактерицидной активности испытываемого вещества.
Результаты исследования образцов ранозаживляющего средства, выполненных по примерам 1, 2 и 3, показали, что уже через 2 минуты контакта ни в одном случае не обнаружено живой микрофлоры после контаминации питательной среды кишечной палочкой.
Результаты испытаний антимикробной активности показали, что предложенное ранозаживляющее средство наряду со стимулирующим регенерацию действием обладает высоким противомикробным действием, способствующим значительному снижению уровня бактериального заражения, что важно в лечении инфицированных ран и профилактике нагноений после повреждения кожных покровов.
| Таблица 2 | |||
| Образцы ранозаживляющего средства | Зоны подавления роста микроорганизмов, мм | ||
| S. aureus | E. coli | Ps. aeruginosa | |
| Пример 1 | 28 | 22 | 24 |
| Пример 2 | 40 | 27 | 26 |
| Пример 3 | 33 | 25 | 20 |
| Пример по прототипу | 24 | 20 | 18 |
Ранозаживляющее средство, включающее соединение полигуанидина и воду, отличающееся тем, что в качестве соединения полигуанидина используют хлорид поли-(4,9-диоксадодекангуанидина), или фосфат поли-(4,9-диоксадодекангуанидина), или сукцинат поли-(4,9-диоксадодекангуанидина) и дополнительно содержит гидроксиэтилцеллюлозу, полидон, глицерин и альгинат натрия при следующем соотношении компонентов, мас.%:
| соединение полигуанидина | 0,2-1,0 |
| гидроксиэтилцеллюлоза | 0,5-1,5 |
| полидон | 20,0-30,0 |
| глицерин | 2,0-5,0 |
| альгинат натрия | 0,1-0,5 |
| вода | остальное |