Функциональные наноматериалы с антибактериальной и антивирусной активностью
Иллюстрации
Показать всеИзобретение относится к нанокристаллическим соединениям формулы
где АОX представляет оксид металла, где А выбран из Ti или Zr, x=2; Men+ представляет собой ион металла, обладающий антибактериальной активностью, выбранный из Ag+ и Сu++, где n=1 или 2; L представляет собой бифункциональную молекулу, или органическую, или металлорганическую, способную одновременно связываться с оксидом металла и ионом металла Men+; где органическая молекула выбрана из пиридина, дипиридила, трипиридила, функционализированных карбоксильными группами (-СООН), бороновыми группами (-В(ОН)2) или фосфоновыми группами (-РО3Н2), или 4-меркаптофенилбороновой кислоты; где металлорганическая молекула представляет собой металлорганический комплекс, содержащий органический лиганд, координированный центральным атомом металла и содержащий бороновую (-В(ОН)2), фосфоновую (-РО3Н2) или карбоксильную (-СООН) функциональную группу, и группы координированы центральным атомом металла, способные связываться с ионами металлов с антибактериальной активностью; где указанный органический лиганд, координированный центральным атомом металла, выбран из пиридина, дипиридила, трипиридила, функционализированных карбоксильными группами (-СООН), бороновыми группами (-В(ОН)2), или фосфоновыми группами (-РО3Н2), или 4-меркаптофенилбороновой кислоты; i представляет число групп L-Men+, связанных с наночастицей АОх. Также предложены композиция, обладающая антибактериальной и/или противовирусной активностью, дерматологические композиции, применение нанокристаллических соединений, способ регенерации нанокристаллических соединений. Технический результат - нанокристаллические соединения обнаруживают эффективное антибактериальное действие. 7 н. и 20 з.п. ф-лы, 4 ил., 4 табл.
Реферат
Описание
Область применения изобретения
Изобретение относится к наноматериалам, состоящим из оксидов металлов, соединенных с катионобразующими металлами, обладающими антибактериальной активностью.
Уровень техники
Известна антибактериальная активность некоторых ионов металлов, также называемая “олигодинамическим эффектом”.
Ионы металлов, обладающие наибольшей антибактериальной активностью, представляют собой, в порядке убывания силы, ионы следующих металлов:
Hg > Ag > Cu > Zn > Fe > Pb > Bi.
Включение таких металлов, в частности ионов серебра, в пластики, керамические материалы и материалы на основе волокон или углерода создает возможность элиминации или уменьшения роста колоний бактерий. Такой эффект особенно выгоден в свете совместимости Ag+ с организмом человека и возрастающей резистентности многих бактерий к антибиотикам. Таким образом, использование материалов, которые содержат серебро, может служить цели избежания или ограничения бактериальной пролиферации.
Что касается механизма действия серебра, то известно, что антибактериальная активность реализуется одновалентным положительным ионом Ag+. Отмечалось, что присутствие платины в смеси с серебром промотирует окисление Ag до Ag+ из-за гальванического эффекта; это приводит к соответствующему усилению антибактериальной активности пленки, состоящей из платины и серебра. Более того, фармацевтические препараты на основе серебра, например сульфадиазин серебра, используемые для предотвращения инфекций в случае тяжелых ожогов, действуют путем постепенного высвобождения ионов Ag+, которые могут обратимо адсорбироваться в бактериальных клетках за счет ассоциации с группами -SH цистеина в бактериальных белках, присутствующих в клеточных стенках. Цитотоксическое действие Ag+ также связано со способностью данного иона вытеснять существенно важные ионы из клеток, такие как ионы кальция (Са2+) и цинка (Zn2+). Предшествующие исследования (см., например, Carr H.S., Wlodkowski T.J. and Rosenkranz H.S., 1973, “Antimicrobial agents and chemotherapy”, vol.4, p.585) показали, что антибактериальная активность инов Ag+ прямо пропорциональна их концентрации и эффективна против большого числа видов бактерий. Подобные соображения высказаны для ионов меди (Cu2+), которые известны в сельском хозяйстве как антибактериальные средства.
По состоянию на сегодня в технике известно получение нанокристаллических материалов на основе оксидов металлов (МОх) с высокой площадью поверхности, таких как диоксид титана, оксид цинка, оксид олова (SnO2), диоксид циркония и коллоидный диоксид кремния, которые можно осаждать на различные сусбстраты с прочным сцеплением. Также известны наноматериалы на основе диоксида титана, включающие ионы серебра, которые получают смешиванием суспензий наноматериала с растворами, содержащими ионы Ag+. Адгезия ионов Ag+ к нанокристаллической структуре оксида металла весьма вероятно связана с внедрением ионов между нанокристаллами.
Однако для того, чтобы получить гомогенные пленки, которые обнаруживают эффективное антибактериальное действие, необходимо использовать взаимодействия, которые распространяются равномерно по поверхности наноматериала и которые допускают гомогенное осаждение ионов серебра в высокой концентрации.
Данная проблема решается настоящим изобретением, посредством которого также можно получать пленки, которые можно осаждать на различные материалы и на фильтры, используемые для очистки окружающей атмосферы.
Сущность изобретения
Настоящее изобретение относится к получению новых антибактериальных и антивирусных наноматериалов на основе оксидов металлов, таких как, например, TiO2, ZrO2, SnO2, ZnO и SiO2, функционализированных молекулами органической или неорганической природы, способными одновременно связываться с оксидом и с ионами переходных металлов, такими как Ag+ или Cu2+.
Для целей иллюстрации составные блоки таких новых материалов можно представить, например, формулой (I)
где АОх представляет оксид металла или оксид металлоида, где х = 1 или 2;
Men+ представляет собой ион металла, обладающий антибактериальной активностью, где n = 1 или 2, предпочтительно, Ag+ или Cu++;
L представляет собой бифункциональную молекулу, или органическую или металлорганическую, способную одновременно связываться с оксидом металла или оксидом металлоида и ионом металла Меn+;
i представляет число групп L-Men+, связанных с наночастицей АОх.
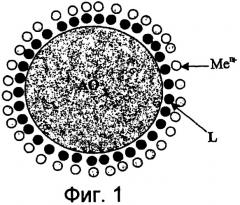
Оксиды металлов или оксиды металлоидов АОх для применения в настоящем изобретении представляют собой, например, коллоидный диоксид кремния, диоксид титана, диоксид циркония, оксид олова и оксид цинка. Они являются изоляционными материалами или полупроводниками, которые способны сцепляться, или сами по себе, или с применением подходящего подслоя, с большим числом материалов, включая дерево, пластмассу, стекло, металлы, керамику, цемент и внутренние и наружные поверхности зданий, и могут быть получены в виде наночастиц размерами порядка нанометров. Такие наноматериалы способны адсорбировать, за счет электростатического или химического взаимодействия, такого как эфирные связи, молекулы, имеющие подходящие функциональные группы, такие как следующие группы: карбоксильная (-СООН) (или карбоксилатная), фосфоновая (-РО3Н2) (или фосфонатная) или бороновая (-В(ОН)2) (или боронатная), которые может предоставить бифункциональная молекула L. С учетом малых размеров лигандов L и ионов металлов Men+, например, ионов серебра или меди, которые могут являться размерами порядка пикометров, результат таков, что какждая наночастица оксида металла может быть равномерно покрыта ионами металлов, такими как Ag+ или Cu2+, что схематично иллюстрируется, например, Фиг. 1.
В результате такие наноматериалы, содержащие положительно заряженные наночастицы, могут образовывать суспензии или в водных растворителях, или в полярных растворителях органической природы, которые устойчивы и прозрачны.
Другой существенный аспект связан с возможностью смешивания суспензий наноматериалов по изобретению с катионогенными поверхностно-активными веществами, такими как алкиламмониевые соли. С учетом этого бактерицидную активность наноматериалов по изобретению можно усилить за счет присутствия алкиламмониевой соли. Действительно, поверхностно-активные вещества такого типа проявляют бактерицидную активность, которая может быть комплементарна активности антибактериально активных ионов металла. Неожиданно авторы обнаружили, что алкиламмониевые соли, например хлорид бензалкония, который имеет склонность выпадать в осадок в щелочной среде или в присутствии высоких концентраций анионов, устойчивы в присутствии суспензий, полученных из положительно заряженных наночастиц по настоящему изобретению.
Экспериментальные данные, описанные в данном описании ниже, также показывают, что катионогенные поверхностно-активные вещества, такие как хлорид бензалкония, могут вызывать адсорбцию на наноматериалах на основе диоксида титана при значениях рН, близких к нейтральному. Это предоставляет дополнительное преимущество уменьшения летучести алкиламмониевых солей после нанесениях их на поверхность.
Вследствие широкого спектра антибактериального действия материалов, содержащих ионы серебра и меди, применение таких материалов в качестве покрытий для внутренней отделки зданий, ванных комнат, кухонь, элементов фурнитуры и арматуры вообще, стеклянных поверхностей (таких как двери и окна) и рабочих комнат, и для фильтров, используемых для очистки воздуха в различных средах, а также фильтров для воды, бесспорно представляет область применений существенной важности. Получение фильтров, изготовленных из керамики, стекла или целлюлозных материалов и содержащих ионы серебра или ионы меди и включение указанных материалов в установки кондиционирования или устройства принудительной рециркуляции воздуха дают возможность предотвращать многие заболевания.
Конструирование таких фильтров требует, чтобы материалы, которые наносят как покрытие на фильтры, допускали высокую скорость потока воздуха и чтобы бактерицидной активности можно было достичь в условиях короткого времени контакта.
Данная проблема решена с помощью наноматериалов по изобретению в том отношении, что они являются причиной заметного повышения площади поверхности с показателями площади поверхности, возрастающими на порядок 103, и они способны реально проявлять бактерицидное действие при времени контакта порядка 5 минут, как предусматрено в стандартах UNI-EN 1276, апрель 2000, и UNI-EN 13697, декабрь 2001.
Фильтры с покрытием из наноматериалов по изобретению также можно легко восстанавливать до их начальной антибактериальной эффективности погружением в спиртовые растворы, содержащие ионы металлов, такие как Ag+ или Cu2+.
Краткое описание чертежей
Фиг. 1 схематически иллюстрирует структуру наночастицы по изобретению;
Фиг. 2 иллюстрирует электронный спектр поглощения, показывающий степень адсорбции 4-меркаптофенилбороновой кислоты на TiO2;
Фиг. 3 иллюстрирует электронный спектр поглощения, показывающий степень адсорбции ТВА (Hdcb) на TiO2;
Фиг. 4 является схематическим представлением определенного варианта осуществления наночастицы по изобретению.
Подробное описание изобретения
Согласно особенности настоящего изобретения получают нанокристаллические субстраты, содержащие АОх, которые модифицируют бифункциональными лигандами L, состоящими из органических молекул, содержащих функциональные группы, способные связывать органическую молекулу с нанокристаллическим субстратом, а также функциональные группы, способные связываться с ионами металлов, обладающими антибактериальной активностью, например ионами Ag+ или Cu2+.
Согласно другой особенности настоящего изобретения получают нанокристаллические субстраты, содержащие АОх, которые модифицируют бифункциональными лигандами L, состоящими из металлоорганических молекул, таких как комплексы переходных металлов, содержащих функциональные группы, способные связывать комплекс с нанокристаллическим субстратом, а также функциональные группы, способные связываться с ионами металлов, обладающими антибактериальной активностью, например ионами Ag+ или Cu2+.
Такие нанокристаллические соединения представлены формулой (I)
где АОх представляет оксид металла или оксид металлоида, где х = 1 или 2;
Men+ представляет собой ион металла, обладающий антибактериальной активностью, где n = 1 или 2, предпочтительно, Ag+ или Cu++;
L представляет собой бифункциональную молекулу, или органическую, или металлорганическую, способную одновременно связываться с оксидом металла или оксидом металлоида и ионом металла Меn+;
i представляет число групп L-Men+, связанных с наночастицей АОх.
Величина параметра i будет зависеть от различных факторов, таких как размер наночастицы АОх, природа лиганда L и способ, используемый для его получения. В контексте настоящего изобретения i соответствует числу лигандов L, с которыми наночастица способна связываться, когда указанную наночастицу АОх вводят в контакт с раствором лиганда L в течение времени в интервале от 10 мин до 72 час, предпочтительно в интервале 3-24 часа.
Наночастицы по изобретению имеют размер менее 40 нм, предпочтительно менее 30 нм, предпочтительнее менее 15 нм. Наночастицы размером менее 15 нм дают прозрачные суспензии, которые имеют относительно широкий интервал применений.
Оксиды металлов или оксиды металлоидов АОх, которые можно использовать согласно настоящему изобретению, представляют собой, например, коллоидный диоксид кремния, диоксид титана, диоксид циркония, диоксид олова и оксид цинка.
Согласно общей особенности настоящего изобретения антибактериальная и антивирусная активность описанных наноматериалов проявляется даже в отсутствие слабого излучения.
Согласно другой особенности настоящего изобретения нанокристаллические материалы по изобретению или нанокристаллические материалы, состоящие только из оксида АОх, смешивают с катионогенными поверхностно-активными веществами, обладающими антибактериальной активностью, которые способны адсорбироваться на поверхности наночастиц АОх или которые способны образовывать смеси, устойчивые во времени, содержащие суспензии описанных наноматериалов.
Согласно еще одной особенности настоящего изобретения возможно восстановление начальной бактерицидной активности субстратов в случае обеднения антибактериальными ионами металлов (Ag+ или Cu2+) до ее начальной величины просто путем погружения субстратов в спиртовый раствор, содержащий определнный(ые) ион(ы) металла(ов).
Согласно еще одной своей особенности настоящее изобретение относится к дерматологическим композициям для лечения дерматологических расстройств, например акне и пролежней.
Бифункциональные лиганды L на основе комплексов переходных металлов
Комплексы переходных металлов, которые можно использовать для описанной цели, должны содержать органические лиганды, координируемые центральным атомом металла, с одной из следующих функциональных групп: бороновой (-В(ОН)2), фосфонильной (-РО3Н2) или карбоксильной (-СООН). Такие функциональные группы служат для связывания комплекса с нанокристаллическим субстратом АОх. Другие группы, которые координирует центральный атом металла, способны связываться с ионами металлов с антибактериальной активностью. Примерами таких групп являются лиганды типа Cl-, Br-, I-, CNS-, NH2, CN- и NCS-.
Металлоорганические комплексы L по изобретению предпочтительно содержат органические лиганды типа дипиридила и/или трипиридила, координируемые центральным атомом металла (М) и содержащие следующие функциональные группы: карбоксильную (-СООН), фосфоновую (-РО3Н2) или бороновую (-В(ОН)2), способные связываться с наночастицами, состоящими из АОх; и также содержащие следующие функциональные группы: Cl-, Br-, I-, CNS-, NH2, СN- и NCS-, координируемые указанным центральным атомом металла (М) и способные связываться с ионами Ag+ или Cu2+. Предпочтительно указанные дипиридильные и трипиридильные группы замещены карбоксильными группами, предпочтительнее в пара-положении относительно азота пиридина. В случае, когда в указанном металлоорганическом комплексе L присутствуют более одной дипиридильной или трипиридильной группы, необязательно, одна из таких групп может быть незамещенной.
Что касается ионов металла (М), присутствующих в L, имеющих координации октаэдрического типа или имеющих другие типы координации, соответствующие тетраэдрической конфигурации, конфигурации плоского прямоугольника или конфигурации плоского квадрата, конфигурации тригональной пирамиды или конфигурации пирамиды с квадратным или прямоугольным основанием, кандидатами являются любые металлы, находящиеся в первом, втором или третьем ряду переходных металлов в Периодической таблице элементов, которые могут образовывать устойчивые бифункциональные молекулы описанного типа.
Предпочтительнее, описанные металлоорганические комплексы L имеют координацию октаэдрического типа. Предпочтительно, переходные металлы, координирующие такие комплексы, выбирают из Cr, Mn, Fe, Co, Ni, Cu, Zn, Ru, Rh, Pd, Re, Os, Ir и Pt.
С другой стороны, металлоорганические комплексы L по изобретению могут иметь отрицательный заряд и могут образовывать соли с катионами, предпочтительно органическими катионами, такими как тетраалкиламмониевые катионы. Такие катионы создают возможность солюбилизации таких частиц в органических растворителях, что вносит вклад в процесс адсорбции наноматериалов на основе оксидов металлов или оксидов металлоидов.
Таким образом, такие молекулы могут служить в качестве бифункциональных лигандов, образующих однородный адсорбированный слой на наночастицах АОх, и в то же время могут связываться с ионами металлов с антибактериальной активностью.
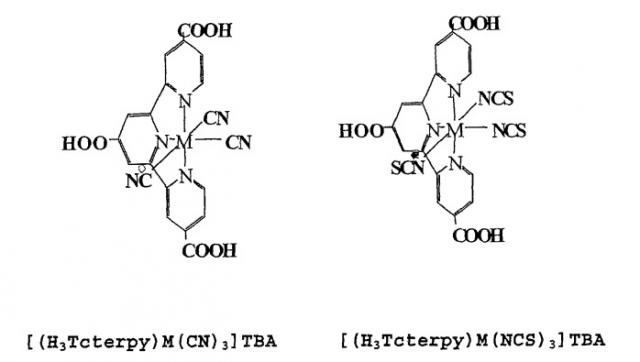
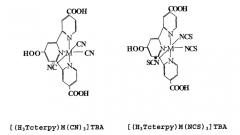
Примеры таких комплексов с октаэдрической координацией представлены в данном описании ниже.
ТВА = катион тетрабутиламмония
Н 3 Tcterpy = 4,4',4”-трикарбокситрипиридил
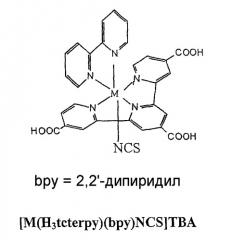
Группу ТВА можно заменить другими тетраалкиламмониевыми катионами, которые создают возможность солюбилизации комплекса в органических растворителях.
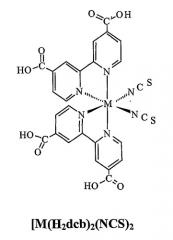
H 2 dcb = 2,2'-дипиридил-4,4'-дикарбоновая кислота
Бифункциональные лиганды L на основе органических соединений
Бифункциональные лиганды L органического типа, которые применимы в контексте настоящего изобретения, включают виды молекул, содержащих группы, которые могут привести к взаимодействию с наночастицами АОх, и также содержат функциональные группы, которые могут связываться с ионами, обладающими антибактериальной активностью. Примеры таких видов молекул включают органические молекулы, содержащие функциональные группы: карбоксильную (-СООН), фосфоновую (-РО3Н2) и бороновую (-В(ОН)2), которые способны внести вклад в адсорбцию на поверхности оксида АОх; и функциональные группы >N, >NH2, -CN, -NCS или -SH, которые способны связываться с ионами металлов с антибактериальной активностью, такими как Ag+ или Cu2+.
Такие органические лиганды, предпочтительно, выбирают из
-- азотсодержащих гетероциклов с 6-18 членами, предпочтительно пиридина, дипиридила или трипиридила, замещенных одним или несколькими заместителями, выбранными из карбоксила (-СООН), бороновой группы (-В(ОН)2), фосфоновой группы (-РО3Н2), меркаптановой группы (-SH) и гидроксила (-ОН);
-- арилов С6-С18, предпочтительно выбранных из фенила, нафтила и бифенила, замещенных одним или несколькими заместителями, выбранными из карбоксила (-СООН), бороновой группы (-В(ОН)2), фосфоновой группы (-РО3Н2), меркаптановой группы (-SH) и гидроксила (-ОН); и
-- монокарбоновых и дикарбоновых кислот С2-С18, замещенных одной или несколькими меркаптановыми группами (-SH) и/или гидроксильными группами (-ОН).
Предпочтительнее, примеры таких бифункциональных органических лигандов включают
-- пиридин, дипиридил или трипиридил, функционализированные карбоксильными группами, бороновыми группами или фосфоновыми группами; меркаптоянтарную кислоту, меркаптоундекановую кислоту, меркаптофенол, меркаптоникотиновую кислоту, 5-карбоксипентантиол, меркаптомасляную кислоту и 4-меркаптофенилбороновую кислоту.
Экспериментальные методы
Теперь будут описываться экспериментальные методы, относящиеся к получению наноматериалов, состоящих из АОх, используемых при разработке настоящего изобретения, характеристики указанных наноматериалов и антибактериальные свойства указанных наноматериалов.
Получение прозрачных суспензий наноматериалов на основе диоксида титана и диоксида циркония
Наноматериалы на основе диоксида титана можно получить с наночастицами таких размеров, что они образуют прозрачные или непрозрачные суспензии в водных или органических растворителях. Суспензии TiO2, состоящие из наночастиц размером менее 15 нанометров, обычно являются прозрачными и при нанесении на поверхность они не изменяют ее цвет. Коммерческие продукты диоксиды титана, такие как “Biossido di Titanio P 25” (поставляются Degussa), дают суспензии, которые являются белыми и непрозрачными, поскольку средний диаметр наночастиц TiO2 находится в интервале 25-30 нм. Для целей настоящего изобретения можно использовать или непрозрачные или прозрачные наноматериалы. Однако прозрачные наноматериалы представляют больший интерес, поскольку они предоставляют более широкий интервал возможных применений. Прозрачные коллоидные суспензии на основе коллоидного диоксида кремния или диоксида олова являются коммерчески доступными.
Способы получения суспензий на основе диоксида титана и диоксида циркония будут описаны далее. Указанные количества реагентов можно изменять без отхода от новизны и объема настоящего изобретения.
(А) Прозрачные суспензии на основе TiO 2
В химический стакан загружают 300 мл дистиллированной Н2О и 2,1 мл сильной кислоты, например концентрированной HNO3 (65%, мас./мас.). Через 10 мин при перемешивании через капельную воронку добавляют 50 мл изопропоксида титана (поставляемого Fluka). Сразу же образуется выпадающий в осадок TiO2 молочного цвета. Затем смесь греют при 80°С в течение 8-12 часов, обеспечивая продолжение перемешивания и поддержание постоянной температуры. Во время нагревания осадок снова растворяется, и смесь становится опалесцирующей. Во время фазы нагревания коллоидную суспензию концентрируют до конечного объема 100-200 мл, что соответствует концентрации TiO2 150-75 г/л. Наночастицы диоксида титана, полученные по окончании процесса, имеют диаметр в интервале 6-15 нм. Затем суспензию, сконцентрированную до 100 мл, разбавляют дистиллированной водой и этанолом, и получают конечный прозрачный раствор (рН ≈ 2), который содержит, в объеме 1 литр, TiO2 в концентрации 1,5% и спирт в интервале 10-50%, предпочтительно, 25%.
(В) Прозрачные суспензии на основе ZrO 2
В химический стакан загружают 300 мл дистиллированной Н2О и 2,1 мл сильной кислоты, например концентрированной HNO3 (65%). Через примерно 10 мин при перемешивании с помощью капельной воронки добавляют 76 мл 70% раствора тетраизопропоксида циркония в изопропаноле.
Сразу же видно образование выпадающего в осадок ZrO2 беловато-молочного цвета. Затем смесь греют при 90°С в течение 8-12 часов, обеспечивая продолжение перемешивания и поддержание постоянной температуры. Во время нагревания осадок снова растворяется, причем образуется суспензия на вид молочного цвета, которую концентрируют до 140-280 мл, что соответствует концентрации ZrO2 150-75 г/л. Затем суспензию, сконцентрированную до 140 мл, разбавляют дистиллированной водой и этанолом, и получают опалесцирующую суспензию (рН ≈ 2), которая содержит ZrO2 в концентрации 1,5% и спирт в интервале 10-50%, предпочтительно 25%.
(С) Непрозрачные суспензии на основе TiO 2
Нейтральные водные непрозрачные суспензии на основе диоксида титана можно получить, добавляя диоксид титана Р 25 в водные растворы “Тритона Х 100” (поставляемого Fluka).
Нейтральные водные опалесцирующие суспензии на основе диоксида титана также можно получить из пероксититановой кислоты путем модификации процедуры, описанной в литературе (Ichinose H., Terasaki M. and Katsuki H., 1996, J. Ceramic Soc. Japan, 104, 715).
При типичном получении 150 мл TiCl4 в 20% HCl загружают в 1-л химический стакан и к полученному раствору добавляют 826 мл NH4OH, разбавленного 1:9 дистиллированной водой. Полученный раствор имеет нейтральный рН (рН 7), и выпадает в осадок титановая кислота Ti(OH)4. Полученный преципитат белый по цвету и имеет консистенцию геля. Преципитат собирают на фильтре пористостью G3 и промывают 750-1000 мл дистиллированной воды (до тех пор, пока не достигнут полного удаления хлорида, что можно показать обработкой жидкого фильтрата AgNO3). Если хлорид присутствует, отмечают выпадение в осадок белого творожистого AgCl. Преципитат, содержащий титановую кислоту (Ti(OH)4), собирают и суспендируют в 200 мл дистиллированной воды, имеющей проводимость менее 1,5 мкСм с рН в интервале 5-7; к полученной смеси постепенно в течение 20-30 минут добавляют 92 мл 30% Н2О2. Отмечают растворение преципитата и образование раствора желтого цвета, содержащего пероксититановую кислоту общей формулы
где х равен величине в интервале 3-6.
Наконец, раствор греют в течение 1 часа при 70°С для разложения избытка Н2О2, и затем обрабатывают в автоклаве в течение 8 час при 120°С. На данном этапе процедуры пероксититановая кислота разлагается до диоксида титана, преимущественно, в аллотропной форме анатаза. Полученная суспензия наночастиц имеет рН, близкий к нейтральному, непрозрачна по внешнему виду и является устойчивой во времени.
Получение суспензий наноматериалов, обладающих антибактериальной и антивирусной активностью
Для того чтобы придать суспензиям наноматериалов бактерицидную активность и антивирусную активность, осуществляют первую стадию адсорбции, на которой адсорбируется бифункциональный лиганд L, с последующим смешиванием с водным или спиртовым раствором, содержащим ионы Ag+ или Cu2+. Затем к суспензии наноматериалов, функционализированной ионами Ag+ или Cu2+, можно добавить аммониевую соль, действующую как катоиногенное поверхностно-активное вещество, которая имеет антибактериальную активность, или можно добавить независимо к или адсорбировать на наноматериалах, которые являются предметом настоящего изобретения; такое получение описано выше.
Как правило, для адсорбции бифункционального лиганда L на наноматериале АОх, описанном в настоящем изобретении, требуется время порядка 12-36 час, в то время как связывание ионов Ag+ или Cu2+ с лигандом L стабилизируется почти мгновенно добавлением растворов, содержащих указанные ионы, к суспензиям наноматериалов, функционализированных лигандом L. Накопленные экспериментальные данные, описанные в данном описании ниже, показывают, что катионогенные поверхностно-активные вещества, такие как алкиламмониевые соли, также могут частично адсорбироваться на поверхности наноматериалов.
Способы получения, описанные ниже, детально показывают препаративную методологию получения суспензий наноматериалов с бифункциональными лигандами L, с ионами Ag+ и с катионогенными поверхностно-активными веществами. Аналогичные способы получения можно использовать для получения таких суспензий с ионами Cu2+. Указанные количества реагентов можно изменять в пределах объема настоящего изобретения.
(D) Адсорбция 4-меркаптофенилбороновой кислоты и ионов Ag+ на “TiO2 P25” (поставляется Degussa)
К раствору, содержащему 2×10-5 молей 4-меркаптофенилбороновой кислоты, растворенной в 50 мл этанола, добавляют 1 г TiO2 P25 (поставляется Degussa). Суспензию перемешивают 24 часа. 4-Меркаптофенилбороновая кислота имеет полосу поглощения при 255 нм, которую можно приписать переходу π-π* в фенольном цикле. Такая полоса электронного поглощения создает возможность контроля за адсорбцией бороновой кислоты на поверхности наноматериала как функции времени. Известно, что адсорбция происходит за счет взаимодействия бороновой функциональной группы с поверхностью полупроводника. Спектры электронного поглощения на Фиг. 2 показывают, что количество 4-меркаптофенилбороновой кислоты, адсорбированной на поверхности “TiO2 P25”, достигает 35% от начальной концентрации за 24 часа.
Раствор центрифугируют 10 мин при 4000 об/мин, получая прозрачный раствор, твердое вещество промывают 20 мл этанола и затем ресуспендируют в 50 мл этанола при перемешивании. К полученной суспензии добавляют 7,2×10-6 молей растворимой соли серебра, предпочтительно лактата серебра или ацетата серебра. Полученная суспензия белая по цвету, не имеет запаха и устойчива во времени.
(Е) Адсорбция 4-меркаптофенилбороновой кислоты и ионов Ag+ на прозрачных суспензиях TiO2 по способу (А) и на продуктах фирмы NM Tech
Разбавляют 100 мл прозрачного раствора диоксида титана, полученного согласно способу (А) и содержащего 15% TiO2, 100 мл дистиллированной воды и 200 мл раствора 0,052 г 4-меркаптофенилбороновой кислоты в этаноле. Суспензию перемешивают 24 часа, и по окончании указанного периода спектрофотометрическое определение показывает, что бороновая кислота полностью адсорбирована на наночастицах полупроводника. Небольшие размеры наночастиц относительно “TiO2 P25” и являющаяся результатом большая площадь поверхности суспендированного вещества ответственны за полную адсорбцию бифункционального лиганда. К прозрачной, не имеющей запаха, суспензии при перемешивании добавляют стехиометрическое количество (относительно L) соли серебра, например, лактата серебра (0,06 г) или ацетата серебра (0,05 г). После 1-час непрерывного перемешивания добавляют 10-20 мл, предпочтительно, 12 мл, 50% (мас./об.) водного раствора хлорида бензалкония, и суспензию перемешивают еще в течение 1 часа. Затем концентрированную суспензию разбавляют дистиллированной водой и этанолом и получают 1 л опалесцирующей суспензии (рН ≈ 2), которая содержит TiO2 в концентрации 1,5% и этанол в интервале 10-50%, предпочтительно 25%.
Обнаружено, что прозрачная суспензия неограниченно устойчива. Ниже в данном описании такой продукт для краткости называется “бактерклином” (“Bactercline”).
Такую же процедуру можно использовать для модификации прозрачных суспензий наноматериалов, продаваемых NM Tech. Ltd. и называемых “PSO 419”, когда количества бифункционального лиганда и ионов серебра подбирают на основании количества диоксида титана в продукте. Например, продукт “PSO 419”, который схож с продуктом, полученным согласно способу (А), и в котором содержание TiO2 составляет 2%, и рН примерно равен 2, можно превратить в антибактериальный и антивирусный продукт с использованием способа, аналогичного описанному выше.
В частности, 50 мл раствора “PSO 419D2”, содержащего 2% TiO2, разбавляют 2,2 мг 4-меркаптофенилбороновой кислоты (2,05×10-5 М), и суспензию перемешивают 24 часа. К полученному раствору, не имеющему запаха, добавляют 2,05×10-5 М лактата серебра или ацетата серебра. Наконец, после 1-час непрепрывного перемешивания добавляют 8-20 мл, предпочтительно 12 мл, водного раствора хлорида бензалкония, и суспензию перемешивают еще в течение 1 часа. Полученная прозрачная суспензия неограниченно устойчива.
Следует отметить, что другие непрозрачные продукты на основе TiO2, продаваемые NM Tech. Ltd., такие как “AT-01” и “AT-03”, можно обрабатывать согласно описанным способам по настоящему изобретению и получать устойчивые суспензии или порошки, которые обладают антибактериальной и антивирусной активностью. Например, образец в 50 мл раствора “AT-01”, содержащего 1,7% TiO2, разбавляют 50 мл этанола, содержащего 3,8 мг растворенной 4-меркаптофенилбороновой кислоты (1,9×10-5 М), суспензию перемешивают 24 часа, и получают продукт, не имеющий запаха. Затем добавляют 1,9×10-5 М лактата серебра или ацетата серебра. Полученная суспензия со временем дает тонкий осадок.
(F) Адсорбция катионогенных поверхностно-активных веществ на диоксиде титана
Катионогенные поверхностно-активные вещества с антибактериальной активностью, как правило, адсорбируются на наноматериалах на основе TiO2, ZrO2, SnO2, ZnO и SiO2. Адсорбция на отрицательно заряженных или нейтральных наночастицах происходит почти мгновенно. В случае суспензий наноматериалов с щелочным рН добавление солей типа солей бензалкония, таких как, например, хлорид бензилдодецилдиметиламмония или хлорид бензилгексадецилдиметиламмония или хлорид бензалкония, вызывает осаждение суспензий; в то время как в случае суспензий наноматериалов с нейтральным или кислотным рН суспензия устойчива.
В косвенных испытаниях по адсорбции хлорида бензалкония на наноматериалах на основе TiO2 при нейтральном рН используют кондуктометрические измерения. Ассоциация через адсорбцию катиона бензилдиалкиламмония на TiO2 должна, как и ожидалось, вызывать уменьшение проводимости, что подтверждается экспериментом, описанным далее.
Разбавленный 1:10 50% (мас./об.) раствор хлорида бензалкония имеет проводимость 4,7 мСм. Если объем такого раствора увеличить от 10 до 15 мл добавлением дистиллированной воды, проводимость снижается до 3,90 мСм. Если вместо этого разбавить раствор, добавляя 5 мл нейтральной суспензии диоксида титана, полученной из пероксититановой кислоты согласно способу (С), или эквивалентного продукта “AT-03” при нейтральном рН, измеренная проводимость составляет 3,60 мСм. Уменьшение проводимости на 300 мкСм можно отнести к адсорбции катионогенного поверхностно-активного вещества на поверхности диоксида титана.
(G) Адсорбция 2,2'-дипиридил-4-карбокси-4'-карбоксилаткислоты, Ag+ и Cu2+ на “TiO2 P25” (поставляется Degussa)
Анион 2,2'-дипиридил-4-карбокси-4'-карбоксилаткислоты (сокращенно “Hdcb”) получают, добавляя один эквивалент гидроксида тетрабутиламмония (сокращенно ТВАОН) к 2,2'-дипиридил-4,4'-дикарбоновой кислоте (сокращенно “H2dcb”), которая плохо растворима в воде и находится в твердой форме. Лиганд в форме монокарбоксилата (также называемой “монопротонированной формой”) и в виде соли тетрабутиламмония (сокращенно “TBA(Hdcb)”) таким образом можно солюбилизировать в метаноле или этаноле и можно адсорбировать на диоксиде титана.
К раствору 1х10-4 молей TBA(Hdcb) в 100 мл этанола добавляют 5 г “TiO2 P25” (поставляется Degussa). Суспензию перемешивают 24 часа. Лиганд TBA(Hdcb) имеет полосу поглощения при 294 нм из-за переходов π-π*, что допускает контроль за его адсорбцией на наноматериалах как функции времени.
Спектры на Фиг. 3 показывают, что через 24 часа лиганд полностью адсорбирован на поверхности нанокристаллического субстрата. Известно, что адсорбция происходит за счет взаимодействия карбоксильных функциональных групп с поверхностью полупроводника.
Затем суспензию центрифугируют 10 мин при 4000 об/мин, и твердое вещество промывают 50 мл метанола. Затем полученный наноматериал, функционализированный лигандом (сокращенно TiO2/TBA(Hdcb)), окончательно сушат в вакууме при температуре окружающей среды.
Две порции TiO2/TBA(Hdcb) по 2 г каждая ресуспендируют в 100 мл этанола. К одной суспензии при перемешивании добавляют 8 мг лактата серебра; а к другой суспензии добавляют 7 мг CuCl2. Две суспензии имеют различные заместители: суспензия, функционализированная ионами меди - TiO2/TBA[Hdcb]/Cu2+ - остается устойчивой, TiO2/TBA[Hdcb]/Ag+ со временем образует осадок.
(Н) Адсорбция металлоорганических лигандов (L) и ионов Ag+ на нейтральных суспензиях TiO2
Бифункциональные металлорганические лиганды L, описанные выше, можно закрепить на нейтральных суспензиях диоксида титана, полученных согласно способу (С), причем наноматериалы суспендируют в спиртовых растворах металлорганических лигандов концентрации примерно 10-3-10-4 М. Суспензию перемешивают 12 час, в течение которых металлорганический лиганд L полностью адсорбируется на поверхности наноматериалов.
Добавление стехиометрических количеств серебра относительно лиганда L в спиртовом растворе соответствует образованию аддуктов, в которых ион серебра Ag+ закреплен на неорганическом лиганде, что схематически иллюстрируется на Фиг. 4 в случае комплекса (H2dcb)2Ru(NCS)2 (H2dcb = 2,2'-дипиридил-4,4'-дикарбоновая кислота). Присутствие карбоксильных функциональных групп делает возможной адсорбцию комплекса и равномерного покрытия нанокристаллического материала за время порядка 2-3 час при 50°С и за 12 час при температуре окружающей среды. На следующей стадии к метанольному раствору добавляют соль сербера, например нитрат серебра, лактат серебра или ацетат серебра, в стехиометрическом отношении 2:1 к числу молей (H2dcb)2Ru(NCS)2. Наличие двух групп NCS дает возможность ионам Ag+ связываться моментально, как показано на Фиг. 4.
Согласно частному варианту осуществления настоящего изобретения нанокристаллические материалы формулы (I) можно включать в дерматологические композиции для лечения бактериальных дерматологических болезней, таких как, например, акне или пролежни.
Получение некоторых таких композиций описано в данном описании ниже в качест