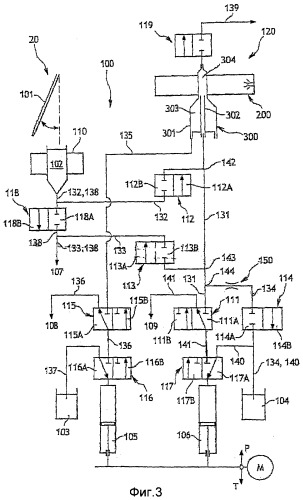
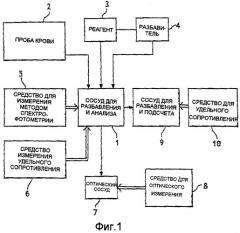
Гидравлическое устройство для устройства для анализа крови, способ, связанный с указанным устройством, и анализатор, оснащенный таким устройством
Иллюстрации
Показать всеНастоящее изобретение относится к гидравлическому устройству для устройства для анализа крови. Гидравлическое устройство для автоматического устройства для анализа крови содержит первый шприц для инжектирования потока пробы крови в проточный оптический сосуд и второй шприц для создания потока обволакивающей жидкости вокруг потока пробы с обволакивающей жидкостью. Причем гидравлический контур, в котором движутся поток пробы крови и поток обволакивающей жидкости, выполнен таким образом, что по меньшей мере один из первого или второго шприцев по выбору выполняет, в первом случае, выталкивание соответствующей жидкости в проточный оптический сосуд или, во втором случае, другую функцию, такую как разбавление пробы или обработка пробы на основе реагента. При этом гидравлический контур дополнительно содержит клапаны для переключения различных контуров в гидравлическом контуре для упомянутого выбора. Также гидравлический контур дополнительно содержит регулировочное средство, которое выполнено с возможностью регулировки расхода потока пробы относительно расхода обволакивающей жидкости. Техническим результатом изобретения является упрощение и производство автоматического устройства, использование единственного аналитического раствора и повышение точности измерений. 3 н. и 18 з.п. ф-лы, 1 табл., 21 ил.
Реферат
Настоящее изобретение относится к гидравлическому устройству для устройства для анализа крови, способу, связанному с указанным устройством, и анализатору, оснащенному таким устройством.
При анализе образца крови обычно стремятся определить:
- общее количество лейкоцитов;
- более конкретно, количество лейкоцитов по субпопуляциям (базофилы, эозинофилы, нейтрофилы, моноциты и лимфоциты);
- количество эритроцитов и тромбоцитов и
- уровень гемоглобина.
Известно несколько методик анализа, в частности:
- оценку гемоглобина производят после лизиса эритроцитов, т.е. разрушения мембран клеток эритроцитов и путем измерения гемоглобина, выделившегося в среду спектрофотометрическими методами; оценка гемоглобина также требует стабилизации гемоглобина в сложной форме (оксигемоглобин и цианметгемоглобин) для измерения спектральной поглощательной способности одного соединения на соответствующей длине волны;
- в образце крови проводят общий подсчет лейкоцитов по резистивности, проводя специфический лизис эритроцитов и защищая лейкоциты;
- дифференцируют лейкоциты, подсчитывая их количество по субпопуляции:
- либо измеряя волюметрическую резистивность после конкретного лизиса эритроцитов, защиты лейкоцитов и регулировки рН; однако такой способ не позволяет дифференцировать все субпопуляции в одном анализе;
- или оптическим способом, в частности, методом проточной цитометрии, после специфического лизиса и защиты лейкоцитов, измеряя различные параметры (в частности, дифракцию, флуоресценцию, поглощательную способность) в потоке лейкоцитов по оси узкого, среднего и широкого углов и, опционально, после добавления метящего агента (например, хлоразол черный, или пигменты для маркирования ДНК и РНК, или флуоресцентные пигменты) и путем измерения на разных длинах волн; такая методика позволяет дифференцировать субпопуляции лейкоцитов;
- подсчет эритроцитов и тромбоцитов проводят в разведенном образце путем измерения резистивности без добавления конкретного реагента.
Существует много автоматических анализаторов клеток крови, в которых используются эти методики для проведения как можно более полного анализа образца крови.
В таких автоматических анализаторах традиционно сосуществуют два разных контура анализа:
- первый контур, выполненный с возможностью измерения гемоглобина и/или проведения подсчета общего числа лейкоцитов; и
- второй контур, выполненный с возможностью проведения дифференциации образца крови и/или подсчитывать лейкоциты методом проточной цитометрии.
Каждый контур характеризуется степенью разбавления образца крови в соответствии с используемым измерительным средством, добавлением одного или более реагента и соответствующим средством для проведения измерений.
Так, для измерения гемоглобина и подсчета лейкоцитов контур типично содержит так называемую счетную камеру, в которой разбавляют образец крови, реагент, содержащий в частности соединение для лизиса эритроцитов, стабилизирующее соединение для комплекса, сформированного из гемоглобина, и к нему добавляют соединение лейкопротектора и непосредственно в ней измеряют гемоглобин спектрофотометрическим методом и количество лейкоцитов по резистивности. Степень разбавления выбрана такой, чтобы аналитический раствор был идеально гомогенен и чтобы устройство обнаружения не переполнялось. Степень разбавления составляет от 1/100 до 1/500, обычно от 1/160 до 1/180.
Для дифференциации лейкоцитов путем проточной цитометрии в контуре используется сосуд для разбавления образца крови, к которому добавляют один или более реагентов, содержащих агент для лизиса эритроцитов, факультативно дифференцирующий агент (например, флуоресцентный пигмент для ДНК или РНК лейкоцитов), затем часть этого раствора отбирают для инъекции в проточную оптическую камеру проточного цитометра. Здесь используется степень разбавления менее 1/100, что обеспечивает оптимальное время анализа в имеющихся в настоящее время на рынке цитометрах (гидрофокусного типа).
Следовательно, обычно для двух контуров анализа приходится использовать по меньшей мере два разных реагента и в этих двух контурах анализа приходится применять две разные степени разбавления.
Главной целью производителей является упрощение существующих автоматических устройств за счет уменьшения количества компонентов и реагентов, что позволяет снизить расходы на производство и обслуживание, уменьшить габариты автоматических устройств, без уменьшения, однако, времени на полный анализ образца крови.
Настоящее изобретение направлено на достижение этих целей.
В международной публикации WO 2004/003517 для этой цели предлагается способ и оборудование, в котором два контура анализа имеют общие средства. Принцип заключается в проведении первого разбавления образца крови в единственном разбавляющем сосуде и в последовательном переносе частей этого раствора, имеющих выбранный объем, в блок измерения или подсчета, чтобы каждый раз измерять или подсчитывать разные элементы, содержащиеся в образце крови. Для проведения полного анализа, а именно подсчета эритроцитов и тромбоцитов, подсчета лейкоцитов, измерения гемоглобина и дифференциации лейкоцитов, в документе описано следующее решение: используют первый перенос для подсчета эритроцитов и тромбоцитов, в разбавляющий сосуд добавляют лизирующий агент, затем выполняют второй перенос для подсчета лейкоцитов, осуществляют третий перенос лизированного раствора для измерения уровня гемоглобина, добавляют реагент для дифференциации лейкоцитов и выполняют четвертый перенос для проведения дифференциации лейкоцитов в блоке измерения.
Этот принцип может позволить использовать единственный так называемый разбавляющий сосуд, но не позволяет сократить время анализа, поскольку измерения или подсчеты выполняются последовательно после каждого переноса части раствора. Более того, он требует точного управления объемом последовательно добавляемых реагентов и разбавителей, переносимых в блок измерения. Кроме того, он также требует применения нескольких шприцов и лизирующих реагентов.
Целью настоящего изобретения является также устранение указанных недостатков.
Согласно первому объекту, настоящее изобретение относится к способу автоматического анализа образца крови, а также к монореагенту и к устройству для реализации этого способа.
Способ по настоящему изобретению отличается тем, что:
- в едином сосуде для разбавления и анализа формируют аналитический раствор, содержащий образец крови, разбавитель и:
- по меньшей мере одно соединение для лизирования эритроцитов;
- по меньшей мере одно соединение для защиты лейкоцитов; и
- по меньшей мере одно соединение для стабилизации гемоглобина в форме хромогенного комплекса;
- после лизирования эритроцитов методом спектрофотометрии измеряют уровень гемоглобина в этом аналитическом растворе в сосуде; и
- отбирают из сосуда соответствующее количество аналитического раствора, на котором оптическими средствами проводят дифференциацию лейкоцитов.
Подсчет лейкоцитов может проводиться совместно в сосуде для анализа и/или оптическими средствами.
Подсчет эритроцитов и факультативно тромбоцитов может проводиться, например, на предыдущем этапе способа, на образце единого раствора в сосуде для анализа.
Таким образом, настоящее изобретение основано на концепции единственного аналитического раствора, используемого в том виде, в котором он существует для двух типов анализа которые обычно проводят в двух отдельных контурах, а именно, с одной стороны, для подсчета гемоглобина и опционально подсчета лейкоцитов и, с другой стороны, для дифференциации лейкоцитов оптическими средствами, при этом в аналитическом растворе объединены соединения реагентов, способные выполнить эти виды анализа, благодаря их природе и их количеству. Эти введенные соединения реагентов выбирают так, чтобы они были химически совместимы друг с другом и в количествах, подходящих для нужного анализа. Их можно выбирать из соединений, типично применяемых в предшествующем уровне техники. Можно также использовать коммерческие составы, которые обычно используются для дифференциации лейкоцитов, т.е. содержащие соединение для лизирования эритроцитов и соединение лейкопротектора, и добавить к нему третье соединение реагента, предназначенное для стабилизации гемоглобина в форме хромогенного комплекса.
Благодаря такому единственному аналитическому раствору настоящее изобретение, в частности, дает следующие преимущества:
- автоматическое устройство может содержать единственный сосуд для подготовки аналитического раствора;
- измерение гемоглобина можно проводить непосредственно в этом сосуде, наряду с глобальным подсчетом лейкоцитов, измерением резистивности аналитического раствора;
Можно использовать монореагент, объединяющий все соединения "реагентов", необходимые для измерения гемоглобина и для дифференциации лейкоцитов оптическими средствами; это особенно позволяет упростить гидравлические контуры, как будет показано ниже;
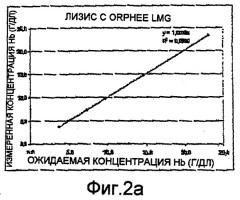
- монораствор образца крови можно переносить непосредственно в единственный раствор и аналитический сосуд, при этом степень разбавления определяется как функция измерения и использованного средства обнаружения. Монореагент может служить разбавителем для получения этого монораствора. Предпочтительно, степень разбавления выбирают от 1/100 до 1/500, в соответствии со степенью разбавления, необходимой для измерения уровня гемоглобина, предпочтительно, также, выбирают степень разбавления 1/175 (1/173 в описанном ниже варианте).
Возможность использования монораствора и монореагента позволяет, благодаря первому объекту настоящего изобретения, значительно упростить аналитическое оборудование, тем не менее, давая возможность проводить полный анализ образца крови.
Согласно настоящему изобретению также предлагается средство для оптических измерений, позволяющее проводить анализ лейкоцитов (подсчет и дифференциацию по субпопуляциям) при степени разбавления выше 1/100, которое определено и описано ниже.
Согласно настоящему изобретению также предлагается монореагент для лизиса для реализации способа по настоящему изобретению, отличающийся тем, что содержит:
- по меньшей мере одно соединение для лизиса эритроцитов;
- по меньшей мере одно соединение для защиты лейкоцитов;
- по меньшей мере одно соединение для стабилизации гемоглобина в форме хромогенного комплекса.
Такой монореагент позволяет методом спектрофотометрии оптическими средствами проводить измерения концентрации гемоглобина в образце крови и дифференциацию лейкоцитов. Он также позволяет проводить резистивный и/или оптический подсчет лейкоцитов. Предпочтительно он выбран так, чтобы обеспечить возможность дифференциации по меньшей мере 5 субпопуляций. Предпочтительно, он выбран так, чтобы не содержать цианидов. Согласно настоящему изобретению соединение для лизиса эритроцитов предпочтительно образовано по меньшей мере одним катионным поверхностно-активным веществом. В известной предпочтительной форме, оно выбрано для образования комплекса оксигенированного гемоглобина (поскольку он не токсичен по сравнению с цианметгемоглобиновым комплексом, в котором имеются ионы цианида). Катионное поверхностно-активное вещество, таким образом, также выбирается так, чтобы формировать только комплекс оксигенированного гемоглобина. Количество катионного поверхностно-активного вещества, таким образом, выбирается так, чтобы эффективно гемолизировать эритроциты и окислять высвобожденный гемоглобин. Он предпочтительно выбран из ряда, содержащего:
- четвертичные аммониевые соли, предпочтительно алкилтриметиламмониевые соли, и еще более конкретно, цетил- додецил- тетрадецил- и гексадецилтриметиламмониевые бромиды и хлориды;
- пиридиновые соли;
- длинноцепочечные этоксилированные амины и
- алкиловые сульфаты (SDS).
Соединение-лейкопротектор по настоящему изобретению - это соединение, которое задерживает или предотвращает разрушение лейкоцитов. Предпочтительно, это неионное или амфотерное поверхностно-активное вещество, предпочтительно выбранное из ряда, содержащего:
- этоксилированные спирты, в частности, 2-феноксиэтанол, полиокисэтиленалкилфениловые эфиры, такие как коммерческие продукты IPEGAL990®, TRITON®, X100 или X114, plurafac® A38 или Brij35®;
- бетаины и сульфобетаины четвертичных аммониевых солей, в частности, лаурамидопропилбетаин (LAB), и додецилдиметил-3-аммоний-1-пропансульфонат (DDAPS), или тетрадецилдиметил-3-аммоний-1-пропансульфонат (TDAPS);
- третичные аминовые оксиды, такие как N,N-диметиллауриламин-N-оксид (LDAO) или 3-[(холамидопропил)-диметиламино-]-1-пропан сульфонат (CHAPS или CHAPSO);
- соединения гликозидного типа и, более конкретно, тритерпеновый сапонин;
- соединения глюцидного типа (маннитол, D-глюкоза, трегалоза, декстран сульфат).
Соединение, которое стабилизирует гемоглобин в форме хромогенного комплекса предпочтительно, выбрано из ряда, содержащего:
- моно- или полидентатные хелаты, имеющие атомы лигандов (не связывающие пары O, N, S и карбоксильных групп СОО- и пр.), в частности:
этилендиаминтетрауксусная кислота (EDTA) или этиленгликоль-бис-(3-аминоэтленэфир)N-N'-тетрауксусная кислота (EGTA) и, в частности, их натриевые или дикалиевые соли;
оксалат калия K2OxOx=C2O4 2;
гидроксиламиновые соли (предпочтительно, гидрохлориты); и
органические кислоты (в частности, муравьиная или уксусная).
- ароматические соединения (моно- или полидентатные хелаты), имеющие атомы лигандов (не связывающие пары O, N, S и т.д.), в частности:
Tiron®;
8-гидроксихинолин и его производные;
пиридин или бипиридин и их производные;
1,10-фенантролин и его производные;
соединения фенола (моно или бис и их производные);
пиразол и/или пиразолоны и их производные;
имидазол и его производные;
сульфосалициловая кислота; и
- сапонины, третичные оксиды амина, бетаины и сульфобетаины четвертичных аммониев (такие, как DDAPS, TDAPS, LAB).
В дополнение к этим трем соединениям, определенным настоящим изобретением, можно добавлять (моно-)реагент(ы):
- по меньшей мере один пигмент (или смесь), специфически помечающий определенные лейкоциты и, более конкретно, эозинофилы (или базофилы), для обеспечения возможности выделения по меньшей мере 5 основных субпопуляций, выбранный из ряда, содержащего:
цианины;
Oxazine 750;
реагенты Райта и Романовского;
DAPI;
Хлоразол черный Е;
толуидиновый синий;
астра синий;
триазоловый оранжевый G или синий;
другие флуоресцентные реагенты;
- по меньшей мере один фиксирующий агент, позволяющий укреплять мембрану лейкоцитов, которым предпочтительно является альдегид и, более конкретно, глутаральдегид или формальдегид;
- по меньшей мере один смачивающий агент для оптимизации струйной техники и предотвращения формирования пузырьков, который также действует как солюбилизатор для остатков органических веществ, выбранный из ряда, содержащего:
спирты (метанол, этанол или пропан-2-ол);
гликоли (этилен- или пропиленгликоль);
этоксилированные гликоли (в частности, Triton® X100 или Brij35®);
гликозидные соединения (TWEEN80® или TWEEN20®);
при этом концентрация фиксирующего агента и солюбилизатора строго ограничена, поскольку их избыток может воспрепятствовать лизису эритроцитов и изменить оптические свойства лейкоцитов; и
- буферную систему для задания водородного показателя рН между 5,0 и 10,0 и предпочтительно между 6,0 и 8,0 и, оптимально, близко к нейтральному (7,0±0,4). Выбор такого рН обусловлен стремлением учесть естественные условия клетки. Более того, такой рН обеспечивает лучшее растворение составляющих, используемых по настоящему изобретению. Такой буфер образован парой солей (неорганических или органических), приведенных к такому рН соляной кислотой или содой (4-6N), выбранную из ряда, содержащего:
дигидрофосфат/гидрофостфат натрия или калия Н2РО4/НРО4 2;
гидрокарбонат/карбонат натрия NaHCO3/Na2CO3;
буфер из лимонной кислоты/цитрата натрия (III);
TRIS-HCl;
триэтаноламинат (TEA);
имидазол;
- кислоту, выбранную из ряда, содержащего:
органические кислоты: фталевую, сульфосалициловую или муравьиную, которые также участвуют в формировании и стабилизации хромогенного комплекса гемоглобина; и
минеральные кислоты: HCl, H3PO4 и т.д.;
- фоновую соль, обеспечивающую проводимость порядка 10-50 мс/см, необходимую для измерения резистивности, и осмотическую концентрацию раствора порядка 120-500 мОсм, и, предпочтительно, близкую к изотоничности (290±5 мОсм), выбранную из ряда, содержащего:
хлорид натрия (NaCl);
хлорид калия (KCl);
хлорид магния (MgCl2);
хлорид кальция (CaCl2);
безводный сульфат натрия (Na2SO4);
при этом эта фоновая соль может быть включена в буферную систему;
- по меньшей мере один консервант, обладающий свойствами ингибитора окисления и/или антибиотика, выбранный из ряда, содержащего:
2-феноксиэтанол;
парабены;
BHT;
изотиазолоны (Proclin® 150 или 300);
имидазол или производные мочевины;
антибиотики;
- натуральный антибиотик, проникающий в клетки (ионофор), который также облегчает проникновение пигмента или пигментов, выбранный из ряда, содержащего:
ионофор I для NH4 + (нонатин);
ионофор III для Са2+ (кальцимицин);
ионофор для Cl-;
ионофор I для К+ (валиномицин).
Составляющие по настоящему изобретению, а также диапазоны их концентрации сведены в нижеприведенную таблицу.
| Составляющее | Количество |
| Катионное ПАВ | 0,1-50 г/л |
| Лейкопротекторное ПАВ | 0,1-20 г/л |
| Хелат гемоглобинового комплекса | 0,0001-10 г/л |
| Пигмент | 0,01-1 г/л |
| Фиксирующий агент | 0,01-2% по объему |
| Смачивающий агент | 0-50% по объему |
| Буфер | 0-6 г/л |
| Фоновая соль | -50 г/л |
| Кислота | в количестве, необходимом для регулирования рН |
| Консервант | соответствующее количество 0,1-3 г/л |
| Ионофор | Эффективное количество 0-200 мг/л |
| Дистиллированная вода | до 1 л |
Согласно настоящему изобретению также предлагается устройство для реализации способа по настоящему изобретению, отличающееся тем, что:
- содержит аналитический сосуд, выполненный с возможностью принимать указанный аналитический раствор;
- содержит средство для измерения уровня гемоглобина, присутствующего в указанном аналитическом растворе методом спектрофотометрии в указанном сосуде;
- содержит средства для отбора проб указанного аналитического раствора;
- содержит средство для оптического измерения пробы для проведения анализа лейкоцитов.
Согласно второму объекту настоящее изобретение относится к оптическому устройству для автоматического устройства для проведения автоматического анализа образца крови, которое особенно полезно для реализации способа по первому объекту настоящего изобретения.
Как указано выше, определенные субпопуляции лейкоцитов можно дифференцировать только оптическими измерениями, например, измерением дифракции, создаваемой клеткой под одним углом или более, или измерением поглощающей способности клетки. Оптические системы для определения параметров клетки крови имеют общее основание, на котором расположен источник света, излучающий световой луч, оптический сосуд, в котором клетки крови пересекают световой луч, система для регулировки светового луча в соответствии с потоком клеток, и средство для измерения света, исходящего из оптического сосуда после того, как он будет перекрыт клетками. В частности, для определения параметров лейкоцитов лейкоциты движутся в потоке в этом сосуде. Они освещаются световым лучом, сфокусированным на потоке, который обозначен как "поток пробы".
Такие устройства дороги: в частности лазеры, которые используются в качестве источника света и которые громоздки и обычно требуют системы отвода теплоты; лазерные диоды, как и лазеры, требуют дорогих систем юстировки. Световые лучи, излучаемые такими источниками света, имеют приблизительно гауссово поперечное распределение света. Поэтому, интенсивность является постоянной лишь приблизительно и максимальна в узкой и центральной части луча. Юстировочные системы позволяют выравнивать центральную часть [луча] с потоком пробы. Более того, ширина потока пробы не должна превышать ширину этой центральной части [луча] и чем меньше разница между этими двумя ширинами, тем выше должна быть точность юстировочной системы. В результате, необходимо как можно больше уменьшить ширину потока пробы.
Поток пробы, содержащий подсчитываемые и/или дифференцируемые клетки крови, должен быть тем уже, чем больше сфокусирован свет. Поэтому используется поток с шириной в сечении менее 50 мкм, который должен пересекать сфокусированный узкий световой луч, сечение которого превышает сечение потока пробы. Это требует особо точной и поэтому дорогой системы для инжектирования потока в оптический сосуд. Согласно предшествующему уровню техники такой результат достигается путем использования системы гидрофокусного типа (сокращение от английского выражения "гидродинамическое фокусирование"). Поток пробы окружен потоком-оболочкой. Инжектор потока пробы погружен в центр потока оболочки. Созданный таким образом поток пробы при движении от инжектора к зоне, освещенной световым лучом, расширяется или фокусируется так, чтобы в этой точке он имел требуемый диаметр, приблизительно от 5 до 50 мкм. Для достижения этой цели требуется одинарный, а иногда двойной поток-оболочка.
Кроме того, как указано выше, учитывая требуемый уровень точности, для того, чтобы поток клеток совпадал со световым лучом, существенную роль играет юстировочная система. В этом случае можно использовать два подхода: можно перемещать поток клеток или световой луч. Если перемещается поток клеток крови, нужно перемещать весь узел оптического сосуда. В этом случае сосуд устанавливается на подвижном столике, который обеспечивает точное и равномерное перемещение по двум осям, поскольку установлен на шариковых подшипниках. Такой прецизионный механический узел весьма дорог. Можно также перемещать световой луч, чтобы он совпадал с потоком клеток крови. Обычно это достигается с помощью нескольких регулируемых призм. Это решение, в котором соединены оптические элементы и прецизионная механика, также требует больших затрат.
Кроме того, что касается светового луча, клетки крови могут отклонять траекторию световых лучей. Интенсивность и угол отклоненных световых лучей дают информацию о типе клеток. Обычно используют два диапазона углов: узкие углы менее 10 градусов относительно оптической оси и широкие углы, приблизительно перпендикулярные оптической оси. В диапазоне узких углов полезны два вида информации: потери по оси и дифракция. Перпендикулярно оптической оси обычно измеряют диффузию и флуоресценцию. Следовательно, для этих двух диапазонов углов свет нужно распределить по двум разным каналам. Это обычно делается с помощью дихроичных зеркал или интерференционными фильтрами. Оптические компоненты обоих этих типов изготавливаются путем нанесения тонких пленок на стеклянную подложку. Они имеют высокую эффективность, но между разными экземплярами фильтра имеется значительное рассогласование и срок их службы невелик. Поэтому их приходится регулярно заменять.
Все эти обычно громоздкие устройства также достаточно непрочны и требуют обслуживания, которое также обходится очень дорого. Поэтому применение таких устройств ограничено аналитическими лабораториями, достаточно большими, чтобы иметь возможность приобретать такие автоматические устройства.
Целью настоящего изобретения является создание устройства для дифференциации лейкоцитов и/или подсчета лейкоцитов, более простого и более экономичного как в производстве, так и в обслуживании, позволяющего использовать автоматические устройства, которые оснащены таким устройством, небольшими лабораториями, сохраняя при этом адекватное качество измерений.
Согласно второму объекту настоящего изобретения, предлагается оптическое устройство для подсчета и/или дифференциации лейкоцитов в автоматическом анализаторе крови, отличающееся тем, что содержит источник света, относящийся к типу электролюминесцентного диода, для освещения пробы крови, циркулирующей в оптическом сосуде по оси впрыска, используя луч от источника света. Такой диод позволяет получить световой луч, который более однороден по ширине его сечения и, следовательно, имеет увеличенную и более однородную зону считывания.
Предпочтительно, диод излучает свет, длина волны которого составляет менее 600 нм и, еще более предпочтительно, менее 500 нм. Такая длина волны обеспечивает повышенную эффективность дифракции и, следовательно, повышенную точность измерений, в которых используется дифракция.
Кроме того, ширина луча, излучаемого оптическим устройством, т.е. исходного луча, который освещает поток пробы, предпочтительно составляет от 50 до 200 мкм рядом с осью инжектирования, что позволяет освещать более широкий поток пробы, в то же время давая адекватную точность проводимого измерения. Еще более преимущественно эта ширина составляет от 90 до 120 мкм. Такую ширину потока, в частности, позволяет использовать применение электролюминесцентных диодов.
Предпочтительно, исходный световой луч излучается приблизительно в направлении сосуда, приблизительно поперечно направлению потока пробы. Прозрачная пластина, выполненная так, чтобы исходный луч проходил сквозь нее между двумя противолежащими поверхностями, которая установлена и расположена с возможностью вращения между диодом и сосудом, может позволить перемещать световой луч в поперечном направлении, благодаря двойному преломлению луча, когда он проходит сквозь пластину. Поворот пластины позволяет менять угол падения луча на пластину и, таким образом, регулировать величину поперечного сдвига. Предпочтительно, прозрачная пластина установлена с возможностью поворота вокруг оси, проходящей приблизительно параллельно движению образца крови в сосуде.
За оптическим сосудом преимущественно используется средство для разделения по потерям на отражение результирующего светового луча исходящего от источника света, которое разделяет этот луч на осевой луч и по меньшей мере один луч, полученный в результате потерь на отражение во время прохождения через разделяющее средство. Разделяющее средство содержит по меньшей мере одну разделяющую поверхность, которая является поверхностью в прозрачном разделяющем материале, при этом осевой луч проходит сквозь прозрачный материал, а луч, полученный в результате потерь на отражение, отражается разделяющей поверхностью, которая наклонена относительно светового луча за сосудом. Разделяющим средством может быть единственная недорогая стеклянный пластина. Кроме того, она имеет по существу неограниченный и не требующий обслуживания срок службы, в отличие от дихроичных зеркал или интерференционных фильтров.
Устройство также может содержать устройство для измерения света осевого луча и по меньшей мере одно другое устройство для измерения света по меньшей мере одного луча, полученного в результате потерь на отражение. Эти измерительные устройства могут содержать в частности средства для измерения флуоресценции, либо световых потерь рядом с осью, либо дифракции рядом с осью. Оно также может содержать средство для измерения дифракции светового луча на широких углах под воздействием пробы в сосуде. Например, эти широкие углы могут быть углами в диапазоне от 60° до 150°.
Устройство также может содержать на пути луча, перед сосудом, по меньшей мере одну диафрагму, блокирующую паразитный свет.
Настоящее изобретение также относится к гематологическому устройству, в частности к автоматическому анализатору крови, оснащенному таким устройством.
Согласно третьему объекту, настоящее изобретение также относится к проточному оптическому сосуду для оптического устройства, предназначенного для подсчета и дифференциации лейкоцитов, например, проточного цитометра, а также к аналитическому устройству, оснащенному таким сосудом. Целью настоящего изобретения является создание более простого и более экономичного в производстве и обслуживании сосуда, позволяющего использовать автоматические устройства, оснащенные таким сосудом, в небольших лабораториях, сохраняя адекватное качество измерений.
Согласно настоящему изобретению, проточный сосуд для оптического устройства для подсчета и дифференциации лейкоцитов в автоматическом анализаторе крови отличается тем, что в аналитической зоне сосуда сечение сосуда имеет по меньшей мере один поперечный размер, составляющий от 1 до 5 мм. Это сечение может быть приблизительно прямоугольным, и поперечное направление может измеряться по одной и/или по другой стороне прямоугольника.
Таким образом, такой сосуд может производиться, по меньшей мере частично из пластмассы, методом литья под давлением. Такой способ изготовления сосуда является особенно преимущественным по сравнению с известными сосудами, которые обычно изготавливают из кварцевых стенок, соединенных склеиванием.
Сосуд также может содержать по меньшей мере одну линзу, отлитую заодно с сосудом. Эта по меньшей мере одна линза может содержать линзу, выполненную с возможностью расположения сбоку относительно оптической оси. Она может содержать полусферическую линзу.
Сосуд может содержать расположенное вдоль его оптической оси окно для подачи светового луча и окно для выхода светового луча. По меньшей мере одно окно может быть отлито заодно с сосудом и/или быть выполнено в виде вставки в прозрачный материал, например, из кварца или стекла.
Сосуд может преимущественно содержать инжектор для потока пробы и средство для формирования потока-оболочки вокруг впрыснутого потока. Инжектор может содержать выходное отверстие, диаметр которого составляет от 20 до 150 мкм, позволяющее получить поток пробы, который заметно больше, чем потоки по предшествующему уровню техники. В отличие от устройств по предшествующему уровню техники ширина потока пробы определяется не потоком-оболочкой, который растягивает его, а формой и сечением выходного отверстия инжектора. Поток-оболочка, таким образом, играет не активную, а просто пассивную роль, в частности, например, центрируя поток пробы в широком сосуде.
Согласно первому варианту, этот инжектор может быть сформирован как одна деталь из более или менее жесткого материала. Этим материалом может быть, например, нержавеющая сталь, керамика, синтетический рубин, или пластмасса или несколько из этих материалов.
Согласно второму варианту осуществления изобретения, такой инжектор может содержать жесткую структурную трубку, например выполненную из металла, например, из нержавеющей стали, и расположенную внутри металлической трубки пластмассовую вставную трубку, заканчивающуюся соплом, сформированным заодно с вставной трубкой. Пластмассой инжектора может быть политетрафторэтилен, который позволяет пробе легче циркулировать по трубке и уменьшает риск загрязнения.
Настоящее изобретение также относится к инжектору для сосуда по настоящему изобретению, выполненному по одному из этих вариантов.
Настоящее изобретение также относится к гематологическому устройству, в частности к автоматическому анализатору крови, оснащенному сосудом по настоящему изобретению.
Согласно четвертому объекту, настоящее изобретение также относится к гидравлическому устройству для гематологического аналитического устройства, которое проще и экономичнее и в производстве и в обслуживании и которое позволяет использовать автоматическое устройство, оснащенное таким устройством, в небольших лабораториях, сохраняя адекватное качество измерений. Настоящее изобретение также относится к способу анализа, пригодному для такого устройства.
Согласно настоящему изобретению предлагается гидравлическое устройство для устройства для анализа крови, в частности автоматического устройства, содержащего средство для инжектирования под давлением потока пробы в проточный оптический сосуд и для создания потока-оболочки обволакивающей жидкости вокруг потока пробы, отличающееся тем, что содержит средство для регулировки расхода потока пробы относительно расхода потока обволакивающей жидкости. Такая регулировка может позволить поддерживать гомогенные и приблизительно нетурбулентные потоки в сосуде.
Средство инжектирования может содержать шприцы, гидравлический контур и электромагнитные клапаны. Эти средства могут содержать средства для инжектирования пробы под давлением относительно потока-оболочки.
Такое устройство может преимущественно содержать средство для формирования поршня из вытесняющей жидкости для впрыскиваемой пробы. Такая вытесняющая жидкость позволяет использовать лишь небольшие пробы, достаточные для анализа, а остальная жидкость, необходимая для впрыска, является жидкостью, имеющейся в аналитическом устройстве и не являющейся имеющей большую ценность пробой.
Поток-оболочка особенно полезен при использовании сосуда с широким сечением, позволяя поддерживать малое сечение потока пробы. Как одно из средств регулирования потока пробы относительно потока-оболочки, устройство может преимущественно содержать средство для регулирования расхода вытесняющей жидкости относительно расхода обволакивающей жидкости. Регулировочное средство может содержать средство для создания падения давления в шунтирующей цепи для вытесняющей жидкости и/или средство для создания падения давления в шунтирующей цепи для обволакивающей жидкости. Например, средство для создания падения давления может быть выбрано из известного ряда, содержащего калиброванную трубку, фиксированное гидравлическое сопротивление и переменное гидравлическое сопротивление.
Гидравлическое устройство может содержать только один привод, например, единственный электродвигатель, для одновременного генерирования потока пробы и потока-оболочки. Кроме того, оно может содержать по меньшей мере два шприца для генерирования потока пробы и потока-оболочки, при этом поршни шприцов прочно прикреплены друг к другу. Таким образом, они совершают общее перемещение и поток пробы, и поток-оболочка генерируются действительно одновременно.
В частности, в описанной выше цепи по настоящему изобретению можно использовать гидрофокусный сосуд по предшествующему уровню техники и впрыск пробы в такой сосуд может осуществляться без давления, относительно потока-оболочки.
Согласно настоящему изобретению также предлагается способ анализа пробы крови и проточном цитометре, отличающийся тем, что инжектируют пробу крови, опционально под давлением, в проточный сосуд цитометра, при этом проба образует в нем поток пробы, и вокруг потока пробы создают поток-оболочку обволакивающей жидкости, отличающийся тем, что расход потока пробы регулируют относительно расхода потока обволакивающей жидкости.
В частности, можно вводить пробу в инжекторную ветвь гидравлического контура и выше по потоку от пробы можно вводить в инжекторную ветвь вытесняющую жидкость, при этом вытесняющая жидкость служит для выталкивания пробы при ее впрыске в сосуд. Такая вытесняющая жидкость может быть выбрана из ряда, содержащего реагент и разбавитель, предпочтительно реагент. Таким образом, нет необходимости использовать жидкости, кроме строго необходимых для приготовления пробы для анализа или анализов.
Если используется метод гидрофокусировки или сосуд по третьему объекту настоящего изобретения, преимущества дает регулировка расхода вытесняющей жидкости относительно расхода обволакивающей