Полипептид, способный преодолевать гематоэнцефалический барьер, и его конъюгат
Иллюстрации
Показать всеИзобретение относится к области генной инженерии, конкретно к носителям для доставки лекарственного средства, и может быть использовано в медицине. Получают аналог апротинина с последовательностью TFFYGGSRGKRNNFKTEEY, а также конъюгат на его основе. Изобретение позволяет осуществлять доставку соединения или лекарственного средства через гематоэнцефалический барьер млекопитающего. 3 н. и 3 з.п. ф-лы, 9 ил., 6 табл.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к усовершенствованиям в области доставки лекарственного средства. Более конкретно, это изобретение относится к полипептидам, конъюгатам и фармацевтическим композициям, содержащим полипептиды или конъюгаты согласно изобретению. Настоящее изобретение также относится к применению этих полипептидов и конъюгатов для транспорта соединения или лекарственного средства через гематоэнцефалический барьер млекопитающего и для лечения и диагностики неврологических заболеваний.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
При разработке нового лекарственного средства от патологий головного мозга гематоэнцефалический барьер (ГЭБ) считается основным препятствием для потенциального применения лекарственных средств для лечения нарушений центральной нервной системы (ЦНС). Всемирный рынок лекарственных средств для ЦНС в 1998 году составлял $33 миллиардов, что составляло приблизительно половину глобального рынка лекарственных средств для сердечно-сосудистой системы, несмотря на то, что в США нарушениями ЦНС страдает вдвое больше людей, чем сердечно-сосудистыми заболеваниями. Причина этого несоответствия состоит в том, что более 98% всех потенциальных лекарственных средств для ЦНС не преодолевают гематоэнцефалический барьер. Кроме того, более 99% всемирной разработки лекарственных средств для ЦНС посвящено исключительно изобретению лекарственных средств для ЦНС и менее 1% направлено на доставку лекарственного средства в ЦНС. Это соотношение может объяснить причину отсутствия доступного в настоящее время эффективного лечения основных неврологических заболеваний, таких как опухоли мозга, болезнь Альцгеймера и инсульт.
Головной мозг защищен от потенциально токсических веществ наличием двух барьерных систем: гематоэнцефалического барьера (ГЭБ) и гематоликворного барьера (BCSFB). Полагают, что ГЭБ является основным путем для захвата сывороточных лигандов, поскольку площадь его поверхности приблизительно в 5000 раз выше, чем площадь поверхности BCSFB. Эндотелий головного мозга, который образует ГЭБ, представляет собой основное препятствие для применения потенциальных лекарственных средств против многих нарушений ЦНС. В качестве общего правила, через ГЭБ, т.е. из крови в головной мозг, могут проходить только липофильные молекулы приблизительно менее 500 Дальтон. Однако размер многих лекарственных средств, для которых показаны перспективные результаты в исследованиях в отношении лечения нарушений ЦНС на животных, является значительно более высоким. Таким образом, транспорт пептидных и белковых лекарственных средств из крови в головной мозг главным образом исключен вследствие очень низкой проницаемости клеточной стенки капилляров головного мозга для этих лекарственных средств. Эндотелиальные клетки капилляров головного мозга (BCEC) плотно скреплены посредством плотных межклеточных контактов, они обладают малым количеством отверстий и малым количеством эндоцитозных везикул по сравнению с капиллярами других органов. BCEC окружены внеклеточным матриксом, астроцитами, перицитами и клетками микроглии. Тесная связь эндотелиальных клеток с опорными отростками астроцита и базальной мембраной капилляров важна для развития и поддержания свойств ГЭБ, которые обеспечивают строгий контроль обмена кровь-головной мозг.
В международной публикации WO 2004/060403 описано изобретение авторов изобретения, касающееся молекул для транспорта лекарственного средства через гематоэнцефалический барьер. К настоящему времени не существует иного подхода для доставки лекарственного средства, пригодной для головного мозга. Исследуемые способы доставки пептидного и белкового лекарственного средства в головной мозг можно подразделить на три принципиальных стратегии. Во-первых, инвазивные способы включают в себя прямое внутрижелудочковое введение лекарственных средств посредством хирургической операции и временное повреждение ГЭБ посредством инфузии в сонную артерию гиперосмолярных растворов. Во-вторых, основанная на фармакологии стратегия состоит в упрощении прохождения через ГЭБ посредством повышения растворимости пептидов или белков в липидах. В-третьих, в основанных на физиологии стратегиях используют различные транспортные механизмы в ГЭБ, которые были описаны в последние годы. В этом подходе лекарственные средства присоединяют к белковому вектору, которые функционируют подобно направленному на рецепторы носителю для доставки в ГЭБ. Этот подход является высоко специфичным, и он обеспечивает высокую эффективность и высокую универсальность для клинических целей с неограниченными мишенями. Последний подход изучали и в настоящий момент времени изучают авторы изобретения, которые начинали работу с молекул, описанных в приведенной выше публикации, и молекул согласно изобретению.
В патенте США No. 5807980 описаны ингибиторы на основе ингибитора трипсина бычьей поджелудочной железы (апротинина), а также способ их получения и терапевтического применения. Эти пептиды используют для лечения состояния, характеризующегося аномальной структурой или количеством тканевого фактора и/или фактора VIIIa, такого как аномальный тромбоз.
В патенте США No. 5780265 описаны ингибиторы сериновых протеаз, которые способны ингибировать калликреин плазмы.
В патенте США No.5118668 описаны варианты ингибитора трипсина бычьей поджелудочной железы.
Предоставление усовершенствованных молекул, которые могут выступать в качестве носителей или векторов для транспорта соединения или лекарственного средства через ГЭБ индивидуума, является крайне желательным.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Одной целью настоящего изобретения является осуществление усовершенствования в области доставки лекарственного средства.
Другой целью настоящего изобретения является предоставление неинвазивного и универсального способа и носителя для транспорта соединения или лекарственного средства через гематоэнцефалический барьер индивидуума.
В настоящей заявке описаны новые молекулы, которые могут быть способными, например, транспортировать требуемые соединения через гематоэнцефалический барьер.
В первом аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающего в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- апротинина (SEQ ID NO:98),
- аналога апротинина,
- фрагмента апротинина, который может содержать (или может по существу состоять из) аминокислотную последовательность, определяемую SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1,
- биологически активного фрагмента SEQ ID NO:1 и
- биологически активного фрагмента аналога SEQ ID NO:1.
Во втором аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающих в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- фрагмента апротинина, который может содержать аминокислотную последовательность, определяемую SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1,
- биологически активного фрагмента SEQ ID NO:1 и
- биологически активного фрагмента аналога SEQ ID NO:1.
В соответствии с настоящим изобретением фрагмент апротинина может состоять из последовательности, определяемой SEQ ID NO:1. Кроме того, в соответствии с настоящим изобретением фрагмент апротинина может содержать SEQ ID NO:1 и может иметь длину приблизительно от 19 аминокислот до приблизительно 54 аминокислот, например, длину от 10 до 50 аминокислот, длину от 10 до 30 аминокислот и т.д.
В соответствии с настоящим изобретением биологически активный аналог SEQ ID NO:1 может имеет длину приблизительно от 19 аминокислот до приблизительно 54 аминокислот (например, включая, например, от 21 до 23, от 25 до 34, от 36 до 50 и от 52 до 54), или приблизительно от 19 аминокислот до приблизительно 50 аминокислот, или приблизительно от 19 аминокислот до приблизительно 34 аминокислот (например, 19, 20, 21, 22, 23, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34), приблизительно от 19 аминокислот до приблизительно 23 аминокислот или приблизительно 19, 20, 21, 22, 23, 24, 35, 51 аминокислот.
Биологически активный фрагмент полипептида (например, из 19 аминокислот), описанный в настоящем описании, может включать в себя, например, полипептид из приблизительно от 7, 8, 9 или 10 до 18 аминокислот. Таким образом, в соответствии с настоящим изобретением биологически активный фрагмент SEQ ID NO:1 или аналог SEQ ID NO:1 может иметь длину приблизительно от 7 до приблизительно 18 аминокислот или приблизительно от 10 до приблизительно 18.
В патенте США No. 5807980 описан полипептид, который обозначен в настоящем описании как SEQ ID NO:102.
В патенте США No. 5780265 описан полипептид, который обозначен в настоящем описании как SEQ ID NO:103.
Аминокислотная последовательность апротинина (SEQ ID NO:98), аминокислотная последовательность Angiopep-1, а также некоторые последовательности биологически активных аналогов можно найти, например, в международной заявке No. PCT/CA 2004/000011, опубликованной 22 июля 2004 года как международная заявка No. WO 2004/060403. Кроме того, в международной заявке No. WO04/060403 описан полипептид, который обозначен в настоящем описании как SEQ ID NO:104.
В патенте США No.5118668 описаны полипептиды, которые имеют последовательность, представленную в SEQ ID NO:105.
Примеры аналогов апротинина можно найти посредством выполнения protein blast (Genebank: www.ncbi.nlm.nih.gov/BLAST/) для синтетической последовательности апротинина (или ее части), описанной в международной заявке No. PCT/CA 2004/000011. Иллюстративные аналоги апротинина можно найти, например, под регистрационными No. CAA37967 (GI:58005), 1405218C (GI:3604747) и т.д.
В следующем аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающих в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 19 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 длиной приблизительно от 19 до 50 аминокислот и
- биологически активного фрагмента SEQ ID NO:1 (от 10 до 18 аминокислот) или биологически активного фрагмента аналога SEQ ID NO:1 (приблизительно от 10 до 18 аминокислот).
В соответствии с настоящим изобретением предусмотрен биологически активный аналог SEQ ID NO:1, который может быть выбран, например, из группы, состоящей из
- аналога SEQ ID NO:1, который может иметь по меньшей мере 35% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 40% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 50% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 60% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 70% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 80% идентичность аминокислотной последовательности SEQ ID NO:1,
- аналога SEQ ID NO:1, который может иметь по меньшей мере 90% идентичность аминокислотной последовательности SEQ ID NO:1 и
- аналога SEQ ID NO:1, который может иметь по меньшей мере 95% (т.е. 96%, 97%, 98%, 99% и 100%) идентичность аминокислотной последовательности SEQ ID NO:1.
Например, биологически активный аналог SEQ ID NO:1 может содержать аминокислотную последовательность, выбранную из группы, состоящей из аминокислотной последовательности, определяемой любым из с SEQ ID NO:2 по SEQ ID NO:62, с SEQ ID NO:68 по SEQ ID NO:93, и SEQ ID NO:97, а также 99, 100 и 101. Если полипептид согласно изобретению содержит, например, SEQ ID NO:99, 100 или 101, то полипептид может иметь аминокислотную последовательность длиной из приблизительно от 10 до 50 аминокислот, например от 10 до 30 аминокислот.
Кроме того, в соответствии с настоящим изобретением биологически активный аналог SEQ ID NO:1 может содержать аминокислотную последовательность, определяемую SEQ ID NO:67 (т.е. полипептид No. 67, который представляет собой амидированный вариант SEQ ID NO:67 (Angiopep-1)).
Полипептиды согласно изобретению могут быть амидированными, т.е. они могут иметь амидированную аминокислотную последовательность. Например, может быть амидированным полипептидом SEQ ID NO:67 (полипептид No.67).
Часть соединений согласно изобретению может относиться к полипептидам, определенным в настоящем описании, за исключением полипептидов, определяемых SEQ ID NO:102, 103, 104 и 105, в то время как другая часть соединений согласно изобретению может включать в себя эти пептиды. В качестве неограничивающего примера, настоящее изобретение относится к конъюгатам, содержащим эти пептиды, а также их применению для лечения неврологического заболевания (например, опухоли мозга), способу лечения неврологического заболевания (например, опухоли мозга), фармацевтической композиции для лечения неврологического заболевания и т.д.
В следующем аспекте настоящее изобретение относится к биологически активному полипептиду, который способен преодолевать клеточный слой, имитирующий гематоэнцефалический барьер млекопитающих в анализе in vitro, где полипептид может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 19 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 длиной приблизительно от 19 до 50 аминокислот, при условии, что указанный аналог не является последовательностью SEQ ID NO:102, 103, 104 или 105, и при условии, что если указанный аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным,
- биологически активного фрагмента SEQ ID NO:1 из 10-18 аминокислот и
- биологически активного фрагмента аналога SEQ ID NO:1 приблизительно из 10-18 аминокислот.
Кроме того, в соответствии с настоящим изобретением биологически активный фрагмент SEQ ID NO:1 или биологически активный фрагмент аналога SEQ ID NO:1 может содержать по меньшей мере 9 или по меньшей мере 10 (последовательных или смежных) аминокислот последовательности SEQ ID NO:1 или аналога SEQ ID NO:1.
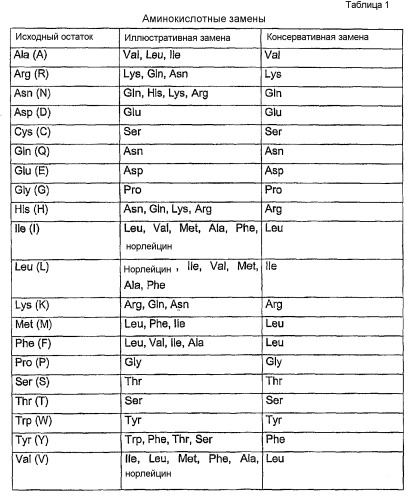
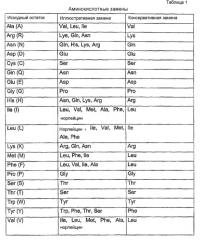
Полипептиды согласно изобретению могут иметь аминокислотную последовательность, которая может содержать от 1 до 12 аминокислотных замен (т.е. SEQ ID NO:91). Например, количество аминокислотных замен может составлять от 1 до 10 аминокислотных замен или от 1 до 5 аминокислотных замен. В соответствии с настоящим изобретением аминокислотная замена может представлять собой неконсервативную аминокислотную замену или консервативную аминокислотную замену.
Например, если полипептид согласно изобретению содержит аминокислоты, которые идентичны аминокислотам SEQ ID NO:1, и другие аминокислоты, которые не являются идентичными (не идентичны), те аминокислоты, которые являются неидентичными могут представлять собой консервативную аминокислотную замену. Сравнение идентичных и неидентичных аминокислот можно проводить посредством проверки соответствующего положения.
Примеры аналога SEQ ID NO:1, который может иметь по меньшей мере 35% идентичность, включают в себя, например, полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:91 (приблизительно 36,8% идентичность, т.е. 7 аминокислот из 19 аминокислот SEQ ID NO:91 являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:98 (приблизительно 68,4% идентичность, т.е. 13 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:67 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:76 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), и полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:5 (приблизительно 79% идентичность, т.е. 15 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1).
Примеры аналога SEQ ID NO:1, который может иметь по меньшей мере 60% идентичность, включают в себя, например, полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:98 (приблизительно 68,4% идентичность, т.е. 13 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:67 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:76 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1) и полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:5 (приблизительно 79% идентичность, т.е. 15 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1).
Примеры аналога SEQ ID NO:1, который может иметь по меньшей мере 70% идентичность, включают в себя, например, полипептид, содержащий (состоящий из) аминокислотную последовательность, определяемую SEQ ID NO:67 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), SEQ ID NO:76 (приблизительно 73,7% идентичность, т.е. 14 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1), SEQ ID NO:5 (приблизительно 79% идентичность, т.е. 15 аминокислот из 19 аминокислот являются идентичными SEQ ID NO:1).
В соответствии с настоящим изобретением носитель, более конкретно, может быть выбран из группы, состоящей из пептидов No. 5, 67, 76, 91 и пептида 97 (т.е. SEQ ID NO:5, 67, 76, 91 и 97 (Angiopep-2)). Носитель можно использовать, например, для транспорта присоединенного к нему вещества через гематоэнцефалический барьер. В соответствии с настоящим изобретением носитель может быть способным преодолевать гематоэнцефалический барьер после присоединения вещества и, таким образом, может быть способным транспортировать вещество через гематоэнцефалический барьер.
В соответствии с настоящим изобретением полипептиды могут находиться в выделенной форме или по существу в очищенной форме.
Более конкретно, настоящее изобретение относится к носителю для транспорта присоединенного к нему вещества через гематоэнцефалический барьер, где носитель может быть способным преодолевать гематоэнцефалический барьер после присоединения к веществу и, таким образом, транспортировать вещество через гематоэнцефалический барьер. Носитель может содержать по меньшей мере один полипептид согласно изобретению (при условии, что если указанный полипептид или носитель состоит из SEQ ID NO:67, то указанный полипептид является модифицированным по группе, например амидированным). Например, носитель может быть выбран из класса молекул, относящегося к апротинину.
Активность транспорта, который осуществляют посредством носителя, не влияет на целостность гематоэнцефалического барьера. Транспорт вещества может приводить, например, к доставке вещества в центральную нервную систему (ЦНС) индивидуума.
В рамках настоящего описания следует понимать, что полипептиды согласно изобретению можно синтезировать химически (например, твердофазным синтезом) или их можно получать посредством технологии рекомбинантных ДНК. Кодоны, которые кодируют конкретные аминокислоты, хорошо известны в данной области и описаны, например, в Biochemistry (третье издание; 1988, Lubert Stryer, Stanford University, W. H. Freeman and Company, New-York). Таким образом, в рамках настоящего описания предусмотрена нуклеотидная последовательность, кодирующая носитель согласно изобретению. Более конкретно, настоящее изобретение относится к нуклеотидным последовательностям (дезоксирибонуклеотиды или рибонуклеотиды или их производные), кодирующим полипептид, выбранный из группы, состоящей из любого из с SEQ ID NO:1 по 97. Иллюстративная нуклеотидная последовательность, кодирующая аналог апротинина, представлена в SEQ ID NO:106, и ее можно найти в Gene Bank под регистрационным номером No.X04666. Эта последовательность кодирует аналог апротинина, имеющий лизин в положении 16 (по отношению к аминокислотной последовательности, кодируемой SEQ ID NO:106) вместо валина, который находится в SEQ ID NO:98. В нуклеотидную последовательность SEQ ID NO:106 можно вносить мутацию способами, известными в данной области, для замены продукции на пептид SEQ ID NO:98, имеющий валин в положении 16. Способы, известные в данной области, можно использовать для внесения дополнительных мутаций в нуклеотидную последовательность, чтобы она кодировала аналоги согласно изобретению. Фрагменты можно получать из этой нуклеотидной последовательности посредством ферментативного расщепления или полимеразной цепной реакции, и т.д. Альтернативно требуемую нуклеотидную последовательность можно синтезировать химически известными в данной области способами.
В следующем аспекте настоящее изобретение относится к конъюгату, который может содержать носитель, выбранный из группы, состоящей из любого полипептида согласно изобретению, и вещества, выбранного из группы, состоящей, например, из лекарственного средства (например, низкомолекулярного лекарственного средства, например, антибиотика), медикамента, поддающейся детекции метки, белка (например, фермента), соединения на основе белка (например, белкового комплекса, содержащего одну или несколько полипептидных цепей) и полипептида (пептида). Более конкретно, вещество может представлять собой молекулу, которая является активной на уровне центральной нервной системы. Вещество может представлять собой любое вещество для лечения или выявления неврологического заболевания.
В соответствии с настоящим изобретением носитель, который представляет собой часть конъюгата, может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 10 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 (например, длиной приблизительно от 19 до 50 аминокислот), при условии, что если указанный аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным,
- биологически активного фрагмента SEQ ID NO:1 из 10-18 аминокислот и
- биологически активного фрагмента аналога SEQ ID NO:1 приблизительно из 10-18 аминокислот.
В соответствии с настоящим изобретением вещество может иметь максимальную молекулярную массу приблизительно 160000 Дальтон.
Кроме того, в соответствии с настоящим изобретением транспортной активности можно достигать посредством рецептор-опосредованного трансцитоза или адсорбционно-опосредуемого трансцитоза. Вещество может представлять собой вещество, которое может транспортироваться таким механизмом.
Кроме того, в соответствии с настоящим изобретением конъюгат может находиться в форме слитого белка, который может обладать первой группой, по существу состоящей из носителя согласно изобретению, и второй группой, по существу состоящей из белка или вещества на основе белка.
Иллюстративные неврологические заболевания, которые можно лечить или выявлять с помощью носителя и/или конъюгата, представляют собой заболевания, выбранные, например, из группы, состоящей из опухоли мозга, метастаза в головной мозг, шизофрении, эпилепсии, болезни Альцгеймера, болезни Паркинсона, болезни Гентингтона, инсульта и нарушений функции, связанных с гематоэнцефалическим барьером (например, ожирения).
В соответствии с настоящим изобретением нарушение функции, связанное с гематоэнцефалическим барьером, представляет собой ожирение. Также в соответствии с настоящим изобретением вещество, которое может быть конъюгированным с носителем согласно изобретению, может представлять собой лептин. Конъюгат, содержащий лептин и носитель, можно использовать, например, при лечении ожирения.
В соответствии с настоящим изобретением поддающаяся детекции метка может представлять собой радиовизуализирующее средство. Пример метки, которая может быть конъюгирована с носителем согласно изобретению и которая охватывается настоящим описанием, включает в себя в качестве неограничивающего примера изотоп, флуоресцентную метку (например, родамин), репортерную молекулу (например, биотин) и т.д. Другие примеры поддающихся детекции меток включают в себя, например, зеленый флуоресцирующий белок, биотин, белок histag и β-галактозидазу.
Пример белка или соединения на основе белка, которое можно конъюгировать с носителем согласно изобретению и которое охватывается настоящим описанием, включает в себя в качестве неограничивающего примера антитело, фрагмент антитела (например, связывающий фрагмент антитела, такой как Fv-фрагмент, F(ab)2, F(ab)2' и Fab и т.п.), лекарственное средство на основе пептида или белка (например, положительный фармакологический модулятор (агонист) или фармакологический ингибитор (антагонист)) и т.д. Другие примеры вещества, которое охватывается настоящим описанием, включают в себя клеточные токсины (например, монометилауристатин E (MMAE), токсины из бактериальных эндотоксинов и экзотоксинов; дифтерийные токсины, ботулинические токсины, столбнячные токсины, коклюшные токсины, стафилококковые энтеротоксины, токсин TSST-1 синдрома токсического шока, аденилатциклазный токсин, токсин Шига, холерный энтеротоксин и другие) и антиангиогенные соединения (эндостатин, катехины, нутрицевтики, хемокин IP-10, ингибиторы матриксных металлопротеиназ (MMPI), анастеллин, витронектин, антитромбин, ингибиторы тирозинкиназы, ингибиторы VEGF, антитела против рецептора, герцептин, авастин и панитумумаб и другие).
Также в соответствии с настоящим изобретением вещество может представлять собой низкомолекулярное лекарственное средство, такое как противоопухолевое лекарственное средство (например, для лечения опухоли мозга). Противоопухолевое лекарственное средство, охватываемое настоящим изобретением, может включать в себя, например, лекарственное средство, имеющее группу, обеспечивающую его конъюгацию с носителем согласно изобретению. Примеры противоопухолевого лекарственного средства включают в себя в качестве неограничивающего примера лекарственное средство, которое может быть выбрано из группы, состоящей из паклитаксела (таксол), винбластина, винкристина, этопозида, доксорубицина, циклофосфамида, таксотера, мелфалана, хлорамбуцила и любого сочетания.
Более конкретно, конъюгат согласно изобретению может иметь формулу R-L-M или формулу ее фармацевтически приемлемой соли, где R представляет собой молекулы класса, относящегося к апротинину (например, апротинин, фрагмент апротинина, Angiopep-1, Angiopep-2, аналоги, производные или фрагменты). Например, R может представлять собой носитель, выбранный из молекул класса, относящегося к апротинину, способный преодолевать гематоэнцефалический барьер после присоединения к L-M и, таким образом, транспортировать M через гематоэнцефалический барьер. L может представлять собой линкер или связь (химическую связь). M может представлять собой любое вещество, выбранное из группы, состоящей из лекарственного средства (например, низкомолекулярного лекарственного средства), медикамента, (поддающейся детекции) метки, белка или соединения на основе белка (например, антитела, фрагмента антитела), антибиотика, противоопухолевого средства, антиагиогенного соединения и полипептида или любой молекулы, активной на уровне центральной нервной системы. Следует понимать, что в рамках настоящего описания формула R-L-M не предназначена для того, чтобы ограничиваться конкретным порядком или конкретным соотношением. Как представлено в настоящем описании, M может в несколько раз превышать R.
Например, конъюгаты формулы R-L-M или их фармацевтически приемлемые соли можно использовать для транспорта M через гематоэнцефалический барьер, где R может представлять собой, например, носитель, выбранный из группы, состоящей из пептидов No: 5, 67, 76, 91 и 97, как описано в настоящем описании. Носитель может быть способен преодолевать гематоэнцефалический барьер после присоединения к L-M
и, таким образом, может транспортировать M через гематоэнцефалический барьер.
В соответствии с настоящим изобретением M может представлять собой вещество, пригодное для лечения или диагностики неврологического заболевания.
В рамках настоящего описания следует понимать, что если является доступной или существует более одной области для конъюгации носителя, то с носителем согласно изобретению можно конъюгировать более одного лекарственного средства или молекулы лекарственного средства. Таким образом, конъюгат может содержать одну или несколько молекул лекарственного средства. Может быть активным сам конъюгат, т.е. лекарственное средство может быть активным, даже если оно связано с носителем. Также в соответствии с настоящим изобретением соединение может освобождаться (или может не освобождаться) от носителя, т.е., главным образом, после транспорта через гематоэнцефалический барьер. Таким образом, соединение может высвобождаться из конъюгата (или от носителя) и после этого может становиться активным. Более конкретно, вещество может обладать способностью к освобождению от носителя после транспорта через гематоэнцефалический барьер.
В соответствии с другим вариантом осуществления настоящего изобретения предусмотрен конъюгат для транспорта вещества через гематоэнцефалический барьер, где конъюгат может содержать: (a) носитель и (b) вещество, присоединенное к носителю, где конъюгат способен преодолевать гематоэнцефалический барьер и, таким образом, транспортировать вещество через гематоэнцефалический барьер.
В следующем аспекте настоящее изобретение относится к применению носителя или конъюгата согласно изобретению для транспорта вещества через гематоэнцефалический барьер нуждающегося в этом млекопитающего.
В следующем аспекте настоящее изобретение относится к применению молекул класса, относящегося к апротинину, для транспорта соединения, присоединенного к ним, через гематоэнцефалический барьер пациента.
В дополнительном аспекте настоящее изобретение относится к применению носителя или конъюгата, как описано в настоящем описании для диагностики неврологического заболевания или заболевания центральной нервной системы. Например, носитель или конъюгат можно использовать для выявления неврологического заболевания in vivo.
Носитель может быть выбран, например, из группы, состоящей из (биологически активных)
- апротинина (SEQ ID NO:98),
- фрагмента апротинина, который может содержать аминокислотную последовательность, определяемую SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 и
- биологически активного фрагмента SEQ ID NO:1 или биологически активного фрагмента аналога SEQ ID NO:1.
Более конкретно, носитель может быть выбран, например, из группы, состоящей из (биологически активных)
- фрагмента апротинина, который может содержать аминокислотную последовательность, определяемую SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 и
- биологически активного фрагмента SEQ ID NO:1 или биологически активного фрагмента аналога SEQ ID NO:1.
В соответствии с настоящим изобретением, если этот аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным.
Более конкретно, носитель может быть выбран, например, из группы, состоящей из
- фрагмента апротинина длиной от 10 до 54 (например, 19-50) аминокислот, содержащего SEQ ID NO:1,
- фрагмента апротинина, состоящего из SEQ ID NO:1,
- биологически активного аналога SEQ ID NO:1 (например, длиной приблизительно от 19 до 50 аминокислот), при условии, что если указанный аналог состоит из SEQ ID NO:67, то указанный аналог является амидированным,
- биологически активного фрагмента SEQ ID NO:1 из от 10 до 18 аминокислот и
- биологически активного фрагмента аналога SEQ ID NO:1 из приблизительно от 10 до 18 аминокислот.
В другом аспекте настоящее изобретение относится к применению молекул класса, относящегося к апротинину, для изготовления лекарственного средства.
В соответствии с настоящим изобретением предусмотрено применение молекул класса, относящегося к апротинину, для изготовления лекарственного средства для лечения неврологического заболевания или для лечения нарушения центральной нервной системы.
В другом аспекте настоящее изобретение относится к применению носителя или конъюгата, описанного в настоящем описании, для изготовления лекарственного средства для лечения заболевания головного мозга (ассоциированного с головным мозгом заболевания) или неврологического заболевания, для диагностики заболевания головного мозга или неврологического заболевания или для транспорта вещества через гематоэнцефалический барьер.
В дополнительном аспекте настоящее изобретение относится к применению носителя или конъюгата согласно изобретению для лечения млекопитающего, например, с неврологическим заболеванием или для диагностики неврологического заболевания у нуждающегося в этом млекопитающего.
В соответствии с настоящим изобретением неврологическое заболевание, охватываемое настоящим изобретением, включает в себя в качестве неограничивающего примера опухоль мозга, метастаз в головной мозг, шизофрению, эпилепсию, болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона, инсульт и нарушения функции, связанные с гематоэнцефалическим барьером.
В следующем аспекте настоящее изобретение относится к способу транспорта вещества через гематоэнцефалический барьер млекопитающего (человека, животного), который может включать в себя стадию введения млекопитающему соединения, содержащего вещество, присоединенное к молекулам класса, относящегося к апротинину.
В следующем аспекте настоящее изобретение относится к способу лечения неврологического заболевания у пациента, включающему в себя введение пациенту лекарственного средства, содержащего молекулы класса, относящегося к апротинину, и соединение, адаптированное для лечения заболевания, где соединение присоединено к молекулам класса, относящегося к апротинину.
В дополнительном аспекте предусмотрен способ лечения нарушения центральной нервной системы пациента, включающий в себя введение пациенту лекарственного средства, содержащего молекулы класса, относящегося к апротинину, и соединение, адаптированное для лечения заболевания, где соединение присоединено к апротинину.
В следующем аспекте предусмотрен способ транспорта вещества через гематоэнцефалический барьер, который включает в себя стадию введения индивидууму фармацевтической композиции согласно изобретению.
В следующем аспекте настоящее изобретение также относится к способу лечения млекопитающего (например, пациента), нуждающегося в этом (например, пациента с неврологическим заболеванием). Способ может включать в себя введение млекопитающему носителя, конъюгата и/или фармацевтической композиции согласно изобретению.
Кроме того, настоящее изобретение относится к способу диагностики (т.е. к диагностическому способу) неврологического заболевания у млекопитающего (например, у пациента), нуждающегося в этом. Способ может включать в себя введение носителя, конъюгата и/или фармацевтической композиции согласно изобретению млекопитающему (человеку, пациенту, животному).
В соответствии с настоящим изобретением введение можно проводить внутриартериально, интраназально, внутрибрюшинно, внутривенно, внутримышечно, подкожно, чрескожно или перорально.
В соответствии с настоящим изобретением фармацевтическую композицию можно вводить млекопитающему в терапевтически эффективном количестве.
Нуждающееся млекопитающее (нуждающийся индивидуум) может представлять собой, например, млекопитающее, которое обладает риском неврологического заболевания, заболевания центральной нервной системы, злокачественной опухоли мозга, метастаза в головной мозг и т.д.
В дополнительном аспекте настоящее изобретение