Новые сшивающие реагенты для получения биосовместимых материалов на основе хитозана
Иллюстрации
Показать всеИзобретение относится к области биотехнологии и медицины, а именно к созданию полимерных материалов на основе хитозана, обладающих низкой токсичностью и повышенной биосовместимостью, в частности, пленок, микрокапсул, гидрогелей, раневых покрытий, скаффолдов и т.д. Изделия на основе биологически активных полимерных материалов могут быть использованы в хирургии при лечении ран и в качестве материалов для временного замещения тканей организма, в области биотехнологии для получения матриц для выращивания клеточных культур, в фармацевтике как носители ферментов и других биологически активных соединений. Сшивающие реагенты представляют собой 2,4-производные 3-оксаглутарового альдегида (2,2'-оксидиацетальдегида). Эти соединения могут быть получены периодатным окислением моносахаридов, нуклеозидов, нуклеотидов. Низкая токсичность и биосовместимость материалов на основе хитозана достигается использованием сшивающих реагентов. 2 ил.
Реферат
Изобретение относится к области биотехнологии и медицины, а именно к созданию полимерных материалов на основе хитозана, обладающих низкой токсичностью и повышенной биосовместимостью, в частности, пленок, микрокапсул, гидрогелей, раневых покрытий, скаффолдов и т.д. Изделия на основе биологически активных полимерных материалов могут быть использованы в хирургии при лечении ран и в качестве материалов для временного замещения тканей организма, в области биотехнологии для получения матриц для выращивания клеточных культур, в фармацевтике как носители ферментов и других биологически активных соединений.
В качестве реагентов для сшивания хитозана используют фталевый и янтарный диангидриды, диэпоксиды, краун-эфиры, дивинилсульфон [Серейкайте И., Бассус Д., Бобнис Р. и др. // Биоорганическая химия, 2003, т.29, №3, с.254-257] альдегиды различного строения: глутаровый альдегид (ГА), генипин [Mi F.L., Tan Y.C., Liang H.C. e.a. // J. Biomater. Sci. Polym. Ed., 2001, v.12, №8, p.835-850], формальдегид [A. Singh, S.S. Narvi, P.K. Dutta and N.D. Pandey. // Bull. Mater. Sci., 2006, V.29, №.3, p.233-238], ацетальдегид, глиоксаль, олигоэтиленгликоль [Ohya Y., Cai R., Nishizawa H., Нага К., Ouchi T. //S.T.P. Pharma Sci., 2000, v.10., №1., p.77-82]. Как показали авторы [S.J. Meade et al Bioorg. Med. Chem. 11, 853-862, 2003], на основании сравнительного изучения реакционной способности альдегидов наиболее легко реагирует с аминогруппами глутаровый альдегид (ГА). Использование ГА позволяет проводить сшивку хитозана в мягких условиях (низкие температуры, физиологические рН).
Из полимерных аминосодержащих носителей в сочетании с ГА использовали как синтетические полимеры (аминополистирол, модифицированные диаминами стиролдивинилбензольные полимеры, а также продукт сополимеризации этилена с малеиновым ангидридом), так и искусственные (аминоэтилцеллюлоза), а также аминосодержащие полимеры природного происхождения (желатин [Draye J.P., Delaey В., Van de Voorde A., Van Den Bulcke A., De Reu В., Schacht E. // Biomaterials, 1998, v.18. p.1677-1687], альбумин, белок птичьих перьев, казеин, коллаген и др.).
Наиболее перспективным полимером для создания биологически активных полимерных материалов является биосовместимый и биодеградируемый аминополисахарид хитозан [A.J.Varma et al. Carboh. Polymers, 55, 77-93,2004; J.Berger et al. Eur. J. Pharm. Biopharm. 57, 19-34, 2004; H. Yi et al. Biomacromolecules, 6, 2881-2894 2005; K. Kurita. Marine Biotech. 8, 203-226, 2006]. Растворимость хитозана в разбавленных водных растворах кислот, наряду с волокно- и пленкообразующей способностью и наличием реакционноспособных аминогрупп облегчает модификацию этого полимера и переработку его в полимерные изделия.
Ранее на основе системы хитозан - ГА (патент РФ 2261911) был разработан биокатализатор, содержащий иммобилизованную органофосфатгидролазу - фермент, гидролизующий фосфоэфирные связи, предназначенный для удаления фосфорорганических соединений с различных поверхностей, в т.ч. кожных покровов, и последующей их детоксикации, а также для использования в качестве средств индивидуальной защиты.
Гели, полученные в результате последовательной обработки хитозана ГА и затем диоксидом серы в водном растворе (US Patent 4125708), а также триполифосфатом и затем ГА (US Patent 5322935), предложено использовать в качестве наполнителей в аппаратах колоночного типа для очистки воды от растворенных в ней соединений, содержащих ионы хрома и марганца, и для изготовления высокоселективных сшитых мембран, предназначенных для разделения компонентов жидких смесей, например водно-спиртовых (US Patent 5006255). Смесь ГА и хитозана с низкой молекулярной массой представляет собой эффективный флокулянт при обезвоживании осадков сточных вод (US Patent 4609470). Пленки на основе хитозана, сшитого ГА или содержащим карбонильные группы сшивающим реагентом генипином (Mt F.-L., HuangC.-T., Liang H.-F. et al. // J.Agr.Food Chem., 2006, v.54, p.3290-3296), предложены в качестве покрытий различных пищевых продуктов; хитозановые пленки замедляют процессы окисления, роста микроорганизмов, потери влаги, сорбируют посторонние запахи, что позволяет использовать их в качестве съедобных пленок для качественного хранения пищевых продуктов.
Использование ГА при получении различных физических форм полимерных материалов на основе хитозана, в особенности биотехнологического и медицинского назначения, обладающих различными видами биологической активности, обусловлено его способностью при взаимодействии с аминополисахаридом образовывать обладающие высокой влагоудерживающей способностью прочные биосовместимые пористые структуры [Вихорева Г.А., Кильдеева Н.Р., Устинов М.Ю., Ночевкина Ю.Н. // Хим. волокна, 2002, №6, с. 29-33; Вихорева Г.А., Шаблыкова Е.А., Кильдеева Н.Р. // Хим. волокна, 2001, №3, с.38-42; Acharya A.S., Suseman L.G., Manning J.M. /А J. Biol. Chem., 1983, v.285, №4, p.2296-2302; Jameela S.R., Jayakrishnan A. //Biomaterials, 1995, №16, p.769-775].
Исследование процесса сшивки хитозана ГА показало присутствие в образцах сшитого хитозана продуктов кротоновой конденсации ГА [V.Crescenzi et al. // Biomacromolecules. 2003, v.4, p.1045-1054; П.А.Перминов. Канд. дисс. Москва, 2007], содержащих карбонильные группы и С=С-связи.
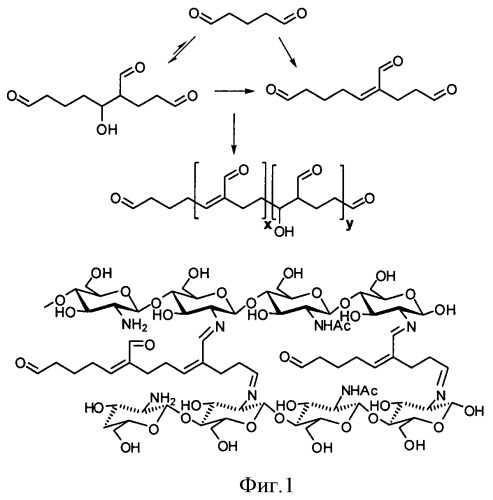
Кротоновая конденсация ГА катализируется аминогруппами, поэтому в случае хитозана ГА расходуется не только на сшивку аминополисахарида, но и на рост олигомерных цепей ГА, длину и структуру которых контролировать не представляется возможным (фиг.1). На фиг.1 приведено строение продуктов кротоновой конденсации ГА и продуктов взаимодействия ГА с хитозаном. Присутствие в составе образующихся гидрогелей реакционно-способных карбонильных групп и С=С-связей ограничивает использование системы хитозан - алифатический диальдегид в биомедицинских целях.
В этой связи весьма актуальным является поиск новых сшивающих реагентов, способных, подобно ГА, эффективно реагировать с хитозаном с образованием гидрогелей, но не образующих при этом олигомерных продуктов.
Задачей данного изобретения является создание на основе хитозана нетоксичных и биосовместимых материалов медицинского и биотехнологического назначения, а также новых сорбционно-активных материалов.
Указанная задача решается путем использования новых сшивающих реагентов, 2,4-производных 3-оксаглутарового альдегида (2,2'-оксидиацетальдегида). Введение электроотрицательного атома кислорода в 3-положение ГА, а также наличие заместителей в 2,4-положениях препятствуют альдольной и кротоновой конденсации и образованию нерегулярных продуктов.
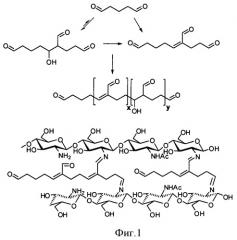
Эти соединения могут быть легко получены периодатным окислением нуклеозидов, нуклеотидов и моносахаридов (таких как производные рибозы, арабинозы, эритрозы, глюкозы, галактозы, арабинозы). Следует отметить, что получение производных 3-оксаглутарового альдегида осуществляется в водных растворах в мягких условиях, за реакцией можно наблюдать с помощью ТСХ или ЯМР-спектроскопии. Методика проведения реакции очень проста: к раствору соединения с диольной группой в воде добавляют небольшой избыток NaIO4 и выдерживают 10-30 мин при 20°С [С.Н.Михайлов, Г.И.Яковлев. // Химия природных соединений, 1987, с.40-43; Ермолинский Б.С., Михайлов С.Н. //Биоорган, химия. 2000, т.26, с.483-504] (фиг.2). На фиг.2 приведена схема реакции периодатного окисления, которая используется для получения производных 3-оксаглутарового альдегида. Следует отметить, что указанные производные могут быть также получены периодатным окислением соединений с триольными группами, в этом случае используется 2 эквивалента NaIO4.
Особенностями использования предлагаемых новых сшивающих реагентов являются: 1) строение диальдегидных производных моносахаридов, нуклеозидов и нуклеотидов исключает возможность кротоновой конденсации диальдегида, приводящей к образованию двойных С=С-связей и образованию токсичных продуктов с непредсказуемым составом; 2) наличие в составе сшивающих реагентов дополнительных функциональных групп (фосфатной группировки и гетероциклических оснований) дает возможность их использования не только в качестве сшивающих реагентов, но и модифицирующих соединений, обеспечивающих дополнительную функционализацию хитозана; 3) использование предлагаемых реагентов открывает новые возможности: а) создания новых биосовместимых материалов на основе хитозана; б) реализации в процессе сшивки не только ковалентных, но и ионных взаимодействий; в) приводит к получению новых сорбционно-активных материалов.
Ниже приводятся конкретные примеры реализации заявляемого технического решения.
Пример 1. Периодатное окисление уридина
0.899 г (4.2 ммоль) периодата натрия растворяли в 8 мл воды, затем добавляли при перемешивании 0.976 г (4 ммоль) уридина и раствор выдерживали при комнатной температуре. По данным ТСХ в системе хлороформ - спирт 4:1 реакция заканчивается через 1 час. Реакционую смесь оставляли в холодильнике на 20 часов при 0°С, выпавший белый кристаллический осадок NaIO3 отфильтровывали и получали 0.5 М раствор диальдегидного производного уридина (oxUrd), который использовывали для сшивки хитозана. Раствор диальдегидного производного уридина стабилен при хранении в холодильнике в течение нескольких месяцев.
Пример 2. Периодатное окисление динатриевой соли аденозин-5'-монофосфата
К раствору 0.782 г (2 ммоль) динатриевой соли аденозин-5'-монофосфата в 2.5 мл воды добавляли при перемешивании 4.2 мл 0.5 М раствора периодата натрия (2.1 ммоль) при комнатной температуре. Смесь перемешивали 2 часа при комнатной температуре и смесь оставляли в холодильнике на 20 часов при 0°С. Выпавший белый кристаллический осадок NaIO3 отфильтровывали и получали 0.3 М раствор диальдегидного производного аденозин-5'-монофосфата (oxAMP). Раствор диальдегидного производного стабилен при хранении в холодильнике в течение месяца.
Пример 3. Периодатное окисление метил β-D-рибофуранозида
0.899 г (4.2 ммоль) периодата натрия растворяли в 8 мл воды, затем добавляли при перемешивании 0.648 г (4 ммоль) метил β-D-рибофуранозида и раствор выдерживали при комнатной температуре. По данным ТСХ в системе хлороформ - спирт 4:1 реакция заканчивается через 1 час. Реакционую смесь оставляли в холодильнике на 20 часов при 0°С, выпавший белый кристаллический осадок NaIO3 отфильтровывали и получали 0.5 М раствор диальдегидного производного метил β-D-рибофуранозида, который использовали для сшивки хитозана. Раствор диальдегидного производного стабилен при хранении в холодильнике в течение нескольких месяцев.
Пример 4. Получение раствора 3-оксаглутарового альдегида (2,2'-оксидиацетальдегида)
0.450 г (2.1 ммоль) периодата натрия растворяли в 5 мл воды, затем добавляли при перемешивании 0.208 г (2 ммоль) 1,4-ангидроэритритола и раствор выдерживали при комнатной температуре. По данным ТСХ в системе хлороформ - спирт 5:1 реакция заканчивается через 1 час. Реакционую смесь оставляли в холодильнике на 20 часов при 0°С, выпавший белый кристаллический осадок NaIO3 отфильтровывали и получали 0.4 М раствор 3-оксаглутарового альдегида, который использовывали для сшивки хитозана. Раствор 3-оксаглутарового альдегида стабилен при хранении в холодильнике в течение нескольких месяцев.
Пример 5. Получение гидрогеля хитозана
К 2,5 г 3%-ного раствора хитозана с молекулярной массой 460 кДа в 2%-ной уксусной кислоте (рН 4,1) добавляют 0,4 мл 0,5М oxUrd. Полученный гель имеет следующий состав, мас. %: хитозан - 2,43, oxUrd - 1,54, остальное до 100%. Соотношение oxUrd/NH2 составляет 0,67 моль/моль. Гелеобразование завершается в течение 120 минут.
Пример 6. Получение гидрогеля хитозана
3%-ный раствор хитозана (молекулярная масса 460 кДа) в 2%-ной уксусной кислоте титруют 10М NaOH до рН 5,0. К 2,5 г этого раствора добавляют 0,4 мл 0,5М oxUrd. Полученный гель имеет следующий состав, мас. %: хитозан - 2,43, oxUrd - 1,54, остальное до 100%. Соотношение oxUrd/NH2 составляет 0,67 моль/моль. Гелеобразование завершается в течение 60 минут.
Пример 7. Получение гидрогеля хитозана
К 2,5 г 2%-ного раствора хитозана с молекулярной массой 460 кДа в 2%-ной уксусной кислоте (рН 4,1) добавляют 0,64 мл 4 мМ oxUMP. Полученный гель имеет следующий состав, маc.%: хитозан - 1,60, oxUMP - 0,026, остальное до 100%. Соотношение oxUMP/NH2 составляет 0,01 моль/моль. Гелеобразование завершается в течение 10 минут.
Пример 8. Получение гидрогеля хитозана.
К 2,5 г 2%-ного раствора хитозана с молекулярной массой 190 кДа в 2%-ной уксусной кислоте (рН 4,1) добавляют 0,64 мл 4 мМ охАМР. Полученный гель имеет следующий состав, мас. %: хитозан - 1,60, охАМР - 0,028, остальное до 100%. Соотношение охАМР/NH2 составляет 0,01 моль/моль. Гелеобразование завершается в течение 14 часов.
Пример 9. Получение гидрогеля, содержащего иммобилизованный трипсин
К 2,5 г 3%-ного раствора хитозана с молекулярной массой 190 кДа в 2%-ной уксусной кислоте (рН 4,1) добавляют 0,2 мл водного раствора трипсина (5 мг/мл) и 0,4 мл 0,5М oxUrd. Полученный гель имеет следующий состав, мас. %: хитозан - 2,43, oxUrd - 1,54, трипсин - 0,032, остальное до 100%. Соотношение охUrd/NH2 хитозана составляет 0,67 моль/моль. Гелеобразование завершается в течение 120 минут. Гель имеет активность, равную 90 ед./г высушенного геля.
Пример 10. Получение микрокапсул на основе хитозана
Микрокапсулы получали методом высокочастотного (до 200 Гц) разбиения струи формовочной композиции, представляющей собой совместный раствор хитозана с молекулярной массой 300 кДа и oxUrd, в теплое (60°С) растительное масло. Соотношение oxUrd/NH2 составляло 0,4 и 2 моль/моль. Для завершения процесса гелеобразования капсулы выдерживали в растительном масле в течение 5-10 минут при перемешивании. Полученные микрокапсулы, диаметром 300-500 мкм, имели правильную сферическую форму. Степень набухания в воде микрокапсул, полученных при соотношении oxUrd/NH2=2,0 моль/моль, составляет 300%, а при oxUrd/NH2=0,4 моль/моль - 2000%.
Пример 11. Получение объемно модифицированной пленки на основе хитозана
К 45 г 2%-ного раствора хитозана с молекулярной массой 460 кДа в 2%-ной уксусной кислоте (рН 4,1) добавляют 11,26 мл 2 мМ диальдегидного производного метил β-D-рибофуранозида. После перемешивания раствор выливали на чашку Петри диаметром 10 см и оставляли на ночь при температуре 40°С. Полученная пленка имеет следующий состав, мас.%: хитозан - 95,40, диальдегидное производное метил β-D-рибофуранозида - 0,80, остальное до 100%. Соотношение диальдегидное производное метил β-D-рибофуранозида /NH2 составило 0,005 моль/моль. Толщина сформованной пленки 50 мкм, степень набухания в воде 800%.
Пример 12. Получение поверхностно модифицированной пленки на основе хитозана
Раствор хитозана (2%) массой 45 г с молекулярной массой 467 кДа в 2%-ной уксусной кислоте (рН 4,1) выливали на чашку Петри диаметром 10 см и оставляют на 5 суток при температуре 25°С. Толщина сформованной пленки составила 50 мкм. Сформованную пленку заливали 20 мл 0,1 М водного раствора NaOH для нейтрализации уксусной кислоты, а затем после промывки дистиллированной водой и помещали в 11,3 мл 4 мМ 3-оксаглутарового альдегида на 2 часа. Толщина полученной пленки составляет 83 мкм, степень набухания в воде 1000%.
Пример 13. Получение волокнистого биокатализатора на основе хитозана
Тканый целлюлозный материал (хлопчатобумажную бязь) массой 1,2 г помещали в 3%-ный раствор хитозана с молекулярной массой 190 кДа (2,55 г), содержащий 0,2 мл водного раствора α-химотрипсина (5 мг/мл) и 0,40 мл 0,5М oxUrd. Бязь отжимали и выдерживали на воздухе в течение 25 минут. Полученный биокатализатор имел следующий состав, мас. %: белок - 2,05, хитозан - 12,92, нерастворимый носитель -51,37, oxUrd - 0,032, остальное до 100%. Активность биокатализатора составила 87 ед./г.
Сшивающие реагенты для получения на основе хитозана биосовместимых и нетоксичных материалов биомедицинского и биотехнологического назначения, а также новых сорбционно активных материалов, представляющие собой 2,4-производные 3-оксаглутарового альдегида (2,2'-оксидиацетальдегида).