Способ лечения больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к разделу «внутренние болезни», и касается лечения больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа. Проводят медикаментозную терапию и внутривенное лазерное облучение крови длиной волны 0,63 мкм, мощностью излучения на торце световода 1,5-2,0 мВт. Облучение назначают дифференцированно: в зависимости от выявляемого гемодинамического типа микроциркуляции, выраженности эндотелиальной дисфункции, а именно по уровню содержания нитратов/нитритов, нарушений агрегации тромбоцитов и эритроцитов, гликемического профиля, липидного спектра крови. При гиперемическом гемодинамическом типе микроциркуляции или нормоциркуляторном гемодинамическом типе микроциркуляции, уровне нитратов/нитритов 37,4±2,4 мкмоль/л и более, степени агрегации тромбоцитов в пределах 33,2±2,4 - 60,3±2,2%, степени агрегации эритроцитов в пределах 27,5±1,4 - 48,2±0,4%, уровне гликемии 8,4±1,2 ммоль/л, липидного спектра крови - общий холестерин 5,41±0,21 ммоль/л, триглицеридов 2,10±0,19 ммоль/л, холестерина липопротеидов низкой плотности (ЛПНП) 3,41±0,21 ммоль/л проводят 7 сеансов ежедневно в течение 15-20 минут. При спастическом гемодинамическом типе микроциркуляции или застойно-стазическом гемодинамическом типе микроциркуляции, уровне нитритов/нитратов менее 37,4±1,4 мкмоль/л, степени агрегации тромбоцитов 60,3±0,8% и более, степени агрегации эритроцитов 48,2±0,9% и более, уровне гликемии выше 8,4±1,2 ммоль/л, общего холестерина более 5,41±0,21 ммоль/л, триглицеридов более 2,10±0,19 ммоль/л, холестерина ЛПНП более 3,41±0,21 ммоль/л, проводят 10 сеансов ежедневно в течение 15-20 минут. Способ позволяет повысить эффективность проводимой медикаментозной терапии. 9 табл.
Реферат
Изобретение относится к медицине, а именно к разделу «внутренние болезни», и касается лечения больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа.
Наблюдающийся последние три десятилетия неуклонный рост числа больных сахарным диабетом 2 типа обуславливает все возрастающее внимание клиницистов к проблеме ранней диагностики, лечения и предупреждения его осложнений. По данным статистики в глобальном масштабе число пациентов с сахарным диабетом 2 типа составляет около 250 млн., причем, согласно прогнозам, к 2025 году эта цифра возрастет до 380 млн. человек. Высокий уровень инвалидизации и смерть больных связана с его микро- и макрососудистыми осложнениями. Проведенные эпидемиологические исследования показывают, что при сахарном диабете 2 типа риск развития ИБС увеличивается 3-6 раз. Очень длительно сердечно-сосудистые заболевания протекают в субклинической форме, а первая их клиническая манифестация проявляется в виде инфаркта миокарда, инсульта или диабетической гангрены. Сердечно-сосудистые заболевания являются причиной смерти 50-60% всех больных, страдающих диабетом. В соответствии с этим сахарный диабет 2 типа можно выделить в число заболеваний, имеющих социальное значение, а поиск путей эффективного лечения, направленного на снижение инвалидизации и смертности, является актуальной задачей. Изучение патогенетических механизмов становления сахарного диабета 2 типа, и разработка на этой основе новых групп лекарственных средств и методов лечения, остается одной из важнейших проблем современного здравоохранения. В последние годы внимание многих исследователей привлекают немедикаментозные методы лечения. Одним из современных методов немедикаментозного лечения различных заболеваний является применение низкоинтенсивного лазерного излучения (НИЛИ). Патогенетическое воздействие НИ ЛИ проявляется рядом эффектов: иммуномодулирующим действием, анальгезирующим, сосудорасширяющим действием, улучшением микроциркуляции, реологических свойств крови, повышением антиоксидантной активности, нормализацией ионного состава крови, повышением кислородтранспортной функции.
Наиболее близким по совокупности существенных признаков к заявляемому изобретению является способ лечения больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа, взятый за прототип (Н.Е.Сарано, С.Г.Козлов, М.Г.Творогова, А.А.Лякишев, В.Г.Наумов. Кардиология. - 2003 - №43 - с.30-35), включающий комбинированную терапию флувастатином и фенофибратом у больных со смешанной гиперлипидемией, лечение проводилось в течение 12 недель. При назначении медикаментозной терапии учитывались сопутствующая патология, гликемический профиль. Указанный способ лечения позволял достичь целевых значений общего холестерина, холестерина липопротеинов низкой плотности, триглицеридов.
Недостатком прототипа является использование только медикаментозной терапии, достаточно высокая стоимость лечения, в указанном способе не отражено влияние проводимого лечения на такие важные патогенетические звенья в развитии ИБС и сахарного диабета, как эндотелиальная дисфункция, нарушения в системе микроциркуляции; отсутствует дифференцированный подход к лечению в зависимости от исходного уровня изучаемых показателей.
Заявляемое изобретение направлено на решение задачи, заключающейся в создании способа лечения больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа.
Решение этой задачи обеспечивает улучшение самочувствия, повышает эффективность проводимой медикаментозной терапии, снижает стоимость лечения больных с данной патологией, дает обоснование эффективности лазерной терапии в комплексном лечении больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа с учетом наиболее важных патогенетических звеньев развития ишемической болезни сердца и сахарного диабета 2 типа.
Для достижения этого технического результата, заявляемое изобретение способа лечения больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа включает следующие существенные признаки - внутривенное лазерное облучение крови длиной волны 0,63 мкм, назначают вместе с медикаментозной терапией дифференцированно в зависимости от выявляемого гемодинамического типа микроциркуляции, выраженности эндотелиальной дисфункции, а именно по уровню содержания нитратов/нитритов, нарушений агрегации тромбоцитов и эритроцитов, гликемического профиля, липидного спектра крови, при гиперемическом гемодинамическом типе микроциркуляции или нормоциркуляторном гемодинамическом типе микроциркуляции, уровне нитратов/нитритов 37,4±2,4 мкмоль/л и более, степени агрегации тромбоцитов в пределах 33,2±2,4 - 60,3±2,2%, степени агрегации эритроцитов в пределах 27,5±1,4 - 48,2±0,4%, уровня гликемии 8,4±1,2 ммоль/л, липидного спектра крови - общий холестерин 5,41±0,21 ммоль/л, триглицериды 2,10±0,19 ммоль/л, холестерин ЛПНП 3,41±0,21 ммоль/л, проводят 7 сеансов ежедневно в течение 15-20 минут, при спастическом гемодинамическом типе микроциркуляции или застойно-стазическом типе микроциркуляции, уровне нитритов/нитратов менее 37,4±2,4 мкмоль/л, степени агрегации тромбоцитов 60,3±0,8% и более, степени агрегации эритроцитов 48,2±0,9% и более, уровня гликемии выше 8,4±1,2 ммоль/л, общий холестерин более 5,41±0,21 ммоль/л, триглицериды более 2,10±0,41 ммоль/л, холестерин ЛПНП 3,82±0,9 ммоль/л и более, проводят 10 сеансов ежедневно в течение 15-20 минут.
По отношению к прототипу у заявляемого изобретения имеются следующие отличительные признаки - внутривенное лазерное облучение крови при ишемической болезни сердца с сопутствующим сахарным диабетом 2 типа назначают дифференцированно в зависимости от гемодинамического типа микроциркуляции, выраженности эндотелиальной дисфункции, а именно по уровню содержания нитратов/нитритов, нарушений агрегации тромбоцитов и эритроцитов, гликемического профиля, липидного спектра крови, при гиперемическом гемодинамическом типе микроциркуляции или нормоциркуляторном гемодинамическом типе микроциркуляции, уровне нитратов/нитритов 37,4±2,4 мкмоль/л и более, степени агрегации тромбоцитов в пределах 33,2±2,2 - 60,3±2,2%, степени агрегации эритроцитов в пределах 27,5±1,4 - 48,2±0,4%, уровне гликемии 8,4±1,2 ммол/л, липидного спектра крови - общий холестерин 5,41±0,21 ммоль/л, триглицериды 2,10±0,91 ммоль/л, холестерин ЛПНП 3,41±0,9 ммоль/л, проводят 7 сеансов ежедневно в течение 15-20 минут; при спастическом гемодинамическом типе микроциркуляции или застойно-стазическом гемодинамическом типе микроциркуляции, уровне нитратов/нитритов менее 37,4±2,4 мкмоль/л, степени агрегации тромбоцитов 60,3±0,8% и более, степени агрегации эритроцитов 48,2±0,9% и более, уровне гликемии выше 8,4±1,2 ммоль/л, общий холестерин более 5,41±0,21 ммоль/л, триглицериды 2,10±0,19 ммоль/л, холестерин ЛПНП более 3,41±0,21 ммоль/л, проводят 10 сеансов ежедневно в течение 15-20 минут. В лечении больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа используется внутривенное лазерное облучение крови, как метод коррекции микроциркуляторных нарушений, коррекции дисфункции эндотелия, улучшения гемореологических свойств крови, коррекция липидного спектра крови, снижение уровня гликемии. Между отличительными признаками и техническим результатом существует следующая причинно-следственная связь: за счет дифференцированного подхода к лечению больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа производится более конкретное назначение внутривенного лазерного облучения крови, которое учитывает патогенетические механизмы, участвующие в формировании ишемической болезни сердца и сахарного диабета 2 типа, такие как нарушения в системе микроциркуляции, дисфункция эндотелия, нарушения в системе гемостаза, гиперлипидемия, гипергликемия, что повышает эффективность проводимой медикаментозной терапии.
По имеющимся у авторов сведениям, совокупность существенных признаков, характеризующих сущность заявляемого изобретения не известна, что позволяет сделать вывод о соответствии изобретения критерию «новизна».
По мнению авторов, сущность заявляемого изобретения не следует явным образом из известного уровня медицины, так как у него не выявляется вышеуказанный дифференцированный подход к назначению процедур лазерной терапии, которые отличают от прототипа заявляемое изобретение, что позволяет сделать вывод о соответствии его критерию «изобретательский уровень».
Совокупность существенных признаков, характеризующих сущность изобретения, в принципе, может быть использована многократно в медицине с получением технического результата, заключающийся в повышении эффективности комплексной терапии (медикаментозная терапия + ВЛОК) у больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа, что позволяет сделать вывод о соответствии изобретения критерию «промышленная применимость».
Данный способ лечения осуществляется следующим образом.
Всем больным с ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа проводилась медикаментозная терапия (ингибиторы АПФ, бета-адреноблокаторы, блокаторы ангиотензиновых рецепторов, диуретики, статины, гипогликемические препараты) с одновременным применением курса внутривенного лазерного облучения крови.
Предлагаемый дифференцированный подход в лечении больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа использовался у 102 пациентов (42 мужчин и 60 женщин) с диагнозом ИБС, сахарный диабет 2 типа, стадия декомпенсации (классификация ВОЗ 1999, 2001), в возрасте - 55,4±3,3 лет, длительность сахарного диабета 6,2±2,3 лет. Все пациенты проходили клинико-лабораторное обследование, включающее сбор анамнеза, клинический и биохимический анализы крови, гликемический профиль, общий анализ мочи, запись ЭКГ, УЗИ внутренних органов, рентгенографию, осмотр глазного дна. Критериями исключения из исследования были: больные перенесшие инфаркт миокарда, стенокардия напряжения III-IV-го функционального класса, хроническая сердечная недостаточность II Б-III стадии, экстрасистолы высоких градаций, мерцательная аритмия, острая декомпенсации углеводного обмена, облитерирующие поражения магистральных сосудов.
Все больные были разделены на 2 группы. В контрольной группе (30 человек) для лечения использовалась медикаментозная терапия (ингибиторы АПФ, бета-адреноблокаторы, блокаторы ангиотензиновых рецепторов, гипогликемические препараты, статины) без включения курса лазерной терапии. Больным основной группы (72 человек) дополнительно к медикаментозной терапии назначалось внутривенное лазерное облучение крови. Группы были сопоставимы по полу, возрасту, длительности заболевания, уровню гликемии. Все пациенты были обследованы в динамике - до назначения курса терапии и после ее завершения.
Курс внутривенной лазерной терапии проводили с помощью аппарата лазерной терапии «Мулат» с длиной волны 0,63 мкм, выходной мощностью на торце световода 1,5-2,0 мВт, непрерывный режим излучения. Процедуры выполняются ежедневно, продолжительность одной процедуры 15-20 минут. Назначение внутривенной лазерной терапии проводилось дифференцированно.
I группе - 30 человек при выявлении гиперемического гемодинамического типа микроциркуляции (показатель микроциркуляции (ПМ) - 9,5±0,3 перф. ед., резерв каппилярного кровотока (РКК) - 144±23%) или нормоциркуляторного гемодинамического типа микроциркуляции (ПМ) 4,2±0,7 перф. ед., РКК - 240±23%), уровне нитратов/нитритов 37,6±2,4 мкмоль/л и более, степени агрегации тромбоцитов в пределах 33,2±2,4 - 60,3±2,2%, степени агрегации эритроцитов в пределах 27,5±1,4 - 48,2±0,4%, уровне гликемии 8,4±1,2 ммоль/л, липидного спектра крови - общий холестерин 5,41±0,21 ммоль/л, триглицериды 2,10±0,19 ммоль/л, холестерин ЛПНП 3,41±0,9 ммоль/л, проводят 7 сеансов ежедневно в течение 15-20 минут. При выявлении спастического гемодинамического типа микроциркуляции (ПМ) - 2,2±0,5 перф. ед., РКК - 410±23%) или застойно-стазического гемодинамического типа микроциркуляции (ПМ 3,0±0,3 перф. ед., РКК - 143±20%, уровне нитратов/нитритов менее 37,4±1,4 мкмоль/л, степени агрегации тромбоцитов 60,3±0,8% и более, степени агрегации эритроцитов 48,2±0,9% и более, уровне гликемии выше 8,4±1,2 ммоль/л, липидного спектра крови - общий холестерин более 5,41±0,21 ммоль/л, триглицериды более 2,10±0,19 ммоль/л, холестерин ЛПНП более 3,41±0,21 ммоль/л, проводят 10 сеансов ежедневно в течение 15-20 минут (II группа - 40 человек).
Эффективность лазерной терапии оценивали на основании динамики показателей гемостаза, микроциркуляции, нитратов/нитритов, уровню гликемии, липидного спектра крови, по изменению клинического статуса. Исследуемые показатели сравнивались с группой практически здоровых людей (25 человек).
Исследование агрегации тромбоцитов и эритроцитов проводилось турбодиметрическим методом G. Born. В модификации J. О Brien с помощью анализатора агрегации АР 2110, SOLAR. В качестве индуктора агрегации тромбоцитов использовали адреналин в дозе 5 мкг/мл, а в качестве индуктора эритроцитов - алциановый голубой в дозе 0,2 мкг/мл. Оценивались следующие параметры агрегации: степень агрегации (СтА, %), скорость определения альбумина в моче.агрегации (СкА, % мин). Липидный спектр крови определяли с помощью набора реагентов фирмы «Ольвекс Диагностикум». В набор входили реагенты для определения концентрации общего холестерина, триглицеридов, холестерина липопротеидов высокой плотности в плазме крови. Уровень липопротеидов низкой плотности определяли по формуле Фридвальда: ЛПОНП=ТГ/2,2; ЛПНП=ОХС - «Микральтест» (фирмы «Roch») для количественного ЛПВП - ЛПОНП. Для диагностики микроальбуминурии использовали тест - полоски.
Исследование микроциркуляции проводилось методом лазерной доплеровской флоуметрии (ЛДФ) на аппарате ЛАКК-02 (производство НПП ЛФЗМА, РФ). ЛДФ-сигнал регистрировался в точке, расположенной на тыльной поверхности левого предплечья на 4 см выше лучезапястного сустава (зона Захарьина-Геда) в положении пациента лежа на спине, руки вытянуты параллельно вдоль туловища. За 2 часа до начала исследования пациентам не разрешали прием пищи и жидкости. В течение 15-20 мин перед исследованием проводилась адаптация пациента к температуре помещения (21-24°С). Исходно проводилась запись базального кровотока в течение 3 минут, затем проводилась окклюзионная проба (ОП). Оценивались следующие параметры: показатель микроциркуляции (ПМ), характеризующий степень перфузии, амплитуда медленных колебаний микрокровотока (ALF), амплитуда быстрых колебаний (AHF), амплитуда кардиоритмов (ACF), внутрисосудистое сопротивление (CC=ACF/M), индекс эффективности микроциркуляции (ИЭМ), отражающий соотношение активных и пассивных колебаний тканевого кровотока. При проведении ОП рассчитывались: биологический ноль (Mmin.), максимальный показатель реактивной гиперемии (Mmax), резерв капиллярного кровотока (РКК). При соотношении ПМ в исходной ЛДФ-грамме и РКК в окклюзионной пробе, давалась оценка гемодинамических типов микроциркуляции (ГТМ).
Продукцию NO определяли по суммарной концентрации стабильных метаболитов (NOX) нитратов (NO3 -) и нитритов (NO2 -) в плазме крови, колориметрическим методом по развитию окраски в реакции диазотирования нитритом сульфаниламида, входящего в состав реактива Грисса. Восстановление нитратов до нитритов проводили с помощью ванадия хлорида (VCl3). Интенсивность окраски определяли на приборе Victor2 фирмы Perkin Elmer, измеряли оптическую плотность образцов в стандартном 96-луночном планшете (для иммуноферментного анализа) при длине волны 540 нм. Для построения калибровочной кривой использовали 1 М раствор NaNO2 в воде, который перед употреблением разводили в 1000 раз и готовили серию разведений. Статистическая обработка результатов исследования проводилась с использованием пакета статистических программ Microsoft Excel 2003. Все данные представлены в виде М±m. Достоверность различий между группами определялась по критерию Стьюдента. Различия считались достоверными при p<0,05. Корреляционный анализ проводился с расчетом коэффициента корреляции Пирсона.
При поступлении более половины пациентов как основной группы, так и контрольной предъявляли жалобы на боли в области сердца сжимающего характера без иррадиации, не связанные с физической нагрузкой, купирующиеся самостоятельно, на повышенную утомляемость, раздражительность, возбудимость, эмоциональную лабильность, снижение трудоспособности, нарушение сна, сухость во рту, жажду, похудание, частое мочеиспускание.
У пациентов основной группы уже после 5-7 сеансов лазеротерапии отмечалось изменение общего самочувствия, уменьшились или полностью исчезли боли в области сердца, сухость во рту. После курса лазерной терапии почти у всех больных 87% (26) в I группе и у 80% (32) во II группе повысилась работоспособность, нормализовался сон, уменьшились вегетативные проявления, сократилась частота ощущения перебоев в работе сердца и интенсивность кардиалгии. Ни у одного пациента не отмечено реакции вторичного обострения, что свидетельствует об адекватности воздействия и хороших компенсаторных возможностях. На фоне проведения курса лазерной терапии в I группе уже после 5-й процедуры отмечалось снижение уровня гликемии до 6,5 ммол/л, во II группе уровень гликемии снизился до 7,5 ммоль/л после 7-ой процедуры. Следует отметить, что терапевтическая эффективность ВЛОК зависит от степени тяжести течения сахарного диабета и наибольший терапевтический эффект был достигнут в основной группе у больных с сахарным диабетом 2 типа, в стадии компенсации. У пациентов контрольной группы также отмечалась динамика субъективных данных, сократилась частота и интенсивность кардиалгий, перебоев в работе сердца, однако изменения у больных, получавших ВЛОК, наступали быстрее, были несколько более выраженными и отмечались у большего количества наблюдаемых пациентов.
При анализе показателей микроциркуляции у больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа до лечения были выявлены различия в структуре ГТМ. Как в основной, так и в контрольной группе отмечалось преобладание ЗСГТМ у 65% (26) больных во II группе, и у 36% (13) в группе контроля и СГТМ у 35% (14) во II группе, и 40% (14), в группе контроля, что обусловлено спазмом сосудов, функциональным и структурным разрежением микроциркуляторной сети. ГГТМ регистрировался в 63% (19) случаев в I группе и в 16% (5) случаев в группе контроля, что свидетельствует об увеличении числа функционирующих капилляров, способствующих уменьшению давления на каждый сосуд микроциркуляторного русла в ответ на увеличение сердечного выброса. Реже всего наблюдался НГТМ лишь в 37% (11) случаев в I группе и в 8% (3) случаев в группе контроля.
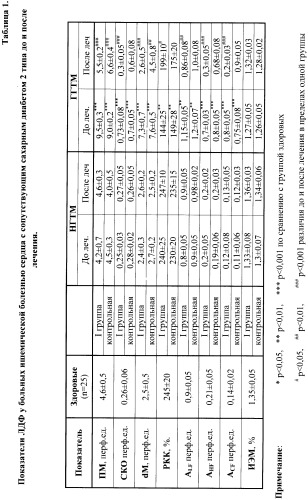
Исходно у всех больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа выявлены существенные отклонения основных параметров ЛДФ-граммы от нормального уровня (табл.1, 2). У больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа с ЗСГТМ отмечалось достоверное снижение ПМ, отражающего скорость периферического кровотока - 3,0±0,3 перф. ед. (p<0,05) во II группе и 3,2±0,2 перф. ед. (p<0,05) в контрольной, по сравнению с группой здоровых. Сниженным ПМ был и у больных со СГТМ - 2,2±0,5 перф. ед. (p<0,01) во II группе и 2,4±0,3 перф. ед. (p<0,01) в контрольной. Снижение ПМ свидетельствует о сниженных компенсаторных возможностях микроциркуляторного русла: уменьшении числа функционирующих капилляров, снижении скорости кровотока за счет спазма приносящих сосудов. У больных с ГГТМ, для которого характерен больший приток крови к тканям, отмечалось достоверное повышение ПМ по сравнению со здоровыми - 9,5±0,3 перф. ед. (p<0,001) в I группе и 9,2±0,2 перф. ед. (p<0,001) в группе контроля.
Показатель СКО, позволяющий определить выраженность нарушений механизмов регуляции тканевого кровотока, был повышен только у больных с ГГТМ в обеих группах и составил 0,73±0,08 перф. ед. (p<0,001) в I группе и 0,7±0,05 перф. ед. (p<0,001) в контрольной, что свидетельствует о более интенсивном включении регуляторных механизмов.
При проведении в группе больных с ЗСГТМ и ГГТМ окклюзионной пробы (ОП) нами отмечено достоверное снижение РКК. При ЗСГТМ РКК составил 143±20%, (p<0,01) во II группе и 145±25% (p<0,01) в контрольной, по сравнению со здоровыми, а у больных с ГГТМ 144±25% (p<0,01) в I группе и 146±28% (p<0,01) в контрольной, что отражает развитие стаза и застоя в посткапиллярном звене микроциркуляторного русла, а также функциональное и морфологическое разрежение сети артериол и капилляров. Высокий РКК отмечался у больных с СГТМ - 410±26% (p<0,001) во II группе и 402±23% (p<0,001) в группе контроля. При проведении реактивной постокклюзионной гиперемии в группе больных с ГГТМ выявлено увеличение показателя dM (разница между исходным и минимальным кровотоком во время окклюзии) - 7,3±0,7 перф. ед., (p<0,001) у больных I группы и 7,6±0,5 перф. ед., (p<0,001) у пациентов контрольной группы. Возрастание этого показателя говорит об увеличении числа функционирующих капилляров и скорости потока эритроцитов. При СГТМ этот показатель уменьшался - 0,9±0,1 перф. ед., (p<0,01) во II группе и 1,1±0,2 перф. ед., (p<0,01) в контрольной; уменьшение dM отмечалось и при ЗСГТМ - 1,2±0,1 перф. ед. (p<0,05) и 1,1±0,3 перф. ед., (р<0,05) соответственно, что характерно при явлениях стаза и разрежении сети артериол и капилляров.
При анализе амплитудно-частотного спектра у больных ГБ выявлено существенное изменение активных медленных колебаний (ALF), пассивных пульсовых колебаний (ACF) и быстрых колебаний (AHF) микрокровотока. У больных ИБС выявлено достоверное уменьшение по сравнению с группой здоровых амплитуды медленных колебаний (ALF) при ЗСГТМ - 0,32±0,05 перф. ед. (p<0,001) во II группе и 0,34±0,08 перф. ед., (p<0,001) в контрольной, при СГТМ - 0,36±0,04 перф. ед., (p<0,001) во II группе и 0,38±0,06 перф. ед., (p<0,001) в контрольной. В норме показатель ALF, связанный с ритмической активностью собственных компонентов микроциркуляторного русла (эндотелий капилляров, прекапиллярные сфинктеры, пути «шунтирующего» кровотока) является преобладающим среди других в спектре колебаний. Уменьшение амплитуды колебаний свидетельствует о патологических изменениях в микрососудах, в результате чего снижается способность прекапиллярных сфинктеров к активному сокращению. Амплитуда быстрых колебаний (AHF), связанных с актом дыхания была достоверно выше только в группе больных с ГГТМ - 0,6±0,03 перф. ед. (p<0,001) в I группе и 0,7±0,05 перф. ед. (p<0,001) в контрольной, что можно объяснить участием при ИБС объемзависимых механизмов, которые и обеспечивают большую амплитуду колебаний кровотока в капиллярах. Колебания HF связаны с дыхательными движениями и обусловлены увеличением притока крови к сердцу во время вдоха и его уменьшением на выдохе и у здоровых лиц выражены слабо, либо отсутствуют. Уровень пульсовых колебаний (ACF) был достоверно повышен только в группе больных с ГГТМ - 0,8±0,05 перф. ед. (p<0,001) в I группе и 0,75±0,08 перф. ед. (p<0,001) в контрольной, тогда как у больных с ЗСГТМ и СГТМ отмечалось некоторое уменьшение ACF. При ЗСГТМ и при СГТМ уровень пульсовых колебаний был достоверно снижен и составил при ЗСГТМ - 0,08±0,01 (p<0,01) во II группе и 0,07±0,01 (p<0,01) в контрольной, а при СГТМ - 0,09±0,01 (p<0,05) во II группе и 0,08±0,01 (p<0,01) в группе контроля. Снижение ACF обусловлено, вероятно, нарушениями гемостаза, процессами ремоделирования артериолярно-капиллярного русла - увеличением соотношения медия/просвет в системе артериол, разрежением артериол и капилляров, а также участием объемзависимых механизмов, за счет которых при ГБ депонируется избыточное количество крови в венулах, что еще более усиливает демпфирующую роль микрососудов в отношении пульсовых колебаний.
Анализ ИЭМ свидетельствует о его достоверном уменьшении в группе больных с ЗСГТМ - 0,72±0,05 (p<0,001) во II группе и 0,68±0,06 (p<0,01) в группе контроля, что характеризует преобладание пассивных механизмов регуляции кровотока. Повышение ИЭМ отмечалось у больных со СГТМ - 1,87±0,08 (p<0,001) во II группе и 1,7±0,05 (p<0,001) в группе контроля и может свидетельствовать о выраженном преобладании активных вазоконстрикторных механизмов регуляции кровотока. Таким образом, полученные нами данные свидетельствуют о преобладании при ГБ спазма микрососудов с явлениями стаза - застоя крови.
После проведенного лечения существенное и достоверное перераспределение ГТМ произошло в основной группе больных, получавших вместе с медикаментозной терапией ВЛОК.
Динамика основных показателей микроциркуляции в группах после лечения отражена в таблицах 1, 2.
В основной группе после лечения возросло число пациентов с НГТМ до 74% (52) за счет уменьшения доли ЗСГТМ до 8% (3), СГТМ до 5% (2) и ГГТМ до 13% (4). В контрольной группе достоверного перераспределения ГТМ не произошло. Доля СГТМ составила 25% (9), ЗСГТМ 40% (14), ГГТМ 10% (3) и НГТМ 25% (9). У больных II группы с ЗСГТМ после лечения отмечалось повышение ПМ до 6,3±0,2 перф. ед., (p<0,001) в отличие от больных в контрольной группе, где ПМ достоверно не изменился и составил 3,6±0,3 перф. ед. Достоверно не изменился ПМ в контрольной группе и при СГТМ 2,2±0,2 перф. ед. в отличие от ПМ во II группе, где он стал достоверно выше и составил 4,6±0,1 перф. ед. (р<0,001). Повышение ПМ отражает увеличение объемного периферического кровотока, что обусловлено вазодилатирующим эффектом, улучшением реологических свойств крови. Определенная доля прироста ПМ обусловлена обратным ремоделированием микрососудистого русла, а также увеличением числа функционирующих капилляров. Снижение исходно повышенного ПМ при ГГТМ произошло в обеих группах и составило 5,5±0,2 перф. ед. (p<0,001) в I группе и 6,9±0,4 перф. ед. (p<0,001) в контрольной.
Показатель СКО, изначально повышенный у больных с ГГТМ снизился до 0,3±0,05 перф. ед. (p<0,001) в I группе, что свидетельствует о нормализации регуляторных механизмов. В группе контроля после лечения достоверного снижения не наблюдалось, показатель СКО там составил - 0,6±0,08 перф. ед. Увеличение РКК при проведении ОП под влиянием терапии является важным свидетельством улучшения реактивности микрососудов в ответ на изменения напряжения сдвига в ходе окклюзии. Так у больных с ЗСГТМ во II группе после лечения произошло достоверное повышение РКК до 235±15% (p<0,01). В контрольной группе РКК достоверно не увеличился и составил 180±10%. У больных I группы с ГГТМ также отмечалось повышение РКК до 199±10% (p<0,05), в отличие от контрольной группы, где достоверного повышения РКК не наблюдалось - 175±20%. Достоверное снижение исходно повышенного показателя РКК у больных с СГТМ наблюдалось только у больных II группы - 245±10% (p<0,001), в отличие от контрольной группы, где достоверного снижения РКК не отмечалось - 380±20 перф. ед.
При проведении реактивной постокклюзионной гиперемии у больных с ЗСГТМ и СГТМ во II группе выявлено увеличение показателя dM - 2,8±0,2 перф. ед. (p<0,001) и 2,3±0,2 перф. ед. (p<0,001) соответственно, что говорит об увеличении числа функционирующих капилляров и скорости потока эритроцитов. В контрольной группе показатель dM не изменился и составил 1,16±0,2 перф. ед у больных с ЗСГТМ и 1,3±0,3 перф. ед. у больных с СГТМ. У больных с ГГТМ в I группе после лечения dM уменьшился и составил 2,6±0,5 перф. ед. (p<0,001), в контрольной группе это снижение не достигло нормальных значений - 4,5±0,8 перф. ед. (р<0,01).
При анализе амплитудно-частотного спектра (АЧС) ЛДФ-граммы после лечения во II группе выявлено достоверное увеличение амплитуды медленных колебаний (ALF) У больных с ЗСГТМ до 0,84±0,05 перф. ед. (p<0,001) и у больных с СГТМ до 0,87±0,06 перф. ед. (p<0,001), что связано с повышением миогенного тонуса артериол и прекапиллярных сфинктеров. В контрольной группе достоверного увеличения (ALF) не произошло. У больных с ГГТМ с исходно повышенным уровнем медленных колебаний периферического кровотока, означающим исходно повышенный сосудистый тонус, в процессе терапии было выявлено уменьшение ALF До 0,86±0,08 перф. ед. (p<0,01) в I группе и до 1,0±0,08 перф. ед. в контрольной группе.
Амплитуда быстрых колебаний (AHF), связанных с актом дыхания достоверно снизилась у больных с ГГТМ только в I группе и составила 0,3±0,05 перф. ед. (p<0,001), что связано с уменьшением нагрузки на артериолярное звено микроциркуляторного русла, уменьшением ишемии ткани. В контрольной группе достоверного снижения не отмечалось - 0,68±0,08 перф. ед.
Амплитуда пульсовых колебаний (ACF), сниженная до лечения у больных с ЗСГТМ и СГТМ в обеих группах нормализовалась после лечения только во II группе и составила 0,13±0,02 перф. ед. (p<0,01) и 0,15±0,01 перф. ед. (p<0,001) соответственно. В контрольной группе этот показатель после лечения не изменился и составил 0,09±0,01 перф. ед. при ЗСГТМ и 0,08±0,01 перф. ед. при СГТМ. Таким образом, после лечения в основной группе улучшилось проведение пульсовых волн по периферическим микрососудам. Исходно повышенная ACF при ГГТМ достоверно снизилась у больных I группы до 0,2±0,03 перф. ед. (p<0,001), в контрольной группе произошло даже некоторое повышение ACF - 0,8±0,05 перф. ед.
При оценке ИЭМ (соотношение активных и пассивных колебаний тканевого кровотока) у больных СГТМ после лечения во II группе определенно достоверное его уменьшение - 1,3±0,02 (p<0,001), в отличие от контрольной группы - 1,6±0,05. Снижение ИЭМ при СГТМ после лечения может свидетельствовать о подавлении активных вазоконстрикторных механизмов регуляции кровотока. У больных с ЗСГТМ отмечалось повышение исходно сниженного показателя ИЭМ во II группе до 1,4±0,06 (p<0,001), в контрольной до 0,9±0,08 (p<0,05), что связано со снижением пассивных механизмов регуляции кровотока.
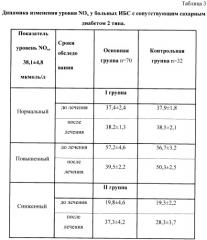
Таким образом, медикаментозная терапия в комплексе с НИЛИ оказывает нормализующее действие на различные типы нарушений микроциркуляции у сахарным диабетом 2 типа, проявляющееся в увеличении числа функционирующих капилляров, активации периферической гемоциркуляции, улучшении оксигенации тканей и повышении уровня метаболических процессов в клетках. При оценке степени эндотелиальной дисфункции учитывались продукция стабильных метаболитов оксида азота нитратов/нитритов в плазме крови. Анализ показателей продукции оксида азота у пациентов с ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа позволил установить, что уровень стабильных метаболитов NO-нитратов и нитритов (NOX) в плазме крови у больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа был различным (табл.3).
Так у больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа до лечения отмечалось: нормальное содержание NOx - 37,4±2,4 мкмоль/л у больных I группы и 37,9±1,8 мкмоль/л у больных контрольной группы, повышенное содержание NOx - 57,2±4,6 мкмоль/л (p<0,001) у больных I группы и 56,7±3,2, мкмоль/л у больных контрольной группы и сниженное содержание NOx - 19,8±4,6 мкмоль/л, (p<0,05) у больных II группы и 9,3±2,2 мкмоль/л у больных контрольной группы.
Таким образом, у больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа существует 3 типа ответа систем генерации NO: 1) угнетение синтеза NO; 2) отсутствие изменений; 3) усиление синтеза NO. Снижение уровня конечных метаболитов NO в плазме крови можно рассматривать как истощение стресс-лимитирующего и адаптационного эффектов NO. Нормальный и повышенный уровень метаболитов NO в плазме крови отражает сохраненный уровень реактивности и более высокие адаптационные возможности организма.
После проведенного лечения лишь в группе, получающей ВЛОК, нами была отмечена коррекция исходно измененного показателя NOX (табл.3). У больных ИБС при исходно повышенном содержании NOx этот показатель снизился до 39,5±2,2 мкмоль/л в I группе, получающей ВЛОК, в контрольной группе достоверного снижения уровня NOx не произошло 50,3±2,5 мкмоль/л. При исходно сниженном уровне NOx во II основной группе наблюдалось достоверное повышение до 37,3±4,2 мкмоль/л, тогда как в контрольной группе этот показатель достоверно не изменился и составил 28,3±3,7 мкмоль/л. При исходно нормальном содержании NOx как в основной, так и в контрольной группе после лечения существенных изменений не выявлено.
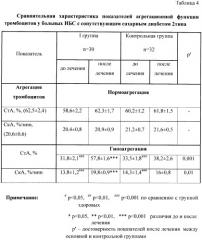
При анализе показателей агрегационной функции тромбоцитов и эритроцитов до лечения у всех больных были выявлены различные типы агрегационных кривых. (Табл.4, 5, 6, 7)
Повышение агрегации тромбоцитов имело место у 81% (57) больных во II группе и у 77% (27) в контрольной группе, при этом СтА у них составила 85,2±2,5 (p<0,001) и 83,6±2,3 (p<0,001) соответственно, а СкА 36,6±2,7 (p<0,001) и 35,8±2,5 (p<0,001). Гипоагрегация регистрировалась у 12% (8) пациентов в I группе, при этом СтА составила 31,8±2,1 (p<0,001), а СкА 13,8±1,2 (p<0,001) и у 14% (5) больных в группе контроля, где СтА составила 33,5±1,8 (p<0,001), а СкА 14,3±1,4 (p<0,001). Нами также были отмечены случаи с нормальной агрегацией тромбоцитов у 7% (5) больных в I группе и у 9% (3) в группе контроля. В I группе больных с нормальной агрегацией тромбоцитов СтА и СкА составили 58,6±2,2 и 20,4±0,8, а в группе контроля 60,2±1,2 и 21,6±0,7 соответственно.
В норме при воздействии индуктора агрегации (адреналин) на агрегатограмме регистрируется двойная волна агрегации: 1-ая связана с влиянием индуктора (определяет сокращение тромбоцитов), 2-ая образуется за счет реакции высвобождения собственных агонистов, содержащихся в δ-гранулах тромбоцитов. Качественный анализ агрегатограмм показал, что у большинства больных ИБС в обеих группах до лечения отмечалось отсутствие двухфазности агрегационной кривой в отличие от здоровых лиц. У здоровых людей в первой фазе агрегации происходит образование мелких агрегатов, а образование крупных агрегатов характерно для второй фазы агрегации. У больных ИБС в самом начале процесса агрегации наблюдается образование крупных агрегатов. Таким образом, наличие однофазности агрегации тромбоцитов, образование крупных агрегатов позволяет предположить, что тромбоциты в плазме больных ИБС находятся в частично стимулированном состоянии. Гиперагрегация тромбоцитов не только способствует повышению вязкости крови, но и потенцирует микроциркуляторные нарушения за счет секреции вазоконстрикторных субстанций активированными тромбоцитами. Анализ агрегационной способности эритроцитов также показал преобладание процессов гиперагрегации. Гиперагрегация эритроцитов регистрировалась у 86% (60) больных во II группе и у 83% (29) в контрольной группе. СтА и СкА при этом составили 58,8±0,9 (p<0,001) и 20,2±0,7 (p<0,001) во II группе и 59,4±1,2 (p<0,001) и 19,8±0,9 (p<0,001) в группе контроля. Гипоагрегация эритроцитов регистрировалась у 8% (6) больных в I группе, СтА и СкА в этой группе больных составили 26,4±1,3 (p<0,001) и 10,1±0,9 (p<0,001) соответственно. В группе контроля гипоагрегация эритроцитов отмечена у 11% (4) больных, а СтА и СкА составили 27,2±1,4 (p<0,001) и 10,4±0,7 (p<0,001) соответственно. Нормальная агрегация эритроцитов регистрировалась у 6% (4) пациентов в I группе и у 6% (2) в контрольной группе. СтА и СкА в I группе составили 46,8±0,6 и 15,4±0,5 соответственно, а в группе контроля - 46,6±1,0 и 14,8±0,4 соответственно. Повышенная агрегация эритроцитов приводит к окклюзии прекапилляров и капилляров эритроцитарными агрегатами, медленному прохождению эритроцитов в узких участках русла, общему замедлению скорости периферического кровотока. Повышение агрегационной способности эритроцитов возможно обусловлено нарушением поверхностной архитектоники клеток, ухудшением их деформируемости. В физиологических условиях эритроциты способны значительно деформироваться, что имеет чрезвычайное значение для поддержания оптимальной диффузии газов. Способность эритроцитов видоизменять свою форму зависит от свойств мембраны. Потеря вязкоэластических свойств мембраны эритроцитов приводит к их диск-сферической трансформации и может быть одной из причин обеднения сети артериол и капилляров.
Таким образом, у больных ишемической болезнью сердца с сопутствующим сахарным диабетом 2 типа выявлены разнообразные нарушения в агрегационной способности тромбоцитов и эритроцитов с преимущественным преобладанием процессов гиперагрегации.
Так во II группе