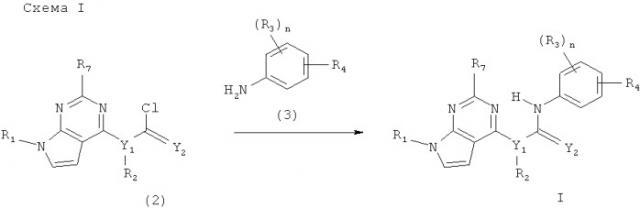
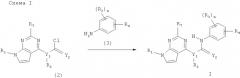
Соединения и композиции в качестве ингибиторов протеинкиназ
Иллюстрации
Показать всеИзобретение относится к новым соединениям формулы I и их фармацевтически приемлемым солям, обладающим ингибирующей активностью в отношении киназ, выбранных из Abl, Bcr-Abl, Bmx, ВТК, b-RAF, c-RAF, CSK, cSRC, Fes, FGFR3, Flt3, IKKα, IKKβ, JNK1α1, JNK2α2, Lck, Met, MKK4, MKK6, p70S6K, PAK2, PDGFRα, PKA, PKCα, PKD2, ROCK-II, Ros, Rsk1, SAPK2α, SAPK2β, SAPK3, SAPK4, SGK, Syk, Tie2 и TrkB. Соединения могут найти применение для лечения или профилактики заболеваний или нарушений, ассоциированных с аномальной или разрегулированной киназной активностью, таких как пролиферативные заболевания, заболевания иммунной и нервной системы. В соединениях формулы I
n равно 1, m равно 0, Y1 выбран из N и CR5, причем R5 представляет собой водород, Y2 представляет собой О, R1 представляет собой водород, R2 выбран из водорода и С1-С6алкила, R3 выбран из группы, включающей водород, C1-С6алкил, C1-С6алкокси, R4 выбран из -NR5C(O)R6 и -C(O)NR5R6, где R5 выбран из водорода и C1-C6алкила, а R6 представляет собой фенил, необязательно замещенный 1-3 радикалами, выбранными из группы, включающей NR5R5, галогензамещенный C1-С6алкил, C5-С6гетероарил(С0-С4)алкил, где гетероарил содержит 1-2 гетероатома, выбранных из N и О, C5-C6гетероцикло(С0-С4)алкил, где гетероциклил содержит 1-2 гетероатома N, и C5-С6гетероцикло(С0-С4)алкокси, где гетероциклил содержит 1-2 гетероатома N, причем любой гетероарил или гетероциклил в составе R6 необязательно замещен 1-3 радикалами, независимо выбранными из группы, включающей C1-С6алкил и гидрокси (C1-С6)алкил. 4 н. и 4 з.п. ф-лы.
Реферат
Предпосылки создания настоящего изобретения
Область изобретения
В настоящем изобретении предлагается новый класс соединений, фармацевтические композиции, включающие указанные соединения и способы применения указанных соединений для лечения или профилактики заболеваний или нарушений, ассоциированных с аномальной или разрегулированной киназной активностью, прежде всего заболеваний или нарушений, вызванных аномальной активацией киназ Abl, Bcr-Abl, Bmx, ВТК, b-RAF, c-RAF, CSK, cSRC, Fes, FGFR3, Flt3, IKKα, IKKβ, JNK1α1, JNK2α2, Lck, Met, MKK4, MKK6, p70S6K, PAK2, PDGFRα, PKA, PKCα, PKD2, ROCK-II, Ros, Rsk1, SAPK2α, SAPK2β, SAPK3, SAPK4, SGK, Syk, Tie2 и TrkB.
Протеинкиназы представляют собой многочисленное семейство белков, которые играют центральную роль в регуляции широкого круга клеточных процессов и в осуществлении контроля клеточных функций. Перечень таких киназ включает, без ограничения перечисленным, рецепторные тирозинкиназы, такие как рецепторная киназа тромбоцитарного фактора роста (PDGF-R), рецептор фактора роста нервов, trkB, Met, и рецептор фактора роста фибробластов, FGFR3; не-рецепторные тирозин киназы, такие как Abl и гибридная киназа BCR-Abl, Lck, Csk, Fes, Bmx и c-src, а также серин/треонинкиназы, такие как c-RAF, sgk, киназы MAP (например, МКК4, MKK6 и т.п.) и SAPK2α, SAPK2β и SAPK3. Аномальная активность киназ наблюдается при многих патологических состояниях, включая доброкачественные и злокачественные пролиферативные заболевания, а также заболевания, обусловленные аномальной активацией иммунной и нервной систем.
Новые соединения по настоящему изобретению ингибируют активность одной или более протеинкиназ и, следовательно, их можно использовать для лечения заболеваний, ассоциированных с киназами.
Краткое описание сущности изобретения
В одном объекте настоящего изобретения предлагаются соединения формулы I
где
n равно 0, 1 и 2,
m равно 0, 1 и 2,
Y1 выбирают из N и CR5, причем R5 выбирают из водорода и С1-С6алкила,
Y2 выбирают из О и S,
R1 выбирают из водорода и С1-C6алкила,
R2 выбирают из водорода и С1-С6алкила,
R3 выбирают из группы, включающей водород, галоген, гидрокси, С1-С6алкил, C1-С6алкокси, галогензамещенный C1-С6алкил и галогензамещенный C1-С6алкокси,
R4 выбирают из -NR5C(О)R6 и -C(О)NR5R6, где R5 выбирают из водорода и C1-С6алкила, а R6 выбирают из группы, включающей С6-С10арил(С0-С4)алкил, С5-С10гетероарил (С0-С4)алкил, С3-С10циклоалкил(С0-С4)алкил и С3-С10гетероциклоалкил(С0-С4)алкил, причем любой арил, гетероарил, циклоалкил или гетероциклоалкил в составе R6 необязательно замещен 1-3 радикалами, выбранными из группы, включающей галоген, гидрокси, -NR5R5, C1-С6алкил, C1-С6алкокси, галогензамещенный C1-С6алкил и галогензамещенный C1-С6алкокси, С5-С10гетероарил (С0-С4)алкил, С3-С8гетероцикло (С0-С4) алкил и С3-С8гетероцикло(С0-С4)алкокси, причем любой гетероарил или гетероциклоалкил в составе R6 необязательно замещен 1-3 радикалами, независимо выбранными из группы, включающей C1-С6 алкил и гидрокси(С1-С6)алкил,
R7 выбирают из группы, включающей водород, галоген, гидрокси, С1-С6алкил, C1-С6алкокси, галогензамещенный C1-С6алкил, галогензамещенный С1-С6алкокси, С6-С10арил(С0-С4)алкил, С3-С10гетероарил(С0-С4)алкил, С3-С10циклоалкил (С0-С4)алкил и С3-С10гетероциклоалкил(С0-С4)алкил, а также N-оксиды, пролекарства, защищенные производные, индивидуальные изомеры и смеси изомеров, а также фармацевтически приемлемые соли и сольваты (например, гидраты) таких соединений.
Во втором объекте настоящего изобретения предлагается фармацевтическая композиция, включающая соединение формулы I или N-оксид, индивидуальные изомеры и смеси изомеров, или их фармацевтически приемлемые соли, в смеси с одним или более пригодных эксципиентов.
В третьем объекте настоящего изобретения предлагается способ лечения заболевания у животного, который заключается в том, что при ингибировании киназной активности, прежде всего активности Abl, Bcr-Abl, Bmx, ВТК, b-RAF, c-RAF, CSK, cSRC, Fes, FGFR3, Flt3, IKKα, IKKβ, JNK1α1, JNK2α2, Lck, Met, МКК4, МКК6, p70S6K, PAK2, PDGFRα, PKA, PKCα, PKD2, ROCK-II, Ros, Rskl, SAPK2α, SAPK2β, SAPK3, SAPK4, SGK, Syk, Tie2 и/или TrkB, наблюдается предотвращение, подавление или снижение интенсивности заболевания и/или симптомов заболеваний, причем способ включает введение животному терапевтически эффективного количества соединения формулы I или N-оксида, индивидуальных изомеров и смеси изомеров, или их фармацевтически приемлемой соли.
В четвертом объекте настоящего изобретения предлагается применение соединения формулы I для получения лекарственного средства, предназначенного для лечения заболевания у животного, причем киназная активность, прежде всего активность Abl, Bcr-Abl, Bmx, ВТК, b-RAF, c-RAF, CSK, cSRC, Fes, FGFR3, Flt3, IKKα, IKKβ, JNK1α1, JNK2α2, Lck, Met, МКК4, МКК6, p70S6K, PAK2, PDGFRα, PKA, PKCα, PKD2, ROCK-II, Ros, Rsk1, SAPK2α, SAPK2β, SAPK3, SAPK4, SGK, Syk, Tie2 и/или TrkB, связана с развитием заболевания и/или симптомов заболевания.
В пятом объекте настоящего изобретения предлагается способ получения соединения формулы I и N-оксидов, пролекарств, защищенных производных, индивидуальных изомеров и смеси изомеров, а также фармацевтически приемлемых солей.
Подробное описание предпочтительных вариантов осуществления изобретения
Определение терминов
«Алкил» в качестве группы и структурного элемента других групп, например, галогензамещенный алкил и алкокси, является линейным или разветвленным. С1-С4алкокси включает метокси, этокси и т.п. Галогензамещенный алкил включает трифторметил, пентафторэтил и т.п.
«Арил» означает моноциклический или конденсированный бициклический ароматический цикл, содержащий 6-10 атомов углерода в цикле. Например, арил означает фенил или нафтил, предпочтительно фенил. «Арилен» означает двухвалентный радикал, производное арила.
«Гетероарил» имеет значения, определенные выше для арила, причем один или более атомов в цикле являются гетероатомами. Например, гетероарил включает пиридил, индолил, индазолил, хиноксалинил, хинолинил, бензофуранил, бензопиранил, бензотиопиранил, бензо[1,3]диоксол, имидазолил, бензимидазолил, пиримидинил, фуранил, оксазолил, изоксазолил, триазолил, тетразолил, пиразолил, тиенил и т.п.
«Циклоалкил» означает насыщенный или частично ненасыщенный, моноциклический, конденсированный бициклический или мостиковый полициклический цикл, содержащий указанное количество атомов в цикле. Например, С3-С10циклоалкил включает циклопропил, циклобутил, циклопентил, циклогексил и т.п.
«Гетероциклоалкил» означает циклоалкил, как определено в данном контексте, при условии, что один или более указанных атомов углерода в цикле заменены на группу, выбранную из следующих групп: -О-, -N=, -NR-, -С(О)-, -S-, -S(О)- или -S(О)2-, где R означает водород, С1-С4алкил или азотзащитную группу. Например, С3-С8гетероциклоалкил, использованный в данной заявке для описания соединений по настоящему изобретению, включает морфолино, пирролидинил, пирролидинил-2-он, пиперазинил, пиперидинил, пиперидинилон, 1,4-диокса-8-азаспиро[4.5]дец-8-ил и т.п.
«Галоген» предпочтительно означает хлор или фтор, но также может означать бром или иод.
«Панель киназ» включает следующие киназы: Abl (человека), Abl (T315I), JAK2, JAK3, ALK, JNK1α1, ALK4, KDR, Aurora-A, Lck, B1k, MAPK1, Bmx, MAPKAP-K2, BRK, MEK1, CaMKII (крысы). Met, CDK1/циклинВ, p70S6K, CHK2, PAK2, CK1, PDGFRα, CK2, PDK1, c-kit, Pim-2, c-RAF, РКА(человека), CSK, PKBα, cSrc, PKCα, DYRK2, Plk3, EGFR, ROCK-I, Fes, Ron, FGFR3, Ros, Flt3, SAPK2α, Fms, SGK, Fyn, SIK, GSK3β, IGF-1R, Tie-2, IKKβ, TrKB, IR, WNK3, IRAK4, ZAP-70, ITK, AMPK (крысы), LIMK1, Rsk2, Ax1, LKB1, SAPK2β, BrSK2, Lyn (человека), SAPK3, ВТК, МАРКАР-К3, SAPK4, KaMKIV, MARK1, Snk, CDK2/циклинА, MINK, SRPK1, CDK3/циклинЕ, МКК4(мыши), ТАК1, CDK5/p25, МКК6(человека), ТВК1, CDK6/циклинD3, MLCK, TrkA, CDK7/циклинН/МАТ1, MRCKβ, TSSK1, CHK1, MSK1, Yes, CK1d, MST2, ZIPK, c-Kit (D816V), MuSK, DAPK2, NEK2, DDR2, NEK6, DMPK, PAK4, DRAK1, PAR-1Bα, EphA1, PDGFRβ, EphA2, Pim-1, EphA5, PKBβ, EphB2, PKCβI, EphB4, PKCδ, FGFR1, РКСη, FGFR2, PKCθ, FGFR4, PKD2, Fgr, PKG1β, Fit1, PRK2, Hck, PYK2, HIPK2, Ret, IKKα, RIPK2, IRR, ROCK-II (человека), JNK2α2, Rse, JNK3, Rsk1 (человека), PI3 Kγ, PI3 Kδ и PI3-Кβ. Соединения по настоящему изобретению анализировали с использованием указанной панели киназ (дикий тип и/или мутантная форма), и полученные результаты свидетельствуют о том, что соединения ингибируют активность по крайней мере одной киназы из указанной панели.
"Мутантные формы BCR-Abl" означают замену одной или многих аминокислот в последовательности киназы дикого типа. Мутации в киназе BCR-ABL часто приводят к повреждению важных контактных участков между белком и ингибитором (например, ингибитором Gleevec, и т.п.), индуцируя переход из неактивного состояния в активное состояние, т.е. переход в конформацию, при которой BCR-ABL и Gleevec неспособны связываться. Анализ клинических случаев свидетельствует о том, что спектр мутаций, ассоциированных с устойчивым фенотипом, со временем медленно, но неуклонно увеличивается. По-видимому, мутации накапливаются в четырех основных фрагментах. Одна группа мутаций (G250E, Q252R, Y253F/H, E255K/V) включает аминокислоты, которые образуют фосфат-связывающую петлю для АТФ (известную также, как Р-петля). Вторая группа мутаций (V289A, F311L, T315I, F317L) обнаружена в участке связывания с ингибитором Gleevec и непосредственно взаимодействует с ингибитором за счет водородных связей и Вандер-Ваальсовых сил. Третья группа мутаций (М351Т, E355G) расположена вблизи каталитического домена. Четвертая группа мутаций (H396R/P) локализована в петле активации, конформация которой является молекулярным переключателем, регулирующим активацию/инактивацию киназной активности. Точечные мутации в BCR-ABL, ассоциированные с устойчивостью к ингибитору Gleevec, обнаруженные у пациентов с диагнозом CML и ALL, включают M224V, L248V, G250E, G250R, Q252R, Q252H, Y253H, Y253F, Е255К, E255V, D276G, Т277А, V289A, F311L, T315I, T315N, F317L, М343Т, М315Т, E355G, F359V, F359A, V379I, F382L, L387M, L387F, Н396Р, H396R, А397Р, S417Y, Е459К и F486S (положения аминокислот, указанных однобуквенным кодом, приводятся в соответствии с последовательностью, указанной в базе данных GenBank, номер ААВ60394, соответствующей ABL тип la, Martinelli и др., Haematologica/The Hematology Journal, 90-94, (2005, апрель). Если не указано иное, Bcr-Abl означает фермент дикого типа и его мутантные формы.
"Лечение" означает способ снижения или ослабления интенсивности заболевания и/или его симптомов.
Подробное описание предпочтительных вариантов осуществления настоящего изобретения
Гибридный белок BCR-Abl образуется в результате взаимной транслокации, которая гибридизует протоонкоген Abl с геном Bcr. Затем BCR-Abl трансформирует В-клетки благодаря увеличению митогенной активности. Такое увеличение активности приводит к снижению чувствительности к апоптозу, а также к изменению адгезии и хоминга клеток-предшественников CML (хронического миелолейкоза). В настоящем изобретении предлагаются соединения, композиции и способы лечения заболевания, ассоциированного с киназой, прежде всего заболеваний, ассоциированных с киназой Abl, Bcr-Abl, ВМХ, ВТК, b-RAF, c-RAF, CSK, c-SRC, Fes, FGFR3, Flt3, IKKa, IKKβ, JNK1α1, JNK2α2, Lck, Met, MKK4, MKK6, p70S6K, PAK2, PDGFRα, PKA, PKBα, PKD2, ROCK-II, Ros, Rsk1, SAPK2α, SAPK2β, SAPK3, SGK, Syk, Tie2 и TrkB. Например, лейкоз и другие пролиферативные заболевания, ассоциированные с Bcr-Abl, можно лечить при ингибировании киназы Bcr-Abl дикого типа и ее мутантных форм.
В одном варианте осуществления изобретения соединение формулы I означает соединение формулы Ia,
где
n равно 0 и 1,
Y1 выбирают из N и СН,
Y2 выбирают из О и S,
R1 выбирают из водорода и C1-С6алкила,
R2 выбирают из водорода и C1-С6алкила,
R3 выбирают из следующих групп: водород, галоген, гидрокси, С1-С6алкил, C1-С6алкокси, галогензамещенный C1-С6алкил и галогензамещенный C1-С6алкокси,
R4 выбирают из -NR5C(O)R6 и -C(O)NR5R6, где R5 выбирают из водорода и C1-С6алкила, a R6 выбирают из следующих групп: С6-С10арил(С0-С4)алкил, С5-С10гетероарил(С0-С4)алкил, С3-С10циклоалкил(С0-С4)алкил и С3-С10гетероциклоалкил(С0-С4)алкил, причем любой арил, гетероарил, циклоалкил или гетероциклоалкил в составе R6 необязательно замещен 1-3 радикалами, выбранными из группы, включающей галоген, гидрокси, -NR5R5, C1-С6алкил, C1-С6алкокси, галогензамещенный C1-С6алкил, галогензамещенный C1-С6алкокси, С5-С10гетероарил(С0-С4)алкил, С3-С8гетероцикло(С0-С4)алкил и С3-С8гетероцикло(С0-С4)алкокси, причем любой гетероарил или гетероциклоалкил в составе R6 необязательно замещен 1-3 радикалами, независимо выбранными из группы, включающей C1-С6алкил и гидрокси (С1-С6)алкил.
В другом варианте R2 выбирают из водорода и метила, а R3 выбирают из метила и метокси.
В другом варианте R4 выбирают из -NHC(O)R6 и -C(O)NHR6, где R6 выбирают из фенила, необязательно замещенного 1-3 радикалами, выбранными из группы, включающей трифторметил, диметиламино, имидазолил, морфолино, морфолинометил, пиперазинил, пиперазинилметил и пирролидинилметокси, причем указанные имидазолил, пиперазинил, пиперазинилметил необязательно замещены группой, выбранной из метила, этила и гидроксиэтила.
Предпочтительные соединения по настоящему изобретению выбирают из группы, включающей N-[4-(4-этилпиперазин-1-илметил)-3-трифторметилфенил]-4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]бензамид, 4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]-N-(4-пиперазин-1-илметил-3-трифторметилфенил)бензамид, 3-(4-метилимидазол-1-ил)-N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-5-трифторметилбензамид, N-[4-метил-3-(2-7Н-пирроло[2,3-d]пиримидин-4-илацетиламино)фенил]-3-трифторметилбензамид, N-(3-имидазол-1-ил-5-трифторметилфенил)-4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]бензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-трифторметилбензамид, 4-(2-метилимидазол-1-ил)-N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-4-морфолин-4-ил-3-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-4-(4-метилпиперазин-1-илметил)-3-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-4-морфолин-4-илметил-3-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-(1]пиримидин-4-ил)уреидо]фенил}-3-морфолин-4-ил-5-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-4-(4-метилпиперазин-1-ил)-3-трифторметилбензамид, 4-(4-этилпиперазин-1-ил)-N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-(4-метилпиперазин-1-ил)-5-трифторметилбензамид, 3-диметиламино-N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-5-трифторметилбензамид, 4-(4-этилпиперазин-1-илметил)-N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-трифторметилбензамид, 3-(4-этилпиперазин-1-ил)-N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-5-трифторметилбензамид, 4-метил-[3-(4-метилимидазол-1-ил)-5-трифторметилфенил]-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]бензамид, 3-[4-(2-гидроксиэтил)пиперазин-1-ил]-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-5-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7H-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-пиперазин-l-ил-5-трифторметилбензамид, N-{4-метил-3-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-(пирролидин-2-илметокси)-5-трифторметилбензамид, N-{3-метокси-5-[3-метил-3-(7H-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-морфолин-4-ил-5-трифторметилбензамид, N-{3-метокси-5-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-(4-метилимидазол-1-ил)-5-трифторметилбензамид, 4-(4-этилпиперазин-1-илметил)-N-{3-метокси-5-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-3-трифторметилбензамид, N-{3-метокси-5-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-4-(4-метилпиперазин-1-илметил)-3-трифторметилбензамид и N-{3-метокси-5-[3-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-ил)уреидо]фенил}-4-(2-метилимидазол-1-ил)-3-трифторметилбензамид.
Другие предпочтительные соединения по изобретению подробно описаны в примерах и таблице 1.
Фармакология и промышленная применимость
Соединения по изобретению модулируют активность киназ и как таковые используются для лечения заболеваний или нарушений, при которых киназы принимают участие в развитии патологии и/или симптоматике заболевания. Примеры киназ, которые ингибируются соединениями и композициями, описанными в данном контексте, и для подавления которых используются методы, описанные в данном контексте, включают, без ограничения перечисленным, Abl и Bcr-Abl.
Тирозинкиназа Абельсона (т.е. Abl, с-Abl) принимает участие в регуляции клеточного цикла, в клеточном ответе на генотоксический стресс и в передаче информации о клеточном окружении через интегриновый сигнал. Таким образом белок Abl выполняет сложную функцию в качестве клеточного модуля, который интегрирует сигналы от различных межклеточных и внутриклеточных источников, что оказывает влияние на принятие решений относительно клеточного цикла и апоптоза. Тирозинкиназа Абельсона включает подтипы, такие как химерный гибридный белок (онкопротеин) BCR-Abl с разрегулированной тирозинкиназной активностью или v-Abl. BCR-Abl играет решающую роль в патогенезе в 95% случаев хронического миелогенного лейкоза (CML) и в 10% случаев острого лимфолейкоза. STI-571 (Gleevec) является ингибитором онкогенной тирозинкиназы BCR-Abl и используется при лечениии хронического миелоидного лийкоза (CML). Однако у некоторых пациентов на стадии бластного криза CML наблюдается устойчивость к STI-571 из-за мутаций в киназе BCR-Abl. К настоящему времени идентифицировано 22 мутации, наиболее частыми из которых являются G250E, E255V, T315I, F317L и М351Т.
Соединения по настоящему изобретению ингибируют киназу abl, прежде всего киназу v-abl. Соединения по настоящему изобретению также ингибируют дикий тип киназы BCR-Abl и мутированные формы киназы BCR-Abl и, следовательно, пригодны для лечения Bcr-abl-позитивного рака и опухолевых заболеваний, таких как лейкоз (прежде всего хронический миелоидный лейкоз и острый лимфолейкоз, при развитии которых прежде всего установлен апоптотический механизм действия), а также оказывают действие на подгруппу лейкозных стволовых клеток и могут использоваться для очистки этих клеток in vitro после их удаления из организма (например, удаления костного мозга) и реплантации популяции клеток, очищенных от раковых клеток (например, реплантации очищенных клеток костного мозга).
Сигнальный путь Ras-Raf-MEK-ERK опосредует клеточный ответ на ростовые сигналы. Ras мутирован в онкогенную форму в ~15% случаев рака человека. Семейство Raf относится к семейству серин/треонинпротеинкиназ и включает три члена семейства A-Raf, B-Rafn c-Raf(или Raf-1). Исследование Raf как мишени лекарственных средств направлено на изучение действия Raf в качестве подавляющего эффектора на Ras. Однако полученные недавно данные свидетельствуют о том, что B-Raf выполняет важную функцию в образованиия некоторых опухолей без обязательного участия активированной аллели Ras (Nature, 417, 949-954 (01 июля 2002)). Мутации B-Raf прежде всего обнаружены в большинстве злокачественных меланом.
Существующие методы лечения меланомы характеризуются недостаточной эффективностью, прежде всего на поздней стадии заболевания. Соединения по настоящему изобретению ингибируют также клеточные процессы с участием киназы b-Raf и представляют собой новый терапевтически подход к лечению рака человека, прежде всего меланомы.
Соединения по настоящему изобретению кроме того ингибируют клеточные процессы с участием киназы c-Raf. c-Raf активируется онкогеном ras, который мутирован при многих видах рака человека. Следовательно, ингибирование киназной активности c-Raf представляет собой перспективный способ предотвращения роста опухоли, опосредованного геном ras (Campbell S.L., Oncogene, 17, 1395 (1998)).
PDGF (фактор роста тромбоцитов) представляет собой очень распространенный ростовой фактор, который играет важную роль как в процессе нормального роста, так и в патологической клеточной пролиферации, например, которая наблюдается при онкогенезе и при заболеваниях клеток гладкой мускулатуры кровеносных сосудов, например при атеросклерозе и тромбозе. Соединения по изобретению ингибируют активность рецептора PDGF (PDGFR) и, следовательно, могут использоваться при лечении опухолевых заболеваний, таких как глиома, саркома, рак предстательной железы и рак ободочной кишки, молочной железы и яичника.
Соединения по настоящему изобретению можно использовать не только в качестве подавляющих опухоль агентов, например при мелкоклеточном раке легких, но и в качестве агента для лечения незлокачественных пролиферативных нарушений, таких как атеросклероз, тромбоз, псориаз, склеродерма и фиброз, а также для защиты стволовых клеток, например, для борьбы с гемотоксическим действием химиотерапевтических агентов, таких как 5-фторурацил, и для лечения астмы. Соединения по изобретению прежде всего можно использовать для лечения заболеваний, которые чувствительны к ингибированию рецепторной киназы PDGF.
Соединения по настоящему изобретению оказывают лечебное действие при лечении нарушений, возникающих в результате трансплантации, например аллогенной трансплантации, прежде всего при отторжении тканей, таких как прежде всего облитерирующий бронхиолит (OB), т.е. хроническое отторжение аллогенных трансплантатов легкого. В отличие от пациентов, не страдающих от OB, у пациентов с диагнозом OB часто наблюдается повышенная концентрация PDGF в бронхоальвеолярной промывной жидкости.
Соединения по настоящему изобретению также являются эффективными при заболеваниях, ассоциированных с миграцией и пролиферацией клеток гладкой мускулатуры сосудов (при которых PDGF и PDGF-R часто играют заметную роль), таких как рестеноз и атеросклероз. Такое воздействие и его последующее влияние на пролиферацию и миграцию клеток гладкой мускулатуры сосудов in vitro и in vivo можно оценивать при введении соединений по настоящему изобретению, а также при исследовании воздействия на утолщение внутренней оболочки сосудов после механического повреждения in vivo.
Семейство trk рецепторов нейтрофина (trkA, trkB, trkC) стимулирует выживание, рост и дифференциацию нейронных и ненейронных тканей. Белок TrkB экспрессируется в клетках нейроэндокринного типа в тонкой кишке и ободочной кишке, в α-клетках поджелудочной железы, в моноцитах и макрофагах лимфатических узлов и селезенки, и в гранулярных слоях эпидермиса (Shibayama и Koizumi, 1996). Экспрессия белка TrkB ассоциируется с неблагоприятным прогнозом и прогрессированием опухолей Вилмса и нейробластомы. Более того, TkrB экспрессируется в злокачественных клетках предстательной железы, но не обнаруживается в нормальных клетках. Сигнальный путь подавления (экспрессии) рецепторов trk включает каскад активации МАРК с участием Shc, активированного Ras, генов ERK-1 и ERK-2, и пути трансдукции PLC-γ1 (Sugimoto и др., 2001).
Киназа c-Src передает онкогенные сигналы многих рецепторов. Например, сверхэкспрессия EGFR или HER2/neu в опухолях приводит к конститутивной активации c-src, что является характеристикой злокачественных клеток, но не наблюдается в нормальных клетках. С другой стороны, мыши с дефицитом экспрессии c-src представляют собой фенотип «мраморной болезни», что свидетельствует о ключевой роли c-src в функционировании остеокластов и возможном участии в развитии ассоциированных нарушений.
Киназа семейства Tec, Bmx, не-рецепторная протеинтирозинкиназа, контролирует пролиферацию эпителиальных раковых клеток молочной железы.
Установлено, что рецептор 3 фактора роста фибробластов обладает отрицательным регуляторным действием на рост костной ткани и ингибирование пролиферации хондроцитов. Летальная дисплазия вызывается различными мутациями в рецепторе 3 фактора роста фибробластов, а одна мутация, TDII FGFR3, обладает конститутивной тирозинкиназной активностью, которая активирует фактор транскрипции Stal1, что приводит к экспрессии ингибитора клеточного цикла, остановке роста и аномальному развитию костной ткани (Su и др., Nature, 386, 288-292 (1997)). Кроме того, FGFR3 часто экспрессируется в опухолях типа множественной миеломы. Ингибиторы активности FGFR3 можно использовать для лечения воспалительных или аутоиммунных заболеваний, опосредованных Т-клетками, включающих, без ограничения перечисленным, ревматоидный артрит (RA), коллагеновый артрит II, рассеянный склероз (МС:), системную красную вочанку (SLE), псориаз, юношеский диабет, болезнь Шенгрена, заболевание щитовидной железы, саркоидоз, аутоиммунный увеит, воспалительное заболевание кишечника (болезнь Крона и язвенный колит), глютеновую болезнь и тяжелую псевдопаралитическую миастению.
Активность сывороточной и глюкокортикоид-регулируемой киназы (SGK) коррелирует с активностями возмущенных ионных каналов, прежде всего активностью натриевых и/или калиевых каналов, и соединения по изобретению можно использовать для лечения гипертензии.
В работах Lin и др., J. Clin. Invest. 100, 8, 2072-2078 (1997) и Р.Lin, PNAS, 95, 8829-8834 (1998) установлено подавление роста опухоли и васкуляризации, а также снижение метастазирования в легких при аденовирусных инфекциях или при инъекциях внеклеточного домена Tie-2 (Tek) в опухоли молочной железы и модели ксенотрансплантата меланомы. Ингибиторы Tie2 можно использовать в случаях, при которых наблюдается аномальная неоваскуляризация (например, при диабетической ретинопатии, хроническом воспалении, псориазе, саркоме Капоши, хронической неоваскуляризации при дегенерации желтого пятна, ревматоидном артрите, инфантильной гемангиоме и раке).
Lck принимает участие в передаче сигнала Т-клетками. У мышей с отсутствием гена Lck наблюдается низкий уровень тимоцитов. Функция Lck в качестве положительного активатора передачи сигнала Т-клетками свидетельствует о том, что ингибиторы Lck можно использовать для лечения аутоиммунного заболевания, такого как ревматоидный артрит.
Киназы JNK и другие МАРК принимают участие в опосредовании клеточного ответа на рак, тромбин-индуцированную агрегацию тромбоцитов, нарушения типа иммунодефицита, аутоиммунные заболевания, гибель клеток, аллергию, остеопороз и болезнь сердца. Терапевтические мишени, связанные с активацией пути JNK, включают хронический миелогенный лейкоз (CML), ревматоидный артрит, астму, остеоартрит, ишемию, рак и нейродегенеративные заболевания. В связи с активацией JNK, ассоциированной с заболеванием печени или приступами гепатической ишемии, соединения по изобретению можно также использовать для лечения различных нарушений функции печени. Сообщается также об участии JNK в развитии сердечно-сосудистого заболевания, такого как инфаркт миокарда или застойная сердечная недостаточность, а также установлено, что JNK опосредует гипертрофические ответные реакции на различные формы сердечного стресса. Установлено, что каскад JNK принимает участие в активации Т-клеток, включая активацию промотора IL-2. Таким образом, ингибиторы JNK могут оказывать лечебное действие при коррекции патологических ответных иммунных реакций. Установлена также роль активации JNK при развитии различных видов рака, что свидетельствует о возможности эффективного использования ингибиторов JNK при заболевании раком. Например, конститутивно активируемая JNK ассоциируется с онкогенезом, опосредованным HTLV-1 (Oncogene, 13, 135-142 (1996)). JNK принимает участие в развитии саркомы Капоши (KS). Пролиферативное действие других цитокинов, принимающих участие в пролиферации KS, таких как эндотелиальный фактор роста сосудов (VEGF), IL-6 и TNFa, также может оказаться опосредованным JNK. Кроме того, регуляция гена c-jun в клетках р210, трансформированных BCR-ABL, соответствует активности JNK, что свидетельствует о возможности применения ингибиторов JNK при лечении хронического миелогенного лейкоза (CML) (Blood 92, 2450-2460 (1998)).
Принято считать, что некоторые аномальные пролиферативные состояния ассоциированы с экспрессией raf и, следовательно, чувствительны к ингибированию экспресии raf. Аномально высокие уровни экспрессии белка raf также связаны с трансформацией и аномальной пролиферацией клеток. Предполагается также, что указанные аномальные пролиферативные состояния чувствительны к ингибированию экспрессии raf. Например, предполагается, что экспрессия белка c-raf играет роль в аномальной клеточной пролиферации, поскольку сообщается, что 60% всех клеточных линий карциномы легкого экспрессируют необычно высокий уровень мРНК и белка c-raf. Другими примерами аномальных пролиферативных состояний являются гиперпролиферативные нарушения, такие как рак, опухоли, гиперплазия, фиброз легких, ангиогенез, псориаз, атеросклероз и пролиферация клеток гладкой мускулатуры кровеносных сосудов, такие как стеноз или рестеноз после пластической операции на сосудах. Клеточный сигнальный путь, частью которого является raf, также принимает участие в воспалительных нарушениях, характеризующихся пролиферацией Т-клеток (активация и рост Т-клеток), таких, например, как отторжение тканевого трансплантата, эндотоксиновый шок и гломерулярный нефрит.
Стресс-активируемые протеинкиназы (SAPK) представляют собой семейство протеинкиназ, которые принимают участие на предпоследней стадии пути передачи сигнала, при этом происходит активация фактора транскрипции с-jun и экспрессия генов, регулируемых c-jun. Прежде всего c-jun принимает участие в транскрипции генов, которые кодируют белки, связанные с репарацией ДНК, поврежденной вследствие генотоксических эффектов. Следовательно, агенты, которые ингибируют активность SAPK в клетке, предотвращают репарацию ДНК и сенсибилизируют клетку к агентам, которые индуцируют повреждение ДНК или ингибируют синтез ДНК и индуцируют апоптоз клетки, или к агентам, которые ингибируют клеточную пролиферацию.
Митоген-активируемые протеинкиназы (МАРК) являются членами консервативных путей передачи сигнала, которые активируют факторы транскрипции, факторы трансляции и другие молекулы-мишени в ответ на различные внеклеточные сигналы. МАРК активируются митоген-активируемыми протеинкиназами (МКК) за счет двойного фосфорилирования по двум аминокислотам в последовательности Thr-X-Tyr. У высших эукариотов физиологическая роль передачи сигнала МАРК коррелирует с клеточными процессами, такими как пролиферация, онкогенез, развитие и дифференциация. Соответственно, способность регулировать передачу сигнала по указанным путям (прежде всего с участием МКК4 и МКК6) можно использовать при разработке способов лечения и профилактики заболеваний человека, ассоциированных с передачей сигнала МАРК, таких как воспалительные заболевания, аутоиммунные заболевания и рак.
Семейство протенкиназ рибосомального белка S6 человека включает по крайней мере 8 членов (RSK1, RSK2, RSK3, RSK4, MSK1, MSK2, p70S6K и p70S6 Kb). Протеинкиназы рибосомального белка S6 выполняют важные плеотропные функции, в том числе играют ключевую роль в регуляции трансляции мРНК при биосинтезе белка (Eur. J. Biochem., 267(21), 6321-6330 (2000, ноябрь); Exp Cell Res., 253 (1), 100-109 (1999, 25 ноября); Mol Cell Endocr1nol., 151(1-2), 65-77 (1999, 25 мая)). Кроме того, фосфорилирование рибосомального белка S6 киназой p70S6 связано с регуляцией клеточной подвижности (Immunol. Cell B1ol., 78(4), 447-451 (2000, август)) и клеточного роста (Prog. Nucle1c Ac1d Res. Mol. Biol., 65, 101-127 (2000)), и, следовательно, является важным фактором при метастазировании опухоли, иммунном ответе и репарации ткани, а также при других патологических состояниях.
Киназы SAPK (называемые также "jun N-концевые киназы" или "JNK") представляют собой семейство протеинкиназ, которые принимают участие на предпоследней стадии пути передачи сигнала, при этом происходит активация фактора транскрипции c-jun и экспрессия генов, регулируемых c-jun. Прежде всего c-jun принимает участие в транскрипции генов, которые кодируют белки, связанные с репарацией ДНК, поврежденной вследствие генотоксических эффектов. Агенты, которые ингибируют активность SAPK в клетке, предотвращают репарацию ДНК и сенсибилизируют клетку к таким терапевтическим противоопухолевым агентам, которые оказывают действие за счет индуцирования повреждения ДНК.
ВТК играют важную роль в развитии аутоиммунного и/или воспалительного заболевания, такого как системная красная волчанка (SLE), ревматоидный артрит, рассеянный васкулит, идиопатическая тромбоцитопеническая пурпура (ITP), тяжелая псевдопаралитическая миастения и астма. Благодаря участию ВТК в активации В-клеток, ингибиторы ВТК можно использовать для подавления патогенных состояний, опосредованных В-клетками, таких как продуцирование аутоантител, и при лечении лимфомы и лейкоза В-клеток.
СНК2 является киназой контрольных точек семейства серин/треонинпротеинкиназ и принимает участие в механизме контроля повреждений ДНК, таких как повреждения, вызванные мутагенами окружающей среды и эндогенными видами активного кислорода. В результате, ее можно использовать в качестве супрессора опухоли и мишени при онкотерапии.
CSK влияет на метастазирующую активность опухолевых клеток, прежде всего рака ободочной кишки.
Fes является не-рецепторной протеинтирозинкиназой, которая принимает участие в ряде путей передачи сигнала с участием цитокинов, а также дифференциации миелоидных клеток. Fes является также ключевым компонентом в механизме дифференциации гранулоцитов.
Рецепторная тирозинкиназа Flt3 принимает участие в развитии лейкоза и миелодиспластического синдрома. Приблизительно 25% клеток лейкоза AML экспрессируют конститутивно активную форму аутофосфорилированной тирозинкиназы (ф)FLT3 на клеточной поверхности. Активность ф-FLT3 обеспечивает рост и выживание предпочтительно лейкозных клеток. Пациенты с острым лейкозом, у которых лейкозные клетки экспрессируют киназу ф-FLT3, в основном характеризуются неблагоприятным клиническим прогнозом. Ингибирование киназы ф-FLT3 индуцирует апоптоз (программируемую гибель клеток) лейкозных клеток.
Ингибиторы IKKα и IKKβ (1 и 2) являются лекарственными средствами для лечения заболеваний, включающих ревматоидный артрит, отторжение трансплантата, воспалительное заболевание кишечника, остеоартрит, астму, хроническое обструктивное заболевание легких, атеросклероз, псориаз, рассеянный склероз, инсульт, системную красную волчанку, болезнь Альцгеймера, ишемию головного мозга, травматическое повреждение мозга, болезнь Паркинсона, боковой амиотрофический склероз, субарахноидальное кровоизлияние и другие заболевания или нарушения, ассоциированные с избыточным продуцированном воспалительных медиаторов в головном мозге и центральной нервной системе.
Met ассоциируется с большинством типов основных раков человека и экспрессия этого фермента часто коррелирует с неблагоприятным прогнозом и метастазированием. Ингибиторы Met являются лекарственными средствами для лечения заболеваний, включающих различные виды рака, такие как рак легких, NSCLC (немелкоклеточный рак легких), рак костной ткани, рак поджелудочной железы, рак кожи, рак головы и шеи, кожная и внутриглазная меланома, рак матки, рак яичника, ректальный рак, рак анальной области, рак желудка, рак ободочной кишки, рак молочой железы, гинекологические опухоли (например, саркома матки, карцинома маточных труб, карцинома эндометрия, карцинома шейки матки, карцинома влагалища или карцинома вульвы), болезнь Ходжкина, рак пищевода, рак тонкой кишки, рак эндокринной системы (например, рак щитовидной железы, паратиреоидный рак или рак надпочечников), саркомы мягких тканей, рак мочеиспускательного канала, рак пениса, рак предстательной железы, хронический или острый лейкоз, детские солидные опухоли, лимфоцитарные лимфомы, рак мочевого пузыря, рак почек или мочеточника (например, почечноклеточный рак, карцинома почечного пелвиса), детские злокачественные заболевания, опухоли центральной нервой системы (например, первичная лимфома ЦНС, опухоли позвоночника, глиома мозгового ствола или гипофизарная аденома), рак крови, такой как острый миелоидный лейкоз, хронический миелоидны