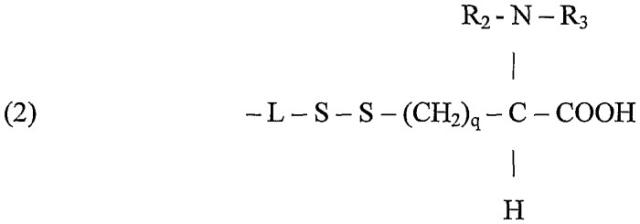Противомикробное средство, содержащее цистеиновое соединение, ковалентно связанное с субстратом, в частности, связыванием при помощи s-s мостика через спейсерную молекулу
Иллюстрации
Показать всеИзобретение относится к противомикробному средству. Противомикробное средство. Способ предотвращения или ингибирования роста и/или пролиферации грамположительных бактерий и/или грамотрицательных бактерий. Субстрат, который входит в контакт с микроорганизмами и/или который желательно должен быть свободным от аккумуляции и/или адгезиии микроорганизмов. Применение противомикробного средства. Набор составных частей для применения в обработке поверхности устройства противомикробным агентом. Способ изготовления противомикробного устройства. Вышеописанное средство обладает эффективным противомикробным действием и может быть применено для покрытия поверхностей и субстратов различных устройств, таких как медицинские устройства и устройства, применяемые для обработки пищевых продуктов, для предотвращения или ингибирования аккумулирования и/или роста и/или пролиферации и/или жизнеспособности микроорганизмов и/или образования биопленки. 6 н. и 7 з.п. ф-лы, 1 табл.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к противомикробным средствам или устройствам, которые контактируют с микроорганизмами и/или которые желательно содержать свободными от аккумулирования и/или адгезии микроорганизмов. Субстрат или поверхность устройства проявляет противомикробное средство изобретения.
Уровень техники
В различных ситуациях и применениях, например при медицинском обслуживании, пищевой обработке и хранении пищи, важно, чтобы устройства и продукты, которые используют, были свободными от роста или пролиферации микроорганизмов. Не в меньшей степени это чрезвычайно важно по отношению к медицинским устройствам, которые вводятся в контакт с пациентами в госпитале, так как зараженные устройства могут участвовать в распространении заболевания и микроорганизмов, что может серьезно повлиять на здоровье многих пациентов.
Например, было бы очень полезно, если бы устройства и продукты, которые контактируют с потенциально вредными микроорганизмами, обладали способностью ингибировать или уничтожать бактерии и/или другие микроорганизмы, такие как вирусы и грибки, чтобы препятствовать распространению заболеваний.
Задача состоит в предотвращении начальной колонизации, которая впоследствии может создать биопленку. Начальная фаза колонизации может быть подавлена либо ингибированием, либо уничтожением микроорганизмов.
Известно, что для получения такой защиты поверхность в устройстве снабжают ионами металлов, такими как ионы элементов Ag и Ni. Часто Ag используют в виде сплава для высвобождения Ag+-ионов с подходящей скоростью в окружающую среду, таким путем предотвращают аккумулирование микроорганизмов.
Однако одной из проблем данного решения является адгезия металла или сплава на рассматриваемой поверхности. Кроме того, противомикробное действие нелегко контролируется, и дополнительно поверхность, покрытая ионами металла, может проявлять цитотоксические эффекты.
US-А-6475434 раскрывает проникающую через биопленку композицию для удаления биопленок, образованных и состоящих из инфекционных микроорганизмов, а также для покрытия медицинских устройств с целью предотвращения образования таких биопленок. Композиция содержит цистеин и их аналоги или производные, предназначенные для выбора в качестве одного из компонентов. Роль цистеина или компонента, родственного цистеину, не ясна, и особенно для применений для покрытий они используются в комбинации с известными противомикробными средствами, такими как рифамицины, тетрациклины и пенициллины. То есть, как показано в примерах 2 и 3 в US-А-6475434, единственный цистеиновый испытанный компонент (который представляет собой N-ацетилцистеин) не проявляет эффекта, если не объединен с испытанными антибиотиками. Кроме того, для биопленочной защиты все компоненты наносят пропиткой устройства или смешиванием с материалом устройства в процессе производства. Компоненты затем становятся физически связанными адгезией и проникновением в материал устройства, что означает, что их функция в большой степени имеет место при их высвобождении в окружающую среду. Особенно при применении в медицине такие концепции требуют точного контроля баланса между противомикробным, цитотоксическим и иммуногенным эффектами. Так как диффузия является зависимой от времени и температуры, то хранение и долговечность устройств с покрытием также становятся проблемами для серьезного рассмотрения.
Авторами Olofsson et al. (Applied and Environmental Microbiology, August 2003; 69(8), 4814-4822) описано, что N-ацетилцистеин может влиять на бактериальный рост в растворе. Другие эффекты N-ацетилцистеина состояли в уменьшении адгезии бактерий многих видов на поверхностях нержавеющей стали или облегчении прикрепления биопленки на поверхностях нержавеющей стали.
Главная цель данного изобретения состоит в обеспечении противомикробного средства, обладающего способностью предотвращать или, по меньшей мере, значительно уменьшать аккумулирование и/или адгезию индивидуальных микроорганизмов на поверхности устройства стабильным и долговременным способом.
Данная цель осуществляется согласно первому аспекту изобретения, относящемуся к противомикробному средству, содержащему субстрат с ковалентно связанным цистеиновым соединением.
В частности, изобретение относится к противомикробному средству, в котором цистеиновое соединение присоединено при помощи S-S мостика через спейсерную молекулу с субстратом. Спейсер содержит углеродную цепь, необязательно прерванную одним или несколькими гетероатомами, например, O, S, N, P или Si, и цепь необязательно замещена одной или несколькими алкильными группами, предпочтительно низшими алкильными группами с 1-6 атомами углерода, гидроксильными группами или алкоксигруппами. В примерах, представленных ниже, цистеиновое соединение присоединено в терминальном положении спейсера при помощи S-S мостика, что представляет собой предпочтительный вариант осуществления изобретения. Однако возможны также другие положения в спейсерной цепи, поскольку цистеиновая функция подвержена действию окружающей среды.
Согласно предпочтительному варианту осуществления изобретения цистеинсодержащий лиганд, присоединенный к субстрату, имеет общую формулу:
(1) R1-X-L-S-S-(цистеиновый компонент)
в которой
- R1 представляет собой растворимый или нерастворимый субстрат; например твердую поверхность или растворимую органическую молекулу или полимер;
- X представляет собой связывающую группу от реакции конденсации между субстратом и L;
- L представляет собой спейсерную молекулу, выбранную из группы, содержащей (СН2)m, где m равно 1-20, предпочтительно 1-12, 1-8 или 1-6; (СН2СН2О)n(СН2)р или (СН(СН3)СН2О)n(СН2)р, где n равно 1-1000, предпочтительно 1-100 или 3-50, и р равно 1-20, предпочтительно 1-12, 1-10 или 1-6. Сегмент (СН2)р присоединен к дисульфидному мостику, но может необязательно также находиться между сегментами (СН2СН2О)n и/или (СН(СН3)СН2О)n в блок-сополимере;
- цистеиновый компонент в данном описании относится к остатку цистеинового соединения, включающего цистеин, аналог цистеина или цистеиновое производное, обеспечивающее противомикробную активность, которая по существу одинакова или имеет сравнимый уровень с активностью, сопоставимой с цистеином. Отмечено, что вариант осуществления изобретения, где цистеиновое соединение присоединено при помощи S-S мостика, содержащего одну S из тиольной группы цистеина и одну S из спейсерной молекулы, имеет особое значение, по меньшей мере, в некоторых применениях из-за его исключительной противомикробной активности.
Таким образом, предлагается противомикробное средство, которое ковалентно присоединено к поверхности устройства и которое вследствие исключительно полезных эффектов ковалентно связанного цистеина проявляет высокое и длительное воздействие, смотрите примеры, представленные ниже, на индивидуальные микроорганизмы, и тем самым предотвращает или по существу ингибирует адгезию и аккумулирование индивидуальных микроорганизмов. Таким образом, данное изобретение представляет огромный потенциал для всех применений, где желательно, если поверхность или субстрат будут проявлять противомикробные/антибактериальные свойства. Дополнительное и существенное преимущество изобретения, как показано заявителями, состоит в том, что средство изобретения показывает отсутствие цитотоксических эффектов, что делает его полезным во многих различных применениях.
В одном из аспектов данного изобретения различные устройства, которые желательно содержать свободными от аккумулирования и/или адгезии микроорганизмов, покрывают полностью или частично противомикробным средством согласно изобретению.
В дополнительном аспекте данное изобретение относится к применению противомикробного средства изобретения для предотвращения роста и/или пролиферации микроорганизмов на субстрате и/или поверхности устройства.
В противоположность US-A-6475434 в данном изобретении предлагается способ, чтобы получить цистеин или родственный цистеину компонент, ковалентно присоединенный к субстрату. Основное применение изобретения состоит в обеспечении противомикробного покрытия на твердом устройстве. По данной концепции противомикробные средства перманентно прикреплены к поверхности и противомикробный эффект имеет место при поверхностном контакте, а не от реакции с высвобождаемыми средствами, что будет в большой степени снижать риск вредных воздействий в биологической окружающей среде. Это представляет собой главное отличие по сравнению с ранее известными способами в данной области в тех случаях, когда цистеин предложен в качестве такого высвобождаемого средства. Кроме того, ковалентным присоединением поверхность может быть сделана более специфической через концентрацию поверхности и химическую структуру. Таким образом, не только поверхностно связанный цистеин или цистеиновый родственный компонент сам по себе, но, по меньшей мере, в некоторых применениях также и дисульфидная связь, с помощью которой он прикреплен к поверхности, представляет собой одну из изобретенных особенностей данной концепции относительно противомикробного эффекта. Кроме того, ковалентное присоединение обеспечивает поверхность, которая в месте нахождения, а также при хранении является исключительной по консистенции и долговечности по сравнению с поверхностями, где диффузия и утечка активных средств представляют собой главную проблему.
“Противомикробное средство” включает субстрат, который модифицирован для проявления ковалентно связанного цистеинового компонента и оказывает влияние на предупреждение или, по меньшей мере, значительно на предотвращение аккумулирования и/или пролиферации, по меньшей мере, одного специфического микроорганизма. Данный эффект можно наблюдать, например, в способах, известных в данной области, например способах, использованных в разделе, где описаны примеры настоящего описания.
“Цистеиновый компонент” включает остаток цистеина, цистеиновый аналог или цистеиновое производное с наличием противомикробного эффекта, например гомоцистеин или N-замещенные цистеины, такие как N-ацетил-L-цистеин и N-алкилированные цистеины.
“Субстрат” (R1) включает любое изделие, устройство, молекулу или полимер, растворимый или нерастворимый, который может быть функционализирован для создания противомикробных свойств связыванием цистеинового компонента. Особый интерес представляют собой твердые изделия, подобные медицинским устройствам, которые предназначены для использования внутри или в контакте с телом человека или животного, особенно с чувствительными тканями и жидкостями организма. Данный перечень потенциальных применений является огромным, смотрите ниже, и включает имплантаты, трубчатые дренажные катетеры и так далее, предназначенные для использования, например, в экстракорпоральных применениях, дренаж (например, ухо или гидроцефалия), диализ, контактные линзы, внутриглазные линзы, искусственные кожи, аппараты для диализа, аппараты искусственного кровообращения, сшивающие материалы, устройства для лечения ран, стоматологические продукты, парентеральное введение, доставку лекарственного средства, стенты, насосы (например, для инсулина), слуховые аппараты, шприцы, пейсмекеры и так далее.
“Предотвращение” или “ингибирование” включает способность остановить или значительно снизить рост, и/или пролиферацию, и/или аккумулирование и/или значительно уменьшить жизнеспособность микроорганизмов в месте, где присутствует средство изобретения.
Главный потенциал данного изобретения состоит в создании возможности для обеспечения противомикробной поверхности на твердом устройстве, которое потенциально контактирует с микроорганизмами и которое желательно поддерживать свободным от аккумулирования и/или пролиферации микроорганизмов и/или от осуществления роли резервуара для жизнеспособных микроорганизмов. Большое число устройств, предназначенных для применения в медицине, а также при обработке пищи, где присутствие микроорганизмов может быть более или менее опасным, иллюстрирует потенциал данного изобретения. Для того чтобы сделать это возможным, заявители успешно использовали субстанцию цистеина, который, как показали авторы, проявляет неожиданно сильный противомикробный эффект, когда ковалентно связан, как описано и заявлено в данном описании. Противомикробные эффекты также показаны для аналогов цистеина и производных, таких как N-ацетилцистеин и гомоцистеин.
Полимеры или олигомеры этиленоксида и пропиленоксида, например полиэтиленоксид или полиэтиленгликоль, легко растворимы в воде, и, кроме того, полиэтиленоксид имеет протеин-отталкивающие свойства, которые могут добавляться к бактерицидной функции данного изобретения, особенно при применении в связи с поверхностями. В зависимости от цистеинового компонента следующие структуры представляют собой примеры подходящих лигандов, предназначенных для применения:
В формуле (2) заместители R2, R3 могут представлять собой водород или алкил с 1 до 20, предпочтительно от 1 до 12, более предпочтительно от 1 до 6 атомами углерода в любой комбинации в R2 и R3 и q может также изменяться, как m и р для метиленовых составляющих сегмента L, как описано ранее, например, от 1 до 20, предпочтительно от 1 до 12, более предпочтительно от 1 до 6. Когда q = 1 и R2 = R3 = H, цистеиновый компонент становится остатком цистеина, который подобно цистеиновым гомологам и производным связывается при помощи тиольной группы, которая вносит одну серу в дисульфидную связь. В дополнение к прямому алкилированию цистеиновой аминогруппы R2 и R3 алкилы могут быть присоединены через амидную связь, включающую азот цистеинового компонента, например, когда R2 означает водород и R3 означает метил, цистеиновый компонент становится ацетилцистеином.
В формуле (3) R2, R3, R4 представляют собой алкильные заместители, которые дают положительно заряженную четвертичную аминогруппу. В данном случае число атомов углерода в алкильных цепях R2, R3, R4 заместителей может изменяться от 1 до 25, предпочтительно от 1 до 18 в любой комбинации. Кроме того, q может также изменяться, как m и р для метиленовых составляющих L сегмента, как описано ранее, например, от 1 до 20, предпочтительно от 1 до 12, более предпочтительно от 1 до 6.
В зависимости от рН заряженные ионные группы могут также встречаться как протонированные аминогруппы в (2) и карбоксилатные группы в (2) и (3).
Связывание -Х- между субстратом R1 и лигандом получают химическими реакциями между функциональными группами R1 и перспективным лигандом. Если R1 имеет химическую функциональную группу Y и лиганд функциональную группу Z, что при взаимодействии дает Х, то принципиальная реакция связывания, где опущены побочные продукты, может быть записана как:
(4) R1-Y + Z-L-S-S-(цистеиновый компонент) →
→ R1-X-L-S-S-(цистеиновый компонент)
В зависимости от выбора Y и Z и условий реакции полученная группа Х может представлять собой амид, вторичный амин, сложный эфир, простой эфир, гидразин, уретан, мочевину, карбонат и др. Доступно большое число специфических и эффективных реакций, которые хорошо разработаны в органической химии. Группы Y, Z и X, а также и реакции, представленные в настоящем описании, поэтому являются примерами и при этом не ограничивают изобретение.
| Таблица 1 | ||||||
| (а) | когда | Y = COOH | и | Z = NH2 | затем | Х = СОNH |
| (b) | ″ | Y = COCl | ″ | Z = NH2 | ″ | Х = СОNH |
| (c) | ″ | Y = COOH | ″ | Z = OH | ″ | X = COO |
| (d) | ″ | Y = COCl | ″ | Z = OH | ″ | X = COO |
| (e) | ″ | Y = NH2 | ″ | Z = CHO | ″ | X = NH |
| (f) | ″ | Y = NHNH2 | ″ | Z = CHO | ″ | X = NHNH |
| (g) | ″ | Y = NH2 | ″ | Z = NCO | ″ | X = NHCONH |
| (h) | ″ | Y = NH2 | ″ | Z = OCOOφNO2 | ″ | X = NHCOO |
| (i) | ″ | Y = NH2 | ″ | Z = сукцинимидил- | ″ | X = NHCO |
| (j) | ″ | Y = NH2 | ″ | Z = эпокси- | ″ | X = NHCH2CH(OH) |
| (k) | ″ | Y = OH | ″ | Z = NCO | ″ | X = OCONH |
| (l) | ″ | Y = OH | ″ | Z = эпокси- | ″ | X = OCH2CH(OH) |
| (m) | ″ | Y = OSO2CH2CF3 | ″ | Z = NH2 | ″ | X = CH2NH |
| (n) | ″ | Y = OSO2CH2CF3 | ″ | Z = SH | ″ | X = CH2S |
| (o) | ″ | Y = SS | ″ | Z = SH | ″ | X = SS |
| (p) | ″ | Y = (алкил)3COK | ″ | Z = (алкил)Br | ″ | X = O |
| (q) | ″ | R1 = Au, Ag | ″ | Z = SH | ″ | X = S |
| (r) | ″ | R1 = Au, Ag | ″ | Z = SS | ″ | X = S |
| (s) | ″ | R1 = R1• | ″ | Z = CH2=C- | ″ | X = CH-C- |
Группы Y и Z в примерах от (а) до (р) можно обменивать между собой у R1 и лиганда, получая то же самое связующее звено Х, но с обратным расположением элементов между R1 и лигандом. Например, когда функциональные группы в (а) обменивают до Y = NH2 и Z = СООН, связующее звено Х имеет вид НNOC. В примерах (е) и (f) первоначально полученный имин, обычно известный, как основание Шиффа, восстанавливают до связующего звена в виде вторичного амина с помощью NaCNBH3. Часто используют промежуточные стадии для повышения селективности и выхода. Хорошо известные примеры представляют собой активацию карбоксильной группы (Y) в (а) с карбодиимидом и/или N-гидроксисукцинилимидом перед образованием амида с аминогруппой (Z). Аминогруппы могут быть активированы с дисукцинимидилкарбонатом для образования мочевинного связующего звена с другой аминогруппой.
В дополнение к карбоксильным и аминогруппам также применимы гидроксильные группы в большом ряду реакций конденсации:
- последующая дериватизация в карбонаты с получением группы Z в (h), где φ означает бензольное кольцо, или в трезилатные группы, как в (m) и (n);
- последующая активация гидроксильных групп в тозил- или сукцинимидилкарбонатные группы или обработка с Вr2 или CNBr для реакций конденсации с нуклеофилами, подобными аминам и/или тиолам;
- две гидроксильные группы могут быть связаны вместе с фосгеном для образования карбонатного связующего звена.
Исчерпывающие обзоры по химии связывания с помощью реакций, упоминаемых в данном описании, а также дополнительные реакции конденсации имеются в литературе (Ref. Herman S. et al. J. Bioact. Compat. Pol. 1995, 10, 145-187).
В примере (s) в таблице 1, R1• означает твердый субстрат со свободными радикалами, доступными для взаимодействия с ненасыщенными группами, проиллюстрированными, но без ограничения только ими, этиленовыми, акриловыми или метакриловыми двойными связями. Применением мономеров, которые имеют лиганд -L-S-S-(цистеиновый компонент), прикрепленный к реакционноспособным углерод-углеродным связям, могут быть получены олигомерные или полимерные цепи, которые ковалентно связаны с субстратом и которые содержат лиганд в виде боковых групп. Концентрацию данных боковых групп в олигомерных или полимерных цепях можно контролировать сополимеризацией с подходящими мономерами, представленными, но без ограничения только ими, акриловой и метакриловой кислотами или сложными эфирами или акриламидом. Другой путь предполагает применение мономеров, подобных малеиновой кислоте, малеиновому ангидриду, тиглиновой кислоте или аллиламину, которые легко связываются с поверхностью, снабженной свободными радикалами, но сильно снижают развитие цепи. Функциональные группы, предоставляемые данными мономерами, то есть ангидридные, карбоксильные или аминные, поэтому станут ограниченными очень тонким поверхностным слоем на субстрате. По данному способу каждое связывание лиганда будет происходить в основном за счет терминального прикрепления прямо к функциональным группам на поверхности, таким образом обеспечивается другая структура по сравнению с той, которая получается, когда лиганд участвует в графт-полимеризации.
Реакция конденсации с R1-Y может проходить согласно уравнению (4) при условии, что группа Y селективно взаимодействует с группой Z лиганда, а не с амино или карбоксильной группами в цистеиновом компоненте.
В случаях, где группа Y не может взаимодействовать исключительно с группой Z лиганда, представленного формулой:
(5) Z-L-S-S-(цистеиновый компонент),
но также с амино и/или карбоксильной группой цистеинового компонента, данные группы, если требуется, могут быть защищены замещением или этерификацией, соответственно. Аминогруппа может быть защищена заместителями, проиллюстрированными третичным бутилоксикарбонилом (трет-BuO). Это необходимо только в случае, когда аминогруппа не алкилирована до третичных или четвертичных аминов, как показано в уравнениях (2) и (3). Карбоксильная группа цистеинового компонента может быть защищена метилированием. После реакции конденсации между R1-Y и Z-лигандом для получения Х связанного лиганда по уравнению (4) трет-BuO и сложноэфирные метильные группы могут быть удалены кислотным и щелочным гидролизом, соответственно, и, таким образом, регенерируется начальная структура Z-лиганда. При наличии данных выборов Z-лиганд, определенный в уравнениях (2)-(4) и формулой (5) и к тому же доступный, с различными функциональностями Z представляет собой отдельный продукт данного изобретения, предназначенный для применения в качестве сборного компонента для одноступенчатого модифицирования функционализированных поверхностей. Данный аспект изобретения также охватывает пример, описанный ранее, где функциональность Y субстрата является свободнорадикальной и функциональность Z лиганда представляет собой ненасыщенную реакционноспособную углерод-углеродную связь.
Когда функциональная группа Y присоединена к твердому субстрату, лиганд может быть синтезирован в месте нахождения на поверхности субстрата. Это является преимуществом, заключающимся в том, что нереагирующие группы Y, а также побочные продукты устраняются на промежуточных стадиях.
По данной процедуре первая стадия будет представлять взаимодействие R1-Y поверхности с соединением, имеющим общее строение
(6) Z-L-S-S-R5,
где L имеет то же определение, что и раньше, и где заместитель R5 легко замещается при взаимодействии с тиолами, образуя новую дисульфидную связь с тиольным соединением.
Первая стадия конденсации может быть выражена в виде:
(7) R1-Y + Z-L-S-S-R5 →
→ R1-X-L-S-S-R5
и следующая стадия:
(8) R1-X-L-S-S-R5 + HS-цистеиновый компонент →
→ R1-X-L-S-S-цистеиновый компонент (+ R5HS)
Обычный пример R5 представляет собой пиридинил, но также применяют дансил. В альтернативном случае дисульфидная связь в (6) может относиться к тиосульфатной группе, которая будет также давать дисульфидный мостик при взаимодействии с тиолом.
Кроме того, имеется альтернативный способ получения по существу такой же химической структуры, как и ранее, и который также находится в объеме данного изобретения. В данном случае тиольный сегмент или группа -L-SH присоединяется к R1 через связывающую группу Х и где L и Х определены, как и ранее, и -SH представляет собой терминальную тиольную группу. Данный продукт может взаимодействовать исключительно с тиольной группой цистеинового компонента в присутствии окислителей с образованием дисульфидного связующего звена с цистеиновым компонентом:
(9) R1-X-L-SН + HS-(цистеиновый компонент) →
→ R1-X-L-S-S-(цистеиновый компонент)
+ (Н2 или водородсодержащий побочный продукт)
Когда цистеиновый компонент окончательно связывается согласно формуле (9), получается противомикробный лиганд, который ковалентно присоединен к R1, как схематически показано в формуле (9).
Функционализация поверхности полимерных материалов, таких как пластмассы, каучук, целлюлозы и т.д., может быть достигнута привитой сополимеризацией или адсорбцией соединений, несущих функциональные группы, такие как, например, карбоксильные или аминные. Осуществление привитой сополимеризации, которое дает ковалентную связь к субстрату, требует функционализацию поверхности. Соединения, которые могут взаимодействовать со свободными радикалами, подвержены привитой сополимеризации в течение или после активации УФ, электронным потоком или гамма-излучением или газовой плазмой. В данных способах свободные радикалы могут появиться в полимерных субстратах, которые могут инициировать привитую сополимеризацию на таких субстратах. Данные способы модифицирования для твердых полимерных субстратов представлены примером (q) в таблице 1. В данном процессе привитая сополимеризация обычно включает развитие цепи из поверхности субстрата, известная как графт-полимеризация.
Мономеры, которые часто используют в свободнорадикальной графт-полимеризации, представляют собой акриловые соединения, такие как акриловая кислота, метакриловая кислота и их сложные эфиры или акриламид, а также винилпирролидон. Графт-полимеризацией таких мономеров, содержащих функциональные группы, например карбоксил, амино, галогены и т.д., твердая поверхность может быть снабжена ковалентно связанными функциональными группами для ковалентного прикрепления противомикробного лиганда. Специальное применение графт-полимеризации, также охваченное данным изобретением, было описано ранее, где противомикробный лиганд, представленный в формуле (6), можно подвергнуть графт-полимеризации, когда Z представляет собой свободнорадикальную реакционноспособную группу, содержащую реакционноспособные ненасыщенные углерод-углеродные связи. Это дало бы противомикробные лиганды в качестве боковых групп в графт-полимеризованных цепях, концентрацию и расположение которых можно контролировать графт-полимеризацией с подходящими виниловыми и акриловыми мономерами. Однако, как также ранее было описано, противомикробный лиганд может быть терминально прикреплен прямо к субстрату. В данном случае функционализацию субстрата делают на первой стадии с помощью мономолекулярной графт-сополимеризации с ненасыщенными соединениями, имеющими незначительный рост цепи, такими как малеиновый ангидрид, малеиновая кислота и трифлиновая кислота или самообрывающийся мономер, подобный аллиламину. С помощью данной процедуры функциональные группы могут появиться на поверхности для непосредственного терминального прикрепления противомикробного лиганда химическим связыванием. Также в случаях, когда виниловый или акриловый лиганд в формуле (6) не будет полимеризоваться, например, по пространственным причинам, он должен прикрепиться непосредственно терминальной реакцией со свободными радикалами на субстрате.
В случаях, где субстрат как таковой представляет собой способный гидролизоваться полимерный материал, такой как сложный полиэфир (РЕТ), полиамид (Nylon™, Nomex™, Kevlar™) или полиакрилат (РММА), функционализация поверхности может быть получена гидролизом в растворе основания или кислоты. Сложные полиэфиры должны дать карбоксильные и гидроксильные группы и полиамиды - карбоксильные и аминные группы, которые можно использовать в последующих модификациях с применением конденсации или адсорбции.
Металлические субстраты, подобные нержавеющей стали, могут представлять собой поверхность, функционализированную карбоксильными группами излучением или плазменной обработкой. Медицинские изделия, подобные стентам, карбоксилируются под действием газовой плазмы силана и акриловой кислоты. Золотые и серебряные поверхности можно подвергать привитой сополимеризации использованием их реакционной способности по отношению к тиольным и дисульфидным соединениям, которые должны также нести другие группы, подобные карбоксилу или амину. Также для металлических субстратов свободнорадикальную графт-сополимеризацию поверхностей можно осуществлять катодной поляризацией субстратов, проводящих электрический ток, в течение воздействия мономеров, способных к образованию ковалентных связей при реакции со свободными радикалами. Поверхностная графт-полимеризация является аналогичной графт-сополимеризации для твердых полимерных субстратов, исходя из инициирования, развития и мономеров, и также представлена примером (s) в таблице 1.
Когда поверхностное модифицирование полимерных субстратов проводят через адсорбцию, грунтование субстрата часто проводят химическим окислением, обработкой в коронном разряде или окислительной газовой плазмой для получения гидрофильных и ионных групп в поверхностном слое. Один из примеров представляет собой адсорбцию полиэтиленимина на полимерных субстратах, которые окислены перманганатом или персульфатом. Полученные аминоповерхности можно использовать для химических реакций связывания, а также адсорбции отрицательно заряженных полимеров, таких как полиакриловая кислота, декстрансульфат или гепарин при подходящем рН. Часто такие полиэлектролиты в их ионнозаряженных состояниях адсорбируются в чередующие слои со свойствами, представляющими интерес в наиболее удаленном от центра слое. В основном, карбоксилирование металлических поверхностей часто осуществляют адсорбцией полиакриловой или полиметакриловой кислоты. Как описано выше, они затем могут быть аминированы химическим связыванием или ионной адсорбцией, например, полиэтиленимина или полиаллиламина.
Другой способ для получения адсорбции, который не требует никакой начальной функционализации субстрата, представляет собой применение блок-сополимеров, содержащих как гидрофобные, так и гидрофильные блоки, или сегменты, которые будут селективно адсорбировать и функционализировать поверхность субстрата. Такие типичные блок-сополимеры представляют собой полиэтиленгликоль-полипропилен (Pluronic) и полиакрилаты-полистирол, полиакрилаты-полиэтилен, полибутадиены-полистирол и другие, которые могут также содержать амино или карбоксильные функциональные группы.
По определению противомикробный лиганд -L-S-S-(цистеиновый компонент) данного изобретения всегда ковалентно связан с субстратом R1.
Однако, так как определение R1 включает органические и полимерные соединения, R1 будет также охватывать полимеры, которые впоследствии способны к связыванию с твердым субстратом за счет ковалентного связывания или адсорбции.
Варианты ковалентного связывания бактерицидного средства данного изобретения на твердом субстрате особо выделены определением R1, включающим такое прикрепление противомикробного средства к твердому субстрату адсорбцией. В данном случае R1 является растворимым субстратом, представленным, например, способными к ионизации полимерами, такими как полиэтиленимин или полиакриловая кислота или блок-сополимеры с гидрофобными/гидрофильными блоками, такие как полиэтиленгликоль-полипропиленгликоль или полиакрилаты в блок-сополимерах с полистиролом, полиэтиленом и др. Цистеиновый компонент ковалентно связан с растворимым субстратом, который на последующей стадии иммобилизуется на твердом субстрате, как описано в данном описании.
Таким образом, модифицирование порверхности, а также последующее химическое связывание или адсорбцию, применяемые для прикрепления бактерицидных средств, можно выполнять многими различными способами. Кроме того, субстраты могут представлять собой органические и неорганические материалы, содержащие синтетические или природные полимеры, а также металлы и минералы. Поэтому способы, химические реакции и субстраты, которые присутствуют здесь и в примерах ниже, являются только описательными и неограничительными для получения бактерицидных средств и поверхностей, охваченных данным изобретением.
Поверхностная концентрация средства изобретения, такого как L-цистеин, находится в интервале от 10-11 до 10-4 моль/см2 и предпочтительно в интервале от 10-9 до 10-5 моль/см2.
Для получения ингибирования клинически или технически важных микроорганизмов 100-кратное ингибирование предпочтительно достигают согласно изобретению на клейких жизнеспособных бактериях, которые можно выделять количественно, причем начинают с большой экспозиции (титр 400 cfu/мл в исходной культуре). Это может частично зависеть от специфического организма и степени/титра экспозиции. Тестируемые условия крайне разнообразны, которые следует ожидать в действительной клинической ситуации.
Примеры микроорганизмов, по которым изобретение может быть применено для предотвращения их роста и/или пролиферации, представляют собой анаэробные и аэробные бактерии, которые включают как различные грамположительные бактерии, выбранные, но без ограничения только ими, из различных видов Staphylococci, таких как S. aureus, S. epidermides и другие коагулаза-негативные стафилококки, S. saphrophyticus, Enterococcus spp, Nesseriae (менингококки, гонококки), Streptococci (зеленящие, гемолитические и негемолитические, группа В и D, S. pneumoniae), Chlostridia (perfringens, botulinum), Bacillus megaterium, а также и различные грамотрицательные виды, выбранные, но без ограничения только ими, из различных Enterobacter spp, Escherichia coli, Klebsiella spp, Proteus, Campylobacter, Yersinia, Shigella, Salmonella, Hemophilus (influenza), Bacteriodes (fragilis, bivius), Pseudomonas (aeruginosa, cepacia), Legionella (pneumophilia). Также включенными являются микоплазма-виды и кандида-виды и различные грибки. Предпочтительные примеры бактерий представляют собой грамположительную бактерию Staphylococcus aureus, грамотрицательную бактерию Escherichia coli или грамположительную бактерию Bacillus megaterium.
Данное изобретение можно применять для предотвращения или ингибирования роста микроорганизмов на поверхностях различных аппликаций, которые могут создать проблему вследствие образования колонии или инфекции. В данном описании показано, что оно является эффективным как против грамположительных, так и грамотрицательных бактерий (грамотрицательная бактерия Escherichia coli или грамположительная бактерия Staphylococcus aureus и Bacillus megaterium). Несколько различных организмов описаны в связи с образованием колоний на катетере и инфекцией в медико-санитарном секторе и окружающей среде больницы. Данные микроорганизмы включают, но без ограничения только ими, грамположительные бактерии и грамотрицательные бактерии, перечисленные ниже. Также частую задачу представляют собой различные грибки, особенно у иммунокомпромиссных пациентов (подвергающихся трансплантации или другой иммуноподавляющей терапии и т.д.). Изобретение может быть применено там, где инфекция, образование колонии или биопленки на искусственных устройствах (катетеры, трахеостомические трубки и т.д.) может быть проблемой при медицинском обслуживании. Примеры известных и описанных микроорганизмов, переносимых катетером, и против которых может быть использовано изобретение, представляют собой (но без ограничения только ими): Staphylococci spp (такие как S. aureus, S. epidermides и другие коагулазанегативные стафилококки, такие как S. saphrophyticus); Streptococci spp (зеленящие, гемолитические и негемолитические, группа В и D, S. pneumoniae); Enterococcus spp, S. facealis; Chlostridia (perfringens, botulinum); различные Enterobacter spp, такие как Escherichia coli, Klebsiella spp (pneumonia), Enterobacter cloace, аэрогены, Proteus (mirabilis), Campylobacter, Yersinia, Shigella, Salmonella, Hemophilus (influenza), Neisseriae (meningococcus и gonococcus), Bacteroides (Bacteroides spp и фузобактерия), Pseudomonas (aeruginosa, cepacia), Legionella (pneumophilia), Serratia marcenens, Acinetobacter spp, Morganella morganii, Stenotrophomonas, Citrobacter spp, Corynebacterium spp, Burkholder cepafia, Acinetobacter spp; различные микоплазма-виды (М. avian и другие); и также грибки, такие как Candida spp, C. tropicales, C. parapsilosis, Cryptococcus neoformans, Aspergillus fumigatus, Tricosporun, Blastoschizomyces, Stenotrophomonas maltophilia, Malassezia, Bukholderia cepafia, Aspergillus.
При многих применениях данного изобретения субстрат представляет собой часть устройства, аппарата и/или поверхности, выбранных из (а) медицинских устройств, таких как экстракорпоральные медицинские устройства, которые применимы на внешней стороне организма челове