N-дигидроксиалкилзамещенные производные 2-оксоимидазола
Иллюстрации
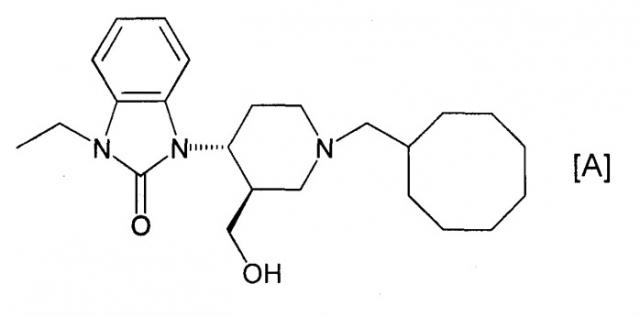
Показать всеИзобретение относится к соединениям формулы (I):
в которой R означает дигидроксизамещенную С2-С6алкильную группу, и Су представляет собой спиро[4.5]дец-6-ил, спиро[2.5]окт-4-ил, спиро[3.5]нон-5-ил, 3,3-диметилбицикло[2.2.1]гепт-2-ил или 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-3-ил-группу. Данные соединения действуют как антагонисты ноцицептинового рецептора и применимы, например, в качестве средств, улучшающих переносимость наркотических аналгетиков, облегчающих зависимость от наркотического аналгетика или наркомании; в качестве усилителей аналгетиков; средств против ожирения или средств для подавления аппетита; средств для лечения снижения познавательной способности и возрастной деменции/амнезии; средств для лечения развивающегося нарушения познавательной способности; лечебных средств при шизофрении; средств для лечения нейродегенеративных заболеваний; антидепрессантных или лечебных средств при аффективном расстройстве; лечебных или профилактических средств при несахарном диабете; лечебных или профилактических средств при полиурии; и лечебных средств при гипотензии и тому подобное. 3 н. и 8 з.п. ф-лы, 3 табл.
Реферат
Область техники
Данное изобретение относится к веществам, которые проявляют антагонизм к связыванию ноцицептина с ноцицептиновым рецептором ORL1 (рецептор, подобный опиоидному рецептору типа 1).
Соединения, которые ингибируют связывание ноцицептина с ноцицептиновым рецептором ORL1, применимы в качестве аналгетика при заболеваниях, сопровождаемых болью, такой как раковая боль, послеоперационная боль, мигрень, подагра, хронический ревматизм, хроническая боль и невралгия; средств, улучшающих переносимость наркотических аналгетиков, представленных морфином; средств, ослабляющих зависимость от наркотического аналгетика, представленного морфином, или против наркомании; усилителей аналгетиков; средств против ожирения или средств для подавления аппетита; лечебных или профилактических средств при снижении познавательной способности и возрастной деменции/амнезии, сосудисто-мозговых заболеваниях и болезни Альцгеймера; средств для лечения развивающегося нарушения познавательной способности с дефицитом внимания, гиперфункционального расстройства и неполноценности усвоения; лечебного средства при шизофрении; средств для лечения нейродегенеративных заболеваний, представленных паркинсонизмом и хореей; антидепрессантных или лечебных средств при аффективном расстройстве; лечебных или профилактических средств при несахарном диабете; лечебных или профилактических средств при полиурии; и лечебного средства при гипотензии и тому подобное.
Описание предшествующего уровня
Ноцицептин (то же самое вещество в виде орфанина FQ) представляет собой пептид, состоящий из 17 аминокислотных фрагментов, причем имеет структуру, одинаковую со структурой опиоидного пептида. Ноцицептин влияет на реакционную способность в отношении ноцицептивной стимуляции, обладает аппетит стимулирующей активностью, активностью при снижении способности пространственного усвоения, антагонизмом в отношении аналгезирующего действия классических опиатных агонистов, ингибирующим действием в отношении высвобождения дофамина, действием в отношении водного диуреза, сосудорасширяющим действием и системным действием по снижению кровяного давления, и, как полагают, он принимает участие во внутримозговом контролировании боли, аппетита и формирования памяти посредством ноцицептинового рецептора ORL1 [cм. Nature, 377, 532 (1995); Society for Neuroscience, 22, 455 (1996); NeuroReport, 8, 423 (1997); Eur. J. Neuroscience, 9, 194 (1997); Neuroscience, 75, 1 (1996); ibid., 333 (1996); Life Science, 60, PL15 (1997); ibid., PL141 (1997); Proceeding for National Academy of Sciences, 94, 14858 (1997)].
Кроме того, известно, что у пораженной мыши, в случае ингибирования экспрессии ноцицептинового рецептора снижается толерантность к морфину или память и способность к усвоению повышаются [см. Neuroscience Letters, 237, 136 (1997); Nature, 394, 577 (1998)].
Также было опубликовано, что ноцицептин сам по себе вызывает симптомы, схожие с симптомами абстиненции, наблюдаемыми при привыкании к чрезмерному употреблению морфина, и что непептидный антагонист ноцицептинового рецептора повышает толерантность к морфину, зависимость и симптомы, схожие с симптомами абстиненции [см. Psychopharmacology, 151, 344-350 (2000); Journal of Neuroscience, 20, 7640 (2000)].
C другой стороны, сообщают, что дефектные мыши по белковому предшественнику ноцицептина демонстрируют поведения, схожие с состоянием тревоги, и изменения в ответе на стресс [см. Proceeding for National Academy of Sciences, 96, 10444 (1999)].
Следовательно, вещества, которые особенно ингибируют связывание ноцицептина с ноцицептиновым рецептором ORL1, применимы в качестве аналгетика в отношении заболеваний, сопровождаемых болью, такой как раковая боль, послеоперационная боль, мигрень, подагра, хронический ревматизм, хроническая боль и невралгия; средств, улучшающих переносимость наркотических аналгетиков, представленных морфином; средств, облегчающих зависимость от наркотического аналгетика, представленного морфином, или против наркомании; усилителей аналгетиков; средств против ожирения или средств для подавления аппетита; лечебных или профилактических средств при снижении познавательной способности и возрастной деменции/амнезии, сосудисто-мозговых заболеваниях и болезни Альцгеймера; средств для лечения развивающегося нарушения познавательной способности с дефицитом внимания, гиперфункционального расстройства и неполноценности усвоения; лечебных средств при шизофрении; средств для лечения нейродегенеративных заболеваний, представленных паркинсонизмом и хореей; антидепрессантных или лечебных средств при аффективном расстройстве; лечебных или профилактических средств при несахарном диабете; лечебных или профилактических средств при полиурии; и лечебных средств при гипотензии и тому подобное.
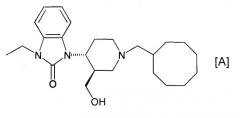
Международная публикация WO98/54168 или J. Med. Chem. 5061-5063 (1999) раскрывают соединения, проявляющие антагонизм к связыванию ноцицептина с ноцицептиновым рецептором ORL1. В частности, раскрыто соединение следующей формулы (А):
(в дальнейшем обозначенное как “cоединение А”) в качестве соединения с отличным селективным антагонизмом к связыванию ноцицептина с ноцицептиновым рецептором.
Международная публикация WO98/54168.
J. Med. Chem. 5061-5063 (1999).
Раскрытие изобретения
Заявители исследовали соединения со структурами, аналогичными структуре соединения А, для создания соединений, которые проявляют антагонистическую активность к связыванию ноцицептина с ноцицептиновым рецептором ORL1, чтобы открыть, что данные соединения, имеющие би- или трициклическую алифатическую карбоциклическую группу с определенными числами атомов углерода вместо циклооктильной группы и также имеющие дигидроксиалкильный заместитель на атоме азота, обладают хорошо сбалансированными активностями, заключающимися не только в селективном ингибировании связывания ноцицептина с ноцицептиновым рецептором ORL1, но также в проявлении отличных метаболических свойств in vivo, и могут быть соединениями, особенно пригодными для человека. Данное изобретение выполнено, основываясь на этом открытии.
Таким образом, данное изобретение относится к
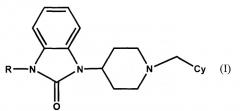
(1) производным 2-оксоимидазола формулы (I):
в которой R означает дигидроксизамещенную С1-С6алкильную группу, и Су означает необязательно замещенную С6-С10-би- или трициклическую алифатическую карбоциклическую группу, или к их фармацевтически приемлемым солям.
Данное изобретение также относится к
(2) фармацевтической композиции, содержащей фармацевтически приемлемый адъювант и соединение, описанное выше в (1), или его фармацевтически приемлемую соль; и к
(3) способу получения лекарственного средства для применения в качестве аналгетика; средства, улучшающего переносимость наркотических аналгетиков; средства, облегчающего зависимость от наркотических аналгетиков или против наркомании; усилителя аналгетиков; средства против ожирения или средства для подавления аппетита; средства для лечения снижения познавательной способности и возрастной деменции/амнезии, сосудисто-мозгового заболевания и болезни Альцгеймера; средства для лечения развивающегося нарушения познавательной способности с дефицитом внимания, гиперфункционального расстройства и неполноценности усвоения; лечебного средства при шизофрении; средства для лечения нейродегенеративных заболеваний, представленных паркинсонизмом и хореей; антидепрессантного или лечебного средства при аффективном расстройстве; лечебного или профилактического средства при несахарном диабете; лечебного или профилактического средства при полиурии; и лечебного средства при гипотензии, который включает смешивание соединения, описанного выше в (1), или его фармацевтически приемлемой соли и фармацевтически приемлемого адъюванта.
Наилучший путь осуществления изобретения
Ниже изобретение рассмотрено в деталях со ссылкой к определенным примерам.
В формуле (I) R означает С1-С6алкильную группу, содержащую две гидроксильных группы, причем определенные примеры включают: 2-гидрокси-1-(гидроксиметил)этил, 2,3-дигидроксипропил, 2,3-дигидрокси-2-метилпропил, 2,3-дигидроксибутил, 2,4-дигидроксибутил, 3,4-дигидроксибутил, 2,3-дигидрокси-1-метилпропил, 2-гидрокси-1-(гидроксиметил)пропил, 3-гидрокси-1-(гидроксиметил)пропил, 3-гидрокси-2-(гидроксиметил)пропил, 2,3-дигидроксипентил, 2,4-дигидроксипентил, 2,5-дигидроксипентил, 3,4-дигидроксипентил, 3,5-дигидроксипентил, 4,5-дигидроксипентил, 2,3-дигидрокси-1-метилбутил, 2,4-дигидрокси-1-метилбутил, 3,4-дигидрокси-1-метилбутил, 2-гидрокси-1-(гидроксиметил)бутил, 3-гидрокси-1-(гидроксиметил)бутил, 4-гидрокси-1-(гидроксиметил)бутил, 2,3-дигидрокси-2-метилбутил, 2,4-дигидрокси-2-метилбутил, 3,4-дигидрокси-2-метилбутил, 2-гидрокси-2-(гидроксиметил)бутил, 3-гидрокси-2-(гидроксиметил)бутил, 4-гидрокси-2-(гидроксиметил)бутил, 2,3-дигидрокси-3-метилбутил, 2,4-дигидрокси-3-метилбутил, 3,4-дигидрокси-3-метилбутил, 4-гидрокси-3-(гидроксиметил)бутил, 2,3-дигидрокси-1,1-диметилпропил, 2-гидрокси-1-(гидроксиметил)-1-метилпропил, 3-гидрокси-1-(гидроксиметил)-1-метилпропил, 1,1-бис(гидроксиметил)пропил, 2,3-дигидрокси-1,2-диметилпропил, 2-гидрокси-1-(гидроксиметил)-2-метилпропил, 3-гидрокси-2-(гидроксиметил)-2-метилпропил, 2,3-дигидрокси-1-этилпропил, 2-гидрокси-1-(2-гидроксиэтил)пропил, 2-гидрокси-1-(1-гидроксиэтил)пропил, 3-гидрокси-1-(2-гидроксиэтил)пропил, 2,3-дигидроксигексил, 2,4-дигидроксигексил, 2,5-дигидроксигексил, 2,6-дигидроксигексил, 3,4-дигидроксигексил, 3,5-дигидроксигексил, 3,6-дигидроксигексил, 4,5-дигидроксигексил и 4,6-дигидроксигексил. Предпочтительные примеры представляют собой С3-С4алкильные группы, содержащие две гидроксильные группы и, в частности, рекомендуются 2,3-дигидроксипропильная, 2-гидрокси-1-(гидроксиметил)этильная и 2,3-дигидрокси-2-метилпропильная группы.
Су означает необязательно замещенную С6-С10-би- или трициклическую алифатическую карбоциклическую группу.
В качестве “заместителя” в “необязательно замещенной С6-С10-би- или трициклической алифатической карбоциклической группе” можно назвать, например, галоген, такой как фтор, хлор и тому подобное, и С1-С6алкильные группы, такие как метил, этил, н-пропил, изопропил, н-бутил, н-пентил и тому подобное. Предпочтительно рекомендуются С1-С4алкильные группы.
“С6-С10-би- или трициклические алифатические карбоциклические группы” означают насыщенные алифатические карбоциклические группы, которые представляют собой би- или трициклические группы. Например, приведены спиро[2.5]окт-4-ил, спиро[2.5]окт-5-ил, спиро[2.5]окт-6-ил, спиро[3.5]нон-5-ил, спиро[3.5]нон-6-ил, спиро[3.5]нон-7-ил, спиро[4.5]дец-6-ил, спиро[4.5]дец-7-ил, спиро[4.5]дец-8-ил, бицикло[2.2.1]гепт-2-ил, бицикло[2.2.2]окт-2-ил, 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-3-ил, 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-5-ил, 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-6-ил и тому подобное.
В качестве конкретных примеров заместителя Су можно назвать спиро[2.5]окт-4-ил, спиро[2.5]окт-5-ил, спиро[2.5]окт-6-ил, спиро[3.5]нон-5-ил, спиро[3.5]нон-6-ил, спиро[3.5]нон-7-ил, спиро[4.5]дец-6-ил, спиро[4.5]дец-7-ил, спиро[4.5]дец-8-ил, бицикло[2.2.1]гепт-2-ил, 3,3-диметилбицикло[2.2.1]гепт-2-ил, 3,3-диметилбицикло[2.2.1]гепт-5-ил, 3,3-диметилбицикло[2.2.1]гепт-6-ил, бицикло[2.2.2]окт-2-ил, 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-3-ил, 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-5-ил, 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-6-ил и тому подобное. Предпочтительно рекомендуются спиро[4.5]дец-6-ил, спиро[2.5]окт-4-ил, спиро[3.5]нон-5-ил, 3,3-диметилбицикло[2.2.1]гепт-2-ил, 1-спиро(бицикло[2.2.1]гептан-2,1'-циклопропан)-3-ил и тому подобное.
Согласно изобретению производные 2-оксоимидазола, имеющие на атоме азота в положении 1 дигидроксиалкильную группу и, кроме того, имеющие в качестве заместителя Су необязательно замещенную С6-С10-би- или трициклическую алифатическую карбоциклическую группу обладают очень хорошей сбалансированной физиологической активностью с высоким антагонизмом к ноцицептиновому рецептору и также высокой метаболической стабильностью.
В качестве конкретных примеров соединений формулы (I) могут быть названы следующие:
1) 1-(2,3-дигидроксипропил)-3-[1-(спиро[4.5]дец-6-илметил)пиперидин-4-ил]-1,3-дигидро-2Н-бензимидазол-2-он,
2) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(6S)-спиро[4.5]дец-6-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
3) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(6R)-спиро[4.5]дец-6-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
4) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(6S)-спиро[4.5]дец-6-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
5) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(6R)-спиро[4.5]дец-6-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
6) 1-(2,3-дигидроксипропил)-3-[1-(спиро[3.5]нон-5-илметил)пиперидин-4-ил]-1,3-дигидро-2Н-бензимидазол-2-он,
7) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(5S)-спиро[3.5]нон-5-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
8) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(5R)-спиро[3.5]нон-5-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
9) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(5S)-спиро[3.5]нон-5-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
10) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(5R)-спиро[3.5]нон-5-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
11) 1-(2,3-дигидроксипропил)-3-{1-[(3,3-диметилбицикло[2.2.1]гепт-2-ил)метил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
12) 1-[(2R)-2,3-дигидроксипропил]-3-(1-{[(1S,2S,4R)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
13) 1-[(2R)-2,3-дигидроксипропил]-3-(1-{[(1S,2R,4R)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
14) 1-[(2R)-2,3-дигидроксипропил]-3-(1-{[(1R,2R,4S)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
15) 1-[(2R)-2,3-дигидроксипропил]-3-(1-{[(1R,2S,4S)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
16) 1-[(2S)-2,3-дигидроксипропил]-3-(1-{[(1S,2S,4R)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
17) 1-[(2S)-2,3-дигидроксипропил]-3-(1-{[(1S,2R,4R)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
18) 1-[(2S)-2,3-дигидроксипропил]-3-(1-{[(1R,2R,4S)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
19) 1-[(2S)-2,3-дигидроксипропил]-3-(1-{[(1R,2S,4S)-3,3-диметилбицикло[2.2.1]гепт-2-ил]метил}пиперидин-4-ил)-1,3-дигидро-2Н-бензимидазол-2-он,
20) 1-(2,3-дигидроксипропил)-3-[1-(спиро[2.5]окт-4-илметил)пиперидин-4-ил]-1,3-дигидро-2Н-бензимидазол-2-он,
21) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(4S)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
22) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(4R)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
23) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(4S)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
24) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(4R)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
25) 1-(2,3-дигидроксипропил)-3-[1-(спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил)пиперидин-4-ил]-1,3-дигидро-2Н-бензимидазол-2-он,
26) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(1R,3S,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
27) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(1R,3R,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
28) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(1S,3R,4R)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
29) 1-[(2R)-2,3-дигидроксипропил]-3-{1-[(1S,3S,4R)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
30) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(1R,3S,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
31) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(1R,3R,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
32) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(1S,3R,4R)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
33) 1-[(2S)-2,3-дигидроксипропил]-3-{1-[(1S,3S,4R)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
34) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-[1-(спиро[2.5]окт-4-илметил)пиперидин-4-ил]-1,3-дигидро-2Н-бензимидазол-2-он,
35) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-{1-[(4R)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
36) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-{1-[(4S)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
37) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-[1-(спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил)пиперидин-4-ил]-1,3-дигидро-2Н-бензимидазол-2-он,
38) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-{1-[(1R,3S,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
39) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-{1-[(1R,3R,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
40) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-{1-[(1S,3R,4R)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
41) 1-[2-гидрокси-1-(гидроксиметил)этил]-3-{1-[(1S,3S,4R)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
42) 1-(2,3-дигидрокси-2-метилпропил)-3-[1-(спиро[2.5]окт-4-илметил)пиперидин-4-ил]-1,3-дигидро-2Н-бензимидазол-2-он,
43) 1-[(2R)-2,3-дигидрокси-2-метилпропил]-3-{1-[(4S)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
44) 1-[(2R)-2,3-дигидрокси-2-метилпропил]-3-{1-[(4R)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
45) 1-[(2S)-2,3-дигидрокси-2-метилпропил]-3-{1-[(4S)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
46) 1-[(2S)-2,3-дигидрокси-2-метилпропил]-3-{1-[(4R)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он.
Предпочтительно рекомендуются:
1-[(2R)-2,3-дигидроксипропил]-3-{1-[(1R,3S,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
1-[(2S или 2R)-2,3-дигидрокси-2-метилпропил]-3-{1-[(4S)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
1-[2-гидрокси-1-(гидроксиметил)этил]-3-{1-[(1R,3S,4S)-спиро[бицикло[2.2.1]гептан-2,1'-циклопропан]-3-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он,
1-[(2R)-2,3-дигидроксипропил]-3-{1-[(4S)-спиро[2.5]окт-4-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он и
1-[(2R)-2,3-дигидроксипропил]-3-{1-[(6S или 6R)-спиро[4.5]дец-6-илметил]пиперидин-4-ил}-1,3-дигидро-2Н-бензимидазол-2-он.
Способы получения соединений формулы (I)
Эти соединения формулы (I) можно получать следующими способами или также способами, описанными в WO98/54168.
Способ получения 1
Способ получения 1 использует 1,3-дигидро-1-(4-пиперидинил)-2Н-бензимидазол-2-он, который представляет собой известное соединение, и обеспечивает получение соединения формулы (I) посредством трех- или четырехступенчатых стадий.
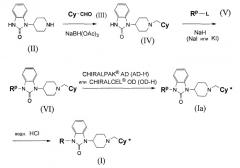
Схема реакций 1
в которой Rp означает низшую алкильную группу, имеющую две защищенные гидроксильные группы, L означает удаляемую группу, Су∗ означает оптически активную группу Су, и Су и R имеют те же значения, описанные ранее.
Соединение формулы (II) и соединение формулы (III) подвергают реакции восстановительного алкилирования в органическом растворителе в присутствии восстановителя для получения соединения формулы (IV).
Что касается количества используемых соединений формул (II) и (III), соответственно, то они обычно используются в эквимолярных количествах, или либо один из них используется в небольшом молярном избытке.
В качестве восстановителя, например, можно назвать цианоборогидрид натрия, триацетоборогидрид натрия, бисцианоборогидрид цинка, бисцианоборогидрид никеля и тому подобное.
Количество восстановителя составляет от моля до молярного избытка, предпочтительно 1-5 молей на моль соединения формулы (II).
Реакцию обычно проводят в органическом растворителе. Примеры используемого растворителя включают спирты, такие как метанол, этанол и пропанол; эфиры, такие как диэтиловый эфир, тетрагидрофуран (ТГФ/”THF”) и диоксан; галогенированные углеводороды, такие как метиленхлорид, хлороформ и дихлорэтан; ароматические углеводороды, такие как бензол, толуол, хлорбензол и ксилол; и апротонные полярные растворители, такие как диметилформамид (ДМФА/”DMF”), ацетонитрил и гексаметилтриамид фосфорной кислоты, или смеси растворителей.
Примерная температура реакции обычно находится в интервале -20°С-100°С, предпочтительно 0°С-комнатная температура, и продолжительность реакции обычно составляет от 5 минут до 7 суток, предпочтительно 1-6 часов.
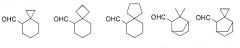
В качестве соединений формулы (III) могут быть использованы, например, следующие соединения.
Затем соединение формулы (IV) конденсируют с соединением формулы (V) в органическом растворителе в присутствии основания для получения соединения формулы (VI).
Соединение формулы (V) используют в количестве от моля до молярного избытка, предпочтительно 1-5 молей на моль соединения формулы (IV).
Примеры используемого основания включают гидрид натрия, гидрид калия, гексаметилдисилазид литий, гексаметилдисилазид натрий, гексаметилдисилазид калий, карбонат калия и карбонат натрия. Предпочтительно рекомендуются гидрид натрия и гидрид калия.
Количество используемого основания составляет от моля до молярного избытка, предпочтительно 1-5 молей на моль соединения формулы (V).
Для ускорения реакции в реакционную систему может быть добавлен галогенид щелочного металла, такой как иодид натрия, иодид калия или тому подобное. При этом может быть использован, например, 0,1 моль - молярный избыток галогенида щелочного металла на моль соединения формулы (IV).
В качестве органического растворителя, например, можно назвать ДМФА, ТГФ, гексаметилтриамид фосфорной кислоты и тому подобное.
Примерная температура реакции обычно находится в интервале -0°С-150°С, причем предпочтительно рекомендуется интервал комнатная температура-130°С. Продолжительность реакции обычно находится в интервале от 5 минут до 7 суток, предпочтительно от часа до 12 часов.
В соединении формулы (V) L означает удаляемую группу, которая может представлять собой, например, бензолсульфонилокси, п-толуолсульфонилокси, метансульфонилокси группу, фтор или бром.
Конкретные примеры соединений формулы (V) включают следующие соединения:
Для получения оптически активного соединения формулы (Ia), когда необходимо соединение формулы (VI) последовательно разделяют на оптические изомеры с помощью оптически активной колонки, и снимают защиту с гидроксильных групп соединения формулы (Ia) с получением соединения формулы (I).
Такие гидроксил-защитные группы не ограничены, пока они обладают требуемой функцией. Например, можно назвать такие группы, как трет-бутил; алкилсилил, например, триметилсилил, трет-бутилдиметилсилил и трет-бутилдифенилсилил; метоксиметил; тетрагидропиранил; триметилсилилэтоксиметил; аралкил, например, бензил, п-метоксибензил, 2,3-диметоксибензил, о-нитробензил, п-нитробензил и тритил; и ацил, например, формил и ацетил, среди которых особенно предпочитают метоксиметил, тетрагидропиранил, тритил, триметилсилилэтоксиметил, трет-бутилдиметилсилил и ацетил.
В частности, в качестве защитных групп 1,2- или 1,3-диолов, например, можно назвать метиленкеталь, этилиденацеталь, фенилэтилиденацеталь, 4-метоксифенилэтилиденацеталь, изопропилиденкеталь и бензилиденацеталь.
Способы удаления защитных групп различаются в зависимости от вида защитной группы и стабильности отдельных соединений, изображенных формулой [Ia]. Например, удаление осуществляют способами, описанными в литературе [см. Protective Groups in Organic Synthesis, T.W. Greene, John Wiley and Sons Co., (1981)], или способами, аналогичными им, сольволизом при использовании кислоты или основания, т.е., способом, например, в котором кислота, количество которой составляет от 0,01 моля до большого молярного избытка, предпочтительно трифторуксусной кислоты, муравьиной кислоты, хлористо-водородной кислоты или тому подобное; или в котором основание, количество которого составляет от эквимолярного до большого молярного избытка, предпочтительно гидроксида натрия, гидроксида кальция или тому подобное, взаимодействует на целевое соединение; химическим восстановлением, при этом используют гидрированный комплекс металла, или каталитическим восстановлением, при этом используют катализатор палладий-на-угле или катализатор никель Ренея.
В случае диол-защитных групп, таких как кеталь, ацеталь и тому подобное, удаление защиты может быть осуществлено гидролизом соединения формулы (VI) с использованием хлористо-водородной кислоты, в растворителе, таком как ТГФ, диоксане или тому подобное, при температурах от комнатной температуры до 100°С.
При необходимости, соединение формулы (VI) можно оптически разделять методами хроматографии с использованием оптически активной колонки с получением оптически активного соединения формулы (Ia).
В качестве оптически активной колонки можно назвать, например, CHIRALPAK® AD, CHIRALPAK® AD-H, CHIRAL CELL® OD и CHIRAL CELL® OD-H (Daicel C., Ltd.).
В качестве элюента-растворителя в данном случае можно назвать смешанные растворители, такие как гексан/2-пропанол/диэтиламин = 1900/100/2 - 800/200/1 по объему, или гексан/этанол/диэтиламин = 1900/100/2 - 800/200/1 по объему.
В качестве способов обнаружения соединений в таком случае можно применять, например, ультрафиолетовые лучи в диапазоне длин волн вблизи 280 нм.
Способ получения 2
Способ получения 2 представляет собой способ для получения соединений формулы (I), используя соединения формулы (IV) в качестве исходного продукта.
Схема реакций 2
в которой Ms означает метансульфонильную группу, ТЕА означает триэтиламин, и Су, Су∗, Rp, L и R имеют те же самые значения, которые определены выше.
В соединение формулы (IV) вводят мезильную группу известными способами, предназначенными для превращения его в соединение формулы (VII), которое успешно разделяют на оптические изомеры согласно способу получения 1 с получением соединения формулы (VIIа). Затем мезильную группу (метилсульфонильную группу) в соединении формулы (VIIа) удаляют, используя фторид тетра-н-бутиламмония (ТВАF) для получения соединения формулы (VIIb), которое подвергают взаимодействию с соединением формулы (V) согласно способу получения 1 для получения соединения формулы (Iа), которое затем превращают в соединение формулы (I) путем удаления защиты.
Соединение формулы (I), полученное таким образом, может быть легко выделено и очищено обычными способами выделения, например, экстракцией растворителем, перекристаллизацией, колоночной хроматографией, препаративной тонкослойной хроматографией или тому подобное.
Данные соединения могут быть превращены в фармацевтически приемлемые соли согласно принятой практике. Наоборот, соли могут быть переведены в свободные соединения обычно используемыми способами.
В качестве солей соединений формулы (I) можно назвать аддитивные соли кислот при пиперидинильной группе.
В качестве примеров таких аддитивных солей кислот можно назвать соли неорганических кислот, такие как гидрохлорид, сульфат, нитрат, фосфат, перхлорат и тому подобное; соли карбоновых кислот, такие как малеат, фумарат, тартрат, цитрат, аскорбат, трифторацетат и тому подобное; и сульфонаты, такие как метансульфонат, изэтионат, бензолсульфонат, п-толуолсульфонат и тому подобное.
Действие соединений данного изобретения как антагонистов ноцицептинового рецептора показано в следующих фармакологических тестовых примерах.
Фармакологический тестовый пример 1 (количественный анализ ингибирования связывания ноцицептинового рецептора)
кДНК, которая кодирует ген человеческого рецептора ноцицептина, объединяли с вектором экспрессии pCR3 (Invitrogen) для приготовления pCR3/ORL1. Затем pCR3/ORL1 подвергали трансфекции в СНО клетки, используя трансфектам (Nippongene) для получения линии с устойчивой экспрессией (CНО/ORL1 клетки), имеющей устойчивость против 1 мг/мл G418. Мембранные фракции готовили из данной линии с устойчивой экспрессией для выполнения количественного анализа по связыванию рецептора. Мембранную пробу, составляющую 11 мкг, 50 пМ [125I] Tyr14-ноцицептина (Amersham Pharmacia), 1 мг SPA гранул агглютинина проростков пшеницы (на основе PVT; Amersham Pharmacia) и каждое тестируемое соединение суспендировали в NC буфере (50 мМ Hepes, 10 мМ хлорид натрия, 1 мМ хлорид магния, 2,5 мМ хлорид кальция, 0,1% BSA, 0,025% бацитрацин, рН 7,4) и инкубировали при 37°С в течение 60 минут, и затем определяли радиоактивность. Активность связывания с ноцицептиновым рецептором обозначали концентрацией 50%-ного ингибирования (IC50 величина) [125I] Tyr14-ноцицептинового связывания каждого тестированного соединения. Результаты были, как показано в таблице 1.
| Таблица 1 | |
| Соединение | IC50 величина (нМ) |
| Пример 1 | 1,6 |
| Пример 2 | 5,1 |
| Пример 3 | 8,7 |
| Пример 4 | 1,9 |
| Пример 5 | 2,8 |
Фармакологический тестовый пример 2 (антагонизм против активации G белков, вызванной ноцицептином)
СНО клетки, которые стабильно представляли ноцицептиновый рецептор ORL1, применяли для исследования действия каждого тестируемого соединения против активации G белков, вызванной ноцицептином. Мембранную пробу, приготовленную из СНО/ORL1 клеток, 50 нМ ноцицептина, 200 пМ GTPy[35S] (NEN), 1,5 мг SPA гранул агглютинина проростков пшеницы (Amersham Pharmacia) и каждое из тестируемых соединений смешивали в GDР буфере (20 мМ Hepes, 100 мМ хлорид натрия, 10 мМ хлорид магния, 1 мМ EDTA, 5 мкМ GDP, рН 7,4) и инкубировали при 25°С в течение 150 минут, и затем определяли радиоактивность. Антагонизм против активации G белков, вызванной ноцицептином, обозначали концентрацией 50%-ного ингибирования (IC50 величина) для каждого тестированного соединения против GTPy[35S] связывания. Результаты были, как показано в таблице 2.
| Таблица 2 | |
| Соединение | IC50 величина (нМ) |
| Пример 1 | 3,9 |
| Пример 2 | 8,6 |
| Пример 3 | 18,0 |
| Пример 4 | 6,0 |
| Пример 5 | 4,5 |
Фармакологический тестовый пример 3 (оценка метаболической стабильности)
Метаболическую активность тестовых соединений исследовали, используя микросому печени человека. Готовили 100 мМ буфер фосфата калия (рН 7,4), содержащий 10 мМ G-6-Р, 1,0 мМ НАДФ+(NADP+), 10 единицы/мл G-6-P DH, 3,0 мМ MgCl2 и 0,25 мг протеин/мл микросомы печени человека, каждую порцию которого в 392 мкл выливали во множество сосудов и предварительно инкубировали при 37°С в течение 5 минут. Затем 8 мкл каждого 50 мкМ тестируемого соединения (50% раствор в ацетонитриле) добавляли для инициирования реакции (конечная концентрация тестируемого соединения: 1 мкМ). В период инициирования и через 30 мин после реакции 150 мкл каждого реакционного раствора добавляли к 450 мкл этанола для суспендирования реакции с последующим разделением центрифугированием (12000 g, 12 минут, 4°C). Полученный супернатант анализировали с помощью ЖХ/МС/МС(LC/MS/MS). Основываясь на площади пиков тестируемого соединения в каждом образце в начальный период реакции, принятой за 100%, вычисляли остаточное отношение тестируемого соединения в образце после 30-минутной реакции. Результаты были, как показано в таблице 3.
Остаточное отношение (%) =
[площадь пиков (после 30-минутной реакции)/
площадь пиков (после 0-минутной реакции)] × 100.
| Таблица 3 | |
| Соединение | Остаточное отношение (%) |
| Пример 2 | 82 |
| Пример 4 | 72 |
| Пример 5 | 65 |
Фармацевтические препаративные формы, содержащие соединения формулы (I)
Соединения данного изобретения могут быть введены перорально или парентерально и, в виде готовых препаративных форм, пригодных для таких путей введения, могут быть использованы в качестве аналгетика против заболеваний, сопровождаемых болью, такой как раковая боль, послеоперационная боль, мигрень, подагра, хронический ревматизм, хроническая боль и невралгия; средств, улучшающих переносимость наркотических аналгетиков, представленных морфином; средств, облегчающих зависимость от наркотических аналгетиков, представленных морфином или против наркомании; усилителей аналгетиков; средств против ожирения или средств для подавления аппетита; лечебных или профилактических средств при снижении познавательной способности и возрастной деменции/амнезии, сосудисто-мозговых заболеваниях и болезни Альцгеймера; средств для лечения развивающегося нарушения познавательной способности с дефицитом внимания, гиперфункционального расстройства и неполноценности усвоения; лечебного средства при шизофрении; средств для лечения нейродегенеративных заболеваний, представленных паркинсонизмом и хореей; антидепрессантных или лечебных средств при аффективном расстройстве; лечебных или профилактических средств при несахарном диабете; лечебных или профилактических средств при полиурии; и лечебного средства при гипотензии и тому подобное.
Фактически при применении соединений данного изобретения они могут быть приготовлены в различных препаративных формах, подходящих для индивидуального пути введения, с фармацевтически приемлемыми адъювантами. В качестве адъювантов можно использовать различные добавки, обычно применяемые в области медицинских препаратов, примеры которых включают желатин, лактозу, сахарозу, оксид титана, крахмал, кристаллическую целлюлозу, гидроксипропилметилцеллюлозу, карбоксиметилцеллюлозу, кукурузный крахмал, мелкокристаллический воск, белый вазелин, магния алюминат метасиликат, безводный фосфат кальция, лимонную кислоту, тринатрий цитрат, гидроксипропилцеллюлозу, сорбит, сложный эфир сорбитана и карбоновой кислоты, полисорбат, сложный эфир сахарозы и карбоновой кислоты, полиоксиэтилен, отвержденное касторовое масло, поливинилпирролидон, стеарат магния, кремневый ангидрид, тальк, растительное масло, бензиловый спирт, аравийскую камедь, пропиленгликоль, полиалкиленгликоль, циклодекстрин или гидроксипропилциклодекстрин и тому подобное.
В качестве препаративных форм, приготовленных в виде фармацевтических композиций, используя данные адъюванты, можно назвать твердые препаративные формы, такие как таблетки, капсулы, порошки и суппозитории; жидкие препаративные формы, такие как сиропы, элексиры и препараты для инъекций. Данные препаративные формы могут быть приготовлены традиционными способами, применяемым в области фармации. Жидкие препараты могут представлять собой форму, которую растворяют или суспендируют в воде или другой подходящей среде непосредственно перед применением. В частности, препараты для инъекций могут быть в форме раствора или суспензии в физиологическом растворе или растворе глюкозы, к которому может быть добавлен буферный агент, консервант и тому подобное.
Данные препаративные формы могут содержать соединение или соединения данного изобретения в соотношениях 1-100 мас.%, предпочтительно 1-60 мас.% в расчете на общую фармацевтическую препаративную форму. Данные препаративные формы могут содержать еще другие терапевтически активные соединения.
В тех случаях, когда соединения данного изобретения применяются в качестве аналгетика в отношении заболеваний, сопровождаемых болью, такой как раковая боль, послеоперационная боль, мигрень, подагра, хронический ревматизм, хроническая боль и невралгия; средств, улучшающих переносимость наркотических аналгетиков, представленных морфином; средств, облегчающих зависимость от наркотического аналгетика, представленного морфином, или против наркомании; усилителя аналгетиков; средств против ожирения или средств для подавления аппетита; лечебных или профилактических средств при снижении познавательной способности и возрастной деменции/амнезии, сосудисто-мозговых заболеваниях и болезни Альцгеймера; средств для лечения развивающегося нарушения познавательной способности с дефицитом внимания, гиперфункционального расстройства и неполноценности усвоения;