Бактерицидный агент и бактерицидная композиция
Иллюстрации
Показать всеИзобретение относится к области бактерицидных средств. Бактерицидный агент содержит 5,7,4′-тригидрокси-3′,5′-диметоксифлавон в качестве эффективного ингредиента против микроорганизмов Salmonella sp. и Pseudomonas aeruginosa. Бактерицидная композиция содержит указанный бактерицидный агент. Изобретение обеспечивает бактерицидную активность против Salmonella sp. и Pseudomonas aeruginosa. 2 н.п. ф-лы, 13 табл.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к бактерицидному агенту и бактерицидной композиции.
Уровень техники
В течение продолжительного времени известно, что экстракт бамбука (Sasa) имеет бактерицидную активность. Например, сообщалось, что этот экстракт имеет бактерицидное действие против Staphylococcus aureus, Pseudomonas aeruginosa и Escherichia coli, которые являются этиологическими факторами раневой инфекции (Патентные документы 1 и 2), а также против Helicobacter pilori, который считается этиологическим фактором язвы желудка.
Кумазаса является растением, принадлежащим к семейству Gramineae, роду Sasa. Обычно Sasa, растущий в горах, называют Кумазаса, причем этот термин является общим для растений Sasa, край листьев которых становится заболевающим и этиолированным зимой. Имеются различные Sasa, называемые Кумазаса, некоторые из которых имеют научное название “Sasa albo marginata Makino et Shibata”, и другие имеют названия, отличающиеся от этого названия. Кумазаса (Sasa albo marginata) растет в настоящее время почти по всей Японии, так как он искусственно культивируется.
В течение продолжительного времени известно, что Кумазаса (Sasa albo marginata) обнаруживает чрезвычайно большое разнообразие эффектов, сравнимое с Gymnema sylvestre из Индии, гуайявой (гуавой) из Китая и Lycium chinense из Южной Кореи, которые известны в качестве травяного лекарственного средства, используемого в восточной медицине. В Японии также использовали Кумазаса в качестве традиционного этнофармакологического лекарственного средства при гастропатии, сахарном диабете, гипертензии и т.д. (Непатентные документы 1-3), а также использовали в качестве упаковочного материала для пищевых продуктов, например Sasa-dango или Chimaki, а также аналептического средства.
Эксперименты на животных, выполненные в послевоенные годы, выявили, что Кумазаса имел ингибирующую активность против гепатомы в мышах, и некоторые фармакологические исследования проводились с точки зрения канцеростатического действия (Непатентный документ 4). Кроме того, проводились исследования превосходной консервирующей активности (Непатентный документ 5) и микробиологической активности (Непатентный документ 6), которые имеет Кумазаса. Однако в большинстве этих исследований не сообщалось ничего кроме анализа органических кислот с использованием газовой хроматографии. Имеется несколько сообщений, которые раскрывают выделение и очистку основных компонентов, которые обеспечивают бактерицидное действие.
Было также известно, что кумаровая кислота и ее производные имеют бактерицидную активность против E. coli, Staphylococcus aureus и Pseudomonas aeruginosa (Патентный документ 3).
Кроме того, было также известно, что экстракт Кумазаса содержит фенилпропаноиды, такие как кумаровая кислота, феруловая кислота, кофейная кислота, и ванилин, 3-гидроксипиридин и т.п., и смесь этих соединений обнаруживает бактерицидную активность против Escherichia coli, Staphylococcus aureus и Pseudomonas aeruginosa (Патентный документ 4).
Патентный документ 1: WO 00/067707
Патентный документ 2: JP 2003-201247 А
Патентный документ 3: JP 2004-359626 А
Патентный документ 4: JP 2006-36731 А
Непатентный документ 1: M. Shibata, K. Kubo, M. Onoda, Journal of the Pharmaceutical Society of Japan, 98, 1436 (1978).
Непатентный документ 2: S. Okabe, K. Takeuchi, K. Takagi, M. Shibata, Jpn. J. Pharmacol., 25, 608 (1975).
Непатентный документ 3: M. Shibata, F. Sato, K. Takeshita, K. Otani, Natural Medicines (Shoyaku-gaku zasshi), 34, 274 (1980).
Непатентный документ 4: M. Shibata, K. Kubo, M. Onoda, Folia Pharmacol. Jpn, 72, 531-541 (1976).
Непатентный документ 5: N.V. Chuyen, T. Kurata, H. Kabo, J. Antibact. Antifung. Agents, 11, 69-75 (1983).
Непатентный документ 6: N. V. Chuyen, H. Kato, Agric. Biol. Chem., 46, 2795-2801 (1982) 3-1128 (2004).
Описание изобретения
Проблемы, подлежащие решению посредством данного изобретения
Задачей данного изобретения является предоставление бактерицидного агента.
Другой задачей данного изобретения является предоставление бактерицидной композиции, содержащей этот бактерицидный агент.
Средства для решения проблемы
Данное изобретение предоставляет бактерицидный агент и бактерицидную композицию, содержащую его, следующим образом.
1. Бактерицидный агент, содержащий в качестве эффективного ингредиента по меньшей мере один ингредиент, выбранный из группы, состоящей из п-гидроксибензальдегида, 5,7,4'-тригидрокси-3',5'-диметоксифлавона, 3-гидроксипиридина и ванилина.
2. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный микроорганизм выбран из группы, состоящей из Streptococcus, Enterococcus, Staphylococcus, Escherichia, Salmonella, Yersinia, Vibrio, Pseudomonas, Bacillus и Candida.
3. Бактерицидный агент, содержащий в качестве эффективного ингредиента по меньшей мере один ингредиент, выбранный из группы, состоящей из п-гидроксибензальдегида и 5,7,4'-тригидрокси-3',5'-диметоксифлавона.
4. Бактерицидный агент согласно абзацу 3, приведенному выше, где указанный микроорганизм выбран из группы, состоящей из Streptococcus, Enterococcus, Staphylococcus, Escherichia, Salmonella, Yersinia, Vibrio, Pseudomonas, Bacillus и Candida.
5. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит 3-гидроксипиридин в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp.
6. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит п-гидроксибензальдегид в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Pseudomonas aeruginosa, Bacillus cereus, Bacillus subtilis и Candida sp.
7. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит ванилин в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Bacillus cereus, Bacillus subtilis и Candida sp.
8. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит 5,7,4'-тригидрокси-3',5'-диметоксифлавон в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Salmonella sp. и Pseudomonas aeruginosa.
9. Бактерицидная композиция, содержащая бактерицидный агент по любому из абзацев 1-8, приведенных выше.
Термин «микроорганизм» в данном контексте включает в себя бактерии, микобактерии, цианобактерии, архебактерии, грибы, дрожжи, водоросли, вирусы и тому подобное, и, в частности, этот термин обозначает микроорганизмы, которые оказывают нежелательное действие на животных и растения, в том числе на человека.
Эффекты изобретения
Бактерицидный агент в соответствии с данным изобретением имеет высокую микробиологическую активность против различных микроорганизмов, в частности Streptococcus, Enterococcus, Staphylococcus, Escherichia, Salmonella, Yersinia, Vibrio, Pseudomonas, Bacillus, Candida и т.д.; более конкретно, Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Pseudomonas aeruginosa, Bacillus cereus, Bacillus subtilis и Candida sp.
Наилучший способ осуществления изобретения
Для выяснения природы бактерицидного действия Кумазаса (Sasa albo marginata) и описания компонентов, эффективных для супрессии бактерий, авторы данного изобретения фракционировали экстракт, полученный с использованием горячей воды, листа Кумазаса при помощи различных растворителей. После фракционирования его хроматографией на силикагеле авторы выполняли разделение с использованием ТСХ, а также с использованием препаративной колонки ODS для высокоэффективной жидкостной хроматографии для достижения выделения и очистки. Кроме того, они определяли структуру выделенных соединений с использованием различных спектров и проводили микробиологические тесты с использованием 13 типов бактерий. В результате они обнаружили, что вышеописанные п-гидроксибензальдегид, 5,7,4'-тригидрокси-3',5'-диметоксифлавон (здесь также называемый далее «трицином»), 3-гидроксипиридин, транс-п-кумаровая кислота (транс-п-гидроксикоричная кислота) и ванилин проявляют специфические виды бактерицидной активности против различных микроорганизмов, завершив тем самым данное изобретение.
Данное изобретение будет далее описано в деталях.
В качестве экспериментального материала использовали экстракт Кумазаса (Sasa albo marginata), полученный с использованием горячей воды, из Hououdou Co., Ltd. (товарное название: TWEBS). Растворитель в 10 г экстракта, полученного с использованием горячей воды (далее называемого “Sa”), удаляли с получением 6,2 г сухого вещества, что показало, что экстракт, полученный с использованием горячей воды, листа Кумазаса, исходного материала, содержал 38% воды.
Этот горячий водный экстракт подвергали фракционированию с использованием различных растворителей. То есть горячий водный экстракт (Sa) жизнеспособных клеток экстрагировали этилацетатом и растворитель в полученном этилацетатном слое выпаривали с получением посредством этого растворимой в этилацетате фракции (далее называемой “Sa-1”). Водный слой дополнительно экстрагировали н-бутанолом и выполняли ту же самую обработку с получением посредством этого растворимой в н-бутаноле фракции и водного слоя. Растворимую в этилацетате фракцию (Sa-1), растворимую в н-бутаноле фракцию и водный слой, которые получали посредством этих обработок, и исходный материал - горячий водный экстракт (Sa) подвергали бактерицидному тесту против Staphylococcus aureus. В этом тесте использовали чашечный способ. В чашечном способе чашку диаметром 7,32 мм помещают на центр среды, на которой растут бактерии. Затем раствор пробы добавляют по каплям в эту чашку, и раствор пробы распределяется концентрически от этой чашки. Если проба имеет бактерицидную активность, образуется кольцо ингибирования, которое указывает на ингибирование бактериального роста. Имеется положительная корреляция между бактерицидной активностью и размером кольца ингибирования и, следовательно, степень микробиологической активности может оцениваться на основе размера кольца ингибирования. Результаты микробиологического теста против Staphylococcus aureus на каждой фракции показаны в таблице 1.
| Таблица 1 | ||
| План эксперимента | Диаметр кольца ингибирования (мм) | Оценка |
| Слепой опыт | 7,32 | - |
| Материал-источник (Sa) | 12,81 | ++++ |
| Растворимая в этилацетате фракция (Sa-1) | 12,23 | ++++ |
| Растворимая в н-бутаноле фракция | 8,37 | + |
| Водный слой | 9,64 | ++ |
| «Оценка» представляет степень бактерицидной активности следующим образом: ++++, очень сильная; ++, активность показана; +, активность слабо показана; -, нет активности.«7,32 мм» в слепом опыте указывает диаметр чашки. |
Согласно этому бактерицидному тесту, растворимая в этилацетате фракция имела бактерицидную активность, почти эквивалентную активности горячего водного экстракта Кумазаса. С другой стороны, бактерицидная активность растворимой в н-бутаноле фракции и фракции водного слоя была слабой.
Вышеописанный бактерицидный тест выявил, что бактерицидная активность была распределена в растворимой в этилацетате фракции. Таким образом, 2,3 кг горячего водного экстракта листа Кумазаса (Sa) экстрагировали этилацетатом. Растворитель в полученном этилацетатном слое выпаривали с получением 78 г растворимой в этилацетате фракции (Sa-1).
Бактерицидную активность полученной фракции Sa-1 оценивали против Staphylococcus aureus. В результате эта фракция показала бактерицидную активность.
Бактерицидная активность против Staphylococcus aureus
Фракционирование и очистка компонентов, имеющих бактерицидную активность
Фракционирование растворимой в этилацетате фракции (Sa-1)
С использованием хроматографии на нейтральном силикагеле фракционировали 52 г растворимой в этилацетате фракции (Sa-1), которая обнаруживала бактерицидную активность. Для элюции колонки использовали ступенчатый способ, в котором соотношения смешивания растворителей ступенчато изменяли. Используемыми растворителями были: н-гексан/этилацетат = 5:5 в количестве 2,5 л и 4:6, 3:7, 2:8, в каждом случае в количестве 1 л, и метанол отдельно в количестве 2,5 л. Разделение элюированных соединений выполняли на основании результата ТХА и детектирование пятен на хроматограмме выполняли с использованием УФ 254 нм. В результате растворимую в этилацетате фракцию фракционировали на 7 фракций. Эти 7 фракций были названы, соответственно, Sa-1-A (90 мг), Sa-1-B (250 мг), Sa-1-C (3,36 г), Sa-1-D (3,00 г) Sa-1-Е (110 мг), Sa-1-F (1,56 г), Sa-1G (30,0 г).
Сначала Sa-1-С (3,36 г) растворяли в 5 мл хлороформа и к раствору добавляли н-гексан в равном количестве с последующим оставлением этой смеси стоять в течение ночи. В результате эта смесь разделялась на два слоя. Верхний слой (далее называемый “Sa-1-C(1)”) и нижний слой (далее называемый “Sa-1-C(2)”) извлекали по отдельности. Количество Sa-1-C(1) было равно 2,22 г после удаления растворителя, а количество Sa-1-C(2) было равно 1,14 г.
Анализ Sa-1-(C)
К 2,22 г Sa-1-С(1) добавляли 3,50 г силикагеля и эти компоненты адсорбировали в нем с последующим фракционированием с использованием колоночной хроматографии на силикагеле. Для элюции колонки использовали ступенчатый способ. Использовали следующий состав растворителей, хлороформ:ацетон = 20:1 в количестве 2 л, и 7:3, 6:4, в каждом случае в количестве 100 мл, и только ацетон в количестве 500 мл. Для извлечения использовали флаконы объемом 50 мл. Среди 110 флаконов объемом 50 мл флаконы № 21 и 22, которые имели пятно в одном и том же положении согласно ТСХ, смешивали и полученную смесь концентрировали с получением концентрата (далее называемого “Sa-1-С(1)-а”. Этот концентрат растворяли в метаноле (0,5 мл) и фракционирование проводили с использованием препаративной колонки ODS для высокоэффективной жидкостной хроматографии (ВЖХ).
ВЖХ-разделение концентрата (Sa-1-С(1)-а) из флаконов № 21 и 22
Условия элюции: колонка: Wakosil-II 5C18HG prep, 20,0 мм × 250 мм, подвижная фаза: 20% водный раствор ацетонитрила, скорость тока: 5 мл/мин, температура колонки: 30°С, детектирование: УФ 260 нм.
Основной пик при 34,5 мин разделяли с получением 60 мг белого твердого вещества (далее называемого “Sa-1-С(1)-аа”). С использованием дейтерированного метанола измеряли 1Н- и 13С-ЯМР-спектры этого белого твердого вещества.
1Н- и 13С-ЯМР-спектры белого твердого вещества (Sa-1-С(1)-аа)
1Н-ЯМР (500 МГц, CD3OD): δ 3,91 (с, 3Н), 6,94 (д, J=8,6 Гц, 1Н), 7,42 (д, J=8,6 Гц, 1Н), 7,43 (с, 1Н), 9,74 ((с, 1Н)
13С-ЯМР (125 МГц, CD3OD): δ 56,3, 111,2, 116,3, 127,9, 130,6, 149,6, 154,6, 192,8
ИК (Kbr): 3179, 1668 см-1
Т. пл.: 114-115°С
Сигнал водорода при δ 9,74 наблюдали в 1Н-ЯМР-спектре и сигнал δ 192,8 наблюдали в 13С-ЯМР-спектре, что указывает на то, что присутствовала альдегидная группа. Сигнал при δ3,91 наблюдали в 1Н-ЯМР-спектре и сигнал δ56,3 наблюдали в 13С-ЯМР-спектре, что указывает на то, что присутствовала метоксигруппа. Далее, сигналы, соответствующие трем атомам водорода в δ 6,94 (д, J=8,6 Гц, 1Н) и δ 7,42 (д, J=8,6 Гц, 1Н), δ 7,43 (с, 1Н), и шесть сигналов в δ 111,2-154,6, происходящие из ароматического кольца, наблюдали в 13С-ЯМР-спектре. В ИК-спектре наблюдали характерное поглощение при 3179 см-1 для гидроксильной группы. Эти результаты показывают, что было расшифровано, что структура этого твердого вещества (Sa-1-С(1)-аа) соответствует 3-гидрокси-4-метоксибензальдегиду (ванилину). Поскольку ванилин был известным соединением, эти данные сравнивали с литературной оценкой (The Aldrich Library of 13С and 1Н FT NMR Spectra EDITION 1 Volume 2, Aldrich Chemical Company, Inc.). Кроме того, поскольку существовала возможность, что это соединение было изомерным изованилином, это твердое вещество (Sa-1-С(1)-аа) сравнивали с ванилином и изованилином, которые покупали в виде реагентов, с использованием колонки ODS для высокоэффективной жидкостной хроматографии (ВЖХ), посредством чего было определено, что это твердое вещество Sa-1-С(1)-аа было ванилином.
Затем, среди 110 флаконов с объемом 50 мл флаконы № 48-55, которые имели пятно в одном и том же положении согласно ТСХ, смешивали и полученную смесь концентрировали с получением 152 мг концентрата (далее называемого “Sa-1-С(1)-b”). Его фракционировали опять с использованием колоночной хроматографии на силикагеле. Для элюции колонки использовали ступенчатый способ. Используемыми растворителями были: сначала только хлороформ в количестве 200 мл, затем смесь хлороформ/ацетон = 9,5:0,5 в количестве 200 мл, 9:1, 8:2, 7,3 и только ацетон, в каждом случае в количестве 100 мл и, наконец, только метанол в количестве 200 мл. Для извлечения использовали 42 флакона на 50 мл.
Среди 42 флаконов с объемом 50 мл, флаконы № 23-33, которые имели пятно в одном и том же положении согласно ТСХ, смешивали и полученную смесь концентрировали с получением 102 мг концентрата (далее называемого “Sa-1-С(1)-ba”). Этот концентрат очищали с использованием препаративной ТСХ. Смесь хлороформ/ацетон = 7/3 использовали в качестве проявляющего растворителя и УФ 254 нм использовали для детектирования. Извлеченный силикагель подвергали элюции ацетоном и этот элюент подвергали фильтрации под вакуумом с последующим выпариванием растворителя с получением 86 мг светло-желтого твердого вещества (далее называемого “Sa-1-С(1)-baa”. С использованием дейтерированного метанола измеряли 1Н- и 13С-ЯМР-спектры этого светло-желтого твердого вещества “Sa-1-С(1)-baa”.
1Н- и 13С-ЯМР-спектры светло-желтого твердого вещества (Sa-1-С(1)-baa)
1Н-ЯМР (500 МГц, CD3OD): δ 6,92 (д, J=8,4 Гц, 2Н), 7,77 (д, J=8,4 Гц, 2Н), 9,76 (с, 1Н)
13С-ЯМР (125 МГц, CD3OD): δ 116,8, 130,2, 133,4, 165,1, 192,8
ИК (KBr): 3168, 1670 см-1
Т. пл.: 118-119°С
Сигнал водорода в δ 9,76 наблюдали в 1Н-ЯМР-спектре и сигнал δ 192,8 наблюдали в 13С-ЯМР-спектре, что указывает на то, что присутствовала альдегидная группа. Дублетный сигнал 8,6 Гц, соответствующий двум атомам водород в δ 6,92, 7,77, наблюдали в 1Н-ЯМР-спектре и четыре сигнала в δ 116,8-165,1, происходящие из ароматического соединения, наблюдали в 13С-ЯМР-спектре, что указывало на то, что имелось ароматическое кольцо, имеющее замещение в пара-положении. Далее, в ИК-спектре наблюдали характерное поглощение при 3168 см-1 для гидроксильной группы. На основании этих результатов можно было предположить, что светло-желтое твердое вещество (Sa-1-С(1)-baa) является п-гидроксибензальдегидом, имеющим альдегидную группу и гидроксильную группу в его пара-положении. Эти данные сравнивали с литературной оценкой (The Aldrich Library of 13С and 1Н FT NMR Spectra EDITION 1 Volume 2, Aldrich Chemical Company, Inc.) для определения, что это светло-желтое твердое вещество (Sa-1-С(1)-baa) было п-гидроксибензальдегидом.
Анализ Sa-1-(С(2)
Перекристаллизацию (ацетон/гексан) 1,14 г Sa-1-С(2) проводили два раза с получением 478 мг светло-желто-зеленого твердого вещества (далее называемого “Sa-1-С(2)-а”). С использованием дейтерированного метанола измеряли 1Н- и 13С-ЯМР-спектры этого светло-желто-зеленого твердого вещества (Sa-1-С(2)-а).
1Н- и 13С-ЯМР-спектры светло-желто-зеленого твердого вещества (Sa-1-С(2)-а)
1Н-ЯМР (500 МГц, CD3OD): δ 6,28 (д, J=16,0 Гц, 1Н), 6,81 (д, J=8,6 Гц, 2Н), 7,45 (д, J=8,6 Гц, 2Н), 7,61 (д, J=16,0 Гц, 1Н)
13С-ЯМР (125 МГц, CD3OD): δ 115,6, 116,8, 127,2, 131,1, 146,7, 161,1, 171,0
ИК (KBr): 3168, 2830, 975 см-1
Т. пл.: 213-214°С
Два дублетных сигнала, соответствующих четырем атомам водорода, в δ 6,81 (д, J=8,6 Гц, 2Н) и 7,45 (д, J=8,6 Гц, 2Н) наблюдали в 1Н-ЯМР-спектре, и два сильных сигнала, соответствующих двум атомам углерода, в δ 115,6 и 131,1, наблюдали в 13С-ЯМР-спектре, что указывает на то, что это соединение имело ароматическое кольцо, имеющее замещение в пара-положении. Кроме того, в 1Н-ЯМР-спектре наблюдали два атома водорода, имеющие константу взаимодействия 16,0 Гц, в δ 6,28 (д, J=16,0 Гц, 1Н) и 7,61 (д, J=16,0 Гц, 1Н), соответственно, что указывает на то, что имелась пара алкенов, локализованных в транс-положении относительно друг друга. Сигнал в δ 171,0 в 13С-ЯМР выявил существование карбонильной группы. В ИК-спектре наблюдали характерное поглощение при 3168 см-1 для гидроксильной группы. На основании этих результатов можно было предположить, что структура этого светло-желто-зеленого твердого вещества (Sa-1-(С(2)-а) является транс-п-кумаровой кислотой. Эти данные сравнивали с литературной оценкой (The Aldrich Library of 13С and 1Н FT NMR Spectra EDITION 1 Volume 2, Aldrich Chemical Company, Inc.) для определения, что это светло-желто-зеленое твердое вещество (Sa-1-С(2)-а) было транс-п-кумаровой кислотой.
Анализ Sa-1-F
К Sa-1-F (1,56 г), который был одной из фракций, полученных фракционированием растворимой в этилацетате фракции колоночной хроматографией на силикагеле, добавляли хлороформ и полученную смесь тщательно перемешивали с последующим удалением жидкого слоя, содержащего компоненты, которые растворяются в хлороформе. После этого к остатку добавляли ацетон, который не растворяется в хлороформе, и полученную смесь разделяли на растворимый в ацетоне жидкий слой (далее называемый “Sa-1-F(1)”) и не растворимый в ацетоне жидкий слой (далее называемый “Sa-1-F(2)”). Sa-1-F(1) был в количестве 162 мг после выпаривания растворителя, а Sa-1-F(2) был в количестве 1,40 г.
Анализ Sa-1-F(1)
К 162 мг Sa-1-F(1) добавляли опять ацетон для его растворения и полученную смесь оставляли стоять. После этого извлекали прозрачную светлую часть жидкого слоя. Растворитель ацетон выпаривали с получением 10 мг желтого твердого вещества (далее называемого “Sa-1-F(1)-а”). Чистоту данного соединения подтверждали с использованием колонки ODS для высокоэффективной жидкостной хроматографии (ВЖХ) для определения, что чистота была очень высокой. Было обнаружено, что это соединение проявляло сильное поглощение при УФ 260 нм.
С использованием дейтерированного ацетона измеряли 1Н- и 13С-ЯМР-спектры этого желтого твердого вещества (Sa-1-F(1)-а).
1Н- и 13С-ЯМР-спектры желтого твердого вещества (Sa-1-F(1)-а)
1Н-ЯМР (500 МГц, (CD3)2CO): δ 3,97 (с, 6Н), 6,26 (д, J=2,3 Гц, 1Н), 6,56 (д, J=2,3 Гц, 1Н), 6,74 (с, 1Н), 7,39 (с, 2Н)
13С-ЯМР (125 МГц, (CD3)2CO): δ 56,9, 94,9, 99,7, 104,7, 105,2, 105,4, 122,4, 140,9, 149,1, 158,8, 163,4, 164,9, 165,1, 183,1
ИК (KBr): 3357, 1615 см-1
Т. пл.: 276-277°С
13С-ЯМР-спектр выявил, что имелись 17 атомов углерода, и DEPT выявил, что имелись 2 первичных атома углерода, 5 третичных атомов углерода и 10 четвертичных атомов углерода. Синглетный сигнал, соответствующий 6 атомам водорода в δ3,97 (с, 6Н), наблюдали в 1Н-ЯМР-спектре и сигнал в δ56,9 наблюдали в 13С-ЯМР-спектре, что указывает на то, что имелись две эквивалентные метоксигруппы. В ИК-спектре наблюдали существование гидроксильной группы при 3357 см-1 и поглощение для карбонильной группы при 1615 см-1, которая, возможно, имела водородную связь. Масс-спектрометрия выявила, что молекулярная масса была равна 330, что позволяет предположить, что это соединение было С17Н14О7. Было сделано предположение, что это желтое твердое вещество (Sa-1-F(1)-а) является 5,7,4'-тригидрокси-3',5'-диметоксифлавоном описанной ниже формулы. Эти результаты сравнивали с литературной оценкой, посредством чего было определено, что это желтое твердое вещество было 5,7,4'-тригидрокси-3',5'-диметоксифлавоном.
Анализ Sa-1-F(2)
К 1,40 г Sa-1-F(2) добавляли 3,00 г силикагеля, и эти компоненты адсорбировались в нем, после чего проводили фракционирование с использованием колоночной хроматографии на силикагеле. Для элюции колонки использовали ступенчатый способ. Использованными растворителями были смесь хлороформ/ацетон = 10:1, 8:2 в количестве 200 мл, 5:5, 3:7 и только ацетон, в каждом случае в количестве 300 мл, и только метанол в количестве 200 мл. Для извлечения использовали 53 флакона объемом 50 мл.
Среди 53 флаконов объемом 50 мл флаконы № 42-48, которые имели пятно в одном и том же положении согласно ТСХ, смешивали и полученную смесь концентрировали с получением 46 мг светло-желтого твердого вещества (далее называемого “Sa-1-F(2)-а”). С использованием дейтерированного метанола измеряли 1Н- и 13С-ЯМР-спектры этого светло-желтого твердого вещества (Sa-1-F(2)-а).
1Н- и 13С-ЯМР-спектры светло-желтого твердого вещества (Sa-1-F(2)-а)
1Н-ЯМР (500 МГц, CD3OD): δ 7,21-7,28 (м, 2Н), 7,99 (дд, J=4,1, 0,7 Гц, 1Н), 8,09 (д, J=2,3 Гц, 1Н)
13С-ЯМР (125 МГц, CD3OD): δ 124,4, 125,9, 138,3, 140,8, 155,9
ИК (KBr): 3449 см-1
Т. пл.: 127-128°С
Сигналы, соответствующие четырем атомам водорода, в δ 7,21-7,28 (м, 2Н), δ 7,99 (дд, J=4,1, 0,7 Гц, 1Н), δ 8,09 (d, J=2,3 Гц, 1Н) наблюдали в 1Н-ЯМР-спектре, и пять сигналов в δ 124,4-155,9, происходящих из ароматического кольца, наблюдали в 13С-ЯМР-спектре. Характерное поглощение при 3168 см-1 для гидроксильной группы наблюдали в ИК-спектре. На основании этих результатов можно было предположить, что это светло-желтое твердое вещество Sa-1-F(2)-а является 3-гидроксипиридином. Эти результаты сравнивали с литературной оценкой (The Aldrich Library of 13С and 1Н FT NMR Spectra EDITION 1 Volume 2, Aldrich Chemical Company, Inc.). С учетом того, что эти результаты были близки к литературной оценке и к ее точке плавления (литературная оценка: 126-129°С), было определено, что это светло-желтое твердое вещество является 3-гидроксипиридином.
Бактерицидный тест
Способ разведения с использованием агара
В качестве бактерицидного тест-способа для транс-кумаровой кислоты, 3-гидроксипиридина, п-гидроксибензальдегида и ванилина использовали способ разведений с применением агара.
В способе разведений с использованием агара раствор, в котором растворена проба, серийно разводят несколько раз и каждый из растворов разведенных проб смешивают с агаровой средой для получения агаров для чашек, имеющих различную концентрацию проб. Затем бактерии инокулируют на эти агары для проб. В случаях, когда проба имеет бактерицидную активность, рост бактерий на этих чашках может быть ингибирован. Самую низкую концентрацию, которая может ингибировать рост этих бактерий, называют минимальной ингибирующей концентрацией (MIC), оценивая посредством этого степень бактерицидной активности пробы.
Сначала 400 мг пробы растворяли в 1 мл ДМСО с получением раствора пробы 400 мг/мл. Затем 0,5 мл этого раствора пробы 400 мг/мл разводили в 2 раза с получением раствора пробы 200 мг/мл. Таким же образом готовили раствор пробы 300 мг/мл. После этого 0,2 мл каждого из этих растворов пробы смешивали с 19,8 мл среды BHI (агара для инфузии головного мозга и сердца, (Becton Dickinson, MD) и готовили чашки с агаровой средой, имеющие концентрацию пробы 4,0 мг/мл, 3,0 мг/мл, 2,0 мг/мл, 1,0 мг/мл, 0,5 мг/мл и 0,25 мг/мл в чашках. В качестве контроля для сравнения бактерицидной активности проб готовили чашки с агаровой средой, содержащие катехин, имеющий вышеуказанные концентрации. Для растворения катехина использовали стерилизованную воду, так как катехин был нерастворимым в ДМСО.
В качестве тестируемых бактерий использовали 13 типов бактерий, т.е. Streptococcus pneumoniae, Streptococcus pyogenes, Enterococcus faecalis, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemoliticus, Pseudomonas aeruginosa, Bacillus cereus Bacillus subtilis MB-32, Bacillus subtilis ATCC6633 и Candida sp. Каждую из этих бактерий смешивали с 2 мл стерилизованной жидкой среды MBHR (Muller Hinton BrothR (Becton Dickinson, MD) для получения бактериальной суспензии, имеющей мутность 1 (концентрация бактерий 108/мл). Предварительно небольшие пробирки устанавливали в каждую ячейку решетки и стерилизовали, и 1 мл из 13 бактериальных суспензий добавляли в каждую из этих небольших пробирок, установленных в решетке, соответственно. С использованием микроплантера (SAKUMA, model: MIT-P), аликвоту 10 мкл брали из каждой тест-пробирки в этой решетке и переносили в другую тест-пробирку, и перенесенные бактериальные суспензии разводили в 100 раз (бактериальная концентрация 106/мл).
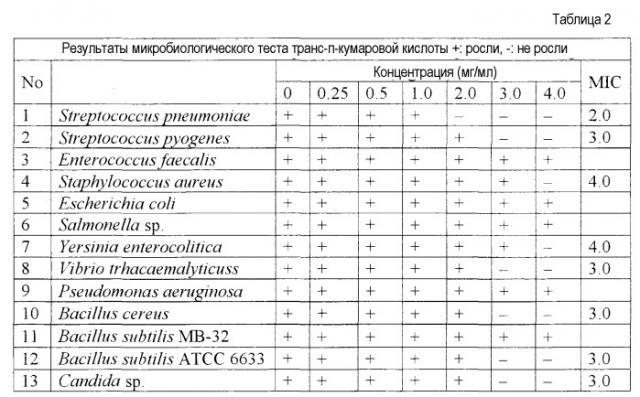
С использованием микроплантера 10 мкл (№ бактерий 14,0) этой бактериальной суспензии инокулировали на чашки, содержащие раствор проб различных концентраций. Эти чашки инкубировали в течение 18 часов в термостате при 37°С и затем оценивали бактерицидную активность каждого соединения. Эти результаты показаны в таблицах 2-6.
Описанные выше результаты показали, что транс-п-кумаровая кислота имела активность против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Vibrio parahaemoliticus, Bacillus cereus, Bacillus subtilis АТСС6633, Candida sp.. Ее MIC были 2,0 мг/мл против Streptococcus pneumoniae, 3,0 мг/мл против Streptococcus pyogenes, Vibrio parahaemoliticus, Bacillus cereus, Bacillus subtilis АТСС6633 и Candida sp. и 4,0 мг/мл против Staphylococcus aureus и Yersinia enterocolitica.
Было показано, что 3-гидроксипиридин имел активность против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp. Его MIC были 4,0 мг/мл против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp.
Было показано, что п-гидроксибензальдегид имел активность против многих типов бактерий, т.е. Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Pseudomonas aeruginosa, Bacillus cereus, Bacillus subtilis МВ-32, Bacillus subtilis АТСС6633 и Candida sp. В частности, п-гидроксибензальдегид показал сильную активность против Yersinia enterocolitica и его MIC против Yersinia была равна 0,5 мг/мл.
Было показано, что ванилин имел активность против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Bacillus cereus, Bacillus subtilis МВ-32, Bacillus subtilis АТСС6633 и Candida sp. Ванилин имел также активность против многих типов бактерий. В частности, среди них, ванилин показал сильную активность против Yersinia enterocolitica, и его MIC против Yersinia была равна 0,5 мг/мл.
Способ бумажных дисков
В качестве бактерицидного тест-способа для 5,7,4'-тригидрокси-3',5'-диметоксифлавона использовали способ бумажных дисков, при помощи которого бактерицидная активность могла оцениваться даже в случаях, когда растворитель имел некоторые действия.
В способе бумажных дисков готовят растворы пробы, имеющие различную концентрацию пробы, и раствор пробы абсорбировался в специальный бумажный диск с последующим высушиванием этого бумажного диска. На чашку, которую готовят смешиванием приготовленной бактериальной суспензии с агаровой средой, помещают бумажные диски. Если проба имеет бактерицидную активность, кольцо ингибирования, которое показывает ингибирование бактериального роста, образуется таким образом, что центр этого кольца совпадает с этим бумажным диском. Степень бактерицидной активности оценивают на основе размера кольца ингибирования.
Сначала 4 мг пробы 5,7,4'-тригидрокси-3',5'-диметоксифлавона растворяли в 200 мкл для приготовления раствора пробы 20 мг/мл. К 100 мкл этого раствора пробы 20 мг/мл добавляли 100 мкл стерилизованной воды для приготовления 200 мкл раствора пробы 10 мг/мл. К этому раствору добавляли 60 мкл ДМСО и 140 мкл стерилизованной воды для приготовления 400 мкл раствора пробы 5,0 мг/мл. ДМСО использовали в концентрации 40%, так как эта проба осаждалась из 30% ДМСО. К 350 мкл раствора пробы 5,0 мг/мл добавляли 140 мкл ДМСО и 210 мкл стерилизованной воды для приготовления 700 мкл раствора пробы 2,5 мг/мл. Таким же образом готовили растворы проб 1,25 мг/мл и 0,625 мг/мл. В качестве контроля готовили раствор, содержащий 40% ДМСО и 60% стерилизованной воды. В качестве контроля для сравнения готовили водные растворы катехина, имеющие вышеописанные концентрации. В бумажном диске (с диаметром 8,12 мм) абсорбировали каждый из этих растворов, и эти бумажные диски сушили в течение одного дня.
В качестве тестируемых бактерий использовали Staphylococcus aureus, Salmonella sp., Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp. Эти бактерии смешивали с 2 мл стерилизованной воды для приготовления бактериальных суспензий, имеющих мутность 1 (108/мл). Агар чашек готовили смешиванием 0,2 мл бактериальной суспензии с 19,8 мл среды BHI. Высушенный бумажный диск помещали на агар чашки и эту чашку инкубировали в термостате при 37°С с последующей оценкой активности. Эти результаты показаны в таблице 7. В этой таблице (-) обозначает, что не наблюдалась бактерицидная активность.
Эти результаты показывают, что 5,7,4'-тригидрокси-3',5'-диметоксифлавон имел бактерицидную активность против Salmonella sp. и Pseudomonas aeruginosa. Его бактерицидная активность была очень сильной даже в сравнении с катехином.
Горячий водный экстракт листа Кумазаса (Sa, 2,3 кг) экстрагировали этилацетатом с получением растворимой в этилацетате фракции (Sa-1, 78 г). Бактерицидный тест против Staphylococcus aureus выявил, что бактерицидная активность распределялась в растворимой в этилацетате фракции (Sa-1). Растворимую в этилацетате фракцию (Sa-1) фракционировали на 7 фракций с использованием колоночной хроматографии на нейтральном силикагеле. Эти 7 фракций были названы Sa-1-А (90 мг), Sa-1-В (250 мг), Sa-1-С (3,36 г), Sa-1-D (3,00 г), Sa-1-Е (110 мг), Sa-1-F (1,56 г) и Sa-1-G (30,0 г), соответственно. Фракцию Sa-1-С (3,36 г) разделяли на два слоя добавлением к ней хлороформа и н-гексана с получением Sa-1-С(1) (2,22 г) и Sa-1-С(2) (1,14 г). Sa-1-С(1) (2,22 г) фракционировали с использованием колоночной хроматографии на нейтральном силикагеле с получением Sa-1-С(1)-а и Sa-1-С(1)-b. Sa-1-С(1)-а фракционировали с использованием препаративной колонки ODS для высокоэффективной жидкостной хроматографии (ВЖХ) с получением 60 мг белого твердого вещества (Sa-1-С(1)-аа). Данные спектров и анализ при помощи ВЖХ выявил, что это белое твердое вещество Sa-1-С(1)-аа было ванилином. Sa-1-С-(1)-b фракционировали опять с использованием колоночной хроматографии на нейтральном силикагеле с получением Sa-1-С(1)-ba, и этот Sa-1-С(1)-ba подвергали препаративной ТСХ с получением 86 мг светло-желтого твердого вещества (Sa-1-С(1)-baa). Данные спектров выявили, что это светло-желтое твердое вещество (Sa-1-С(1)-baa) было п-гидроксибензальдегидом. Далее, Sa-1-С(2) (1,14 г) подвергали перекристаллизации два раза с получением 478 мг светло-желто-зеленого твердого вещества (Sa-1-С(2)-а). Данные спектров выявили, что это светло-желто-зеленое твердое вещество (Sa-1-С(2)-а) было транс-п-кумаровой кислотой. Затем Sa-1-F (1,56 г) разделяли на растворимую в ацетоне фракцию Sa-1-F(1) (162 мг) и не растворимую в ацетоне фракцию Sa-1-F(2) (1,40 г). Опять добавляли ацетон к Sa-1-F(1) (162 мг) и жидкий слой разделяли с получением 10 мг желтого твердого вещества (Sa-1-F(1)-а). Данные спектров выявили, что это желтое твердое вещество Sa-1-F(1)-a) было 5,7,4'-тригидрокси-3',5'-диметоксифлавоном. Далее, Sa-1-F(2) (1,40 г) подвергали колоночной хроматографии на нейтральном силикагеле с получением 46 мг светло-желтого твердого вещества Sa-1-F(2)-a). Данные спектров выявили, что это светло-желтое твердое вещество было 3-гидроксипиридином:
Бактерицидную активность ванилина, п-гидроксибензальдегида, транс-кумаровой кислоты и 3-гидроксипиридина испытывали при помощи способа разведения с использованием агара. В результате было подтверждено, что ванилин, п-гидроксибензальдегид, транс-кумаровая кислота и 3-гидроксипиридин имели бактерицидную активность. Среди них ванилин и п-гидроксибензальдегид показывали сильную бактерицидную активность против Yersinia enterocolitica, бактерии-возбудителя пищевого отравления. Для бактерицидного тестирования 5,7,4'-тригидрокси-3',5'-диметоксифлавона использовали способ бумажных дисков. В результате 5,7,4'-тригидрокси-3',5'-диметоксифлавон показал бактерицидную активность против Salmonella sp. и Pseudomonas aeruginosa. Его активность была очень сильной даже в сравнении с катехином.
Автор данного изобретения пытался экстрагировать вышеописанные эффективные компоненты из растений, других, чем Кумазаса. В результате было показано, что 5,7,4'-тригидрокси-3',5'-диметоксифлавон (трицин) существовал в изобилии во многих растениях, принадлежащих к семейству Gramineae, например в растении риса (рисе), пшенице, кукурузе, ячмене, ржи, сахарном тростнике, бамбуке (Take), Японской пампасной траве, пампасной траве, тростнике (также называемом Phragmites или Yoshi) и т.д. Конкретными названиями растений являются следующие названия:
растение риса, пшеница, ячмень, Avena fatua, рожь, просо, просо итальянское, просо японское, кукуруза, просо пальчатое, сорго, Take, дикий рис (Makomo), сахарный тростник, куикс (слезы Иовы), тростник, Японская пампасная трава, Sasa (бамбук), Arundo donax, Cortaderia argentea и газонная трава.
Семейство Gramineae
Подсемейство Bambusioideae (Семейство Bambusaceae)
Род Bambusa: Houraichiku (Bambusa multiplex (Lour.) Raeusch.), Houraichiku (Bambusa multiplex (Lour.) Raeusch. ex J.A. et J.H. Schult. “Fernleaf”) (далее упоминаемый в отношении бамбука)
Род Shibataea: Okamezasa (Shibataea kumasasa (Zoll. ex Steud.) Nakai
Род Phyllostachys: Mousouchiku (Phyllostachys heterocycla (Carriere) Matsum.), Madake (Phyllostachys bambusoides Sieb. et Zucc.), Hachiku (Phyllostachys nigra (Lodd. ex Loud.) Munro var. henonis (Bean) Stapf ex Rendle)
Род Semiarundinaria: Narihiradake (Semiarundinaria fastuosa (Mitford) Makino ex Nakai), Yashyadake (Semiarundinaria yashadake (Makino) (далее относится к Take)
Род Pleioblastus: Nezasa (Pleioblastus argenteostriatus (Regel) Nakai f. glaber (Makino) Murata), Azumanezasa (Pleioblastus chino (Franch. Et Sav.) Makino), Medake (Pleioblastus Simonii (Carr.) Nakai), Ryukyuchiku (Pleioblastus linearis (