Способ получения пропилена
Иллюстрации
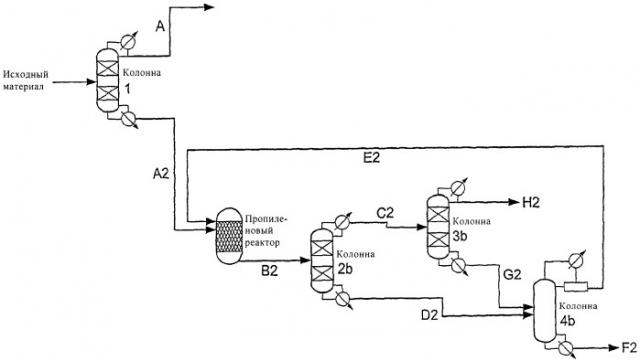
Показать всеИзобретение относится к способу получения пропилена из пропанольного исходного материала А2, характеризующемуся следующими стадиями: 1) пропанольный исходный материал А2 вступает в реакцию в парофазном реакторе, в котором при температуре, находящейся в пределах от 160 и 270°С и под давлением выше 0,1 МПа, но ниже 4,5 МПа, пропанол превращают в поток Б2 продуктов, включающий пропилен, пропиловые эфиры, воду и не подвергшиеся превращению и/или изомеризованные пропанолы, 2) упомянутый поток Б2 продуктов охлаждают, 3) упомянутый охлажденный поток Б2 продуктов разделяют в разделительной установке с получением первого потока В2, включающего пропилен и пропиловые эфиры, и второй поток Г2 продуктов, включающий воду, пропиловые эфиры и не подвергшиеся превращению и/или изомеризованные пропанолы, 4) упомянутый поток Г2 продуктов направляют в обезвоживающую установку, в которой из потока Д2 пропиловых эфиров и не подвергшихся превращению и/или изомеризованных пропанолов выделяют водный поток Е2, 5) упомянутый поток Д2 возвращают в дегидратационный реактор стадии 1, 6) упомянутый поток В2 продуктов охлаждают и 7) упомянутый охлажденный поток В2 продуктов направляют в очищающую установку, в которой из потока З2 пропилена выделяют поток Ж2 пропиловых эфиров. Также изобретение относится к способу превращения углеводородов в пропилен, включающему обозначенный выше способ. Применение настоящего изобретения позволяет усовершенствовать отделение побочных продуктов. 2 н. и 9 з.п. ф-лы, 1 ил.
Реферат
Объектом настоящего изобретения является способ получения пропилена из исходного материала, включающего пропанол.
Олефин (олефины) традиционно получают крекингом с водяным паром или каталитическим крекингом углеводородов. Однако по мере того как запасы нефти уменьшаются, цена нефти неизбежно будет увеличиваться, что делает получение легкого олефина (олефинов) дорогостоящим процессом. Таким образом, существует постоянно растущая потребность в не нефтяных путях получения олефина (олефинов) C2+, практически этилена и пропилена. Такой олефин (олефины) представляет собой эффективный исходный материал для получения многочисленных химических продуктов, включающих полимерные продукты, такие как полиэтилен и полипропилен.
В последние годы поиск альтернативных материалов для получения олефина (олефинов) C2+приводит к применению спиртов, таких как метанол, этанол и высшие спирты. Упомянутые спирты могут быть получены, например, ферментацией сахаров и/или целлюлозных материалов.
По другому варианту спирты могут быть получены из синтез-газа. Синтез-газом называют взаимодействие водорода и оксидов углерода, полученных в установке для синтез-газа из такого источника углерода, как природный газ, нефтяные дистилляты, биомасса и углеродистые материалы, включая уголь, перерабатываемые для вторичного использования пластмассы, муниципальные отходы и любой органический материал. Таким образом, спирт и производные спиртов могут явиться путями для получения олефина (олефинов) и других родственных углеводородов на не нефтяной основе.
Обычно получение оксигенатов, главным образом метанола, проводят осуществлением трех технологических стадий. Этими тремя технологическими стадиями являются получение синтез-газа, синтез метанола и очистка метанола. На стадии получения синтез-газа может быть использована дополнительная стадия, на которой исходный материал обрабатывают, например исходный материал очищают перед превращением в синтез-газ для удаления серы и других потенциальных каталитических ядов. Эта дополнительная стадия может быть также осуществлена после получения синтез-газа, например когда используют уголь или биомассу.
Способы получения смесей оксида (оксидов) углерода и водорода (синтез-газа) известны хорошо. Каждый обладает своими преимуществами и недостатками, и выбор для применения конкретного способа реформинга определяется соображениями экономики и доступности потока исходных материалов, а также целевым мольным соотношением H2:CO в исходном материале, получаемом в результате реакции реформинга. Синтез-газ может быть получен с использованием любых методов, известных в данной области техники, включая частичное окисление углеводородов, реформинг с водяным паром, реформинг с газовым нагревом, микроканальный реформинг (как это изложено, например, в US 6284217), плазменный реформинг, автотермический реформинг и любое их сочетание. Обсуждение этих технологий получения синтез-газа приведено в журналах "Hydrocarbon Processing", V 78, №4, 87-90, 92-93 (апрель 1999 г.) и "Petrole et Thechniques", №415, 86-93 (июль-август 1998 г.). Известна также возможность получения синтез-газа каталитическим частичным окислением углеводородов в микроструктурном реакторе, пример которого представлен в "IMRET 3: Proceedings of the Third International Conference on Microreaction Technology", Editor W Ehrfeld, Springer Verlag, 1999, cc. 187-196. По другому варианту синтез-газ может быть получен каталитическим частичным окислением углеводородистых исходных материалов с кратковременным контактированием так, как изложено в ЕР 0303438. Синтез-газ как правило получают посредством способа с "компактной реформинг-установкой" так, как изложено в "Hydrocarbon Engineering", 2000, 5, (5), 67-69; "Hydrocarbon Processing", 79/9, 34 (сентябрь 2000 г.); "Today's Refinery", 15/8, 9 (август 2000 г.); WO 99/02254 и WO 200023689.
В случае промышленного получения синтез-газа давление, под которым получают синтез-газ, как правило находится в интервале от приблизительно 20 до 75 бар, а температура, при которой синтез-газ выходит из реформинг-установки, находится в интервале от приблизительно 700 до 1100°C. Синтез-газ содержит водород и оксид углерода в молярном соотношении, которое, в зависимости от исходного материала для синтез-газа, находится в интервале от 0,8 до 3.
Синтез спиртов из синтез-газа требует молярного соотношения H2:CO, которое как правило находится в пределах от 1:1 до 2:1.
Авторы изобретения считают, что реакция получения спирта, такого как этанол, из синтез-газа может быть представлена следующим образом: 2 CO+4 H2→EtOH+H2O со стехиометрией реакции 2:1. Однако, в дополнение к этому, может также легко протекать реакция конверсии водяного газа и таким образом равновесие в типичных условиях синтеза спиртов сильно благоприятствует образованию диоксида углерода и водорода.
CO+H2O=CO2+H2
Таким образом, общий синтез спиртов может может быть представлен следующим образом:
3 CO+3 H2→EtOH+CO2 со стехиометрией реакции 1:1
В дополнение к этому, реакция конверсии водяного газа позволяет CO2 и H2 заменять CO. Таким образом, требуемое молярное соотношение в синтез-газе для синтеза спиртов может быть представлено следующим образом: (H2-CO2):(CO+CO2), и в этом случае требуемое значение соотношения равно 2.
Однако благодаря образованию побочных продуктов, таких как алканы, используемое молярное соотношение H2:CO на практике как правило оказывается более высоким. Получение синтез-газа, также известное, в дополнение к тому, что сказано выше, как реформинг, можно осуществлять в одну стадию, на которой протекают все потребляющие и генерирующие энергию реакции реформинга. Так, например, в единственной трубчатой установке реформинга с водяным паром реакция в общем является эндотермической, в то время как для уравновешивания теплопроизводительности в автотермическом реформинге используют сжигание некоторого количества исходного материала и продукта. Применение установки одностадийного реформинга с водяным паром обычно приводит к получению добавочного водорода. В предпочтительном другом варианте получение синтез-газа может происходить в двухстадийном способе реформинга, при осуществлении которого первичный реформинг в трубчатой установке реформинга с водяным паром совмещают со вторичной стадией реформинга со сжиганием в кислороде, на которой, если ее используют изолированно, получают синтез-газ с нехваткой водорода. С применением такого сочетания существует возможность регулировать состав используемого синтез-газа с достижением наиболее приемлемого состава для синтеза метанола. В качестве альтернативы автотермический реформинг приводит к упрощенной технологической схеме с уменьшенными капитальными затратами. Автотермический реформинг является процессом, в котором в автономно работающей реформинг-установке со сжиганием в кислороде вначале получают синтез-газ с нехваткой водорода, а затем удаляют по меньшей мере часть содержащегося диоксида углерода для того чтобы добиться целевого молярного отношения водорода к оксидам углерода.
Реакция превращения синтез-газа в оксигенаты, такие как метанол, является ограниченной экзотермическим равновесием реакцией. Превращению в метанол за проход содействуют низкие температуры, но по экономическим соображениям необходимо поддерживать равновесие между скоростью и превращением. Над гетерогенным катализатором требуются также высокие давления, поскольку реакции, в которых образуется метанол, проявляют уменьшение объема среды. Как это изложено в US №3326956, синтез метанола под низким давлением основан на катализаторе из оксида меди/оксида цинка/оксида алюминия, который среди разнообразных катализаторов, включая CuO/ZnO/Al2O3, CuO/ZnO/Cr2O3, ZnO/Cr2O3, Fe, Co, Ni, Ru, Os, Pt и Pd, как правило работает под номинальным давлением от 5 до 10 МПа и при температурах в интервале от приблизительно 150 до 450°C. Для получения метанола и диметилового эфира предпочтительны катализаторы на основе ZnO. Катализатор синтеза метанола под низким давлением на основе меди технически доступен у таких поставщиков, как фирмы BASF, ICI Ltd. of the United Kingdom и Haldor-Topsoe. Значения выхода метанола в случаях катализаторов на основе меди обычно превышают 99,5% от подвергшихся превращению содержавшихся CO+CO2. Побочным продуктом превращения синтез-газа в оксигенаты является, как известно, вода. В статье, озаглавленной "Selection of Technology for Large Methanol Plants", написанной Helge Holm-Larsen, представленной на Всемирной конференции по метанолу 30 ноября - 1 декабря 1994 г. в Женеве, Швейцария, которая включена в настоящее описание в качестве ссылки, приведен обзор разработок в получении метанола и показано, как дальнейшее снижение стоимости получения метанола скажется на конструировании очень больших установок производительностью, приближающейся к 10000 метрических т/день.
В US №4543435 описан способ превращения оксигенатного исходного материала, включающего метанол, диметиловый эфир или т.п., в реакторе превращения оксигепата в жидкие углеводороды, включающие C2-C4олефин (олефины) и углеводороды C5+. C2-C4олефин (олефины) сжимают для выделения богатого этиленом газа. Этот богатый этиленом газ возвращают в реактор превращения оксигената. В US №4076761 описан способ превращения оксигенатов в бензин с возвратом богатого водородом газообразного продукта в установку для синтез-газа или реакционную зону превращения оксигената. В US №5177114 описан способ превращения природного газа в жидкие углеводороды бензинового сорта и/или олефин (олефины) превращением природного газа в синтез-газ, превращением синтез-газа в сырой метанол и/или диметиловый эфир и последующим превращением сырого метанола/диметилового эфира в бензин и олефин (олефины). Международная заявка на патент №93/13013, поданная Kvisle и др., относится к усовершенствованному способу приготовления кремнеалюмофосфатного катализатора, который более стабилен к дезактивации от закоксовывания. В этой заявке на патент говорится, что по истечении некоторого периода времени все такие катализаторы, используемые для превращения метанола в олефин (олефины) (МвО), утрачивают способность к активному превращению метанола в углеводороды главным образом потому, что микропористая кристаллическая структура закоксовывается, т.е. заполняется низколетучими углеродистыми соединениями, которые блокируют пористую структуру. Эти углеродистые соединения могут быть удалены по обычным методам, таким как сжигание на воздухе.
В ЕРО публикации №0407038 А1 описан способ получения диалкиловых эфиров, включающий подачу потока, содержащего алифатический спирт, в дистилляционную колонну как реактора в зоне подачи, контактирование этого потока с неподвижным слоем твердой кислой каталитической дистилляционной структуры с получением соответствующего диалкилового эфира и воды и одновременное отделение ректификацией простого эфира как продукта от воды и непрореагировавших материалов.
В US №5817906 описан способ получения легкого олефина (олефинов) из сырого оксигенатного исходного материала, включающего спирт и воду. В этом способе применяют две реакционные стадии. Во-первых, с использованием реакции с дистилляцией спирт превращают в простой эфир. Затем простой эфир в дальнейшем направляют в зону превращения оксигената, содержащую металлалюмосиликатный катализатор, с получением потока легких олефинов.
Существует хорошо известный химизм, который можно использовать для получения олефина (олефинов) из спирта (спиртов), т.е. процесс метанола в олефин (олефины), МвО (как это изложено в работе Handbook of Petroleum refining processes, издание третье, глава 15.1, редактор R.A.Meyers, опубликованной издательством McGraw Hill).
Этот упомянутый процесс МвО может быть описан как дегидративная реакция метанола до олефина (олефинов). Полагают, что этот механизм осуществляется посредством взаимодействия C1 фрагментов, образуемых катализируемой кислотой дегидратацией метанола, возможно через метилоксониевый промежуточный продукт. Однако главный недостаток упомянутого процесса МвО заключается в том, что совместно с ароматическими и алкановыми побочными продуктами образуется ряд олефинов, вследствие чего, в свою очередь, выделение целевого олефина (олефинов) высокой степени чистоты сопряжено с очень большими затруднениями технологического порядка и затратами.
Как содействующие превращению оксигенатов благодаря химическому пути от метанола до олефина (МвО) к углеводородным смесям известны молекулярные сита, такие как микропористый кристаллический цеолит и нецеолитные катализаторы, особенно кремнеалюмофосфаты (SAPO). Такой метод для этих катализаторов различных типов описан в многочисленных патентах: US №№3928483, 4025575, 4252479 (Chang и др.), 4496786 (Santilli и др.), 4547616 (Avidan и др.), 4677243 (Kaiser), 4843183 (Inui), 4499314 (Seddon и др.), 4447669 (Harmon и др.), 5095163 (Barger), 5191141 (Barger), 5126308 (Barger), 4973792 (Lewis) и 4861938 (Lewis).
Реакция МвО характеризуется высокоэнергетической активацией, возможно стадией метанольной или диметилэфирной активации, вследствие чего для достижения приемлемых скоростей часто существует потребность в высоких температурах, например от 300 до 450°C. Однако, к сожалению, проведение процесса при этих упомянутых высоких температурах приводит к возникновению таких основных проблем, как дезактивация катализатора, закоксовывание и образование значительных количеств побочных продуктов. Для того чтобы свести к минимуму эти проблемы, реакции можно проводить при более низких температурах, но это требует наличия более крупногабаритных реакторов в дополнение к дорогостоящему возврату в процесс промежуточных продуктов и реагентов.
Другой главный недостаток, связанный с методом МвО, заключается в том, что совместно с олефином (олефинами) образуются ароматические и алкановые побочные продукты, отделение которых от целевых продуктов сопряжено как с затруднениями технологического порядка, так и с большими затратами; так, например, выделение этилена и этана является дорогостоящим процессом.
Эти и другие недостатки известных технических решений показывают, что существует потребность в разработке усовершенствованного и/или альтернативного способа получения олефинов C2 и C3 из спиртов.
Эти и другие недостатки позволяет устранить создание настоящего изобретения, которое относится конкретно к новому, не-МвО способу, который осуществляют посредством дегидратации пропанола до олефинов. Эта реакция дегидратации характеризуется тем, что углерод-углеродные двойные связи образуются только за счет элиминирования воды и не включают взаимодействие углеродных фрагментов, как это происходит в случае химизма МвО. Необходимо отметить, что при дегидратации пропанола образуются побочные продукты. Они могут образовываться при взаимодействии алкильных фрагментов, например при катализируемой кислотой олигомеризации олефинов, в частности:
2 пропилена → гексен.
Побочные продукты могут быть также образованы дегидрогенизацией спиртов, например
этанол → ацетальдегид + H2 (J.Catalysis, 1989, 117, сс.135-143, Y.Matsumura, К.Hashimoto и S.Yoshida).
Состояние высвобождающегося водорода может быть не таким, как у свободного водорода, а как у хемосорбированного водорода. Конкретно уместна реакция гидрогенизации с переносом, например этилен + H2 → этан
2 этанола→ ацетальдегид + этан + вода
Известно, что образование алканов с таким же числом углеродных атомов в значительной мере добавляет сложности и затрат к получению очищенных олефинов для получения полимеров. Так, например, практикуемый в промышленности каталитический крекинг углеводородных исходных материалов с получением олефинов для получения полимеров представляет собой процесс с большими капитальными затратами со значительной долей расходов, связанных с разделением олефинов и алканов с аналогичным числом углеродных атомов, т.е. отделение этана от этилена и пропана от пропилена (как это изложено в работе Handbook of Petroleum refining processes, издание третье, глава 3, редактор R.A.Meyers, опубликованной издательством McGraw Hill). Это также является недостатком процесса МвО (там же, глава 15.1). Дегидратация этанола до этилена находит промышленное применение в таких регионах, как Бразилия и Индия, хотя и в небольшом масштабе. Сообщаемые реакционные условия таковы, что высокой степени превращения в олефин за проход добиваются, например, под манометрическим давлением от 1 до 2 бар и при >350°C. Это является процессом высокой селективности, но сопровождается образованием неприемлемых для прямого применения при получении полиэтилена количеств алканов. Приемлемые количества часто цитируются как составляющие меньше 500 част./млн объединенных этана и метана. Современная практика дегидратации приводит к образованию олефинов, которые перед применением в современных способах полимеризации нуждаются в дорогостоящей очистке, так же, как и в случае МвО.
В US №5475183 описан способ получения легких олефинов дегидратацией низших спиртов, содержащих от 2 до 4 углеродных атомов, на катализаторе на основе оксида алюминия в паровой фазе. Типичные реакционные условия, приведенные в примерах, включают от 300 до 400°C и манометрическое давление от 8 до 18 бар при сообщаемых значениях селективности в отношении олефинов в пределах от 65 до 97%.
В GB №2094829 говорится о том, каким образом может быть получен этилен в нескольких парофазных адиабатических реакторах, причем части жидких продуктов, содержащие не подвергшийся превращению спирт, возвращают в процесс. Реакционные условия описаны как следующие: подача исходного материала при температуре от 400 до 520°C и под манометрическим давлением от 19 до 39 бар, а выходящий продукт перед криогенной очисткой выдерживают под манометрическим давлением по меньшей мере 18 бар. Примеры прогнозируемой селективности приведены не были. В US №4232179 также говорится о том, каким образом в адиабатических реакторах может быть дегидратирован этанол. Примеры с диоксидом кремния/оксидом алюминия и оксидом алюминия показывают, что содержание этана в получаемом этилене превышает от 923 до 100000 мас. част./млн в пересчете на этилен. Для получения полиэтилена без дополнительной очистки это неприемлемо.
В DD №245866 говорится о том, каким образом олефины с C3 по C4 могут быть получены из дериватизированных из синтез-газа смесей спиртов парофазной обработкой с цеолитным катализатором при температуре в пределах от 300 до 500°C и под давлением от 200 до 1000 кПа. Анализ примеров показывает, что происходило заметное превращение в C5 и более высокомолекулярные углеводороды. В примерах описана дегидратация смесей спиртов с C1 по C7. В примере 1 описана дегидратация смеси 76% метанола, 7,1% этанола, 4,3% этанола, 0,5% изопропанола, 4,3% н-пропанола, 3,9% изобутанола, 2% бутанолов, 2,1% амилового спирта, 0,9% гексанолов, 0,2% гептанолов + остальные, другие оксигенаты, с получением 143,2 г этилена, 96,8 г пропена, 77,9 г бутена, 174,3 г углеводородов C5+. Ясно, что на модифицированном цеолитном катализаторе происходит заметное превращение низших углеродных остатков в высшие углеродные фрагменты.
В US №4398050 описаны синтез потока смешанных спиртов и очистка с получением смеси этанола и пропанола, которые в дальнейшем дегидратируют под давлением от 0,5 до 1 бара и при температуре от 350 до 500°C (пример 1). В первичной формуле изобретения упоминается удаление метанола перед дегидратацией, но не удаление C4 и более высокомолекулярных спиртов.
В US №4423270 описана парофазная дегидратация этанола под атмосферным давлением над нанесенной на носитель фосфорной кислотой как катализатором с добавляемыми водой и алкилзамещенной фосфорной кислотой. Используемые реакционные температуры находились в пределах от 300 до 400°C, а эксперименты проводили под атмосферным давлением в стеклянной трубке. Сообщаемые значения выхода этилена находились в интервале от 88 до 101%, ни о каких подробностях образования побочных продуктов не сказано.
В патенте US №4727214 описана дегидратация этанола над кристаллическим алюмосиликатным цеолитом. Заявленные условия составляют: давление в пределах от 1 до 10 бар и температура от 126 до 526°C. Подробности образования побочных продуктов сведены в один десятичный разряд и сообщается, что селективность в отношении этилена составляет 100%. Однако из патента не ясно, может ли быть получен этилен как материал приемлемого для полимеров сорта без дополнительной очистки для удаления этана.
Основываясь на доступной ограниченной экспериментальной информации о дегидратации н-пропанола (Journal of Catalysis 169, 67-75 (1997) G.Larsen и др., J.Phy.Chem. В 109/8 3345-3354), авторы настоящего изобретения установили, что дегидратация протекает аналогично тому, как сообщается в отношении этанола, с образованием аналогичных побочных продуктов, например алканов, альдегидов, кетонов, олигомеров. Однако скорость образования олигомеров оказывается более значительной.
Объектом настоящего изобретения является способ получения пропилена из пропанола.
На чертеже представлен один вариант технологической схемы в соответствии с настоящим изобретением. Этот вариант включает необязательные и/или предпочтительные технологические стадии в соответствии с настоящим изобретением. Буквенные ссылки соответствуют тем, которые использованы в настоящем описании и прилагаемой формуле изобретения.
Объектом настоящего изобретения является способ получения пропилена из пропанольного исходного материала А2, характеризующийся следующими стадиями:
1) пропанольный исходный материал А2 вступает в реакцию в парофазном реакторе, в котором пропанол превращают в поток Б2 продуктов, включающий пропилен, пропиловые эфиры, воду и не подвергшиеся превращению и/или изомеризованные пропанолы,
2) упомянутый поток Б2 продуктов охлаждают,
3) упомянутый охлажденный поток Б2 продуктов разделяют в разделительной установке с получением первого потока В2, включающего пропилен и пропиловые эфиры, и второй поток Г2 продуктов, включающий воду, пропиловые эфиры и не подвергшиеся превращению и/или изомеризованные пропанолы,
4) упомянутый поток Г2 продуктов направляют в обезвоживающую установку, в которой из потока Д2 пропиловых эфиров и не подвергшихся превращению и/или изомеризованных пропанолов выделяют водный поток Е2,
5) упомянутый поток Д2 возвращают в дегидратационный реактор стадии 1,
6) упомянутый поток В2 продуктов охлаждают,
7) упомянутый охлажденный поток В2 продуктов направляют в очищающую установку, в которой из потока З2 пропилена выделяют поток Ж2 пропиловых эфиров, и
8) поток Ж2 пропиловых эфиров необязательно возвращают либо в обезвоживающую установку стадии 4, либо непосредственно в дегидратационный реактор стадии 1.
В соответствии с предпочтительным вариантом объектом настоящего изобретения является способ превращения углеводорода в пропилен, в котором пропанольный исходный материал А2, используемый на представленной выше стадии 1, поступает из процесса разделения смешанного этанольного и пропанольного оксигенатного исходного материала.
В соответствии с другим предпочтительным вариантом объектом настоящего изобретения является способ превращения углеводородов в пропилен, включающий следующие стадии:
а) превращение углеводородов в реакторе синтез-газа в смесь оксида (оксидов) углерода и водорода,
б) превращение упомянутой смеси оксида (оксидов) углерода и водорода со стадии (а) в присутствии порошкообразного катализатора в реакторе при температуре, находящейся в пределах от 200 до 400°C, и под давлением от 5 до 20 МПа в исходный материал, включающий пропанол, и
в) применение по меньшей мере части упомянутого исходного материала, включающего пропанол, в качестве пропанольного исходного материала А2 и проведение процесса в соответствии со стадиями с 1 по 8, приведенными в настоящем описании выше, и в соответствии с настоящим изобретением с получением упомянутого пропилена.
При осуществлении способов по изобретению может быть использован любой поток углеводородсодержащего сырья, который может быть подвергнут превращению в исходный материал, включающий моноксид углерода и водород, наиболее предпочтительно синтез-газ.
Углеводородный исходный материал, используемый для получения синтез-газа, в предпочтительном варианте представляет собой углеродистый материал, например биомассу, пластик, бензино-лигроиновую фракцию, кубовые остатки нефтепереработки, отходящий из плавильной печи газ, муниципальные отходы, уголь, кокс и/или природный газ, причем предпочтительным углеродистым материалом являются уголь и природный газ, а наиболее предпочтительный углеводородный исходный материал представляет собой природный газ.
Исходные материалы, включающие моноксид углерода и водород, например синтез-газ, перед подачей в любые реакционные зоны можно подвергать очистке. Очистку синтез-газа можно проводить по способам, известным в данной области техники (см., например, Weissermel, К. и Arpe H.-J. в работе Industrial Organic Chemistry, издание второе, переработанное и расширенное, 1993, сс.19-21).
В соответствии с настоящим изобретением способ получения олефинов из спиртов осуществляют посредством дегидратации упомянутых спиртов. Эти реакции дегидратации отличаются от вышеупомянутого процесса МвО тем, что хотя в процессе дегидратации никакого взаимодействия углеродных фрагментов не требуется, во время элиминирования воды образуется двойная связь C-C, и в результате может быть достигнута очень высокая селективность. Обычно условия, применяемые в процессе МвО, оказываются намного более жесткими, чем условия, применяемые при дегидратации спиртов, представленной в настоящем описании.
Дегидратация исходного материала в соответствии с настоящим изобретением протекает, как полагают (Chem. Eng. Comm. 1990, том 95, сс.27-39, C.L.Chang, A.L.DeVera и D.J.Miller) либо непосредственно как дегидратация до олефина (олефинов) и воды;
уравнение 1
либо посредством простого эфира как промежуточного продукта;
уравнение 2
уравнение 3
где R обозначает этильную или пропильную группу, R' обозначает водородный атом или метальную группу.
Сообщается также о прямом превращении простого эфира в два моля олефина и воду (Chem.Eng.Res. and Design 1984, том 62, сс.81-91).
Все реакции, представленные выше, как правило катализируют кислотами Льюиса и/или Бренстеда. Уравнение 1 демонстрирует эндотермическое прямое элиминирование спирта до олефина (олефинов) и воды; с уравнением 1 конкурируют уравнения 2 и 3, т.е. экзотермическая реакция этерификации (уравнение 2) и эндотермическое элиминирование простого эфира (эфиров) с получением олефина (олефинов) и спирта (уравнение 3). Однако о реакции дегидратации спиртов до олефина (олефинов) в общем говорят как о являющейся эндотермической.
Как сказано в настоящем описании выше, осуществление способа в соответствии с настоящим изобретением в предпочтительном варианте начинают с оксигенатного исходного материала, включающего этанол и пропанол, например смесь этанола и н-пропанола и/или изопропанола.
Упомянутый оксигенатный исходный материал может включать гомо- и смешанные простые эфиры этих спиртов, например диэтиловый эфир, н-пропиловый эфир, этил-н-пропиловый эфир, этилизопропиловый эфир, н-пропилизопропиловый эфир и изопропиловый эфир.
Оксигенатный исходный материал в предпочтительном варианте включает в качестве спиртов смесь только этанола и н-пропанола.
В соответствии с настоящим изобретением молярное отношение этанола к н-пропанолу в оксигенатном исходном материале, из которого должен быть выделен пропанольный исходный материал А2, в предпочтительном варианте превышает 1:2, но меньше 20:1, а более предпочтительно превышает 1:1, но меньше 10:1, наиболее предпочтительно превышает 2:1 и меньше 5:1.
В соответствии с предпочтительным вариантом выполнения настоящего изобретения оксигенатный исходный материал и/или исходный материал А2 обладают содержанием изопропанола меньше 5 мас.%, предпочтительнее меньше 1 мас.%, наиболее предпочтительно меньше 0,1 мас.%, а в идеальном варианте изопропанола не содержит
Предпочтительная характеризующая особенность в соответствии с настоящим изобретением заключается в том, что оксигенатный исходный материал и/или исходный материал А2 обладает общим содержанием спиртов C3+ (причем спирты C3+ определяют как спирты, содержащие по меньшей мере 4 углеродных атома, например н-бутанол, изобутанол, пентанол) меньше 5 мас.%, предпочтительно меньше 1 мас.%, наиболее предпочтительно меньше 0,1 мас.%, а в идеальном варианте спиртов C3+ не содержит. В соответствии с настоящим изобретением с целью уменьшить/удалить из соответствующего исходного материала продукты C3+ можно использовать обычную дистилляцию.
В самом деле, при создании настоящего изобретения было установлено, что присутствие спиртов C3+ оказывается вредным для осуществления способа получения олефина (олефинов) по настоящему изобретению; так, например, авторы настоящего изобретения полагают, что эти спирты ответственны за увеличение образования алканов во время получения олефинов.
Другой предпочтительный вариант в соответствии с настоящим изобретением заключается в том, что оксигенатный исходный материал и/или исходный материал А2 обладают содержанием метанола меньше 5 мас.%, предпочтительно меньше 2 мас.%, наиболее предпочтительно меньше 0,5 мас.%, а в идеальном варианте метанол отсутствует. Удаление метанола может обусловить соответствующие преимущества, т.е.
(I) предотвращение образования диметилового эфира - ДМЭ трудно отделить от пропилена и этилена, если сравнивать с диэтиловым эфиром,
(II) предотвращение химизма МвО,
(III) предотвращение алкилирования олефинов, например пропилена до бутена,
(IV) предотвращение образования метилэтилового эфира (который трудно отделить от этилена),
(V) меньше отходов,
(VI) пониженная токсичность,
(VII) более низкое давление пара - легче транспортировать,
(VIII) улучшенное соотношение C:O в исходном материале для транспортировки, т.е. меньше образование воды.
В соответствии с настоящим изобретением с целью уменьшить количество/удалить метанол и спирты C3+ из соответствующего исходного материала можно использовать обычную дистилляцию.
Когда с представленной выше стадии б) получают смешанный этанольный и пропанольный исходный материал, тогда в предпочтительном варианте осуществляют разделение этанольного и пропанольного исходного материала на этанольный исходный материал А и пропанольный исходный материал А2. Упомянутое разделение в предпочтительном варианте осуществляют в обычной дистилляционной колонне.
Это разделение в предпочтительном варианте осуществляют таким образом, что получаемый пропанольный исходный материал А2 включает меньше 5 мас.% этанола (например, меньше 1 мас.% этанола, в частности меньше 0,1 мас.% этанола; например, А2 этанола не содержит). Предпочтительные реакционные условия парофазной дегидратации в соответствии со стадией 1 по настоящему изобретению являются такими, в которых в реакторе происходит умеренное превращение в олефин. Поток жидких продуктов после удаления олефинов включает в основном непрореагировавшие спирты, простые эфиры и воду. В предпочтительном варианте основную часть спиртов и простых эфиров после удаления воды как побочного продукта возвращают в дегидратационный реактор. Как указано в настоящем описании выше, пропанол может существовать в виде двух изомеров, н-пропанола и изопропанола; эти изомеры в упомянутых реакционных условиях способны к взаимопревращению, вследствие чего спиртовой рецикловый поток может включать некоторое количество изопропанола, в дополнение к непрореагировавшим этанолу и н-пропанолу. Эта изомеризация может также повлиять на соединения, содержащиеся во фракции простых эфиров рециклового потока. Принимая во внимание цель настоящего изобретения и прилагаемую формулу изобретения, умеренное превращение пропанольного исходного материала А2 в пропилен означает, что за проход превращают от 10 до 80%, более предпочтительно от 20 до 60% упомянутого пропанола. При этом "превращение" определяют как являющееся соотношением между числом молей получаемого пропилена и числом молей пропанола совместно с дериватизированными из пропанола фрагментов в простых эфирах (как это указано в последующих абзацах), которые направляют в упомянутый парофазный дегидратационный реактор (реакторы).
Что касается генерирующего пропилен реактора, то в соответствии с настоящим изобретением во время стадии дегидратации получают некоторое количество дериватизированного из пропанола простого эфира (эфиров), такого как ди-н-пропиловый эфир, н-пропилизопропиловый эфир и диизопропиловый эфир. В предпочтительном варианте в соответствии с настоящим изобретением осуществляют дополнительную стадию разделения. Таким образом, в предпочтительном варианте из олефина (олефинов) выделяют по меньшей мере 80 мас.%, более предпочтительно по меньшей мере 90 мас.%, наиболее предпочтительно по меньшей мере 99 мас.%, еще более предпочтительно по меньшей мере 99,9 мас.%, простого эфира (эфиров). Затем по меньшей мере часть (предпочтительнее все количество) выделенного простого эфира (эфиров) в предпочтительном варианте возвращают в парофазный дегидратационный реактор (реакторы).
В соответствии с одним из вариантов выполнения настоящего изобретения перед поступлением в парофазный дегидратационный реактор стадии 1 по меньшей мере часть, предпочтительно все количество, упомянутого возвращаемого в процесс простого эфира предварительно смешивают со свежим пропанольным исходным материалом (поток А2).
Образование простых эфиров термодинамически благоприятно. Такое образование простых эфиров упрощает выделение воды из рециклового потока. Этанол, н-пропанол и изопропанол все полностью или в значительной мере смешиваются с водой и легко образуют с водой азеотропы, которые таким образом затрудняют выделение воды, побочного продукта реакции, из рецикловых потоков. Однако образование таких простых эфиров, как диэтиловый эфир и ди-н-пропиловый эфир (которые оба обладают ограниченной смешиваемостью с водой и азеотропом с очень низким содержанием воды), позволяет извлекать воду применением декантатора, даже в присутствии непрореагировавших спиртов.
В соответствии с настоящим изобретением наличие воды в пропанольных исходных материалах А2, которые должны быть дегидратированы, допустимо; упомянутые исходные материалы могут включать до 50 мас.% воды, но в предпочтительном варианте упомянутые исходные материалы включают меньше 25 мас.% воды, а в наиболее предпочтительном варианте исходный материал включает меньше 20 мас.% воды. Однако вследствие технологических затрат, в частности из-за размера реактора, тепла выпаривания и теплоемкости воды, в предпочтительном варианте процесс проводят с исходными материалами, содержащими уменьшенные количества воды, например меньше 10 мас.%, предпочтительно меньше 5 мас.%, воды. Когда в качестве катализаторов используют гетерополикислоты, количество воды в контакте с катализатором может повлиять на стабильность и активность катализатора. Так, например, гетерополикислоты демонстрируют пониженную стабильность катализатора при низких концентрациях воды (<1 мас.%) и пониженную активность при высоких концентрациях воды (>50 мас.%). Для специалиста в данной области техники очевидно, что оптимальная концентрация воды обычно зависит от взаимодействия сложной совокупности переменных, включая состав спиртового сырья, давление, температуру и природу используемой гетерополикислоты. Другими словами, осуществление предлагаемого способа создает хорошую возможность для выделения воды и, следовательно, упрощает применение биоэтанола и другого биоспирта (биоспиртов). Проведение процесса при среднем превращении с удалением воды во время возврата в процесс характеризуется тем преимуществом, что это позволяет сводить в одной точке оптимальные реакционные условия процесса. Присутствие воды в исходном материале может также увеличить трудность выделения спирта вследствие наличия азеотропов спирта/воды, кото