Этидий этилсульфат - флуоресцентный краситель для обнаружения нуклеиновых кислот
Иллюстрации
Показать всеНастоящее изобретение относится к области органической химии, а именно к новому химическому соединению - флуоресцентному красителю этидий этилсульфату (3,8-диамино-5-этил-6-фенилфенантридиний этилсульфату) формулы I, усиливающему интенсивность флуоресценции при экспозиции в УФ-свете в результате связывания с нуклеиновыми кислотами. Технический результат: получено новое соединение, которое может быть применимо при обнаружении ДНК. 2 ил.
Реферат
Изобретение относится к новому химическому соединению, конкретно к этидий этилсульфату (3,8-диамино-5-этил-6-фенилфенантридиний этилсульфату), формулы I:
который может использоваться как флуоресцентный краситель для обнаружения нуклеиновых кислот.
Аналог этидий этилсульфата - этидий бромистый широко используется в молекулярной биологии, генной инженерии и диагностической медицине для обнаружения нуклеиновых кислот {[1]. Маниатис Т., Фрич Э., Сэмбрук Дж. Методы генетической инженерии. Молекулярное клонирование. Пер. с англ. М.: Мир, 1984. 480 с., [2]. Pat. 4683202 U.S., Int. C1. C12Q 1/68, C12N 15/10, B01L 7/00, C07K 14/795, C07K 14/805. US C1. 435/91.2, 435/317.1, 435/320.1, 536/23.1, 536/24.33. Process for amplifying nucleic acid sequences. [3]. Using molecular marker technology in studies on plant genetic diversity, DNA-based technologies. PCR-based technologies. Sequence-tagged sites (Microsatellites, SCARs, CAPS, ISSRs), IPGRI and Cornell University, 2003. 38 pp.}.
Целью изобретения является синтез флуоресцентного красителя, обладающего свойством усиления интенсивности флуоресценции при экспозиции в УФ-свете в результате связывания с нуклеиновыми кислотами.
Поставленная цель достигается новым химическим соединением этидий этилсульфатом формулы (I), обладающим свойством усиления интенсивности флуоресценции при экспозиции в УФ-свете в результате связывания с нуклеиновыми кислотами.
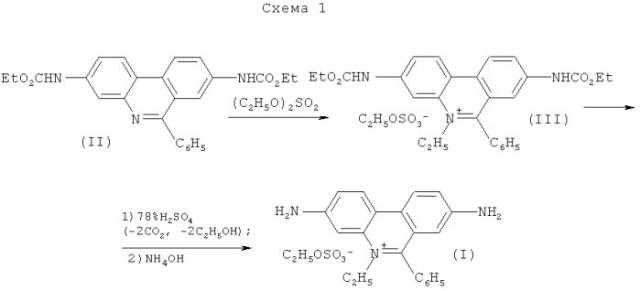
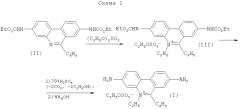
Синтез соединения (I) осуществлялся в соответствии со схемой 1.
Первая стадия этого синтеза - кватернизация 3,8-дикарбоэтоксиамино-6-фенилфенантридина (II) с диэтилсульфатом. Причем диэтилсульфат выступает в качестве реагента и растворителя. Смесь 3,8-дикарбэтоксиамино-6-фенилфенантридина (II) и диэтилсульфата нагревали 30 мин при 160-165°C. После остывания смесь растерли с сухим эфиром, продукт отфильтровали, промыли сухим эфиром и сухим ацетоном. Получили с 87%-ным выходом этилсульфат (III). Строгое доказательство состава и строения полученного продукта кватернизации осуществляется на основании данных элементного анализа и анализа спектров (ЯМР 1H, ИК и ЭСП) продукта. Установлено образование 3,8-дикарбоэтоксиамино-6-фенилфенантридиний этилсульфата (III) с выходом 87%.
На второй стадии синтеза неочищенный этилсульфат (III) подвергали гидролизу в среде 78%-ной серной кислоты при 135-140°C в течение 1 часа при перемешивании для удаления карбоэтоксигрупп. Смесь охладили и вылили в ледяную воду. При перемешивании добавили по каплям 25%-ный раствора аммиака. Смесь экстрагировали н. бутанолом. Из н. бутанольного экстракта, оставленного при 0÷/+5°C на 16 ч, отфильтровали мелкокристаллический темно-красный осадок, высушили на воздухе и перекристаллизовали из горячей воды. Получили с 61%-ным выходом этидий этилсульфат (I).
Строение соединения (I) установлено на основании данных элементного анализа, спектра ЯМР 1H, который аналогичен спектру этидия бромистого {[4]. Firth W.J., Watkins C.L., Graves D.E., Yielding L.W. // J. Heterocycl. Chem. 1983. V.20. N 3. P.759-765}, и спектров ИК и ЭСП. Спектры эмиссии флуоресценции водных растворов этих двух соединений практически идентичны.
Проведена сравнительная характеристика практического применения нового флуоресцентного красителя этилсульфата этидия (I) и стандартно применяемого бромистого этидия для обнаружения ДНК. Установлена практически одинаковая чувствительность этих красителей при обнаружении амплифицированных ДНК, полученных в результате полимеразной цепной реакции. Таким образом, новое соединение может быть использовано для замены этидия бромистого при обнаружении нуклеиновых кислот.
ИК-спектры записывали на спектрометре Vector 22 в таблетках с KBr, электронные спектры поглощения (ЭСП) - на спектрофотометре Specord UV-vis (10-4 н. растворы в спирте), спектры эмиссии флуоресценции (СЭФ) - на флуоресцентном спектрофотометре Саrу Eclipse фирмы «Varian» (возбуждение при длинах волн, имеющих λмакс: 247, 333 и 486 нм, облучение 10-4 н. растворов в H2O). Температуры плавления определяли на аппарате Kofler. Спектры ЯМР 1H записаны на приборе Bruker AC 200 (1H - 200.13 МГц) для растворов при 25°C с резонансной стабилизацией по сигналу дейтерия растворителя ДМСО-D6. Химические сдвиги (м.д.) измеряли относительно сигналов внутренних стандартов: ДМСО (δн 2.50 м.д.).
Фиг.1 - Окрашивание геля: A - этидий этилсульфатом (0,5 мкг/мл), B - бромистым этидием (0,5 мкг/мл).
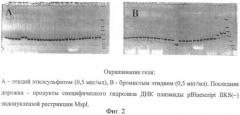
Фиг.2 - Окрашивание геля: A - этидий этилсульфатом (0,5 мкг/мл), B - бромистым этидием (0,5 мкг/мл). Последняя дорожка - продукты специфического гидролиза ДНК плазмиды pBluescript IIKS(-) эндонуклеазой рестрикции MspI.
Данное изобретение иллюстрируется примерами
Пример 1. 3,8-Дикарбоэтоксиамино-5-этил-6-фенилфенантридиния этилсульфат (III). Смесь 1.48 г (3.45 ммоля) 3,8-дикарбоэтоксиамино-6-фенилфенантридина (II) и 2.59 г (16.8 ммоля) диэтилсульфата нагревали 30 мин при 160-165°C. Наблюдали интенсивную кристаллизацию в первоначально образующемся растворе. После остывания смесь растерли с 10 мл сухого эфира, продукт отфильтровали, промыли 3×3 мл сухого эфира, 3×3 мл сухого ацетона. Получили 1.74 г (87%) этилсульфата (III), т. разл. 200-220°C (без расплавления).
Найдено, %: C 59.47, 59.32; H 5.97, 5.87; N 7.31, 7.32; S 5.50, 5.70. C29H33N3O8S.
Вычислено, %: C 59.67, H 5.71, N 7.20, S 5.49.
Спектр ЯМР 1H (5%-ный раствор в ДМСО-D6, δ/м.д., J/Гц): 1.09, 1.18 и 1.30 (все т, по 3 H, J=7, три группы CH3 трех фрагментов C2H5O); 1.51 уш. т (3 H, J=7, группа CH3 фрагмента C2H5N); 3.73, 4.06 и 4.22 (все к, по 2 H, J=7, три группы CH2 трех фрагментов C2H5O); 4.63 уш. к (2 H, J=7, группа CH2 фрагмента C2H5N); 7.7-7.9 м (6 H, H-4 или H-7 и C6H5); 8.02 и 8.18 (оба д.д, по 1 H, J=9 и J=2, H-2, H-9); 8.72 д (1 H, J=2, H-7 или H-4); 8.95 и 9.01 (оба д, по 1 H, J=9, H-1, H-10); 10.24 и 10.51 (оба с, по 1 H, 2 группы NH).
ИК-спектр, KBr: 720, 730, 760, 780, 930, 1030, 1080, 1090, 1100, 1160, 1190, 1240, 1320, 1350, 1380, 1410, 1490, 1540, 1570, 1590, 1610, 1630, 1730 см-1 (C=O). ЭСП (EtOH) λмакс/нм (lg ε): 217 (4.54), 285 (4.80) и 425 (3.82).
Пример 2. 3,8-Диамино-5-этил-6-фенилфенантридиния этилсульфат (этидий этилсульфат) (I). Раствор 1.00 г (1.74 ммоля) этилсульфата (III) в 2.79 мл 78%-ной серной кислоты (содержит 37.8 ммоля H2SO4) нагревали 1 ч при 135-140°C при перемешивании. В образовавшемся темноокрашенном растворе наблюдали выделение газа, в конце выдержки раствор посветлел, выделение газа заметно ослабело. Смесь охладили и вылили в 2.5 мл ледяной воды. При перемешивании добавили по каплям 10 мл 25%-ного раствора аммиака (133 ммоля NH3), наблюдали образование темно-красного смолистого осадка. Смесь экстрагировали 2 раза по 4 мл н. бутанола. Водный слой после экстракции стал почти бесцветным. Из н. бутанольного экстракта, оставленного при 0÷/+5°C на 16 ч, отфильтровали мелкокристаллический темно-красный осадок, высушили на воздухе и перекристаллизовали из 5.2 мл горячей воды. Получили 0.48 г (61%) этидий этилсульфата (I), т.пл. 250-252°C (с разл.).
Найдено, %: C 63.23, 62.90; H 5.89, 5.87; N 9.68, 9.65; S 7.60, 7.30. C23H25N3O4S.
Вычислено, %: C 62.84, H 5.74, N 9.56, S 7.29.
Спектр ЯМР 1H (5%-ный раствор в ДМСО-D6, δ/м.д., J/Гц): 1.10 т (3 H, J=7, CH3 этилсульфатной группы); 1.40 уш. т (3 H, J=7, группа CH3 фрагмента C2H5N); 3.74 к (2 H, J=7, группа СН2 этилсульфатной группы); 4.47 уш. к (2 H, J=7, группа CH2 фрагмента C2H5N); 5.93 и 6.36 (оба уш. с по 2 H, 2 группы NH2); 6.25 д (1 H, J=2, H-7); 7.3-7.4 м (2 H, H-2, H-4); 7.51 д.д (1 H, J=9 и J=2, H-9); 7.7-7.8 м (5 H, С6Н5); 8.60 и 8.65 (оба д, по 1 H, J=9, H-10 и H-1 соответственно). Отнесения сигналов в спектре ЯМР 1H сделаны по аналогии с приведенными лит. данными [4] для этидия бромистого.
ИК-спектр, KBr: 720, 790, 840, 930, 1030, 1070, 1170, 1190, 1220, 1240, 1280, 1330, 1410, 1480, 1490, 1510, 1640 см-1. ЭСП (MeOH), λмакс/нм (lg ε): 216 (4.61), 293(4.81) и 528 (3.81). СЭФ (H2O): λмакс 619 нм. Для этидия бромистого фирмы «Fluka» СЭФ (H2O): λмакс 619 нм.
Пример 3. Сравнение чувствительности выявления двухцепочечной ДНК этидием бромидом и этидий этилсульфатом.
Для проверки чувствительности выявления двухцепочечной ДНК этидием бромидом и этидий этилсульфатом продукты специфического гидролиза ДНК плазмиды pBluescript IIKS(-) эндонуклеазой рестрикции MspI в количествах 200 нг, 150 нг, 100 нг и 50 нг на дорожку анализировали электрофорезом в 6% акриламидном геле. Для получения 6%-ного или 8%-ного ПААГ к 6%-ному или 8%-ному раствору ПАА в 0,5×ТВЕ добавляли 1/100 ПСА и 1/1000 ТЕМЕД. Гель заливали между двумя стеклами, расположенными горизонтально и соединенными зажимами, вставляли гребенку. После полимеризации гель использовали для проведения электрофореза.
Вертикальный электрофорез проводили в буфере 0,5×ТВЕ. Раствор анализируемой ДНК смешивали с буфером для нанесения (1:10) и помещали в карманы геля, подвергали электрофорезу (10 V/см). Гель окрашивали бромистым этидием или этидий этилсульфатом (0,5 мкг/мл) в течение 15 мин, визуализировали ДНК под УФ-светом. Изображение фиксировали с помощью CD-камеры Watec AD-901 (Watec Co., LTD. Japan). Результаты сравнения представлены на фиг.1.
Из чертежа видно, что оба метода окрашивания геля имеют практически одинаковую чувствительность.
Пример 4. Использование этидия бромида и этидия этилсульфата для выявления продуктов ПЦР после электрофореза в 5%-ном полиакриламидном геле.
Для проверки использовали амплификацию и анализ длины точного тандемного повтора ETRD на образцах ДНК 60 изолятов M.tuberculosis из Западно-Сибирского региона РФ. ПЦР проводили с олигонуклеотидными праймерами
ETRD-1 GTCAAACAGGTCACAACGAGAGGAA
ETRD-2 CCTCCACAATCAACACACTGGTCAT
в конечном объеме 20 мкл, содержащем 67 мМ трис. - HCl (pH 8,9), 16 мМ сульфата аммония; 1,5 мМ MgCl2; 0,01% Твин 20; 0,2 мМ дНТФ; по 0,5 мкМ растворов олигонуклеотидных праймеров, 1 ед. акт. Taq-ДНК-полимеразы.
Реакцию проводили на амплификаторе «Терцик» («ДНК-Технология», Россия) с начальной денатурацией при 96°C 2 мин, далее в течение 35 циклов с денатурацией при 95°C 5 сек, отжигом при температуре 62°C в течение 10 сек и элонгацией при 72°C 10 сек. Финальная элонгация проводилась при 72°C 5 мин. Продукт амплификации анализировали в 6% акриламидном геле.
Результаты выявления продуктов ПЦР представлены на фиг.2.
Анализ полученных электрофореграмм позволяет заключить, что этидий сульфат пригоден для выявления продуктов ПЦР при их электрофоретическом анализе.
При этом заявляемое соединение является более дешевым по сравнению с этидием бромистым, так как в его синтезе устраняется необходимость затрат реактивов и времени на замену промежуточного аниона анионом брома и выделения этидия бромистого.
Этидий этилсульфат формулы (I), обладающий свойствами флуоресцентного красителя для обнаружения нуклеиновых кислот.