Композиции, содержащие эпотилон, и способы их получения
Иллюстрации
Показать всеИзобретение относится к композиции для лечения злокачественного новообразования у пациента, которая содержит эпотилон - (1S, 3S, 7S, 10R, 11S, 12S, 16R)-7,11-дигидрокси-3-(2-метил-бензотиазол-5-ил)-10-(проп-2-ен-1-ил)-8,8,12,16-тетраметил-4,17-диоксабицикло[14.1.0] гептадекан-5,9-дион, гидроксипропил-β-циклодекстрин или простой сульфобутиловый эфир β-циклодекстрина и наполнители, выбранные из маннита и трометамола. Изобретение также относится к способу получения указанной композиции, который включает растворение эпотилона в спирте, растворение гидроксипропил-β-циклодекстрина или простого сульфобутилового эфира β-циклодекстрина в водном растворе вместе с маннитом и трометамолом, доведение рН водного раствора до значения 5-9 с помощью соляной кислоты и смешивание полученных растворов. Изобретение также относится к способу лечения злокачественного новообразования у пациента, который включает внутривенную инфузию указанной композиции в течение периода около 30 минут в дозе от 10 мг/м2 до 35 мг/м2. 7 н. и 10 з.п., ф-лы, 2 ил., 12 табл.
Реферат
Область техники изобретения
Настоящее изобретение относится к способам получения лекарственных препаратов эпотилонов и композиций, пригодных для парентерального введения, такого как внутривенное введение.
Предпосылки создания изобретения
Эпотилоны относятся к классу встречающихся в природе веществ с цитотоксическим действием, которые следует вводить парентерально. К сожалению, встречающиеся в природе вещества не являются достаточно стабильными, химически или метаболически, для предоставления возможности использования в виде лекарственных средств. Лактоновая структура в эпотилоновом скелете обуславливает чувствительность молекулы к разложению, в особенности при повышенных значениях рН, таких как значения рН, выше нейтрального. Кроме того, эпотилоны являются высоколипофильными веществами и практически нерастворимы в воде, поэтому внутривенное введение соединений этого класса чрезвычайно затруднено. Для парентерального введения лекарственных препаратов необходимо, чтобы эпотилоны были полностью растворены в растворителе, совместимом с физиологическими жидкостями, такими как кровь.
Некоторые успехи были достигнуты в получении новых производных эпотилонов, которые обладают как химической, так и метаболической стабильностью, достаточной для развития лекарственных средств. Кроме того, производные эпотилонов должны превышать свойства естественных производных относительно их терапевтического интервала, селективности их действия и/или нежелательных побочных токсических действий и/или их терапевтической эффективности. В WO 00/66589 описаны такие улучшенные эпотилоны, в которых шестой атом углерода эпотилона, приведенного на странице 1 заявки WO 00/66589, имеет алкенильный, алкинильный или эпокси радикал. Однако такие дополнительные боковые цепи делают такие эпотилоны даже еще более липофильными и плохо смачиваемыми в растворителях, что делает их приготовление в виде лекарственных средств еще более затруднительным для специалиста в данной области техники.
Были описаны некоторые способы повышения растворимости трудно растворимых в воде лекарственных средств для получения лекарственных препаратов, пригодных для парентерального введения. В US 6407079 (Janssen Pharma) описаны инъецируемые лекарственные препараты, в которых к лекарственному средству, которое нестабильно или только труднорастворимо в воде, добавляют частично этерифицированный β-циклодекстрин (гидроксиэтиловый, гидроксипропиловый, дигидроксипропиловый, метиловый или этиловый простые эфиры). Полученное инклюзированное соединение является лучше растворимым в воде, чем само лекарственное средство.
Простые сульфоалкиловые эфиры циклодекстринов и их производные для применения в качестве солюбилизирующих средств для нерастворимых в воде лекарственных средств ранее были описаны в US 5376645 и US 5134127.
В WO 99/396945 описаны препараты эпотилонов типа А и В, приготовленные в виде инфузионного концентрата или в виде лиофилизированной композиции. Перед введением эпотилон следует растворить в предпочтительных растворителях, таких как смеси ПЭГ/вода, пропиленгликоль/вода или этанол/вода. Растворимость эпотилона существенно повышается при применений таких смесей растворителей. В качестве наполнителя добавляют β-циклодекстрин или маннит.
В WO 2004/032866 описаны лиофилизированные композиции, содержащие эпотилоны, предпочтительно эпотилон D вместе с β-циклодекстринами, включая простые сульфоалкиловые эфиры циклодекстринов.
Получение эпотилонов и их производных осуществляют в соответствии со способами, которые известны специалисту в данной области, так как они описаны, например, в DE 19907588, WO 98/25929, WO 99/58534, WO 99/2514, WO 99/67252. WO 99/67253, WO 99/7692, EP 99/4915, WO 00/1333, WO 00/66589, WO 00/49019, WO 00/49020, WO 00/49021, WO 00/71521, WO 00/37473, WO 00/57874, WO 01/92255, WO 01/81342, WO 01/73103, WO 01/64650, WO 01/70716, US 6204388, US 6387927, US 6380394, US 02/52028, US 02/58286, US 02/62030, WO 02/32844, WO 02/30356, WO 02/32844, WO 02/14323 и WO 02/8440. Эпотилоны, представляющие особый интерес согласно настоящему изобретению, могут быть получены согласно WO 00/66589.
Задачей настоящего изобретения является обеспечение композиции, которая содержит производное эпотилона и которая предназначена для парентерального введения, предпочтительно внутривенного введения. Композиция должна быть стабильной, по меньшей мере по отношению к эпотилону, при хранении и восстановлении, если это является необходимым, путем добавления растворителя, совместимого с кровью и пригодного для парентерального введения без необходимости добавления поверхностно-активных веществ и органических растворителей.
Краткое изложение сущности изобретения
Настоящее изобретение относится к дозированным формам для парентерального введения, содержащим эпотилоны, и их приготовлению, при котором конечная дозированная форма или способ приготовления соответствует следующим характеристикам.
- Быстрое растворение эпотилона в жидкости, которая может быть удалена в условиях лиофилизации, таким образом удается уменьшить потерю интактного эпотилона при процессе растворения.
- Лиофилизация жидкой композиции эпотилона без потери интактного эпотилона.
- Лиофилизат является достаточно тяжелым.
- Полное и быстрое растворение лиофилизированного осадка в физиологически приемлемом растворителе с образованием при этом восстановленной композиции, которая легко может быть введена или в дальнейшем разбавлена подходящим физиологически приемлемым растворителем.
- Химически стабильные лиофилизированные композиции, по меньшей мере, относительно стабильности эпотилона.
- Физически стабильные лиофилизированные композиции.
- Химически стабильный восстановленный раствор, по меньшей мере относительно стабильности эпотилона.
- Физически стабильный восстановленный раствор.
- Высокая концентрация эпотилона в лиофилизированном осадке и/или восстановленном растворе.
- Высокая максимальная переносимая доза последующего парентерального введения.
Согласно настоящему изобретению обеспечиваются лиофилизированные композиции, а также их восстановленные композиции, которые в качестве общего признака содержат эпотилон или его производное, или их смеси в комбинации с циклодекстрином.
В отличие от ранее описанных композиций эпотилонов, которые вводили парентерально, композиции согласно настоящему изобретению обеспечивают композиции, которые получают при восстановлении лиофилизата в простых растворителях, таких как вода или минерализованная вода и необязательно дополнительно разведенные раствором глюкозы или декстрозы. Для обеспечения достаточного растворения эпотилона не требуется добавление органического растворителя и гликоля. Как описано в WO 2004/032866, для восстановления лиофилизата требуются смеси воды, этанола и гликоля. В лиофилизатах согласно WO 99/39694 также необходимым является органический растворитель. Очевидно, что лиофилизаты согласно настоящему изобретению обладают преимуществами по сравнению с ранее описанными, поскольку для приготовления конечной восстановленной композиции необходима только вода для инъекций или солевой раствор.
В одном варианте осуществления изобретение относится к композициям, содержащим эпотилон или смеси эпотилонов, в которых эпотилон имеет более липофильную боковую цепь по сравнению с эпотилонами, которые встречаются в природе. Согласно формуле I, приведенной в настоящем изобретении, липофильная боковая цепь относится к R4 и расположена у атома углерода под номером 10 таким образом, что эпотилон конденсирован с эпокси кольцом, или расположена у атома углерода под номером 7 таким образом, что R7 и R8 представляют собой атом водорода или вместе представляют собой дополнительную связь. В WO 00/66589 этот атом углерода обозначен номером 6. Композиции по изобретению дополнительно содержат циклодекстрин, предпочтительно производное β-циклодекстрина, которое этерифицировано гидроксиалкильными группами и/или сульфоалкильными группами, что приводит к получению гидроксиалкилированных циклодекстринов или сульфоалкилированных циклодекстринов.
Было обнаружено, что общий принцип приготовления лекарственных препаратов эпотилонов, пригодных для парентерального введения, обеспечивается подходящим выбором наполнителей, которые обеспечивают требуемую тоничность, рН, стабилизацию композиции, содержащей циклодекстрин и эпотилон, химическую и физическую стабильность при лиофилизации, химическую и физическую стабильность лиофилизированной композиции. Этот принцип чрезвычайно пригоден для эпотилонов с очень плохими смачиваемыми свойствами и/или низкой растворимостью в воде, такие как предпочтительные производные, охватываемые формулой I, приведенной в настоящей заявке.
Типичными примерами дополнительных наполнителей являются тонизирующее средство, наполнитель, криозащитное вещество, лиозащитное вещество и вещество, регулирующее рН. В предпочтительных вариантах осуществления изобретения дополнительный фармацевтически приемлемый наполнитель выбирают из маннита; сорбита; ксилита; 2-амино-2-гидроксиметил-1,3-пропандиола; кислотной формы или солей лимонной кислоты, уксусной кислоты, гистидина, яблочной кислоты, фосфорной кислоты, винной кислоты, янтарной кислоты, MES, HEPES, имидазола, молочной кислоты, глутаровой кислоты и/или глицилглицина, предпочтительно маннита и/или трометамола (TRIS).
Изобретатели также обнаружили, что особенно пригодными циклодекстринами является простой сульфоалкиловый эфир циклодекстринов, который обеспечивает получение композиций, обладающих желательной тоничностью без необходимости добавления дополнительных наполнителей или средств, модифицирующих тоничность.
Таким образом, в другом варианте осуществления, изобретения относится к композициям, содержащим эпотилон и сульфоалкилированный циклодекстрин (например, сульфопропилированный и сульфобутилированный циклодекстрин).
В дальнейшем варианте осуществления изобретение относится к композиции, которая содержит эпотилон в соответствии с формулой I, описанной в настоящем изобретении, и β-циклодекстрин. Циклодекстрин представляет собой предпочтительно гидроксиалкилированный β-циклодекстрин или сульфоалкилированный β-циклодекстрин, как описано выше.
В другом предпочтительном варианте осуществления изобретение относится к композиции, которая содержит эпотилон в соответствии с формулой I, описанной в настоящем изобретении, и сульфоалкилированный β-циклодекстрин, предпочтительно простой сульфобутиловый эфир β-циклодекстрина.
В предпочтительном варианте осуществления изобретение относится к композиции, которая содержит эпотилон в соответствии с формулой I, описанной в настоящем изобретении, и гидроксилированый, наиболее предпочтительно частично этерифицированный гидроксипропил-β-циклодекстрин.
Кроме того, изобретатели обеспечили способ получения лиофилизированной композиции по изобретению, который преодолевает начальную критическую стадию растворения очень гидрофобных эпотилонов, а именно начальное смачивание эпотилона в подходящей жидкости перед последующим осуществлением процесса солюбилизации.
Этот способ предоставляет возможность быстрого и полного растворения эпотилона и в дальнейшем обеспечивает поддержание стабильности эпотилона в растворе, в течение достаточного периода времени, перед удалением растворителя.
Например, способ растворения эпотилона осуществляется намного быстрее, чем способ, описанный в WO 99/39694, пример 10. Фактически, для эпотилонов, раскрытых в настоящем изобретении, не является возможным использовать способ, описанный в примере 10 заявки WO 99/39694. Для перевода в раствор эпотилонов, раскрытых в настоящем изобретении, могут потребоваться дни, в течение этого периода времени может произойти гидролиз. Следовательно, это приведет к значительной потере эпотилона и описанный процесс не является подходящим для осуществления в промышленном масштабе.
Следовательно, в еще другом варианте осуществления изобретение относится к приготовлению твердой композиции, такой как лиофилизат, которая может быть получена из растворов (в дальнейшем в настоящем изобретении называемых "исходными растворами"), содержащих эпотилон, как описано в настоящем изобретении, циклодекстрин, как описано в настоящем изобретении, и необязательно по меньшей мере один дополнительный фармацевтически приемлемый наполнитель, как определено в настоящем изобретении.
Специфической характеристикой способа является обеспечение возможности растворения эпотилона в растворителе, подходящем для процесса лиофилизации, в течение более короткого промежутка времени, чем известный из уровня техники, который является коротким, но достаточным для обеспечения поддержания стабильности эпотилона и отсутствия разложения.
Рассматриваемый промежуток времени составляет от 0,5 до 5 часов, предпочтительно от 0,5 до 3 часов, более предпочтительно от 1 до 2,5 часов.
В одном варианте осуществления метод получения композиции по изобретению (способ) предусматривает стадии:
а) растворение эпотилона - независимо от того, является он кристаллическим или аморфным - как определено в настоящем изобретении, в органическом растворителе, таком как спирт, (предпочтительно этанол); и
б) растворение циклодекстрина, как определено в настоящем изобретении, в водном растворе, необязательно вместе с по меньшей мере одним дополнительным фармацевтически приемлемым компонентом, как определено в настоящем изобретении, таким как маннит и/или трометамол; необязательно
в) доведение значения рН полученной смеси на стадии б) до рН в интервале от 5 до 9, предпочтительно от 6 до 8, такое как приблизительно 7,4, с помощью неорганической кислоты, такой как соляная кислота; и
г) смешивание растворов, полученных на стадиях а) и б) или а) и в); и необязательно
д) осуществление стерильной фильтрации продукта со стадии г) для получения так называемого "исходного раствора";
е) удаление растворителей из "исходного раствора" с получением твердой композиции.
В одном варианте осуществления метод получения композиции по изобретению (способ) предусматривает стадии
а) растворение эпотилона - независимо от того, является он кристаллическим или аморфным - как определено в настоящем изобретении, в органическом растворителе, таком как спирт (предпочтительно этанол); и
б) упаривание указанного органического растворителя; и
в) растворение циклодекстрина, как определено в настоящем изобретении, в водном растворе, необязательно вместе с по меньшей мере одним дополнительным фармацевтически приемлемым компонентом, как определено в настоящем изобретении, таким как маннит и/или трометамол; необязательно;
г) доведение значения рН полученной смеси на стадии б) до рН в интервале от 5 до 9, предпочтительно от 6 до 8, такое как приблизительно 7,4, с помощью неорганической кислоты, такой как соляная кислота; и
д) растворение порошка, полученного на стадии б), в растворе, полученном на стадии в) или г); и необязательно
е) осуществление стерильной фильтрации продукта со стадии д) для получения так называемого "исходного раствора";
ж) удаление растворителя из "исходного раствора" с получением твердой композиции.
Органические растворители, пригодные для стадии а), если вторая стадия б) представляет собой упаривание растворителя, могут быть выбраны из полярных апротонных или протонных растворителей, например, могут быть выбраны из галогенированных углеводородов, таких как монохлорметан, дихлорметан; спиртов, таких как метанол, этанол, пропанол; ацетон. Предпочтительными растворителями являются метиленхлорид и этанол.
Удаление растворителя в контексте настоящего изобретения охватывает все методики для удаления растворителя или растворителей, которые известны специалисту в данной области техники, такие как, но не ограничиваясь только ими, сушка вымораживанием, лиофилизация, вакуумная сушка или упаривание.
В предпочтительном варианте осуществления изобретение относится к методам получения композиции, которая содержит эпотилон (способам), описанным выше, в которых эпотилон используют в аморфной форме, и к композициям, получаемым этими способами.
Аморфный представляет собой твердую фазу без кристаллической решетки. Это может быть подтверждено с помощью порошковой дифракции рентгеновских лучей.
Эпотилон может быть получен в аморфной форме, например, путем растворения кристаллического эпотилона в органическом растворителе и последующего удаления его растворителя.
В предпочтительном варианте осуществления изобретение относится к методам получения композиции, которая содержит эпотилон (способам), описанным выше, в которых эпотилон используют в аморфной форме или его переводят в аморфную форму и циклодекстрин представляет собой гидроксипропил-β-циклодекстрин, и к композициям, получаемым этими способами.
В предпочтительном варианте осуществления изобретение относится к методам получения композиции, которая содержит эпотилон (способам), описанным выше, в которых эпотилон используют в аморфной форме или его переводят в аморфную форму и циклодекстрин представляет собой простой сульфобутиловый эфир β-циклодекстрина, и к композициям, получаемым этими способами.
В предпочтительном варианте осуществления изобретение относится к методам получения композиции, которая содержит эпотилон (способам), описанным выше, в которых используемый эпотилон представляет собой производное эпотилона (1S, 3S, 7S, 10R, 11S, 12S, 16R)-7,11-дигидрокси-3-(2-метил-бензотиазол-5-ил)-10-(проп-2-ен-1-ил)-8,8,12,16-тетраметил-4,17-диоксабицикло[14.1.0]гептадекан-5,9-дион, дополнительно, эпотилон находится в аморфной форме или его переводят в аморфную форму, и циклодекстрин представляет собой гидроксипропил-β-циклодекстрин и к композициям, получаемым этими способами.
В предпочтительном варианте осуществления изобретение относится к методам получения композиции, которая содержит эпотилон (способам), описанным выше, в которых используемый эпотилон представляет собой производное эпотилона (1S, 3S, 7S, 10R, 11S, 12S, 16R)-7,11-дигидрокси-3-(2-метил-бензотиазол-5-ил)-10-(проп-2-ен-1-ил)-8,8,12,16-тетраметил-4,17-диоксабицикло[14.1.0]гептадекан-5,9-дион, дополнительно эпотилон находится в аморфной форме или его переводят в аморфную форму, и циклодекстрин представляет собой простой сульфобутиловый эфир β-циклодекстрина и к композициям, получаемым этими способами.
В другом предпочтительном варианте осуществления изобретение относится к композициям, получаемым методами получения композиции, которая содержит эпотилон (способами), описанными выше.
В еще другом варианте осуществления изобретение относится к композициям, содержащим эпотилон и гидроксилалкилированный циклодекстрин в специфическом молярном отношении от 1:8 до 1:100, предпочтительно от 1:11 до 1:80, которое эквивалентно массовому отношению от 1:21 до 1:300, предпочтительно от 1:29 до 1:200. Особенно предпочтительными являются отношения, получаемые в примерах, приведенных в настоящей заявке.
В еще другом варианте осуществления изобретение относится к композициям, содержащим эпотилон и простой сульфобутиловый эфир циклодекстрина в специфическом молярном отношении от 1:9 до 1:100, предпочтительно от 1:9 до 1:50 которое эквивалентно массовому отношению от 1:38 до 1:300, предпочтительно от 1:38 до 1:200. Особенно предпочтительными являются отношения, получаемые в примерах, приведенных в настоящей заявке.
Подробное описание изобретения
Композиции, обеспечиваемые настоящим изобретением, представляют собой композиции с достаточной и высокой растворимостью эпотилона путем комбинирования эпотилона, предпочтительно используемого в аморфной форме, и циклодекстрина в комбинации с дополнительными адаптированными наполнителями и/или путем тщательного выбора циклодекстрина. После этого композиции предпочтительно приготавливают в виде лекарственного препарата, позволяющего осуществить парентеральное введение композиции, такого как в виде твердого раствора, такого как лиофилизированная композиция, которую затем превращают в композицию, получаемую вследствие восстановления лиофилизата подходящим растворителем.
Термин "приготовленные в виде лекарственного препарата в форме для парентерального использования" в целом относится к композициям для инъекций. Композиции для инъекций могут вводиться внутривенно, подкожно или путем инфузии. В предпочтительных вариантах осуществления изобретения композиции для инъекций предназначены для внутривенного введения.
Термины "лиофилизированная композиция", "лиофилизированный осадок" и "лиофилизат" являются взаимозаменяемыми терминами и используются в настоящем изобретении для описания твердой композиции, получаемой в результате обработки жидкой композиции, такой как раствор, содержащий эпотилон, который растворен или по меньшей мере частично растворен, в условиях, включающих по меньшей мере одну стадию замораживания раствора, с последующей сублимацией растворителя (ей) в вакууме (основная сушка) и необязательно и дополнительно упаривание/удаление растворителя (ей) при осуществлении вторичной сушки и необязательно послесушки, например, в следующих условиях:
- Замораживание при -45°С под давлением 1013 мбар в течение вплоть до 24 часов, предпочтительно в течение 5 часов,
- Первая стадия основной сушки до 15°С под давлением 8,9×10-2 мбар в течение 60 часов, предпочтительно в течение 48 часов,
- Вторая стадия основной сушки при 25°С под давлением 8,9×10-2 мбар в течение 2 часов, предпочтительно в течение 1 часа и
- Стадия послесушки при 25°С при 6,5×10-3 мбар в течение 10 часов, предпочтительно в течение 6 часов, используя, например, установку для сушки Fa. Hof, тип СОМ 0590.
Термины "лиофилизация" и "сушка вымораживанием" относятся к процессу, при котором из растворенной или по меньшей мере частично растворенной композиции удаляют жидкость в условиях, включающих по меньшей мере одну стадию замораживания раствора, с последующей сублимацией растворителя (ей) в вакууме (основная сушка) и необязательно дополнительное упаривание растворителя (ей) при осуществлении вторичной сушки, и необязательно послесушки, например, в условиях, описанных в предыдущем абзаце.
Термин "восстановленный раствор" относится к жидкой композиции, полученной при полном растворении лиофилизата, который может представлять собой твердый раствор, в растворителе, таком как вода (вода для инъекций), солевой раствор или стерильный раствор Рингера. Растворитель может содержать дополнительные наполнители, таким образом, чтобы обеспечить совместимость восстановленной композиции с физиологически релевантными жидкостями, такими как кровь. Восстановленные композиции предназначены для того, что сами представляют форму, готовую для парентерального введения, или их дополнительно разводят перед применением.
Под термином "простой сульфоалкиловый эфир циклодекстрина" подразумевают производное, получаемое путем введения заместителя анионного типа, такого как (С2-6алкилен)-SO3 -- анионный заместитель в циклодекстрин. Сульфоалкильное производное циклодекстрина может представлять собой единственное производное или смесь производных. Поскольку производные циклодекстрина функционализируют с (С2-6 алкилен)-SO3 -- группами, то производные имеют заряд. Простые сульфоалкиловые эфиры циклодекстрина либо замещены по меньшей мере в одном из положений первичных гидроксильных групп или они замещены в обоих положениях первичных гидроксильных групп и в 3-ем положении гидроксильной группы. Замещение во 2-м положении теоретически возможно.
Термин гидроксиалкилированный β-циклодекстрин, в особенности гидроксипропил-β-циклодекстрин означает производное циклодекстрина, в котором в определенных условиях (открыто опубликовано поставщиком, например Roquette GmbH, циклодекстрина) свободные гидроксильные группы β-циклодекстрина частично или полностью этерифицированы в результате контролируемой реакции алкиленоксида, в особенности пропиленоксида, и встречающегося в природе бета-циклодекстрина при основном катализе с образованием гидроксиметильных, гидроксиэтильных или гидроксипропильных групп соответственно. В случае частичной этерификации гидроксильных групп полученный β-циклодекстрин характеризуется средней молярной степенью замещения (MS), которая представляет собой среднее количество молей гидроксипропильных групп на ангидроглюкопиранозную единицу. Это, согласно информации производителя, не следует путать со степенью замещения (DS) или общей степенью замещения (TDS), которая характеризует среднее количество замещенных гидроксилов на ангидроглюкопиранозную единицу.
Обычно растворитель для восстановления представляет собой водный раствор, содержащий 75-100 об.% воды, предпочтительно 85-100 об.%, более предпочтительно 90-100 об.%, наиболее предпочтительно 95-100 об.%. Растворитель может содержать дополнительные наполнители, такие как неорганические соли, например, хлорид натрия, для обеспечения совместимости с физиологически релевантными жидкостями.
Термин "растворимость" относится к растворимости эпотилона в растворителе.
В соответствии с изобретением эпотилон следует объединять с одним или несколькими средствами, которые повышают растворимость эпотилона в воде. В качестве первого солюбилизирующего средства, было обнаружено, что циклодекстрин улучшает растворимость эпотилона. Тем не менее, в некоторых случаях можно добавлять другие наполнители для дальнейшего повышения растворимости эпотилона или для ограничения разложения эпотилона при приготовлении парентеральной композиции. Например, дополнительные наполнители можно добавлять для стабилизации эпотилона при смешивании наполнителей, при удалении жидкости, или при хранении или после восстановления.
Следовательно, в одном варианте осуществления изобретения обеспечивается композиция, которая содержит эпотилон, циклодекстрин и по меньшей мере один фармацевтически приемлемый наполнитель, выбранный из тонизирующего средства, наполнителя, криозащитного вещества, лиозащитного вещества и регулятора рН.
В другом варианте осуществления изобретения обеспечивается композиция, которая содержит эпотилон, такой как производное эпотилона, определенное формулой I, и циклодекстрин, эпотилон представлен формулой I,
в которой
R1 означает водород, OR1a, или галоген, где R1a означает водород, SO2-алкил, SO2-арил, или SO2-аралкил,
R2, R3 означают независимо C1-C10 алкил,
R4 означает -(CH2)r-C≡C-(CH2)p-R4a,-(CH2)r-СН=СН-(CH2)p-R4a,
.или.
n означает 0-5,
r означает 0-4,
р означает 0-3,
R4a означает водород, C1-С10 алкил, С6-С12 арил или С7-С20 аралкил, каждый необязательно замещен; C1-С10 ацил, или, если р>0, дополнительно группу OR4b,
R4b означает водород или защитную группу PG;
R5 означает C1-С10 алкил,
R6 означает водород или необязательно замещенный C1-C10 алкил,
R7, R8 каждый означает атом водорода, или вместе представляют собой дополнительную связь или вместе представляют собой атом кислорода,
G означает группу X=CR9- или би- или трициклический ароматический гетероциклический радикал,
R9 означает водород, галоген, CN, или C1-C20 алкил,
Х означает группировку CR10R11,
причем
R10, R11 являются одинаковыми или разными и означают водород, C1-C20 алкил, C6-C12 арил, или С7-20 аралкильный радикал, каждый необязательно замещен; или R10 и R11 образуют вместе с метиленовым углеродом 5-7-членное карбоциклическое кольцо;
А означает группу -О- или -NR12-,
R12 означает водород или C1-С10 алкил.
Эпотилон согласно формуле I может быть конденсирован с эпоксидным кольцом, в случае, когда R7, R8 вместе представляют собой атом кислорода или может существовать в виде одной кольцевой системы, в случае, когда R7, R8 каждый означает атом водорода или вместе представляют собой дополнительную связь.
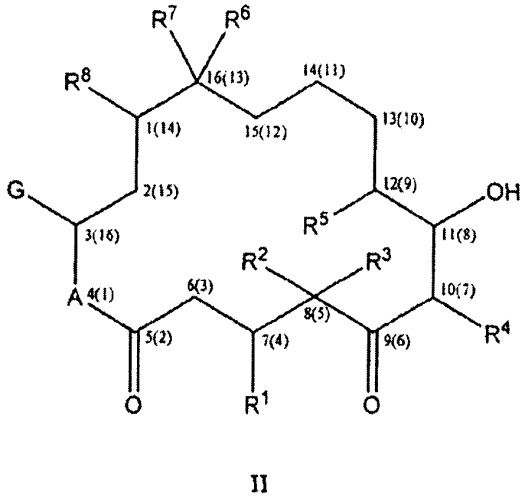
Нумерация атомов углерода в эпотилоновом скелете будет зависеть от того, является ли эпотилон конденсированным с дополнительным кольцом, таким как эпоксидное кольцо. На формуле II, приведенной ниже, показана нумерация атомов углерода в обоих случаях. Обозначения 1-16 относятся к нумерации эпотилонового скелета, когда R7, R8 вместе образуют эпоксидное кольцо. Обозначения (1)-(16) относятся к нумерации эпотилонового скелета, когда R7, R8 каждый означает атом водорода или вместе представляют собой дополнительную связь.
Термин "галоген" означает фтор, хлор, бром и йод.
Термин SO2-алкил относится к "C1-С10 алкилу", который однозамещен -SO2 группой.
Термин SO2-арил относится к "C6-C12 арилу", который однозамещен -SO2 группой.
Термин SO2-аралкил относится к "C6-C12 арилу", замещенному одной группой -SO2 и одним или двумя "C1-С10 алкилами".
Термин "С1-С10 алкил" относится к линейной или разветвленной насыщенной углеводородной цепи, где наиболее длинные цепи содержат от одного до десяти атомов углерода, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, гексил, гептил, октил, ундекацил, додецил и т.д. C1-С10 алкильная цепь согласно настоящему изобретению может быть необязательно замещенной.
Аналогично, термин "C1-C20 алкил" относится к линейной или разветвленной насыщенной углеводородной цепи, где наиболее длинные цепи содержат от одного до двадцати атомов углерода.
Термин "С6-С12 арил" относится к замещенному или незамещенному карбоциклическому ароматическому радикалу или гетероциклическому радикалу, содержащему от 6 до 12 атомов углерода. Кроме того, термин "арил" охватывает конденсированные кольцевые системы, в которых по меньшей мере два арильных кольца имеют по меньшей мере одну общую химическую связь. Иллюстративными примерами "арильных" колец являются фенил, нафталенил. Предпочтительной арильной группой является фенил и замещенные фенильные группы, которые несут один или два, одинаковых или различных заместителя, перечисленные выше. Предпочтительно заместители находятся в пара- и/или мета-положении. Характерными примерами арильных групп являются, но не ограничиваясь только ими, фенил, 3-галофенил, 4-галофенил, 3-гидроксифенил, 4-гидроксифенил, 3-аминофенил, 4-аминофенил, 3-метилфенил, 4-метилфенил, 3-метоксифенил, 4-метоксифенил, 3-цианофенил, 4-цианофенил, диметилфенил, нафтил, гидроксинафтил, гидроксиметилфенил, трифторметилфенил, алкоксифенил.
Термин "ароматический гетероциклический радикал" относится к замещенному или незамещенному ароматическому гетероциклическому радикалу, содержащему от 6 до 12 атомов углерода, включающему один или несколько гетероатомов. Типичными примерами ароматических гетероциклических радикалов являются фурил, тиенил, пиридил, пиразолил, пиримидинил, оксазолил, пиридазинил, пиразинил, хинолил, тиазолил, бензотиазолил, бензоксазолил, хинолин, который может быть однократно или многократно замещен галогеном, ОН, O-алкилом, СО2Н, СО2-алкилом, NO2, N3, CN, C1-С10 алкилом, C1-С10 ацилом, C1-C10 ацилокси группами. Гетероатомы в гетероарильных кольцах могут быть окислены; таким образом, например, бензотиазольное кольцо может находиться в виде N-оксида. Предпочтительными ароматическими гетероциклическими радикалами являются бензотиазолил, бензоксазол и хинолин; более предпочтительно бензотиазолил, замещенный C1-С10 алкилом.
Термин "С7-С20 аралкил" относится к карбоциклическому ароматическому кольцу или кольцевой системе, содержащей от 6 до 12 атомов углерода, предпочтительно от 6 до 10, и в алкильной цепи от 1 до 8, предпочтительно от 1 до 4 атомов, в котором по меньшей мере одно арильное кольцо имеет по меньшей мере одну общую химическую связь с C1-C8 алкилом. В качестве аралкильных радикалов, подходящими являются, например, бензил, фенилэтил, нафтилметил, нафтилэтил, фурилметил, тиенилэтил и пиридилпропил. Кольца могут быть однократно или многократно замещены галогеном, ОН, O-алкилом, CO2H, CO2-алкилом, NO2, N3, CN, C1-C10 алкилом, C1-С10 ацилом, C1-С10 ацилокси группами.
Термин "С1-С10 ацил" относится к линейной или разветвленной насыщенной углеводородной цепи, в которой наиболее длинные цепи содержат от одного до десяти атомов углерода и в которой один из атомов углерода представляет собой С(=O)O радикал.
Алкокси группы, которые содержатся в Х в общей формуле I, в каждом случае содержат от 1 до 20 атомов углерода, из них предпочтительными являются метокси, этокси, пропокси, изопропокси и трет-бутилокси группы.
Термин "эпотилон" и "эпотилон*" в целом понимают как такие, которые охватывают все виды веществ, относящихся к классу эпотилонов, которые встречаются в природе или получены синтетическим путем, либо в виде отдельного эпотилона или смеси эпотилонов. Это означает, что термин "эпотилон" относится к любому эпотилону, такому как эпотилон А, эпотилон В, эпотилон С, эпотилон D, эпотилон Е, эпотилон F, их аналогам, производным, солям и смесям. Предпочтительно, эпотилон представляет собой эпотилон А, эпотилон В, эпотилон С, эпотилон D или их производные или их соли или их смеси. В некоторых предпочтительных вариантах осуществления изобретения эпотилон представляет собой производное эпотилона В согласно формуле I, приведенной выше.
В некоторых представляющих интерес вариантах осуществления изобретения эпотилон представляет собой производное эпотилона, в котором атом углерода 10(7) в 16-ти членной макролидной системе имеет алкенильную, алкинильную или эпоксидную группу, как определено выше (R4 в формуле I) вместо метильной группы в эпотилонах, которые встречаются в природе. Таким образом, эпотилон согласно настоящему изобретению относится в целом к производному любого эпотилона, такому как эпотилоны А, В, С, D, Е или F, в которых атом углерода 10(7) 16-членной макролидной системы имеет алкенильную, алкинильную или эпоксидную группу, как определено с помощью R4 в формуле I. Поскольку указанные эпотилоны В представляют особый интерес согласно настоящему изобретению, то это означает, что вышеописанные производные предпочтительно представляют собой производные эпотилона В.
В других представляющих интерес вариантах осуществления изобретения эпотилон представляет собой производное эпотилона, выбранное из группы, включающей:
(1S, 3S (Е), 7S, 10R, 11S, 12S, 16R)-7,11-дигидрокси-10-(проп-2-ин-1-ил)-3-(1-метил-2-(2-метилтиазол-4-ил)этенил)-8,8,12,16-тетраметил-4,17-диоксабицикло [14.1.0] гептадекан-5,9-дион;
(1S, 3S, 7S, 10R, 11S, 12S, 16R)-7,11-дигидрокси-10-(проп-2-ен-1-ил)-3-(2-метил-бензоксазол-5-ил)-8,8,12,16-тетраметил-4,17-диоксабицикло [14.1.0] гептадекан-5,9-дион;
(1S, 3S (Е), 7S, 10R, 11R, 12S, 16R)-7,11-дигидрокси-10-(проп-2-ин-1-ил)-3-(1-фтор-2-(2-метилоксазол-4-ил)этенил)-8,8,12,16-тетраметил-4,17-диоксабицикло [14.1.0] гептадекан-5,9-дион;
(4S, 7R, 8S, 9S, 13E/Z, 16S (Е))-4,8-дигидрокси-16-(1-хлор-2-(2-метилтиазол-4-ил)этенил)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-ил)-циклогексадец-13-ен-2,6-дион;
(4S, 7R, 8S, 9S, 13E/Z, 16S)-4,8-дигидрокси-16-(2-метил-бензотиазол-5-ил)-1-окса-5,5,9,13-тетраметил-7-(проп-2-ен-1-ил)-циклогексадец-13-ен-2,6-дион;
(4S, 7R, 8S, 9S, 13E/Z, 16S (Е))-4,8-дигидрокси-16-(1-метил-2-(2-пиридил)этенил)-1-окса-5,5,9,13-тетраметил-7-(бут-3-ин-1-ил)-циклогексадец-13-ен-2,6-дион;
(4S, 7R, 8S, 9S, 13E/Z, 16S (Е))-4,8-дигидрокси-16-(1-метил-2-(2-пиридил)этенил)-1-окса-5,5,9,13-тетраметил-7-(бут-3-ен-1-ил)-циклогексадец-13-ен-2,6-дион;
(1S, 3S (E), 7S, 10R, 11S, 12S, 16Р)-7,11-дигидрокси-10-(проп-2-ен-1-ил)-3-(1-метил-2-(2-метилтиазол-4-ил)этенил)-8,8,12,16-тетраметил-4,17-диоксабицикло [14.1.0] гептадекан-5,9-дион;
(4S, 7R, 8S, 9S, 13E/Z, 16S (Е))-4,8-дигид