Средство для лечения заболеваний опорно-двигательного аппарата человека и животных, в том числе переломов костей и заболеваний, связанных с дефицитом кальция в организме, на основе соли кальция
Иллюстрации
Показать всеИзобретение относится к лекарственным средствам для лечения заболеваний опорно-двигательного аппарата человека и животных. Средство представляет собой коллоидный раствор водной суспензии минерального состава морского происхождения с размером микрочастиц 10-6-10-7 м с активной поверхностью микрочастиц в виде мицелл не более 500 м2/мл и плотностью водной суспензии, не превышающей 1,7 кг/л, при следующем содержании компонентов, мас.%: минеральный состав 58 вода остальное, при этом минеральный состав по сухому остатку содержит макроэлементы - углекислый кальций и углекислый магний и микроэлементы: цинк, железо, кремний, медь, йод и др. в определенном соотношении. Использование средства приводит к повышению уровня кальция, магния и фосфата в сыворотке крови лишь в тех случаях, когда отмечается недостаток этих элементов в результате возрастных изменений минерального обмена или наличия каких-либо заболеваний, но не приводит к значительному повышению содержания кальция в крови, выше критического, а доводит его до нормального уровня и, кроме того, способствует значительному сокращению сроков сращения переломов. 2 табл., 5 ил.
Реферат
Изобретение относится к созданию лекарственных средств на основе кальция для лечения заболеваний опорно-двигательного аппарата человека и животных.
О значимости для организма кальция и его солей говорит тот факт, что их дефицит является причиной ряда заболеваний костной системы, прежде всего остеопороза. Так, низкое потребление кальция рассматривается как ключевой фактор в развитии остеопороза и уменьшении минеральной плотности ткани.
Лекарственные средства, стимулирующие восстановление костной ткани, хорошо известны практикующим врачам. Однако возможности широкого применения таких препаратов ограничены. К недостаткам медикаментозного лечения заболеваний костной системы следует отнести прекращение положительного действия препарата на костную ткань после отмены лечения, а также наличие большого спектра противопоказаний. Ввиду того, что в последние годы наблюдается тенденция к уменьшению потребления пищевого кальция, препараты кальция обязательно должны назначаться совместно с другими средствами борьбы с остеопорозом. Особенно эффективными являются препараты, в которых содержание элементов сбалансировано в соответствии с их содержанием в костной ткани. Поэтому большой интерес в ортопедотравматологической практике представляет использование биологически активных добавок, имеющих высокую усвояемость кальция, магния и других микроэлементов, а также обеспечивающих поддержание минерального гомеостаза организма человека.
Известны Биологически Активные Добавки (БАД): «Нутрикон Грин»-зерновые оболочки пшеницы и ржи, плоды шиповника, витамины группы В, С, Е, Д, йодиды, микроэлементы и др.; «Нутрикон Плюс Е» - зародыши пшеницы, пшеничные отруби, микроводоросли спирулины, микроэлементы (железо, магний, марганец, цинк); «Нутрикон Хром» - зерновые оболочки пшеницы и ржи, овес в зерновой оболочке, плоды шиповника, лист крапивы, спорыш, витамины группы В, аскорбиновая кислота, незаменимые аминокислоты, хром и другие микроэлементы; «Грация Коктейль» - изолят соевого белка, сухая лактоза, фруктоза, 18 аминокислот, витамины группы В, А, С, Е, Д, биотин, фолиевая и пантотеновая кислоты, минералы и микроэлементы - кальций, фосфор, калий, йод, железо, медь, цинк и др.; «Энергия Коктейль»- изолят соевого белка, фруктоза, соевый протеин, витамины группы В, А, С, Е, Д, биотин, минералы и микроэлементы - кальций, фосфор, калий, йод, железо, цинк. (Федеральный Реестр БАДов, 2005)
Известна БАД производства компании Nutri-Care, США. КАЛ-ДИ-МАГ (CAL-D-MAG), включающая кальция карбонат, хелатные соединения кальция, магния, витамины С, Д, петрушка, корень одуванчика, люцерна, лактоза, гомеопатические препараты - кальция фосфат, кальция сульфат, магния фосфат, кремния оксид. В состав «Ливер-Плас» (Liver-Plus) входит: лиофилизированная ткань печени быка, бурые водоросли, корень одуванчика, витамины группы В.
Широко известен препарат «Остеогенон», который включает неколлагеновые пептиды, коллагены, кальций и фосфор. Кальций и фосфор содержатся в препарате в физиологической пропорции 2:1. Входящие в состав препарата органические компоненты (коллаген и неколлагеновые пептиды) содержат инсулиноподобные факторы роста I и II, бета-трансформирующий фактор роста (Родионова С.С. и др., Вестник травматологии и ортопедии им. Н.Н.Пирогова. 2001. - №4. - С.41-46). Основными показаниями для его применения являются остеопорозы различного происхождения, ускорение консолидации переломов, восстановление баланса кальция и фосфора во время беременности. Препарат противопоказан больным с гиперкальциемией и гиперкальциурией, больным с мочекаменной болезнью или предрасположенностью к ней, препарат следует применять в малых дозах или отказаться от приема.
Задачей настоящего изобретения является разработка средства с широким диапазоном показаний, а именно для лечения заболеваний опорно-двигательного аппарата человека и животных, в том числе переломов костей и заболеваний, связанных с дефицитом кальция в организме на основе соли кальция.
Технический результат от применения данного средства заключается в сокращении сроков сращения различных переломов типа - поперечного, клиновидного, сегментарного и т.д. Кроме того, применение данного средства не приводит к значительному повышению содержания кальция в крови, а доводит его до нормального уровня.
Данная задача решается следующим образом.
Предложено средство для лечения заболеваний опорно-двигательного аппарата человека и животных, в том числе переломов костей и заболеваний, связанных с дефицитом кальция в организме на основе соли кальция, отличающееся тем, что оно представляет собой коллоидный раствор водной суспензии минерального состава морского происхождения с размером микрочастиц 10-6-10-7 м с активной поверхностью микрочастиц в виде мицелл не более 500 м2/мл и плотностью водной суспензии, не превышающей 1,7 кг/л, при следующем содержании компонентов, мас.%:
| минеральный состав | 58 |
| вода | остальное, |
при этом минеральный состав по сухому остатку содержит макроэлементы - углекислый кальций и углекислый магний и микроэлементы: цинк, железо, кремний, медь, йод, марганец, селен и хром, мас.%:
| углекислый кальций | 92-98 |
| углекислый магний | 1-5 |
микроэлементы:
| цинк | 0,1-0,5 |
| железо | 0,1-0,3 |
| кремний | 0,1-0,5 |
| медь | 0,05-0,3 |
| йод | 0,003-0,01 |
| марганец | 0,05- 0,3 |
| селен | 0,03-0,1 |
| хром | 0,03-0,1 |
Средство, разработанное с помощью новейшей технологии, которое содержит минеральные элементы в виде мицелл, что значительно улучшает их усвоение и обеспечивает появление новых свойств.
Средство получают из экологически чистых природных карбонатных минералов путем глубокой пептизации с применением селективного кавитационного воздействия в резонансном режиме на пересыщенные сорбированные оболочки агрегатных систем в маточном растворе. В результате высокой нестехиометричности состава получаемый препарат проявляет аномально высокую адгезию, направленную диффузию, автолизию, каталитические и другие физико-химические свойства. При поступлении в организм каждая частица минерала, покрытая многочисленными водными слоями, в виде нейтрально заряженной мицеллы, благодаря высокому «дзета - потенциалу», высокой подвижности и большой активности, доставляет необходимые макро- и микроэлементы в те органы и системы, где они необходимы. Средство представляет собой водную коллоидную суспензию белого цвета без запаха.
Для изучения влияния средства на регенерацию костной ткани было проведено 2 серии опытов на 32 беспородных собаках обоего пола. Возраст животных составил от 2 до 10 лет. Каждая серия разделена на 2 группы - опытную и контрольную. Животным опытных групп назначали средство по рекомендуемому регламенту:
A) Капли под язык: по 2-3 капли два раза в день утром и вечером за 15-20 минут до кормления, в течение 15 дней с первых дней лечения перелома.
Б) Добавление в состав питьевой воды: по 5-7 капель на 1 л питьевой воды при тщательном перемешивании в течение всего периода эксперимента, начиная с первого дня.
B) Компрессы: на мокрую поверхность кожи (без волосяного покрова) в область перелома нанести 3-4 капли. Накрыть полиэтиленовой пленкой на 15-20 минут, остатки после компресса удалить влажной салфеткой, курс 10 дней, первые пять дней два раза в день, последние пять дней один раз в день.
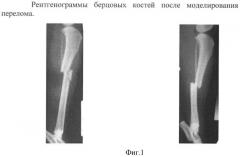
В первой серии (n=20) у наркотизированных животных моделировали ударные открытые крупно- и мелкооскольчатые переломы с полным смещением отломков костей голени при помощи специального устройства (удар определенной силы по наружной поверхности сегмента).
На фиг. 1 представлены рентгенограммы берцовых костей после перелома.
После перелома конечность планировали лонгетой.
Во второй серии, эксперименты были проведены на 12 беспородных животных - 6 опытных и 6 контрольных. На собаках моделировали перелом тела и ветви седалищной кости путем поперечной остеотомии долотом. В опытной группе эксперимент длился 35 суток (фиксация в аппарате) на двух животных и 65 суток (фиксация плюс 30 суток после снятия аппарата) также на двух животных. В контрольной группе одна собака находилась в опыте 35 суток и одна 65 суток.
В работе использовали клинический, рентгенологический, биохимический, морфологический и статистический методы исследования.
Результаты клинических исследований.
После удара груза по наружной поверхности голени при моделировании перелома у животных повреждались мягкие ткани в виде рассечения кожи и нижележащих мышц длиной до 1 см. У всех животных после перелома на следующие сутки возникал отек, увеличивая объем мягких тканей от 4 до 11%. В дальнейшем динамика отека мягких тканей в обеих группах первой серии была волнообразной. Как видно из графиков (фиг.2, 3), до 21 суток эксперимента у животных наблюдался отек, далее возникала атрофия мягких тканей вплоть до снятия аппарата. Однако у животных опытной группы восстановление объема мягких тканей происходило быстрее, чем в контроле.
Все животные первой серии хорошо переносили манипуляции со средством. Аппетит был сохранен. К концу первой недели после остеосинтеза появлялась опорная функция оперированной конечности, которая сохранялась весь дальнейший период фиксации.
Двигательная и опорная функции у животных обеих групп после операции были незначительно снижены. На 14-е сутки у всех животных наблюдали близкое к норме восстановление функций тазовой конечности.
Результаты рентгенологических исследований.
В первой серии опытов рентгенологические признаки регенерации переломов берцовых костей в обеих группах появлялись на 14 сутки эксперимента. Однако в опытной группе в большинстве случаев отсутствовали признаки резорбции краев костных отломков в зоне перелома, в то время как в контроле они были ярко выражены
На 28 сутки эксперимента на рентгенограммах в опытной группе в зоне перелома наблюдались тени формирующегося регенерата по оптической плотности, приближенной к плотности костно-мозговой полости. Осколки соединены между собой периостальными тенями. Признаков резорбции (лизиса) костных отломков нет (фиг.4 опытная группа - а). На данном этапе после проведения клинической пробы и оценки состоятельности регенерата аппарат снимали.
К этому сроку в контрольной группе линия перелома хорошо просматривалась. На отломках имелись обширные периостальные тени толщиной от 2 до 7 мм, распространяющиеся от зоны перелома на расстояние 30-50 мм. Смыкания их не происходило, тем самым не обеспечивалась прочность регенерата (фиг.4 контрольная группа - б). Сращение данных переломов происходило к 49 суткам фиксации.
Рентгенограммы берцовых костей собак первой серии на 28 сутки эксперимента представлены на фиг.4: а - опытной группы; б - контрольной
Сроки сращения переломов в опытной группе следующие: тип A3 (поперечный) - 21 сутки, тип В2 (клиновидные) 30-35 суток, тип С2 (сегментарные) - 35-49 суток. В контрольной группе сращение подобных переломов (типы В и С) происходило через 49 суток. В среднем сроки сращения всех переломов в опытной группе составили 40,1 суток, а в контроле 49 суток.
Через месяц после снятия аппарата в обеих группах первой серии опытов линия перелома практически не просматривалась, на большеберцовой кости имелись плотные ампулообразные утолщения надкостницы (периостальный регенерат) - компенсаторная реакция на ее повреждение спицами и при переломе. Плотность регенерата была приближена к плотности отломков.
Общая рентгенологическая картина сращения перелома берцовых костей через месяц после снятия аппарата в обеих группах была схожей. Однако общий срок эксперимента в опытной группе был меньше контроля на 19 суток.
Во второй серии по рентгенограммам таза, выполненным в прямой и боковой проекциях, четко определяли поперечные переломы тела и ветви седалищной кости. Величина диастаза между смещенными костными фрагментами тела седалищной кости составляла в сагиттальной плоскости 0,3-0,9 см. Смещение отломка в сегментальной плоскости было незначительное.
На 21-е сутки после операции на рентгенограммах животных опытной группы края отломков были сглажены, плотность теней диастаза увеличилась, появлялись просветления. Линия диастаза была прерывистая и неоднородная. В зоне регенерата наблюдались облаковидные тени и плотные включения. Периостальные тени приобретали более ограниченные формы и уплотнялись - определялось формирование кортикальной пластинки. У собак контрольной группы значительных изменений не происходило.
На 35-е сутки у собак опытной группы кортикальная пластинка была выражена. Периостальные тени на рентгенограммах всех животных уплотнялись и приобретали четкие контуры, образовывая над зоной перелома веретенообразную муфту (периостальную мозоль). По всей высоте регенерата определялись костные балки средней интенсивности в сочетании с плотными вкраплениями. В одном случае (№4698) регенерат по структуре приближался к материнской кости. У собаки №4681 определялись тени единичных костных балок средней интенсивности в сочетании с вкраплениями различной плотности. На рентгенограммах животных контрольной группы также наблюдалась консолидация переломов тела и ветви седалищной кости. Хотя линия диастаза еще была более четкая, чем у собак опытной группы. Кортикальная пластинка была не сформирована.
На фиг.5 представлена рентгенограмма собаки опытной группы, выполненная на 35 сутки после фиксации аппаратом (после снятия аппарата): б - рентгенограмма собаки контрольной группы, выполненная на 35 сутки после фиксации аппаратом (после снятия аппарата). 1 - зона перелома тела седалищной кости, 2 - зона перелома ветви седалищной кости.
После клинической пробы (ротационные движения отломком при ослабленных шарнирных узлах) аппарат демонтировали у собак обеих групп.
Через 42 суток у 3 собак опытной группы (№4698, 4688, 4685) линия диастаза была едва заметна, контуры кости четкие. Определялась хорошо сформированная кортикальная пластинка. Регенерат по структуре приближался к плотности материнской кости. У собаки №4681 линия диастаза была еще заметна, контуры кости - не четкие, кортикальная пластинка несформированная. Периостальная реакция была интенсивной. У собак контрольной группы линия диастаза прерывистая с включениями различной плотности, просматриваются единичные костные балки.
На 65-е сутки после операции у двух животных из обеих групп периостальная муфта была истончена, зона сращения рентгенологически не отличалась от контрлатеральной области. Структура и плотность регенерата максимально приближались к материнской кости. Кортикальная пластинка была хорошо выражена. У собаки №4672 линия диастаза была заметна, кортикальная пластинка слабо выражена, тени зоны периостальной реакции плотные, края четкие.
Средние сроки сращения в опытной группе второй серии составили 40 суток фиксации, а в контроле 60 суток.
Таким образом, рентгенографически процесс формирования регенерата у животных опытной группы второй серии, чей возраст составлял 5 лет, соответствовал общебиологическим срокам формирования регенерата (35-42 суток). У животного в возрасте 2-х лет костное сращение происходило в ранние сроки - на 35 сутки после операции. У животного в возрасте 10 лет процесс формирования регенерата рентгенографически протекал медленнее.
У животных контрольной группы в возрасте 4-5 лет процессы регенерации рентгенологически протекали медленнее (65 суток), чем в опытной группе. Можно предположить, что применение средства способствует ускорению костеобразования соответственно возрасту животного.
Результаты биохимических исследований.
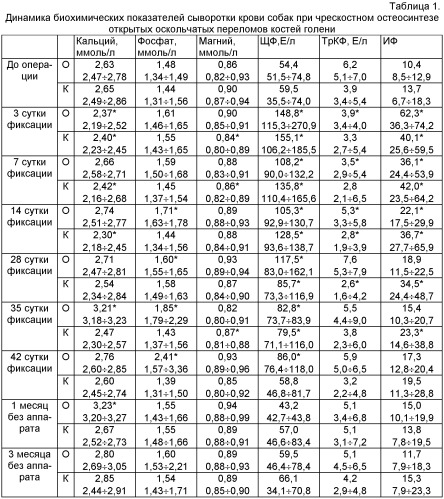
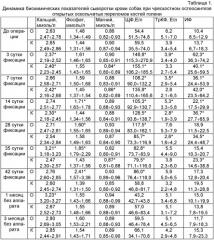
Результаты биохимического исследования сыворотки крови собак при заживлении открытых оскольчатых переломов костей голени представлены в таблице 1.
В динамике эксперимента обнаружены значительные отличия показателей минерального обмена у животных, получавших заявляемое средство (опытная группа), в отличие от животных, не получавших его (контрольная). Так, если у животных опытной группы на 3-е сутки фиксации снижалась только концентрация кальция, то у животных контрольной группы дополнительно снижался и уровень магния в сыворотке крови. В дальнейшем уровень кальция и магния у собак контрольной группы оставался достоверно сниженным до 14-х суток фиксации, тогда как в опытной группе уровень кальция достигал дооперационных значений уже на 7-е сутки эксперимента, а содержание магния относительно дооперационного уровня не изменялось вообще. Кроме того, в конце фиксации и через месяц после снятия аппарата, у животных, получавших препарат, уровень кальция достоверно превышал дооперационные значения. В дополнение к этому у животных опытной группы отмечалось достоверное увеличение неорганического фосфата в сыворотке крови с 14-х суток фиксации вплоть до момента снятия аппарата.
Несмотря на обнаруженные отличия в минеральном обмене, отличий остеорепаративных процессов у животных опытной группы относительно контрольной не выявлено, о чем свидетельствовала схожая динамика активности фосфатаз сыворотки крови и их соотношения.
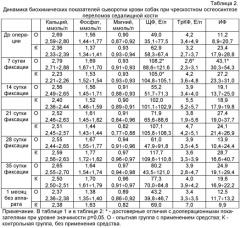
Динамика биохимических показателей сыворотки крови собак при лечении экспериментальных переломов седалищной кости с использованием средства представлена в таблице 2.
Изученные биохимические показатели у животных этой серии в ходе эксперимента незначительно отличались от дооперационных значений, каких-либо особенностей динамики их изменений, связанных с применением средства, не обнаружено.
Таким образом, проведенное биохимическое исследование позволяет сделать следующий вывод. Применение средства, как дополнительного источника минеральных веществ, в ходе лечения экспериментальных переломов приводит к повышению уровня кальция, магния и фосфата в сыворотке крови лишь в тех случаях, когда отмечается недостаток этих элементов.
В проведенном исследовании наиболее значимые изменения минерального состава сыворотки крови были получены при лечении открытых оскольчатых переломов костей голени, когда прием препарата способствовал восстановлению минерального баланса в организме, нарушения которого в условиях данной экспериментальной модели были наиболее значительны.
Следует также особо отметить, что при лечении переломов тела и ветви седалищной кости применение препарата хотя и не привело к значительному изменению минерального состава крови, но при этом способствовало сокращению сроков сращения переломов данного типа.
В ходе лечения экспериментальных переломов аппаратом Илизарова с применением средства, как дополнительного источника минеральных веществ, было выявлено, что его использование у животных первой серии опытной группы способствовало более раннему восстановлению объема мягких тканей, чем в контроле.
Применение заявленного средства сокращает сроки сращения переломов типа A3 (поперечный), тип В2 (клиновидные), тип С2 (сегментарные) на 20-30%, а сложных переломов тела и ветви седалищной кости в среднем на 33%.
Использование средства приводит к повышению уровня кальция, магния и фосфата в сыворотке крови лишь в тех случаях, когда отмечается недостаток этих элементов в результате возрастных изменений минерального обмена или наличия каких-либо заболеваний.
Средство не приводит к значительному повышению содержания кальция в крови, выше критического, а доводит его до нормального уровня.
Применение средства оправдано не только для восстановления минерального баланса в организме, но и при лечении переломов с незначительным изменением минерального состава крови, так как его использование способствует значительному сокращению сроков сращения переломов.
Кроме того, результаты световой микроскопии и морфометрического анализа показали, что в серии с применением средства при более коротких сроках фиксации развиваются более активные репаративные процессы, способствующие формированию костного сращения и ускоряющие процесс органотипической перестройки. Результаты рентгеновского электронно-зондового микроанализа свидетельствовали о формировании более зрелой компактной пластинки, содержание кальция в которой через 90 суток после снятия аппарата было приближено к показателям интактных животных.
Экспериментальные исследования показали, что включение средства в регенерирующие участки кости и в места, прилегающие к перелому, приводит к восстановлению структуры кости, близкой к интактной. Кроме того, усиливает репаративные процессы и сокращает дегенеративные процессы в поврежденных тканях суставного хряща и нервов.
Средство для лечения заболеваний опорно-двигательного аппарата человека и животных, в том числе переломов костей и заболеваний, связанных с дефицитом кальция в организме, на основе соли кальция, отличающееся тем, что оно представляет собой коллоидный раствор водной суспензии минерального состава морского происхождения с размером микрочастиц 10-6-10-7 м с активной поверхностью микрочастиц в виде мицелл не более 500 м2/мл и плотностью водной суспензии, не превышающей 1,7 кг/л, при следующем содержании компонентов, мас.%:
| минеральный состав | 58 |
| вода | остальное, |
| углекислый кальций | 92-98 |
| углекислый магний | 1-5 |
| цинк | 0,1-0,5 |
| железо | 0,1-0,3 |
| кремний | 0,1-0,5 |
| медь | 0,05-0,3 |
| йод | 0,003-0,01 |
| марганец | 0,05-0,3 |
| селен | 0,03-0,1 |
| хром | 0,03-0,1 |