Конъюгат хризофанола, способ его получения, применение его в качестве лекарственного средства для лечения диабетической нефропатии, спаек кишок, остеоартрита
Иллюстрации
Показать всеИзобретение относится к конъюгату хризофанола или его производного, характеризующемуся общей формулой (I), в которой R1-R8 представляют собой группу, выбранную из групп -Н, -ОН, -ОСН3, -СН3, при условии, что не менее двух групп из R1-R8 означают -Н и при условии, что одна или две группы R2, R3, R6, R7 является группой -СООН, М представляет собой азотное органическое основание, выбранное из группы, состоящей из хитозамина, глюкозамина, или основную аминокислоту, выбранную из группы, состоящей из аргинина, лизина, карнитина, и группа М связана с хризофаноловой частью в конъюгат. Изобретение также относится к способу получения этого конъюгата, к применению конъюгата в качестве лекарственного средства для профилактики или лечения диабетической нефропатии, остеоартрита, ревматического или ревматоидного артрита, спаек кишок, восстановление перистальтики кишечника, и к лекарственному средству на его основе.
4 н. и 4 з.п. ф-лы, 4 ил., 19 табл.
Реферат
Изобретение касается конъюгатов хризофанола или его производных, образованных путем взаимодействия хризофанола или его соответствующего производного с различными азотными органическими основаниями, способа получения и применение конъюгата в качестве лекарственных средств для профилактики и лечения диабетической нефропатии, остеоартрита, ревматического или ревматоидного артрита, спаек кишок, восстановления перистальтики кишечника.
Описано применение хризофанола и производных хризофанола в изготовлении различных лекарственных препаратов, например, в Патентной Заявке КНР № 200410049948 описана соль хризофанола, характеризующаяся следующими двумя общими формулами - хризофанолом и солью хризофанола соответственно:
где «М» обозначает щелочной металл, щелочно-земельные металлы, остаток алкалоида.
Хризофанол является соединением, получаемым путем обработки растительного сырья, содержащего в своем составе хризофанол или производные хризофанола, такого как ревень (Rheum palmatum L., Rheum tanruticum Maxim. Ex Balf. или Rheum officinale Baill), горец японский (Polyronum cuspidatum sieb. Et Zucc.), кассия остролистная (Folium sennae), горец многоцветковый (Polyronum multiflorum Thunb., кассия торы (Semen cassiae) и другие, то есть растительного сырья, типовой состав которых по основному действующему веществу характеризуется общей формулой (1).
Данные Медицинских рефератов КНР (поисковое слово «хризофанол»), база данных CNKI (поисковое слово «хризофанол»), Патенты КНР (поисковое слово «хризофанол»), СА (поискать «номер логина № 478-43-3»), Патенты США (поисковое слово «Rhein»), Патенты Европы (поисковое слово «Rhein») показывают, что наиболее известными соединениями хризофанола являются соль натрия хризофанола и соль калия хризофанола (US 6197818, CN 97107137), диацетил хризофанола [13739-02-1] (CN 97192531, CN 93101181, СА 96:193416) и соль калия диацетила хризофанола (ЕР 243968).
Сахарный диабет является болезнью обмена веществ, затрагивающей все системы организма. Хотя механизм заболевания зависит от разных факторов, дефект инсулин рецепторов (IR) и функциональный дефект β-клеток считаются главными звеньями возникновения сахарного диабета. Адипоз, гипертония, гиперлипемия, гиперурикемия и состояние гиперкоагуляции составляют группу заболеваний, являющихся клиническими проявлениями дефекта рецепторов (IR) к инсулину. Дефект рецепторов (IR) к инсулину зачастую существует до появления диабета, он является не только непосредственной причиной возникновения сахарного диабета, но и основой сердечно-сосудистых заболеваний при сахарном диабете.
Диабетическая нефропатия (DN) является распространенным следствием болезни сахарного диабета.
Хризофанол эффективно снижает уровень сахара, регулирует количество жировой ткани, улучшает действие инсулина, снижает выделение мочевого альбумина, поэтому хризофанол играет многоцелевую и многоярусную роль для профилактики и лечения диабетического нефроза.
Абдоминальная хирургия является наиболее распространенной хирургической операцией. Как правило, пациенты после операции имеют относительно слабые функции желудочно-кишечного тракта, поэтому восстановление функции желудочно-кишечного тракта после операции имеет большое значение в реабилитации пациента, в том числе восстановление перистальтики после операции, снижает риск возникновения спаек кишок.
Послеоперационные кишечные спайки кишок являются трудной хирургической проблемой, которая трудно разрешима в клинической практике. Исследовательские работы последних лет показывают, что у 90%-100% пациентов, прошедших операцию в брюшной полости, возникает спайка кишок [Luijendijk RW, etal Foreign material in postoperative Adhesions AnnSurg, 1996,223(3):242; Scott Coombers D.etal Human intraperitoneal fibrinolytic respond to elective surgery BrJSurg, 1995,82:414]. Среди пациентов, у которых возникла спайка кишок, у более 80% это спайка соединительно-тканной пленки, у 50% пациентов это спайка тонких кишок [Menxies D, etal Intestinal obstruction from adhesions: How big is the problem? AnnR Coll Surg Engl, 1990, 72(1):60]. Возникновение спайки кишок связано с брюшным всасыванием и ослаблением кишечной перистальтики. Сокращение экссудации или улучшение энтерокинеза приведет к сокращению числа спаек.
Существующие лекарства для содействия энтерекинезу могут ускорить энтерокинез, но они не уменьшают воспалительные процессы, оказывает слишком мощное воздействие на желудок, поэтому легко вызывают рвоту и плохое самочувствие.
В клинической практике описано использование ревеня для восстановления перистальтики. У пациента сохранялась сильная боль, не удалось фактически восстановлить функционирование желудочно-кишечного тракта [Ли Цисинь и др. Клинический осмотр воздействия ревеня на восстановление функций желудка и кишок пациентов, болеющих диффузным перитонитом и прошедших операцию. Chinese Journal of Coal Industry Medicine, 1998, 1(4):372].
В клинической практике тоже применяется сок сырого ревеня в качестве лекарственного средства [Гэ Хэнвэнь и др. Осмотр при лечебной эффективности сока сырого ревеня для восстановления функций желудка и кишок после операции. Научный вестник Медицинского института санитарных сотрудников провинции Хубэй, 2002, 15(2), 19]. Известно также сочетание ревеня с другими лекарственными растениями китайской медицины для внутреннего приема или приема в качестве настоек. [Хуан Хунхэн и др. Исследование о клиническом применении препаратов для восстановления спайки кишок, Вестники китайской медицины и китайских лекарств, 2006, 5(2), 42]. Но использование в клинической практике затруднительно по причинам нерегулируемости дозы, способов доставки лекарственного средства в организм, в связи с чем клиническое использование средств из ревеня и другого растительного сырья ограничено.
Остеоартрит, ревматический и ревматоидный артриты являются распространенными заболеваниями суставов, имеющие высокую вероятность возникновения. Заболеваемость остеоартритом составляет около 10% от общей численности жителей для пациентов, возраст которых выше 60 лет, более 50% из них подвергаются воздействию данного заболевания, для женщины возрастом моложе 45 лет, а от 45 до 60 лет и свыше 65 лет заболеваемость составляет 2%, 30% и 68% соответственно. А у мужчин - составляет 3%, 24,5% и 58% соответственно.
Существующие лекарственные препараты для лечения остеоартрита в основном включают в себя противовоспалительные средства как стероидного типа, так и нестероидного типа. Всем уже известна негативная реакция стероидного противовоспалительного лекарства. Среди нестероидных препаратов, содержащих ингибитор циклооксигеназы (СОХ) тоже имеет ряд неблагоприятных реакций. Например, при внутреннем приеме или инъекции нестероидных препаратов, содержащих ингибитор циклооксигеназы (СОХ), возникает желудочно-кишечное кровотечение, особенно эти негативные проявления возникают у пожилых людей, что очень вредно для лечения остеоартрита, которое в большей части возникает у пожилых людей.
В связи с тем, что соединение хризофанола нерастворимо в воде, оно не может быть усвоено желудочно-кишечным трактом, что приводит к снижению эффективности биологического применения и ограничивает использование хризофанола. Натриевая соль хризофанола и его производные повышают растворимость хризофанола в воде, вследствие чего повышается биологичекая эффективность при приеме внутрь. Но так как натриевая соль хризофанола, калиевая соль хризофанола (US 6197818, CN 97107137, диацетил хризофанола [13739-02-1] (CN 97192531, CN 93101181, СА 96:193416) и каливая соль диацетил хризофанола (ЕР 243968) являются или сильнощелочными или слабокислыми солями, а водный раствор является щелочным раствором, это делает невозможным их использование в качестве инъекционных растворов, а при снижении значения рН стабильность препаратов снижается.
Технической задачей настоящего изобретения является создание нового конъюгата хризофанола или его производного путем взаимодействия хризофанола или его производного с различными органическими основаниями, которые не только повышают растворимость хризофанола в воде, но и могут преодолеть основной недостаток таких соединений хризофанола, а именно: получение водорастворимого соединения хризофанола с рН, достаточной для использования в инъкционной форме, сохраняющее при этом высокие биологическую активность и стабильность.
Второй задачей настоящего изобретения является создание способа получения водорастворимого конъюгата хризофанола или его производного, путем взаимодействия хризофанола или его производного с органическими основаниями и носителем, допустимым для лекарственного применения.
Третьей задачей настоящего изобретения является применение конъюгата хризофанола или его производного в качестве лекарственного средства для профилактики или лечения диабетической нефропатии, остеоартрита, ревматического или ревматоидного артрита, спаек кишок, восстановления перистальтики кишечника.
Дополнительной задачей является создание стабильного конъюгата хризофанола или его производного с органическим основанием, имеющим в качестве носителя воду.
Лекарственное средство для профилактики или лечения диабетической нефропатии, остеоартрита, ревматического или ревматоидного артрита, спаек кишок, восстановление перистальтики кишечника, содержащее конъюгат хризофанола или его производного с органическими основаниями и носителем в качестве активного ингредиента и носитель, пригодный для лекарственного применения, представляющее собой таблетку, капсулу, желатиновую капсулу, гель, пероральное лекарственное средство, суспензию, настойку, пластырь, мазь, пилюлю, инъекцию, трансфузию, лиофилизированную инъекцию, эмульсию внутреннего вливания, липосомную инъекцию, лекарственное средство для направленной терапии, суппозиторий, лекарственное средство замедленного высвобождения или лекарственное средство с контролируемым высвобождением.
Поставленные изобретательские задачи решаются тем, что конъюгат хризофанола или его производного характеризуются общей формулой (I):
где левая часть возможна в одном из вариантов:
(1) хризофанол или его производное, в котором R1-R8 представляют собой группу, выбранную из групп -Н, -O-глюказа, -ОН, -ОСН3, -СН3, при условии, что не менее двух групп из R1-R8 означают -Н, и при условии, что одна или две группы R2, R3, R6, R7 является группой -СООН;
(2) экстракт растительного сырья, содержащий хризофанол или его производное;
«М» представляет собой азотное органическое основание, выбранное из группы, состоящей из хитозамина, глюкозамина, или основную аминокислоту, выбранную из группы, состоящей из аргинина, лизина, карнитина, и группа М связана с хризофаноловой частью в конъюгат, например, через гидроксил -СООН.
Под экстрактом растительного сырья (2), содержащим хризофанол или его производное, понимается группа соединений, полученная путем экстракции, концентрации, отделением и точной обработкой определенных растений, имеющих единственное действующее активное вещество (материнское ядро). В данном изобретении, действующим активным веществом (материнским ядром) является антрахинон.
Иными словами, его левая часть является экстрактом растительного сырья с содержанием хризофанола, или его производного, в котором R1-R8 представляют собой группу, выбранную из групп -Н, -О-глюказа, -ОН, -ОСН3, -СН3, при условии, что не менее двух групп из R1-R8 означают -Н, и при условии, что одна или две группы R2, R3, R6, R7 является группой -СООН.
R1~R8, выбранные в указанной группе оказывают существенное влияние на лекарственную характеристику вещества, представленного в настоящей заявке.
В указанном решении конъюгат хризофанола или его производного с азотным органическим основанием или основной аминокислотой кардинально отличается от простых солей хризофанола или его производных.
При реакции азотного органического основания или основной аминокислоты с хризофанолом или его производным образуется соль и вода, соединенные ковалентной связью, а при конъюгатном соединении соединение азотного органического основания или основной аминокислоты с хризофанолом или его производным вода не образуется. Конъюгатное соединение образуется с помощью сил межмолекулярного воздействия между двумя молекулами, в реакции отсутствует механизм образования воды и электровалентной связи. Данная структура может быть подтверждена авторами в реакции хризофанола и аргинина до и после проведения реакции, молекулярным весом продукта реакции, элементным анализом двойного соединения хризофанола-аргинина, С-спектром, Н-спектром и другими результатами.
Например данные элементного анализа конъюгата хризофанола-аминокислоты представлены в Табл.2.
| Табл. 2. | ||||
| Результаты элементного анализа двойного соединения хризофанола-аминокислоты | ||||
| Элемент | С (%) | Н (%) | N (%) | S (%) |
| Теоретическое значение | 55.021 | 4.837 | 12.222 | 0.000 |
| Измерительное значение | 55.28 | 4.873 | 12.04 | 0.000 |
| 55.20 | 4.885 | 12.05 | 0.000 |
Из данных Табл.2, очевидно, что разница между теоретическими и измерительными данными, полученными путем элементного анализа в отношении элементов С, Н, N, S, содержащихся в конъюгате хризофанола-аминокислоты, составляет менее 0,5%. Это объясняет то, что полученный продукт соответствует требуемой молекулярной формуле С15Н8О6·C6H14N4O3, и то, что в данной реакции не возникла дегидратация.
Причем, спектральные данные конъюгата хризофанола-аминокислоты в Табл.2 показывают отсутствие кристаллической воды.
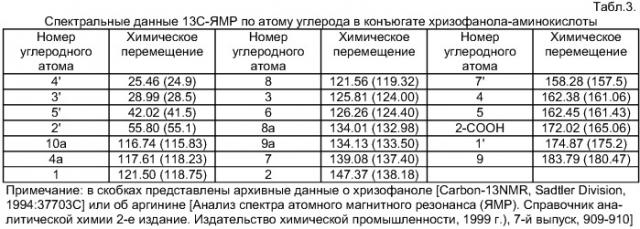
Спектральные данные 13С-ЯМР (ядерно-магнитного резонанса) по атому углерода в конъюгате представлены в Табл.3
При сравнении данных, полученных при измерении спектров 13С-ЯМР в конъюгате, с данными архивных работ, явно понятно, что химическое перемещение 2-й позиции углерода [δ (пик спектра): 147.37(138.18)] и углерода карбоксила со 2-й позиции [δ:172.02(165.06)] перемещается к нижней позиции 9 или 7 единиц, для аргинина в связи с тем, что в его структуре имеется гуанидиновая группа основного радикала, имеющая среднюю интенсивность. В связи с чем можно представить, что карбоксил на 2-й позиии у хризофанола и гуанидиновая группа аргинина образуют соль, смотрите структурную формулу.
После дальнейшего совершенствовании могут появиться следующие оптимальные решения.
1. Левая часть общей формулы (I) является экстрактом растительного сырья,
содержащим хризофанол или его производное в количестве 50-99%.
2. Левая часть общей формулы (I) - хризофанол или его производное, в котором R1-R8 представляют собой группу, выбранную из групп -Н, -O-глюказа, -ОН, -ОСН3, -СН3, при условии, что не менее двух групп из R1-R8 означают -Н, и при условии, что одна или две группы R2, R3, R6, R7 является группой -СООН.
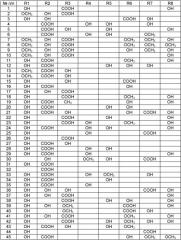
R1~R8 представляют собой следующие варианты групп:
| № п/п | R1 | R2 | R3 | R4 | R5 | R6 | R7 | R8 |
| 1 | ОН | СООН | ОН | |||||
| 2 | ОСН3 | ОН | СООН | |||||
| 3 | ОН | ОН | СООН | ОН | ||||
| 4 | СООН | ОН | ОН | ОН | ||||
| 5 | СООН | ОН | ОН | ОН | ||||
| 6 | СООН | ОН | ОН | ОСН3 | ||||
| 7 | ОСН3 | ОН | СООН | ОСН3 | ОСН3 | ОН | ||
| 8 | ОСН3 | ОН | СООН | ОСН3 | ОСН3 | ОСН3 | ||
| 9 | ОСН3 | ОН | СООН | ОН | ОСН3 | ОН | ||
| 10 | ОСН3 | ОН | СООН | ОН | ||||
| 11 | ОН | СООН | ОСН3 | ОН | ||||
| 12 | ОН | СООН | ОН | ОН | ОН | |||
| 13 | ОСН3 | СООН | ОН | |||||
| 14 | ОСН3 | СООН | ОН | |||||
| 15 | ОН | ОН | СООН | |||||
| 16 | ОН | СООН | ОН | |||||
| 17 | ОН | ОН | СООН | |||||
| 18 | ОН | СООН | ОСН3 | ОН | ||||
| 19 | ОН | СООН | СН3 | ОН | ОН | |||
| 20 | ОН | СООН | ОН | ОН | ||||
| 21 | ОН | СООН | ОН | ОН | СООН | ОН | ||
| 22 | ОН | СООН | ОН | ОН | ||||
| 23 | ОН | СООН | ОН | ОСН3 | ОН | |||
| 24 | ОН | СООН | ОН | ОН | ОН | |||
| 25 | ОН | ОН | СООН | |||||
| 26 | ОН | СООН | ||||||
| 27 | ОН | СООН | ОН | |||||
| 28 | ОН | СООН | ОН | ОН | ||||
| 29 | ОН | СООН | ОН | ОН | ||||
| 30 | ОН | ОСН3 | ОН | СООН | ||||
| 31 | ОН | СООН | ||||||
| 32 | СООН | |||||||
| 33 | ОН | СООН | ОН | ОСН3 | ОН | |||
| 34 | ОН | СООН | ОН | |||||
| 35 | ОН | СООН | ОН | |||||
| 36 | ОН | ОН | ОН | СООН | ОН | |||
| 37 | ОН | ОН | СООН | ОН | ||||
| 38 | ОН | СООН | ОН | ОН | ОН | |||
| 39 | ОН | ОН | ОСН3 | СООН | ОН | |||
| 40 | ОН | ОСН3 | СООН | ОН | ||||
| 41 | ОН | ОН | СООН | ОСН3 | ОН | |||
| 42 | ОН | СООН | ОН | ОСН3 | ОН | ОН | ||
| 43 | ОН | СООН | ОН | ОН | ОСН3 | |||
| 44 | ОН | СООН | ||||||
| 45 | ОН | СООН | ОН | ОСН3 | ОСН3 |
Самым оптимальным вариантом левой части общей формулы (I) является экстракт ревеня (Rhein).
3. В общей формуле (1) «М» может быть: основной аминокислотой, аргинином, лизином или карнитином.
4. В общей формуле (1) «М» может быть: органическое азотное основание, хитозамин, глюкозамин.
Способ получения вышеуказанных конъюгатов хризофанола и его производных заключается во взаимодействии экстракта, содержащего хризофанол или хризофанол и производные хризофанола, с азотным органическим основанием или основной аминокислотой, реакцию проводят в водном и/или спиртовом растворе при соотношении компонентов в молях 1:0,5-4,0. В указанных способах получения описаны азотное органическое основание, выбранное из группы, состоящей из хитозамина, глюкозамина или основной аминокислотой, выбранной из группы, состоящей из аргинина, лизина, карнитина.
Полученный конъюгат хризофанола или его производного с азотным органическим основанием или с основной аминокислотой хорошо растворим в воде, рН его водного раствора наиболее приемлем для человеческого организма, за счет чего снижается его токсичность и побочные действия, что позволяет создать из конъюгата водорастворимый лекарственный препарат, что в свою очередь повышает его биологическую эффективность.
Хризофанол или соединение хризофанола получают путем экстракции и сгущения экстракта лекарственных растений или другим известным способом.
Лекарственное растение ревень (Rheum - корень или стебель растений, относящихся к одинаковому роду) дробят, экстрагируют водой, добавляя в водный раствор неорганическую кислоту и окисляющее средство для осуществления реакции, получают экстракт (часть с содержанием хризофанола), осуществляют разделение смеси на хроматографической колонке с последующим выделением хризофанола.
В том числе 1: способ получения лекарственного конъюгата из экстракта хризофанола и основной аминокислоты или азотного органического основания состоит из следующих этапов.
Смешивают полученный экстракт хризофанола и воду и/или этиловый спирт в пропорции 1:0,5-4,0 (в молях), добавляют основную аминокислоту, выбранную из группы аргинин, лизин или карнитин, проводят реакцию, растворитель удаляют при пониженном давлении; или смешивают полученный экстракт хризофанола и воду и/или этиловый спирт по пропорции 1:0,5-4,0 (в молях), добавляют азотное органическое основание, выбранное из группы хитозамин, аминоглюкоза, выполняют реакцию при постоянном помешивании, растворитель удаляют при пониженном давлении.
В том числе 2: способ получения лекарственного конъюгата из хризофанола основной аминокислоты или азотного органического основания состоит из следующих этапов.
Смешивают хризофанол и воду и/или этиловый спирт по пропорции 1:0,5-4,0 (в молях), добавляют основную аминокислоту, выбранную из группы аргинин, лизин или карнитин, проводят реакцию, растворитель удаляют при пониженном давлении; или смешивают хризофанол и воду и/или этиловый спирт по пропорции 1:0,5-4,0 (в молях), добавляют азотное органическое основание, выбранное из группы хитозамин, аминоглюкоза, выполняют реакцию при постоянном помешивании, растворитель удаляют при пониженном давлении.
Затем конъюгат хризофанола и его производных идут на производство лекарственных средств.
Различные лекарственные формы препаратов из конъюгата хризофанола и его производных могут быть получены простыми способами, принятыми в фармацевтической промышленности, например путем смешения конъюгата по формуле (I) с вспомогательными веществами, с последующим изготовлением требуемого препарата.
Решением третьей задачи по настоящему изобретению является применение конъюгата хризофанола или его производного в любой лекарственной форме, принятой в фармацевтической промышленности, в качестве лекарственного средства для профилактики или лечения диабетической нефропатии, остеоартрита, ревматического или ревматоидного артрита, спаек кишок, восстановления перистальтики кишечника.
При этом содержание конъюгата хризофанола или его производного по формуле (I) в молях составляет 0.1%~99.5%, в том числе содержание хризофанола составляет 1,0%-95%.
Лекарственное средство для профилактики или лечения диабетической нефропатии, остеоартрита, ревматического или ревматоидного артрита, спаек кишок, восстановления перистальтики кишечника, содержащее конъюгат хризофанола или его производного в качестве активного ингредиента, содержит вспомогательное вещество, пригодное для лекарственного применения, представляющее собой таблетку, капсулу, желатиновую капсулу, гель, пероральное лекарственное средство, суспензию, настойку, пластырь, мазь, пилюлю, инъекцию, трансфузию, лиофилизированную инъекцию, эмульсию внутреннего вливания, липосомную инъекцию, лекарственное средство для направленной терапии, суппозиторий, лекарственное средство замедленного высвобождения или лекарственное средство с контролируемым высвобождением.
Вышеуказанные вспомогательные вещества, допустимые в фармацевтике, - это, например, вода и этиловый спирт для настоек, крахмал, используемый в твердых лекарственных формах и в качестве стабилизатора суспензий и эмульсий, тростниковый сахар, молочный сахар, микрокристаллическое волокно др., закрепитель волокнистый дериват, альгинаты - разрыхляющие, эмульгирующие, прологирующие, пленкообразующие вспомогательные вещества, а также для приготовления мазей и паст, агароид обладает стабилизирующими, разрыхляющими и скользящими свойствами, в смеси с глицерином в 1,5% концентрации используется в качестве мазевой основы, желатин - для изготовления мазей, желатиновых капсул, суппозиториев, бентонит - в обеспечивают лекарственным препаратам мягкость, дисперсность, высокие адсорбционные свойства, легкую отдачу лекарственных веществ, аэросил - используют с целью стабилизации сухих экстрактов (уменьшается их гигроскопичность, метилцеллюлоза растворимая - в качестве эмульгатора и стабилизатора при изготовлении суспензий и эмульсий, а также как пролонгирующий компонент, поливинол - синтетический водорастворимый полимер винилацетата, поливинилпирролидон (ПВП), карбоксиметилцеллюлоза поперечной связи, декстрин, агар-агар, углекислый калий, двууглекислый натрий; акселератор абсорбции как четвертичное соединение аммония; поверхностный активатор как сетанол, додецилсульфат натрия; носитель абсорбции как каолин и бентонит; тальк, стеориновокислый калий, стеориновокислый магний, тонкозернистый силикагель, поликликоль и другие вспомогательные вещества, используемые в фармацевтической промышленности.
Инъекционными формами конъюгата хризофанола или его производственных в виде трансфузии, лиофилизированной инъекции, эмульсии внутреннего вливания, липосомной инъекции могут быть получены путем распыления в масле - соевом, полигликоле 400, хлопковом, арахисовом, кунжутном, кукурузном, оливковом - при добавлении солюбилизирующего средства, совместимого растворителя, антиоксиданта, в суспензии, полученной путем смешения измельченного порошка конъюгата и полисорбитола 80, с последующим растворением смеси в водном растворе однозамещенного фосфата калия, фосфата калия двузамещенного, нипакина и карбоксиметилцеллюлозы натрия.
В качестве солюбилизирующего средства могут быть полиоксиэтилен кунжутного масла, гидрированное кунжутное масло полиоксиэтилена, кеторурролидин полиоксиэтилена, полоксамер, полисорбит, полигликоль, плюроник F-68, а указанный совместимый растворитель включает аргинин, лизин, хитозамин, или глюкозамин, диэтиламин, этилиндиамин, карбамид, карнитин, ниацинамид, пролин, глюкозу, лимонную кислоту и соль натрия.
Суточная доза лекарственного средства, содержащего конъюгат хризофанола или его производного в качестве активного ингредиента по формуле (I) в зависимости от назначения, заболевания, возраста, массы тела пациента, может составлять 1~300 мг/м2, а оптимальное значение 10~200 мг/м2.
Приведенные ниже примеры предназначены для демонстрации, но не ограничивают воплощения данного изобретения.
В данном изобретении конъюгат хризофонала или его производного преодолевает недостаток хризофанола или его производных, таких как плохая растворимость, высокое значение рН солей хризофанола, приводящее к нестабильности водного инъекционного раствора и невозможности применения его в качестве лекарственного средства. Конъюгат хризофонала или его производного не только хорошо растворим в воде, но и из него возможно промышленно производить разные препараты различных лекарственных форм, особенно водорастворимые инъкционные формы.
В данном изобретении предложен способ получения лекарственного конъюгата хризофонала путем взаимодействия экстракта, содержащего хризофанол или производные хризофанола, с азотным органическим основанием или основной аминокислотой.
В данном изобретении предложено применение конъюгата хризофонала в изготовления лекарственных средств для лечения диабетической нефропатии.
По данному изобретению рН конъюгата хризофонала имеет диапазон от слабокислого до слабощелочного, а его водный раствор для инъекции, водная настойка для приема внутрь имеют нейтральную рН, что является преимуществом при фармакологической доступности препарата. Стабильность лекарственных средств на основе конъюгата выше стабильности соответствующих солей натрия и калия, что позволяет производить на их основе лекарственные средства против диабетической нефропатии.
Существующая сегодня на рынке продукция является просто сбором лекарственного ревеня или экстрактом ревеня. До сих пор не встречались работы, описавшие конъюгаты хризофанола или его производных с основными аминокислотами и азотными органическими основаниями, на рынке нет фармацевтической продукции на их основе.
Поэтому, в данном изобретении впервые раскрыта информация о конъюгатах хризофанола или его производных, о способе его получения, о применении конъюгата хризофанола в изготовлении лекарственных средств.
Приложенные чертежи:
фиг.1. Результаты элементарного анализа аргинина хризофанола;
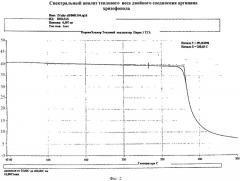
фиг.2. Спектр анализа теплого веса двойного соединения аргинина хризофанола;
фиг.3. фиг.4. Углеродный спектр атомного магнитного резонанса.
Приведенные ниже Примеры предназначены для демонстрации, но не ограничивают воплощения данного изобретения.
Практические примеры:
ПРИМЕР 1. Экстракция и извлечение хризофанола
В 500 г измельченного в порошок ревеня, добавить 2500 мл 60% этилового спирта, в течение 1 часа экстрагировать методом обратной рециркуляции не менее 2-х раз, соединенный экстракт загустить до 1000 мл, дополнить в густой экстракт 100 мл концентрированной соляной кислотой, гидролизовать концентрат в течение 1 часа при температуре в 50°С, остудить, осадок отфильтровать, дополнить 1000 мл 5% раствора NaHCO3, подогреть раствор, отфильтровать, дополнить в фильтрованную жидкость спирт до концентрации его 50-90%, отфильтровать, регулировать значение рН с помощью густой соляной кислоты до того, когда оно станет ниже 3, отфильтровать желтый осадок, промыть водой до нейтрального состояния, перекристаллизовать с помощью ледяной уксусной кислоты до получения вещества, содержание хризофанола в котором должно быть выше 98%.
ПРИМЕР 2. Получение хризофанола
6 г фенола хризофанола поместить в 150 мл раствора смеси уксусного ангидрида и пиридина в соотношении 1:1, оставить полученную смесь на ночь при комнатной температуре, перелить смесь в холодную воду для кристаллизации, отфильтровать, высушить, налить 300 мл раствора смеси уксусного ангидрида и ледяной уксусной кислоты в соотношении 1:1, каплями добавить раствор хромового ангидрида при температуре 45°С, с последующим смешиванием в течение 8 часов при температуре 65°С, вылить полученную смесь в воду, после кристаллизации отфильтровать, дополнить 1000 мл 25% раствора Na2CO3, экстрагировать 3 раза с помощью хлороформа, подогреть раствор Na2CO3 до кипения, дополнить соляной кислотой для окисления, подождать, пока прекратится газообразование, нагревать в течение 1 часа до кипения, остудить, после кристаллизации отфильтровать, промыть водой, перекристаллизовать ледяной уксусной кислотой для получения 2 г вещества, содержание хризофанола в котором будет свыше 98%.
ПРИМЕР 3. Экстракция и извлечение хризофанола с содержанием 50%.
100 г грубого порошка ревеня поместить в подходящую емкость, добавить 2500 мл 60% этилового спирта; подогреть, в течение 1 часа экстрагировать методом обратной рециркуляции не менее 2-х раз, соединенный экстракт загустить до 30% от общего объема оригинального раствора для получения не густого сиропа, при помешивании в течение не более 10 мин добавлять в горячем состоянии концентрированную соляную кислоту в соотношении 1 единица объема густой соляной кислоты на 10 объемов густого экстракта, затем центрифугировать для получения осадка, добавить раствор 5% NaHCO3 в количестве, равном концентрату, подогреть раствор; центрифугировать, отделить верхнюю светлую жидкость, в осадок добавить спирт до достижения его содержания 60-90%, смешивать, центрифугировать, отделить верхнюю светлую жидкость; добавлять концентрированную соляную до значения рН 2, центрифгировать и высушить до получения темно-коричневого порошка.
ПРИМЕР 4. Получение коъюгата хризофанола с аргинином, с 50% содержанием хризофанола
40 г экстракта, содержащего 50% хризофанола, поместить в подходящую емкость, добавить воду, добавить 22 г L-аргинина и подогреть, затем остудить, добавить спирт до достижения его содержания 60-90%, смешивать до растворения, отфильтровать, концентрировать раствор, дбавить этиловый спирт в концентрированный раствор до достижения его содержания 40-80%, выдержать до выпадения осадка, отфильтровать, осушить до получения твердой массы 28 г.
ПРИМЕР 5. Получение коъюгата хризофанола с лизином с 50% содержанием хризофанола
40 г экстракта, содержащего 50% хризофанола, поместить в подходящую емкость, добавить воду, добавить 20 г лизина и подогреть, остудить, затем остудить, добавить спирт до достижения его содержания 50-90%, смешивать до растворения, отфильтровать, концентрировать раствор, добавить этиловый спирт в концентрированный раствор до достижения его содержания 40-80%, выдержать до выпадения осадка, отфильтровать, осушить до получения твердой массы 25 г.
ПРИМЕР 6. Получение конъюгата хризофанола с аргинином
2 г хризофанола поместить в подходящую емкость, добавить этилового спирта до растворения, добавить 2,5 г растворенного в воде L-аргинина, подогреть, перемешивая до растворения хризофанола, отогнать растворитель при пониженном давлении до получения твердого осадка 3,1 г.
ПРИМЕР 7. Получение конъюгата хризофанола с лизином
2 г хризофанола поместить в подходящую емкость, добавить этилового спирта до растворения, добавить растворенного в воде 2,3 г лизина, подогреть, перемешивая до растворения хризофанала, отогнать растворитель при пониженном давлении до получения твердого осадка 2,9 г.
ПРИМЕР 8. Получение конъюгата хризофанола с хитозамином
2 г хризофанола поместить в подходящую емкость, добавить этилового спирта до растворения, добавить растворенного в воде 3 г хитозамина, подогреть, перемешивая до растворения хризофанола, отогнать растворитель при пониженном давлении до получения твердого осадка 3,1 г.
ПРИМЕР 9. Получение конъюгата хризофанола с карнитином
2 г хризофанола поместить в подходящую емкость, добавить этилового спирта до растворения, добавить растворенного в воде 2,5 г карнитина, подогреть, перемешивая до растворения хризофанала, отогнать растворитель при пониженном давлении до получения твердого осадка 3 г.
ПРИМЕР 10. Получение конъюгата хризофанола с глюкозамином
6,3 г глюкозамина растворить в 250 мл дистиллированной воды, при помешивании добавить 2,5 г хризофанола, при нагревании осуществлять рециркуляцию в течение 2-х часов. Затем смесь охладить, добавить 700 мл этилового спирта, центрифугировать и отделить осадок. Часть растворителя отогнать при пониженном давлении до объема 100 мл, затем добавить 70 мл этилового спирта, охладить. Выделенный желтый осадок отфильтровать, перекристаллизовать в этиловом спирте, полученный конъюгат хризофанола-глюкозамина высушить под вакуумом при 40°С.
ПРИМЕР 11. Получение конъюгата экстракта хризофанола с глюкозамином с содержанием хризофанола 50%
6,3 г глюкозамина растворить в 250 мл дистиллированной воды, при помешивании добавить 5 г экстракта, содержащего 50% хризофанола, при нагревании осуществлять рециркуляцию в течение 2-х часов. Затем смесь охладить, добавить 700 мл этилового спирта, центрифугировать и отделить осадок. Часть растворителя отогнать при пониженном давлении до объема 100 мл, затем добавить 70 мл этилового спирта, охладить. Выделенный желтый осадок отфильтровать, перекристаллизовать в этиловом спирте, полученный конъюгат экстракта хризофанола с глюкозамином высушить под вакуумом при 40°С.
ПРИМЕР 12. Получение конъюгата экстракта хризофанола с карнитином с содержанием хризофанола 50%
40 г экстракта, содержащего 50% хризофанола, поместить в подходящую емкость, добавить воду, добавить 22 г карнитина и подогреть, затем остудить, добавить этиловый спирт до достижения его содержания 50-90%, перемешивать до растворения, отфильтровать, концентрировать раствор, затем добавить этиловый спирт до достижения его содержания 40-80%, дать постоять до выпадения осадк