Соединения для ингибирования обратного захвата 5-гидрокситриптамина и норэпинефрина или для лечения депрессивных состояний, способы их получения и применения
Иллюстрации
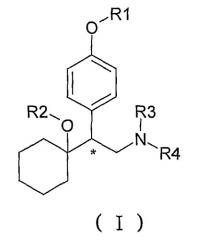
Показать всеНастоящее изобретение относится к новым соединениям формулы (I), их оптическим изомерам или фармацевтически приемлемым солям, которые могут быть использованы для ингибирования или блокирования обратного захвата 5-гидрокситриптамина (5-НТ) и/или норэпинефрина (NA), а также для лечения заболеваний, связанных с центральной нервной системой, к фармацевтической композиции на их основе и к их применению для изготовления лекарственного средства.
где хиральный центр (*) может быть R или S или RS (рацемическая смесь), R3 и R4 независимо выбраны из насыщенного алкила, имеющего 1-6 атомов углерода, а значения заместителей R1 и R2 такие, как указаны в формуле изобретения. 4 н. и 8 з.п. ф-лы, 10 табл., 3 ил.
Реферат
Область техники, к которой относится изобретение
Изобретение относится к соединениям формулы (I) и их солям, способам их получения, фармацевтическим композициям, содержащим соединения, и их применениям для ингибирования обратного захвата 5-гидрокситриптамина (5-НТ) и норэпинефрина (NA) и для лечения или вспомогательной терапии нарушений центральной нервной системы, таких как депрессия и т.д.
Уровень техники
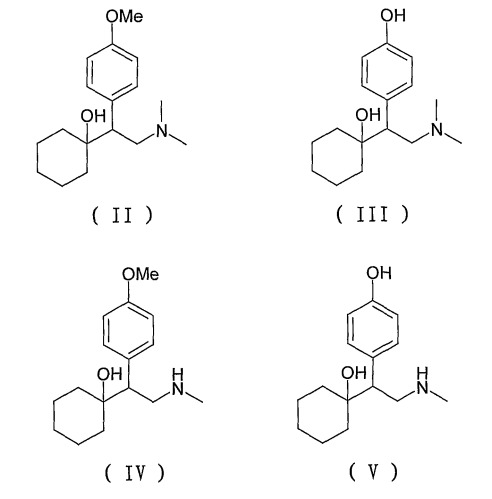
Сообщается, что венлафаксин формулы (II), 1-[2-диметиламино-1-(4-метоксифенил)этил]циклогексанол, является ингибитором обратного захвата 5-гидрокситриптамина (5-НТ) и норэпинефрина (NA) и широко применяется для лечения депрессивных состояний и т.д. Кроме того, после введения в организм соединения формулы (II) оно подвергается метаболизму в печени с образованием высокоактивного метаболита (III), 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола, и слабоактивных метаболитов, (IV), 1-[2-метиламино-1-(4-метоксифенил)этил]циклогексанола и (V), 1-[2-метиламино-1-(4-гидроксифенил)этил]циклогексанола, где соединения (II) и (III) имеют одинаковые терапевтические действия (см. также US4535186, US20040176468, US20040147601, US20030191347, Wyeth Effexor description).
По сравнению с введением соединения (II) непосредственное введение соединения (III) для лечения заболеваний, связанных с центральной нервной системой, особенно депрессии, имеет преимущество по принципу применения одного активного соединения, что облегчает регулирование дозы и терапевтических воздействий, смягчает побочные действия и уменьшает риск взаимодействия с другими лекарственными средствами (см. US6673838). Однако соединение (III) c большим числом гидроксильных групп приводит к увеличению гидрофильности и, следовательно, уменьшает скорость абсорбции при пероральном или чрескожном введении и, возможно, приводит к большим предсистемным побочным действиям вследствие неабсорбированного лекарственного средства. Для преодоления вышеназванных недостатков соединения (III) были синтезированы производные соединения (III), [соединения формулы (I)], которые как пролекарства соединения (III) подвергаются метаболизму in vivo с образованием соединения (III), проявляющего при этом терапевтические действия.
Сущность изобретения
Задача настоящего изобретения состоит в разработке новых соединений, которые применяют как пролекарства ингибитора обратного захвата 5-гидрокситриптамина (5-НТ) и норэпинефрина (NA), в особенности применяемого для лечения депрессии и т.д. Полученные при этом соединения формулы (I) имеют преимущество по принципу применения одного активного соединения, что в свою очередь облегчает регулирование дозы и терапевтических воздействий, облегчает побочные действия, уменьшает риск взаимодействия с другими лекарственными средствами, повышает биодоступность и уменьшает предсистемные побочные действия вследствие неабсорбируемого лекарственного средства.
Настоящее изобретение относится к соединениям формулы (I), их оптическим изомерам или фармацевтически приемлемым солям, которые применяют как пролекарства ингибиторов обратного захвата 5-гидрокситриптамина (5-НТ) и норэпинефрина (NA), в особенности для лечения депрессии и т.д.
где хиральный центр (*) может быть R, S или RS (рацемическая смесь);
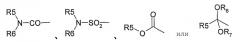
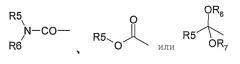
R1 выбран из С1-С20 насыщенного алкилацила или С2-С20 ненасыщенного алкилоила, предпочтительно формила, ацетила, пропионила, бутаноила, изобутирила и насыщенного или ненасыщенного жирного ацила; или арилоила, имеющего 7-20 углеродных атомов, предпочтительно бензоила с заместителем, имеющим 1-10 углеродных атомов, или незамещенного бензоила; или циклоалкилоила, имеющего 4-10 углеродных атомов, или гидроксиалкилоила или углевода, имеющего 1-10 углеродных атомов, а также С1-С10 органической ацильной группы, содержащей кислород, азот и фтор, серу, фосфор или другие гетероатомы или следующие группы:
,
где R5, R6 и R7 независимо выбраны из водорода, насыщенного алкила, имеющего 1-10 углеродных атомов, или ненасыщенного алкила, имеющего 2-20 углеродных атомов, или арила, имеющего 7-20 углеродных атомов, такого как фенил или бензил с заместителем, имеющим 1-10 углеродных атомов, или незамещенный фенил или бензил, и т.д.;
R2 выбран из водорода, насыщенного алкила, имеющего 1-20 углеродных атомов, ненасыщенного алкила, имеющего 2-20 углеродных атомов, арила, имеющего 6-20 углеродных атомов, циклоалкила, имеющего 4-10 углеродных атомов, гидроксиалкильного или углеводного заместителя, имеющего 1-10 углеродных атомов, насыщенного алкилоила, имеющего 1-20 углеродных атомов, ненасыщенного алкилоила, имеющего 2-20 углеродных атомов, предпочтительно формила, ацетила, пропионила, бутаноила, изобутирила и ненасыщенного жирного ацила; арилоила, имеющего 7-20 углеродных атомов, предпочтительно бензоила с заместителем, имеющим 1-10 углеродных атомов, или незамещенного бензоила; циклоалкилоила, имеющего 4-10 углеродных атомов, гидроксиалкилоила, имеющего 1-10 углеродных атомов, С1-С10 органической ацильной группы, содержащей кислород, азот и фтор, серу, фосфор или другие гетероатомы или следующие группы:
,
где R5, R6 и R7 независимо выбраны из водорода, насыщенного алкила, имеющего 1-20 углеродных атомов, ненасыщенного алкила, имеющего 2-20 углеродных атомов, или арила, имеющего 6-20 углеродных атомов, такого как фенил или бензил с заместителем, имеющим 1-10 углеродных атомов, или незамещенный фенил или бензил, и т.д.;
R3 и R4 независимо выбраны из водорода, насыщенного алкила, имеющего 1-20 углеродных атомов, ненасыщенного алкила, имеющего 2-20 углеродных атомов, арила, имеющего 6-20 углеродных атомов, такого как фенил или бензил с заместителем, имеющим 1-10 углеродных атомов, или незамещенный фенил или бензил; циклоалкила, имеющего 4-10 углеродных атомов, гидроксиалкила или углевода, имеющего 1-10 углеродных атомов, а также С1-С10 органического алкила, содержащего кислород, азот и фтор, серу, фосфор или другие гетероатомы, и т.д.;
предпочтительно, R1 представляет собой арилоил, имеющий 7-20 углеродных атомов, алкоксилоил, имеющий 1-10 углеродных атомов, или арилоксилоил, имеющий 7-10 углеродных атомов, 1,1-диалкоксилалкил, имеющий 1-10 углеродных атомов, и алкиламинокарбонил, имеющий 1-10 углеродных атомов; R2 представляет собой водород, R3 и R4 представляют собой метил.
Вышеуказанный арилацил, предпочтительно, представляет собой
где R8 и R9 независимо выбраны из водорода, насыщенного алкила, имеющего 1-6 углеродных атомов, или алкоксила, имеющего 1-6 углеродных атомов, ненасыщенного алкила, имеющего 2-6 углеродных атомов, ОН, Cl, F, CN, карбоксила и сложноэфирной группы, предпочтительно водорода, метила, этила, метокси, этокси, фтора или карбоксила.
Согласно настоящему изобретению термин «оптические изомеры» относится к оптическим изомерам R или S, или к рацемической смеси RS соединений (I), или их фармацевтически приемлемым солям.
Согласно настоящему изобретению репрезентативными соединениями формулы (I) являются:
4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоат,
4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоат,
4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоат,
4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-фторбензоат,
4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-2-карбоксилбензоат,
4-[2-диметиламино-1-(1-бензоилоксициклогексил)этил]фенилбензоат,
4-[2-диметиламино-1-(1-(4-метил)бензоилоксициклогексил)этил]фенил-4-метилбензоат,
4-[2-диметиламино-1-(1-(4-метокси)бензоилоксициклогексил)этил]фенил-4-метоксибензоат,
4-[2-диметиламино-1-(1-(4-фтор)бензоилоксициклогексил)этил]фенил-4-фторбензоат,
4-[2-диметиламино-1-(1-бензоилоксициклогексил)этил]фенил-4-метилбензоат,
1-[2-диметиламино-1-(1-бензоилоксициклогексил)этил]циклогексил-4-метоксибензоат,
4-[2-диметиламино-1-(1-(4-метокси)бензоилоксициклогексил)этил]фенил-4-метилбензоат,
4-[2-диметиламино-1-(1-бензилоксициклогексил)этил]фенил-N-метилкарбамат,
4-[2-диметиламино-1-(1-бензилоксициклогексил)этил]фенил-N,N-диметилкарбамат,
4-[2-диметиламино-1-(1-бензоилоксициклогексил)этил]фенилэтилкарбонат и их различные соли и оптические изомеры.
Согласно общепринятым в области техники способам изготовления лекарственных средств соединения формулы (I) настоящего изобретения, включающие в себя их оптические изомеры и рацемические смеси, а также фармацевтически приемлемые соли, можно обрабатывать с образованием соответствующих лекарственных форм, таких как лекарственные формы для перорального, инъекционного, чрескожного, назального введения, введения через слизистую оболочку или путем ингаляции. Лекарственными формами для перорального введения могут быть твердые таблетки, или капсулы, или мягкие капсулы, или драже, а также растворы, или суспензии, или эмульсии, или порошки, могут быть стандартные лекарственные формы, или с замедленным высвобождением, или с сайт-специфической доставкой, или быстро высвобождаемые, или дезинтегрирующиеся лекарственные формы. Лекарственными формами для инъекционного введения могут быть внутривенная инъекция, или подкожная инъекция, или внутримышечная инъекция, или внутрибрюшинная инъекция, могут быть растворы, или суспензии, или эмульсии, и могут быть стандартные или продолжительно действующие лекарственные формы, такие как имплантаты, микросферы или гели. Лекарственными формами для чрескожного введения могут быть чрескожный пластырь, гели или другие формы. Ингаляционным путем можно вводить растворы, суспензии, эмульсии или порошки. Лекарственными формами для введения через слизистую оболочку могут быть растворы, суспензии, эмульсии, порошки или суппозитории.
Настоящее изобретение, кроме того, относится к фармацевтическим композициям, включающим в себя эффективное количество соединения формулы (I), и совместимые и фармацевтически приемлемые носители или разбавители. Носителями могут быть любые инертные органические или неорганические вещества, такие как вода, желатин, целлюлоза, крахмал и т.д., или другие фармацевтически активные вещества и другие общепринятые добавки, такие как стабилизаторы, увлажняющие агенты, эмульгаторы, корригентные агенты и буферы и т.д.
Соединения формулы (I) настоящего изобретения, включающие в себя их оптические изомеры и рацемические смеси, а также фармацевтически приемлемые соли, можно применять для лечения соответствующих заболеваний или нарушений, например депрессии, тревожных расстройств, генерализованных тревожных расстройств, панической атаки, агорафобии, посттравматических стрессовых расстройств, предменструальных дисфорических нарушений, фибромиалгии, ухудшения внимания, обсессивно-компульсивного синдрома, социальных тревожных расстройств, аутистических нарушений, шизофрении, ожирения, нервно-психической гиперорексии и нервно-психической анорексии, синдрома Туретта, вазомоторной гиперемии, кокаиновой и алкогольной аддикции, сексуального расстройства, пограничного расстройства личности, синдрома хронической усталости, недержания мочи, болей, синдрома Шая-Дрейджера, синдрома Рейно, болезни Паркинсона, эпилепсии и т.д., путем однократной или многократной дозы от 1 мг до 1000 мг в сутки.
Краткое описание чертежей
На фиг.1 показан метаболизм in vivo пролекарства гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата в организме крыс, где А обозначает внутривенное введение, В обозначает пероральное введение; в группе I, □ обозначает пролекарство: 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоат, и ■ обозначает активный метаболит: соединение (III); в группе II ◯ обозначает пролекарство: 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоат, и ● обозначает активный метаболит: соединение (III).
На фиг.2 показана in vivo абсорбция и метаболизм сукцината 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) (ODV сукцинат) (обозначенного -□-) и его пролекарства: гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата (бензоат) (обозначенного -▲-), гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата (4-метилбензоат) (обозначенного -♦-) и сукцината 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоата (4-метоксибензоат) (обозначенного -∇-), в организме гончих собак, где все концентрации крови относятся к активному метаболиту - соединению (III).
Конкретные способы осуществления изобретения
Настоящее изобретение далее иллюстрируется следующими примерами, но не ограничивается ими.
2,52 г (10 ммоль) соединения (III) и 9,98 ммоль органического ацилхлорида добавляли в 100 мл дихлорметана, перемешивали и охлаждали до 0°С. Добавляли по каплям 1,05 г (9,9 ммоль) триэтиламина в растворе дихлорметана (приблизительно десять минут), затем непрерывно перемешивали при комнатной температуре в течение 18 часов. Реакционный раствор промывали 50 мл воды и разделяли, затем органическую фазу сушили над безводным сульфатом натрия, растворитель удаляли выпариванием в вакууме и продукт сушили в вакууме.
Образование соли (например, гидрохлорида) соединения VI
30 мл раствора безводного простого эфира, содержащего 5 ммоль вышеназванного продукта, охлаждали до 0°С и затем добавляли 1М раствор простого эфира, содержащий 4,8 ммоль хлористого водорода, в атмосфере газообразного азота. Маслянистый осадок повторно промывали безводным простым эфиром и затем сушили в вакууме. Большинство продуктов были аморфными пеноподобными твердыми веществами.
Согласно вышеуказанной схеме реакции были синтезированы и охарактеризованы следующие соединения.
Пример 1. Синтез фенилового моноэфира карбоновой кислоты [формулы (VI)] соединения (III)
Соединение (III) синтезировали согласно US4535186.
А. Общие методы и способы
Общая схема реакции:
где R представляет собой фенил, толил, метоксифенил или другой арил и т.д.
4-[2-Диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоат получали в качестве примера.
10 г дезметил-венлафаксина (соединение III) растворяли в 200 мл безводного пиридина и охлаждали до 0°С. Добавляли по каплям эквимолярное количество 4-метилбензоилхлорида, растворенного в безводном тетрагидрофуране, и реакцию проводили при этой температуре при перемешивании в течение 5 часов. Затем большую часть растворителя удаляли выпариванием в вакууме. Остаток выливали в 400 мл воды, устанавливали при перемешивании рН 9 и сохраняли в течение ночи. Осажденное твердое вещество отфильтровывали, промывали водой три раза и сушили с получением неочищенного продукта. Неочищенный продукт перекристаллизовывали с применением 80 мл безводной смеси этанол/этилацетат (1:1) с получением 8,0 г белого твердого вещества с точкой плавления 159,0-162,2°С и выходом 55,2%.
Получение гидрохлорида: 20 мл безводного этанола добавляли к 2,0 г вышеуказанного продукта, добавляли по каплям концентрированную хлористоводородную кислоту до растворения всего продукта, затем растворитель удаляли выпариванием в вакууме, продукт промывали безводным этанолом три раза и растворяли добавлением этилацетата. Осажденное твердое вещество отфильтровывали с получением 2,0 г белого кристаллического твердого вещества, имеющего точку плавления 203,2-206,5°С.
Согласно этому способу были синтезированы и охарактеризованы следующие соединения.
Соединение 1: 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоат
1Н-ЯМР (ДМСО) δ 1,14-1,59 (10Н, м, -(СН2)5-), 2,11 (6Н, с, -N(CH3)2), 2,42 (3H, c, Ar-CH3), 2,55 (1H, м, -СН<), 2,86 (2Н, м, -СН2-N-), 5,02 (1H, ушир., -ОН), 7,11, 7,27, 7,40, 8,00 (8Н, д, д, д, д, Ar-H);
13С-ЯМР (ДМСО) 21,40, 21,65 (2С), 24,79, 39,89, 40,81 (2С), 45,89 (2С), 57,94, 76,57, 120,19 (2С), 123,01 (2С), 126,42, 127,95 (2С), 128,13 (2С), 136,97, 141,90, 147,42, 164,18;
точка плавления: 159,0-162,2°С, точка плавления его гидрохлорида: 203,2-206,5°С.
Соединение 2: 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоат
Все условия реакции были, как описано выше, за исключением того, что 4-метилбензоилхлорид заменяли бензоилхлоридом.
1Н-ЯМР (ДМСО) δ 0,97-1,61 (10Н, м, -(СН2)5-), 2,12 (6Н, с, -N(CH3)2), 2,57 (1H, т, >СН-), 2,84 (2Н, м, -СН2-N-), 4,98 (1Н, ушир., -ОН), 7,13-8,13 (9Н, м, Ar-H);
13С-ЯМР (ДМСО) 21,65 (2С), 24,79, 39,89, 40,81 (2С), 45,89 (2С), 57,94, 76,57, 120,19 (2С), 123,01 (2С), 125,92, 128,80 (2С), 132,99 (2С), 133,85, 136,97, 147,42, 164,18;
точка плавления: 176,3-179,1°С, точка плавления его гидрохлорида: 206,6-207,7°С.
Соединение 3: 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоат
Все условия реакции были, как описано выше, за исключением того, что 4-метилбензоилхлорид заменяли 4-метоксибензоилхлоридом.
1Н-ЯМР (ДМСО) δ 1,14-1,59 (10Н, м, -(СН2)5-), 2,11 (6Н, с, -N(CH3)2), 2,55 (1Н, м, -СН<), 2,86 (2Н, м, -СН2-N-), 3,86 (3Н, с, -ОСН3), 5,02 (1Н, ушир., -ОН), 7,10, 7,26, 8,06 (8Н, т, д, д, Ar-H);
13С-ЯМР (ДМСО) 21,65 (2С), 24,79, 39,89, 40,81 (2С), 45,89 (2С), 55,25, 57,94, 76,57, 113,14 (2С), 120,19 (2С), 122,52, 123,01 (2С), 132,28 (2С), 137,01, 147,42, 162,50, 164,18;
точка плавления: 133,4-135,7°С, точка плавления его гидрохлорида: 195,7-196,9°С.
Соединение 4: 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-фторбензоат
Все условия реакции были такими, как описано выше, за исключением того, что 4-метилбензоилхлорид заменяли 4-фторбензоилхлоридом.
1Н-ЯМР (ДМСО) δ 1,25-1,59 (10Н, м, -(СН2)5-), 2,16 (6Н, с, -N(CH3)2), 2,55 (1H, м, -СН<), 2,86 (2Н, м, -СН2-N-), 5,02 (1Н, ушир., -ОН), 7,00, 7,16, 7,26, 8,12 (8Н, т, д, д, Ar-H);
13С-ЯМР (ДМСО) 21,65 (2С), 24,79, 39,90, 40,81 (2С), 45,90 (2С), 57,94, 76,57, 114,41, 115,12, 120,19 (2С), 123,02 (2С), 130,91, 131,08, 137,02, 147,42, 158,38, 164,19, 164,88;
точка плавления: 146,2-148,5°С, точка плавления его гидрохлорида: 199,2-201,3°С.
Пример 2. Синтез диэфира карбоновой кислоты [формулы (VII)] соединения (III)
Общая схема реакции:
где R представляет собой фенил, толил, метоксифенил или другой арил или алкил и т.д.
Метод синтеза был идентичен методу примера 1 за исключением того, что добавляли двойное или большее количество органического ацилхлорида и триэтиламина.
4-[2-Диметиламин-1-(1-бензоилоксициклогексил)этил]фенилбензоат получали в качестве примера.
В реакционную колбу добавляли 17,4 г дезметил-венлафаксина (соединение III), 18,58 г бензоилхлорида и 200 мл безводного тетрагидрофурана и охлаждали до 0°С. Добавляли по каплям 50 мл безводного раствора триэтиламина в тетрагидрофуране. После того как все исходные вещества растворились, реакционный раствор выливали в 400 мл воды и перемешивали. Затем осажденное твердое вещество отфильтровывали, промывали водой три раза и сушили с получением неочищенного продукта. Затем неочищенный продукт растворяли в 10-кратном количестве безводного этанола и перекристаллизовывали с получением 19,3 г белого твердого вещества, имеющего точку плавления 127,8-129,7°С и выход 60,9%.
Получение гидрохлорида: 5,0 г вышеуказанного продукта растворяли в 20 мл безводного простого эфира, затем добавляли по каплям безводный насыщенный раствор хлористого водорода в простом эфире. Выпавшее в осадок твердое вещество отфильтровывали с получением 5,0 г белого кристаллического твердого вещества, имеющего точку плавления 176,1-179,0°С.
Согласно этому способу синтезировали следующие соединения.
Соединение 2.1: 4-[2-диметиламино-1-(1-бензоилоксициклогексил)этил]фенилбензоат
1Н-ЯМР (ДМСО) δ 1,07-1,58 (10Н, м, -(СН2)5-), 2,01 (6Н, с, -N(CH3)2), 2,33, 4,06 (2Н, дд, -CH2-N-), 3,00 (1Н, т, -СН<), 7,16-8,13 (14Н, м, Ar-H),
13С-ЯМР (ДМСО) 21,56 (2С), 24,64, 37,70 (2С), 37,94, 45,89 (2С), 57,85, 81,50, 120,35 (2С), 123,37 (2С), 125,90, 128,67 (2С), 128,80 (2С), 129,42, 129,47 (2С), 132,86, 132,99 (2С), 133,85, 136,41, 148,19, 164,18, 166,21;
точка плавления: 127,8-129,7°С, точка плавления его гидрохлорида: 176,1-179,0°С.
Соединение 2.2: 4-[2-диметиламино-1-(1-(4-метил)бензоилоксициклогексил)этил]фенил-4-метилбензоат
Условия реакции были такими, как описано выше, за исключением того, что бензоилхлорид заменяли 4-метилбензоилхлоридом.
1Н-ЯМР (ДМСО) δ 1,10-1,59 (10Н, м, -(СН2)5-), 2,11 (6Н, с, -N(CH3)2), 2,45 (6Н, с, Ar-CH3), 2,55 (1Н, м, -СН<), 2,86 (2Н, м, -СН2-N-), 7,11-8,00 (12Н, д, д, д, д, Ar-H);
13С-ЯМР (ДМСО) 21,40 (2С), 21,56 (2С), 24,64, 37,70 (2С), 37,94, 45,89(2С), 57,85, 81,50, 120,35 (2С), 123,42 (2С), 125,31, 126,43, 127,59 (2С), 127,95 (2С), 128,10 (2С), 128,13 (2С), 136,41, 141,90 (2С), 148,19, 164,19, 166,21;
точка плавления: 122,8-125,1°С.
Соединение 2.3: 4-[2-диметиламино-1-(1-(4-метокси)бензоилоксициклогексил)этил]фенил-4-метоксибензоат
Условия реакции были такими, как указано выше, за исключением того, что бензоилхлорид заменяли 4-метоксибензоилхлоридом.
1Н-ЯМР (ДМСО) δ 1,14-1,59 (10Н, м, -(СН2)5-), 2,11 (6Н, с, -N(CH3)2), 2,55 (1Н, м, -СН<), 2,86 (2Н, м, -СН2-N-), 3,86 (6Н, с, -ОСН3), 5,02 (1Н, ушир., -ОН), 7,10-8,06 (12Н, т, д, д, Ar-H);
13C-ЯМР (ДМСО) 21,56 (2С), 24,64, 37,70 (2С), 37,94, 45,89 (2С), 55,25 (2С), 57,85, 81,50, 113,11 (2С), 113,14 (2С), 120,35 (2С), 121,03, 122,52, 123,37 (2С), 131,21 (2С), 132,28 (2С), 136,41, 148,19, 162,50 (2С), 164,16, 166,21;
точка плавления: 112,6-114,9°С.
Пример 3: Синтез асимметрического диэфира карбоновой кислоты [формулы (VIII)] соединения (III)
Сложный асимметрический диэфир получали ацилированием соответствующего сложного моноэфира, и его синтез был идентичен синтезу примера 1.
Общая схема реакции:
где R, R1 представляют собой фенил, толил, метоксифенил или другой арил или алкил и т.д.
4-[2-Диметиламино-1-(1-бензоилоксициклогексил)этил]фенил-4-метилбензоат получали в качестве примера.
10 ммоль сложного моноэфира (соединение 1 примера 1), синтезированного согласно примеру 1, и 10-15 ммоль бензоилхлорида добавляли в 200 мл безводного пиридина и охлаждали до 0°С при перемешивании, затем добавляли по каплям (приблизительно 10 мин) раствор безводного тетрагидрофурана, содержащий 1,05 г (9,9 ммоль) триэтиламина, и реакцию проводили непрерывно при комнатной температуре при перемешивании в течение 18 часов. Реакционный раствор промывали 50 мл воды и разделяли, затем органическую фазу сушили над безводным сульфатом натрия и затем растворитель удаляли выпариванием в вакууме, остаток выливали в 400 мл воды, устанавливали при перемешивании рН 9 и сохраняли в течение ночи. Осажденное твердое вещество отфильтровывали, промывали водой три раза и сушили с получением неочищенного продукта. Неочищенный продукт перекристаллизовывали из безводного этанола с получением белого твердого вещества.
Следующие соединения синтезировали согласно этому способу.
Соединение 3.1: 4-[2-диметиламино-1-(1-бензоилоксициклогексил)этил]фенил-4-метилбензоат
1Н-ЯМР (ДМСО) δ 1,10-1,59 (10Н, м, -(СН2)5-), 2,17 (6Н, с, -N(CH3)2), 2,42 (3Н, с, Ar-CH3), 2,55 (1Н, м, -СН<), 2,86 (2Н, м, -СН2-N-), 7,11-8,20 (13Н, д, д, д, д, Ar-H);
13С-ЯМР (ДМСО) 21,40, 21,56 (2С), 24,64, 37,70 (2С), 37,94, 45,89 (2С), 57,86, 81,52, 120,36 (2С), 123,38 (2С), 126,43, 127,95 (2С), 128,13 (2С), 128,67 (2С), 129,42, 129,47 (2С), 132,86, 136,41, 141,90, 149,19, 164,19, 166,22;
точка плавления: 127,8-130,2°С.
Соединение 3.2: 4-[2-диметиламино-1-(1-бензоилоксициклогексил)этил]фенил-4-метоксибензоат
Условия реакции были такими, как описано выше, за исключением того, что соединение 1 примера 1 заменяли соединением 3 примера 1.
1Н-ЯМР (ДМСО) δ 1,22-1,76 (10Н, м, -(СН2)5-), 2,15 (6Н, с, -N(CH3)2), 2,58 (1Н, м, -СН<), 2,76 (2Н, м, -СН2-N-), 3,86 (3Н, с, -ОСН3), 7,16-8,10 (9Н, т, д, д, Ar-H);
13С-ЯМР (ДМСО) 21,56 (2С), 24,64, 37,70 (2С), 37,94, 45,89 (2С), 55,25, 57,85, 81,50, 113,12 (2С), 120,35 (2С), 121,03, 123,37 (2С), 125,92, 128,81 (2С), 131,22 (2С), 132,99 (2С), 133,85, 136,41, 148,19, 162,50, 164,18, 166,26;
точка плавления: 119,6-122,8°С.
Пример 4. Синтез сложного карбамоилфенилового моноэфира [формулы (IX)] простого бензилового эфира соединения (III)
Общая схема реакции:
или
где R1, R2 или R' представляют собой Н, метил, этил, пропил, изопропил, фенил, толил или другой алкил или арил и т.д.
Соединение 4.1: 4-[2-диметиламино-1-(1-бензилоксициклогексил)этил]фенил-N-метилкарбамат
6 ммоль метилизоцианата добавляли при перемешивании в 20 мл раствора дихлорметана, содержащего 5 ммоль простого бензилового эфира соединения (III), реакцию проводили при комнатной температуре в течение 16 часов, затем реакционный раствор промывали 10 мл 5% водного раствора бикарбоната натрия, сушили над безводным сульфатом натрия и растворитель удаляли выпариваем с получением маслянистого или белого твердого продукта.
1Н-ЯМР (ДМСО) δ 1,33-1,69 (10Н, м, -(СН2)5-), 2,17 (6Н, с, -N(CH3)2), 2,65 (1Н, м, -СН<), 2,76 (2Н, м, -СН2-N-), 2,78 (3Н-NCH3), 5,37 (NH), 6,90-7,59 (9Н, Ar-H);
13C-ЯМР (ДМСО) 22,43 (2С), 25,22, 27,35, 35,14, 39,29 (2С), 45,89 (2С), 56,72, 81,67, 120,30 (2С), 122,81 (2С), 122,89, 124,36 (2С), 128,81 (2С), 135,34, 147,41, 156,11, 160,37;
точка плавления: 138,6-140,8°С.
Соединение 2: 4-[2-диметиламино-1-(1-бензилоксициклогексил)этил]фенил-N,N-диметилкарбамат
6 ммоль N-диметилформилхлорида добавляли при 0°С при перемешивании в раствор 30 мл дихлорметана, содержащий 5 ммоль производного простого бензилового эфира соединения (III) и 1 мл триэтиламина, реакцию проводили непрерывно при 0°С в течение 6 часов, затем реакционную жидкость промывали 10 мл 5% водного раствора бикарбоната натрия, сушили над безводным сульфатом натрия и растворитель удаляли выпариванием с получением маслянистого или белого натриевого продукта.
1Н-ЯМР (ДМСО) δ 1,33-1,69 (10Н, м, -(СН2)5-), 2,17 (6Н, с, -N(CH3)2), 2,65 (1Н, м, -СН<), 2,76 (2Н, м, -СН2-N-), 2,89 (6НN(CH3)2), 6,90-7,59 (9H, Ar-H);
13С-ЯМР (ДМСО) 20,43 (2С), 25,15, 35,14, 36,42, 36,65, 39,29 (2С), 45,89 (2С), 56,72, 81,67, 122,70 (2С), 122,80 (2С), 122,90, 124,71 (2С), 128,81 (2С), 135,45, 148,50, 155,12, 156,11;
точка плавления: 126,2-129,3°С.
Пример 5. Исследование метаболизма соединения в клетках печени с образованием активного компонента 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединения III)
40 мкг соединения 1 (или соединения 2, или 3, или 4) примера 1 растворяли в 0,01 М буферном растворе фосфата калия, содержащем 1 мМ NADPH, смешанном с 25 мкл клеток S9 печени человека (20 мг белка/мл, Н961), и культивировали при 37°С в течение 2 часов. Затем реакционную смесь гасили концентрированной перхлорной кислотой. После того как осажденные белки удаляли центрифугированием, в супернатанте устанавливали рН 3 концентрированным фосфатом калия и снова центрифугировали. Супернатант непосредственно вводили в ВЭЖХ и анализировали.
Результаты метаболизма представлены в таблице 1. Скорости метаболизма из соединений в активный компонент 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанол (соединение III) в клетках печени в интервале 2 часа изменялись от 80% до 100% соответственно в зависимости от различных сложноэфирных групп.
| Таблица 1 | ||||
| Скорость метаболизма соединений в клетках печени в интервале 2 часа | ||||
| X/Y | Соединение 1 примера 1 | Соединение 2 примера 1 | Соединение 3 примера 1 | Соединение 4 примера 1 |
| Скорость метаболизма (%) | 99 | 96 | 92 | 88 |
Пример 6. Исследование метаболизма 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата (соединения 1 примера 1) при пероральном и внутривенном введении в организм крыс
Шесть крыс разделили на две группы и подвергали внутрижелудочному или внутривенному введению гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата в дозе 13,5 мг/кг. Образцы крови испытывали согласно заранее заданным схемам и измеряли в крови концентрации пролекарства 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата и активного метаболита 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III).
Результаты внутривенного введения в организм крыс (см. фиг.1А) показали, что пролекарство гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата быстро подвергается метаболизму в крови крыс, и активный метаболит 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанол (соединение III) (ODV) достигал Смакс через 30 минут, и в среднем концентрация пролекарства в крови была только 10-15% его активного метаболита 4-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) (ODV) и непрерывно снижалась.
Результаты перорального введения представлены на фиг.1В. После введения пролекарства в организм через желудочно-кишечный тракт оно немедленно продвергалось метаболизму с образованием с высокой скоростью и степенью активного метаболита 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) (ODV) и снижением концентрации пролекарства. Пролекарство при пероральном введении по существу полностью превращалось в требуемый активный метаболит 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанол (соединение III), что удовлетворительно подтвердило метаболизируемость пролекарства 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата. По расчету биодоступность пролекарства гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата при пероральном введении в организм крыс была выше 80%, что было несомненно выше, чем биодоступности 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) (ODV) и его различных солей, непосредственно введенных перорально.
Пример 7. Экспериментальные результаты перорального введения в организм гончих собак сукцината 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) и его пролекарств: гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата (соединение 2 примера 1), гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата (соединение 1 примера 1) и сукцината 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоата (соединение 3 примера 1)
Девять гончих собак с массой тела приблизительно 10 кг разделили на три группы и подвергали внутрижелудочному введению сукцината О-дезметил-венлафаксина (ODV), гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата, гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата и сукцината 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоата в дозе 0,016 ммоль/кг. Анализировали образцы крови согласно заранее заданным схемам и измеряли концентрации в крови активного метаболита 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) и его пролекарств.
Результаты представлены на фиг.2. После введения пролекарств в организмы гончих собак через желудочно-кишечный тракт они немедленно подвергались метаболизму в активный метаболит дезметил-венлафаксин, и концентрации пролекарства были ниже, чем предел измерения, поэтому полагают, что почти все пролекарства при пероральном введении превращались в требуемый активный метаболит 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанол (соединение III). В среднем результаты показывают, что биодоступности пролекарств ODV очевидно были выше, чем биодоступность сукцината ODV, который имеет самую высокую биодоступность среди солей ODV, и AUC увеличивалось более чем на 30% (таблица 2), где AUC гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата увеличивалось более чем на 60% (таблица 2), биодоступность значительно улучшалась, и это продемонстрировало очевидное преимущество над сукцинатом 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III).
| Таблица 2 | ||||
| Сравнение по результатам испытаний в организме гончих собак между пролекарствами и сукцинатом 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) по концентрации активного метаболита 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола (соединение III) | ||||
| Соединение | Смакс, нг/мл | tмакс, ч | AUC, нг/мл ч | AUC увеличение скорости, % (сукцинат ODV =100%) |
| Сукцинат ODV | 100 | 0,5 | 261 | 100 |
| Гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата | 93 | 1,0 | 342 | 132 |
| Гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата | 117 | 1,0 | 421 | 161 |
| Сукцинат 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоата | 97 | 1,0 | 386 | 148 |
Пример 8. Изготовление стандартных пероральных таблеток
Композиция:
| Гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата, или сукцинат 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоата, или гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата | 23% |
| Микрокристаллическая целлюлоза | 58% |
| Гидроксипропилметилцеллюлоза | 5% |
| Дигидрат гидрофосфата кальция | 12% |
| Стеарат магния | 0,8% |
| Безводный коллоидный диоксид кремния | 1,2% |
Эти компоненты непосредственно таблетировали с получением таблеток, содержащих лекарственное средство, 100 мг на таблетку (рассчитано на основе 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола). Результаты испытания растворения этого вида таблеток представлены ниже по тексту.
| Таблица 3 | ||||
| Растворение стандартных пероральных таблеток | ||||
| Время растворения (ч) | 2 | 4 | 8 | |
| Процент растворения (%) | 4-Метилбензоат | 43,1 | 68,2 | 88,5 |
| 4-Метоксибензоат | 53,6 | 78,2 | 92,8 | |
| Бензоат | 45,8 | 76,3 | 93,6 |
Пример 9. Изготовление капсул с замедленным высвобождением гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата для перорального введения
А. Образование гранул:
| Гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]-фенил-4-метилбензоата | 40% |
| Микрокристаллическая целлюлоза | 59% |
| Гидроксипропилметилцеллюлоза | 1% |
Гранулирование осуществляли стандартным ожижением слоя.
В. Покрытие:
| Этилцеллюлоза | 85% |
| Гидроксипропилметилцеллюлоза | 15% |
После того как покрытие высушили, покрытые гранулы нагружали в твердые желатиновые капсулы, в капсуле находилось 100 мг лекарственного средства (рассчитанного на основе 1-[2-диметиламино-1-(4-гидроксифенил)этил]циклогексанола), и степень покрытия была 6%. Испытание на растворение капсул проводили согласно методу Pharmacopoeia of People's Republic of China, и результаты были такими, как следует ниже по тексту.
| Таблица 4 | |||||
| Испытание на растворение капсул с замедленным высвобождением гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата для перорального введения | |||||
| Время растворения (ч) | 2 | 4 | 8 | 12 | 24 |
| Растворенное лекарственное средство (%) | 5,7 | 27,8 | 61,1 | 79,9 | 96,2 |
Пример 10. Изготовление капсул с замедленным высвобождением гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата для перорального введения
Способ изготовления был идентичен способу примера 9 за исключением того, что гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоата заменяли гидрохлоридом 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата. Испытание на растворение капсул проводили согласно методу Pharmacopoeia of People's Republic of China, и результаты были такими, как следует ниже по тексту.
| Таблица 5 | |||||
| Испытание на растворение капсул с замедленным высвобождением гидрохлорида 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенилбензоата для перорального введения | |||||
| Время растворения (ч) | 2 | 4 | 8 | 12 | 24 |
| Растворенное лекарственное средство (%) | 3,8 | 19,8 | 41,2 | 63,8 | 88,2 |
Пример 11. Изготовление капсул с замедленным высвобождением сукцината 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метоксибензоата для перорального введения
Способ изготовления был идентичен способу примера 9 за исключением того, что гидрохлорид 4-[2-диметиламино-1-(1-гидроксициклогексил)этил]фенил-4-метилбензоа