Фотобиокатализатор для получения восстановленных форм никотинамидных коферментов nadh или nadph и фотокаталитический способ получения nadh или nadph
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Предложен фотобиокатализатор для получения восстановленных форм никотинамидных коферментов NADH или NADPH. Фотобиокатализатор представляет собой ферредоксин-NADP-редуктазу, иммобилизованную на поверхности наноструктурированной мезопористой пленки диоксида титана TiO2 в количестве 0,8-1,24 нмоль на 1 см2 поверхности пленки. Пленка приготовлена из нанокристаллов диоксида титана размером 15-25 нм с удельной поверхностью 50-100 м2/г на стеклянной подложке или на стеклянной подложке с токопроводящим покрытием. Предложен также фотокаталитический способ получения восстановленных форм никотинамидных коферментов NADH или NADPH с использованием фотобиокатализатора на основе ферредоксин-NADP-редуктазы, иммобилизованной на поверхности пленки диоксида титана TiO2. Фотобиокатализатор позволяет с высокой скоростью и специфично получать NADH или NADPH из NAD+ или NADP+ под действием света. Способ получения восстановленных форм никотинамидных коферментов NADH или NADPH с использованием полученного фотобиокатализатора обеспечивает легкое отделение продуктов реакции от фермента и полупроводника и многократное использование фотобиокатализатора. 2 н. и 2 з.п. ф-лы, 5 ил.
Реферат
Изобретение относится к биотехнологии, а именно к фотобиокатализатору на основе фермента ферредоксин-NADP-редуктазы, иммобилизованного на наноструктурированной мезопористой пленке диоксида титана (TiO2) - фотоактивного полупроводника, и может быть использовано в энзиматических процессах получения восстановленных форм никотинамидных коферментов NADH и NADPH под действием света.
Восстановленные формы никотинамидных коферментов NADH (восстановленный никотинамидадениндинуклеотид) и NADPH (восстановленный никотинамидадениндинуклеотидфосфат) широко применяются в ферментативных и биокаталитических процессах для получения оптически активных соединений (аминокислот, их производных, алифатических и ароматических аминоспиртов и аминов) и лекарств, в биомедицинской диагностике.
Однако применение NADH или NADPH невыгодно с экономической точки зрения в связи с высокой стоимостью восстановленных коферментов - цена восстановленных форм никотинамидных коферментов в десятки раз превосходит стоимость окисленных форм, выделяемых из микроорганизмов.
Для восстановления окисленных форм никотинамидных коферментов NAD+ и NADP+ используют биокатализаторы на основе ферментов (Mihaela D. Leonida. "Redox Enzymes Used in Chiral Syntheses Coupled to Coenzyme Regeneration". Current Medicinal Chemistry, 2001, 8, pp.345-369; Тишков В.И. «Регенерация кофакторов в биосинтезе хиральных соединений с помощью дегидрогеназ». Вестник Московского Университета, СЕР.2, Химия, 2002. Т.43, №6, с.381-388). Наиболее широкое применение в практике нашли биокатализаторы на основе NAD+-зависимой формиатдегидрогеназы (Тишков В.И., Попов В.О. «Механизм действия формиатдегидрогеназы и ее практическое применение». Биохимия, 2004, Т.69, №11, с.1537-1554). Применение ферментов для восстановления NAD+ и NADP+ требует использования специфических (пригодных только для используемого фермента) органических соединений в качестве доноров электрона, которые имеют высокую стоимость. Кроме того, процессы регенерации NADH или NADPH ограничены активностью ферментов.
В настоящее время исследуются электрохимические (Nakamura K. et al. "Electro-enzymology Coenzyme Regeneration". Springer-Verlag, Berlin, 1988, 165 p.; A.A.Karyakin et al. "Electroreduction of NAD+ to enzymatically active NADH at poly (Neutral Red) modified electrodes". J. Electroanal. Chem., 399 (1-2) (1995) pp.179-184; Damian and S. Omanovic. "Electrochemical Reduction of NAD+ on a Polycrystalline Gold Electrode". J. Molec. Catal. A: Chemical, 253 (2006) p.222) и фотохимические методы восстановления NAD+ и NADP+ до NADH и NADPH (Rainer Wienkamp and Eberhard Steckhan. "Selective Generation of NADH by Visible Light". Angew. Chem. Inf. Ed. Engl. 22 (1983), No. 6,497; Shumilin LA., Nikandrov V.V. et al. "Photogeneration of NADH under coupled action of CdS semiconductor and hydrogenase from Alcaligenes eutrophus without exogenous mediators". FEBS Letters (1992), 306 [2-3], pp.125-128; Chan Beum Park et al. "Solar energy in production of L-glutamate through visible light active photocatalyst-redox enzyme coupled bioreactor". Chem. Commun. 2008, pp.5423-5425; Lee SH et al. "Eosin Y-sensitized artificial photosynthesis by highly efficient visible-light-driven regeneration of nicotinamide cofactor". Chembiochem. 2009, Jul 6, 10(10), pp.1621-1624). Описаны электрохимические и фотохимические методы восстановления NAD+ и NADP+ до NADH и NADPH как с применением ферментов, так и без их использования. Недостатком этих методов является низкая специфичность процесса восстановления NAD+ и NADP+, который сопровождается образованием димера (NAD)2 и других побочных продуктов. Использование ферментов при восстановлении NAD+ и NADP+ позволяет снизить выход побочных продуктов реакции, но требует введения дополнительных дорогостоящих переносчиков электрона от электрода, а наблюдаемые при этом скорости образования NADH и NADPH ниже, чем в чисто ферментативном процессе. Кроме того, в описанных методах ферменты или переносчики электронов находятся в растворе, что ограничивает использование этих методов в биотехнологии, так как в свободном виде ферменты нестабильны и увеличивается расход соединений-переносчиков электрона.
Повышение стабильности и технологичности применения ферментов достигается иммобилизацией ферментов на различных носителях.
Известно большое количество иммобилизованных биокатализаторов как на органических носителях (RU 2327738, C12N 11/00, C12N 11/04, C12N 11/12, C12N 11/14, 27.06.2008; RU 2233327, C12N 11/04, C12N 11/18, 27.07.2004; RU 2261911, C12N 11/02, 10.10.2005; RU 2210596, C12P 35/00, 20.08.2003), так и на неорганических (RU 2281328, C12N 11/14, C12N9/26, 10.08.2006; RU 2279475, C12N 11/14, C12N 9/26, 10.07.2006; RU 2224020, C12N 11/14, C12N 9/26, 20.02.2004; RU 2167197, C12N 11/14, 20.05.2001; RU 2007456, C12N 11/14, 15.02.1994; RU 1473358, C12N 11/00, C12N 11/14, 20.02.2000). Такие иммобилизованные биокатализаторы решают проблему повышения стабильности и технологичности применения ферментов, но они не позволяют осуществлять фотохимические процессы.
Известно, что неорганические полупроводники, например TiO2, являются катализаторами окислительно-восстановительных фотохимических реакций (RU 2275238, B01J 21/06, C01G 23/053, 27.04.2006; RU 2151632, B01D 53/86, B01J 21/06, 27.06.2000; RU 2259866, B01D 53/86, B01J 21/06, 10.09.2005; US 6939611, B32B 9/00, B01J 23/00, 06.09.2005; US 6387844, B01J 23/00, B01J 21/08, 14.05.2002).
Исследование сопряженного действия неорганических полупроводников и ферментов в окислительно-восстановительных реакциях в биохимических системах привело к развитию нового направления в катализе - фотобиокатализа (В.В.Никандров. "Неорганические полупроводники в биологических и биохимических системах: биосинтез, свойства и фотохимическая активность". Успехи биологической химии, 2000, т.40, с.357-396). Установлено, что при сопряжении полупроводника и фермента полупроводник фотосенсибилизирует окисление донора электрона, а фермент восстанавливает субстрат ферментативной реакции, используя электроны, фотогенерированные в зоне проводимости полупроводника. Фермент выступает в роли катализатора окислительно-восстановительной реакции, фотосенсибилизированной полупроводником. Сопряжение полупроводника и фермента позволяет получить продукт ферментативной реакции при использовании в качестве доноров электронов доступных и дешевых органических соединений, которые фермент в отсутствие полупроводника использовать не способен.
В настоящее время в связи с развитием нанобиотехнологии основное внимание исследователей обращено к наноструктурированным полупроводниковым носителям для иммобилизации ферментов. Наноструктурированные полупроводниковые пленки TiO2 использовались для иммобилизации ферментов (RU 2326818, C01G 23/047, C12N 11/14, B01J 37/36, 20.06.2008) и разработки биосенсоров (Qingwen Li et al. "Amperometric Detection of Glucose with Glucose Oxidase Absorbed on Porous Nanocrystalline TiO2 Film". Electroanalysis, (2001) V.13, Iss. 5, pp.413-416; M. Viticoli et al. "Third-generation biosensors based on TiO2 nanostructured films". Materials Science and Engineering (2006), 26, Iss. 5-7, pp.947-951). В данных работах фотокаталитические свойства полученных пленок ТiO2 с иммобилизованными ферментами не исследовались.
Наиболее близким к предлагаемому фотобиокатализатору является фотобиокатализатор для образования водорода, включающий фермент, иммобилизованный на наноструктурированной мезопористой пленке ТiO2 (RU 2322498, C12N 9/00, C12N 11/00, 20.04.2008 - прототип). Фотобиокатализатор-прототип содержит гидрогеназу в количестве 0,1-2,3 нмоль на 1 см2 поверхности наноструктурированной мезопористой пленки TiO2, полученной из нанокристаллов TiO2 размером от 15 до 25 нм с удельной поверхностью 50-100 м2/г на стеклянной подложке или на стеклянной подложке с токопроводящим покрытием.
Фотобиокатализатор-прототип на основе гидрогеназы позволяет с достаточно высокой скоростью получать водород под действием света, но не пригоден для восстановления окисленных форм никотинамидных коферментов.
Наиболее близким к предлагаемому фотокаталитическому способу получения восстановленных форм никотинамидных коферментов NADH или NADPH является способ, описанный в работе Z.Goren, N.Lapidot and I.Willner Photocatalysed regeneration of NAD(P)H by CdS and TiO2 semiconductors: applications in enzymatic synthesis. J. Mol. Cat. 47, 1988, pp.21-32 (прототип). В способе-прототипе реакция фотовосстановления NAD+ или NADP+ до NADH или NADPH осуществляется при сопряженном действии полупроводника TiO2 и фермента липоамид-дегидрогеназы или ферредоксин-NADP-редуктазы в присутствии органического донора электрона с помощью переносчика электронов - метилвиологена. Реакция проводится в коллоидном растворе полупроводника, содержащем фермент, донор электрона и метилвиологен. При освещении коллоидного раствора TiO2 полупроводник фотосенсибилизирует окисление донора электрона и происходит восстановление метилвиологена за счет электронов, фотогенерированных в зоне проводимости полупроводника. Восстановленный метилвиологен используется в последующих реакциях восстановления NAD+ или NADP+ катализируемых ферментом липоамид-дегидрогеназой или ферредоксин-NADP-редуктазой. Контрольными экспериментами было показано, что NAD(P)H не образуется в темноте, а также при освещении, но в отсутствие метилвиологена, то есть в способе-прототипе реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH осуществляют путем предварительного переноса электрона от полупроводника к переносчику электронов - метилвиологену, восстановленная форма которого используется затем ферментом.
Необходимость использования в известном способе дорогостоящего и токсичного переносчика электронов метилвиологена существенно снижает практическую ценность этого способа. Кроме того, в данном способе фермент находится в растворе, что ограничивает использование способа в биотехнологии, так как, во-первых, в свободном виде ферменты нестабильны, во-вторых, требуется трудоемкая процедура отделения продуктов реакции от фермента и полупроводника и, в-третьих, практически невозможно повторное использование фермента.
Задачей изобретения является создание фотобиокатализатора на основе ферредоксин-NADP-редуктазы, иммобилизованной на наноструктурированной мезопористой пленке TiO2, способного с достаточно высокой скоростью специфично восстанавливать окисленные формы никотинамидных коферментов NAD+ или NADP+ до NADH или NADPH под действием света.
Задачей изобретения является также разработка более эффективного и технологичного фотокаталитического способа получения NADH и NADPH, который позволит исключить применение дорогостоящих соединений в качестве переносчика электронов, обеспечит повышение устойчивости фермента ферредоксин-NADP-редуктазы при осуществлении процесса, позволит легко отделять продукты реакции от фермента и полупроводника и обеспечит возможность многократного использования фотобиокатализатора.
Решение поставленной задачи достигается предлагаемым фотобиокатализатором для получения восстановленных форм никотинамидных коферментов NADH или NADPH, включающим фермент, иммобилизованный на наноструктурированной мезопористой пленке диоксида титана, приготовленной из нанокристаллов диоксида титана размером 15-25 нм с удельной поверхностью 50-100 м2/г на стеклянной подложке или на стеклянной подложке с токопроводящим покрытием, который в качестве иммобилизованного фермента содержит ферредоксин-NADP-редуктазу в количестве 0,8-1,24 нмоль на 1 см2 поверхности наноструктуриванной мезопористой пленки диоксида титана.
Решение поставленной задачи достигается также предлагаемым фотокаталитическим способом получения восстановленных форм никотинамидных коферментов NADH или NADPH реакцией фотовосстановления NAD+ или NADP+ при сопряженном действии полупроводника TiO2 и фермента ферредоксин-NADP-редуктазы при освещении УФ-светом в анаэробных условиях в присутствии органического донора электрона, в котором реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH осуществляют путем прямого переноса электрона от полупроводника TiO2 к ферменту ферредоксин-NADP-редуктазе, для чего используют ферредоксин-NADP-редуктазу, иммобилизованную на наноструктурированной мезопористой пленке ТiO2, приготовленной из нанокристаллов TiO2 размером 15-25 нм с удельной поверхностью 50-100 м2/г на стеклянной подложке или на стеклянной подложке с токопроводящим покрытием, в количестве 0,8-1,24 нмоль на 1 см2 поверхности пленки TiO2.
Реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH можно проводить при освещении УФ-светом с λ=365 нм.
В качестве органического донора электрона можно использовать трис(гидроксиметил)аминометан - компонент водного буферного раствора 0,05 М ТРИС, рН 7.2, в котором проводят реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH.
Главным отличием предлагаемого способа от известного является то, что реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH осуществляют путем прямого переноса электрона от полупроводниковой наноструктурированной пленки TiO2 к иммобилизованному на пленке ферменту ферредоксин-NADP-редуктазе, что позволяет исключить применение дорогостоящих соединений в качестве переносчика электронов.
Использование в заявленном способе фермента, иммобилизованного на наноструктурированной пленке TiO2, повышает устойчивость ферредоксин-NADP-редуктазы, обеспечивает эффективное сопряжение фермента с полупроводником, позволяет легко отделять NADH или NADPH от фотобиокатализатора и позволяет использовать фотобиокатализатор многократно.
Ферредоксин-NADP-редуктаза - фермент, катализирующий реакцию:
NADP++2е-+H+↔NADPH
Этот фермент способен также катализировать реакцию восстановления NAD+:
NAD++2е-+H+↔NADH
Природным донором электрона - субстратом - для ферредоксин-NADP-редуктазы является белок ферредоксин.
Ферредоксин-NADP-редуктаза из листьев шпината получена от фирмы Sigma (мол. вес 41 кДа, ε280нм=55600 М-1 см-1).
Ферредоксин-NADP-редуктазу иммобилизовывали на наноструктурированных мезопористых пленках TiO2, полученных из наночастиц TiO2 размером 15-25 нм с удельной поверхностью 50-100 м2/г. Получение пленок TiO2 описано в приведенных далее примерах. См. также патент RU 2326818, C01G 23/047, C12N 11/14, 20.06.2008. Иммобилизацию фермента осуществляли выдерживанием мезопористой пленки TiO2 площадью 1-4 см2, толщиной 8-10 мкм в 3 мл водного буферного раствора (ТРИС, 0,05 М, рН 7,2), содержащего 0,5-1,5·10-5 М ферредоксин-NADP-редуктазы, при температуре 4°С в течение 2 суток. Получен фотобиокатализатор, содержащий 0,8-1,24 нмоль (0,033-0,051 мг) ферредоксин-NADP-редуктазы на 1 см2 поверхности пленки диоксида титана.
Активность ферредоксин-NADP-редуктазы, иммобилизованной на мезопористой пленке TiO2, в темновой реакции определяли спектрофотометрически по скорости окисления NADPH в присутствии метилвиологена (MV2+) в аэробных условиях.
Ферредоксин-NADP-редуктаза катализирует перенос электрона от NADPH к MV2+; восстановленный метилвиологен (MV+) окисляется кислородом:
4MV++4H++О2→4MV2++2H2O
В спектрофотометрическую кювету добавляли 2,54 мл буфера (ТРИС, 0,05 М, рН 7,20), 0,3 мл 10-3М NADPH, 150 мкл 0,01М MV2+ и образец полученного фотобиокатализатора. Изменение концентрации NADPH определяли спектрофотометрически при 340 нм, используя ε340нм=6220 М-1см-1.
Темновая каталитическая активность иммобилизованной ферредоксин-NADP-редуктазы в реакции окисления NADPH составила 2,58±0,25 мкмоль NADPH / мг фермента · час.
Фотообразование NADH или NADPH из NAD+ или NADP+ в присутствии предлагаемого фотобиокатализатора исследовали, используя в качестве донора электрона широко применяемый в биохимических и биомедицинских опытах компонент буферного раствора ТРИС - трис(гидрокси-метил)аминометан - органическое соединение, которое не способно выступать в качестве субстрата для ферментов, в том числе и для ферредоксин-NADP-редуктазы, и не способно восстанавливать NAD+ или NADP+ в отсутствие фермента. В качестве доноров электрона возможно также использование спиртов, органических кислот и других соединений, которые окисляются диоксидом титана при световом возбуждении.
Фотокаталитическую реакцию проводили в спектрофотометрической кювете, содержащей 1·10-4 М NAD+ или NADP+ и наноструктурированную мезопористую пленку TiO2 с иммобилизованной ферредоксин-NADP-редуктазой в водном буферном растворе: 0,05М ТРИС, рН 7,2. Перед экспериментами кюветы с образцами продували аргоном для удаления кислорода. Фотокаталитические процессы реализовывали при комнатной температуре при перемешивании раствора.
Источником света служила ртутная лампа ДРШ 250 мощностью 250 Вт. Освещение проводили через конденсор и водный тепловой фильтр. При помощи граничных светофильтров из спектра излучения ртутной лампы выделяли линии 365 нм. Интенсивность света 4·105 эрг/см2·с. Добавление растворов и газов в кювету и отбор проб осуществляли шприцем.
Идентификацию образования NADH и NADPH проводили по спектрам поглощения с помощью спектрофотометров «Beckman Coulter» DU-650 (Германия) и СФ-2000-2, по спектрам люминесценции на флуориметре «Shimadzu» RF-5301 PC, Япония и энзиматически по реакции окисления NADH и NADPH кислородом в присутствии метилвиологена и ферредоксин-NADP-редуктазы.
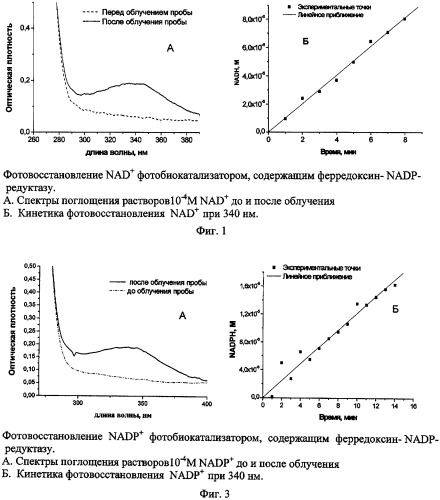
На фиг.1А приведен спектр поглощения, на фиг.2А - спектр флуоресценции растворов NAD+, подвергшихся облучению в присутствии предлагаемого фотобиокатализатора. Продукт фотореакции, также как контрольный раствор NADH, имеет спектр поглощения с максимумом при 340 нм и спектр флуоресценции с максимумом при 460 нм. Полное совпадение спектров поглощения и спектров флуоресценции растворов продукта фотореакции и контрольных растворов NADH, имеющих одинаковую оптическую плотность при 340 нм, указывает на то, что при фотокаталитическом восстановлении NAD+ не образуются иные продукты реакции помимо NADH. Известно, что димер (NAD)2, образующийся при электрохимическом восстановлении NAD+, имеет, как и NADH, максимум в спектре поглощения при 340 нм, но не обладает флуоресценцией с максимумом при 460 нм (Land Е.J. and Swallow A.J. Biochim. Biophys. Acta (1968) 162, pp.327-337).
На фиг.1Б представлена кинетическая кривая фотообразования NADH из NAD+. Фотокаталитическая активность фотобиокатализатора (скорость образования NADH из NAD+ мезопористой пленкой TiO2 площадью 1 см2, содержащей 1 мг фермента) составила 7,2±0,7 мкмоль NADH/см2·мг фермента · час.
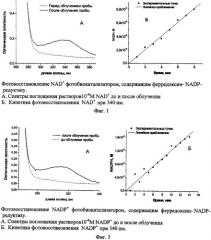
На фиг.3А приведен спектр поглощения, на фиг.4А - спектр флуоресценции растворов 1·10-4M NADP+, подвергшихся облучению в присутствии предлагаемого фотобиокатализатора. Продукт фотореакции, так же как и NADPH, имеет спектр поглощения с максимумом при 340 нм и спектр флуоресценции с максимумом при 460 нм. На фиг.4Б представлены результаты энзиматического окисления продукта фотореакции кислородом в присутствии метилвиологена и ферредоксин-NADP-редуктазы: 2 мл пробы раствора, облученного в фотокювете, насыщали воздухом и добавляли 0,15 мл 10-2 М метилвиологена и 0,0668 мг ферредоксин-NADP-редуктазы. Наблюдается падение оптической плотности пробы на длине волны 340 нм, что указывает на энзиматическое окисление продукта фотореакции - NADPH.
Типичная кинетическая кривая фотогенерации NADPH в фотокаталитическом процессе восстановления NADP+ представлена на фиг.3Б. Фотокаталитическая активность фотобиокатализатора (скорость образования NADPH на 1 см2 мезопористой пленки, содержащей 1 мг фермента) составила 8,3±0,8 мкмоль
NADPH/см2·мг белка · час.
Нами был проведен контрольный эксперимент фотохимического восстановления NAD+ наноструктурированной мезопористой пленкой TiO2, не содержащей фермента.
Облучение мезопористой пленки TiO2 без фермента в кювете, содержащей 1,36·10-3 М NAD+ в водном буферном растворе (0,05 М ТРИС, рН 7,2), не приводит к образованию NADH. Продукт фотореакции, так же как и NADH, имеет спектр поглощения с максимумом при 340 нм, однако он не флуоресцирует при 460 нм (см. фиг.2Б), что указывает на образование димера (NAD)2.. Кроме того, продукт данной фотореакции в отличие от NADH не окисляется кислородом воздуха в присутствии ферредоксин-NADP-редуктазы и метилвиологена.
Образование димера (NAD)2, как уже упоминалось выше, наблюдалось ранее при фотохимическом восстановлении NAD+ в отсутствие ферментов и при электрохимическом восстановлении. Образование (NAD)2 происходит в результате одноэлектронного восстановления с последующей димеризацией радикалов:
NAD++е-→NAD
2 NAD→(NAD)2
Последовательность реакций при фотокаталитическом образовании NADH или NADPH в присутствии фотобиокатализатора, содержащего ферредоксин-NADP-редуктазу, можно представить следующим образом:
| TiO2+hν→e-+h+ | фотогенерация электрона и дырки(1) |
| е-+Ti(IV)O-H→Ti(III)O-H- | захват поверхностной ловушкой (2) |
| h++Ti(IV)O-H→Ti(IV)O-H+ | захват поверхностной ловушкой (3) |
| 2e-+NAD(P)++H+→NAD(P)H | межфазный перенос заряда; реакция, катализируемая ферментами оксиредуктазами (4) |
| h++Ti(III)O-H-→Ti(IV)O-H | рекомбинация (5) |
| е-+Ti(IV)O-H+→Ti(IV)O-H | рекомбинация (6) |
| h++е-→тепло | рекомбинация (7) |
| h++RH→R+H+ | межфазный перенос заряда, окисление донора |
| электрона (8) | |
| Ti(IV)O-H++RH→Ti(IV)O-H+R+H+ | окисление донора электрона на поверхности (9) |
В качестве донора электрона использовали 0,05 М ТРИС - трис(гидроксиметил)аминометан.
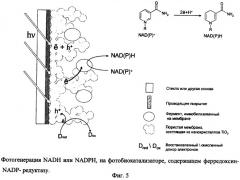
В целом процесс фотогенерации NADH или NADPH на предлагаемом фотобиокатализаторе, содержащем ферредоксин-NADP-редуктазу, можно представить схемой, приведенной на фиг.5. В результате связывания фермента с мезопористой поверхностью пленки TiO2 происходит формирование фотобиокатализатора, представляющего собой комплекс молекул фермента с несколькими нанокристаллами неорганического полупроводника. При световом возбуждении в наночастицах полупроводника происходит разделение зарядов с последующим восстановлением реакционного центра фермента фотогенерированными электронами. Фермент использует электроны для восстановления NAD+ или NADP+ до NADH или NADPH. Фотогенерированная в полупроводнике дырка мигрирует от наночастиц к поверхности наноструктурированной пленки, где происходит окисление донора электронов.
Приводим примеры осуществления изобретения.
А. Получение фотобиокатализатора для восстановления окисленных форм никотинамидных коферментов NAD+ или NADP+ до NADH или NADPH соответственно.
Пример 1.
Наноструктурированную мезопористую пленку TiO2 получали из промьппленного порошка нанокристаллов со средним размером 15 нм с удельной поверхностью 100 м2/г (ТКР 102, фирма Тауkа, Япония). 2 г порошка смешивали с 0,3 мл 0,1 М раствора азотной кислоты и подвергали дезагрегированию в ультразвуковом диспергаторе мощностью 300 Вт в течение 15 мин. Полученную однородную массу разбавляли 2 мл 0,1% раствора Тритон X100. Добавляли 0,2 г полиэтиленгликоля с молекулярной массой 20000 и гомогенизировали ультразвуком (600 Вт) в течение 15 минут. Полученную пасту равномерно наносили на подложку из обычного стекла с использованием прокладки для получения пленки заданной толщины (10 мкм) и высушивали при комнатной температуре. Затем органические вещества выжигались в течение 30 мин при 450°С в токе воздуха.
Иммобилизацию ферредоксин-NADP-редуктазы на полученной пленке (площадь 2 см2) осуществляли адсорбцией в среде водного буферного раствора (ТРИС, 0,05 М, рН 7,2), содержащего 1,5·10-5 М ферредоксин-NADP-редуктазы, при температуре 4°С в течение 2 суток. Полученный фотобиокатализатор промывали буферным раствором от остатков фермента, величина адсорбции ферредоксин-NADP-редуктазы составила 1,24 нмоль (0,051 мг) на 1 см2 поверхности пленки диоксида титана.
Пример 2.
Иммобилизацию ферредоксин-NADP-редуктазы осуществляли на пленке TiO2, полученной аналогично примеру 1 из порошка нанокристаллов со средним размером 25 нм с удельной поверхностью 50 м2/г (Aeroxide P25) с использованием 0,1 М азотной кислоты. Адсорбцию проводили на пленке площадью 3 см2 толщиной 8 мкм (подложка из стекла с токопроводящим покрытием) в среде водного буферного раствора (ТРИС, 0,05 М, рН 7,2), содержащего 0,5·10-5 М ферредоксин-NADP-редуктазы, при температуре 4°С в течение 2 суток. Полученный фотобиокатализатор промывали буферным раствором от остатков фермента, величина адсорбции ферредоксин-NADP-редуктазы составила 0,8 нмоль (0,033 мг) на 1 см2 поверхности пленки диоксида титана.
Б. Фотокаталитическая реакция восстановления окисленных форм никотинамидных коферментов.
Пример 3. Фотовосстановление NAD+ до NADH.
Для проведения фотокаталитической реакции использовали фотобиокатализатор, полученный по примеру 1 - удельная сорбция ферредоксин-NADP-редуктазы составила 1,24 нмоль (0,051 мг) на 1 см2 поверхности пленки диоксида титана. В спектрофотометрическую кювету, приспособленную для создания анаэробных условий, помещали водный буферный раствор (0,05 М ТРИС, рН 7,2), компонент которого - трис(гидроксиметил)аминометан - служил донором электронов, 1·10-4 М раствор NAD+ и фотобиокатализатор. Перед экспериментами кювету с образцами продували аргоном для удаления кислорода. Реакцию проводили при комнатной температуре при перемешивании раствора. Отбор проб осуществляли шприцем.
Источником света служила ртутная лампа ДРШ 250 мощностью 250 Вт. Освещение проводили через конденсор и водный тепловой фильтр. При помощи граничных светофильтров из спектра излучения ртутной лампы выделяли линии 365 нм. Интенсивность света 4·105 эрг/см2·с.
На основании анализа кинетических данных определялась фотокаталитическая активность фотобиокатализатора, которая составила 7,2±0,7 мкмоль NADH/см2·мг фермента · час.
Пример 4. Фотовосстановление NADP+ до NADPH.
Для фотокаталитической реакции использовали фотобиокатализатор, полученный по примеру 2 - удельная сорбция ферредоксин-NADP-редуктазы составила 0,8 нмоль (0,033 мг) на 1 см2 поверхности пленки диоксида титана.
Реакцию проводили аналогично примеру 3. Фотокаталитическая активность фотобиокатализатора (скорость образования NADPH на 1 см2 мезопористой пленки, содержащей 1 мг фермента) составила 8,3±0,8 мкмоль NADPH/см2·мг белка · час.
Таким образом, предложен фотобиокатализатор на основе ферредоксин-NADP-редуктазы, иммобилизованной на наноструктурированной мезопористой пленке TiO2, позволяющий с достаточно высокой скоростью получать NADH или NADPH из NAD+ или NADP+ под действием света. Катализатор отличается высокой специфичностью. Разработан фотокаталитический способ получения восстановленных форм никотинамидных коферментов NADH или NADPH. Способ не требует использования дорогостоящих соединений в качестве переносчиков электрона и является высоко технологичным, так как обеспечивает повышение устойчивости фермента ферредоксин-NADP-редуктазы при осуществлении процесса, позволяет легко отделять продукты реакции от фермента и полупроводника и обеспечивает возможность многократного использования фотобиокатализатора.
Изобретение может применяться в различных энзиматических процессах, использующих восстановленные формы никотинамидных коферментов NADH и NADPH, в биомедицинских исследованиях, для разработки биосенсоров никотинамидных коферментов.
1. Фотобиокатализатор для получения восстановленных форм никотинамидных коферментов NADH или NADPH, включающий фермент, иммобилизованный на наноструктурированной мезопористой пленке диоксида титана TiO2, приготовленной из нанокристаллов диоксида титана размером 15-25 нм с удельной поверхностью 50-100 м2/г на стеклянной подложке или на стеклянной подложке с токопроводящим покрытием, отличающийся тем, что в качестве иммобилизованного фермента он содержит ферредоксин-NADP-редуктазу в количестве 0,8-1,24 нмоль на 1 см2 поверхности наноструктурированной мезопористой пленки диоксида титана.
2. Фотокаталитический способ получения восстановленных форм никотинамидных коферментов NADH или NADPH реакцией фотовосстановления NAD+ или NADP+ при сопряженном действии полупроводника TiO2 и фермента ферредоксин-NADP-редуктазы при освещении УФ-светом в анаэробных условиях в присутствии органического донора электрона, отличающийся тем, что реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH осуществляют путем прямого переноса электрона от полупроводника TiO2 к ферменту ферредоксин-NADP-редуктазе, для чего используют ферредоксин-NADP-редуктазу, иммобилизованную на наноструктурированной мезопористой пленке TiO2, приготовленной из нанокристаллов TiO2 размером 15-25 нм с удельной поверхностью 50-100 м2/г на стеклянной подложке или на стеклянной подложке с токопроводящим покрытием, в количестве 0,8-1,24 нмоль на 1 см поверхности пленки TiO2.
3. Способ по п.2, отличающийся тем, что реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH проводят при освещении УФ-светом с λ=365 нм.
4. Способ по п.2 или 3, отличающийся тем, что в качестве органического донора электрона используют трис(гидроксиметил)аминометан - компонент водного буферного раствора 0,05 М ТРИС, рН 7,2, в котором проводят реакцию фотовосстановления NAD+ или NADP+ до NADH или NADPH.