Олигонуклеотидные праймеры, способ и тест-система для выявления генома вирусной геморрагической болезни кроликов методом обратной транскрипции - полимеразной цепной реакции
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, а именно к синтетическим олигонуклеотидным праймерам, комплементарным высоко консервативной области гена VP60 генома вируса вирусной геморрагической болезни кроликов, способу выявления вируса вирусной геморрагической болезни кроликов и к тест-системе для выявления РНК вируса вирусной геморрагической болезни кроликов. Предложенное изобретение может быть использовано в ветеринарной вирусологии. Способ выявления вируса вирусной геморрагической болезни кроликов включает пробоподготовку, выделение РЫК из биологического материала. После чего осуществляют постановку полимеразной цепной реакции с использованием праймеров 5'-саа cgt get cca gtt ttg gta cg-3', 5'-att ctg tct ggt tgg ggc gtg t-3'. Далее проводят амплификацию РНК вируса. Затем осуществляют оценку проведения реакции гель-электрофорезом в агарозе, при этом результат реакции считается положительным, если продукт ПЦР соответствует размеру 398 пар оснований. Предложенное изобретение позволяет повысить чувствительность метода, а также сократить время проведения диагностической работы с пробами органов и крови от инфицированных животных. 3 н.п. ф-лы, 4 табл.
Реферат
Изобретение относится к ветеринарной вирусологии, а именно к средствам диагностики.
Вирусная геморрагическая болезнь кроликов (ВГБК) - остропротекающая высококонтагиозная болезнь, характеризующаяся явлениями геморрагического диатеза во всех органах, в особенности в легких и печени [1].
Высокая смертность кроликов при вирусной геморрагической болезни кроликов обуславливают необходимость разработки экспресс-методов диагностики ВГБК с целью быстрого и своевременного принятия карантинных мер и профилактических мероприятий. Одним из таких методов является полимеразная цепная реакция (ПЦР), которая уже нашла широкое применение в диагностических исследованиях в ветеринарии.
Известны многие методы лабораторной диагностики ВГБК, такие как реакция гемагглютинации (РГА), реакция длительного связывания комплемента (РДСК), реакция торможения гемагглютинации (РТГА), реакция иммуноферментного анализа (ИФА) [2]. Однако в некоторых случаях применение этих методов не дает четких результатов, например при исследовании разложившихся патматериалов или объектов ветсаннадзора. Кроме того, перед постановкой реакции требуется предварительное приготовление суспензии органов, что достаточно трудоемко.
Известен способ обнаружения вируса ВГБК методом ПНР, в котором для выделения РНК используют метод фенольно-хлороформенной экстракции с использование протеиназы К [3, 4]. Необходимость работы с токсичными реагентами и длительность процедуры ограничивает его широкое применение. Кроме того, данный способ включает этап приготовления суспензии органов, что увеличивает время проведения реакции.
Целью изобретения является разработка более специфичного, чувствительного экспресс-способа и соответствующей тест-системы для выявления вируса ВГБК с помощью гнездового варианта ОТ-ПЦР с использованием пары синтезированных олигонуклеотидных праймеров, комплементарных к консервативной области гена VP60 генома вируса, позволяющий амплифицировать фрагмент комплементарной ДНК размером 398 п.о.
Для достижения поставленной цели были подобраны и синтезированы специфические праймеры для идентификации возбудителя ВГБК, которые используются для синтеза кДНК и постановки ПЦР:
5' - саа cgt get cca gtt ttg gta cg-3'
5' - att ctg tct ggt tgg ggc gtg t-3'
Способ обнаружения РНК вируса ВГБК в пробах органов, образцах крови инфицированных кроликов включает предварительный этап денатурации РНК и отжига праймеров при 75°С в течение 5 мин с последующим синтезом кДНК при 37°С в течение 30 мин. Реакция ПНР включает 42 цикла амплификации: 94°С - 30 сек, 60°С - 30 сек, 72°С - 30 сек. Затем проводят оценку и учет результатов реакции без предварительной рестрикции полученного продукта с применением набора для постановки электрофореза.
Тест-система, состоит из трех отдельных наборов с пластиковыми флаконами и пробирками:
Набор 1 - для выделения нуклеиновых кислот, содержащий нуклеосорбент с отмывочным буфером на основе гуанидинтиоционата, буфер для реакции, отрицательный контроль;
Набор 2 - для постановки ОТ-ПЦР, включающий пластиковые пробирки, содержащие: олигонуклеотидные праймеры, термостабильный фермент Taq-полимеразу, фермент M-MLV обратная транскриптаза, ПЦР-буфер и буфер для обратной транскрипции, смесь нуклеозидтрифосфатов, положительный и отрицательный контроли;
Набор 3 - для проведения электрофореза, содержащий агарозу, буфер для электрофореза.
Первый набор позволяет быстро и качественно выделить РНК вируса ВГБК без предварительной подготовки суспензии из органов и без использования токсичных веществ.
При постановке ОТ-ПЦР с использованием второго набора производится денатурация вирусной РНК при 75°С и одновременная гибридизация праймеров. В результате дальнейшей амплификации концентрация синтезированного фрагмента в исследуемой пробе увеличивается в миллионы раз, что позволяет визуально учитывать результаты анализа с помощью электрофореза в агарозном геле (третий набор).
Техническим результатом изобретения является общедоступность, безопасность, чувствительность, а также сокращение времени проведения диагностической работы с пробами органов и крови от инфицированных животных.
Сущность изобретения заключается в том, что выявление генома вируса ВГБК проводят методом полимеразной цепной реакции, предусматривающим амплификацию кДНК вируса, электрофоретическое разделение продуктов амплификации и учет результатов реакции. При наличии в исследуемых образцах вируса ВГБК синтезируется ДНК фрагмент длиной 398 п.о. Для определения размера фрагмента вносится маркер молекулярного веса.
Существенным отличием заявляемого способа является то, что:
1. Анализ можно проводить непосредственно из пробы органа (например, печени, легкого, сердца, мышцы) без предварительного приготовления суспензии. При этом навеска органа гомогенизируется в лизирующем буфере. Таким образом, значительно сокращается время постановки реакции.
2. Для анализа можно использовать пробы крови. Таким образом, данный способ позволяет определять наличие возбудителя у инфицированных животных на ранних сроках после заражения.
Изобретение иллюстрируется следующими примерами.
Тест-система укомплектована пластиковыми флаконами и пробирками.
Пример 1. Набор №1 для выявления нуклеиновых кислоты используют для работы с пробами органов и кровью.
Исследуемый материал (кровь) в объеме 200 микролитров (далее мкл) или пробу органа весом 0,2 г вносят в 1,5 см3 пробирку и добавляют лизирующий буфер на основе гуанидинтиоцианата. Пробы органов гомогенизируют в лизирующем буфере и инкубируют 40 мин при 56°С, затем центрифугируют 5 минут и отбирают супернатант в чистые пробирки. В течение 10 мин пробы с кровью и супернатантом инкубируют при комнатной температуре с 40 мкл нуклеосорбента, периодически встряхивая на миксере. Пробирки центрифугируют при 5000 об/мин, и удаляют надосадочную жидкость. В пробирки вносят 300 мкл отмывочного буфера, встряхивают пробирки и центрифугируют при 5000 об/мин, удаляют надосадочную жидкость. Процедуру повторяют дважды. В пробирки вносят 400 мкл 70% спирта. Пробирки встряхивают и центрифугируют при 12000 об/мин, удаляют надосадочную жидкость. Процедуру повторяют дважды. Пробирки инкубируют 8 мин при 56°С, и вносят в пробирки 50 мкл бидистиллированной воды, тем самым эллюируя нуклеиновые кислоты с нуклеосорбента в воду. 5 мкл этого раствора используют для дальнейшего синтеза комплементарной ДНК.
Пример 2. Синтез кДНК и амплификация участка кДНК вируса ВГБК с применением набора №2 для проведения ОТ-ПЦР с синтетическими олигонуклеотидными праймерами.
Расчет первичной структуры олигонуклеотидных праймеров.
Для идентификации вируса геморрагической болезни кроликов
методом полимеразной цепной реакции необходимо было определить участок генома, нуклеотидная последовательность которого позволяла бы дифференцировать данный вирус от других представителей семейства Caliciviridae и одновременно являлась бы достаточно консервативной для различных штаммов и изолятов вируса ГБК. Проанализировав данные литературы, мы пришли к выводу, что геном, подходящим для идентификации ВГБК, является ген VP60, кодирующий белок капсида.
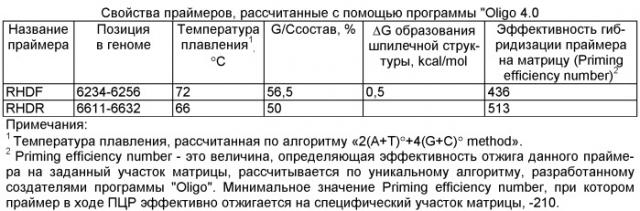
Подбор праймеров осуществляли на основе анализа нуклеотидных последовательностей штаммов и изолятов возбудителя ВГБК, имеющихся в базе данных GeneBank [http://www.ncbi.nlm.nih.gov/genbank]. Множественное выравнивание и анализ последовательностей осуществляли с помощью компьютерной программы «BioEdit 6.0». Для расчета праймеров был выбран участок высококонсервативной области гена VP60. Расчет и анализ олигонкулеотидов проводили с использованием компьютерной программы «OLIGO 6.0». Для подбора и анализа праймеров использовали последовательность гена VP60 штамма Triptis вируса геморрагической болезни кроликов.
Тест-система апробирована на различных штаммах и изолятах вируса ВГБК. В качестве отрицательных контролей использованы штаммы вируса миксомы кроликов и вируса везикулярной экзантемы свиней.
Проводят отжиг праймеров, для чего в предварительно промаркированные пробирки объемом 0,5 или 0,2 мл вносят по 5 мкл РНК, по 0,2 мкл каждого праймера и 5,6 мкл бидистиллированной воды.
Денатурацию РНК и отжиг праймеров проводят в амплификаторе при температуре 75°С в течение 5 минут.
В отдельной пробирке готовят общую реакционную смесь на N образцов, в число которых входят положительный контроль (с водным раствором РНК вируса ВГБК) и отрицательный контроль (с бидистиллированной водой). Реактивы вносят в последовательности, приведенной в таблице. Фермент добавляют в последнюю очередь.
| Реактивы | Кол-во на 1 пробу (мкл) | К-во на N проб (мкл) |
| Буфер для обратной транскрипции | 4 | 4×(N+1) |
| dNTP | 1 | 1×(N+1) |
| Фермент MMLV ревертаза | 0.1 | 0.1×(N+1) |
| Вода бидистиллированная | 4 | 4×(N+1) |
Смесь вносят сверху на масло. Пробы инкубируют при температуре 37°С 30 минут в амплификаторе. После окончания инкубации кДНК используют для дальнейшего анализа или хранят при -20°С 2 недели.
В отдельной пробирке объемом 0,5 или 0,2 мл готовят общую реакционную смесь на N образцов, в число которых входят положительный и отрицательный контроли. Реактивы вносят в последовательности, приведенной в таблице. Фермент добавляют в последнюю очередь.
| Реактивы | Кол-во на 1 пробу (мкл) | К-во на N проб (мкл) |
| Вода бидистиллированная | 14,6 | 14,6×(N+1) |
| Буфер для ПЦР | 4 | 4×(N+1) |
| Праймер RHDF | 0,2 | 0,2×(N+1) |
| Праймер RHDR | 0,2 | 0,2×(N+1) |
| dNTP | 1 | 1×(N+1) |
| Фермент Taq-полимераза | 0.1 | 0.1×(N+1) |
В реакции ПЦР используют 5 мкл кДНК, полученной в ходе реакции обратной транскрипции.
Реакцию ПЦР проводят в амплификаторе при следующих режимах:
| 94°С | 30 сек | |
| 60°С | 30 сек | 42 цикла |
| 72°С | 30 сек |
Пример 3. Определения размера продуктов ПЦР с применением набора для проведения электрофореза.
Продукты ПЦР анализируют методом электрофореза в 2%-ном агарозном геле в стандартном трис-борном буфере.
13 мкл продукта ПЦР вносят в лунку агарозного геля. Электрофорез проводят при напряжении 10 В/см длины геля до тех пор, пока краситель не пройдет от старта не менее половины геля (примерно 15 мин). Результат электрофореза учитывают, просматривая гель в ультрафиолетовом свете с длиной волны 230 нм на приборе «Трансиллюминатор». Результат считается положительным, если продукт ПЦР соответствует размеру фрагмента 398 пар оснований.
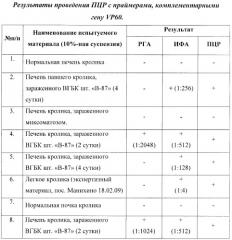
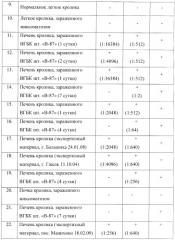
С применением тест-системы и рассчитанных праймеров выявлялись все исследуемые образцы вируса ВГБК. Отрицательные контроли не амплифицировались.
Пример 4. Определение чувствительности и специфичности ОТ-ПЦР на основе синтетических олигонуклеотидных праймеров.
Тест-система и синтетические олигонуклеотидные праймеры были проверены на специфичность и чувствительность. Установлено, что тест-система не амплифицирует кДНК других бактерий и вирусов. Тест-система показала диагностическую специфичность и чувствительность на уровне 100%.
Аналитическая чувствительность была определена относительно активности вируса, выраженной в lg LD50/см3. Для чего проводили серию 10-кратных разведений вируса ВГБК штамма «В-87», с исходным титром 4,5 lg LD50/см3 и анализировали с применением метода ПНР. Пределом чувствительности являлось разведение 1:103 от исходного образца с титром инфекционной активности 4,5 lg LD50/см3.
Аналитическая чувствительность предлагаемого набора была также определена относительно активности вируса, выраженной в ГАЕ, амплификацией очищенной РНК вируса, выделенной из последовательных четырехкратных разведений 10%-ных суспензий проб печени кроликов, инфицированных ВГБК. Рассчитанное значение аналитической чувствительности превышало предел чувствительности РГА в 2 раза.
Источники информации
1. Власов Н.А. Физико-химические свойства и антигенная структура вируса геморрагической болезни кроликов. // Докторская диссертация. - Покров: ВНИИВВиМ, 1998. - 351 с.
2. Шевченко А.А., Вишняков И.О., Бакулов И.А., Власова Т.А. Вирусная геморрагическая болезнь кроликов. // Ветеринария, 1994, №10. - С.22-23.
3. Tian L., Liao J., Li J., Zhou W., Zhang X., Wang H. Isolation and identification of a non-haemagglutinating strain of rabbit hemorrhagic disease virus from China and sequence analysis for the VP60 Gene. // Virus Genes, 2007, №35. P.745-752.
4. Ros Bascuñana С., Nowotny N. and Belák S. Detection and differentiation of rabbit hemorrhagic disease and European brown hare syndrome viruses by amplification of VP60 genomic sequences from fresh and fixed tissue specimens. // J. Clinical Microbiol., 1997, №35. - P.2492-2495.
1. Синтетические олигонуклеотидные праймеры, комплементарные высоко консервативной области гена VP60 генома вируса вирусной геморрагической болезни кроликов, используемые для выявления РНК вируса ВГБК, имеющие следующий нуклеотидный состав:5'-саа cgt gct cca gtt ttg gta cg-3'5'-att ctg tct ggt tgg ggc gtg t-3'.
2. Способ выявления вируса ВГБК, включающий пробоподготовку, выделение РНК из биологического материала, постановку полимеразной цепной реакции с использованием синтезированных праймеров, амплификацию РНК вируса, оценку проведения реакции гель-электрофорезом в агарозе, отличающийся тем, что проводят предварительную денатурацию вирусной РНК при 75°С в течение 5 мин, синтез кДНК проводят при 37°С в течение 30 мин, а для постановки ПНР подобраны и синтезированы две пары олигонуклеотидных праймеров по п.1 с 42 циклами амплификации при температуре денатурации 94°С 30 с, отжига 60°С 30 с, элонгации 72°С 30 с, затем проводят оценку результатов реакции без предварительной рестрикции полученного продукта, при этом результат реакции считается положительным, если продукт ПНР соответствует размеру 398 пар оснований.
3. Тест-система для выявления РНК вируса вирусной геморрагической болезни кроликов, включающая пластиковые флаконы и пробирки, термостабильный фермент Taq-полимеразу, ПЦР-смесь для постановки реакции, положительный и отрицательный контроли, отличающаяся тем, что содержит три набора: 1) набор для выявления нуклеиновой кислоты, содержащий нуклеосорбент с отмывочным буфером на основе гуанидинтиоционата, буфер для реакции, отрицательный контроль; 2) набор для проведения ОТ-ПЦР, включающий пластиковые пробирки, содержащие синтетические праймеры по п.1; 3) набор для проведения электрофореза, содержащий агарозу, буфер для электрофореза.